[color=#444444]帮朋友问的,用甲醛合成丁炔二醇。最终甲醛含量小于0.5%。想用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]做跟踪。有没有人做过这个啊。帮忙给个分析条件吧。[/color]
各位师傅:有谁知道1.4-丁炔二醇的方法,请帮帮忙,谢谢!
用氧化铝柱时,能否用极性判断1-丁炔和乙烯基乙炔那个先出峰?
乙二醇双(2-氨基乙基醚)四乙酸的酸值怎么滴定?
分享一个金属螯合物二丁基二硫代氨基甲酸锌的残留量测定[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]方法。样品经四氢呋喃-乙腈(体积比为10∶90)超声提取制得供试品溶液。流动相:四氢呋喃-乙腈(体积比为35∶65),供试品溶液经SunFire C18色谱柱分离后,用254 nm检测波长进行HPLC测试。本方法检出限和定量限分别为20和30 ng,加标回收率为98. 84~102. 58%,供试品溶液在6 h内稳定。本方法简便、准确、灵敏、稳定。由于二丁基二硫代氨基甲酸锌与二硫代氨基甲酸盐类化合物是类似物,该研究也能为二硫代氨基甲酸盐类物质的分析提供有益借鉴。详见谢兰桂等, 橡胶工业. 2022,69(07)。
最近在检测氨基乙醛缩二甲醇这个产品,用一个滴定的方法,颜色不好判断,哪位高手指点一下,最好有什么先进的方法,比如GC。
求救!!要用GC做空气中丁氨基乙醇,请问用什么解吸液可以把碳管解析出来啊~~~标液用什么溶剂配制啊!多谢!
看到有一些测试塑料中有机锡总含量的方法,用甲醇作为萃取剂,但是做加入一定量的二乙基二硫代氨基甲酸钠(铜试剂),请问有什么用处?
求大神提供氨基乙醛缩二乙醇的生产制备技术指导。
今天小编介绍的高纯气体是有机高纯气体的分类介绍,按照分类我们可以将有机高纯气体进行归类,之前并不是非常了解的朋友可以随小编的介绍进行一个简单的理解。 1、烷烃类:甲烷(CH4)、乙烷(C2H6)、丙烷(C3H8)、环丙烷(cyc-C3H6)、正丁烷(n-C4H10)、异丁烷(i-C4H10)、正戊烷(n-C5H12)、新戊烷(neo-C5H12)、氯甲烷(CH3Cl)、氯乙烷(C2H5Cl)、三氟甲烷(CHF3)、环氧乙烷(C2H4O)、砷烷(AsH3)、磷烷(PH3)、硼烷(B2H6)、硅烷(SiH4)等; 2、烯烃类:乙烯(C2H4)、丙烯(C3H6)、丙二烯(C3H4==)、1-丁烯(1-C4H8)、异丁烯(i-C4H8)、反-2-丁烯(t-2-C4H8)、顺-2-丁烯(c-2-C4H8)、1.2-丁二烯(1.2-C4H6)、1.3-丁二烯(1.3-C4H6)、氯乙烯(C2H3Cl)等; 3、炔烃类:乙炔(C2H2)、1-丁炔(1-C4H6)、2-丁炔(2-C4H6)、甲基乙炔(C3H4)、乙烯基乙炔(C4H4=≡)等; 4、其他:二甲醚(C2H6O)、甲硫醇(CH4S)、熏蒸剂(C2H4O-CO2)等
加入二氨基二甲基丙醇的生产废水测试氨氮结果是未检出,该物质是否对氨氮结果真没有影响?
根据HJ540-2016 二乙基二硫代氨基甲酸钠分光光度法 测定固定污染源中的砷做出来的标曲最大质量25ug吸光度为0.699,空白0.002,曲线为y = 0.0284x - 0.0036这样子可不可以采用?
高纯气体对我们来说之前了解的也是比较多的,但是小编今天想要和大家说的是高纯气体的几种分类,这几种分类对我们来说了解的并不是很多,但是在我们的生活中这几种高纯气体都是比较常见的,下面小编就简单的向大家做一个介绍,希望大家能够了解一下。 1、烷烃类: 甲烷(CH4)、乙烷(C2H6)、丙烷(C3H8)、环丙烷(cyc-C3H6)、正丁烷(n-C4H10)、异丁烷(i-C4H10)、正戊烷(n-C5H12)、新戊烷(neo-C5H12)、氯甲烷(CH3Cl)、氯乙烷(C2H5Cl)、三氟甲烷(CHF3)、环氧乙烷(C2H4O)、砷烷(AsH3)、磷烷(PH3)、硼烷(B2H6)、硅烷(SiH4)等; 2、烯烃类: 乙烯(C2H4)、丙烯(C3H6)、丙二烯(C3H4==)、1-丁烯(1-C4H8)、异丁烯(i-C4H8)、反-2-丁烯(t-2-C4H8)、顺-2-丁烯(c-2-C4H8)、1.2-丁二烯(1.2-C4H6)、1.3-丁二烯(1.3-C4H6)、氯乙烯(C2H3Cl)等; 3、炔烃类: 乙炔(C2H2)、1-丁炔(1-C4H6)、2-丁炔(2-C4H6)、甲基乙炔(C3H4)、乙烯基乙炔(C4H4=≡)等; 4、其他: 二甲醚(C2H6O)、甲硫醇(CH4S)、熏蒸剂(C2H4O-CO2)等
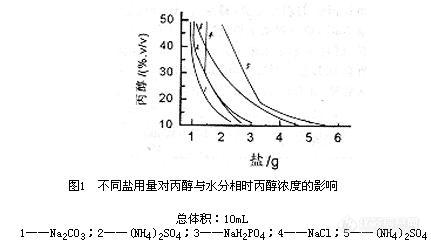
[center]氯化钠-二乙基二硫代氨基甲酸钠-丙醇体系萃取分离铜[/center][center]李全民张丽敏 刘 奇 郭金枝[/center]摘 要:研究了氯化钠-二乙基二硫代氨基甲酸钠-丙醇体系萃取铜的行为及丙醇水溶液分相条件的选择。实验表明,丙醇作为萃取溶剂,能萃取中性螯合物。在EDTA 存在下,调节 pH5~pH10,该体系能使 Cu2+从常见元素 Fe3+、Co2+、Ni2+、Al3+等离子的混合液中分离出来。关键词:铜;二乙基二硫代氨基甲酸钠;丙醇;萃取分离中图分类号:O65 文献标识码:A 文章编号:1000-0720(1999) 02-020-04The Liquid-Liquid Extraction Behaviour of Copper(Ⅱ) Based on Sodium Chloride-Sodium-Diethyldithiocarbamate-n-Propanol System LI Quan-min,ZHANG Li-min,LIU Qi and GUO Jin-zhi(Department of Chemistry,Henan Normal University,Xinxiang 453002),Fenxi Shiyanshi,1999,18(2):20~23 In this paper,the liquid-liquid extraction behaviour of the chelate of copper(Ⅱ) with sodium diethyldithiocarbamate based on sodium chloride-sodium diethyldithiocarbamate-n-propanol system was investigated and the proper conditions of phase separation of n-propanol and water were selected.The quantitative extraction separation of Cu2+ from Fe3+,Co2+,Ni2+ and Al3+ was carried out by adding 1.0mL of 0.001mol/L EDTA as the masking agent to 10mL 30%(V/V) n-propanol solution at pH 7.0 .The separation results are satisfactory. Keywords Sodium chloride sodium diethyldithiocarbamate n-propanol copper extraction separation 在无机盐存在下,乙醇水溶液可以分成液-液两相,已利用该体系进行了钼的萃取分离[1]。研究发现,在丙醇水溶液中加入无机盐也能使丙醇与水分成液-液两相,金属离子的螯合物沉淀可以在丙醇-水两相中进行分配,其分离操作方式及萃取分离体系的特点类似于乙醇溶液体系,从而建立了以丙醇作为萃取溶剂的均相萃取、异相分离的新型萃取体系,还未见国内外文献报道。本文研究了氯化钠-二乙基二硫代氨基甲酸钠(铜试剂)-丙醇体系萃取 Cu2+的行为。实验表明,在丙醇与水相条件下,铜与铜试剂形成的螯合物沉淀能被丙醇相完全萃取,在EDTA存在下,Fe3+、Co2+、Ni2+、Al3+被掩蔽而留在水相,实现了在同一体系中 Cu2+与 Fe3+、Co2+、Ni2+、Al3+的分离。该萃取体系与传统的有机溶剂萃取分离法相比,具有挥发性小,无毒,平衡时间短,相分离界面清晰,无三相乳化,无环境污染,操作简单,均相萃取-异相分离等特点。特别是由于丙醇对某些大分子缔合物及螯合物沉淀有很好的溶解性,用丙醇作为萃取溶剂的萃取体系,可以萃取大分子缔合物或螯合物沉淀后直接进行光度测定,从而避免了萃取浮选体系中的相分离后再选择适当的溶剂溶解沉淀的光度法这一繁琐操作[2,3],使测定更加简便和准确。可见,该体系的研究为建立新型萃取体系打下了基础,具有一定的应用和研究前景。1 主要试剂与仪器 正丙醇(A.R,北京化工厂);硫酸铵(A.R,北京化工厂);铜试剂(A.R.上海试剂三厂);配成 5×10-3mol/L 水溶液;金属离子标准液按文献[4]配制;缓冲溶液:pH1.0~2.0(KCl-HCl 配制);pH3.0(KHC8H4O4-HCl 配制);pH4.0~pH7.0(KHC8H4O4-NaOH 配制);pH8.0~pH10.0(NaOH-H3BO3 配制);所用其它试剂均为分析纯。 721型分光光度计(上海第三分析仪器厂);pHS-2 酸度计(上海第三分析仪器厂);康尔振荡器(江苏盐城医疗器械厂)。 2 试验方法 于 25mL 磨口比色管中,加入一定量的丙醇、铜试剂和被研究的金属离子溶液,根据试验条件不同,分别加入不同 pH值的缓冲溶液 1.0mL 调节溶液所需要的pH值,用水稀至 10mL,再加入一定量的固体 NaCl,振荡 1~2min,放置片刻,使溶液分成丙醇与水两相,移取丙醇相或下层盐水相测量被萃取金属离子的浓度,计算萃取百分率(E%)。在多元混合离子溶液中采用 ICP-AES 法测定各离子的量。3 结果和讨论3.1 不同盐对丙醇水溶液分相条件及 Cu2+萃取率的影响 固定水溶液中丙醇浓度,分别加入不同量的 NaCl、NaNO3、NaH2PO4、KH2PO4、Na2CO3、(NH4)2SO4,实验发现,除了 KH2PO4 之外,其余盐均能使丙醇与水分相。不同浓度的丙醇水溶液其分相时所需盐用量见图1。丙醇的浓度越大,分相时盐的用量就相应减少。原因可能是当溶液中的水用于盐的水合作用到一定程度时,丙醇与水才能分相。在加入质量相同的盐中,几种盐的分相能力按 Na2CO3、NaCl,(NH4)2SO4、NaH2PO4,NaNO3 的顺序递减。这是由于盐析作用能力不仅与离子体积参数a有关[4],而且与离子数目有关。同质量的盐中,离子数目越多,且a越大,盐析作用就越强。在相同条件下,NaCl 电离出的离子数目最多,阴离子中 CO2-3 的 a值最大,综合考虑以上两种因素,因此,Na2CO3 的分相能力最强,NaCl 次之。考虑到多数金属离子的碳酸盐会产生沉淀,在两醇水溶液分相条件下,又分别试验了不同量的 NaCl、(NH4)2SO4、NaNO3, NaH2PO4对 Cu2+萃取率的影响。结果表明,几种盐均能使 Cu2+的萃取率达 100%,但考虑到 (NH4)2SO4 易与碱作用而放出 NH3,NaH2PO4 易与金属离子络合,用 NaNO3 时盐用量又太大,而用 NaCl 不仅萃取效果好,又价廉易得,故在本实验中选择 NaCl 作盐析剂。当 NaCl 用量仅为 1.0g时,Cu2+已能被完全萃取,这说明 Cu2+与铜试剂生成的螯合物沉淀极易溶解在丙醇相。这也说明,用丙醇作为萃取溶剂有很好的应用前景。[img]http://ng1.17img.cn/bbsfiles/images/2008/02/200802161014_79045_1632583_3.jpg[/img]3.2 溶液酸度对丙醇与水分相时 NaCl 用量的影响 固定丙醇加入量为 3.0mL,溶液总体积为 10mL,改变试液 pH,试验了酸度对丙醇与水分相时 NaCl 用量的影响。试验表明,pH 大于 1.0,NaCl 的用量只需 1.0g 就能使丙醇与水分相,且随 pH 增加 NaCl 的用量不再改变。酸浓度为 1mol/L HCl时,加入 1.5g NaCl 才能分相,这是由于高酸度下,丙醇分子质子化增强了在水中的溶解度,这表明高酸度条件下不利于丙醇与水的分相。3.3 NaCl 用量对丙醇相析出体积的影响 调节溶液 pH 为 5.0,丙醇的用量及溶液总体积同 3.2节,NaCl 用量为 1.0g,丙醇相体积为 1.9mL。这表明相分离时,部分丙醇留在了水相,当 NaCl 用量增至 1.5g,丙醇相体积为 2.6mL,大于 2.0g,丙醇相体积为 2.8mL,且不再随盐用量增加而改变,这说明丙醇与水分相程度已基本趋于完全。为了保证在萃取过程中丙醇体积保持不变,实验中选择 NaCl 的用量 2.0g。3.4 铜试剂用量对 Cu2+萃取率的影响 加入 Cu2+的量为 50μg,3.0mL丙醇、1.0mL pH5 的缓冲溶液,稀至 10mL,再加入 2.0g NaCl,改变铜试剂用量测得了 Cu2+的萃取率。试验表明,加入浓度为 5×10-3mol/L 铜试剂 0.5mL 以上时即可使 Cu2+完全萃取。无铜试剂时,对 Cu2+根本无萃取作用,这表明丙醇相不能萃取简单金属离子。3.5 酸度对不同金属离子萃取率的影响 酸度对不同金属离子萃取率的影响的实验表明,氯化钠-铜试剂-丙醇体系中,在 EDTA 掩蔽下,从 pH 5.0~10.0,Fe3+、Co2+、Ni2+、Al3+萃取率很低或根本不被萃取,控制一定的条件,有可能使 Cu2+与这些离子得到满意的分离。3.6 分离试验 在 3.5 条件下,分别试验了合成样中二元及多元体系中 Cu2+与 Fe3+、Co2+、Ni2+、Al3+,分离结果见表1、2。[img]http://ng1.17img.cn/bbsfiles/images/2008/02/200802161015_79046_1632583_3.jpg[/img] 表1、表2 的分离测定结果及不同pH下各金属离子萃取率表明,在 EDTA 存在下,氯化钠-铜试剂-丙醇体系能使 Cu2+与 Fe3+、Co2+、Ni2+、Al3+得到很好分离的适宜酸度范围 pH为(5.0~10.0),最佳 pH 为 7.0,且各离子单独萃取行为与混合液中的萃取行为相同,根据单一离子的萃取行为可以估计混合液中的萃取行为。建立分离富集铜的新方法是分析化学工作者所关心的课题。该工作对于从上述元素混合液中分离富集铜有一定的实际意义。资金来源:河南省科委、省教委自然科学基金资助项目作者简介:李全民,男,41岁,副教授;郭金枝:河南省粮食学校工作作者单位:李全民,张丽敏,刘 奇,郭金枝 河南师范大学化学系,新乡 435002参考文献 [1] 李全民,张青芬,刘 奇.分析化学,1997,25(10):1143 [2] 徐其亨,刘绍璞.理化检验(化学分册),1984,20(4):48 [3] 徐其亨.化学通报,1981,11:682 [4] 常文保,李克安.简明分析化学手册.北京:北京大学出版社,1981:241,255
2-氨基丁醇 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]能测吗?
本人实验中要分开γ-丁内酯、1,4-丁二醇和丁二酸二甲酯,但γ-丁内酯和丁二酸二甲酯可以分,加入少量的1,4-丁二醇也可以分,但一旦量大了1,4-丁二醇就显示两个峰,并且如果继续加1,4-丁二醇则又会变为一个峰,试问高手这是怎么回事呀?是不是我条件有问题呀,我用的是程序升温。非极性柱子
我最近在用Al2O3的柱子分析1,3-丁二烯纯度里面有常量的反二丁烯、顺二丁烯和1,2-丁二烯(偶尔),还有PPM级的乙烯基乙炔和丁炔(一般没有)。最近出一个问题,在乙烯基乙炔和丁炔附近总有一些很缓峰出现,影响乙烯基乙炔和丁炔的定性和定量,我升温烧柱子以后这些东西就不见了,最近每做一个样子就下一个样子就会受污染。我觉得每做一个样少一次柱子应该不是好办法,各位老师有没有好的办法,请不吝赐教。PS:我打算截掉一段柱头不知道算不算是个好办法。
在水溶液里用有机溶剂萃取出2,4- 二氨基甲苯和2,4-二氨基苯甲醚,回收率很低(前者回收率小于50%,后者回收率小于20%),调整pH值也效果不大。请帮分析下原因,如是否跟两个氨基的位置有关系?把这两种物质分别用甲醇配置成溶液,密封,放置一段时间后,溶液浓度会降低,尤其是2,4-二氨基苯甲醚降低的很多,请帮分析下原因。同样情况也出现在1,4-苯二胺中。
[font=&][size=16px][color=#333131]可以做氨丁三醇(三羟甲基)氨基甲烷,杂质峰定性的检测机构请看过来[url=https://www.woyaoce.cn/helptest/detail-dcb6af847ef4628458ecdf6d407180cd.html]点击查看详情[/url][/color][/size][/font]
哪位同道有 对氨基二甲基苯胺比色法 GB 18056 –2000 附录A 用来检测甲硫醇的,急需!!!
有谁知道二乙二醇丁醚和二乙二醇丁醚醋酸酯的极性大小啊,我根据它们的结构,初步判断它们是极性物质,但我用极性色谱柱分离检测时,却发现它们的检测限远远大于它们在非极性柱上的检测限,而且在非极性柱上出的峰形对称又尖锐。有谁能够帮我解释一下啊,谢谢了!

[color=#444444][/color][color=#444444]合成一种月桂酸二乙醇酰胺混合物,里边含有主要成分月桂酸二乙醇酰胺,酰胺单酯,酰胺双酯,二乙醇胺,月桂酸等 想得到这几种物质的有效含量 [/color][color=#444444]如果用[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用[/color][/url],可能有些结构不能正确表征(如酰胺酯) [/color][color=#444444]如果用HPLC,溶剂选择很困难(对此方法操作所需条件不是很清楚)[/color][color=#444444]请各位朋友帮帮忙,给点建设性意见,非常感谢!!![/color][color=#444444][/color]

研究概况 物质的相平衡数据测定及其相平衡研究是化工热力学的一个重要分支,固液相平衡是化工分离的理论基础。固液平衡的研究为结晶分离过程规定了分离极限,并为设备结构尺寸的设计和操作条件的确定提供基础数据,是实现化工生产的重要前提。实验测定固液平衡不仅是工程设计必不可少的基础数据,也是进行理论研究的基础。固液平衡的数学模型参数需要由实验数据来回归,数学模型的准确性需要用实验数据来检验。通过对固液平衡实验数据的处理,找出其内在规律,提出符合溶解行为的数学模型。 4-二甲氨基吡啶(简称DMAP)结构上有共电子的二甲氨基与吡啶环的共振,强烈的激活了环上的氮原子进行亲核取代,明显催化高位阻、低反应性的醇或胺的酰化(磷酰化、磺酰化)反应,其活性为吡啶的106倍。1967年,Litvinenko和Kirichenko用间氯苯胺进行苯甲酰化动力学研究,以4-二甲氨基吡啶代替吡啶,发现其反应速率增加约1万倍。Steglich、Hassner等人开始着手于研究DMAP作为催化剂催化酰化反应,酰化反应应用于醇、胺、酚和烯醇盐,尤其是存在空间位阻的仲醇、叔醇等。至今,DMAP在酰化反应催化剂中,具有反应速度快、副反应少、溶剂选择范围广、反应条件温和、反应温度低、催化剂量少、对空间位阻大与活性低的醇类酰化催化效果明显的特点,被称为“超级催化剂”。 美、欧、日等国家早已实现DMAP的工业化生产与应用研究,广泛地应用于医药、高分子、精细化工等行业中,我国从90年代初开始DMAP的合成与应用研究,目前,在化学制药领域上取得了成功的应用及良好的效益,如乙(丙)酞螺旋霉素、青篙素唬拍酸酷等原料药的生产;农药领域上在胺菊酯的合成已通过中试并投产。1.实验部分1.1实验试剂4-二甲氨基吡啶 (1) DMAP的物性:白色结晶性粉末,溶于水、乙醇、丙酮、苯、甲苯、二甲苯、二氯乙烷、氯仿、乙酸、乙酐、乙酸乙酯、已烷、四氢呋喃、三乙胺、吡啶、DMF 等溶剂。DMAP的分子结构,如图1-1。http://ng1.17img.cn/bbsfiles/images/2015/09/201509272125_568160_2423358_3.jpg1.2实验试剂规格及来源实验试剂规格及来源,均符合分析化学实验的要求,可以保证实验的进行。表1-2 实验所用试剂 试剂名称 生产厂家分子量规格和品级质量分数% DMAP 北京华威锐科化工有限公司122.17分析纯99.00 乙醇 北京化工厂46.07分析纯99.70 正丙醇 天津市福晨化学试剂厂60.10分析纯99.80 异丙醇 北京化工厂60.10分析纯99.70 正丁醇 北京化工厂74.12分析纯99.00 异丁醇 天津市福晨化学试剂厂74.12分析纯99.00 乙酸甲酯 天津市光复精细化工研究所74.08分析纯98.00 乙酸乙酯 北京化工厂88.11分析纯99.50 乙酸丙酯 天津市光复精细化工研究所102.13分析纯98.00 乙酸异丙酯 天津市光复精细化工研究所102.13分析纯99.00 乙酸丁酯 北京化工厂116.16分析纯99.00 乙酸异丁酯 天津市光复精细化工研究所116.16分析纯98.501.3实验装置表1-3 实验的仪器设备 设备名称 型号 生产厂家 精密温度计 制冷和加热循环槽 0-50℃ MPG-10C型 上海精密科学仪器厂 上海一恒科技仪器有限公司 电子分析天平 Sartorius CP124S型 德国Sartorius公司 磁力搅拌器 85-1A型 巩义市于华仪器有限责任公司 激光发射器 JDW-3型激光电源 北京大学物理系 夹套溶解釜 定制 北京化工大学仪器厂 本实验用到的仪器设备列于表1-3。 实验装置主要包括激光监视系统、夹套溶解釜、磁力搅拌器、电子分析天平、制冷和加热循环槽等。激光监视系统是发射激光、接受激光、记录仪等组成的,激光具有单色性好、相干性高、方向性强的特点,应用到测定溶解度,可减少因人为目测试样溶解情况带来的误差。夹套溶解釜是一个双层玻璃的瓶子,外层接通循环水,使内层试样升温或降温,还具有保温功能,内层装实验试样,内层上方有两个瓶口,大瓶口以插有温度计的塞子为塞子,大瓶口加入溶剂或溶质,小瓶口接冷凝管,冷却逸出液面到达瓶口处的试样,减少试样的挥发。磁力搅拌器充分搅拌瓶内试样,加快溶质的溶解。电子分析天平用来称量溶剂、溶质的质量。制冷和加热循环槽是一个超级恒温水浴系统,通过设定循环槽的温度调整溶解釜的温度,确保在加入溶质的实验过程中为恒定温度下。http://ng1.17img.cn/bbsfiles/images/2015/09/20150927212
最近买了一支爽肤水,包装上写的不含乙醇及色素但成份表里写着丁二醇,不知道这种醇类跟乙醇类有什么区别
英文资料上写的是苯基环己基乙醇酸(Phenyl cyclohexyl glycolic acid)与溴丙炔(propargyl bromide)反应,生成苯基环己基乙醇酸丙炔酯(propargyl ester of Phenyl cyclohexyl glycolic acid)。但是反应方程式中写的是 Br-CH2三CH-CH3 (1-溴-2丁炔),我怀疑资料上有个地方写错了。请问与之反应的到底是溴丙炔还是1-溴-2丁炔。谢谢。
我们分析室用的是岛津的GC2010,最近正在做一个项目,3-丁炔-1-醇。用的是PEG-20的强极性柱子。图谱上有溶剂峰,杂质峰,产品峰。最近这两次测样的时候,发现图谱上前面的溶剂峰和杂质峰的保留时间没有变化,但是产品峰的保留时间不太稳定,前后有0.4min左右的波动,我确认过了,不是柱子的问题。还有,3-丁炔-1-醇这个试样,是氢氧化钠处理过的,会不会是因为强碱的关系,导致样品主峰保留时间的波动呢?求高人解释
五种混标用二硫化碳溶解,毛细管柱为安捷伦DB1701,进样口温度250,检测器250,柱温35,程序升温至150,结果只检出甲醇,正丁醇,异戊醇。而乙二醇,异丙醇未检出,是我的仪器条件设置问题吗?求教!
实验室硅表的使用及维护一、测试仪器准备工作1.开机注入高纯水,预热30分钟2.用高纯水冲洗2-3遍,直至数据与下标一致,如差距很大将要用高纯水校准一遍。方法如下:① 退出进入主菜单——标定——选中标一数据更改为下标值。② 倒入高纯水推入拉杆选中“稳定”待电压数据稳定——“确认”。③ 倒入高纯水拉出拉杆,将标二值改为上标值,选“稳定”,待电压数据稳定——“确认”。④ 选中“完成”——“确认”,校准完毕退出进入测量界面,即可测量。二、显色液的配制试剂1:盐酸(1+1)溶液:分析纯盐酸与等体积的高纯水混合而成。试剂2:10%钼酸铵溶液(重/容)试剂3:10%草酸(H2C2O4)溶液(重/容)试剂4:1、2、4酸还原剂:称取1.5g 1-氨基-2萘酚-4磺酸和7g无水亚硫酸钠 (Na2SO3)溶于200ml高纯水中;再称取90g亚硫酸氢钠(NaHSO3),溶于600ml高纯水中。将上述二种溶液混合,用高纯水稀释至1L。
DMA做溶剂,却有醇峰,定位炔丁醇和混合溶剂跑出来的峰,混合溶剂里炔丁醇附近有两个峰,是反应了吗
哪种类型的色谱柱可以用来测甲醇,氨基甲酸甲酯,碳酸二甲酯