哪里有头孢噻呋标准品?
有谁做过头孢噻肟钠 俄罗斯标准的,溶解度和化学鉴别中的试药是什么?
进口兽药质量标准硫酸头孢喹肟注射液Liusuan Toubaokuiwo ZhusheyeCefquinome sulfate Injection本品为硫酸头孢喹肟与油酸乙酯等配制而成的混悬注射液。含头孢喹肟(C23H24N6O5S2)应为标示量的90.0%~105.0%。【性状】 本品为类白色至浅褐色混悬液体;久置分层。【鉴别】(1)含量测定项下记录的色谱图中,供试品主峰的保留时间应与对照品峰的保留时间一致。(2)取摇匀后的供试品2 ml,加水5 ml,稀盐酸1 ml,混匀,置超声浴中超声10分钟,弃去有机层,溶液显硫酸盐的鉴别反应(附录15页)。【检查】有关物质 照含量测定项下的方法。取摇匀后的供试品1.0 ml,加入流动相25.0 ml,置超声浴中超声5分钟,弃去有机层,取水层滤过,取续滤液10µ l,注入液相色谱仪,记录色谱图,2,3-环己基吡啶与头孢喹肟相对保留时间为0.20。按峰面积归一化法计算,2,3-环己基吡啶应不得过3.0%,其他单一杂质应不得过0.50%,杂质总量应不得过4.0%。水分 取本品,照水分测定法(附录58页,第一法)检查,含水分不得过0.2%。细菌内毒素 取摇匀后的供试品2 ml与细菌内毒素检查用水3 ml混匀,分成2等份,振摇30秒,离心15分钟(2000g),吸取水层1 ml,加1 mol/L氢氧化钠溶液0.06 ml调节pH值至6.5~7.5。用细菌内毒素检查用水按1:10稀释后,照细菌内毒素检查法(附录73页)检查,每1 mg头孢喹肟中含细菌内毒素的量应小于0.1 EU。无菌 取供试品8瓶,混合均匀,加入含6%吐温-80的蛋白胨缓冲液(1g/L)400ml,混匀,加入800×106单位青霉素酶(每1ml供试品溶液,加2×106单位青霉素酶),充分振摇,将供试品倒置,在37℃放置4小时;取供试品溶液,依法检查(附录79页,直接接种法),应符合规定。分散性 取本品1瓶,振摇30秒,将供试品转移置玻璃容器中,不得观察到结块或沉淀物。沉降 取本品1瓶,振摇30秒,取供试品10 ml置刻度试管中(内径1.0~1.5 cm),10分钟内不得沉淀。粒度 取摇匀后的供试品,置显微镜下检查,颗粒直径在5µ m以下应不得少于80%,10µ m以下不得少于90%,20µ m以下不得少于95%,50µ m以下不得少于100%。装量 按最低装量检查法(附录67页)检查,应符合规定。【含量测定】 照高效液相色谱法(附录24页)测定。色谱条件与系统适用性试验 用十八烷基硅烷键合硅胶为填充剂;取一水合高氯酸钠3.45g溶于1000 ml水中,加磷酸12 ml和乙腈90 ml,用三乙胺调节pH至3.6为流动相;检测波长为270 nm。取头孢噻肟约25 mg,溶于100.0 ml流动相中,另取头孢喹肟约25 mg,置25 ml量瓶中,精密加入上述头孢噻肟溶液1 ml,用流动相稀释至刻度。精密量取10µ l注入液相色谱仪,记录色谱图;计算头孢喹肟与头孢噻肟的分离度,应大于1.0。

Venusil XBP C18(L)分析头孢噻肟钠的分析报告摘要:本实验按照头孢噻肟钠2010版中国药典方法进行测定,以含量测定和有关物质检测方法共同进行色谱柱的筛选。在选定的色谱柱上,进一步考察了该色谱柱用于头孢噻肟钠系统适用性、含量、有关物质等项测试的结果,并初步考察了色谱柱的使用寿命,结果表明VenusilXBP C18(L)适用于头孢噻肟钠的分析:(1)系统适用性溶液中共检出7个杂质,分离度均符合标准要求;(2)对照品平行进样6针RSD为0.13%,保留时间17.039分钟,柱效5068,拖尾因子1.116,均符合标准要求;(3)含量测定中,头孢噻肟钠保留时间16.936分钟,柱效4779,拖尾因子1.118,符合标准要求;(4)有关物质测定中共检出6个杂质,分离度均符合标准要求;(5)用于头孢噻肟钠含量测试时,连续进样300针,保留时间、柱效和拖尾因子均无显著变化,表明VenusilXBP C18(L)对该样品和流动相有较好耐受性。关键词:头孢噻肟钠;VenusilXBP C18(L);2010版药典;液相色谱法前言头孢噻肟钠为中国药典2010版二部收录品种,本实验按照该标准进行测试,通过测试得出VenusilXBP C18(L)适用于头孢噻肟钠分析,其测试结果令人满意。实验部分试剂材料超纯水、甲醇、无水磷酸氢二钠、磷酸高效液相色谱柱:Venusil XBP C18(L);5 μm,150 Å,4.6 × 150mm样品制备系统适用性溶液制备:取头孢噻肟对照品适量,加流动相溶解并稀释制成每1 ml约含1 mg的溶液,作为系统适用性试验溶液。实验结果系统适用性测定结果表1. Venusil XBP C18(L)用于头孢噻肟钠系统适用性溶液测定结果http://ng1.17img.cn/bbsfiles/images/2017/10/2015082410220596_01_2864683_3.png表2.Venusil XBP C18(L)用于头孢噻肟钠对照品溶液测定结果http://ng1.17img.cn/bbsfiles/images/2017/10/2015082410251562_01_2864683_3.png含量测定结果表3. Venusil XBP C18(L)用于头孢噻肟钠含量测定结果http://ng1.17img.cn/bbsfiles/images/2017/10/2015082410281917_01_2864683_3.png有关物质测定结果表4.Venusil XBP C18(L)用于头孢噻肟钠有关物质测定结果http://ng1.17img.cn/bbsfiles/images/2017/10/2015082410305808_01_2864683_3.png色谱柱批次验证结果表5. Venusil XBP C18(L)批次验证结果http://ng1.17img.cn/bbsfiles/images/2017/10/2015082410355084_01_2864683_3.png色谱柱寿命测试结果表6.Venusil XBP C18(L)用于头孢噻肟钠寿命测试结果http://ng1.17img.cn/bbsfiles/images/2015/08/201508241038_562414_2864683_3.png
各位大师,我要用高效液湘测血浆中的盐酸头孢噻呋含量,可方法一直没有建起来,请大家指点,谢谢!
求购头孢地尼E-异构体对照品头孢地尼做分析方法验证,其中有关物质头孢地尼E-异构体标准品买不到。很多销售公司都有但是资质不全我不能买他们的。请教各位大侠们,帮个忙吧。急用!!谢谢!!!!
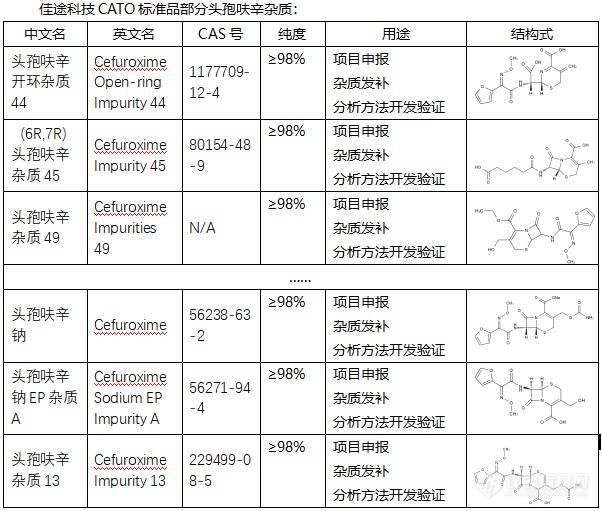
头孢呋辛是一种广泛使用的抗生素,主要用于治疗由敏感细菌引起的各种感染。在生产、储存和使用头孢呋辛的过程中,可能会产生一些杂质。这些杂质的存在可能会影响头孢呋辛的纯度和疗效,因此了解和控制这些杂质对于确保药物的安全性和有效性至关重要。头孢呋辛的杂质有多种,其中一些具有特定的CAS号、化学式和分子量。例如,头孢呋辛杂质33(Cefuroxime Impurity 33)的CAS号为929531-94-2,分子式为C16H16N4O9S,分子量为440.38。此外,还有其他一些头孢呋辛杂质,如头孢呋辛杂质A、B、C、D、E、F、G、H等。 CATO标准品提供的头孢呋辛全套的杂质,这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分。[img=,602,511]https://ng1.17img.cn/bbsfiles/images/2024/02/202402192104451830_7644_6381607_3.png!w602x511.jpg[/img] 广州佳途科技股份有限公司深知药物研发与质量控制的重要性,CATO标准品厂家,提供头孢呋辛全套的杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展,以满足客户在药物研发和质量控制方面的需求。[list][*]原创检测区[/list]◇头孢呋辛杂质头孢呋辛是一种广泛使用的抗生素,主要用于治疗由敏感细菌引起的各种感染。在生产、储存和使用头孢呋辛的过程中,可能会产生一些杂质。这些杂质的存在可能会影响头孢呋辛的纯度和疗效,因此了解和控制这些杂质对于确保药物的安全性和有效性至关重要。头孢呋辛的杂质有多种,其中一些具有特定的CAS号、化学式和分子量。例如,头孢呋辛杂质33(Cefuroxime Impurity 33)的CAS号为929531-94-2,分子式为C16H16N4O9S,分子量为440.38。此外,还有其他一些头孢呋辛杂质,如头孢呋辛杂质A、B、C、D、E、F、G、H等。CATO标准品提供的头孢呋辛全套的杂质,这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分。广州佳途科技股份有限公司深知药物研发与质量控制的重要性,CATO标准品厂家,提供头孢呋辛全套的杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展,以满足客户在药物研发和质量控制方面的需求。
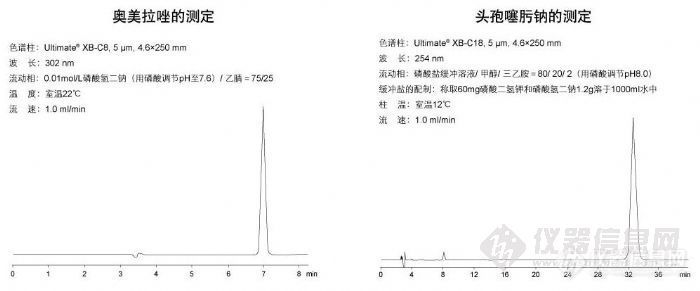
奥美拉唑的测定和头孢噻肟钠的测定http://ng1.17img.cn/bbsfiles/images/2009/11/200911021837_180180_1896702_3.jpg
最近在按照《农业部1025号公告-13-2008 动物性食品中头孢噻呋残留检测高效液相色谱法》测鸡肉中的头孢噻呋,遇到几个问题需要帮助:1.方法中需要将头孢噻呋用碘乙酰胺衍生,但是我将衍生过和没有衍生的头孢噻呋标样上机检测后发现二者保留时间和峰面积都没有区别,不知道是否已经衍生好了?2.方法中的提取液是用硼酸缓冲液配置的0.4%的二硫赤鲜醇,为什么我将衍生过和没有衍生的头孢噻呋标样用一定体积的提取液稀释后直接上机后都检测不到头孢噻呋了?
[color=#444444]有人做过液相色谱法测定头孢塞肟钠吗,液相条件是怎么样的,我看中国药典上的方法流动相偏碱性,对柱子不太好,而且流动相配起来很麻烦,有没有简单一点的方法[/color]
[center]丁基胶塞监管加强 头孢曲松钠缓慢恢复[/center] 为解决头孢类注射剂澄清度问题,保证产品质量,保障公众用药安全,日前,国家食品药品监督管理局就进一步加强对使用丁基胶塞生产头孢类注射剂的监督管理有关问题下发通知,要求各省(区、市)食品药品监督管理部门要在落实《关于做好注射用头孢曲松钠处理工作的通知》的基础上,加强对药品生产企业使用丁基胶塞的监管。 胶塞相容性检验有标准 通知称,在确保药品质量的同时,为保证注射用头孢曲松钠的供应,国家局委托中检所制定了注射用头孢曲松钠与丁基胶塞相容性加速实验方法。要求各省(区、市)食品药品监督管理部门将此方法转发辖区内头孢类注射剂药品生产企业并加强监督。注射用头孢曲松钠生产企业应依据此方法,在选择丁基胶塞生产药品时进行相容性实验,并对购入的每批丁基胶塞和生产的每批药品出厂前,依此方法进行检验,合格后方可出厂。对于其他头孢类注射剂,药品生产企业可参考该方法,自行建立适宜的快速验证方法。 通知规定,药品生产企业应根据产品注册时经相容性实验确定的丁基胶塞生产药品,若变更丁基胶塞的生产厂家,应对药品与变更的丁基胶塞相容性进行实验验证,符合要求并报所在地省(区、市)食品药品监督管理部门备案后方可使用。 通知强调,各地食品药品监督管理部门要加大对2009年1月1日以后生产的头孢类注射剂,特别是注射用头孢曲松钠的抽验力度,重点对生产环节产品的澄清度开展监督抽验,监督药品生产企业严格执行有关规定,确保产品的质量。对违法违规生产的,一经查实,依法处理。 小胶塞影响不小 一些企业界人士表示,此通知下发的主要目的是为了保证药品的质量安全。对购入的每批丁基胶塞和生产的每批药品出厂前进行注射用头孢曲松钠与丁基胶塞相容性加速实验也许会增加成本,但是此类检验是必要的,而且毫无疑义是正确的,毕竟药品质量安全是第一位的,必须要予以保证。 同时有观点认为,此通知对于企业来说未尝不是一件好事,在确定丁基胶塞相容性上有了标准的实验方法,才能切实操作。 此前,由于头孢曲松钠与丁基胶塞的相容性问题导致的溶液浑浊,国家食品药品监督管理局曾下发《关于做好注射用头孢曲松钠处理工作的通知》(食药监市函[2008]118号),要求注射用头孢曲松钠生产企业自查自检,并于2008年12月1日前收回由于丁基胶塞原因而有可能导致澄清度不合格的产品。对2008年12月1日以后在药品流通、使用环节发现澄清度不合格注射用头孢曲松钠,按《药品管理法》相关规定进行查处。 这一纸公文对于国内众多头孢曲松制剂企业无疑是当头棒喝。许多企业因此关闭头孢曲松钠生产线或转产。自1998年罗氏芬专利期满后,头孢曲松在我国得到迅猛发展。因其市场需求量大、产品附加值高、临床疗效突出,迅速崛起为全身抗感染用药金额之首。同时它的成长改变了头孢类抗生素产业格局,扩大了上游中间体7-ACA的需求,成为头孢抗生素的核心品种。此次的查处,加之受困于反倾销等贸易壁垒及头孢曲松钠与含钙溶液同时使用时产生的安全性不良事件等信息,2008年,头孢曲松钠在多重打击下份额锐减。 质量、成本、份额存矛盾 “丁基胶塞质量参差不齐,而药品多种多样,针对性的选择缺乏标准和办法一直是困扰生产企业的突出问题。”中国化学制药工业协会秘书长周燕表示。 专家指出,药品的性质千差万别,要想使一种丁基胶塞的配方适用于所有药品是不太可能的,应该根据各种药品性质的不同以及胶塞与药物的相容性(稳定性)试验,来选择与药物匹配的胶塞产品。头孢曲松只是其中比较突出的一个例子,其他一些药品也有存在此类问题。我国目前胶塞配方品种较少,还不能满足很多药品的包装要求。 业内人士表示,实际上使用复膜胶塞是解决头孢曲松钠药品相容性的一个比较简单的方法,并且该胶塞有数据证实其在药品有效期内的稳定性。但由于国内头孢曲松钠处于低价竞争状态,出于成本原因,复膜胶塞并未被业内普遍接受。 分析认为,头孢曲松钠从1999年的200元左右直到今天的几元钱一支,产品的利润空间不断缩小,目前几近无利可图的情况下,提高质量与降低成本、扩大市场份额之间的矛盾激化。 “头孢曲松钠正在缓慢恢复中。”健康网首席研究员吴惠芳则表示。 信息来源:医药经济报
那位仁兄做过注射用头孢噻肟钠,选用的是什么色谱柱,及相应的流动相 本人采用2010药典方法,使用创新通恒的色谱柱,主峰及杂质峰的拖尾都非常严重。再不改变流动相的情况下,用哪种色谱柱的比较好 2010药典的色谱条件: 用十八烷基硅烷键合硅胶为填充剂;以磷酸盐缓冲液(取无水磷酸氢二钠至量瓶中,加水溶解并稀释至刻度,用磷酸调节值至)-甲醇(:)为流动相;检测波长为"FONT-SIZE: 10.5pt; FONT-FAMILY: 'Times New=" New? Roman?;
头孢类抗生素在食用动物中的有效分析一直是热点。分享一种分子印迹固相萃取联合高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url]紫外检测器(MISPE-HPLC-UV)检测食品样品中头孢噻呋钠(CTFS)的方法。在该方法中,首先合成了一种环保的分子印迹聚合物(MIP)并用作吸附剂,它对水中的CTFS表现出优异的选择性,并且可以在1小时内达到吸附平衡。在优化的条件下,CTFS 在 0.005–1.0 mg L -1范围内获得了良好的线性,定量限为 0.0015 mg L -1,在牛奶、鸡肉、猪肉和牛肉样品的三个加标水平下,平均回收率高于 91.9%(RSD 小于 8.5%)。20个循环后,用于CTFS的MISPE小柱的回收率仍高于95%,证明了MISPE-HPLC-UV方法对食品样品中CTFS的分析具有较高的灵敏度和选择性。相关研究详见https://doi.org/10.1016/j.foodchem.2021.129013
那位仁兄做过注射用头孢噻肟钠,选用的是什么色谱柱,及相应的流动相 本人采用2010药典方法,使用创新通恒的色谱柱,主峰及杂质峰的拖尾都非常严重。再不改变流动相的情况下,用哪种色谱柱的比较好2010药典的色谱条件: 用十八烷基硅烷键合硅胶为填充剂;以0.05mol/L磷酸盐缓冲液(取7.1g无水磷酸氢二钠至1000mL量瓶中,加水溶解并稀释至刻度,用磷酸调节pH值至6.25)-甲醇(85:15)为流动相;检测波长为235nm。
最近在做头孢检测,方法回收率一直不好,以下几个标准有做过的吗?怎么样?讨论下吧GB-T 21314-2007 动物源性食品中头孢匹林、头孢噻呋残留量检测方法 液相色谱-质谱/质谱法GBT 22942-2008 蜂蜜中头孢唑啉 头孢匹林 头孢氨苄 头孢洛宁 头孢喹肟残留量的测定 液相色谱-串联质谱法SNT 1988-2007 进出口动物源食品中头孢氨苄、头孢匹林和头孢唑啉残留量检测方法
各位大侠,我现在正在做毕业论文,检测头孢噻夫在大鼠体内的药物浓度,他要与血浆结合成二硫键,我在处理时也切开了二硫键,但是还是检测不出来,请大家给我出出主义,谢谢……讨论下!
为什么可以利用红外光谱分析法来区分不同的氨噻肟类头孢菌素药物
求助头孢噻呋的检测文献,国标已经有了太繁琐了。谁有好的文献发一下,谢谢
[摘要] 头孢噻呋为第3 代头孢菌素类抗生素, 其具有超广谱强效抗菌、药效持久、不易产生耐药性等特点。本文概述了头孢噻呋的抗菌活性、不良反应和休药期、临床应用及残留等诸多方面的最新研究进展。[关键词] 头孢噻呋 抗菌活性 临床应用[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=92355]头孢噻呋的研究新进展.pdf[/url]
1.概述REAGEN™头孢噻呋酶联免疫反应测试盒是利用竞争性的酶联反应原理,用于牛奶、尿液、组织(肝、肾、肉)、蛋、血清和血浆中头孢噻呋残留的定量检测。该试剂盒具有以下特点:Ø 快速,高回收率(75-105%),多种样品的低成本提取方法。Ø 高灵敏度(2ng/g或ppb)。Ø 高重复性。Ø 检测过程只需要不到2小时。 2.试剂盒原理REAGEN™头孢噻呋酶联免疫反应测试盒基于竞争性酶联反应原理,头孢噻呋已经包被于微孔板上。药物分析时,样品同头孢噻呋捕获蛋白共同被添加到板孔中。如果样品中含有药物,会竞争捕获蛋白,抑制捕获蛋白与板上包被的药物结合。加入酶标记的二抗,形成包被药物-捕获蛋白-酶标二抗复合物。加入底物后,产物的颜色强弱与样品中药物的浓度成反比。
新人有难,还请各位大仙帮助。我需头孢妥仑匹酯片的进口标准,有货源的给新人说声,感谢!我的邮箱ahwuyan@live.cn。
请问头孢噻肟钠残留溶剂中各溶剂的出峰顺序及大概时间,柱子是KB-1,条件参照药典
[color=#444444]本人做了头孢噻呋钠的样品,想用高效液相色谱分析一下,但是不知道具体的分析方法,想求助一下分析方法,谢谢[/color]

抗生素头孢喹肟的动物体内药动学分析 头孢喹肟是目前唯一一个动物专用第四代头孢类抗生素,具有抗菌谱广,抗菌活性强的特点,适用于非肠道用药;源于基本头孢菌素结构的化学修饰提供了头孢喹肟的两性离子性质。头孢喹肟的这一特性可以促进其迅速跨生物膜渗透作用(包括细菌细胞壁的孔蛋白),从而增强生物利用度,较第二代和第三代头孢菌素抗菌谱更广。它对临床重要细菌的染色体和质粒编码的β-内酰胺酶高度稳定。被用于治疗动物呼吸道的疾病,牛的急性乳腺炎和腐蹄病,小牛败血症,猪子宫炎,乳房炎,无乳综合征,马驹败血病,其也是治疗羊的各类疾病的药物。 材料和方法: 头孢喹肟,、色谱乙腈、色谱甲醇、三氟乙酸(TFA)、去离子水。 岛津高效液相色谱仪、SPD-10AVP UV-VIS检测器268纳米处进行检测、柱温箱40°C、Phenomenex Gemini C18色谱柱 (250 mm ×4.6 mm; 5u m)。 流动相为乙腈和0.1%三氟乙酸水溶液,以0.9 ml/min的流速进行洗脱。 标准溶液配制: 头孢喹肟的储备溶液通过直接称量干燥后的标准物质溶解于水中,浓度1mg/ ml,并将该溶液保存于-70℃。头孢喹肟标准溶液通过加入空白血浆配制成溶度为0, 0.02, 0.04, 0.10, 0.40, 1, 2, 4, 10,和 12 ug/ml的溶液。 样品制备:200ul血浆中加入1.5毫升微量离心管中,加入等体积的甲醇使蛋白质沉淀,离心(4000转/min)10分钟后,300ul的上清离心液移入新鲜小瓶中,加入150ul去离子水混合,再吸取50ul上清液进样分析。 液相方法的验证: 选择性-选择性通过分析空白血浆、加入头孢喹肟的血浆、从羊服用头孢喹肟药代动力学研究中获得的血浆样品进行评价,无内源性化合物对目标化合物的干扰。 线性标准曲线-本方法的线性通过在0.02-12ug/ml的范围内的校正曲线评价。 灵敏度-通过进样 0.01ug/ml-0.1 ug/ml评价其信噪比。 精密度和准确度-头孢喹肟样品分低中高浓度分别进样分析,每个浓度分别进样六次日间、日内测定。 回收率-为了计算头孢喹肟的绝对回收率分别加入 0.4ug/ml, 2ug/ml, 和10ug/ml浓度样品,每个浓度分别重复6次进行加入和提取。 稳定性-标准
美国药典标准测定头孢地尼含量色谱条件溶液A:14.2mg/ml无水磷酸氢二钠溶液B:13.6mg/ml磷酸二氢钾缓冲溶液:将溶液A与溶液B按2:1混合(pH7.0)溶液C:0.1%四甲基氢氧化铵水溶液,用1/10稀磷酸调节pH至5.5溶液D:37.2mg/mlEDTA二钠流动相:乙腈、甲醇、溶液C、溶液D (350:200:4500:2)系统适应性溶液:用缓冲溶液配制每0.2mg/ml头孢地尼RS和0.5mg/ml头孢地尼有关物质A RS标准溶液:用缓冲溶液配置0.2mg/ml头孢地尼RS标准品样品溶液:用缓冲溶液配制0.2mg/ml头孢地尼样品色谱柱:C18柱(5um,4.6*150mm)推荐:YMC-Pack ODS-AM(P/N:AM12S05-1546WT)检测波长:254nm柱温:40摄氏度流速:1.0ml/min进样量:5ul系统适应性样品:系统适应性溶液和标准溶液(注:头孢地尼有关物质A RS有4个色谱峰)拖尾因子:以头孢地尼峰计不得超过1.5(系统适应性溶液)分离度:头孢地尼有关物质A RS的第二个峰与头孢地尼峰的分离度不得小于1.2

各位好!有没有做过头孢替坦酸的?按照日本药典方法做头孢替坦酸有关物质实验的时候主峰前面出现了一个小峰,谱图如下:http://ng1.17img.cn/bbsfiles/images/2015/08/201508051144_559190_1866875_3.jpg实验条件:检测器:VWD;检测波长:254nm;色谱柱:C18色谱柱(L=250mm,5μm,φ=4.6mm);0.1mol/L磷酸溶液:取11.53g磷酸加水1000ml,摇匀,即得;流动相:0.1mol/L磷酸-色谱甲醇-色谱乙腈-色谱冰乙酸=1700:105:105:100。(此流动相临用新制)流速:2.0ml/min;柱温:40℃。样品前处理:取甲醇10ml,注入10μl于液相色谱仪。如果样品溶解用甲醇和水的话前面的峰就没有了,不知道什么情况。求各位大侠支招!
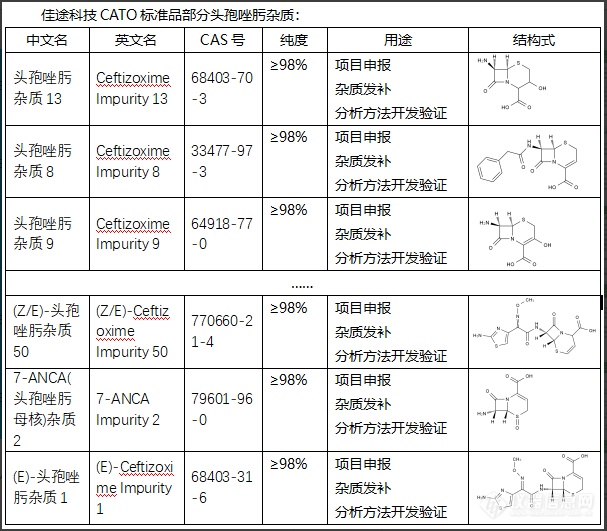
有关头孢唑肟杂质的作用,以下是要注意的一些可能性:1.负面作用:过多的杂质可能导致药物效力下降,并可能引发不良反应或副作用。例如,有些杂质可能导致过敏反应。2.毒性:某些杂质可能具有毒性。例如,某些杂质可能具有致癌性。3.影响药效:杂质可能会影响药物的生物利用度,即药物进入体内后能达到预期药效的能力。CATO标准品药品生产中的质量控制步骤非常重要,目的就是要尽可能减少杂质的存在。任何药品都必须经过严格的质量检测,确保其安全有效。[img=,607,531]https://ng1.17img.cn/bbsfiles/images/2024/02/202402041449269442_4660_6381668_3.png!w607x531.jpg[/img]
[size=5][b][size=3]硫酸头孢喹肟注射[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]量标准[/size][size=3]进口兽药质量标准[/size][size=3]硫酸头孢喹肟注射液[/size][size=3]Liusuan Toubaokuiwo Zhusheye[/size][size=3]Cefquinome sulfate Injection[/size][size=3] [/size][size=3]本品为硫酸头孢喹肟与油酸乙酯等配制而成的混悬注射液。含头孢喹肟(C23H24N6O5S2)应为标示量的90.0%~105.0%。[/size][size=3]【性状】 本品为类白色至浅褐色混悬液体;久置分层。[/size][size=3]【鉴别】(1)含量测定项下记录的色谱图中,供试品主峰的保留时间应与对照品峰的保留时间一致。[/size][size=3](2)取摇匀后的供试品2 ml,加水5 ml,稀盐酸1 ml,混匀,置超声浴中超声10分钟,弃去有机层,溶液显硫酸盐的鉴别反应(附录15页)。[/size][size=3]【检查】有关物质 照含量测定项下的方法。[/size][size=3]取摇匀后的供试品1.0 ml,加入流动相25.0 ml,置超声浴中超声5分钟,弃去有机层,取水层滤过,取续滤液10µ l,注入液相色谱仪,记录色谱图,2,3-环己基吡啶与头孢喹肟相对保留时间为0.20。按峰面积归一化法计算,2,3-环己基吡啶应不得过3.0%,其他单一杂质应不得过0.50%,杂质总量应不得过4.0%。[/size][size=3]水分 取本品,照水分测定法(附录58页,第一法)检查,含水分不得过0.2%。[/size][size=3]细菌内毒素 取摇匀后的供试品2 ml与细菌内毒素检查用水3 ml混匀,分成2等份,振摇30秒,离心15分钟(2000g),吸取水层1 ml,加1 mol/L氢氧化钠溶液0.06 ml调节pH值至6.5~7.5。用细菌内毒素检查用水按1:10稀释后,照细菌内毒素检查法(附录73页)检查,每1 mg头孢喹肟中含细菌内毒素的量应小于0.1 EU。[/size][size=3]无菌 取供试品8瓶,混合均匀,加入含6%吐温-80的蛋白胨缓冲液(1g/L)400ml,混匀,加入800×106单位青霉素酶(每1ml供试品溶液,加2×106单位青霉素酶),充分振摇,将供试品倒置,在37℃放置4小时;取供试品溶液,依法检查(附录79页,直接接种法),应符合规定。[/size][size=3]分散性 取本品1瓶,振摇30秒,将供试品转移置玻璃容器中,不得观察到结块或沉淀物。[/size][size=3]沉降 取本品1瓶,振摇30秒,取供试品10 ml置刻度试管中(内径1.0~1.5 cm),10分钟内不得沉淀。[/size][size=3]粒度 取摇匀后的供试品,置显微镜下检查,颗粒直径在5µ m以下应不得少于80%,10µ m以下不得少于90%,20µ m以下不得少于95%,50µ m以下不得少于100%。[/size][size=3]装量 按最低装量检查法(附录67页)检查,应符合规定。[/size][size=3]【含量测定】 照高效液相色谱法(附录24页)测定。[/size][size=3]色谱条件与系统适用性试验 用十八烷基硅烷键合硅胶为填充剂;取一水合高氯酸钠3.45g溶于1000 ml水中,加磷酸12 ml和乙腈90 ml,用三乙胺调节pH至3.6为流动相;检测波长为270 nm。取头孢噻肟约25 mg,溶于100.0 ml流动相中,另取头孢喹肟约25 mg,置25 ml量瓶中,精密加入上述头孢噻肟溶液1 ml,用流动相稀释至刻度。精密量取10µ l注入液相色谱仪,记录色谱图;计算头孢喹肟与头孢噻肟的分离度,应大于1.0。[/size][size=3]对照品溶液的制备 精密称取硫酸头孢喹肟对照品适量(约相当于头孢喹肟25 mg),置250 ml量瓶中,用流动相溶解并稀释至刻度,摇匀,即得。[/size][size=3]供试品溶液的制备 精密量取摇匀后的供试品适量(约相当于头孢喹肟50 mg),精密加入流动相100 ml,置超声浴中超声5分钟,弃去油层,滤过;精密量取续滤液5 ml,置25 ml量瓶,加流动相稀释至刻度,摇匀,即得。[/size][size=3]测定法 精密量取对照品溶液和供试品溶液各10µ l,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算,即得。[/size][size=3]【作用与用途】抗生素类药。主要用于治疗大肠杆菌引起的奶牛乳房炎,多杀性巴氏杆菌或胸膜肺炎放线杆菌引起的猪呼吸道疾病[/size][size=3]【用法与用量】肌内注射 一次量 每1 kg体重 牛1 mg 一日1次 连用2日 猪2~3 mg 一日1次 连用3日[/size][size=3]【休药期】牛 5日;猪 2日;弃奶期 1日。[/size][size=3]【规格】 50ml:1.25g[/size][size=3]【贮藏】遮光,25℃以下保存。[/size][size=3]【有效期】 2年。[/size][size=3]【生产企业】英特威国际有限公司(Intervet International GmbH)[/size][size=3] [/size][size=3] [/size][size=3]注:[/size][size=3]蛋白胨缓冲液(1g/L)[/size][size=3]蛋白胨(酪蛋白胨或肉蛋白胨) 1g[/size][size=3]KH2PO4 3.6g[/size][size=3]Na2HPO4• 2H2O 7.2g[/size][size=3]NaCl 4.3g[/size][size=3]最终pH为7.0±0.2[/size][size=3]溶液应无色澄清[/size][/b][/size]
在哪里可以买到测WOA--有机弱酸(如甲酸,乙酸,琥珀酸,己二酸)的标准品啊???需要多少钱呵???打电话给国家标准物质中心,他们说很多都没有,并且有腐蚀性,即使有也不方便运输, 这些弱酸的腐蚀性有必要使的我们诚惶诚恐吗???Shit!!!
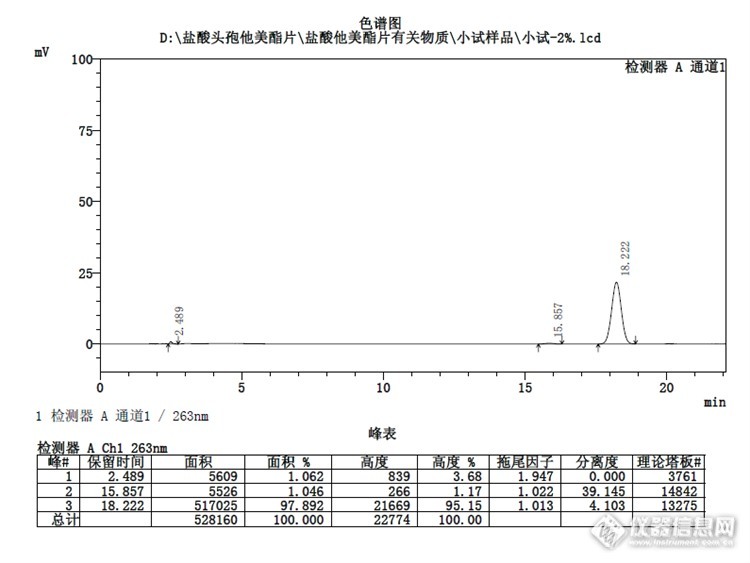
盐酸头孢他美酯是种广谱抗生素,可用于对它敏感细菌感染所引起的炎症。该产品为口服用。化学名:(6R,7R)-3-甲基-7-结构式:http://ng1.17img.cn/bbsfiles/images/2014/03/201403302127_494735_1621890_3.gif 英文名:Cefetamet Pivoxil Hydrochloride Tablets 药物别名:威锐片 成份:本品主要成分为盐酸头孢他美酯 性状:本品为薄膜衣片,除去包衣后呈白色、类白色,有引湿性。 药代动力学:本品单一剂量和多剂量的药代动力学参数基本一致。本品口服后,经过肠黏膜或首次经过肝脏时盐酸头孢他美酯被迅速代谢,在体内转变为头孢他美而发挥作用。本品随食物口服后,平均约55%的剂量转变为头孢他美。口服本品500mg后3~4小时,血药浓度达峰值4.1±0.7mg/L,分布容积为0.29L/kg,与细胞外水平一致。约22%头孢他美与清蛋白结合。年龄、肾脏及肝脏疾病对盐酸头孢他美酯的生物利用度无影响。抗酸剂(镁、铝、氢氧化物等)或雷尼替丁不改变本品生物利用度。本品90%以头孢他美形式随尿液排出,清除半衰期为2~3小时。肾衰竭患者,头孢他美的清除情况同肾功能成正比。 适应症:本品适用于敏感菌引起的下列感染:1.耳、鼻、喉部感染,如中耳炎、鼻窦炎、咽炎、扁桃体炎等。2.下呼吸道感染,如慢性支气管炎急性发作、急性气管炎、急性支气管炎等。3.泌尿系统感染,如非复杂性尿路感染、复杂性尿路感染(包括肾盂肾炎)、男性急性淋球菌性尿道炎等。注意事项 1.对青霉素类药物过敏者慎用。 2.若发生严重过敏反应,应立即停药,并紧急治疗。 3.在使用本品期间,由于肠道微生物的改变,可能导致伪膜性肠炎。若发生假膜性肠炎,应积极治疗(推荐使用万古毒素)。 4.本品应放到儿童触及不到的地方。 孕妇及哺乳期妇女用药:1.由于缺乏有关人类胎儿的临床数据,妇女妊娠期间,不推荐使用本品。若有对该药敏感的微生物严重感染时,必须充分权衡利弊。2.在乳汁中尚未发现本品的代谢物。 儿童用药:本品对新生儿的有效性和安全性尚无可靠的临床数据。 药物相互作用: 抗酸剂,H2受体拮抗剂对本品的药代动力学无影响。目前尚未见到本品对实验室检测值和/或方法有影响的报道,也未观察到伴随利尿药治疗的患者在使用本品时对肾功能的损伤。 药物过量: 若过量服用,发生严重反应,应洗胃,并采取对应治疗。 贮藏:遮光、密封、在干燥处保存。详见:http://baike.so.com/doc/6048874.html该品种国内批准文号有40个,见国家药监局网。截图如下:http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_646694_1621890_3.png试验条件:主要参照中国药典2010年版二部。用十八烷基硅烷键合硅胶为填充剂;以乙腈-甲醇-水-磷酸盐缓冲液(取无水磷酸氢二钠5.8g与磷酸二氢钾3.5g,加水溶解并稀释成1000ml)(360:95:500:45)为流动相;检测波长为263nm。取头孢他美酸和头孢他美酯对照品适量,用乙腈溶液(9→20)溶解并稀释制成每1ml中约含头孢他美酸0.05mg和含头孢他美酯1.4mg的混合溶液,取10μl注入液相色谱仪,头孢他美酯峰与头孢他美酸峰的分离度应不小于28.0,头孢他美酯峰与其相对保留时间约为0.9和1.1处杂质峰的分离度均应大于于2.0,理论板数按头孢他美酯峰计算不低于3000。取本品的细粉适量,加乙腈溶液(9→20)溶解并定量稀释制成每1ml中约含头孢他美1.0mg的溶液,滤过,取续滤液作为供试品溶液;精密量取供试品溶液适量,用乙腈溶液(9→20)定量稀释制成每1ml中约含头孢他美20μg的溶液,作为对照溶液。照含量项下的色谱条件,取对照溶液10μl注入液相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的25%;再精密量取供试品溶液与对照溶液各10μl,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的4.5倍。供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积(2.0%),各杂质峰面积的和不得大于对照溶液主峰面积的2.5倍(5.0%)。色谱柱信息:月旭Welchrom C18, 5μm, 4.6×250mm(货号:00310-02043;序列号:w13211564)试验图谱:1.系统适用性溶液:http://ng1.17img.cn/bbsfiles/images/2014/03/201403302057_494730_1621890_3.png2.供试品溶液:http://ng1.17img.cn/bbsfiles/images/2014/03/201403302112_494732_1621890_3.png3.对照溶液:http://ng1.17img.cn/bbsfiles/images/2014/03/201403302121_494734_1621890_3.png