我想做的是三磷酸腺苷二磷酸腺苷和磷酸腺苷,应该用什么柱子合适?
求助,二磷酸钾有机物的分析方法
摘要:对灭菌乳中乳果糖含量进行研究,初步探索了用紫外分光光度法对其进行测定的方法.牛奶在加热处理过程中, 部分乳糖异构为乳果糖, 经β-D- 半乳糖苷酶水解后生成半乳糖和果糖,通过酶转化为NADPH,确定其最大吸收波长为340nm,可在此波长下测出它的吸光度并计算出其质量浓度.结果表明:该方法灵敏度高,准确性好,适用于灭菌乳中乳果糖含量的测定。关键词:紫外分光光度 灭菌乳 乳果糖国务院办公厅《关于加强液态奶生产经营管理的通知》要求,完善液态奶标准并严格按标准组织生产,凡在灭菌乳 、酸牛乳等产品生产加工过程中使用复原乳的,不论数量多少 ,生产企业必须在其产品包装上醒目标注“复原乳”。农业部近发布的《巴氏杀菌乳和UHT灭菌乳中复原乳的鉴定》标准,为巴氏杀菌乳和UHT灭菌乳中复原灭菌乳中复原乳的乳成分的检测提供了科学依据 。 本实验采用紫外分光光度法对灭菌乳中乳果糖含量进行测定,并优化了试验方法,采用光谱扫描功能对最大吸收波长进行优化,并采用时间扫描功能监控酶的反应速率。确定在紫外光区340nm处测定乳果糖的方法,该方法灵敏度高,准确性好,对乳品中复原乳的监控起到积极作用。 1仪器和试剂1.1 仪器和设备1.1.1 UV-2550型紫外可见分光光度计(岛津有限公司)1.1.2 水浴或干燥箱: 温度能维持在40℃±2℃。1.2 试剂除非另有说明, 在分析中仅用分析纯试剂和GB/T 6682- 1992中一级水。碳酸氢钠(NaHCO3);过氧化氢(H2O2) , 质量分数为30%;辛醇(C8H18O);灭菌水;300g.L-1硫酸锌溶液;150 g.L-1亚铁氰化钾溶液;0.33mol.L-1氢氧化钠溶液;1mol.L-1氢氧化钠溶液;缓冲液A: pH= 7.5称4.8 g 磷酸氢二钠, 0.86 g 磷酸二氢钠和0.1 g 硫酸镁溶解于80mL水中, 用1mol.L-1 氢氧化钠溶液调整pH 到7.5±0.1 ( 20℃) , 稀释到100mL , 摇匀;缓冲液B: pH= 7.6称取14.00g三乙醇胺和0.25g硫酸镁溶解于80mL水中。用1 mol.L-1氢氧化钠溶液调整pH到7.6±0.1( 20

10,抽取5个版友);中奖名单:999youran(注册ID:999youran)zgx3025(注册ID:v2844608)m3071659(注册ID:m3071659)馨语(注册ID:huangdm)莫名其妙(注册ID:moyueqiu)http://ng1.17img.cn/bbsfiles/images/2016/09/201609261647_612177_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/09/201609261647_612178_1610895_3.jpg【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================三磷酸腺苷二钠注射液方法:HPLC应用编号:101389基质:药品应用编号:101389化合物:三磷酸腺苷二钠固定相:Platisil ODS色谱柱/前处理小柱:Platisil ODS 5u 150 x 4.6 mm样品前处理:【含量测定】三磷酸腺苷二钠的重量比 取本品适量,精密称定,加流动相溶解并定量稀释成每1ml中含0.4mg的溶液。色谱条件:检测波长:UV 259 nm 流动相:0.2mol/L磷酸盐缓冲溶液-甲醇(95:5) 缓冲溶液:取磷酸氢二钠35.8g、磷酸二氢钾13.6g,加水900ml溶解,用1mol/L氢氧化钠溶液调pH至7.0,加入四丁基溴化铵1.61g,加水至1000ml,摇匀。 洗脱方式:等度 柱温:35℃ 进样量:10 ul文章出处:P29关键字:三磷酸腺苷二钠注射液,2010版中国药典,HPLC,含量测定,铂金,Platisil ODS谱图:http://www.dikma.com.cn/Public/Uploads/images/atp(1).PNG图例:1. 一磷酸腺苷二钠;2. 二磷酸腺苷二钠;3. 三磷酸腺苷二钠
40mmol/L 果糖-6-磷酸溶液及12 mmol/L UDPG 溶液要求现配现用,药品很贵,这样很浪费,是否可以配好分装,于冰箱冷冻室贮存,每次用一管,使用时解冻?是否会影响其活性?
很多饮品中都在使用果糖,那么果糖到底有危害吗? 果糖是一种单糖,在自然界中主要存在于水果和蜂蜜等食品中,在植物中也有存在,尤以菊科植物为多。在各种天然糖中,果糖的甜度最高,其甜度大约是蔗糖的1.8倍。在蜂蜜中果糖约含49%。在体内,果糖可以转化为葡萄糖或合成糖元,但葡萄糖和糖元不能逆向转化为果糖,机体的果糖主要由肠道的二糖酶将蔗糖分解为葡萄糖和果糖而来。由于果糖可绕过糖酵解中的限速酶,故肝脏中的分解速度快于葡萄糖,且不受胰岛素的影响。正是由于果糖的这些特点,人们往往放松了对果糖的戒备。特别是一些糖尿病患者利用蜂蜜作为甜味剂,认为蜂蜜中的果糖不会造成血糖升高,以此作为养生的佳品。实际上,果糖吃多了危害性更大。在我们的血液中果糖的含量非常少,主要的糖是葡萄糖,我们平时所说的血糖也是指血液中葡萄糖含量。那么我们每天摄入的果糖哪儿去了?当果糖进入体内后,在肠道与肠粘膜上皮细胞载体蛋白结合后,能顺利地被吸收转化,果糖转化的主要场所是肝脏,可分别转化成糖原、葡萄糖和脂肪。所以,血液中果糖的含量不多。从这一点来看,果糖摄入过多后,同样会导致血糖的变化,并不是糖尿病患者安全的甜味剂。果糖不仅可以转化成葡萄糖,还可转化成脂肪,并引起脂肪合成增多。与葡萄糖相比,果糖转化合成脂肪更容易。在人体内有一种物质叫做磷酸果糖激酶,又被称为糖酵解的限制酶,对糖的酵解有调节作用,而果糖则不受磷酸果糖激酶的控制,因而很容易转化为合成脂肪需要的甘油部分。当果糖摄入量少时,果糖能转变为葡萄糖,使肝脏中糖原的储存量增加。但是,当果糖摄入量大时,果糖就成为合成脂肪不受限制的原料。在导致人体肥胖的因素中,可以说果糖的危害性甚至超过了葡萄糖和蔗糖。
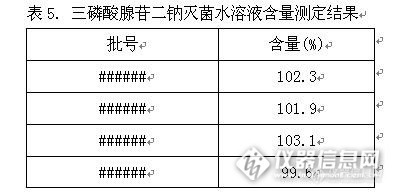
三磷酸腺苷二钠注射液含量方法学研究 三磷酸腺苷二钠的重量比 照高效液相色谱法(中国药典2010年版附录V D)测定。1.色谱条件与系统适用性试验 用十八烷基键合硅胶为填充剂;以0.2mol/L磷酸盐缓冲液(取磷酸氢二钠35.8g,磷酸二氢钾13.6g,加水900ml溶解,用1mol/L氢氧化钠溶液调节pH值至7.0,加入四丁基溴化铵1.61g,加水至1000ml,摇匀)-甲醇(95:5)为流动相;柱温为35℃;检测波长为259nm;理论板数按三磷酸腺苷二钠峰计算应大于1500;各色谱峰的分离度应符合规定。出峰次序依次为一磷酸腺苷钠、二磷酸腺苷二钠与三磷酸腺苷二钠。测定法 取精密量取A液适量,用流动相制成每1ml中含0.2mg的溶液;取20ml注入高效液相色谱仪,记录色谱图,按下式计算: http://ng1.17img.cn/bbsfiles/images/2012/12/201212272334_416487_2583865_3.jpg2. 测定三磷酸腺苷二钠的重量比溶液稳定性试验将供试品溶液在室温放置8小时,记录液相色谱图峰面积,结果见表1。 http://ng1.17img.cn/bbsfiles/images/2012/12/201212272335_416489_2583865_3.jpg验结果表明:本品溶液在8小时内测定稳定。3. 测定三磷酸腺苷二钠的重量比溶液重复性试验取供试品溶液连续进样6针,结果见表2。http://ng1.17img.cn/bbsfiles/images/2012/12/201212272336_416490_2583865_3.jpg试验结果表明:本品重复性良好。4. 测定三磷酸腺苷二钠的重量比溶液精密度试验精密量取040413批A液6份,用流动相制成每1ml中含0.2mg的溶液,分别测定重量比,结果见表3。 http://ng1.17img.cn/bbsfiles/images/2012/12/201212272336_416491_2583865_3.jpg试验证明,本方法测定三磷酸腺苷二钠重量比的精密度良好。5. 回收率试验精密称取三磷酸腺苷二钠约0.4g、0.5g、0.6g各三份,分别置10ml量瓶中,分别加入处方量的辅料空白溶液,超声助溶后,加水稀释至刻度,摇匀,滤过,量取续滤液1.0ml,加0.1mol/L磷酸盐缓冲液制成每1ml中含20μg的溶液,照分光光度法测定259nm波长处的吸收度,计算出总核苷酸。另取续滤液1.0ml,用流动相制成每1ml中含0.2mg的溶液,摇匀,精密量取20μl注入液相色谱仪,记录色谱图,计算三磷酸腺苷二钠重量比。含量按下式计算。测定结果见表4。三磷酸腺苷二钠含量(%)=总核苷酸×三磷酸腺苷二钠重量比 http://ng1.17img.cn/bbsfiles/images/2012/12/201212272337_416492_2583865_3.jpg平均回收率为99.84%;RSD为0.17%结论:由以上结果知,本品含量测定方法准确度较高。6. 含量测定取本品A液1.0ml,加0.1mol/L磷酸盐缓冲液制成每1ml中含20μg的溶液,照分光光度法测定259nm波长处的吸收度,计算出总核苷酸。另取本品A液1.0ml,用流动相稀释制成1ml中约含0.2mg的溶液,取20μl注入液相色谱仪,记录色谱图,计算三磷酸腺苷二钠重量比。按下式计算三磷酸腺苷二钠含量,结果见表5。http://ng1.17img.cn/bbsfiles/images/2012/12/201212272338_416494_2583865_3.jpg 计算公式:三磷酸腺苷二钠含量(%)=总核苷酸×三磷酸腺苷二钠重量比。

大家好: 按照15版药典,检测阿拉伯胶的“葡萄糖和果糖”项目,结果是硅胶板在喷了显色剂,然后放入烘箱加热后,整个硅胶板都变黑了。.且后面研究发现,直接将显色剂喷到板上,板在烘箱中加热,板就变黑了。求助有此经验的同学,问题会出在哪里?我们自己调查的结果可能是如下几个方面,:1- 硅胶板质量问题(用了2个品牌的板,国药集团和上海信宜的,都出现了这样的问题,可能性小);2- 显色剂有问题(用的都是新开瓶的试剂,可能性小);3- 药典的方法有问题,要求用的硅胶G板,是不是应当用不同的板?附:检验方法葡萄糖和果糖 取本品0.1g ,置离心管中,加1%三氟乙酸溶液2 m l ,强力振摇使溶解,密塞120°C加热1 小时,离心,小心转移上层液至50ml烧杯中,加水10ml减压蒸发至干. 残渣加水0 .1m l及甲醇0.9ml,离心分离沉淀。如有必要,用醇1ml稀释上层清液。另分别取阿拉伯糖、半乳糖、葡萄糖、鼠李糖及木糖对照品各lOmg于lm l水中,用甲醇稀释至10ml,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各10μl,分别点于同一硅胶G 薄层板上,以1 .6%磷酸二氢钠溶液-正丁醇-丙酮(10:4 0: 50)为展开剂,展开,取出,晾干,喷以对甲氧基苯甲醛溶液(取对甲氧基苯甲醛0.5ml,加冰醋酸10m丨,甲醇8 5 m l,琉酸5ml,摇匀,即得)至恰好湿润,立即在110C加热10分钟,放冷,立即检视,对照品溶液应显示的5个淸晰分离的斑点,从下到上的顺序依次为半乳糖(灰绿色或绿色)、葡萄糖(灰色)、阿拉伯糖(黄绿色)、木糖(绿灰色或黄灰色)、鼠李糖(黄绿色)。供试品色谱中,在与半乳糖和阿拉伯糖对照品色谱相应的位置之间,不得显灰色或灰绿色斑点。http://ng1.17img.cn/bbsfiles/images/2015/10/201510130951_569848_1835550_3.jpg
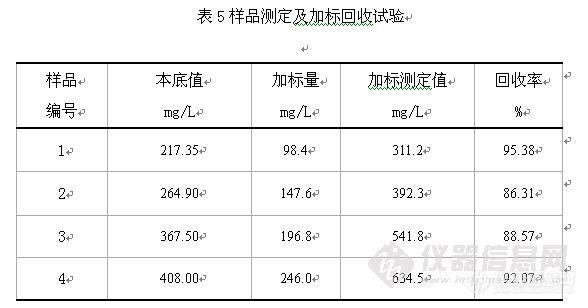
摘要:对灭菌乳中乳果糖含量进行研究,初步探索了用紫外分光光度法对其进行测定的方法.牛奶在加热处理过程中, 部分乳糖异构为乳果糖, 经β-D- 半乳糖苷酶水解后生成半乳糖和果糖,通过酶转化为NADPH,确定其最大吸收波长为340nm,可在此波长下测出它的吸光度并计算出其质量浓度.结果表明:该方法灵敏度高,准确性好,适用于灭菌乳中乳果糖含量的测定。关键词:紫外分光光度 灭菌乳 乳果糖 国务院办公厅《关于加强液态奶生产经营管理的通知》要求,完善液态奶标准并严格按标准组织生产 ,凡在灭菌乳 、酸牛乳等产品生产加工过程中使用复原乳的,不论数量多少 ,生产企业必须在其产品包装上醒目标注“复原乳”。农业部近发布的《巴氏杀菌乳和UHT灭菌乳中复原乳的鉴 定》标准,为巴氏杀菌乳和UHT灭菌乳中复原灭菌乳中复原乳的乳成分的检测提供了科学依据 。 本实验采用紫外分光光度法对灭菌乳中乳果糖含量进行测定,并优化了试验方法,采用光谱扫描功能对最大吸收波长进行优化,并采用时间扫描功能监控酶的反应速率。确定在紫外光区340nm处测定乳果糖的方法,该方法灵敏度高,准确性好,对乳品中复原乳的监控起到积极作用。 1仪器和试剂1.1仪器和设备1.1.1 UV-2550型紫外可见分光光度计(岛津有限公司)1.1.2 水浴或干燥箱: 温度能维持在40℃±2℃。1.2试剂除非另有说明, 在分析中仅用分析纯试剂和GB/T 6682- 1992中一级水。碳酸氢钠(NaHCO3);过氧化氢(H2O2) , 质量分数为30%;辛醇(C8H18O);灭菌水;300g.L-1硫酸锌溶液;150 g.L-1亚铁氰化钾溶液;0.33mol.L-1氢氧化钠溶液;1mol.L-1氢氧化钠溶液;缓冲液A: pH= 7.5称4.8 g 磷酸氢二钠, 0.86 g 磷酸二氢钠和0.1 g 硫酸镁溶解于80mL水中, 用1mol.L-1 氢氧化钠溶液调整pH 到7.5±0.1 ( 20℃) , 稀释到100mL , 摇匀;缓冲液B: pH= 7.6称取14.00g三乙醇胺和0.25g硫酸镁溶解于80mL水中。用1 mol.L-1氢氧化钠溶液调整pH到7.6±0.1( 20℃),稀释到100mL ,摇匀;缓冲液C将40.0mL缓冲液B 用水稀释到100mL ,摇匀;β-D- 半乳糖苷酶悬浮液用3.2 mol.L-1 硫酸铵溶液将活性为30 IU.mg-1 的β-D- 半乳糖苷酶制备成浓度为5mg.mL-1的悬浮液;葡萄糖氧化酶悬浮液;用灭菌水将活性为200 IU• mg-1 的葡萄糖氧化酶制备成浓度为20 mg.mL-1悬浮溶液;过氧化氢酶悬浮液:用灭菌水将活性为65000 IU.mg-1的过氧化氢酶制备成浓度为20 mg.mL-1的悬浮液;己糖激酶/葡萄糖-6-磷酸脱氢酶悬浮液(混酶):在1mL浓度为3.2 mol. L-1硫酸铵溶液中加入2 mg 活性为140 IU.mg-1 的己糖激酶和1 mg 活性为140 IU.mg-1的葡萄糖-6-磷酸脱氢酶,轻摇均匀,成悬浮液;磷酸葡萄糖异构酶悬浮液用3.2 mol. L-1硫酸铵溶液将活性为350 IU.mg-1的磷酸葡萄糖异构酶制备成浓度为2 mg.mL-1 的悬浮液; ATP 溶液将50 mg 5'-ATP-Na2 和50 mg 碳酸氢钠溶于1mL水中;NADP 溶液:将10mgβ-NADP-Na2溶于1mL水中。2 试验方法2.1 试液制备量取50.0mL样品到100mL容量瓶中, 用水稀释到刻度后混匀。2.2 纯化 吸取10.0mL试液于50mL锥形瓶中, 依次加入1.75mL亚铁氰化钾溶液、1.75mL硫酸锌溶液和6.5mL缓冲液A。每加入一种溶液后, 充分振荡均匀。全部溶液加完后, 静置10 min,过滤, 弃去最初的1mL~2mL滤液,收集滤液。2.3 水解乳糖和乳果糖吸取5.00mL滤液于10mL容量瓶中, 加入50μL的β-D-半乳糖苷酶悬浮液, 混匀后加盖。在40℃水浴或干燥箱培养至少10 h。2.4 葡萄糖氧化依次加入2.0mL 缓冲液C、100μL葡萄糖氧化酶悬浮液、1 滴辛醇、0.5mL 浓度为0.33mol.L -1氢氧化钠溶液、50 μL 过氧化氢和0.1 mL 过氧化氢酶悬浮液, 每加入一种试剂均要摇匀。全部溶液加完后, 在40℃水浴或干燥箱中培养3 h。冷却后稀释至10mL , 过滤, 弃去最初的1mL~2mL滤液, 收集滤液。2.5 空白依照2.1到2.4步骤处理空白溶液, 但不加β-D-半乳糖苷酶悬浮液。2.6 测定 在石英比色皿中依次加入1.00mL缓冲液B,0.100mLATP溶液,0.100mLNADP溶液,1mL滤液和1mL水, 每加入一种试剂均要摇匀.混合均匀后,静置3min.加入20μL混酶.混合均匀后上机,并同时做试剂空白. 反应过程大约10min,每隔1min记录一次吸光度的变化,等两次吸光度不再变化,反应停止。此过程中吸光度的变化见表1表1 加入混酶后反应吸光度的变化情况时间/min吸光度/Abs时间/min吸光度/Abs10.11370.20820.16880.21530.17490.22040.182100.23050.195110.23260.202120.232等反应到达终点后,记录下吸光度。加入20μL磷酸葡萄糖异构酶悬浮液,混合均匀后上机。反应过程大约15min,每隔1min记录一次吸光度的变化,等两次吸光度不再变化,反应停止.此过程中吸光度的变化见表2.表2 加入磷酸葡萄糖异构酶后反应吸光度的变化情况时间/min吸光度/Abs时间/min吸光度/Abs10.232720.38580.75830.46890.77640.557100.78250.649110.78660.732120.7862.7结果计算2.7.1吸光值差样品吸光值差△As的计算:△As = As2-As1空白吸光值差△Ab的计算:△Ab= Ab2- Ab1样品净吸光值差△AL的计算:△AL=△A s-△A b 2.7.2乳果糖含量乳果糖的含量以样品的质量浓度c 计, 数值以毫克每升(mg/L) 表示, 按下列公式计算: 式中:△AL-样品净吸光值差;ML-乳果糖的摩尔质量( 342.3 g/mol);ε-NADPH 在340 nm 处的摩尔吸光值( 6.3 L.mmol-1.cm-1) ;V1-比色皿液体总体积, V1=3.240mL ;V2-比色皿中滤液的体积, V2=1.00mL;d -比色皿光通路长度, d = 1.00cm;V-测试样体积( L) 。计算结果精确到小数点后一位。3 结果与讨论3.1最大吸收波长的选择在光谱模式下,测定标准系列的光谱图,仪器条件见表3。表3 仪器条件波长扫描范围/nm420~650光谱带宽/nm0.5采样间隔0.5扫描速度中速在此仪器条件下,扫描出标准系列的吸收光谱图,见图1。 图1 标准系列的吸收光谱图由以上标准系列的吸收光谱图可知,乳果糖的最大吸收波长为540nm,与国标方法的一致。 在样品测定过程中,同样做光谱扫描,结果见图2。图中实线为样品吸收光谱图,虚线为标准溶液吸收光谱图。从图中可以看出,样品和标准溶液的峰形基本吻合,最大吸收波长一致,基本不存在干扰对测定结果的影响。 图2 乳果糖样品吸收光谱图3.2精密度试验在重复性条件下获得六次独立测定结果,其标准偏差S和相对标准偏差见表4。表4 精密度试验结果 n=6样品编号测定值范围mg/L平均值mg/L标准偏差S相对标准偏差RSD1430.9~438.0434.72.4770.0062525.8~534.4529.82.9580.0063722.3~746.8735.09.2940.0134808.5~823.4816.05.3480.0073.3回收率试验本试验采用浓度为984 mg/L的乳果糖标准溶液进行加标回收。分别添加10.00、15.00、20.00、25.00mL的标准溶液进行试验,其结果见表5。表5样品测定及加标回收试验样品编号本底值mg/L加标量mg/L加标测定值mg/L回收率%1217.3598.4311.295.382264.90147.6392.386.313367.50196.8541.888.574408.00246.0634.592.074结论 试验表明:本方法准确性高,重现性好,相对标准偏差在0.006~0.013之间,加标回收率在86.31%~95.38%之间,适用于灭菌乳中乳果糖的测定。参考文献:[1] 中华人民共和国农业行业标准 NY/T939-2005.巴氏杀菌乳和UHT灭菌乳中复原乳的鉴定[S][2] 黄萌萌,王加启等,牛奶乳果糖的研究进展[J],中国乳品工业,2007,35(6):54~57.[3] 黄萌萌,王加启等,UHT灭菌乳贮存期间乳果糖的变化规律[J],中国乳品工业,2007,35(12):10~12.[4] 黄萌萌,王加启等,牛乳中乳果糖含量测定的快速酶法[J],中国农业大学学报,2007 ,12 (5) :57~60[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=146088]紫外分光光度法测定灭菌乳中乳果糖的含量[/url]
测果糖中的二氨基苯乙酮,标准曲线好做吗?为什么我的老是不出峰,且基线不是很稳.紫外220nm,1.0ml/min,柱子C1840度.进样量是300ul很大的,各位有谁做过,给支个招吧谢谢
由于要测一些酶的活性实验室订购了一下一些酶(试剂):辣根过氧化物酶葡萄糖氧化酶磷酸葡萄糖变位酶6-磷酸葡萄糖脱氢酶烟酰胺腺嘌呤二核苷酸磷酸(辅酶Ⅱ,NADP+)尿嘧啶核苷-5'-二磷酸葡萄糖(UDPG)D-果糖-6-磷酸二钠盐(6-磷酸果糖)D-葡萄糖-1-磷酸二钠盐(1-磷酸葡萄糖)现在要稀释这些酶(试剂)1.用蒸馏水稀释可以吗?如果不可以,用什么缓冲剂比较好?2.稀释后的溶液可以长时间保存吗?如不能,最长的时间是多久?小弟初入此道,望各位大侠细心解答,不胜感激!!
想知道齐墩果糖、阿洛糖、葡萄糖这三个极性的大小顺序是怎样?急啊,因为没有标准品了,所以希望大家帮忙啊
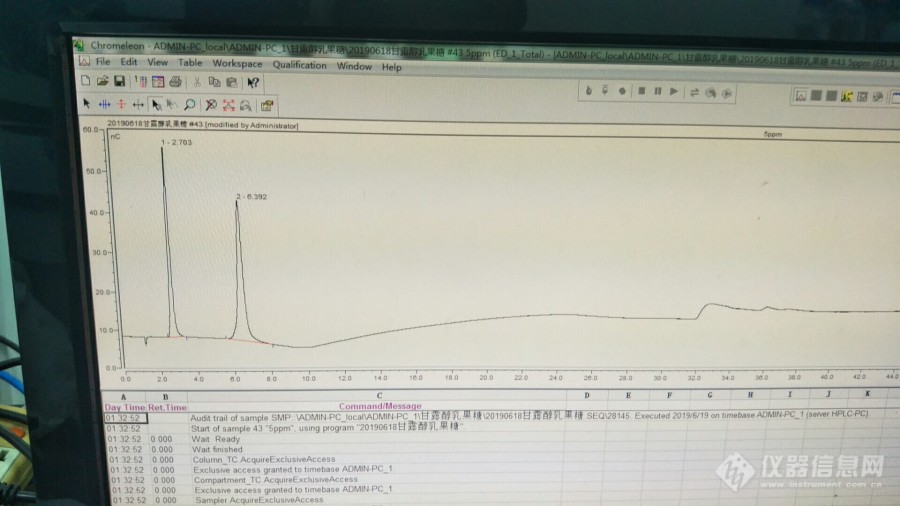
糖标准品的困惑-从购买到假乳果糖谈起最近为了测定一批甘露醇和乳果糖的样品(采用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法),原来乳果糖对照品几乎用完了,需要重新购,于是我在学校的虫洞采购平台上订购,从麦克林公司购买了乳果糖的对照品,一般而言,我不可能去验证糖对照品的准确性。将对照品给学生后,就把以前的色谱条件交给她们,让她们去做。做了几次后,学生反映,跟原来的结果不一样,保留时间对不上,我自己也没仔细查看,就跟学生说,这样品做了数百个了,条件和色谱柱都是固定不变了,不会有问题。不行,继续试,不行,再继续做。在几次失败后,学生无意用了原来剩下的标样试了一下,发现跟新买来的标样保留不一样,跑过来跟我说,这时我才有点醒悟。在仔细观察了色谱图,并查阅色谱条件后,我明白学生为什么做不出来的原因。买来的乳果糖标样不对,因为原来的乳果糖标样不止买过一次,十年来都没出过问题。而且从色谱图的保留时间看,买来的乳果糖标样出峰时间在单糖的位置,肯定是糖标样有问题。本来我想狠狠批评学生,但也怪我,我之前没有仔细查看色谱图,我负有不可推卸的责任!学生第一次做,缺乏经验,但对于单糖双糖的保留时间位置,应该有感性的认识,我只能教育他们,并告诉他们判断的依据。客户在催,我只能再从网上订购,这次另外换了一家公司,从迈瑞尔公司订购了乳果糖。试剂到后,让学生先测试一下,是否是乳果糖。实验的结果跟从麦克林买来一样,不对,还是单糖不是双糖(乳果糖是双糖)。[img=,690,387]https://ng1.17img.cn/bbsfiles/images/2019/08/201908192347296833_4583_1617661_3.jpg!w690x387.jpg[/img]甘露醇和购买的假乳果糖的[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]图[img=,690,387]https://ng1.17img.cn/bbsfiles/images/2019/08/201908192348130616_5401_1617661_3.jpg!w690x387.jpg[/img]甘露醇和原来的乳果糖(原来试剂时间放长了,有变质,图不是很好,但能说明问题,)二次从二个不同的厂家采购相同的乳果糖,结果表明二者都不是乳果糖,都是单糖,可能是半乳糖(没核对),这个漏洞也太大了吧,说明麦克林和迈瑞尔对进货的乳果糖都没有检验,或者检验有缺失,万一出错,这是多么可怕的事,会对实验造成严重的后果,如果一个第一次使用这种糖的人,如果缺乏判断经验,不可想象。我不敢再买了,那个是真的?那些小的试剂公司更不敢碰。用户一边在催实验结果,另一边试剂还没着落,买进口保险吗?或许如此,但价格高很多了。时间上也不见得来得及。为了保险起见,我再次联系了第三家试剂公司,阿拉丁,通过电话沟通,让他们确认试剂的可靠性,如果有检验的话,单糖和双糖是极容易区分的。在他们保证后,第三次购买了乳果糖,实验结果表明,这次购买的是正确的,跟留下来的乳果糖是同一种糖,实验终于可以进行了。通过这次事件,我预感到,试剂市场可能存在一定的乱象,一旦出现滥竽充数,如果不加检验,一些小公司可能根本没有能力判断。错误试剂会对实验结果造成严重的后果。但是让用户去检验试剂的可靠性,虽然我能做到,但是测试成本会远远高于购买的成本。而一般用户,根本没有能力。这也许是低价造成的恶果!大家是否有相同的经历!!!
三磷酸腺苷二钠如何定性啊?我的样品是白色晶体,如何确定里面含有三磷酸腺苷二钠,十万火急,完望大侠们救我[em14] [em14] [em14]
[em0716] 最近要做果糖中乙醇含量的测定,标准中要求是用二乙烯苯-乙基乙烯苯型高分子多孔小球为固定相的毛细管柱,可是我现在没有这种柱子,现有的柱子有HP-5、DB-624、SPB-5三种柱子,请问有没有哪根柱子可以替代的啊?PS:我们是用的溶剂是水。
如何鉴定三磷酸腺苷二钠啊,哪位大侠帮帮我啊
[size=16px][font=宋体, SimSun][b][/b][/font][font=宋体, SimSun]与食品工业常用的甜味剂不同,结晶果糖是货真价实的“糖”,而且被誉为“健康新糖源[i][/i]”。 [/font][font=宋体, SimSun][/font][font=宋体, SimSun]结晶果糖即己酮糖,是一种天然存在的糖,且甜度最高,其甜度为蔗糖的1.3-1.8倍。[/font][font=宋体, SimSun][/font][font=宋体, SimSun]结晶果糖易溶于水(20℃时溶解度为3.5g/mL)与乙醇,不溶于乙醚,为无臭的白色结晶性粉末。[/font][font=宋体, SimSun][/font][font=宋体, SimSun]对光、热稳定,易吸湿。纯净的果糖呈无色针状或三棱型结晶,故称结晶果糖。[/font][font=宋体, SimSun][/font][font=宋体, SimSun]结晶果糖在人体内代谢比葡萄糖快,容易被机体吸收,且不依赖胰岛素,对血糖影响很小,适用于葡萄糖代谢及肝功能不全的患者补充能量,与脂肪同食,可抑制人体脂肪的过量储存,同时它还具有促进有益细菌繁殖,改善肠功能和代谢,促进钙吸收,不致龋齿等特性。[/font][font=宋体, SimSun][/font][font=宋体, SimSun]结晶果糖与蔗糖、麦芽糖一样可被小肠消化、吸收,是人体的营养来源。糖尿病人、肥胖人群、儿童也可以放心食用。[/font][/size]
求助:托吡酯和果糖二丙酮的质量标准(右完整分析方法)
[size=4][/size] 第一张谱是果糖的,下面那张是生成物的我的反应是果糖和酸酐反应,果糖的-OH氢被取代,生成酯。不知道怎么分析取代位置,还有第二张图谱上的H的积分高了很多,可是不知道怎么解释。请教一下各位高手!谢谢!
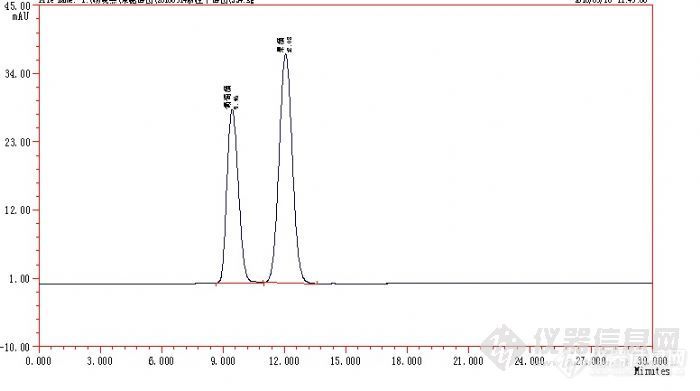
摘 要: 目的:建立并验证了用高效液相色谱-示差折光检测器测定果葡糖浆中果糖和葡萄糖含量的检测方法;方法:以水为溶剂,Ca型阳离子交换柱进行分离;以相对保留时间定性,色谱峰面积定量;结果:该方法平均回收率为98.33%~102.69%,RSD为0.865%~1.253%。检测限(S/N=3)分别为葡萄糖:1.94ug/ml;果糖2.49 ug/ml;结论:实验表明该方法对果葡糖浆中的葡萄糖和果糖含量的测试简单、可靠。关键词:示差折光检测器;果葡糖浆;Ca型阳离子交换柱。HPLC-RI测试果葡糖浆中的果糖和葡萄糖摘 要: 目的:建立并验证了用高效液相色谱-示差折光检测器测定果葡糖浆中果糖和葡萄糖含量的检测方法;方法:以水为溶剂,Ca型阳离子交换柱进行分离;以相对保留时间定性,色谱峰面积定量;结果:该方法平均回收率为98.33%~102.69%,RSD为0.865%~1.253%。检测限(S/N=3)分别为葡萄糖:1.94ug/ml;果糖2.49 ug/ml;结论:实验表明该方法对果葡糖浆中的葡萄糖和果糖含量的测试简单、可靠。关键词:示差折光检测器;果葡糖浆;Ca型阳离子交换柱。HPLC-RI determination of Glucose and Fructose which in High Fructose Corn Syrup Abstract: Objective: Established and tested the Glucose and Fructose which in Fructose Corn Syrup using HPLC-RI. Methods: Using water as solvent, Cation exchange column with Ca type for separate; qualitative with relatively retention time and quantitative with peak area; Results: The average recovery rate is 98.33%~102.69%, RSD is 0.994%~1.377%, and the limit of detection(S/N=3) respectively as Glucose: 1.94ug/ml; Fructose: 2.49 ug/ml; Conclusion: the experiment shows that this method is simple and reliable for the control of Glucose and Fructose which in High Fructose Corn Syrup.Key words: RI Detector; High Fructose Corn Syrup; Cation exchange column with Ca type. 果葡糖浆是由植物淀粉水解和异构化制成的淀粉糖晶,是一种重要的甜味剂。本品为无色或浅黄色、透明的黏稠液体。甜味柔和,具有果葡糖浆特有的香气,无异味。无正常视力可见杂质。因为它的组成主要是果糖和葡萄糖;故称为“果葡糖浆”。 果葡糖浆是由葡萄糖和果糖组成的一种混合生物酶转化糖浆,同时也是一种高甜度的淀粉糖,除作为糖源可替代蔗糖应用于食品加工外,果葡糖浆还具有蔗糖所不具备的优良特性,如在口感上,越冷越甜;甜度;在风味上具有不掩盖性;冰点温度低,以及在营养和代谢方面的功能性作用等。国家标准GB/T 20882-2007果葡糖浆中,将其分为两种类型:F42型(果糖含量不低于42%的果葡糖浆)和F55型(果糖含量不低于55%的果葡糖浆)。其质量要求为:对于果葡糖浆的成分控制,目前常采用HPLC法进行控制。 1 实验部分1.1 仪器和试剂[s
[align=center][b][font=宋体][font=宋体]基于《[/font]NYT939-2016[font=宋体]》标准乳果糖含量测定的操作细则[/font][/font][/b][/align][font=宋体]1 [/font][font=宋体]检测原理[/font][font=宋体][font=宋体]牛奶仔加热处理过程中,部分乳糖结构异构为乳果糖,经[/font]β-D-半乳糖苷酶水解后生成半乳糖和果糖,通过酶法测定产生的果糖量计算牛乳中乳果糖含量。[/font][font=宋体]2 试剂与材料[/font][font=宋体]2.1 碳酸氢钠(NaHCO[/font][sub][font=宋体]3[/font][/sub][font=宋体])[/font][font=宋体]2.2 过氧化氢(H[/font][sub][font=宋体]2[/font][/sub][font=宋体]O[/font][sub][font=宋体]2[/font][/sub][font=宋体][font=宋体]),质量分数为[/font]30%[/font][font=宋体]2.3 辛醇(C[/font][sub][font=宋体]8[/font][/sub][font=宋体]H[/font][sub][font=宋体]18[/font][/sub][font=宋体]O)[/font][font=宋体]2.4 灭菌水[/font][font=宋体]2.5 300g/L硫酸锌溶液[/font][font=宋体] [font=宋体]称量[/font]534g ZnSO[/font][sub][font=宋体]4[/font][/sub][font=宋体]7H[/font][sub][font=宋体]2[/font][/sub][font=宋体]O定容到1L水中[/font][font=宋体]2.6 150g/L亚铁氰化钾溶液[/font][font=宋体] [font=宋体]称量[/font]17.2g K[/font][sub][font=宋体]4[/font][/sub][font=宋体][Fe(CN)[/font][sub][font=宋体]6[/font][/sub][font=宋体]]?3H[/font][sub][font=宋体]2[/font][/sub][font=宋体]O定容到100ml水中[/font][font=宋体]2.7 0.33mol/L氢氧化钠溶液(NaOH)[/font][font=宋体] [font=宋体]称量[/font]3.3g氢氧化钠定容到250mL水中[/font][font=宋体]2.8 3.2mol/L硫酸铵溶液[/font][font=宋体] [font=宋体]称量[/font]42.28g (NH[/font][sub][font=宋体]4[/font][/sub][font=宋体])[/font][sub][font=宋体]2[/font][/sub][font=宋体]?SO[/font][sub][font=宋体]4[/font][/sub][font=宋体][font=宋体]定容到[/font]100ml水中[/font][font=宋体]2.9 1mol/L氢氧化钠溶液(NaOH)[/font][font=宋体]2.10 缓冲液A:pH=7.5[/font][font=宋体][font=宋体]称[/font]4.8g磷酸氢二钠(Na[/font][sub][font=宋体]2[/font][/sub][font=宋体]HPO[/font][sub][font=宋体]4[/font][/sub][font=宋体][font=宋体])[/font],0.86g磷酸二氢钠(NaH[/font][sub][font=宋体]2[/font][/sub][font=宋体]PO[/font][sub][font=宋体]4[/font][/sub][font=宋体]H[/font][sub][font=宋体]2[/font][/sub][font=宋体]O)和0.1g硫酸镁(MgSO[/font][sub][font=宋体]4[/font][/sub][font=宋体]7H[/font][sub][font=宋体]2[/font][/sub][font=宋体]O)溶解于80mL水中,用1mol/L氢氧化钠溶液调整pH到7.5±0.1(20℃),稀释到100ml,摇匀。[/font][font=宋体][font=宋体](注:若是[/font]NaH[/font][sub][font=宋体]2[/font][/sub][font=宋体]PO[/font][sub][font=宋体]4[/font][/sub][font=宋体]2H[/font][sub][font=宋体]2[/font][/sub][font=宋体]O则称量0.972g)[/font][font=宋体]2.11 缓冲液B: pH=7.6[/font][font=宋体] [font=宋体]称取[/font]14.00g三乙醇胺[N(CH[/font][sub][font=宋体]2[/font][/sub][font=宋体]CH[/font][sub][font=宋体]2[/font][/sub][font=宋体]OH)3HCl]和0.25g硫酸镁(MgSO[/font][sub][font=宋体]4[/font][/sub][font=宋体]7H2O)溶解于80ml水中。用1mol/L氢氧化钠溶液调整pH到7.6±0.1(20℃),稀释到100ml,摇匀。[/font][font=宋体]2.12 缓冲液C[/font][font=宋体][font=宋体]将[/font]40.0ml缓冲液B用水稀释到100ml,摇匀。[/font][font=宋体]2.13 β-D-半乳糖苷酶悬浮液[/font][font=宋体][font=宋体]用[/font]3.2mol/L硫酸铵溶液将β-D-半乳糖苷酶制备成浓度为150U/100μl的悬浮液。[/font][font=宋体][font=宋体]若[/font]β-D-半乳糖苷酶酶活为8.9U/mg,则称量337㎎的β-D-半乳糖苷酶,用3.2mol/L硫酸铵溶液定容到2ml;若β-D-半乳糖苷酶酶活为10.3 U/mg,则称量292㎎的β-D-半乳糖苷酶,用3.2mol/L硫酸铵溶液定容到2ml。[/font][font=宋体]2.14 葡萄糖氧化酶悬浮液[/font][font=宋体] [font=宋体]用灭菌水将活性为[/font]200U/mg的葡萄糖氧化酶制备成浓度为20mg/ml(4000U/ml)悬浮溶液。[/font][font=宋体]2.15 过氧化氢酶悬浮液[/font][font=宋体][font=宋体]用灭菌水将活性为[/font]40000—60000U/mg(18mg protein/ml)的过氧化氢酶制备成15000U/ml的悬浮液。(要求15000U/样品管)[/font][font=宋体][font=宋体]可以取[/font]1.2ml活性为40000—60000U/mg(18mg protein/ml)的过氧化氢酶定容到50ml灭菌水,每个样品管加1ml;或者直接向每个样品管中加入21μl的该过氧化氢酶。[/font][font=宋体]2.16 己糖激酶/葡萄糖-6-磷酸脱氢酶悬浮液[/font][font=宋体] [font=宋体]在[/font]0.4ml浓度为3.2mol/L硫酸铵溶液中加入1mg活性为187U/mg或2mg活性为100U/mg的己糖激酶/葡萄糖-6-磷酸脱氢酶,轻摇均匀,成悬浮液。[/font][font=宋体]2.17 磷酸葡萄糖异构酶悬浮液[/font][font=宋体]2.18 ATP溶液[/font][font=宋体] [font=宋体]将[/font]50mg 5′-ATP-Na[/font][sub][font=宋体]2[/font][/sub][font=宋体][font=宋体]和[/font]50mg碳酸氢钠溶于1ml水中。[/font][font=宋体]2.19 NADP溶液[/font][font=宋体] [font=宋体]将[/font]10mgβ-NADP-Na[/font][sub][font=宋体]2[/font][/sub][font=宋体][font=宋体]溶于[/font]1ml水中。[/font][font=宋体] [/font][font=宋体]3 分析步骤[/font][font=宋体]3.1 试液制备[/font][font=宋体] [font=宋体]量取[/font]20.00ml样品和20.00ml水于锥形瓶中,混匀。[/font][font=宋体]3.2 纯化[/font][font=宋体][font=宋体]向锥形瓶中依次加入[/font]7.00ml亚铁氰化钾溶液、7.00ml硫酸锌溶液和26.0ml缓冲液A。每加入一种溶液后,充分振荡均匀。全部溶液加完后,静置10min,过滤,弃去最初的1ml-2ml滤液,收集滤液。[/font][font=宋体]3.3 水解乳糖和乳果糖[/font][font=宋体][font=宋体]慢速法:吸取[/font]5.00ml滤液于10ml容量瓶中,加入100μl的β-D-半乳糖苷酶悬浮液,混匀后加盖。在40℃水浴或干燥箱培养至少10h(10h—13h时间也不要太长)。[/font][font=宋体][font=宋体]快速法:吸取[/font]5.00ml滤液于10ml容量瓶中,加入200μl的β-D-半乳糖苷酶悬浮液,混匀后加盖。在50℃培养1h。[/font][font=宋体]3.4 葡萄糖氧化[/font][font=宋体][font=宋体]依次加入[/font]2.0ml缓冲液C、100μl葡萄糖氧化酶悬浮液、3滴辛醇、0.5ml浓度为0.33mol/L氢氧化钠溶液、50μl过氧化氢和1ml过氧化氢酶悬浮液(或直接加入21μl活性为40000—60000U/mg(18mg protein/ml)的过氧化氢酶原液),每加入一种试剂均要摇匀。全部溶液加完后,在40℃水浴或干燥箱中培养3.5h。冷却后稀释至10ml,过滤,弃去最初的1ml—2ml滤液,收集滤液。[/font][font=宋体]3.5 空白[/font][font=宋体][font=宋体]依照[/font]2.1到2.4步骤处理空白溶液,但不加β-D-半乳糖苷酶悬浮液。[/font][font=宋体]3.6 测定[/font][font=宋体] [/font][font=宋体]测定步骤见下表。[/font][table][tr][td][align=center][font=宋体]步骤[/font][/align][/td][td][align=center][font=宋体]空白[/font][/align][/td][td][align=center][font=宋体]样品[/font][/align][/td][/tr][tr][td][font=宋体]比色皿中依次加入:[/font][font=宋体]缓冲液B[/font][font=宋体]ATP溶液[/font][font=宋体] NADP溶液[/font][font=宋体] 滤液[/font][font=宋体] 水[/font][/td][td][font=宋体] [/font][align=center][font=宋体]1.00ml[/font][/align][align=center][font=宋体]0.100ml[/font][/align][align=center][font=宋体]0.100ml[/font][/align][align=center][font=宋体]1.00ml[/font][/align][align=center][font=宋体]1.00ml[/font][/align][/td][td][font=宋体] [/font][align=center][font=宋体]1.00ml[/font][/align][align=center][font=宋体]0.100ml[/font][/align][align=center][font=宋体]0.100ml[/font][/align][align=center][font=宋体]1.00ml[/font][/align][align=center][font=宋体]1.00ml[/font][/align][/td][/tr][tr][td=3,1][font=宋体]混合均匀后,静置3min (此步骤可省略)[/font][/td][/tr][tr][td][font=宋体]加入己糖激酶/葡萄糖-6-磷酸脱氢酶悬浮液[/font][/td][td][align=center][font=宋体]20μl[/font][/align][/td][td][align=center][font=宋体]20μl[/font][/align][/td][/tr][tr][td][font=宋体]混合均匀,等反应停止后(15min左右),记录吸光值[/font][/td][td][align=center][font=宋体]Ab1[/font][/align][/td][td][align=center][font=宋体]As1[/font][/align][/td][/tr][tr][td][font=宋体]加入磷酸葡萄糖异构酶悬浮液[/font][/td][td][align=center][font=宋体]20μl[/font][/align][/td][td][align=center][font=宋体]20μl[/font][/align][/td][/tr][tr][td][font=宋体]混合均匀,等反应停止后(25min左右),记录吸光值[/font][/td][td][align=center][font=宋体]Ab2[/font][/align][/td][td][align=center][font=宋体]As2[/font][/align][/td][/tr][tr][td=3,1][font=宋体]注1:以上反应均在同一比色皿中完成。[/font][font=宋体]注2:如果1ml滤液吸光值增加超过1.3,则减少样品滤液取样体积,注意增加水以保证比色皿中反应液总体积不变(3.24ml)。[/font][/td][/tr][/table][font=宋体]4 结果计算[/font][font=宋体]4.1 吸光值差[/font][font=宋体][font=宋体]样品吸光值差[/font]△As的计算:[/font][font=宋体] △As=(As2 - As1)[/font][font=宋体][font=宋体]空白吸光值差[/font]△Ab的计算:[/font][font=宋体] △Ab=(Ab2 - Ab1)[/font][font=宋体] [font=宋体]样品净吸光值差[/font]△AL的计算:[/font][font=宋体] △AL=△As - △Ab[/font][font=宋体]4.2 乳果糖含量 [/font][font=宋体][font=宋体]乳果糖的含量以样品的质量浓度[/font]C计,数值以毫克每升(mg/L)表示,按下列公式计算:[/font][font=宋体] [/font][font=宋体]C=[/font][font=宋体]△AL[/font][font=宋体] [/font][font=宋体]式中:[/font][font=宋体] △AL——样品净吸光值差;[/font][font=宋体] ML ——乳果糖的摩尔质量(342.3g/mol);[/font][font=宋体] [/font][font=宋体]——NADPH在340nm处的摩尔吸光值(6.3Lmmol-1cm-1);[/font][font=宋体] V1 ——比色皿液体总体积,V1=3.240mL;[/font][font=宋体] V2 ——比色皿中滤液的体积,V2=1.00mL;[/font][font=宋体] d ——比色皿光通路长度,d=1.00㎝;[/font][font=宋体] V ——测试样体积(L)。[/font][font=宋体] [font=宋体]计算结果精确到小数点后一位。[/font][/font][font=宋体][font=宋体](注:代入数值后公式即为[/font]C=1408.32×△AL)[/font][font=宋体]5 精密度[/font][font=宋体] [font=宋体]在重复性条件下获得两次独立测定结果的绝对差值不得超过算术平均值的[/font]5%。[/font][font='Times New Roman'] [/font]
最近实验室要做高果糖淀粉糖的检测,蜂蜜样品。按照“GB18932-2002蜂蜜中高果糖淀粉糖测定”这个方法。请高人指点下:GB18932-2002蜂蜜中高果糖淀粉糖测定这个国标里面用的这个“二苯胺盐酸盐”纯度有没有什么特别要求啊?这个是配显色剂用的,哪里有卖的啊?实验很急,最好有现成的卖!!!
[font=宋体, SimSun][size=20px][b]结晶果糖不是甜味剂[/b][/size][/font][font=宋体, SimSun][size=20px][b][/b][/size][/font][font=宋体, SimSun][size=15px]与食品工业常用的甜味剂不同,结晶果糖是货真价实的“糖”,而且被誉为“健康新糖源[i][/i]”。 [/size][/font][font=宋体, SimSun][size=15px][/size][/font][font=宋体, SimSun][size=15px]结晶果糖即己酮糖,是一种天然存在的糖,且甜度最高,其甜度为蔗糖的1.3-1.8倍。[/size][/font][font=宋体, SimSun][size=15px][/size][/font][font=宋体, SimSun][size=15px]结晶果糖易溶于水(20℃时溶解度为3.5g/mL)与乙醇,不溶于乙醚,为无臭的白色结晶性粉末。[/size][/font][font=宋体, SimSun][size=15px][/size][/font][font=宋体, SimSun][size=15px]对光、热稳定,易吸湿。纯净的果糖呈无色针状或三棱型结晶,故称结晶果糖。[/size][/font][font=宋体, SimSun][size=15px][/size][/font][font=宋体, SimSun][size=15px]结晶果糖在人体内代谢比葡萄糖快,容易被机体吸收,且不依赖胰岛素,对血糖影响很小,适用于葡萄糖代谢及肝功能不全的患者补充能量,与脂肪同食,可抑制人体脂肪的过量储存,同时它还具有促进有益细菌繁殖,改善肠功能和代谢,促进钙吸收,不致龋齿等特性。[/size][/font][font=宋体, SimSun][size=15px][/size][/font][font=宋体, SimSun][size=15px]结晶果糖与蔗糖、麦芽糖一样可被小肠消化、吸收,是人体的营养来源。糖尿病人、肥胖人群、儿童也可以放心食用。[/size][/font]
大家好,我是新手,我今天做了葡萄糖、果糖和蔗糖的检测,用的岛津的仪器,RID检测器,用的是这三种糖份的混标,结果葡萄糖和果糖像双胎胎连在一起分不开啊,流动相是乙腈+水(85+15),柱温30,流量1ml/min。请教大家,我要怎么改进才能把这两个峰分开呢
我用过Agilent Hi-Plex Pb以及示差检测器可以将葡糖糖、果糖及蔗糖很好的分离,但是我测的是植物幼嫩叶片中的这三种糖,能够获取的样品量非常少,有没有什么好的样品预处理的方法呢?我用纯水以及一定浓度的乙醇均预处理过样品,纯水处理后只能检测到葡糖糖、果糖,而乙醇处理后三种糖均能检测到,但是测到的葡萄糖、果糖量明显降低,均不是很理想。
测定果糖中的乙醛要测定30ppb,用的是填充柱,没有响应,有没有什么办法能检测出来呀换成毛细管柱的化一定能作出来吗?谢谢http://www.cqvip.com/qk/95647x/200506/20608144.html再帮我下载一下这篇文献吧,谢谢了大家推荐一款毛细柱吧
果糖胺是血浆中的蛋白质在葡萄糖非酶糖化过程中形成的一种物质,由于血浆蛋白的半衰期为17天,故果糖胺反映的是1-3周内的血糖水平。 果糖胺是血浆中的蛋白质与葡萄糖非酶糖化过程中形成的高分子酮胺结构类似果糖胺的物质,它的浓度与血糖水平成正相关,并相对保持稳定。它的测定却不受血糖的影响。由于血浆蛋白的半衰期为17~20天,故果糖胺可以反映糖尿病患者检测前1~3周内的平均血糖水平。从一定程度上弥补了糖化血红蛋白不能反映较短时期内血糖浓度变化的不足。果糖胺的测定快速而价廉(化学法),是评价糖尿病控制情况的一个良好指标,尤其是对血糖波动较大的脆性糖尿病及妊娠糖尿病,了解其平均血糖水平有实际意义。但果糖胺不受每次进食的影响,所以不能用来直接指导每日胰岛素及口服降糖药的用量。血清果糖胺正常值为1.64~2.64mmol/L,血浆中果糖胺较血清低0.3mmol/L。
糖心苹果糖度一般在那个范围值
质量标准:WS-10001-(HD-0787)-2002释放度:取本品,照释放度测定法,采用溶出度测定法(中国药典2000年版二部附录X C第一法)装置试验,以0.1mol/L盐酸溶液750ml为溶剂,转速为每分钟100转,依法操作,经2小时,取溶液10ml,滤过,作为供试品溶液(1)。加入0.2mol/L磷酸钠溶液250ml,继续运转60分钟,取溶液10ml,滤过,作为供试品溶液(2)。取供试品溶液(1)以0.1mol/L盐酸溶液为空白,在259nm波长处测定吸收度,吸收值不得大于0.08。取供试品溶液(2),以0.1mol/L盐酸溶液75ml与0.2mol/L磷酸盐缓冲液25ml混合液为空白,按C10H14N5Na2O13P3的吸收系数(E)为279计算出每片的释放量。应符合规定。问题来了:0.2mol/L磷酸钠溶液与0.2mol/L磷酸盐缓冲液,到底用哪个?一般来说,溶出介质采用磷酸盐缓冲液,没有用磷酸钠溶液的吧?请教!!!
我做过多次实验,总是分离不出来。 我的条件是: 流动相乙腈:水=85:15.,柱温为40度,柱子为氨基色谱柱(4.6mm*250mm),流速为1mL/min,进样体积为20ul。 我用这个方法做就把这三种糖分离不出来,蔗糖、果糖、葡萄糖的保留时间分别为3.760、3.761、3.760;峰面积为15086452、15119115、14780051。 有经验的朋友们有没有好的意见和方法,帮忙提供一下,谢谢!!!