
银杏酮酯中萜类内酯的含量测定方法学试验(新手上路) 根据相关文献资料,银杏酮酯中的萜类内酯含量测定方法主要有薄层扫描法、高效液相色谱法、差示检测法、ELSD法等。萜类内酯在紫外吸收较弱,极少量的黄酮杂质能严重干扰测定,紫外检测器检测较为困难,示差检测器灵敏度、稳定性和选择性相对较差。参照中国药典2005年版一部及目前大多数国家标准中多采用ELSD法测定萜类内酯的含量。方法学研究内容如下:1.主要仪器与试药SPD-10AP输液泵(日本岛津公司);ELSD2000蒸发光散射检测器(美国奥泰Alltech);SK3300H型超声清洗器(上海科导KUDOS);乙腈(色谱纯);四腈呋喃(色谱纯);水(重蒸水);其它试剂均为分析纯。银杏内酯A对照品、银杏内酯B、银杏内酯C及白果内酯(中国药品生物制品检定所提供)。2.对照品溶液的制备取在五氧化二磷干燥减压干燥器中放置过夜的白果内酯、银杏内酯A、银杏内酯B、银杏内酯C对照品分别约为5.0mg、5.0mg、3.0mg和2.0mg,精密称定,置同一10ml量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得(每1ml中含白果内酯、银杏内酯A、银杏内酯B、银杏内酯C分别为0.5mg/ml、0.5mg/ml、0.3mg/ml和0.2mg/ml)。3.试验条件的选择(1) 仪器条件流速:1.0ml.min-1,柱温:35℃,漂移管温度:115℃,氮气流速:3.0L/min。(2) 流动相的选择先后比较了正丙醇-四氢呋喃-水(1:15:84)、乙腈-四氢呋喃-水(1:1:6)、乙腈-四氢呋喃-水(11:11:78)。结果以乙腈-四氢呋喃-水([font=Times
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=31408]高含量银杏萜内酯富集方法研究[/url]
上次有朋友问到过银杏内酯,不过我们的情况似乎有所不同。我们的标样出峰总是前延得很厉害,即使含量很低也还是这样,不知道和那个帖子里提到的双峰有没有联系。但我们进的样品却没有前延,反而总有点脱尾。上次有朋友提到waters的某根柱子做这个效果不错,但我们这里不太好专门为了做一个样品而买柱子,所以恳请哪位大侠为我们分析一下可能的原因。另:上次我们这里有人做红霉素(大环内酯),结果也是比较奇怪。这只是偶然么?还是内酯类的样品做起来有什么特别需要注意的地方呢?请教。
我在做银杏叶帖类内酯时出现了问题,跑的时候开始还好好的,但跑了一段时间后,就出现双头峰,或肩峰(就是峰的肩膀出现了点小峰).换了新柱子后,情况还是如此,样品,流动相都没问题.怀疑是柱子跑内酯太久了,里面有强保留物质,有什么方法解决吗????
银杏(Ginkgo bilobaL.)归属于银杏科、银杏属,为中生代孑遗的稀有物种,目前为我国特产,有“活化石”之称。作为中药,常以其叶和种子入药。2020年版《中国药典》描述,银杏叶味甘、苦、涩、平,归心、肺经。有活血化瘀、通络止痛、敛肺平喘、化浊降脂之功效,临床主用于对瘀血阻络、胸痹心痛、中风偏瘫和肺虚咳喘等疾病的治疗。在血管相关性疾病治疗方面,取得了较好的临床疗效。 银杏酮酯(Ginkgo biloba extract50,GBE50)是将银杏叶经过“双重吸附、双重去除”等工艺提取,是我国自主开发研制的第五代新型银杏叶提取物,是银杏叶提取物的标准化产品。 银杏酮酯药物质量标准的测定: ①总黄酮醇苷含量为24.0%~35.0%;同时建立紫外--可见分光光度(UV)法测定银杏总黄酮,规定其含量为44.0%~55.0%; ②规定其萜类内酯(银杏内酯A、B、C和白果内酯)含量在6.0%~12.0%之间; ③毒性成分银杏酸含量≤5mgkg-1; ④建立指纹图谱检测指标,规定其相似度不得低于90.0%。 该提取物展现出较好的科研及药用开发价值,在血管性疾病中具有重要的临床应用价值。

10,抽取5个版友);中奖名单:999youran(注册ID:999youran)dyd3183621(注册ID:dyd3183621)WUYUWUQIU(注册ID:wulin321)zengzhengce163(注册ID:zengzhengce163)ZHAOGUANGXI(注册ID:ZHAOGUANGXI)http://ng1.17img.cn/bbsfiles/images/2016/07/201607151515_600659_708_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/07/201607151515_600660_708_3.png积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================银杏叶提取物中的内酯方法:HPLC基质:植物提取成分应用编号:101191化合物:银杏内酯BB;银杏内酯Gink.C;银杏内酯Gink.J;银杏内酯Gink.A;银杏内酯Gink.B固定相:Diamonsil C18色谱柱/前处理小柱:Diamonsil C18, 250 x 4.6mm,5 μm色谱条件:流动相:A :甲醇,B :水 梯度A/B (18/82) to A/B (45/55) in 30 min 流速:1.0 mL/min 检测:ELSD(SEDEX 55) 柱温:40 ℃关键字:银杏内酯,HPLC,Diamonsil C18,钻石一代,银杏内酯BB;银杏内酯Gink.C;银杏内酯Gink.J;银杏内酯Gink.A;银杏内酯Gink.B,ELSD谱图:http://www.dikma.com.cn/Public/Uploads/images/1-2.bmp图例:1. 银杏内酯BB;2. 银杏内酯Gink.C;3. 银杏内酯Gink.J;4. 银杏内酯Gink.A;5. 银杏内酯Gink.B
我想做从银杏黄酮中提取银杏内酯的生产,不知需要哪些设备和仪器?设备投资大约要多少?
序号:作者:[b]胡军华[size=12px]1,2[/size]钱频非[size=12px]1,3[/size]于桂芳[size=12px]1,2[/size]王雪[size=12px]1,2[/size]王振中[size=12px]1,[/size][size=12px]题名:[b]银杏二萜内酯葡胺注射液与一次性输液器的相容性考察[/b][/size][b]期刊:中国医药工业杂志[font=&][size=12px][color=#666666]. [/color][/size][/font]2020,51(06)[/b][size=12px][b]全文链接:[url=https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CJFD&dbname=CJFDLAST2020&filename=ZHOU202006017&uniplatform=NZKPT&v=chmA29uEAKaP8hXH7w2QzZ7RHLPqUTm30v1zTjBgPI9Dp0kJO0_WR1UryB1aND5w]银杏二萜内酯葡胺注射液与一次性输液器的相容性考察 - 中国知网 (cnki.net)[/url][/b][/size][/b]
请教 :我们现在在做银杏内酯的含量测定方法学,做到进样精密度度时用的是供试品溶液,结果RSD很大有5%-9%,但是用对照品溶液做精密度RSD就小好多在2%以下,用的是蒸发光散射检测器,漂移管温度80度,流速2.2 流动相是正丙醇:四氢呋喃:水=1:15:84 安捷伦色谱柱C18 请教高手帮忙 补充我们的样品是复方制剂,样品处理是参照药典方法银杏提取物中的方法
各位朋友大家好,最近在用药典方法检测银杏内酯时遇到了几个问题,想请大家帮忙解决一下,就是四氢呋喃做流动相,柱压总是一直在走高,最终导致柱子蹦开,起初是用国产的四氢呋喃,后来换用一瓶fisher的四氢呋喃,是不加稳定剂的那种,就不出现压力变化的现象,而且每次用完试剂后,我都是充氮气保存,但是最近情况是有个师妹做实验后忘记充氮气了,现在检测时发现压力有上去了,而且柱子也堵了,请问大家遇到过这种现象吗?怎么解决啊?
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=31407]大孔吸附树脂对银杏内酯和白果内酯吸附性能的研究[/url]
[color=#444444]波长选取 220nm 波速选择 1ml/min 但是流动相选择甲醇的话,内酯A B的峰分不开,出峰时间基本上是一样的,求大神指导?需要调什么才能使银杏内酯A B峰分开?[/color]
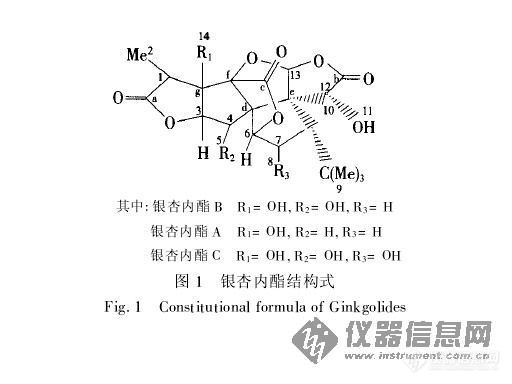
求教 银杏内酯B红外光谱中1630波数的峰是什么基团的峰?[img]http://ng1.17img.cn/bbsfiles/images/2005/11/200511250922_10678_1803986_3.jpg[/img]
脑卒中是全球致伤致残致死3大原因之一,据全球疾病负担统计2019年全世界有1 220万人发病[1],我国有394万人首发[2];另一统计称2020年我国有340万人首发并有约220万人留下残疾[3-4]。缺血性脑卒中(ischemic stroke,IS)约占卒中类型的85%[4-5]。IS预后结局差,复发率高而且极有可能造成后遗症如偏瘫、后肢痉挛、震颤等。其病理机制也十分复杂,涉及细胞过度自噬、离子失衡与谷氨酸过度释放、氧化应激与自由基、炎症爆发和神经细胞凋亡[5-7]等。 目前治疗IS的主要方法为重组组织型纤溶酶原激活剂(recombinant tissue-type plasminogen activator,rt-PA)静脉溶栓、手术取栓和神经保护。手术风险高,rt-PA治疗时间窗短,且有出血风险,符合治疗条件的病人不到10%[8],而神经保护的药物在临床上的效果不如动物实验那么有效,目前急需开发更安全可靠的治疗IS的用药。在长期的医学实践中,银杏叶提取物在治疗脑卒中和心肌梗死方面疗效显著[9]。其中,银杏内酯作为天然的血小板活化因子(platelet activating factor,PAF)受体拮抗剂,因其具有抗炎、抗氧化、抗凋亡和神经保护的作用[10-12]而越来越受到关注。 银杏二萜内酯葡胺注射液(Diterpene Ginkgolides Meglumine Injection,DGMI)以银杏叶提取物为原料,主要组成为银杏内酯A(ginkgolide A,GA,35%)、银杏内酯B(GB,60%)、银杏内酯C(GC,2%)、银杏内酯K(GK,2%),含总银杏内酯5 mg/mL[13],银杏二萜内酯成分达98%以上[14]。临床显示,DGMI可有效改善IS发病90 d时患者的神经缺损评分,同时改善患者认知和行动能力,并且在中老年患者中疗效优于银杏叶提取物注射液(金纳多)[15-18],Zhao等[15]认为DGMI与rt-PA联用治疗急性卒中效果更佳。最新一项临床研究发现,单独使用DGMI对急性缺血性脑卒中治疗有效[19]。也有多项体内外实验证明DGMI具有改善脑缺血再灌注损伤(cerebral ischemia reperfusion injury,CIRI)的作用,主要与PAF受体[20]、磷脂酰肌醇3-激酶(phosphatidylinositol 3-kinase,PI3K)- 蛋白激酶B(protein kinase B,PKB)、核因子-红细胞2相关因子2(nuclear factor-erythroid 2 related factor 2,Nrf2)[13]等通路有关。 黑质为重要的运动和感知调节中枢,是脑内合成多巴胺的主要核团,与背侧基底核、底丘脑构成基底运动环路[21],可能通过多巴胺能神经与IS引发的震颤等运动障碍相关。为明确DGMI在黑质脑区抗CIRI的作用通路,本研究通过建立小鼠大脑中动脉闭塞(middle cerebral artery occlusion,MCAO)模型,模拟急性IS时脑内局灶性缺血缺氧的状态,利用转录组测序对小鼠脑样本进行测序,并结合生信分析鉴定DGMI在黑质脑区抗脑缺血损伤的作用通路及功能效应,为深入探索其作用机制提供思路。 1 材料 1.1 动物 SPF级雄性C57BL/6小鼠,6~8周龄,体质量18~22 g,购自南京市江宁区青龙山动物养殖场公司,生产质量合格证SCXK(浙)2019-0002。动物于江苏康缘药业有限公司动物房普通清洁级环境中适应性饲养1周,温度(24±2)℃、12 h光昼交替,自由进食饮水。动物实验经江苏康缘药业有限公司动物委员会批准(批号2023110101)。 1.2 药品与试剂 DGMI(商品名为尤赛金,国药准字z20120024,批号220703)由江苏康缘药业有限公司提供;银杏叶提取物761(Ginkgo biloba extract-761,EGb-761,商品名为金纳多,3.5 mg/mL,国药准字HC20181022,批号P6001)由台湾济生医药生技股份有限公司提供;1800AA型小鼠硅胶线栓购自广州佳灵生物有限公司;舒泰50(货号BN8G4VA)购自法国维克公司;2,3,5-氯化三苯基四氮唑(2,3,5-triphenyltetrazolium chloride,TTC,批号BCCJ6488)购自美国Sigma公司;RNA提取试剂盒(批号AM90890A)购自日本Takara公司;Qubit RNA BR Assay kit(批号2506001)、Qubit 1X dsDNA HS assay kit(批号2483579)购自美国Invitrogen公司;Illumina Poly(A) Capture(批号20733163)、Illumina RNA Prep Ligation(批号20723247)、IDT for Illumina RNA Index Anchors(批号20717954)、IDT for Illumina DNA/RNA UD Indexes(批号20739487)、NextSeqTM 2000 P3 300循环试剂盒(批号20751014)购自美国Illumina公司;RNA Screen Tape(批号02020849-192)、RNA Screen Tape缓冲液(批号0006698095)、D1000 Screen Tape(批号0202853-39)、D1000试剂(批号0006739609)购自美国Agilent公司。 1.3 仪器 DOM-1001型显微镜、RFLSI ZW型激光散斑血流成像系统(深圳市瑞沃德生命科技有限公司);PY-SM5(LCD)型LCD高精度智能温控器(余姚市品益电器有限公司);NanoDrop分光光度计(美国Thermo Fisher Scientific公司);4150型TapeStation自动化电泳系统(美国Agilent公司);Qubit 4.0型核酸定量仪(美国Invitrogen公司);NextSeqTM 2000型测序仪(美国Illumina公司)。 2 方法 2.1 动物分组、造模及给药 小鼠适应性饲养5 d后,随机分为假手术组、模型组、DGMI(25 mg/kg)组及EGb-761(100 mg/kg)组,为确保各组术后存活10只小鼠,假手术组设置10只,模型组设置16只,EGb-761组和DGMI组设置14只。 小鼠ip舒泰50麻醉后,参照LONGA法[22]复制MCAO模型。用线栓阻塞小鼠大脑中动脉血流,缺血1 h时,拔出线栓恢复血流,进行再灌注,并结扎颈外动脉剪口。假手术组小鼠进行颈动脉暴露处理,但不插入栓线。手术过程室温控制在(26±1)℃,术后使用加热垫等设备维持小鼠体温保持37 ℃。线栓进入后,将小鼠俯卧位固定,纵向剪开头皮,充分暴露颅骨,置于激光散斑血流成像系统下进行血流检测,确保造模成功。采用RFLSI Analysis v2.0.29.26606软件分析数据,在缺血侧及对侧一致位置添加相同的区域,得到脑血流量统计结果。对造模小鼠进行筛选,排除造模不成功、大出血、蛛网膜出血及过早死亡的小鼠,最终纳入统计的共有40只小鼠,每组分别10只。 基于本课题组预实验结果,DGMI对小鼠MCAO模型术后24 h脑梗死面积改善程度的最佳剂量为25 mg/kg。因此,本研究采用25 mg/kg剂量开展DGMI的药效评价。DGMI组术后30 min ip药物(DGMI以生理盐水将稀释成2.5 mg/mL的溶液),EGb-761组术前1 h ip药物,假手术组和模型组ip等体积生理盐水。 2.2 神经功能评分与脑组织TTC染色 小鼠再灌注24 h后进行改良版神经功能缺损评分(modified neurological severity score,mNSS)[23]。评分后取血,迅速取脑组织,?20 ℃冰箱中冷冻15 min,随后将冷冻后的脑组织切成厚度为2 mm的冠状切片共6片,使用2% TTC染液于37 ℃恒温水浴锅中避光染色10 min,用4%多聚甲醛溶液对脑片进行固定,24 h后拍照。使用Image-Pro Plus 6.0软件计算脑梗死面积。 脑梗死面积=白色缺血面积/总面积 2.3 脑黑质RNA提取和转录组测序 取小鼠脑黑质,每组4个样本,经高速冷冻研磨机粉碎成匀浆后,按照RNA提取试剂盒说明书提取RNA。经过RNA质量控制后,筛选3个符合条件的样品,按照Illumina文库制备体系,完成文库的构建稀释与上机测序。 2.4 转录组数据分析 2.4.1 转录组数据处理与质量分析 利用Trimmomatic[24]软件对测序数据进行滤过,获取高质量的数据信息,直接从基因组网站下载参考基因组和基因模型注释文件,使用HISAT2[25]和String Tie[26]软件将clean reads与参照基因组进行比对和拼接。 2.4.2 降维分析与模型评价 将各组数据进行降维分析,主要分为主成分分析和tSNE降维分析,比较各组离散程度。 2.4.3 差异表达基因(differentially expressed genes,DEGs)筛选 采用DESeq[27]软件包对各组细胞的基因表达量进行差异分析,模型组DEGs以模型组vs假手术组筛选,给药组DEGs以给药组vs模型组筛选,筛选标准为|log2差异倍数(fold change,FC)|≥2且Padjust≤0.05。 2.4.4 基因集富集分析(gene set enrichment analysis,GSEA) GSEA通路富集分析不局限于某些目标基因集,而是从所有基因的表达丰度出发,分析在不同的通路中的基因的整体表达影响,理论上更容易囊括细微但协调性的变化对生物通路的影响。参照徐小波等[28]研究,计算药物干预后表达趋势逆转的通路数与模型组特征通路总数的比值(响应值),并评价药物抗脑缺血再损伤的能力。 2.4.5 基因本体(gene ontology,GO)功能及京都基因与基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)通路富集分析 运用R语言limma[29]软件包对差异基因进行GO功能和KEGG通路富集分析,并用R语言将相关信息可视化。GO功能包括生物学过程(biological process,BP)、细胞组分(cellular component,CC)和分子功能(molecular function,MF)。使用超几何检验进行富集分析。FDR校正的P≤0.05被认为显著富集。 2.5 qRT-[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]验证关键基因表达 按照试剂盒说明书提取脑黑质中总RNA并合成cDNA,进行qRT-[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]分析。采用2?ΔΔCt法计算相关关键基因表达。溶质载体家族6成员A3(solute carrier family 18 member A3,Slc6a3)、钙调蛋白样4(calmodulin like 4,Calml4)、G蛋白亚基γ14(G protein subunit gamma 14,Gng14)、C-C基序趋化因子2(C-C motif chemokine ligand 2,Ccl2)、色氨酸羟化酶2(tryptophan hydroxylase 2,Tph2)、C-X-C趋化因子1(C-X-C motif chemokine ligand 1,Cxcl1)、β-actin引物序列见表1。 图片 2.6 统计学分析 实验结果使用Graghpad prism 9.0软件进行统计分析。两组间比较采用独立样本t检验,组间多重比较采用单因素方差分析(One way ANOVA)和Dunnett-t检验,数据以表示。 3 结果 3.1 脑血流成像结果 通过脑血流仪监测小鼠脑皮质血流量变化,如图1和表2所示,发现插入线栓缺血时,与假手术组比较,各组小鼠手术缺血侧脑皮质血流量均显著降低(P<0.001),表明缺血造模成功,建立的小鼠MCAO脑缺血再灌注模型稳定可靠。 图片图片 3.2 DGMI对MCAO模型小鼠的药效评价 3.2.1 DGMI对MCAO模型小鼠mNSS的影响 脑缺血再灌注后24 h,各组小鼠mNSS结果见图2,假手术组为0分,无神经功能损伤;与假手术组比较,模型组小鼠mNSS显著升高(P<0.001),神经功能损伤严重;与模型组比较,各给药组mNSS显著降低(P<0.01、0.001)。表明MCAO造模可导致小鼠神经功能受到损伤,引起小鼠行为学发生变化;EGb-761和DGMI可显著改善小鼠缺血再灌注造成的神经功能损伤。 图片 3.2.2 DGMI对MCAO模型小鼠脑梗死面积的影响 如图3所示,TTC染色后,假手术组脑切片呈均匀的红色,模型组脑切片缺血侧有明显的白色梗死部位;与模型组比较,各给药组小鼠脑梗死面积 显著减小(P<0.001)。表明DGMI和EGb-761可显著改善小鼠脑梗死面积,对小鼠脑梗死有一定治疗作用。 图片 3.3 转录组测序分析 3.3.1 转录组测序数据质量分析 在建立的测序文库中,超过Q30的比例在94%以上,对测序数据中reads进行滤过后,数据质量控制结果显示,与参考基因组的序列比对率在70%以上,表明测序结果较好。 3.3.2 降维分析与模型评价 经主成分分析发现,假手术组和模型组明显分离(图4-A)。对各组进行tSNE降维分析,发现DGMI组与模型组明显分离(图4-B)。 图片 3.3.3 DEGs分析 如图5-A~C所示,与假手术组比较,模型组共筛选得到88个差异表达基因(differentially expressed genes,DEGs),其中78个基因上调,10个基因下调。与模型组比较,DGMI组有21个基因上调,108个基因下调;EGb-761组有92个基因上调,84个基因下调。分别对模型组和DGMI、EGb-761组的DEGs取交集,如图5-D所示,DGMI组与模型组共有32个差异基因重合,EGb-761组与模型组共有31个差异基因重合,三者共有10个DEGs重合。 图片 图6中展示了EGb-761组、DGMI组和模型组DEGs重叠部分的热图,共53个DEGs。可以发现,这部分DEGs在给药后有不同程度的逆转。此外,在Lv等[30]通过131个小鼠和39个大鼠样本MCAO模型筛选出的15个共同DEGs中,模型组DEGs中有活化转录因子3(activating transcription factor 3,Atf3)、组织基质金属蛋白酶抑制剂1(tissue inhibitor of metalloproteinases 1,Timp1)、分化抗原14(cluster of differentiation 14,Cd14)、半乳糖结合凝集素3(lectin, galactoside-binding, soluble 3,Lgals3)、血红素加氧酶(heme oxygenase 1,Hmox1)、Ccl2、上皮膜蛋白1(epithelial membrane protein 1,Emp1)、热休克蛋白家族B成员1(heat shock protein family B member 1,Hspb1)、血小板反应蛋白基序1型去整合素和金属蛋白酶(a disintegrin and metalloproteinase with thrombospondin motifs 1,Adamts1)、波形蛋白(vimentin protein,Vim)共10个基因重合(66.7%)。Lv等[30]发现的与人类卒中易感基因联系最强的基因Adamts1、锌指蛋白(zinc finger protein 36,Zfp36)、核因子κB抑制剂zeta(nuclear factor kappa B inhibitor zeta,Nfkbiz)、Ccl2和Hmox1中,本研究模型组中也有3个重合。 图片 3.3.4 GSEA结果 如图7所示,GSEA结果显示,与假手术组比较,模型组表达相反的通路有35条,定义这些通路为模型组的特征通路;DGMI与模型组趋势相反的通路有7条,如帕金森症、色氨酸代谢、嘧啶代谢等通路,响应值为20%左右。 图片 3.3.5 DEGs的GO功能富集分析 为明确小鼠MCAO造模及药物干预后所涉及的生物学功能变化,对模型组和DGMI组小鼠脑组织DEGs进行GO功能富集分析,见图8。结果显示,模型组主要富集在细胞对白细胞介素-1和γ干扰素的反应、趋化因子互作和免疫细胞的浸润等BP,细胞外空间、细胞外区域等CC,趋化因子受体结合等MF。DGMI干预后,主要富集在分泌颗粒、神经肽激素信号通路等BP,细胞外空间与区域,多巴胺能神经突触等CC,S100蛋白结合、激素与神经肽激素等MF。 图片 3.3.6 DEGs的KEGG通路富集分析 为明确DGMI对MCAO模型小鼠KEGG通路的影响,基于获得的DEGs进行KEGG通路富集分析,见图9。结果显示,模型组前15条KEGG通路主要与炎症、凋亡和免疫反应相关,富集在细胞因子-细胞因子受体相互作用、肿瘤坏死因子(tumor necrosis factor,TNF)信号通路、白细胞介素-17(interleukin-17,IL-17)信号通路、趋化因子信号通路、丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)通路等。DGMI组KEGG通路主要富集在神经活性配体-受体作用、多巴胺能神经突触等。 图片 进一步分析发现,模型组KEGG通路中出现频率较高(≥3)的关键差异基因为Ccl12、Ccl2、Cxcl1等,见表3。DGMI组KEGG通路中出现频率较高(≥3)的关键差异基因是Gng14、Slc6a3、Calml4等,见表4。 图片 Ccl12、Ccl2与免疫细胞趋化浸润脑区有关,Gng14编码的蛋白质参与G蛋白偶联受体通路,而Slc6a3、Calml4与多巴胺在脑内的转运分泌密切相关,提示DGMI治疗IS可能与多巴胺能信号通路密切相关。 3.4 qRT-[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]验证关键基因表达 对模型组和DGMI组部分关键基因表达进行qRT-[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]验证,如图10所示,与对照组比较,模型组小鼠脑组织Slc6a3、Tph2基因表达水平显著降低(P<0.001),Calml4、Ccl2、Gng14、Cxcl1基因表达显著升高(P<0.05、0.01、0.001);与模型组比较,DGMI组小鼠脑组织Slc6a3、Tph2基因表达显著升高(P<0.01、0.001),Calml4、Ccl2、Gng14、Cxcl1基因表达显著降低(P<0.05、0.01、0.001)。6个基因表达量的qRT-[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测结果均与转录组测序结果一致;值得注意的是,Calml4和Gng14 2个基因通过qRT-[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]和转录组测序方法获得的表达量在3个受试样本间差异较大,这可能是由于2种检测方法对基因的检测区域不同产生的,因此说明qRT-[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测对RNA-seq结果验证的必要性。总之,综合qRT-[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]与转录组测序结果,DGMI可能通过影响炎症和多巴胺相关通路改善IS。 图片 4 讨论 目前,银杏叶提取物作为天然药物产物,已被证明具有抗炎、抗氧化等多种药理作用,可以有效治疗IS。DGMI是国内常用的银杏叶提取物制剂之一,目前虽然在临床前和临床研究上都获得一定成果,但是其治疗IS的作用机制尚缺乏深入的探索。在DGMI作用机制探索的初期首先面对3方面主要的问题。第一,缺乏机制研究方向的指导。面对此问题,在组学水平,例如采用转录组测序方法,获得与疾病进程和发展相关,以及药物治疗途径相关的必要信息,将对后续针对性及更深入的研究提供方向指导。第二,对于IS,临床实验样本的获取比较困难,使得目前相关研究集中在细胞和动物实验,目前关于DGMI在动物IS实验上的转录组测序还没有相关研究内容发表以作参考。第三,由于大脑功能的实行分区域进行,且十分复杂,采用全脑均质化样本进行检测难以对获得的结果进行解析,取特定的脑区进行研究可以更精准地反映疾病和药物对脑特定的功能结构造成的变化影响。 4.1 多巴胺能神经、黑质与卒中炎症 CCL2基因编码的单核细胞趋化蛋白,可以吸引单核和淋巴细胞。CCL2/CCR2趋化因子信号通路在卒中急性期中呈现促炎作用[31],临床试验和动物实验都证明CCL2基因高表达是IS的危险因素,而且在临床上CCL2可作为多种卒中亚型急性期的标志物[32-33]。CCL2因子可由小胶质细胞促炎亚型分泌,CCL2还可能与其他趋化因子共同作用,在急性期介导CD8+ T细胞在脑中的活化和浸润[34]。不过在急性期后的慢性期,CCL2可能有利于促进血管生成和卒中恢复[35]。卒中后活化的星型胶质细胞等分泌的CXCL-1是中性粒细胞趋化因子,可以募集中性粒细胞浸润脑区。中性粒细胞会通过胞外诱捕网等方式进一步加剧卒中[36-38]。 DGMI组和模型组黑质脑区DEGs的KEGG以及GO结果显示,DGMI治疗IS可能和多巴胺能神经相关,尤其是多巴胺的转运和代谢。溶质载体蛋白(solute carrier,Slc)是一类跨膜转运蛋白,Slc18a2基因调控的囊泡单胺转运蛋白2(Vesicular monoamine transporter 2,VMAT2)依赖于质子浓度,介导多巴胺在突触前神经元中从胞质溶胶进入囊泡储存[39-41],囊泡经突触小泡循环将多巴胺运至突触前膜附近,释放多巴胺进入突触间隙,多巴胺结合突触后膜的受体后失活,而Slc6a3调控的多巴胺转运蛋白1(dopamine transporter1,DAT1)位于突触前末梢周围,依赖于Na+/Cl?从突触间隙再摄取多巴胺至突触前末梢[42]。包括多巴胺、乙酰胆碱在内的多种神经递质的受体为G蛋白偶联受体,小鼠Gng14编码的蛋白为G蛋白γ亚基,与人类GNG14同源,Gng14可能通过调节G蛋白亚基发挥作用,而Calml4是钙调蛋白,通过与钙离子结合作用于钙离子信号通路对下游信号产生影响。TPH2是5-羟色胺(5-hydroxytryptamine,5-HT)合成的关键酶,同时也会影响多巴胺的浓度,涉及其转运与代谢[43]。 多巴胺能神经元控制着脑内的奖赏系统、成瘾性以及运动功能[44],还能调控疼痛和神经炎症[45-46]。黑质-纹状体通路是主要的多巴胺能通路之一
[size=20px][color=#93c6bc][b]鉴别[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [font=宋体][/font] [font=宋体](1)取本品粉末1g,加40%乙醇10ml,加热回流10分钟,放冷,滤过,取滤液作为供试品溶液。另取银杏叶对照药材1g,同法制成对照药材溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各6μl,分别点于同一用4%醋酸钠溶液制备的硅胶G薄层板上,以乙酸乙酯-丁酮-甲酸-水(5:3:1:1)为展开剂,展开,取出,晾干,喷以3%三氯化铝乙醇溶液,热风吹干,置紫外光灯(365nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光主斑点。[/font] [font=宋体](2)取本品粉末1g,加50%丙酮溶液40ml,加热回流3小时,滤过,滤液蒸干,残渣加水20ml使溶解,用乙酸乙酯振摇提取2次,每次20ml,合并乙酸乙酯液,蒸干,残渣加15%乙醇5ml使溶解,加入已处理好的聚酰胺柱(30~60目,1g,内径为1cm,用水湿法装柱)上,用5%乙醇40ml洗脱,收集洗脱液,置水浴上蒸去乙醇,水液用乙酸乙酯振摇提取2次,每次20ml,合并乙酸乙酯液,蒸干,残渣加丙酮1ml使溶解,作为供试品溶液。另取银杏内酯A对照品、银杏内酯B对照品、银杏内酯C对照品及白果内酯对照品,加丙酮制成每1ml各含银杏内酯A 0.5mg、银杏内酯B 0.5mg、银杏内酯C 0.5mg、白果内酯1mg的混合溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各5μ1,分别点于同一用4%醋酸钠溶液制备的硅胶G薄层板上,以甲苯-乙酸乙酯-丙酮-甲醇(10:5:5:0.6)为展开剂,在15℃以下展开,取出,晾干,在醋酐蒸气中熏15分钟,在140~160℃中加热30分钟,置紫外光灯(365nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点。[/font] [font=宋体][/font][font=宋体][/font] [font=宋体] [/font] [size=20px][color=#93c6bc][b]检查[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [font=宋体][/font] [b][font=宋体][/font][/b] [align=left][b][font=宋体][/font][/b][/align] [b][font=宋体]杂质[/font][/b][font=宋体] [/font][font=宋体]不得过2%(通则2301)。[/font] [b][font=宋体]水分 [/font][/b][font=宋体] [/font][font=宋体]不得过12.0%(通则0832第二法)。[/font] [b][font=宋体]总灰分[/font][/b][font=宋体] [/font][font=宋体]不得过10.0%(通则2302)。[/font] [b][font=宋体]酸不溶性灰分 [/font][/b][font=宋体]不得过2.0%(通则2302)。[/font] [b][font=宋体]【浸出物】 [/font][/b][font=宋体]照醇溶性浸出物测定法(通则2201)项下的热浸法测定,用稀乙醇作溶剂,不得少于25.0%。[/font] [b][font=宋体]【含量测定】 总黄酮醇苷[/font][/b][font=宋体] [/font][font=宋体]照高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法(通则0512)测定。[/font] [b][font=宋体]色谱条件与系统适用性试验 [/font][/b][font=宋体]以十八烷基硅烷键合硅胶为填充剂;以甲醇-0.4%磷酸溶液(50:50)为流动相;检测波长为360nm。理论板数按槲皮素峰计算应不低于2500。[/font] [b][font=宋体]对照品溶液的制备 [/font][/b][font=宋体]取槲皮素对照品、山奈酚对照品、异鼠李素对照品适量,精密称定,加甲醇制成每1ml含槲皮素30μg、山奈酚30μg、异鼠李素20μg的混合溶液,即得。[/font] [b][font=宋体]供试品溶液的制备 [/font][/b][font=宋体]取本品中粉约1g,精密称定,置索氏提取器中,加三氯甲烷回流提取2小时,弃去三氯甲烷液,药渣挥干,加甲醇回流提取4小时,提取液蒸干,残渣加甲醇-25%盐酸溶液(4:1)混合溶液25ml,加热回流30分钟,放冷,转移至50ml量瓶中,并加甲醇至刻度,摇匀,即得。[/font] [b][font=宋体]测定法 [/font][/b][font=宋体]分别精密吸取对照品溶液与供试品溶液各10μl,注入[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url],测定,分别计算槲皮素、山奈酚和异鼠李素的含量,按下式换算成总黄酮醇苷的含量。[/font] [font=宋体]总黄酮醇苷含量=(槲皮素含量+山奈酚含量+异鼠李素含量)×2.51[/font] [font=宋体]本品按干燥品计算,含总黄酮醇苷不得少于0.40%。[/font] [b][font=宋体]萜类内酯[/font][/b][font=宋体] [/font][font=宋体]照高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法(通则0512)测定。[/font] [b][font=宋体]色谱条件与系统适用性试验 [/font][/b][font=宋体]以十八烷基硅烷键合硅胶为填充剂;以甲醇-四氢呋喃-水(25:10:65)为流动相;蒸发光散射检测器检测。理论板数按白果内酯峰计算应不低于3000。[/font] [b][font=宋体]对照品溶液的制备 [/font][/b][font=宋体]取银杏内酯A对照品、银杏内酯B对照品、银杏内酯C对照品、白果内酯对照品适量,精密称定,加50%甲醇制成每1ml含银杏内酯A 0.18mg、银杏内酯B 0.08mg、银杏内酯C 0.10mg、白果内酯0.20mg的混合溶液,即得。[/font] [b][font=宋体]供试品溶液的制备 [/font][/b][font=宋体]取本品中粉约1.5g,精密称定,置索氏提取器中,加石油醚(30~60℃)在70℃水浴上回流提取1小时,弃去石油醚(30~60℃)液,药渣和滤纸筒挥尽石油醚,置于60℃烘箱中烘干,再加甲醇回流提取6小时,提取液蒸干,残渣加甲醇使溶解,转移至10ml量瓶中,超声处理(功率300W,频率50kHZ)30分钟,取出,放冷,加甲醇至刻度,摇匀,静置,精密量取上清液5ml,加入酸性氧化铝柱(200~300目,3g,内径为1cm,用甲醇湿法装柱)上,用甲醇25ml洗脱,收集洗脱液,回收溶剂至干,残渣用甲醇5ml分次转移至10ml量瓶中,加水约4.5ml,超声处理(功率300W,频率50kHz)30分钟,取出,放冷,加甲醇至刻度,摇匀,即得。[/font] [b][font=宋体]测定法 [/font][/b][font=宋体]分别精密吸取对照品溶液10μl、20μl,供试品溶液10~20μl,注入[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url],测定,用外标两点法对数方程分别计算银杏内酯A、银杏内酯B、银杏内酯C和白果内酯的含量,即得。[/font] [font=宋体]本品按干燥品计算,含萜类内酯以银杏内酯A(C[sub]20[/sub]H[sub]24[/sub]O[sub]9[/sub]),银杏内酯B(C[sub]20[/sub]H[sub]24[/sub]O[sub]10[/sub]),银杏内酯C(C[sub]20[/sub]H[sub]24[/sub]O[sub]11[/sub])和白果内酯(C[sub]15[/sub]H[sub]18[/sub]O[sub]8[/sub])的总量计,不得少于0.25%。[/font] [align=left][font=宋体][/font][/align] [font=宋体][/font]
我在做银杏叶片萜类内酯含量测定时,流动相是正丙醇四氢呋喃和水,标准规定对照品溶液(甲醇溶剂)进5和20ul,进5ul峰型很正常,柱效很高,但是在进20ul的时候,峰就变形了,上坡像连绵起伏的山峰,下坡倒正常,后来我进了一针样品(丙酮溶剂,20ul),个个峰都变形。但是非常奇怪的是,我在不久前刚做了这项含量,各个条件基本是一模一样的,连对照都是同一份溶液,对照在进20ul时峰型很正常。柱子不可能有问题,而且换了一根也是同样问题,流动相是配在一起的。1、请教一下,我的流动相是配在一起的,会不会有可能吸滤头脏了。2、另外,我曾在别的液相和蒸发光检测器上按上述方法测过,峰型很好,会是什么原因。
有没有更好的方法检测银杏内酯,银杏内酯的检测条件???
[color=#333333][font=宋体] 供试品溶液的制备取本品20片,除去包衣,精密称定,研细。取相当于萜类内酯19.2 mg的粉末[8],精密加入甲醇50 ml,称定重量。超声处理40 min,放冷,再称定重量。用甲醇补足减失的重量,摇匀,滤过。精密量取续滤液20 ml,回收甲醇,残渣加水10 ml,置水浴中温热使溶散。加2% HCl溶液2滴,用醋酸乙酯振摇提取4次(15,10,10,10 ml)。合并提取液,用5%醋酸钠20 ml洗涤。分取醋酸钠液,再用醋酸乙酯10 ml洗涤。合并醋酸乙酯提取液及洗液,用水洗涤两次,20 ml/次,合并水洗液。用醋酸乙酯10 ml洗涤,合并醋酸乙酯溶液,回收醋酸乙酯至干,残渣用丙酮溶解并转移至5 ml量瓶中。加丙酮至刻度,摇匀,0.45 μm滤膜滤过,即得。请问上述加甲醇 hcl 乙酸乙酯 醋酸钠 水洗 丙酮的 作用以及每部提取的注意事项及原理 上述方法作出的峰杂质很多,是哪步提取不干净吗?[/font][/color]
请问目前银杏叶中的农残检测标准都做了哪些
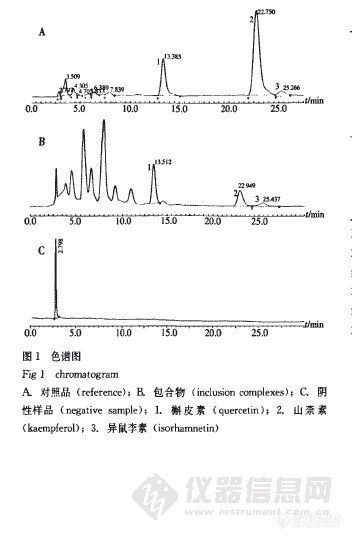
作 者:赵建彬 陈建海(南方医科大学南方医院药学部,广州,510515)摘要: 目的 建立银杏酮酯-羟丙基-β-环糊精包合物的质量标准.方法 采用高效液相色谱法测定制剂中的总黄酮苷含量,色谱柱:Diamonsil C18柱(250 mm×4.6 mm,5 μm),流动相:甲醇-0.4%磷酸(45∶55),检测波长368nm,流速:1 mL·min-1;采用红外光谱分析法鉴别包合物.结果 槲皮素在2~132 μg·mL-1与峰面积具有良好的线性关系,r=0.9995;山奈素在0.9~60 μg·mL-1与峰面积具有良好的线性关系,r=0.9998;异鼠李素在0.1~9 μg·mL-1与峰面积具有良好线性,r=0.9998.槲皮素、山奈素、异鼠李素的平均回收率分别为101.6%、100.4%、99.3%,RSD分别为1.3%,1.4%,0.63%.红外光谱法能有效鉴别包合物.结论 本法可作为该制剂的质量控制参考标准.谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208061012_381701_1606903_3.jpg
大家好,我平时是做理化跟仪器分析的,现在想了解下微生物的一些知识,想请教下标准菌株(阴性对照)的作用是什么,比如金黄色葡萄球菌(阴性标准菌株)我不知道有没有这个,举个例子,它的作用是什么,然后它后面的分离鉴定的相关步骤是不是跟阳性菌株呈现的反应是一样的,忘大家不吝赐教。或者大家有没有哪个标准有提到这些,我可以自己先去看标准,谢谢!
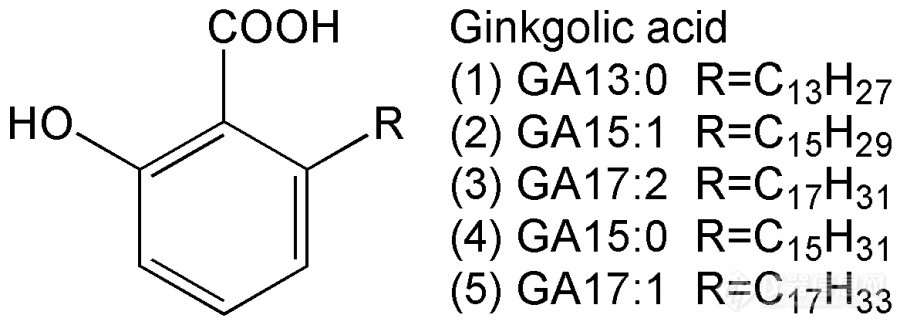
[b]1 引言[/b] 银杏叶提取物是目前临床广泛应用的天然产物药。西方学术界对该药物的成分和疗效也广泛接受。目前银杏叶提取物执行的标准基本上都源自德国EGB-761,其中除规定有效成分含量外,还对银杏酸含量进行了限定。按欧盟药典【European Pharmacopoeia 8.0.Monograph: Ginkgo dry extract. Refined and quantified. [b]2008[/b]】、美国药典【United States Pharmacopeia.Thirty-seventh Revision: Powdered Ginkgo Extract. [b]2015[/b].】要求,总银杏酸含量不得超过5 mg/Kg。我国执行的标准略为宽松,2015版药典【中华人民共和国药典[b]2015[/b], 一部:416-417页】规定总银杏酸含量不得超过10 mg/Kg。.[img=,690,248]http://ng1.17img.cn/bbsfiles/images/2018/07/201807292217347240_855_2204387_3.jpg!w690x248.jpg[/img][b]图1银杏酸的结构式.[/b] 银杏酸的分子结构如图1其中GA13:0、GA15:1、GA17:2是药典规定需要检测的项目。银杏酸的色谱分离并无难点,但是要测定银杏叶提取物中的银杏酸却存在两方面的问题:一是银杏酸限量很低,几乎接近仪器检出限;二是体系中共存的黄酮、内酯、糖类、蛋白质等成分复杂,基体干扰严重。目前通行的检测方法有欧盟药典法、中国药典旧版(2010版)方法、中国药典2015版方法,对比见表1。[img=,690,306]http://ng1.17img.cn/bbsfiles/images/2018/07/201807292218248285_199_2204387_3.png!w690x306.jpg[/img] 色谱分离方面,各种方法均采用反相色谱,条件略有差异,但无本质不同。提取方面,欧盟药典采用甲醇溶剂,提取较为完全,但共存的大量极性组分也一起提取进入溶液中,形成严重的基体干扰。而我国2010版药典方法采用石油醚提取,极性组分溶解少、干扰有所降低,但石油醚对极性试样的浸润性和渗透性不好,提取不完全,因此出现结果偏低的现象。相关研究人员【姚建标, 等.药物分析杂志, [b]2015[/b], 35 (11): 2041-2044.】借鉴了欧盟药典的提取方法提出了2015版药典方法,但是将试样量从0.5g增加到2g。增加样品量是为了弥补检测灵敏度的不足,因为2015版药典方法采用的紫外检测波长为310nm,这一波长下银杏酸的吸收强约为210nm下的五分之一。当然,在310nm下共存杂质的吸收更小、色谱基线漂移的问题也有所缓解,但是取样量增大使得更多的基体杂质进入色谱柱,基体干扰问题有增无减。. 众所周知,通过液液萃取、固相萃取等前处理手段可以起到减少基体干扰、富集目标物的作用,相关研究也有一定报道【Stefan U, Iuliana D S, Victor D,Andrei M. [i]J. Liq. Chromatogr. R. T.[/i], [b]2010[/b], 33 (1): 133-149. Ji W, Ma X, XieH, Chen L, Wang X, Zhao H, Huang L. [i]J.Chromatogr. A[/i], [b]2014[/b], 1368 (1):44-51.】。但是这些前处理过程较为繁琐,不利于推广。也有通过超高效液相色谱-串联质谱方法进行银杏叶提取物中银杏酸的检测【孙健, 等. 色谱, [b]2016[/b], 34 (2): 184-188.】,灵敏度和基体干扰问题都能较好的解决,但仪器昂贵,也难以推广。.[b] 本课题组在进行银杏活性成分提取研究的过程中也遇到了上述测试问题。为了改进现有方法,我们将简便有效的“分散液液微萃取”方法应用到样品的前处理过程中,有效解决了基体干扰问题,灵敏度也显著提高,同时该前处理方法十分简便,样品和试剂的用量也很少。相关研究前沿和创新内容已经撰文投稿,现将较为基础的实验方法介绍如下。[/b].[b]2 实验方法2.1 仪器与试剂[/b] 大连依利特230型高效液相色谱仪,安捷伦HC-C18(4.6*150 mm,5 μm)色谱柱。 色谱纯甲醇、乙腈为上海国药产,纯水为石英亚沸蒸馏。萃取剂为ACS级三氯乙烯,其余试剂为分析纯。 银杏叶提取物试样购于湖北某公司,相关制剂为市售药品(天保宁、金纳多)。 混合银杏酸标准品购于武汉某公司,总含量不低于99%,其中GA13:1占10.1%,GA15:1占50.5%,GA17:1占34.7%,GA17:2占1.7%,GA15:0占3.0%。用甲醇溶解配置成总银杏酸浓度为1.000 g/L的标准储备液,4℃保存。使用时用甲醇稀释成所需浓度的工作标液。.[b]2.2 实验方法 a)提取 准确称取0.5 g试样,加10 mL甲醇,常温超声提取10 min,冷却后定容、摇匀。 上述溶液用微孔滤膜过滤,收集滤液。 b)萃取 取上述滤液3.00 mL移入尖底离心管中,加入萃取剂三氯乙烯0.150 mL混匀,此时不分层。 加入水溶液(含10%无水硫酸钠 + 0.2%三氟乙酸)7.00 mL,加塞、摇匀,此时应得到浑浊液。 4000转离心3min,三氯乙烯萃取剂沉到底层。 c)取样 用注射器吸取三氯乙烯层0.100 mL移入样品瓶,氮气吹干,加0.100mL甲醇溶解。 d)色谱测定 条件见2.3。.2.3 色谱条件[/b] 采用Agilent HC-C18(4.6*150mm,5μm)色谱柱,甲醇-水-三氟乙酸体系(体积比92:8:0.1)为流动相,流速1.00mL/min,检测波长242nm,进样量50.0μL。.[b]2.4 定量分析[/b] 银杏酸工作标液直接进样测定,建立工作曲线,外标法定量。计算待测样时需乘以萃取的富集因子。富集因子为20。.[b]3 实验结果3.1 色谱图[/b] 银杏酸标样、银杏叶提取物试样、试样加标的色谱图见图2,分离效果较好,基线平直、基体干扰小。[img=,690,642]http://ng1.17img.cn/bbsfiles/images/2018/07/201807292222523305_3418_2204387_3.jpg!w690x642.jpg[/img].[b]3.2 方法验证[/b] 将银杏酸的甲醇标液按试样同样方法萃取和检测,考察了方法的重现性、线性范围、定量限(按S/N=10计算),测定了萃取过程的萃取率和富集因子,结果见表2。方法重现性2.9% ~4.8%。方法定量限0.007 ~ 0.020 mg/L,测定上限为5.00 mg/L。按取样0.5g定容至10mL计算,对试样的定量限为0.14 ~0.40 mg/Kg,对试样的测定上限为100 mg/Kg。 萃取率达到95.4% ~98.3%,富集因子达到19.1 ~19.7。[img=,690,231]http://ng1.17img.cn/bbsfiles/images/2018/07/201807292224269505_3788_2204387_3.png!w690x231.jpg[/img][b]3.3 样品测定[/b] 银杏叶提取物试样的测定结果见表3,进行了加标回收实验(总银杏酸加标量为5.00mg/Kg),加标回收率94.0% ~ 100.8%。以欧盟药典方法进行对照试验,结果与本方法一致。药品制剂试样的测定结果见表4,同样进行了加标回收实验和对照实验,结果也较好。[img=,690,306]http://ng1.17img.cn/bbsfiles/images/2018/07/201807292225141669_6540_2204387_3.png!w690x306.jpg[/img][img=,690,312]http://ng1.17img.cn/bbsfiles/images/2018/07/201807292225188364_2915_2204387_3.png!w690x312.jpg[/img].[b]4 相关讨论[/b] (1)试样体积与萃取剂体积之比影响萃取率和富集因子。此比值大时富集因子高但萃取率明显低于100%。反之则导致萃取率接近100%但富集因子很低。本方法选择3.00 mL试样加0.150 mL萃取剂,是兼顾两个方面考虑的结果。此时萃取率达到95.4% ~98.3%,接近100%。富集因子达到19.1 ~19.7,接近体积比计算结果,因此在定量计算时近似认为富集因子为20。 (2)萃取剂要选择低沸点、高密度、弱极性、难溶于水的有机溶剂,符合条件的主要是卤代烃。对比表明三氯乙烯效果最好。 (3)试样溶剂为甲醇,与萃取剂能够互溶,不能分成两相。但加入适量水之后可以实现分层。极性强的基质进入水相,从而使干扰减小。极性弱的银杏酸进入三氯乙烯层实现富集。水中加入10%硫酸钠起盐析作用,加0.2%三氟乙酸可以抑制银杏酸电离,都有利于提高萃取率。不加时萃取率显著降低。 (4)萃取过程形成浑浊的乳状液,两相接触面积大,因此很快达到平衡。加水溶液后震荡30秒到1min即可。萃取时间对结果几乎不影响。 (5)萃取在室温下进行,温度变化对结果影响不大。 (6)银杏酸的紫外吸收有3个特征峰,分别为210 nm、242 nm、310 nm。使用210 nm虽然灵敏度高,但干扰大。本方法使用242 nm检测,实际信噪比高于210 nm。使用310 nm检测的信噪比略有降低。 (7)由于萃取减少了基体干扰、实现了富集,本方法使用等度洗脱进行色谱分离也能获得很好的效果,并且没有基线漂移。本方法灵敏度也显著由于药典方法,定量限达到0.14 ~0.40 mg/Kg,而药典方法的检出限为0.5 mg/Kg。.[b]5 结论[/b] 采用“分散液液微萃取”方法对银杏叶提取物样品进行前处理,具有简单快捷的优点,同时减少基体干扰、实现富集的效果较好,能有效提高信噪比,降低检出限和定量限。方法准确可靠,易于推广。
又有一家知名医药企业中枪“银杏叶事件”,食药总局近日通报哈药集团制药总厂使用了违法银杏叶提取物生产保健食品。 此前,食药总局公告称,大连珍奥集团、汤臣倍健、无限极有限公司、如新(中国)有限公司等21家保健食品企业从桂林兴达药业、宁波立华制药购进银杏叶提取物。 “哈药集团制药总厂使用不合格银杏叶提取物生产了哈药牌银杏叶软胶囊,企业自检2批次产品,经检验均为质量存在问题产品。该企业共购进不合格原料2350公斤,封存1688.85公斤,其余661.15公斤已使用。企业已对质量存在问题产品采取控制措施,截至目前,已封存下架质量存在问题产品5203.01公斤,并启动召回。”食药总局通告中指出,不合格银杏叶提取物原料涉及8家保健食品企业中,其中哈药集团用量是最大的。 据悉,全国目前157家企业使用银杏叶提取物生产保健食品,不合格银杏叶提取物原料涉及8家保健食品企业:大连双迪科技股份有限公司、江苏省庆缘康生物科技有限公司、珠海联邦制药股份有限公司中山分公司、哈药集团制药总厂、杭州太和健康食品有限公司、浙江省磐安县外贸药业有限公司、山东圣海保健品有限公司、会心堂(北京)生物科技有限公司沈阳分公司。 记者致电哈药股份相关人士,但电话一直无人接听。哈药股份在公告中指出,子公司制药总厂生产的银杏叶软胶囊为保健食品,该产品生产所使用的原料银杏叶提取物供应商为徐州恒凯银杏制品有限公司,该公司具有相应生产资质。哈药总厂立即组织专项小组对银杏叶软胶囊产品的供应商资质的合法性、供应商审计流程、采购流程、物料进厂检测环节、生产使用环节及成品放行环节主动开展自检自查。经企业自查,哈药总厂银杏叶软胶囊生产组织过程符合工艺要求,原料购入、产品生产、质量控制环节无违法违规行为,公司产品各项指标符合国家标准。 “6月4日,国家食药监局总局公布银杏叶药品补充检验方法后,哈药总厂立即依照补充检验方法组织了银杏叶软胶囊的对照自检自查,发现企业自2014年1月1日以来生产的57批次产品不符合补充检验标准。目前,哈药总厂已对现有库存产品和原料进行了封存,并启动了银杏叶软胶囊产品的召回措施。”哈药股份说,2014年至今,哈药总厂银杏叶软胶囊产品销售收入为705.7万元。
由于孔雀石绿和无色隐性孔雀石绿均为脂溶性化合物,在鱼体内和环境中残留时间长,并有致突变、致畸和致癌的危险性,因此其是否可作为水产养殖业中使用的兽药在国际上引起了争论。加拿大于1992 年就禁止其作为鱼场杀菌剂使用,且加拿大和美国均规定在食用鱼等水产品中禁止检出孔雀石绿和无色隐性孔雀石绿。欧盟于2002 年6 月颁布法令禁止其在作为食品鱼的鱼场中使用, 我国也于2002 年5 月将孔雀石绿列入《食品动物禁用的兽药及其化合物清单》中。但是,事实上,包括我国和英国在内的许多禁用孔雀石绿的国家,从对市场上销售的鱼类等水产品中孔雀石绿的监测情况来看,仍有在鱼场中非法使用孔雀石绿的现象。 基于这些在水产养殖业中非法使用孔雀石绿的现象,各国政府和消费者密切关注,由此引发各国加大力度进行孔雀石绿的监督检查,同时形成一些标准的检测体系。(一)我国的检测标准【 标准编号 】GB/T 19857—2005 【 标准名称 】水产品中孔雀石绿和结晶紫残留量的测定【 英文名称 】 Determination of malachite green and crystal violet residues in aquatic product【 起草单位 】上海出入境检验检疫局;厦门出入境检验检疫局;广东出入境检验检疫局;福建出入境检验检疫局;江苏出入境检验检疫局;北京出入境检验检疫局;宁波出入境检验检疫局。【 发布日期 】 2005-09-05【 实施日期 】 2005-09-05 【 标准编号 】 SC/T 3021-2004【 标准名称 】 水产品中孔雀石绿残留量的测定.液相色谱法【 英文名称 】 Determination of malachite green residues in fishery products High-performance of liquid chromatography【 起草单位 】 中国海洋大学 国家水产品质量监督检验中心【 发布日期 】 2004-01-17【 实施日期 】 2004-03-01 【 标准编号 】SN/T 1479-2004【 标准名称 】进出口水产品中孔雀石绿残留量检验方法【 发布日期 】2004-11-17【 实施日期 】2005-04-01【 发布单位 】国家质量监督检验检疫总局(二)美国的检测标准1.美国FDA规定的孔雀石绿及其代谢产物实验室检测标准 【 标准编号 】 LIB4363【 标准名称 】鱼和虾中孔雀石绿和隐性孔雀石绿的LC-VIS法和[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]n法【 英文名称 】 Quantitative and Confirmatory Analyses of Malachite Green and Leucomalachite Green Residues in Fish and Shrimp【 起草单位 】U.S. Food and Drug Administration, Animal Drugs Research Center, Denver, CO【 发布日期 】 2005-11 【 标准编号 】LIB4333【 标准名称 】测定和确认鲑鱼中隐性孔雀石绿的[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]方法【 英文名称 】Determination and Confirmation of Leucomalachite Green in Salmon: Laboratory Information Bulletin 4333【 起草单位 】Animal Drugs Research Center, Food and Drug Administration, Denver, CO【 发布日期 】2004-11 【 标准编号 】LIB4334【 标准名称 】快速液相色谱法测定鲑鱼中孔雀石绿和隐性孔雀石绿的方法【 英文名称 】Determination of Malachite Green and Leucomalachite Green in Salmon with In-Situ Oxidation and Liquid Chromatography with Visible Detection【 起草单位 】Food and Drug Administration, Animal Drugs Research Center Denver Federal Center, P.O. Box 25087 Denver, CO 80225-0087【 发布日期 】2004-11 【 标准名称 】美国FDA关于孔雀石绿检测方法4333和4334的补充【 英文名称 】Amendment: Application of Laboratory Information Bulletins 4333 and 4334 for the Determination of Leucomalachite Green and Malachite Green Residues in Catfish, Basa, Tilapia, Trout, and Shrimp 【 发布日期 】 2005-10 2. 美国AOAC协会期刊规定的液相色谱检测方法(J.AOAC Int.1995,78(6):1388-1393 ) 该方法常被等同采用。(三)日本修订孔雀石绿限量标准2006年5月30日,日本厚生劳动省发布食安发第0530002号通知,根据食品卫生法(1947年第233号法律)第11条第1项的规定,规定动物用医药品孔雀石绿是一种食品中不得含有的成分,并制定了孔雀石绿的试验方法,且试验方法的分析对象为孔雀石绿及隐性孔雀石绿。 该修订公布六个月后生效,即2006年11月30日起生效。 此次修订重新制定了孔雀石绿的试验方法,同时向《修订后食品卫生法第11条第3项的相关法令的调整》(2005年11月29日食安发第1129001号当职通知)的附表3中追加如下内容,自2006年11月30日起生效。 农药名称 检出界限(ppm) 孔雀石绿* 0.002 *孔雀石绿的分析对象包括:孔雀石绿及无色孔雀石绿(孔雀石绿的代谢物) 此次修订生效前,暂且施行厚生劳动省制订的一项标准,限量0.01ppm(2005年厚省劳动省告知第497号)。
接连两天,国家食品药品监督管理总局发布关于银杏叶药品违规生产情况。昨日,国家食药监总局表示,对于桂林兴达药业和万邦德(湖南)天然药物有限公司违规生产银杏叶产品一事,广西、湖南两省区要迅速查明产品销售流向。更值得关注的是,包括云南白药集团、河北省涿州东乐制药有限公司等24家药品生产企业,因从桂林兴达药业有限公司购买银杏叶提取物而受到波及,目前也在接受药监部门的核查。 根据国家食药监总局消息,桂林兴达药业有限公司擅自更改银杏叶提取生产工艺,同时从不具备资质的企业购进以盐酸工艺生产的银杏叶提取物,用于生产银杏叶片,并将外购的提取物销售给其他的药品生产企业,伪造原料购进台账和生产检验记录。而万邦德(湖南)天然药物有限公司用购进的银杏叶提取物生产银杏叶片和银杏叶胶囊等制剂,伪造原料购进台账和生产检验记录。食品药品监管部门已对其立案调查。 公开资料显示,银杏叶制剂临床多用于治疗心、脑血管疾病,如冠心病心绞痛、脑血管痉挛、脑供血不全、记忆力衰退等。“此次查处的桂林兴达药业,用盐酸工艺生产银杏叶提取物会分解药品有效成分,影响药品疗效,进而对使用者造成不利影响。”国家食药监总局相关负责人称。 同时,经查包括云南白药集团中药资源公司、黑龙江天宏药业股份有限公司以及河北省涿州东乐制药有限公司等24家药品生产企业,从桂林兴达药业有限公司购买非法银杏叶提取物。药监部门表示,上述公司凡使用盐酸工艺银杏叶提取物生产银杏叶制剂的,必须按通告要求立即采取停售、召回等措施,并向有关省(区、市)食品药品监管部门通报产品销售流向,抄报总局。 国家食药监总局还警示,根据市场监测,还有部分企业存在改变工艺违法生产银杏叶提取物的行为,故要求所有银杏叶提取物和银杏叶制剂生产企业立即开展自查。 土豆点评:那么,问题来了,现在监管部门对中药饮片、中药中间体(提取物)的监管越来越严格了,中药厂家如何应对?以后中药制剂会不会涨价?一堆小饮片企业会不会就此倒闭呢?
大家好.新人来报道.大家多多支持!谢谢.向各位高手请教个问题.1.银杏叶中的农残是在叶表面还是在叶子里?2.采叶前可以用什么方法去除农残?采下的叶子又可以用什么方法去除农残?3.银杏树苗(采叶圃)如果长期不使用农药.需要(几个月或几年)可以大量降低农残.使其达到美国食品药品农残标准?如果您知道请告诉我.不胜感激.谢谢小弟QQ284958788
求助,关于银杏叶提取物的总银杏酸含量测定。请问各位有没有做过的,我怎么做了几次都做不出来呢。条件都是按照药典要求做的,对照品都不出峰。我都要疯了。有谁做过帮忙分析一下或者上传一张图谱,谢谢。

作者:帅英丽;于红艳;李志强; (天津生物化学制药有限公司;)摘要:目的:建立银杏叶提取物的HPLC/UV指纹图谱。方法:以银杏叶提取物的HPLC/UV指纹图谱为参照物,采用HPLC法分析,并加以计算机辅助相似性评价系统对指纹图谱进行了相似度分析。采用Diamonsil(C18,250 mm×4.6mm,5μm)色谱柱;以流动相(A)水-乙腈-异丙醇-柠檬酸(1 000∶470∶50∶6.08)、流动相(B)水-乙腈-异丙醇-柠檬酸(1 400∶200∶30∶6.88)进行梯度洗脱;流速:1.0 ml/min,检测波长:360 nm。结果:在本试验条件下进行测试,可以建立银杏叶提取物以及银杏叶指纹图谱检测方法,得到分离度、重复性均较好的银杏叶提取物HPLC/UV指纹图谱,标示了13个共有峰,可以方便简单、并且有效控制不同厂家来源的银杏叶提取物。结论:银杏叶提取物指纹图谱的建立,为其质量控制提供了依据,也为银杏叶提取物以及银杏叶的指纹图谱国家标准的确立提供了更为科学的依据和有效的鉴别方法。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208201403_384671_1606903_3.jpg
银杏叶[img]https://ng1.17img.cn/bbsfiles/images/2018/11/201811062212384939_9847_2911392_3.png[/img]
[center]秋间银杏黄文/闻禾[/center] 车行天坛东门,绕天坛墙外右行。卧床三天病初愈的我,要去上班。蓝天不动,蓝天下的白云静止。静止的蓝天白云下,各样形状、各种颜色的风筝,在不见身形的风的扶持和梳理下,自由舒展,或上下起伏、或斜线攀援,恬静安闲......坐在车窗边。望窗外,人流车流,熟视无睹。[center][img]http://it.news.tom.com/uimg/2007/11/12/songyuzhen/1194834669529_543315.JPG[/img][/center]我被环绕天坛公园围墙的银杏树深深吸住,默叹着银杏的神奇魅力。一下子就想起几天前看到的一位中学生赞美银杏树的文章。几乎用尽了华丽美妙词句,刻意赞美的那些银杏树,还是没眼前的这般景色令心垂涎,令人神往啊。百闻难抵一见。今年仲秋,见到了以为这辈子都见不到的银杏果。圆圆的,宛若桂圆。初次与其相见,是在一位同事的办公室里,那些大小比较均匀的小圆球,满满地拥挤在白色塑料袋子里。未曾剥皮见肉,据说果肉很臭。今年银杏盛产,那日去台基厂换新电表卡,崇文门大街路南有很多老牌银杏树,果实累累强压枝,几乎每棵树上,各个枝杈,都满满堆砌了圆圆的小球,疙疙瘩瘩,风吹叶落,果实欲重......多,太多了。崇文大街上的银杏果,压过了叶子的风光。我觉得结了果子的银杏树,失去了原有的美丽。这种被称之为白果、银杏果、爷孙果的果实,应该是岁月的扎染,风霜的积淀。银杏又称爷孙树,意思是爷辈栽树,孙辈方能结果。不到一定年龄,银杏树是不结果子的。化学馆前几棵硕大的颇有特色银杏树又出现在眼前。那时我刚刚认识银杏树,经常将绿色的、黄色的、形状规整的、奇异的银杏叶夹在本间书内,爱不释手。那是特别期盼能有机会与银杏果见上一见,可我守望了整整四年,最后还是一无所获。不知是性别原因(有人说,化学馆前的银杏树都是雄性的),年龄问题,还是化学反应的缘故,学校的银杏树就是不见结果实。所以在我的印象中,见到银杏果结在树上,就跟不可能实现的梦幻一样。今秋崇文门大街观银杏,一扫我一直以来天真幼稚略加疯狂的想法。不但见到了结在树上的银杏果,而且一见就是那么多!树上结的,地上落的。“要绿都绿,要黄都黄。竟然不见一叶杂色。”车子向前滑动,银杏树环围天坛墙悠悠移动,心在赞叹眼睛的发现——想起一直喜欢的梧桐树。形色俊美的大叶子,应季变换色形的梧桐球,如同涂鸦墙般的、敦实憨厚不高的树干,总是心甘情愿、欢快自豪地举着硕大唯美、挂了滴溜溜小球的树枝树叶,充分展示着幸福的骄傲。在梧桐树上,我从来读不到文人的那份过于细腻的心情感受——凄凄惨惨戚戚!感情若遭霜打一般。暮秋的梧桐,树干已斑驳,叶子多层色——干焦褐色、将干棕色、染秋黄色、犹存绿色,但它们依然在渐凉渐冷的秋风里,步岁月韵律蹈舞,唱有缘相聚幸福歌,虽有稀稀落落,依然潇潇洒洒......与梧桐树树色的杂不同,银杏颜色的变化竟如此步调一致,整齐划一。纯纯春绿,渐渐绿黄,直至满树纯黄——立正!稍息!起步走!银杏犹如自然界的仪仗队,跟随季节的口令,甩臂抬腿,齐唱“三大纪律、八项注意”,步调一致,出神入化。哦,银杏树!不知该怎么赞美你!突然想起一句毛主席语录:军民团结如一人,试看天下谁能敌!天坛公园上空,不动的蓝天,休闲的白云,隐形的微风,揉合在飘逸潇洒错落安然的风筝中,翱翔轻飞,竟放胸怀,驰骋呼吸......古香古韵的青砖墙外,一道纯天然的、齐色优雅的银杏黄......溶解在这静动行色如此动人的景色里放飞思绪的人啊,不该有不快乐、不幸福的理由?!