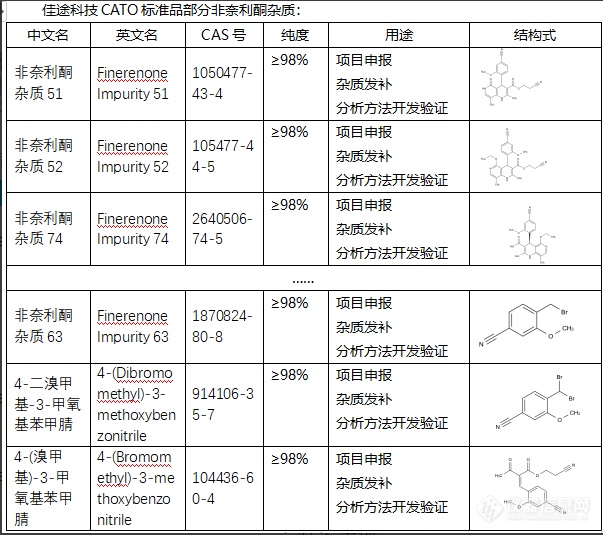
非奈利酮(Fentanyl)是一种强效的合成阿片类药物,常用于治疗严重的疼痛,特别是术后疼痛、慢性疼痛或疼痛癌症。然而,非奈利酮可以引起严重的副作用,包括呼吸困难、心跳异常、意识模糊、过敏反应等。非奈利酮的杂质则对药效和安全性有重大影响。这些杂质可能是生产过程中的副产品,也可能是储存或运输过程中引入的。这些杂质如果不被有效地去除,可能会干扰药物的作用,影响疗效,甚至引起不良反应或毒性反应。例如,一些杂质可能会增加药物的毒性,引起伤害,另一些可能会降低药效,导致疼痛得不到有效的控制。CATO标准品非奈利酮的杂质还可能导致药物稳定性降低,影响药物的质量和有效性。[img=,603,535]https://ng1.17img.cn/bbsfiles/images/2024/02/202402041445203398_9273_6381668_3.png!w603x535.jpg[/img]
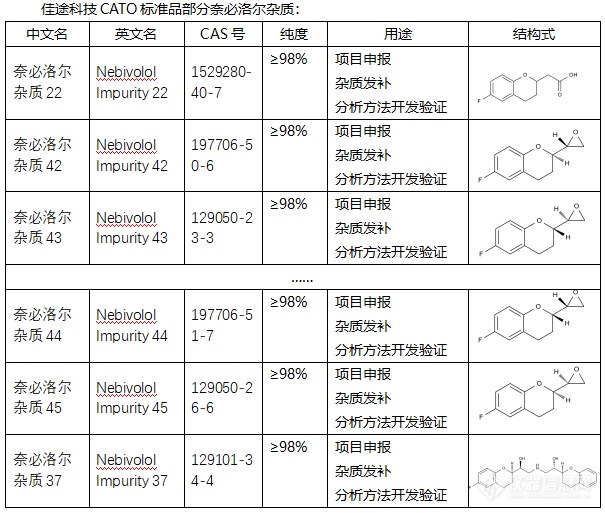
[font=宋体]◇[/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]杂质[/font][font=宋体][font=宋体] 奈必洛尔杂质是指在奈必洛尔([/font][font=Calibri]Nebivolol[/font][font=宋体])的生产或保存过程中产生的非目标化合物。奈必洛尔杂质有多种,包括但不限于以下几种:奈比洛尔杂质([/font][font=Calibri]L-[/font][font=宋体]奈必洛尔),英文名称为[/font][font=Calibri](-)-Nebivolol[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]118457-16-2[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]9[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]920275-23-6[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]C[/font][font=宋体](非对映体混合物),英文名为[/font][font=Calibri]Nebivolol Impurity C (Mixture of Diastereomers)[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]B[/font][font=宋体],英文名为[/font][font=Calibri]Nebivolol impurity B[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]119365-25-2[/font][/font][font=宋体];[/font][font=宋体][font=宋体]去氟奈必洛尔,英文名为[/font][font=Calibri]Desfluoro Nebivolol[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=宋体]Ⅰ和奈必洛尔杂质Ⅱ等。[/font][/font][font=宋体][font=Calibri] CATO[/font][font=宋体]标准品提供的[/font][/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]全套的杂质[/font][font=宋体],[/font][font=宋体]这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分[/font][font=宋体]。[/font][img=,605,513]https://ng1.17img.cn/bbsfiles/images/2024/02/202402182153192686_9605_6381607_3.png!w605x513.jpg[/img][font=宋体][color=#05073b][back=#fdfdfe] 广州[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]佳途科技[/back][/color][/font][font=宋体][color=#05073b][back=#fdfdfe]股份有限公司[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]深知药物研发与质量控制的重要性[/back][/color][/font][font=宋体][font=宋体],[/font][font=Calibri]CATO[/font][font=宋体]标准品厂家,提供[/font][/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]全套[/font][font=宋体]的[/font][font=宋体]杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展[/font][font=宋体],[/font][font=宋体]以满足客户在药物研发和质量控制方面的需求。[/font]
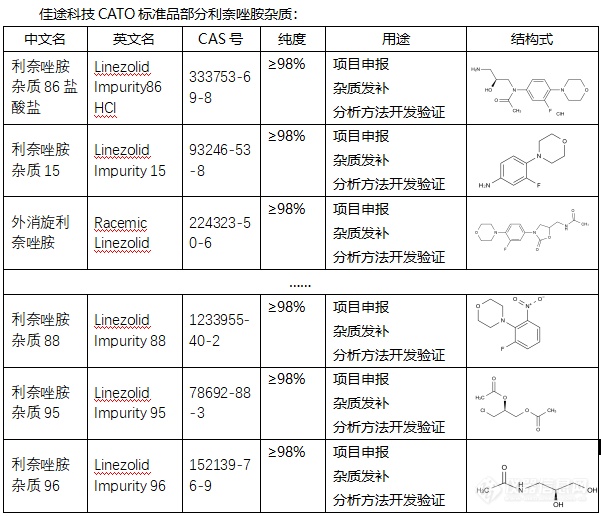
◇关于利奈唑胺杂质 利奈唑胺杂质是在全球第一个由人工合成的恶唑烷酮类抗菌药,利奈唑胺杂质可以通过与细菌的核糖体结合,阻碍[font=.pingfang sc]革兰阳性菌细菌的蛋白质合成过程。它作用于核糖体的[/font]23S亚基,抑制形成功能性的库脱锁酶,从而阻断了转运RNA和信使RNA之间的连接,使得动态脱附无法进行,进而抑[img=,601,516]https://ng1.17img.cn/bbsfiles/images/2024/02/202402040945273495_6026_6381607_3.png!w601x516.jpg[/img]制了肽链的合成。这导致革兰阳性菌无法继续合成新的蛋白质,最终导致细菌的生长和复制受到抑制。[font=UICTFontTextStyleBody] [/font][font=宋体][font=宋体]利奈唑胺上市后在[/font]2006[font=宋体]年全球销售[/font][/font][font=宋体]一直在增长[/font][font=宋体],[/font][font=宋体]在[/font][font=宋体]2015[font=宋体]年达到峰值[/font][font=Calibri]13.53[/font][font=宋体]亿美元,欢迎大家来选购[/font][/font][font=UICTFontTextStyleBody]CATO[/font]标准品提供的[font=宋体]利奈唑胺杂质。[/font]
雷西奈德(lesinurad)是近几年比较热门的药物,是阿斯利康开发的一款药物,与黄嘌呤氧化酶抑制剂一起用于治疗痛风相关高尿酸血症。本文详细列举了雷西奈德的杂质总共26个。并列出了文献中雷西奈德的检测方法,便于新药研发检测方法开发参考。其他信息请看上传的PDF文件。[img=,303,276]http://ng1.17img.cn/bbsfiles/images/2018/07/201807101515021893_6772_3428199_3.png!w303x276.jpg[/img]
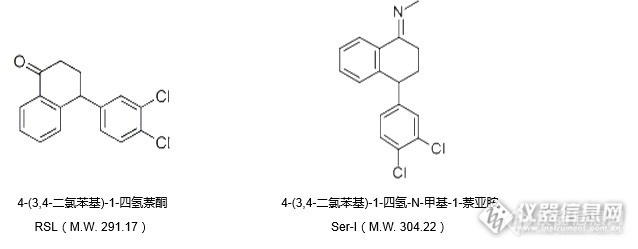
[align=center]萘酮与中间体杂质I的分离[/align]根据客户提出的依赖分析需求,实验室对以下结构的萘酮(RSL)及其中间体杂质I(Ser-I)进行分离尝试。[align=center][img=,638,249]http://ng1.17img.cn/bbsfiles/images/2017/06/201706210849_01_2222981_3.png[/img][/align][align=center][img=,690,226]http://ng1.17img.cn/bbsfiles/images/2017/06/201706210850_01_2222981_3.png[/img][/align]注:在客户给出的数据文件中,RSL命名为萘酮,Ser-I命名为中间体I;在加磷酸体系中,中间体I先出峰,不加磷酸体系中,萘酮先出峰。由于萘酮(RSL)与中间体I(Ser-I)在水相中会发生结构转换现象,因此我们在无水条件下开展实验。使用资生堂疏水性与表面极性得到良好平衡的反相色谱柱CAPCELL PAK C18 MG S5 4.6 mm i.d. × 250 mm进行分析,同时对柱温进行优化,结果如图1所示。[align=center][img=,690,280]http://ng1.17img.cn/bbsfiles/images/2017/06/201706210849_02_2222981_3.png[/img][/align][img=,581,198]http://ng1.17img.cn/bbsfiles/images/2017/06/201706210849_04_2222981_3.png[/img]图2、图3分别为萘酮和杂质I的光谱图。[align=center][img=,690,271]http://ng1.17img.cn/bbsfiles/images/2017/06/201706210849_03_2222981_3.png[/img][/align]由图1可知,在萘酮的分析中,柱温越高其保留时间越短。同时发现在萘酮与杂质I之间出现一较明显倒峰。由图2、图3决定检测波长,由于流动相中添加了三乙胺,会对短波长检测产生一定干扰,因此建议在254nm或者288nm进行检测(本实验选择254nm)。我们对图1中倒峰的来源进行了多方排查,最终发现该实验体系中不得引入任何水,建议客户使用的所有实验容器必须烘干,并且需将洗针液更换为纯有机相。排除水干扰后分析对比结果如图4所示。[align=center][img=,638,363]http://ng1.17img.cn/bbsfiles/images/2017/06/201706210849_05_2222981_3.png[/img][/align]同时,为进一步延长保留时间,我们也尝试使用了资生堂键合金刚烷基团的高表面极性色谱柱CAPCELL PAK ADME S5 4.6 mm i.d. × 250 mm进行分析,所得结果如图5所示,相较于MG色谱柱,ADME色谱柱能够得到更强保留。[align=center][img=,616,304]http://ng1.17img.cn/bbsfiles/images/2017/06/201706210849_06_2222981_3.png[/img][/align]
各位,我想请教下。怎么确认杂质限度的制订呢?我看药典说的很笼统啊,只是给了个决策树。不知道是订0.5%还是1%。还有就是 光学活性是包括手性以及旋光嘛。
看的仪器信息网期刊合作里面有现代仪器,也有朋友推荐投现代仪器杂志,就是不知道现代仪器是几级杂志,网上查了下只查到它是科技核心。

维权声明:本文为zhouyuhu原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现的,均属侵权违法行为,我们将追究法律责任。1 原理 试样经过滤板过滤、冲洗,根据残留于过滤板上的可见带色杂质的数量确定杂质量。关于杂质度,实际是与原料奶有关系,但是到了奶粉中,主要是评价奶粉生产工艺的指标,原料奶的生产中,必然会混入草、沙等杂质,而奶粉生产过程中因为生产工艺的控制问题,会出现奶粉焦化的现象。 2 仪器和设备 2.1 过滤设备:杂质度过滤机或配有可安放过滤板漏斗的 2000 mL~2500 mL 抽滤瓶。 2.2 过滤板:直径 32 mm,单位面积质量为 135g/m ,符合附录 A的要求,过滤时通过面积的直径为28.6 mm。 2.3 杂质度标准板。 2.4 杂质度标准板的制作方法见附录 B。 2.5 天平:感量为 0.1 g。 3 分析步骤 液体乳样量取 500 mL;乳粉样称取 62.5 g(精确至 0.1 g),用 8 倍水充分调和溶解,加热至 60 ℃;炼乳样称取 125 g(精确至 0.1 g),用 4 倍水溶解,加热至 60 ℃,于过滤板上过滤,为使过滤迅速,可用真空泵抽滤,用水冲洗过滤板,取下过滤板,置烘箱中烘干,将其上杂质与标准杂质板比较即得杂质度。 当过滤板上杂质的含量介于两个级别之间时,判定为杂质含量较多的级别。 4 分析结果的表述 与杂质度标准比较得出的过滤板上的杂质量,即为该样品的杂质度。 5 维修过程5.1症状开机后发动机在转,但液体样品无法过滤。5.2 分析主动轮发动机转,说明发动机没问题,排除发动机主动轮部分,看主动轮在转,皮带轮不转,那说明是从动轮的问题。具体见下图:http://ng1.17img.cn/bbsfiles/images/2010/11/201011102148_258596_1644065_3.jpg打开后清理了残留的样品残渣,问题依旧。接下来卸下从动轮,然后打开上图的部分,用的是内六角螺丝刀,见下图http://ng1.17img.cn/bbsfiles/images/2010/11/201011102150_258597_1644065_3.jpg打开后发现里面很脏,样品残渣组织了齿轮的旋转,导致了以上问题,打开后见下图:http://ng1.17img.cn/bbsfiles/images/2010/11/201011102151_258598_1644065_3.jpg所以的残渣全部清理后,涂上机油,放置一个小时,让机油浸润内部。然后再用脱脂棉擦干净,装上,再开机,问题解决。6 后记使用过程中尽量清洗干净,避免残渣糊在机器上,堵塞管路。
牛奶里的杂质是什么原因造成的大家讨论一下。
实验室研发的新产品即将生产,其中有一个[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]监控的步骤,需要用简单的方式来定量控制该物质的含量。杂质是异丙醚,此步是中间控制,需要将该杂质含量控制在1%以内,领导要求开发一个简便的方式来定量从而控制其含量。我想了一下,能否将产品与杂质1:1配制,溶解至100ml,那么此时杂质与产品的含量比即为杂质与产品的峰面积比。问过研发人员,中间产物中,产品大致的量他们是知道的,也就是产品的量已知。那么能否通过直接进样中间产物,观察产品与杂质的比值来判断杂质的大致含量呢?这个方式我在液相的杂质含量中其实有大致了解,但是无奈理解能力有限,其实没有太懂[b][color=#000000]加校正因子主成分自身对照法[/color][/b]与[color=#000000][b]不加校正因子的主成分自身对照法[/b]的[/color]计算方式。[b][color=#ff0000]举个例子:[/color][/b]第一种[font=&][color=#000000][size=14px][b]加校正因子主成分自身对照法[/b][/size][/color][/font]:假设我现在有杂质对照品,和产品对照品,我将两种配制成浓度已知的混合液,进样,已知校正因子(f)=(S杂质*C杂质)/(S产品*C产品)计算出校正因子,假设(f)=杂质:产品=1.2那么我现在有个中控液进样了,杂质:产品峰面积为1:10,产品在混合液中的含量差不多为50%,那么杂质含量占多少呢?杂质含量此时是6%吗?第二种[b]不[/b][font=&][size=14px][color=#000000][b]加校正因子主成分自身对照法[/b][/color][/size][/font]:这种我是完全没懂了,,,懵圈了。如果我第一种方法的理解没错的话,那么此次[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]中控方式能否用这种方式来计算杂质的大致含量呢。求教。
这是某品牌的纯牛奶 在经过一般加热后 出现了黑色的小杂质,经过显微镜的观察,可看见类似与奶酪状的物质,排除了为铁锅本身的问题,经过红外的扫描出现下图,但不知道是什么物质啊 请各位赐教
牛奶中的杂质度如何检测呢?

喝奶的时候你可能喝出过凝结的团块,但是如果里面有很多的细小杂质,除非经过过滤你才可以看到的。这些杂质大家在平时几乎不会去关注。杂质出现的原因分析:1) 原料奶里面就可能含有,按工艺流程来说,在过均质机的时候会有过滤的过程,如果机器出现故障,那么就出现了隐患。2) 管道的清洗,液奶前期处理的CIP,或者是后端出粉的干燥塔,都要定期做清洗。尤其是在对干燥塔清洗时,必须要将糊粉冲洗干净。3) 清洗剂造成的污染,清洗过程中,清洗剂本身的污染4) 机械杂质,工艺上的每一个螺丝铁钉都要有编号,随时进行保养防止机械杂质的脱落。运气不好的出现过铁钉螺丝。再说说杂质的危害:机械性的螺丝铁钉就不用说了,很容易喝道肚子里面的。其他的细小杂质很容易造成微生物的污染。用于巴氏杀菌乳、灭菌乳、生乳、炼乳及乳粉杂质度的测定,不适用于含非乳蛋白质、淀粉类成分、不溶性有色物质及影响过滤的添加物质。原理试样经过滤板过滤、冲洗,根据残留于过滤板上的可见带色杂质的数量确定杂质量。仪器和设备1.过滤设备:杂质度过滤机或配有可安放过滤板漏斗的2000 mL~2500 mL抽滤瓶。2.过滤板:直径32 mm,单位面积质量为135g/m,过滤时通过面积的直径为28.6 mm。3.杂质度标准板(附带图片)。http://ng1.17img.cn/bbsfiles/images/2014/05/201405231325_500242_2227357_3.jpg实验过程:液体乳样量取500 mL;乳粉样称取62.5 g(精确至0.1 g),用8倍水充分调和溶解,加热至60 ℃;炼乳样称取125 g(精确至0.1 g),用4倍水溶解,加热至60 ℃,于过滤板上过滤,为使过滤迅速,http://ng1.17img.cn/bbsfiles/images/2014/05/201405231325_500243_2227357_3.jpg可用真空泵抽滤,用水冲洗过滤板,取下过滤板,置烘箱中烘干,将其上杂质与标准杂质板比较即得杂质度。http://ng1.17img.cn/bbsfiles/images/2014/05/201405231326_500244_2227357_3.jpg当过滤板上杂质的含量介于两个级别之间时,判定为杂质含量较多的级别。异常的杂质版:http://ng1.17img.cn/bbsfiles/images/2014/05/201405231326_500245_2227357_3.jpg合格的杂质版:http://ng1.17img.cn/bbsfiles/images/2014/05/201405231327_500246_2227357_3.jpg
我是一个新手,我做乙醇挥发性杂质时,我们的样品里面均未检出各杂质,是否合理?怎么感觉多少都应该有点呢?还是因为我是放置了几天以后才做样的缘故?请教各位!谢谢谢谢!
请问各位专家,我在用[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]ICP-MS[/color][/url]测量金属杂质的时候,酸空白中杂质的含量比样品中杂质的含量还大,(我们待测样品金属杂质含量一般为几个ppb),请问当酸空白的金属杂质含量大到什么程度的时候,就会干扰,或者是覆盖我的样品的金属杂质呢,从而影响测试结果呢??
空白溶剂中就出现了未知杂质,且后续的每针该未知杂质都往前飘。几个月内的分别六次实验,有三次实验中有未知杂质峰,有三次实验中却没有出现未知杂质峰。方法,色谱柱,仪器都是一样的,唯一不同的就是使用的是不同的品牌乙腈,流动相以及溶剂就是乙腈和水。同样的情况多次出现,难道这和乙腈有关?求各位大佬解答疑惑。感谢
镀金层具有优良的抗变色、抗氧化和耐腐蚀性能 、良好 的芯片焊接和引线键合性能以及较低的接触电阻和较好的 可焊性等优点 ,被广泛应用于军用半导体及微电子封装外 壳。但军用电子器件对镀金层质量要求很高 ,而镀 金液中 的金属 杂质 则 直 接 影 响 镀 金 层 质 量 ,这 些 杂 质 主要 有 铅 、 铜 、铁 、镍等 ,往往在金结晶过程 中共沉积。其 中铅最有害 , 1~10mg/L就能造成非常有害的影响 ,特别是在低 电流密 度区 ;铜可使低电流密度区变暗,与金共沉积使颜色异常 , 纯度下降 ;铁 、镍等在酸性溶液或碱性亚硫酸盐槽液里 与金 共沉 积 的倾 向要 比在 碱 性氰 化 物 槽液 里 大得 多 ,对 金 的纯 度及颜色有害 。因此 ,准确测 定镀金液 中杂质元素 的含量 具有 重 要意 义 。目前 ,国内外对镀金液中杂质元素的测定虽有报道,但 多针对镀金液中单元素的分析研究 ,多元素的同时测定 多采 用 ICP—AES法 和 ICP—MS法 ,由 于镀 金 液 中大 量 基体元素金的存在对杂质元素测定的干扰和抑制作 用,高 盐样品直接进样导致进样系统堵塞和金的记忆效应等诸 多 问题,使得用 ICP—AES法直接测定镀金中杂质元素浓度相 当困难 。为此 ,研究 了用甲基异丁基酮(MIBK)有机试剂萃 取分离 了镀金液中的金后,采用 ICP—AES法测定镀金液中 Pb,cu,Fe,Ni4种杂质元素的方法 。为寻找镀金液中杂质元素的测定方法 ,运用甲基异丁基 酮(MIBK)萃取分离金 ,采用电感耦合等离子体原子发射光谱(ICP—AES)法对镀金液中的杂质元素进行了分析。对分析谱线、基体元素和等离子体参数等进行了讨论。结果表 明,这种方法的检出限为 0.008—0.019 g/mL,回收率为 89.4% 一102.3%,相对标准偏差 (RSD)小于 3.12% 。该法准确 、快速 、简便 ,应用于镀金 液 中杂质元素的测定 ,结果令人满意 。
各位:以下是安宫黄体酮的杂质F 的TLC检测.可是按以下方法我做的薄层效果不好.不能分离,是何原因啊?用薄层色谱法检测 ,使用TLC硅胶色谱板。分别取加10μl的溶液点板,用10体积四氢呋喃试剂、45体积的1,1-二甲基乙基 甲基醚试剂和45体积的环己烷试剂配制的展开剂展开超过10cm,让色谱板在空气中晾干,然后用相同的展开剂在同一方向上再次展开超过10cm,加热色谱板到120℃并保持10min,用200g/l的甲苯亚璜酸乙醇溶液来喷板,加热到120℃并保持10min, 冷却。 在365nm的紫外光下检测,供试液(a)得到的色谱图中任一蓝色荧光斑点的Rf值比安宫黄体酮主斑点的Rf值要高,但是斑点的颜色不能深于参照液(a)得到色谱图中杂质F的蓝色荧光斑点(0.5%)。 只有当参照液(a)得到色谱图中有两个明显分离的斑点时,该测试结果才有效。
[B][center]药物中杂质的来源及杂质限量检查[/center] [/B]药物只有合格品与不合格品;一般化学试剂分为4个等级(基准试剂、优级纯、分析纯、化学纯) [B]药物中一般杂质检查 [/B][B]氯化物为一指示性杂质。[/B] 通过对氯化物的控制,可同时控制与氯化物结合的一些阳离子以及某些同时生成的副产物。可从氯化物检查结果显示药物的纯度,间接考核生产、贮藏过程是否正常。 1. 原理 药物中微量的氯化物在硝酸酸性条件下与硝酸银反应,生成氯化银的胶体微粒而显白色浑浊,与一定量的标准氯化钠溶液在相同条件下产生的氯化银浑浊程度比较,判定供试品中氯化物是否符合限量规定。 Ag+ + Cl- → AgCl ↓ [B]硫酸盐检查法 [/B] 1. 原理 药物中微量的硫酸盐在稀盐酸酸性条件下与氯化钡反应,生成硫酸钡的微粒而显白色浑浊,与一定量的标准硫酸钾溶液在相同条件下产生的硫酸钡浑浊程度比较,判定供试品中硫酸盐是否符合限量规定。 [B]铁盐检查法 [/B]硫氰酸盐法 巯基醋酸法 砷盐检查法 1. 古蔡氏法 1. 原理 金属锌与酸作用产生新生态的氢,与药物中微量砷盐反应生成具挥发性的砷化氢,遇溴化汞试纸产生黄色至棕色的砷斑,与同条件下一定量标准砷溶液所生成的砷比较斑,判断砷盐的含量。 [B]硒、氟及硫化物检查法 [/B]1. 氧瓶燃烧法 适用于以共价键结合的卤素、硫、硒的有机药物。 本法系将有机药物防入充满氧气的密闭燃烧瓶中进行燃烧,将燃烧所产生的欲测组分吸收于适当的吸收液中,然后根据欲测组分的性质,选用合适的分析方法进行鉴别、检查或含量测定。 [B]注意事项及讨论 [/B]1. 根据被燃烧分解的样品量选用适宜大小的燃烧瓶。 2. 测定氟化物时应改用石英燃烧瓶。 1. 硒检查法 (1). 操作方法 样品与对照品液,调节Ph2.0±0.2,加盐酸羟胺,二氨基萘,比色。 [B]硫化物检查法 [/B] 方法同砷盐检查第一法,不装醋酸铅棉花,以醋酸铅试纸代替溴化汞试纸。 标准液取1ml 5/ml [B]澄清度检查法 [/B]将一定浓度的供试品溶液与浊度标准液分别置于配对的比浊用玻璃管,同置黑色背景上,在漫射光下观察。浊度标准液 硫酸肼与乌洛托品溶液混合分五个等级,未超过0.5等级即为澄清。BP98规定未超过1等级即为澄清。 [B]溶液颜色检查法 [/B]CHP2000 [B]1. 比色法[/B] 色调标准贮备液 黄色液 重铬酸钾液(BP98用氯化铁) 红色液 氯化钴液 蓝色液 硫酸铜液 配成各种色调色号标准比色液共50种。 [B]2. 分光光度法 [/B] [B]易碳化物检查法 [/B]检查药物中含有的遇硫酸易碳化或易氧化而呈色的有机杂质。 对照品液 样品液 加硫酸5后,加供试品。 [B]炽灼残渣检查法[/B] 取供试品1.0~2.0g或个药品项下规定的重量,置已炽灼至恒重的坩埚中,精密称定,缓缓炽灼至完全碳化,放冷至室温;除另有规定外,加硫酸使湿润,低温加热至硫酸蒸气除尽后,在700~800炽灼使完全灰化,移至干燥器内,放冷至室温,精密称定,再在700~800炽灼至恒重,即得。残渣限量一般为0.1~0.2% 一般应使炽灼残渣量为1~2mg 若需将炽灼残渣留作重金属检查时,炽灼温度必须控制在500~600。 [B]干燥失重测定 [/B]1. 常压恒温干燥法 2. 干燥剂干燥法 3. 减压干燥法 [B]水分测定法 [/B][B]费休氏法 [/B] 本法是根据碘和二氧化硫在吡啶和甲醇溶液中能与水起定量反应的原理以测定水分。 [B]甲苯法[/B] 在加热状态下,甲苯夹带着水分蒸出,收集蒸出的水分测定。 [B]药物中特殊杂质检查 [/B] [B]一、物理法 [/B] [B]二、化学反应法 [/B](一)容量分析法 (二)重量分析法 (三)比色法和比浊法 [B]三、色谱法 [/B]1.纸色谱法 薄层色谱法 TLC是药典中最常用的特殊杂质限量检查方法。 1.在一定供试品及检查条件下,不允许有杂质斑点存在 2.以待测杂质对照品检测 3.将供试品稀释到适当浓度作为杂质对照品溶液 4.选用质量符合规定的与供试品相同的药物作为杂质对照品 [B]高效液相色谱法 [/B] [B][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法 [/B] 1.面积归一化法 2.主成分自身对照法 3.内标法测定 4.内标法加校正因子法 5.外标法 有机溶剂残留量测定法 [B]分光光度法 紫外分光光度法 比色法 [url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度法[/B]
新手用的是科晓的气相 一样的毛细管柱 一样的气象条件 一样的样品 主峰在十分钟180度左右出峰 杂杂质是在两分钟 估计是90度就出峰的 现在的问题是 杂质峰变大很多 还后拖尾‘调节进样器的温度 从250 到200 杂质峰变小一些 但是拖尾更严重估计杂质是产品在高温状态下引起的 但是 以前走的样品不会这么 离谱 还有就是往下做的下一步产品还是好的。总结:产品是好的 但是现在一样的条件 走出的 图谱很不一样 纯度从98%到了86%请教各位是 仪器的问题吗?衬管是新的 干净的
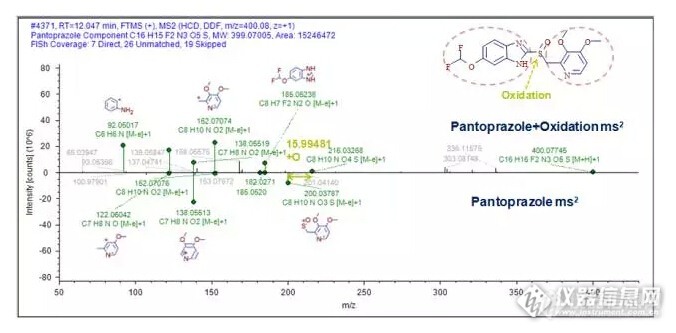
药物杂质是药物活性成分(原料药)或药物制剂中不希望存在的化学成分,会对用药的安全性和有效性带来隐患,因此杂质的检测是保证药物质量至关重要的部分,FDA、EMEA、PMDA、CFDA等各国药品监管部门制定了相应的指导原则对其进行严格管控。http://ng1.17img.cn/bbsfiles/images/2015/12/201512141737_577892_3005330_3.jpg 独有的四极杆静电场轨道阱Q Exactive™ Focus高分辨液质联用技术,凭其高灵敏度、高专属性和高准确性的分析能力,可对样品中药物杂质进行全面的信息采集。结合新一代的智能小分子化合物鉴定软件Compound Discoverer™,以高度灵活的自定义方式制定分析工作流程,对数据中的目标和非目标杂质进行提取、比对及鉴定,工作流程如下:http://ng1.17img.cn/bbsfiles/images/2015/12/201512141737_577893_3005330_3.jpg 通过软件对样品数据的分析和提取,在Compound Discoverer中可以直观、便捷的查看和筛选预期和未知的杂质分析结果,从结果界面中可获得不同条件下样品杂质的变化情况,获得所有杂质保留时间、一级质谱、同位素和二级质谱等丰富信息:http://ng1.17img.cn/bbsfiles/images/2015/12/201512141738_577894_3005330_3.jpg 在获得母药和杂质的一级和二级质谱信息后,软件将调用碎裂数据库(Fragmentation Library)快速的对泮托拉唑的碎片结构进行归属,该数据库几乎涵盖了所有已发表的文献,保证了碎片解析的准确性。在此研究结果之上,通过软件对杂质与母药二级质谱信息之间的比对,可进一步对杂质变化位点进行推测。在本例中,通过152、185等共有碎片和200、216等特征差异碎片的比对,推测出该杂质为泮托拉唑砜:http://ng1.17img.cn/bbsfiles/images/2015/12/201512141738_577895_3005330_3.jpg 基于新一代四极杆-静电场轨道阱质谱Q Exactive Focus和新一代小分子化合物分析软件Compound Discoverer,建立了药物杂质鉴定的新流程。无论是优质数据的有效获取,还是获取后对已知和未知杂质的分析鉴定,该工作流程都可以完美的实现。在本例中,共鉴定到泮托拉唑杂质15个,其中可能的降解杂质9个,可能的工艺杂质6个,为药物杂质的质量控制、安全性评估提供了富有价值的信息。(分享)
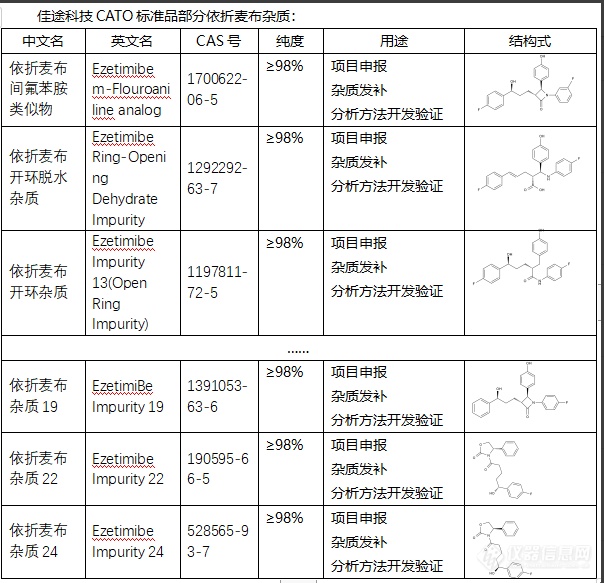
依折麦布是一种抗凝血药物,用于预防和治疗血栓和栓塞疾病。然而,在其生产过程中可能会生成杂质。依折麦布杂质可能会影响依折麦布的质量、疗效和安全性。如果杂质存在过多,可能对药物的抗凝作用产生干扰,造成药效减弱;此外,某些杂质可能对人体产生毒性,增加药物的副作用,甚至引发不良反应。因此,对于依折麦布的杂质需要通过有效的生产工艺和质量控制手段进行控制,以确保药物的质量和安全性。同时,药物注册时,也需要对杂质进行详细的评估,并提供关于杂质来源、性质、水平以及控制措施等的信息。在实际研究过程中,杂质的研究和控制也是药品研发的重要部分。CATO标准品通过研究依折麦布的杂质,可以进一步了解其化学性质和生理作用,有助于更好地理解和优化药物的生产过程,提高药品的质量和疗效。[img=,604,583]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021712539448_6005_6381668_3.png!w604x583.jpg[/img]
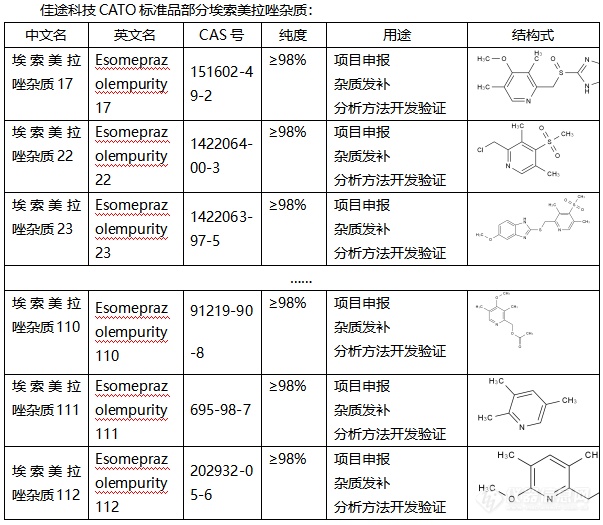
◇关于埃索美拉唑杂质 埃索美拉唑杂质是一种质子泵抑制剂,它不仅是[font=UICTFontTextStyleBody]治疗胃食管反流性杂质,还可以防止胃酸形成,[/font]它的原理主要是通过抑制胃壁细胞中[font=.pingfang sc]的[/font]H+/K+-ATP酶来达到减少胃酸分泌。埃索美拉唑杂质是一种高效且广泛应用于胃酸相关疾病治疗的质子泵抑制剂,通过抑制质子泵的活性,它不仅可以减少胃酸的分泌,还可以帮助溃疡的愈合。其作用机理是通过与胃腺细胞内的质子泵结合,形成稳定的复合物来发挥作用。[font=UICTFontTextStyleBody] [/font][font=UICTFontTextStyleBody]CATO[/font]标准品提供的[font=宋体]埃索美拉唑杂质[/font][font=宋体],在治疗肠胃道疾病中发挥着重要的作用,并且有针对性的抗菌作用。[img=,603,525]https://ng1.17img.cn/bbsfiles/images/2024/02/202402040930531289_1324_6381607_3.png!w603x525.jpg[/img] [/font]
替诺福韦杂质是一种化学物质,它是替诺福韦的同分异构体或相关化合物。替诺福韦是一种核苷酸逆转录酶抑制剂,用于治疗HIV和乙型肝炎。COTO标准品是一种高纯度的标准物质,用于测定替诺福韦及其杂质的纯度、含量和化学性质。通过与COTO标准品进行对比和分析,可以确定替诺福韦及其杂质的结构、组成和含量,从而保证替诺福韦的质量和安全性。在药物研发和生产过程中,COTO标准品的使用非常重要。它可以提供可靠的参照物,用于质量控制、药物分析和化学计量学研究。通过使用COTO标准品,可以确保替诺福韦及其杂质的准确性和可靠性,为药物的安全性和有效性提供保障。总的来说,COTO标准品在替诺福韦杂质的研究和控制中具有重要作用。通过使用COTO标准品,可以更好地了解替诺福韦及其杂质的性质和含量,从而确保药物的安全和有效性。同时,也需要加强生产过程中的管理和监督,加强质量标准和监管措施的执行力度,确保药物质量和安全。
[font=瀹嬩綋, SimSun]中国食品药品检定研究院(以下简称“中检院”)对布地奈德杂质A等8种标准物质原料采购项目进行公告,现诚邀符合项目要求的供应商报名参加。[/font][font=瀹嬩綋, SimSun][/font][font=瀹嬩綋, SimSun][b][font=宋体]一、项目基本情况[/font][/b][font=宋体][/font][/font][font=瀹嬩綋, SimSun]项目名称:中检院布地奈德杂质A等8种标准物质原料采购项目[/font][font=瀹嬩綋, SimSun]项目编号:ZFCG202300028[/font][font=瀹嬩綋, SimSun]项目需求:详见附件1[/font][font=瀹嬩綋, SimSun]提供技术资料要求:[/font][font=瀹嬩綋, SimSun]1[font=宋体]、根据需求清单中“技术要求”提供品种确证报告,报告应包括要求所列明内容;[/font][/font][font=瀹嬩綋, SimSun]2[font=宋体]、具有特殊资质要求的品种,按要求提供相关资质证明文件;[/font][/font][font=瀹嬩綋, SimSun]3[font=宋体]、货期要求:两个月[/font][/font][font=瀹嬩綋, SimSun]4[font=宋体]、质保期要求标化合格后1年。[/font][/font][font=瀹嬩綋, SimSun][b][font=宋体]二、供应商资格要求[/font][font=宋体][/font][/b][/font][font=瀹嬩綋, SimSun][size=14px]1.具有独立承担民事责任的能力;[/size][font=微软雅黑, sans-serif][size=14px][/size][/font][/font][font=瀹嬩綋, SimSun]2.[font=宋体]具有良好的商业信誉和健全的财务会计制度;[/font][/font][font=瀹嬩綋, SimSun]3.[font=宋体]具有履行合同所必需的专业技术能力;[/font][/font][font=瀹嬩綋, SimSun]4.[font=宋体]有依法缴纳税收和社会保障资金的良好记录;[/font][/font][font=瀹嬩綋, SimSun]5.[font=宋体]参加政府采购活动前三年内,在经营活动中没有重大违法记录;[/font][/font][font=瀹嬩綋, SimSun]6.[font=宋体]资格审查时,通过“信用中国”网站、中国政府采购网、国家企业信用信息公示系统、天眼查、企查查网站等渠道查询供应商信用记录,经查询列入失信被执行人、重大税收违法案件当事人名单、政府采购严重违法失信行为记录名单、经营异常名录信息、严重违法失信企业名单(黑名单)信息的,经查询在经营活动中有重大违法记录的,截至本项目采购活动开始前三年内因违法经营受到刑事处罚或者责令停产停业、吊销许可证或者执照、较大数额罚款等行政处罚的,不得参加本项目;[/font][/font][font=瀹嬩綋, SimSun]7.[font=宋体]单位负责人为同一人或者存在控股、管理关系的不同单位,不得参加同一项目响应;[/font][/font][font=瀹嬩綋, SimSun]8.[font=宋体]本项目不接受联合体参加,禁止转包或分包;[/font][/font][font=瀹嬩綋, SimSun]9.[font=宋体]供应商特殊资质要求见项目需求;[/font][/font][font=瀹嬩綋, SimSun]10.[font=宋体]法律、行政法规规定的其他条件。[/font][/font][font=瀹嬩綋, SimSun][b][font=宋体]三、[/font][font=宋体]报名方式[/font][font=宋体][/font][/b][/font][font=瀹嬩綋, SimSun]1.[font=宋体]本项目采取网上报名的方式,不设现场报名及其他形式的报名。符合项目要求的潜在供应商需填写完整报名表(附件2)发送至邮箱hqzc@nifdc.org.cn。(邮件命名:项目名称+报名单位名称)[/font][/font][font=瀹嬩綋, SimSun]2.[font=宋体]报名供应商需提交真实有效的响应文件(附件3)并加盖公章,密封邮寄至中检院联系人处。[/font][/font][font=瀹嬩綋, SimSun]3.[font=宋体]报名和文件邮寄送达时间截止至2023年3月 24 日(北京时间),逾期送达不予接收。[/font][/font][font=瀹嬩綋, SimSun][b][font=宋体]四、供应商确定原则[/font][font=宋体][/font][/b][/font][font=瀹嬩綋, SimSun]本项目以单品种质量和服务均能满足实质性响应且有效报价最低原则确定供应商。[/font][font=瀹嬩綋, SimSun][b][font=宋体]五、联系方式[/font][font=宋体][/font][/b][/font][font=瀹嬩綋, SimSun]采购单位:中国食品药品检定研究院[/font][font=瀹嬩綋, SimSun]地址:北京市大兴区生物医药产业基地华佗路31号院后勤政采部[/font][font=瀹嬩綋, SimSun]联系人: 袁玉萍[/font][font=瀹嬩綋, SimSun]联系电话:010-53852873[/font][font=瀹嬩綋, SimSun]电子邮箱:hqzc@nifdc.org.cn[/font][font=瀹嬩綋, SimSun] [/font][font=瀹嬩綋, SimSun]附件:1.[font=宋体]中检院布地奈德杂质A等8种标准物质原料采购项目需求清单[/font][/font][font=瀹嬩綋, SimSun]2. [font=宋体]标准物质原料项目报名表[/font][/font][font=瀹嬩綋, SimSun]3. [font=宋体]供应商报名响应文件[/font][/font][font=瀹嬩綋, SimSun] [/font][align=right][font=瀹嬩綋, SimSun]中检院 [/font][/align][align=right][font=瀹嬩綋, SimSun]2023[font=宋体]年3月13日[/font][/font][/align]【附件】[list][*][img]https://www.nifdc.org.cn/directory/web/fileTypeImages/icon_xls.gif[/img] [url=https://www.nifdc.org.cn/directory/web/nifdc/infoAttach/f7b10119-e6a8-4cca-94dd-3ca956450bbe.xlsx]附件1:中检院布地奈德杂质A等8种标准物质原料采购项目需求清单.xlsx[/url][*][img]https://www.nifdc.org.cn/directory/web/fileTypeImages/icon_xls.gif[/img] [url=https://www.nifdc.org.cn/directory/web/nifdc/infoAttach/145c64d7-ae60-4efe-8563-f762c0643ecf.xlsx]附件2:标准物质原料项目报名表.xlsx[/url][*][img]https://www.nifdc.org.cn/directory/web/fileTypeImages/icon_xls.gif[/img] [url=https://www.nifdc.org.cn/directory/web/nifdc/infoAttach/31460800-8479-4873-8b30-5de470d3d7bb.xlsx]附件3:供应商报名响应文件.xlsx[/url][/list]
化药质量控制CTD申报资料中杂质研究的几个问题张哲峰成海平宁黎丽田洁化药药学二部 摘要:杂质研究与控制是把控药品质量风险的重要内容之一,基于杂质谱分析的杂质控制是“质量源于设计”基本理念在杂质研究与控制中的具体实践,需要与CMC各项研究乃至药理毒理及临床安全性研究等环节关联思考、综合考虑,而不仅仅拘泥于提供准确的分析数据。本文针对当前CTD申报资料中杂质研究方面存在的问题与不足,结合CTD过程控制和终点控制相结合、研究和验证相结合、全面系统的药品质量控制理念,探讨仿制药杂质研究与控制的基本逻辑思路,提出CTD申报资料中杂质研究与控制方面几个需要关注的问题。 关键词:杂质研究与控制 杂质谱 CTD格式 杂质研究与控制是一项系统工程,需要以杂质谱分析为主线,安全性为核心,按照风险控制的策略,将杂质研究与CMC各项研究,乃至药理毒理及临床安全性研究等环节关联思考、综合考虑,而不仅仅拘泥于提供准确分析数据的传统思维,不是一项孤立的分析工作。CTD(Common Technical Document)申报格式体现了过程控制和终点控制相结合、研究和验证相结合、全面系统的药品质量控制理念,更加符合杂质研究与控制的基本规律和逻辑思路。自2011年4月起,药审中心陆续发布了多项有关CTD格式及技术审评的相关要求及电子刊物,对于国内研发单位正确理解CTD格式内含的基本精神起到了一定的促进作用,但就目前阶段的申报情况看,有些申报资料在杂质研究方面仍存在一些不足,仅仅是形式上的CTD格式,尚未实质性贯彻CTD的基本逻辑思路。以下是针对目前CTD申报资料中杂质研究相关问题的一些考虑。 1、CTD格式中杂质控制的考虑要体现在CMC的各个环节,而不是仅仅局限在“质量控制”模块。如制剂的原辅料控制中,原辅料的选择与控制要考虑以符合制剂质量要求(杂质等)为核心,必要时进行精制处理并制定内控标准;关键工艺步骤及参数的确立、工艺开发过程等要考虑以杂质是否得到有效控制为重点关注之一;制剂相关特性中要体现与原研产品杂质谱等的对比情况;包材、贮藏条件以及有效期的确立等也要以杂质是否处于安全合理的可控范围内为核心等等。实际上这正是源头控制、过程控制与终点控制相结合的杂质控制理念的体现,在研发工作及申报资料的整理中都需要针对性的贯彻实施。 问题与案例:有些申报资料在某种程度上未能充分体现杂质研究的整体性,对杂质控制措施仅强调了终点控制措施,尚未充分体现源头控制与过程控制的基本思路,具体表现在如下方面: (1)制剂杂质控制受制于原料药质控水平的约束,以目前国内批准的原料药杂质水平现状为由,未能根据该品当前杂质控制的水平与趋势,对原料药提出较为严格的针对性的杂质控制要求,并进行质量内控,因而难以确保制剂杂质控制水平与目前国际水平相适应; (2)在论述说明制剂相关特性时,未提供与原研产品杂质谱的对比分析情况; (3)关键工艺步骤及参数的确立、工艺开发过程相关内容中未详细说明杂质谱的变化情况,缺失关键质量数据的支持。 2、CTD格式的特点之一是研究内容模块化呈现,但需关注杂质分析与控制的系统性与整体性,不能割裂各项内容的必然联系和有机统一。比如对原料药而言,杂质分析与控制的相关内容会分布在分析方法(3.2.S.4.2)、方法学验证(3.2.S.4.3)、杂质对比研究与杂质谱分析(3.2.S.4.5)、杂质情况分析总结(3.2.S.3.2)、样品检测与数据积累(3.2.S.4.4)、控制限度(2.3.S.4.1)等各模块中,但杂质研究又是一项系统工程,具有统一的整体性,因此,不要因为申报资料格式的模块化而人为割裂各项研究内容的相互联系,甚至遗漏相关研究内容,要高度关注杂质分析与控制的系统性与整体性,将杂质研究与控制的全部内容和信息体现在相应模块中。如详细的杂质研究报告可以体现在3.2.S.4.5中;3.2.S.3.2要报告杂质研究的结果;杂质分析方法的筛选、研究与验证内容要在3.2.S.4.3中体现;对仿制药而言,杂质限度确定的论证与依据需要在与原研产品进行全面的杂质谱对比研究基础上进行论证说明,因此,与原研产品的对比研究及结论要在3.2.S.4.5中体现。 问题与案例:有些申报资料忽视了各项研究间的关联性,未能充分突出仿制药研发的特点,具体体现如下: (1)对分析方法的来源没有足够明确的说明,在分析方法的筛选、优化等方面做了哪些研究等信息缺失,只有方法学验证内容,缺失方法学筛选研究的相关信息; (2)没有比较说明采用的杂质分析方法与USP、BP/EP、JP等药典同品种分析方法相比有哪些区别和优势,未能从分析方法、杂质控制种类及限度要求等方面的比较情况评估拟定质量标准的杂质控制水平; (3)缺失放行标准质控限度确定的依据进行论述,3.2.S.4.5中只对货架期标准限度的确定进行了相关说明,未从杂质来源与特点、数据积累、稳定性考察等角度论述放行标准中相关限度确定的依据。 3、从杂质谱分析入手确立科学的杂质研究基本思路。杂质谱包括药物中所有杂质的种类、来源及特性等信息,通过杂质谱分析较为全面地掌握产品中杂质概貌(种类、含量、来源和结构等);有针对性地选择合适的杂质分析方法,以确保杂质的有效检出和确认;通过与原研产品杂质谱的对比研究,根据各相应杂质的一致性求证,或跟踪杂质谱对安全性试验或临床试验结果产生的影响,评估各杂质的安全性风险和可接受水平;结合规模化生产时杂质谱的变化情况,确立安全合理的杂质控制水平。 基于杂质谱分析的杂质研究是一种“以源为始”的主动思维模式,以“质量源于设计”的观点,从杂质来源入手,从制备工艺、化学结构、处方组成的分析出发,评估、预测产品中可能存在的及潜在的副产物、中间体、降解物以及试剂、催化剂残留等大体的杂质概况,辅以适当的强制降解、对照物质的加入等验证的手段,考证建立的分析方法是否能够将它们逐一检出,并进行相应的方法学验证工作;相比之下,传统的杂质研究是一种“以终为始”的被动行为和逆向思维模式,从杂质分析的结果出发,仅从建立的某种检测方法所检出的有关物质中归属其来源情况,而未充分分析与验证可能存在的潜在杂质情况,建立的分析方法能否全面检出这些杂质,故容易出现杂质漏检的情况,难以全面掌握产品的杂质谱。 问题与案例:杂质谱分析表明某原料药所采用的合成路线会产生具有遗传毒性的双叠氮杂质ROX,但最初建立的分析方法未检出该杂质,但不能确定是产品中的确不存在该杂质,还是建立的分析方法不能有效检出该杂质,经定向制备该杂质,采用标准加入法有针对性的分析考查,采用改进后分析方法在正常产品中检测到该物质,尽管其含量极低,考虑到其较强的毒性情况,质量标准中仍作为特定杂质予以严格控制,保证了其临床应用的安全性。因此,基于杂质谱分析的杂质研究是一种相对科学的思维模式,对于有效掌控杂质安全性风险具有重要意义。 4、分析方法的验证应具备针对性和全面性。杂质的微量性和复杂性,使得检测方法的专属性、灵敏度和准确度十分关键。杂质分析方法的对象是各个潜在的杂质,因此,其分析方法的验证需要根据不同杂质的特点综合设计验证方案,进行有针对性的规范验证。 问题与案例:一些申报资料中对杂质分析方法的灵敏度、准确度等仅仅针对主药化合物进行验证,仍无法说明是否适用于相关杂质的检出和定量。如下是某药物有关物质测定方法学验证总结,基本体现了方法学验证的针对性与全面性,建议参考。 项目验证结果专属性①统适用性良好,峰形、峰纯度、柱效参数等符合要求。②在酸、碱、高温、氧化各破坏条件下的主峰峰纯度角均小于纯度阈值,主峰峰纯度良好,破坏后的主峰与各杂质峰均能有效分离,分离度均大于1.5。③供试液加入起始原料、反应试剂、副产物及中间体等,均可有效检出,并良好分离。线性和范围①质A浓度在0.036μg/ml~1.204μg/ml范围内,线性关系良好(n=8);y=13703x-174.83;R2=0.9991。②杂质B浓度在0.089μg/ml~1.192μg/ml范围内,线性关系良好(n=7);y=10941x-517;R2=0.9995。③杂质C浓度在0.299μg/ml~4.784μg/ml范围内,线性关系良好(n=7);y=13257x-492.44;R2=0.9999。④主药浓度在0.3μg/ml~4.8μg/ml范围内,线性关系良好(n=6);y=15008x+565.48;R2=0.9999。灵敏度杂质A、B、C及主药最低检出限分别为0.012ng、0.0
如何除石油产品中的杂质 石油里的成分主要是碳氢化合物,但同时还有不少含有硫、氮和氧的化合物,以及微量的金属。它们大多是有害物质。含硫的化合物中有的本身就具有腐蚀性。而它燃烧后生成的二氧化硫和三氧化硫遇水会变成亚硫酸和硫酸。它们更是强腐蚀性物质。石油中的含氧化物大多带有酸性,尽管石油酸有特殊的用途,但是在石油产品中还是属于有害成分。石油中的含氮化合物则多半带有碱性,会使有些催化剂中毒。此外,轻油中的砷以及重油中的镍、钒等也都是对催化剂有害的物质,均属于要脱除的物质。 所以,这些杂质是非要除掉不可的。目前,普遍采用的精制方法是加氢精制。所谓加氢精制是指在较高的压力和温度下,使石油产品中的硫、氮、氧与外加的氢气反应,生成气态的硫化氢、氨和水,从而得到比较干净的液体石油产品。通过加氢,同时还可以除去油中的金属杂质。 加氢精制技术的核心是它所用的催化剂。此类催化剂的品种很多,性能有别、牌号各异,但是万变不离其宗。其活性组分都离不开钴、钼、镍、钨这几种元素,同时一般都是以氧化铝为载体,有时也加入一些分子筛。 有些原油中硫含量高,近年来对汽油等燃料的质量要求越来越高,对含硫量的限制越来越严,所以加氢精制已是必不可少的步骤。有些原油含氮较多,可是脱除氮要比脱除硫更困难些。为此,我国专门研制出了脱氮性能优越的加氢精制催化剂。 加氢精制的操作条件得根据原料所含杂质的性质和数量以及对产品质量的要求来确定。其反应温度的范围很宽,在300摄氏度至400摄氏度,而压力的范围更宽,低的只有十几个大气压(约1兆帕),高的会达100多个大气压(约10兆帕),几乎相差十倍之多。
在做程序升温操作时,载气中的某些杂质,在低温时保留在色谱柱中,当拄温升高时不但引起基线漂移还可能在谱图上出现比较宽的"假峰"。7)仪器影响a.各类过滤器加速失效 b.调节阀(稳压阀,稳流阀,针形阀)被污染,气阻堵塞,调节精度降低或失灵;c.气路系统被污染,若要恢复仪器在高灵敏度情况下操做,有时要吹洗很长时间(可能一周以上)污染严重时有时再也无法恢复。d.检测器的寿命,实践表明,对ECD和TCD的寿命影响最明显,应引起用户特别注意。二.对气体纯度选择的一般原则1.从分析角度讲,微量分析比常量分析要求高,也就是说,气体中的杂质含量必须低于被分析组分的含量,如果用TCD分析10ppm的CO,则载气中的杂质总含量不得超过10ppm,因为99.999%纯度的气体则含0.001%的杂质,相当于10ppm所以对于10ppm的痕量分析,载气的纯度应高于99.999% 对于FID使用气体,碳氢化合物含量必须很低,载气中的大量氧杂质只要不对色谱柱造成影响,就不影响FID的性能,而操作ECD,载气中的氧气和水的含量必须很低等.2.毛细管柱分析比填充柱分析要求高 3.程序升温分析比恒定温度分析要求高 4.浓度型检测器比质量型检测器要求高 5.配有甲烷装置的FID比单FID操作的对载气中的微量CO,CO2要求要高的多.6.从仪器寿命和保持仪器的高灵敏度讲,中高档仪器比低当仪器要求高 三.操作不同检测器推荐使用的气体纯度我们推荐气体纯度的技术要求,通常用于常规分析,对于要求高灵敏度的痕量分析时,也可以使用更高纯度的气体。由于各个制气厂设置不同,其杂质含量将有所不同 为满足不同的使用要求,选用不同厂家不同纯度的气源后,可以通过气体净化处理满足分析要求。对于不同杂质的气体采用何种净化方法和装置有机会在加以讨论。综上所述,新购[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]接入气源时,一定要做到心中有数,决不能随意接入,否则会造成ECD,甲烷化装置等的损伤,信噪比减小的无法使用,下面给出了用于常规分析时,推荐使用的气体纯度(仅供参考):TCD 氦做载气:至少纯度为99.995%。杂质含量分别为:氖<10ppm 氮 <10ppm;氧<2.5 ppm 氩<0.1 ppm 二氧化碳<0.25 ppm。氢做载气: 至少纯度为99.995%。 杂质含量分别为: 氮<1 ppm 氧<5 ppm 二氧化碳<1 ppm 水<5 ppm 总烃<1 ppm 。FID 氮做载气: 至少纯度为99.998%。杂质含量分别为:氢<1 ppm 氧<1 ppm 氩<10ppm 二氧化碳<1 ppm 水<5 ppm 甲烷<1 ppm。氢气: 同TCD 空气: 呼吸级杂质:氩,氪,水,氦,氖均小于1%; 二氧化碳<500 ppm 一氧化碳<10ppm 总烃<0.02 ppm 甲烷<20 ppm。ECD 氮做载气: 至少纯度为99.998%。典型杂质同上。
机械杂质是指石油或石油产品中不熔和油和规定溶剂的物质的量的总和。 如泥砂、尘土、铁屑、纤维和某些不溶性盐类。机械杂质可用沉淀或过滤等方法除去。对轻油来说,机械杂质会堵塞油路,促使生胶或腐蚀;对锅炉燃料,会堵塞喷嘴,降低燃烧效率,增加燃料消耗。对润滑油,则会破坏油膜,增加磨损,堵塞油过滤器,促进生成积炭等。所以称之为机械杂质,机械杂质来源于油品的生产、贮存和使用中的外界污染或机械本身磨损,大部分是砂石和积碳类,以及由添加剂带来的一些难溶于溶剂的有机金属盐。其测定按GB/T 511-83石油产品和添加剂机械杂质测定法(重量法)进行。机械杂质测定仪测试过程是:称取100g的试油加热到70℃到80℃,加入2-4倍的溶剂。在已衡重的空瓶中的纸上过滤,用热溶剂洗净滤纸瓶再称重,定量滤纸的前后重量之差就是机械杂质的重量,由此求出机械杂质的质量分数。[font=&]得利特(北京)科技有限公司专注于油品分析仪器的研发和销售活动,我公司产品有:酸值测定仪、微量水分测定仪、凝点倾点测定仪、体积电阻率测定仪、介电强度测定仪、介质损耗测定仪、水溶性酸测定仪、界面张力测定仪、析气性测定仪、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析仪等多种绝缘油分析仪器、燃料油分析仪器、润滑油分析仪器,水质分析检测仪器、气体检测仪器,型号多,质量保证,可定制。他们家发动机油表观粘度测定仪性能比较稳定且符合GB/T6538标准。[/font][font=&][/font]
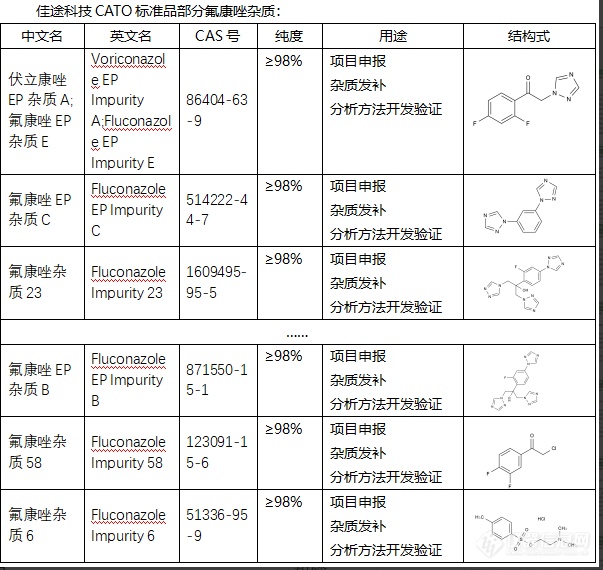
氟康唑杂质可能来自原料药、副反应产物或分解产物,以及其在存储过程中可能发生的变化。这些杂质如果未被及时检测和控制,可能对药物的效力和安全性产生影响,包括药效降低、不良反应增加等。因此,检测和控制氟康唑中的杂质是药品生产过程中的重要环节,对药物质量、安全性以及疗效的保证至关重要。研究分析这些杂质,还可以优化生产工艺,减少杂质产生,提高药物的质量和疗效。CATO标准品对沙格列汀杂质的研究也能帮助优化制药流程,找出产生过多杂质的环节,从而改进工艺,提高药品的质量和疗效。[img=,603,570]https://ng1.17img.cn/bbsfiles/images/2024/02/202402052101491000_1515_6381668_3.png!w603x570.jpg[/img]