[color=#444444]用微生物法检测维生素B12,生物素,叶酸,德国拜发的试剂盒,那个方法确认怎么做[/color]
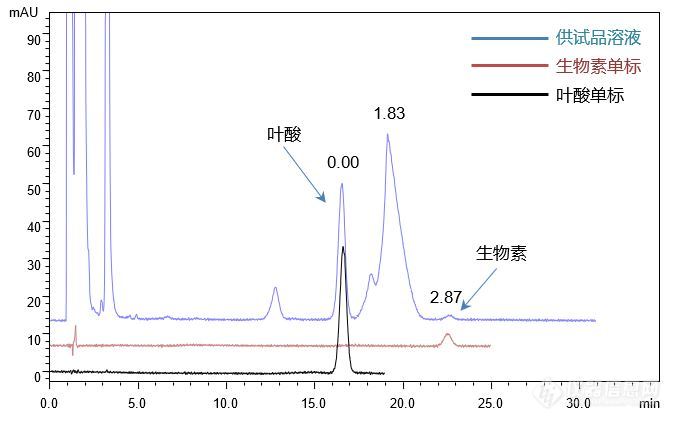
[align=center][b]注射用水溶性维生素的分析(2)[/b][/align][align=center][b]——叶酸,生物素[/b][/align]客户提供了注射用水溶性维生素粉针剂及对照品(叶酸,生物素),要求本实验室依据客户所提供方选择合适色谱柱,满足方法中对叶酸,生物素及其前后相邻杂质的分离要求,进而达到准确定量的目的。首先,依据客户提供的色谱条件我们尝试了使用中等极性色谱柱CAPCELL PAK C18 MGII S5 4.6 mm i.d. × 150 mm(A4AB 07251),分析对照品溶液与供试品溶液,结果如图1所示,对照品溶液中叶酸及生物素得到了良好的分离结果;在分析供试品溶液时,叶酸与其后杂质峰能够得到分离度为1.83的良好分离结果。[align=center][img=,673,421]http://ng1.17img.cn/bbsfiles/images/2018/01/201801110920_3890_2222981_3.jpg!w673x421.jpg[/img][/align][align=center]图1 CAPCELL PAK C[sub]18[/sub] MGII(150 mm)分析对照品及供试品溶液结果[/align]注*峰上所标数字为分离度,下同。[img=,673,298]http://ng1.17img.cn/bbsfiles/images/2018/01/201801110920_2922_2222981_3.jpg!w673x298.jpg[/img]为提高分离能力,使叶酸峰与其后杂质峰分的更远,我们尝试将色谱柱长度由150 mm换为250 mm,再一次分析供试品及对照品溶液,结果发现叶酸和生物素保留时间均明显延长,叶酸峰由16.97 min延长到29.03 min,此时叶酸峰与其后相邻杂质峰能够得到更好的分离,分离度为4.23,但同时也发现生物素峰被包于杂质峰中(如图2)。[align=center][img=,690,437]http://ng1.17img.cn/bbsfiles/images/2018/01/201801111011_6191_2222981_3.jpg!w690x437.jpg[/img][/align][align=center]图2 CAPCELL PAK C[sub]18[/sub] MGII(250 mm)分析对照品及供试品溶液结果[/align][align=left][img=,668,303]http://ng1.17img.cn/bbsfiles/images/2018/01/201801111011_2127_2222981_3.jpg!w668x303.jpg[/img][/align][align=left][/align][align=left]为使客户有更多色谱柱选择,本实验室也尝试了高碳载量的SUPERIOREX ODS色谱柱对对照品溶液及供试品溶液进行分析,同样能够得到待测组分与前后杂质峰的良好分离,分离度均在2.0以上;同时,我们也发现在分析供试品时,由于供试品中复杂基质的影响,叶酸峰会出现一定的拖尾现象(如图3)。[/align][align=left][/align][align=center][img=,619,394]http://ng1.17img.cn/bbsfiles/images/2018/01/201801111012_1478_2222981_3.jpg!w619x394.jpg[/img][/align][align=center] 图3 SUPERIOREX ODS分析对照品及供试品溶液结果[/align][align=center][/align][align=left][img=,687,297]http://ng1.17img.cn/bbsfiles/images/2018/01/201801111012_3462_2222981_3.jpg!w687x297.jpg[/img][/align][align=center][/align][align=left]我们也尝试使用可以在100%水系流动相下使用的高极性AQ色谱柱分析供试品溶液及对照品溶液,发现由于整体保留时间过长而使得生物素峰被包于杂质峰中,因此,我们尝试缩短整体保留时间,在药典规定范围内,提高流动相中有机相比例,将流动相比例由磷酸二氢钾缓冲溶液-乙腈(93:7)调整为(91:9),最终发现供试品中叶酸和生物素也能够与其相邻杂质峰取得良好分离结果,且分离度更佳(见图4)。[/align][align=left][/align][align=center][img=,655,416]http://ng1.17img.cn/bbsfiles/images/2018/01/201801111020_155_2222981_3.jpg!w655x416.jpg[/img][/align][align=center]图4 CAPCELL PAK C[sub]18 [/sub]AQ S3分析对照品及供试品溶液结果[/align][align=left][img=,661,296]http://ng1.17img.cn/bbsfiles/images/2018/01/201801111021_778_2222981_3.jpg!w661x296.jpg[/img][/align][align=left][/align][align=left]综上实验结果,使用中等极性的[b]CAPCELL PAK C[sub]18[/sub] MGII S5[/b] 4.6mm i.d. × 150 mm(A4AB 07251)和高碳载量的[b]SUPERIOREX ODS S5[/b] 4.6 mm i.d. × 150 mm(AZAB 12684)色谱柱,在客户原条件下,均能够实现叶酸、生物素及其相邻杂质间的良好分离;[/align][align=left]使用高极性[b]CAPCELL PAK C[sub]18[/sub] AQ S3[/b] 4.6 mmi.d. × 150 mm(A7AB 02100)色谱柱,在药典规定流动相可调整范围内,将流动相中磷酸盐缓冲液和乙腈比例调整为91 / 9(原条件为93 / 7),也可实现注射用水溶性维生素中叶酸和生物素及相邻杂质的良好分离。[/align]
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=54229]食物中生物素(维生素H)的测定方法[/url]
最近经常做复合维生素片剂中的维生素,其他的维生素还好,用国标的方法都能做出来,就是生物素和维生素B12不太好做,国标中是微生物法,我学化学的,不会做,参考的很多液相测定方法检测限都达不到,大家是怎么做的,有没有用荧光检测器做的
[align=center][font=DengXian]维生素的生物可利用性[/font][/align]1 [font=DengXian]维生素生物可利用性的含义[/font][font=DengXian]维生素的生物可利用性([/font]Bioavailabilityof vitamin[font=DengXian])是指人体摄入的维生素经肠道吸收并在体内被利用的程度。包含两方面含义即吸收与利用。因此,在评价维生素营养完全性时除考虑摄入的食品中维生素的含量和不同化学结构的鉴定外,更重要的应考虑摄入食品中维生素的生物可利用性。[/font]2 [font=DengXian]影响维生素生物可利用性的因素[/font]1[font=DengXian]、消费者本身的年龄、健康以及生理状况等;[/font]2[font=DengXian]、膳食的组成影响维生素在肠道内运输的时间、黏度、[/font]pH[font=DengXian]及乳化特性等;[/font]3[font=DengXian]、同一种维生素构型不同对其在体内的吸收速率、吸收程度、能否转变成活性形式以及生理作用的大小产生影响;[/font]4[font=DengXian]、维生素与其他的组分的反应如维生素与蛋白质、淀粉、膳食纤维、脂肪等发生反应均会影响到其在体内的吸收与利用;[/font]5[font=DengXian]、维生素的拮抗物也影响维生素的活性,从而降低维生素的生物可利用性。例如,硫胺素酶可切断硫胺素代谢分子,使其丧失活性;抗生物素蛋白与代谢物结合,使生物素失去活性;双香豆素具有与维生素[/font]K[font=DengXian]相似的结构,可占据维生素[/font]K[font=DengXian]代谢物的作用位点而降低维生素[/font]K[font=DengXian]的生物可利用性;[/font]6[font=DengXian]、食品加工和贮存也影响到维生素的生物可利用性。[/font]
VitaFast Vitamin B7 生物素试剂盒简单易用,采用微生物方法,在微孔板中定量检测食品和药品中的生物素总量(包括添加和原生生物素)。AOAC – RI认证的样品: 婴幼儿配方乳粉、谷类食品、药丸、散剂、果汁和牛奶
[size=3][size=2]跪求各位雷友: 本人急需维生素C生产过程中,粗VC的熔点测定方法及标准范围,还有食品添加剂维生素C是否做微生物检验。谢谢!

http://ng1.17img.cn/bbsfiles/images/2012/11/201211201436_405528_2518341_3.jpg其一款婴儿奶粉在香港被查出生物素含量不达标,可导致婴儿脱发、皮疹等,香港食环署已建议停售,至此相关奶粉的事件已经成为常态新闻了,三聚氰胺、婴儿提早发育、还有婴儿脱发等等,这些让人触目惊心的新闻背后到底有多少不可告人的秘密?根据食环署近日公布的一份报告,明治细仔奶粉0-12个月(850克)的生物素含量只有0.81微克/100千卡,低于食品法典委员会标准。风险评估发现,如根据标签上的喂哺建议,其生物素摄入量将低于世界卫生组织建议的摄入量5微克/日。而另一款和光堂的初生婴儿奶粉为0.68微克/100千卡,同样低于食品法典委员会标准。食物安全中心发言人表示,膳食生物素缺乏症是非常罕见的,未曾在母乳喂养的婴儿出现。但是如果零至6个月大婴儿长期只单纯靠上述奶粉摄取生物素,不排除对健康有不良影响。生物素缺乏的婴儿可能会出现脱发、皮疹、肌肉张力低、嗜睡等症状。你家的孩子现在吃的是什么奶粉?奶瓶塑化剂事件刚过,奶粉生物素问题又来了,怎样才能给自己孩子的健康给一个安全的保障?奶粉中生物素含量应该怎么来测定?奶粉生物素含量国家标准有哪些?生物素的物性是什么?为什么会引起婴儿脱发?
常常看到一个小小的维生素E标准品,竟然有好多相关标准品,如维生素E/生育酚、α-维生素E、β-维生素E、γ-维生素E和δ-维生素E、维生素E乙酸酯、维生素E棕榈酸酯、维生素E琥珀酸酯、DL-α-维生素E 标准品、DL-α-维生素E醋酸酯 标准品,太多了,我要做食品里面的维生素E的含量检测,到底要选哪个是合适的?http://simg.instrument.com.cn/bbs/images/brow/em09506.gif
我们要开展婴幼儿乳制品中维生素类的测定,维生素A的标准好象有好几种,好象有维生素A乙酸酯、维生素A酸等等,请哪位高手给点意见,具体应该买哪种?
您好:我用三氯化铁,2,2—联吡啶法测量维生素E,我将维生素E标准品(中国药品生物制品检定所)溶于无水乙醇中,加三氯化铁,2,2—联吡啶后溶液没有变色,您看这是因为什么。
本人急需氘代生物素作为内标,不知道在哪里可以买到,请高手指点!感谢!
如题,求液相维生素A标准品的配制方法
微生物法测维生素B12时,标准曲线必须是直线吗?望老师不吝赐教
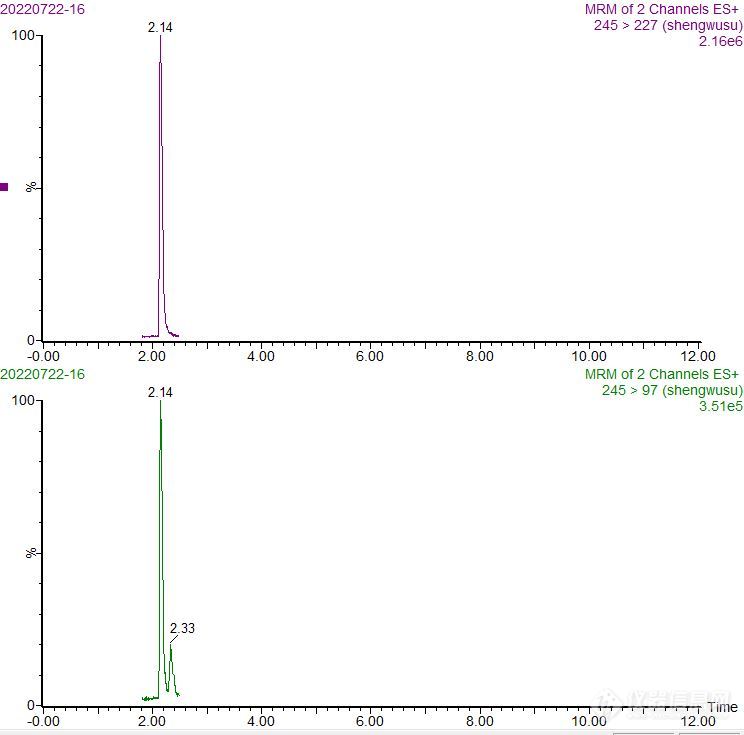
[size=16px]超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法测定奶粉中生物素的含量[/size][align=center][size=16px]户江涛[/size][/align][align=center][size=16px](黑龙江省农垦科学院测试化验中心,黑龙江 佳木斯 154007 )[/size][/align][size=16px]摘要:采用超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法建立了检测奶粉中生物素含量的分析方法,对试样提取、净化条件,流动相、色谱柱和质谱条件进行了优化,结果表明该方法与国标微生物法对同一样品检测得到的生物素含量基本一致,但检测所需时间大大减少,且抗干扰能力、精密度均比微生物法高,特别适和大批量奶粉中生物素含量检测。关键词:超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱;奶粉;生物素生物素又称维生素B7,是生物体内羧基转化酶作用的一种辅酶,在人体生长、代谢、发育过程中发挥着重要的作用。人类自身不能合成生物素,需从膳食中获得,而奶粉是人类(特别是婴幼儿)获取生物素的重要途径,准确测定奶粉中生物素含量有重要意义。目前国家标准规定的生物素测定方法《GB 5009.259-2016 食品安全国家标准 食品中生物素的测定》为微生物法。该方法需要购买特定菌种,成本较高,且菌种难保存、易受污染,实验操作复杂、费时费力、技术难度大、对检验人员和实验室要求较高,且容易受到基质干扰、检测结果重复性较差。同时奶粉成分复杂,所含生物素含量极低,一般为十几个微克/100克。因此,制定一种准确、高效、便捷、灵敏度高的生物素测定方法迫在眉睫。基于高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]的分离能力和质谱的高灵敏度、高选择性,采用[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱测定法具有前处理简单、分析速度快,适用的基质范围广、实用性强,可以为奶粉中生物素含量的测定提供一种有效的检测手段。本文建立的超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法测定奶粉中生物素含量[color=black]的方法前处理过程简便、分析时间短、灵敏度高、抗干扰能力强,特别适用于大批量奶粉样品中生物素[/color]含量的检测。1 实验部分1.1 材料与试剂[color=black]生物素(纯度[/color][font=宋体][color=black]≥[/color][/font][color=black]99%,Sigma公司);婴儿配方乳粉定量分析质控样品(BQC1051147452,北京普天同创生物科技有限公司);乙腈、甲酸(色谱纯,Fisher公司);Prime HLB固相萃取柱(200 mg,3 mL,[/color][font=宋体]Waters[/font][color=black]公司);0.2 um有机系滤膜;实验用水为Millipore纯水仪制备。[/color]1.2 仪器与设备UPLC XEVO TQ-S超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱仪(Waters公司);涡旋振荡器。1.3 [color=black]生物素[/color]标准储备液的配置称取一定量生物素[color=black]标准品[/color],用50%乙醇-水溶液配置成质量浓度为100 ug/mL标准储备液,于2~4℃冰箱保存(有效期1个月),待用;临用前将溶液回温至室温,并吸取一定体积储备液用水逐级稀释成所需浓度的标准工作液。1.4 样品前处理准确称取1.00 g(精确到0.01 g)奶粉试样于50 mL离心管中,加入10.00 mL纯水涡旋混匀2 min,然后加入10.00 mL乙腈,涡旋混匀1 min,然后在离心机中以15000 r/min离心5 min,取出后吸取2 mL上清液置于[color=black]Prime HLB固相萃取柱中,使其自然流出弃去最初几滴,然后用玻璃试管接取流出液约1 mL涡旋混匀,[/color]过0.22[font=宋体]u[/font]m有机系微孔滤膜后供UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS分析测定。1.5 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]及质谱条件[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]:色谱柱:Waters HSS [font=times new roman]T3(1.8 μm,100mm×2.1mm);柱温:30℃[/font];流速:[font=times new roman]0.3 [/font]mL/min;进样量:[font=times new roman]2[/font] [font=times new roman]μL;流动相A:乙腈;流动相B:0.1%的甲酸水溶液。梯度洗脱程序:0~0.5min,10% A;0.5~3. 0 min,10%~100% A;3. 0 ~4. 0 min,100%A,4 ~4.1min,100% A~10% A,4.1 ~5.0min 10% A。[/font]质谱:离子源:电喷雾离子源( ESI [sup]+[/sup] ) ;扫描方式:正离子扫描;检测方式:多反应监测( MRM);毛细管电压:3.2 kv;离子源温度:150℃;去溶剂气温度:500℃;去溶剂气流量:1000 L /h;定性、定量离子对及碰撞能量见表1。[/size][align=center][size=16px]表1生物素的质谱参数[/size][/align][table][tr][td][align=center][size=16px]分析物[/size][/align][/td][td][align=center][size=16px]锥孔电压/V[/size][/align][/td][td][align=center][size=16px]母离子/(m/z)[/size][/align][/td][td][align=center][size=16px]子离子/(m/z) [/size][/align][/td][td][align=center][size=16px]碰撞能量/V[/size][/align][/td][/tr][tr][td][size=16px]生物素[/size][/td][td][align=center][size=16px]30[/size][/align][size=16px][/size][/td][td][align=center][size=16px]245[/size][/align][size=16px][/size][/td][td][align=center][size=16px]227﹡[/size][/align][align=center][size=16px]97[/size][/align][size=16px][/size][/td][td][align=center][size=16px]13[/size][/align][align=center][size=16px]25[/size][/align][size=16px][/size][/td][/tr][/table][size=16px]﹡为定量离子2 结果与讨论2.1 色谱质谱条件及前处理过程的优化流动相的选择:对比了酸性体系(0.1%甲酸水溶液)与甲醇、乙腈的流动相体系组合,结果发现生物素在乙腈体系中响应值比甲醇更好一些,故本研究采用0.1%甲酸水溶液+甲醇流动相体系。色谱柱的选择:比较了[font=宋体]Waters [/font]BEH C[sub]18[/sub](1.7 μm,50mm×2.1mm)和[font=宋体]Waters [/font]HSS T[sub]3[/sub](1.8 μm,100mm×2.1mm)两种不同填料的分析柱,实验时发现目标物在这两款色谱柱上响应值差不多,但目标物在BEH C[sub]18[/sub]上保留时间比HSS T[sub]3[/sub]要短,考虑到生物素本身属于水溶性维生素,极性较强,若出峰太早可能造成奶粉中一些极性强的基质随目标物一起共流出进而干扰目标物测定,因此本方法采用了HSS T[sub]3[/sub]色谱柱。质谱参数优化:将1.0 mg/L 生物素标准溶液直接注射到质谱中,在正离子模式下进行母离子全扫描,发现目标物各自对应的准分子离子峰[M+H][sup]+[/sup]具有很好的响应,然后在分别进行子离子全扫描,各得到两对丰度高、干扰小的子离子对进行MRM监测,最终确定的质谱条件见表1,相应的色谱质谱图见图1、图2。前处理过程优化:生物素属于水溶性维生素,用纯水作为提取试剂可以得到很好的提取效果。但实验过程中发现,用纯水将奶粉溶解后整个溶液呈乳白色,只通过离心方式很难去除其中大量的蛋白、脂肪等杂质,需要对提取液进行除蛋白操作。通过考察乙酸铅、三氯乙酸、乙腈等几种常用的沉淀蛋白方法,综合考虑在去除蛋白的同时要尽可能减少其它杂质的引入,因此本方法采用乙腈除蛋白的方式,比较了几种不同水/乙腈比例,最终选定水/乙腈(1:1体积比)达到最优的实验效果。对于脂肪的去除则选用了目前较流行的[color=black]Prime HLB固相萃取柱通过式方法,即提取液通过Prime HLB时脂肪等大分子保留在SPE小柱上,目标物不保留以达到去除脂肪等杂质的目的,[/color]综合以上因素本实验最终采用了1.4的前处理方法。[/size][align=center][size=16px][img]https://ng1.17img.cn/bbsfiles/images/2022/10/202210071506558084_124_1729077_3.jpg[/img][/size][/align][align=center][size=16px]图1 [color=black]生物素[/color]标准溶液(10 ng/mL)MRM色谱图[/size][/align][size=16px][/size][align=center][size=16px][img]https://ng1.17img.cn/bbsfiles/images/2022/10/202210071506561980_1283_1729077_3.jpg[/img][/size][/align][align=center][size=16px]图2 奶粉样品中[color=black]生物素[/color]MRM色谱图[/size][/align][size=16px][color=black]2.2 线性范围和定量限[/color][color=black]吸取不同体积的生物素标准储备液(1.3),用[/color]纯水[color=black]分别配置不同浓度的[/color]上机标准溶液,以各自定量离子的峰面积(或与内标峰面积比值)为Y对应质量浓度X([color=black]m[/color]g/L)做标准曲线,得到的线性方程和相关系数见表2;以10倍信噪比(S/N)计算得到生物素的定量下限,结果见表2。表2 生物素标准溶液的线性方程、相关系数和定量下限(LOQ)[/size][table][tr][td][align=center][size=16px]分析物[/size][/align][/td][td][align=center][size=16px]线性范围/(ng/mL)[/size][/align][/td][td][align=center][size=16px]线性方程[/size][/align][/td][td][align=center][size=16px]R[/size][/align][/td][td][align=center][size=16px]LOQ/(ug/100g)[/size][/align][/td][/tr][tr][td][align=center][size=16px]生物素[sub] [/sub][/size][/align][/td][td][align=center][size=16px]0.2~50[/size][/align][size=16px][/size][/td][td][align=center][size=16px]Y=3078.1X-106.32[/size][/align][size=16px][/size][/td][td][align=center][size=16px]0.9993[/size][/align][size=16px][/size][/td][td][align=center][size=16px]0.5[/size][/align][/td][/tr][/table][size=16px][color=black]2.3回收率和精密度[/color][color=black]生物素在奶粉中天然存在[/color],选取已知生物素含量的奶粉作为基质进行加标。具体添加水平为:[color=black]0.5,5,50[/color] ug/100g。[color=black]每个[/color]水平重复6次,[color=black]同时做该奶粉的本底实验。[/color]按照1.4前处理方法处理后上机检测,回收率计算结果(扣除空白后)见表3。结果表明,该方法生物素的平均回收率为87.2%~110%,相对标准偏差(RSD,n=6)为2.3%~5.2%,均满足实验要求。[/size][align=center][size=16px]表3 奶粉生物素的加标回收率和相对标准偏差(n=6)[/size][/align][table][tr][td][align=center][size=16px]分析物[/size][/align][/td][td][align=center][size=16px]添加水平(ug/100g)[/size][/align][/td][td][align=center][size=16px]回收率/%[/size][/align][/td][td][align=center][size=16px]相对标准偏差/%[/size][/align][/td][/tr][tr][td][align=center][size=16px]生物素[/size][/align][size=16px][sub] [/sub][/size][/td][td][align=center][size=16px]0.5[/size][/align][align=center][size=16px]5[/size][/align][align=center][size=16px]50[/size][/align][/td][td][align=center][size=16px]86.8[/size][/align][align=center][size=16px]93.2[/size][/align][align=center][size=16px]91.6[/size][/align][size=16px][/size][/td][td][align=center][size=16px]4.6[/size][/align][align=center][size=16px]3.3[/size][/align][align=center][size=16px]2.1[/size][/align][size=16px][/size][/td][/tr][/table][size=16px][color=black]2.4实际样品分析[/color][color=black]为进一步验证该方法的准确性,采用本方法和《[/color]GB 5009.259-2016[color=black]》微生物法同时对北京普天同创生物科技有限公司的奶粉质控样品BQC1051147452生物素含量进行检测,结果见表4[/color]。由表4可知,UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS法测定结果与国标方法的结果基本一致,无显著性差异,但前者所需时间更短,精密度更好。[/size][align=center][size=16px]表4 奶粉质控样品[color=black]BQC1051147452[/color]生物素的测定结果[/size][/align][table][tr][td][align=center][size=16px]检测方法[/size][/align][/td][td][align=center][size=16px]特性值区间(ug/100g)[/size][/align][/td][td][align=center][size=16px]测定平均值(n=6)[/size][/align][/td][td][align=center][size=16px]相对标准偏差/%(n=6)[/size][/align][/td][/tr][tr][td][size=16px]UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS法微生物法[sub] [/sub][/size][/td][td][align=center][size=16px]15.6~22.4[/size][/align][align=center][size=16px]15.6~22.4[/size][/align][size=16px][/size][/td][td][size=16px]18.718.1[/size][/td][td][align=center][size=16px]2.5[/size][/align][size=16px] 4.6[/size][/td][/tr][/table][size=16px]3 结语本文建立了超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法(UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS)测定奶粉中[color=black]生物素[/color]含量的分析方法。该方法具有较高的灵敏度、准确度和精密度,前处理步骤简单,分析速度快,特别适合大批量样品的检测。参考文献:[1] GB 5009.259-2016 食品安全国家标准 食品中生物素的测定.[2] 薛霞, 赵慧男, 魏莉莉, 等. 超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法测定蜂蜜中五种水溶性维生素的含量[J]. 食品与发酵工业. 2021,47(12) : 250-256.[3] 李佳兴, 周利, 金艳, 等. 超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法测定枸杞子中8种水溶性维生素[J]. 食品科技. 2018,43(11) : 336-341.[/size]
那儿有a β γ δ维生素E和三烯酚的标准买啊?E
在检测维生素E和维生素A时,遇到一个棘手的问题。标准品是膏状的,标示为不少于100mg/每瓶,为了配制标准工作液,是直接吸标准品称量配制,还是配制后标定,还是全部配制? 希望有这方面经验的老师,帮忙解答下。
分享标准,均自网络收集,上传者不保证资料完整性以及版权。下载仅供研究,请勿用于其他用途。研究完毕请及时删除,若有正版需求,请联系出版单位。GB 5413.19-2010 婴幼儿食品和乳品中游离生物素的测定
我国食品卫生标准的主要内容 我国《食品卫生法》明确规定:“食品应当无毒、无害,符合应有的营养要求。”不言而喻,“无毒、无害”,谓其食品的“食用安全要求”,“营养要求”则指食品的“营养质量要求”,所以,我国食品卫生标准的主要内容包括了这两方面的技术要求,而食品的其他质量要求不在食品卫生标准的范畴内。 1食用安全要求 (1)食品及其相关产品中有毒有害物质的限量要求,包括化学性、生物性、物理性的各种有毒有害物,如环境污染物、农药、兽药、真菌毒素、致病性微生物、放射性核素等; (2)食品腐败变质的控制要求,包括碳水化合物类、蛋白质类、脂肪类食品腐败变质的鉴别指标,如各类食品的感官要求以及酸度、挥发性盐基氮、酸价、过氧化值等; (3)食品生物性污染的监测指标,如菌落总数、大肠菌群等; (4)食品添加剂的使用要求; (5)食品以及食品添加剂生产经营过程的卫生要求。 2营养要求 (1)婴幼儿配方食品的营养素种类与含量要求; (2)各种营养强化剂的强化要求。
餐饮食品微生物将被“限含量” 昨天,记者从负责起草“餐饮业即食食品微生物限量指标”的单位之一北京市卫生监督所获悉,全国餐饮业将发布首个食品安全“国标”.该标准将分门别类列出在餐饮业加工、制作的冷食、热餐、自制调味品、自制饮品中容许的病菌等微生物含量。 市卫生监督所相关负责人称,该标准将覆盖餐馆、快餐店、小吃店、饮品店、甜品站,还包括食堂、中央厨房等集体就餐、送餐单位。 “这项标准的出台,有助于预防、控制食源性疾病。”该负责人举例说,比如日式餐馆中的三文鱼等生食水产品,过去没有明确允许含有多少致病细菌的标准。“国标”出台后,细菌含量多少将有强制性指标,餐馆必须保证“不超标”.另外,如果市民就餐后发生食物中毒、身体不适等情况,卫生部门可以依据这一标准、化验餐馆的饭菜,从而查明是否与饭馆饭菜不卫生有关及餐馆该负多大责任等,并按照相应的法规处理。希望能为其它城市做一个典范
急!朋友们!能否提供购买维生素标准品的联系方式.你们用的标准品是进口的呢?还是国产的,二者有没有大的区别!可直在站内给我发消息.也可加我的QQ271017409 谢谢了.
哪位老师能告诉我维生素E标准品的价格,生产厂家,包装规格,谢谢
哪里可以买到符合USP标准的维生素C对照品?有USP证书的。
维生素B1是维生素中发现最早的一种。由嘧啶环和噻唑环通过亚甲基结合而成的一种B族维生素。为白色结晶或结晶性粉末;有微弱的特臭,味苦,有引湿性,露置在空气中,易吸收水分。在碱性溶液中容易分解变质。酸碱度在3.5时可耐100℃高温,酸碱大于5时易失效。遇光和热效价下降。故应置于遮光,凉处保存,不宜久贮。 在酸性溶液中很稳定,在碱性溶液中不稳定,易被氧化和受热破坏。还原性物质亚硫酸盐、二氧化硫等能使维生素B1失活。(摘自百度百科) 购买回的维生素B1(盐酸硫胺)纯度标准物质(BW3600,中国计量科学研究所)给出的均匀性检验和稳定性考察的前处理条件是105℃干燥至恒重后称取一定量,加入盐酸水溶液溶解,过滤上机测定。而在GB/T 14700-2002《饲料中维生素B1的测定》标准(本法用的反相HPLC)中,标准储备液是称取一定量,用25%乙醇溶液超声溶解。在GB/T5009.84-2003《食品中硫胺素(维生素B1)的测定》标准中,称取经氯化钙干燥24h的一定量硫胺素,溶于0.01mol/L中。在中国兽药典、中国药典中,维生素B1用的是约0.1mol/L盐酸溶液溶解,而其中检验干燥失重时,用的也是105℃。 疑问:根据第一段说法,VB1并不耐热,为何要用105℃? GB/T 14700-2002中用乙醇溶液溶解,储备液能保证稳定,不选用盐酸溶液,是否更便于HPLC测试?
要做维生素A,文献说要甲醇溶解标准品,可惜根本不容,谁做过,帮忙下,怎么溶解。用液相做
最近做食品中维生素B1的检测,依据GB5009.84-2016,高效液相,按要求配制的一系列浓度的标准液,竟然会有过载的现象,各个浓度峰面积也大概高了一倍,不知道是怎么回事,请有经验的专家帮忙解答就下3.3 标准品维生素B1 标准品:盐酸硫胺素(C12H17ClN4OSHCl)),CAS:67-03-8,纯度≥99.0%。3.4 标准溶液配制3.4.1 维生素B1 标准储备液(500μg/mL):准确称取经五氧化二磷或者氯化钙干燥24h的盐酸硫胺素标准品56.1mg(精确至0.1mg),相当于50mg硫胺素、用0.01mol/L盐酸溶液溶解并定容至100mL,摇匀。置于0℃~4℃冰箱中,保存期为3个月。3.4.2 维生素B1 标准中间液(10.0μg/mL):准确移取2.00 mL 标准储备液,用水稀释并定容至100mL,摇匀。临用前配制。3.4.3 维生素B1 标准系列工作液:吸取维生素B1 标准中间液0μL、50.0μL、100μL、200μL、400μL,800μL,1000μL,用水定容至10mL,标准系列工作液中维生素B1 的浓度分别为0μg/mL,0.0500μg/mL,0.100μg/mL,0.200μg/mL,0.400μg/mL,0.800μg/mL,1.00μg/mL。临用时配制。
[b][font=宋体]一、引言[/font][/b][font=宋体] [/font][font=宋体]在生物学和医学的研究中,抗体标记技术已成为一种重要的研究手段。其中,生物素标记抗体凭借其独特的优势,在许多领域中得到了广泛应用。本文将详细介绍生物素标记抗体的原理、应用及发展前景。[/font][font=宋体] [/font][b][font=宋体]二、生物素标记抗体的原理[/font][/b][font=宋体] [/font][font=宋体][font=宋体]生物素,又称维生素[/font][font=Calibri]H[/font][font=宋体],是一种存在于自然界中的小分子有机物质。它可以通过化学反应与抗体结合,生成生物素标记抗体。这一过程通常是在抗体的氨基基团上连接一个生物素衍生物,形成共价键。这种连接方式不会改变抗体的免疫活性,同时使得生物素标记抗体能够与相应的抗原结合。[/font][/font][b][font=宋体] [/font][font=宋体]三、生物素标记抗体的应用[/font][/b][font=宋体] [/font][font=宋体]免疫分析:生物素标记抗体在免疫分析中发挥了重要作用。通过将生物素标记抗体与相应的抗原结合,可以实现对抗原的灵敏检测。这种方法被广泛应用于生物学、医学及食品安全等领域。[/font][font=宋体]蛋白质组学研究:在蛋白质组学研究中,生物素标记抗体可用于蛋白质的分离和纯化。通过生物素标记抗体与抗原的特异性结合,可以从复杂的蛋白质混合物中分离出目标蛋白质。[/font][font=宋体]细胞生物学研究:生物素标记抗体在细胞生物学研究中具有广泛的应用价值。例如,通过生物素标记抗体追踪细胞内蛋白质的分布和动态变化,有助于深入了解细胞的生命活动。[/font][font=宋体]疾病诊断与治疗:生物素标记抗体在疾病诊断和治疗中也发挥了重要作用。例如,针对癌症的免疫治疗中,生物素标记抗体可以用于识别和攻击癌细胞,从而达到治疗目的。[/font][font=宋体] [/font][b][font=宋体]四、发展前景[/font][/b][font=宋体] [/font][font=宋体]随着生物学和医学技术的不断进步,生物素标记抗体的应用前景日益广阔。未来,随着技术的不断创新和完善,生物素标记抗体的性能将得到进一步提升,从而推动其在更多领域中的应用。同时,随着人类对生命现象认识的深入,将有更多具有挑战性的研究课题需要借助生物素标记抗体这一强大工具。[/font][b][font=宋体] [/font][font=宋体]五、结语[/font][/b][font=宋体] [/font][font=宋体]生物素标记抗体作为一种重要的研究手段,在生物学、医学及其他相关领域中发挥着不可或缺的作用。随着技术的不断进步和应用领域的拓展,我们有理由相信,生物素标记抗体的未来将更加光明,为人类探索生命奥秘提供更多可能性。[/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/category/biotinylated-protein-elite][b]生物素标记蛋白[/b][/url]相关产品,详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/category/biotinylated-protein-elite[/font][/font][b][font=宋体] [/font][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
[align=center][font=DengXian]维生素在食品加工与贮藏过程中的变化[/font]--[font=DengXian]食品加工过程的影响[/font]4[/align][font=DengXian]([/font]5[font=DengXian])贮藏过程[/font][font=DengXian]食品在贮藏期间,维生素的损失与贮藏温度关系密切。罐头食品冷藏保存一年后,维生素[/font]B1[font=DengXian]的损失低于室温保存。包装材料对贮存食品维生素的含量有一定的影响。例如透明包装的乳制品在贮藏期间会发生维生素[/font]B2[font=DengXian]和维生素[/font]D[font=DengXian]的损失。[/font][font=DengXian]食品中脂类的氧化作用产生的氢过氧化物、过氧化物和环过氧化物会引起胡萝卜素、维生素[/font]E[font=DengXian]和维生素[/font]C[font=DengXian]等的氧化,也能破坏叶酸、生物素、维生素[/font]B12[font=DengXian]和维生素[/font]D[font=DengXian]等;过氧化物与活化的羰基反应导致维生素[/font]B1[font=DengXian]、[/font]B6[font=DengXian]和泛酸等的破坏;碳水化合物非酶褐变产生的高度活化的羰基对维生素同样有破坏作用。[/font]
微生物学检验方法国家标准的演变, 建国五十年来,我国食品卫生微生物学检验方法的发展经历了三个阶段。 ——方法逐步建立、统一阶段(1949~1976年) ——方法标准化形成阶段(1977~1984年) ——不断修订和完善阶段(1985年至今) 上海市疾病预防控制中心 国家标准检验方法的演变 GB 4789-94主要修订内容:菌落总数的培养时间由24小时改为48小时;对小肠结肠炎耶尔森氏菌、空肠弯 曲菌、副溶血性弧菌进行了补充和改进;增加了单核细胞增生李斯特氏菌、椰毒假单胞菌酵米面亚种、罐头食品商业无菌、金黄色葡萄球菌肠毒素检验方法, 沙门氏菌、志贺氏菌和致泻大肠埃希氏菌的肠杆菌科噬菌体检验方法。新修订后的GB 4789-94共31项,其检验项目、方法水平与FDA 1992年出版的微生物分析方法手册相近,但未列入嗜水气单胞菌和霍乱弧菌的检验。
[color=#444444]有高手做婴幼儿食品中维生素B[/color][sub][color=#444444]12[/color][/sub][color=#444444]的检测吗? 国标流程,检测用培养基,用的陆桥的,是否本地高啊,得用BD的;菌活化3代,效果不错,长的很好。接种后培养22 h后,无梯度出现。求助ing (还得做生物素和叶酸的测定)[/color]