请问各位,草酸玻璃微珠采样管能否直接把里面的玻璃微珠转移到顶空瓶中,然后加入饱和氢氧化钠,压盖上顶空呢?这种方式能否实验成功?【标准是往管里同时通氢氧化钾和氮气,用真空收集瓶收集游离三甲胺】[img]https://ng1.17img.cn/bbsfiles/images/2022/04/202204230059197210_4127_3513633_3.png[/img]
求草酸钴产品标准
请问草酸亚铁的国家标准或行业标准那里有?
请问磷酸二氢铵、草酸亚铁的国家标准在那里可以找到?
摘要:建立胡黄连中香草酸和桂皮酸的含量测定方法。方法用双波长扫描法测定胡黄连中香草酸和桂皮酸的含量。结果香草酸。桂皮酸斑点峰面积3Il内稳定,香草酸回收率为103.86%,RSD=1.33%,桂皮酸回收率为103.16%,RSD=1.28%。结论该方法稳定,可行。具有实用性。 关键词:胡黄连 薄层扫描法 香草酸 桂皮酸 胡黄连具有保肝利胆、抗炎、抗真菌等药理作用。胡黄连含胡黄连素、胡黄连苷(I II III)、D-甘露醇、香草酸、肉桂酸、胡黄连醇成分。香草酸和桂皮酸是其中的两种抗菌成分。我们对胡黄连中香草酸、桂皮酸含量建立了薄层扫描法,以达到控制胡黄连的质量,从而为临床疗效提供保证。 1 仪器与试剂 药材:胡黄连,太原市药材公司;仪器:日本岛津CS--9301PC薄层扫描仪;手提式荧光灯(上海固村电光仪器厂);对照品:香草酸对照品(中国药品生物制品检定所);桂皮酸对照品溶液(省药检所提供e=0.604mg/50ml);硅胶GF254(青岛海洋化工厂)所用试剂均为分析纯。 2 实验条件 2.l 薄层层析条件:分别以石油醚-氯仿-丙酮-冰醋酸(10:4.4:10.1);正己烷-乙醚-冰醋酸(5:5:0.1);正己烷-氯仿-乙醚-冰醋酸(5:3:2:0.1)以及氯仿:甲醇(2:1)展开,多次比较发现正己烷。氯仿-乙醚-冰醋酸(5:3:2:0.4)分离效果好。 2.2 测定波长及主要扫描参数,分别对香草酸,桂皮酸对照品斑点在200nm-370nm扫描,在290nm处有最大吸收,350nm处无吸收,固定350nm为参比波长,290nm为测定波长。
高锰酸钾标准溶液用草酸标定的问题?为何滴定时一滴颜色就出现红色,而且几分钟都不褪色,加热才能退去,但是按照国标601上做的。国标上说到终点时才能加热的?说明一下每一步都是按照国标进行的。
哪位好心人有炔草酸在小麦中的检测方法?我在这里多谢了!!!
GB/T601-2002草酸标准滴定溶液的不确定度评定,实验中用到高锰酸钾标准溶液----------关于高锰酸钾标准溶液不确定度的是怎样来进行分析的,因为高锰酸钾标准溶液也是配制的(非购买的标准物质),难道由此前配制高锰酸钾标准溶液得出的不确定度直接代入吗?

在一次失效分析的过程中,发现别的实验室在分析我们自己的日常样品中,有比较明显的草酸的结果显示,但是自己内部的测试结果没有很好地显示出来。因为之前没有需要报告草酸这个项目,所以也没有买过草酸的标准溶液。为了研究内部是否可以测试草酸,需要另外购买草酸的标准液(Fig-1)。[align=center] [img=,435,422]https://ng1.17img.cn/bbsfiles/images/2023/09/202309011031011657_3849_2942222_3.jpg!w435x422.jpg[/img][/align] 等草酸标液到了之后,开始配置不同浓度的标液,从低到高开始尝试进样,但是都没有在谱图上发现明显的出峰。到了150ppm仍然没有检测到很明显的峰,这是比较不正常的。在观察谱图时,发现在22分钟左右有一个翘起来的部分,有点像峰(Fig-2)。但是因为之前的程序设定了运行时间都是22分钟,是不是因为运行时间太短,导致草酸的峰还没有出来呢。[align=center] [img=,690,357]https://ng1.17img.cn/bbsfiles/images/2023/09/202309011031471109_959_2942222_3.jpg!w690x357.jpg[/img][/align] 经过更改程序文件,把出峰时间改到26分钟,在22-23分钟左右看到一个非常明显的草酸出峰(Fig-3),果然是之前的运行时间太短了,导致草酸不能够显示出来。[align=center][img=,690,213]https://ng1.17img.cn/bbsfiles/images/2023/09/202309011032034570_2099_2942222_3.jpg!w690x213.jpg[/img][/align] 为了进一步,进行了草酸的标准曲线验证。在新程序条件运行下,草酸在不同浓度都可以显示出来,可以得到一个非常好标准曲线,R2的值达到0.99以上(Fig-4)。[align=center][img=,690,468]https://ng1.17img.cn/bbsfiles/images/2023/09/202309011032193998_3826_2942222_3.jpg!w690x468.jpg[/img][/align][align=center]另外,有继续进行了草酸的回收率实验。把草酸标准溶液加入到正常的7个阴离子溶液中,草酸能够明显检测出来(Fig-5),回收率大概是107%。[/align][align=center][img=,690,328]https://ng1.17img.cn/bbsfiles/images/2023/09/202309011032369340_1786_2942222_3.jpg!w690x328.jpg[/img][/align] [font=等线]在新程序下运行,发现在日常的产品中也可以明显检测出草酸(Fig-6)。这证明了的确是之前的运行时间太短,导致草酸检测不出来.[/font][align=center][img=,690,502]https://ng1.17img.cn/bbsfiles/images/2023/09/202309011032564960_9557_2942222_3.jpg!w690x502.jpg[/img][/align] 经过这次的草酸寻峰计,还得出了一个教训。在以后研究新的物质时,要提前好好查下相关的文献,因为不同的柱子和淋洗方法都会影响到物质的出峰。如果没有资料可查,需要尝试在尽可能的运行时间去检测,以免有峰遗漏。
草酸钠标准溶液中加入硫酸得目的是什么
哪位好心人有炔草酸在小麦中的检测方法?我在这里多谢了!!!我的联系方式ab402@163.com
请问专家:哪里可以买到沙蚕毒素(沙参毒素草酸盐)标准品?谢谢。
草酸钠标准溶液中加入硫酸得目的是什么?
今天有个同事突然问我什么是游离酸,其实我也不知道具体详细的概念,所以在这里求助下各位老师。 他分析的是铜湿法冶金侵出液游戏酸的测定 ,以甲基橙为指示剂,用氢氧化钠标准液滴定游离酸的含量。
最近做小儿七星茶颗粒甘草酸的测定时遇到了很奇怪的问题:对照品有峰,样品却只出杂质峰,开始怀疑是样品没有含量,可是拿以前做过的有含量的样品再做,却没峰了;后来吸一半对照品一半样品进样就出峰了,可是加对照品到样品中一起按标准处理后就又没有峰出来,怎么想都不明白问题出在哪里。所用的试剂换了好几次,也换人配了,结果还是一样没有,会不会是超声引起的呢,因为我们的超声机的功率只有80瓦,不过以前也做得出啊,大家帮帮忙,下面是标准【含量测定】 照高效液相色谱法(中国药典2005年版一部附录VI D)测定。 色谱条件与系统适用性试验 以十八烷基硅烷键合硅胶为填充剂;以甲醇-0.2mol/L醋酸铵溶液—冰醋酸(65:35:1)为流动相;检测波长为250nm。理论板数按甘草酸峰计算应不低于2000。 对照品溶液的制备 取甘草酸铵对照品适量,精密称定,加流动相制成每1ml含16μg的溶液,即得(折合甘草酸为15.672μg)。 供试品溶液的制备 取装量差异项下的本品内容物,混匀,研细,取约7g,精密称定,置50ml量瓶中,加流动相约45ml,超声处理(功率300W,频率40kHz)30分钟,放冷,加流动相至刻度,摇匀,滤过,取续滤液,即得。 测定法 精密吸取对照品溶液与供试品溶液各20μl,注入液相色谱仪,测定,即得。
[align=center][b][size=4][font=宋体]用电位滴定法对食醋中游离矿酸进行准确定量[/font][/size][size=4][/size][/b][/align][align=center][b][size=4][font=Times New Roman] [/font][/size][/b][/align][align=center][b][size=4][font=Times New Roman] [/font][/size][/b][/align][size=3][font=宋体]摘要:国标[/font][font=Times New Roman]GB/T5009.41-2003[/font][font=宋体]对食醋中游离矿酸的检测是采用百里草酚蓝试纸和甲基紫试纸检测。用指示剂法对食醋中游离矿酸的检测会存在着出现假阳性即误判的现象,尤其是当食醋中颜色呈琥珀色等深颜色用甲基紫试纸和白醋用百里草酚蓝试纸检测时均会有不同程度的干扰。因此,有必要对其定性的方法进行改进,本文采用电位滴定法对食醋中游离矿酸进行准确定量,并比较了两种方法对食醋的检测结果。[/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=宋体]关键词:食醋游离矿酸[/font][font=Times New Roman] [/font][font=宋体]假阳性[/font][font=Times New Roman] [/font][font=宋体]电位滴定法[/font][font=Times New Roman] [/font][font=宋体]准确定量[/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=宋体]前言;食醋中游离矿酸的测定[/font][font=Times New Roman],[/font][font=宋体]依[/font][font=Times New Roman]GB/T5009.31-2003[/font][font=宋体]采用百里草酚蓝试纸和甲基紫试纸进行定性检测。用此法不易对食醋中游离矿酸进行准确的检测。本文介绍了用电位滴定法对食醋中游离矿酸进行准确定量的原理及方法。该法简单可行,可与食醋中的总酸同时进行测定。[/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=宋体]一、电位滴定法测游离矿酸[/font][/size][font=Times New Roman][size=3]1.[/size] [/font][size=3][font=宋体]定义:游离矿酸:指硫酸,硝酸,盐酸等无机酸。[/font][/size][font=Times New Roman][size=3]2.[/size] [/font][size=3][font=宋体]原理:[/font][/size][font=Times New Roman][size=3]1)[/size] [/font][font=宋体][size=3]醋酸中存在游离矿酸时电离度的差异,滴定前:[/size][/font][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][font=宋体][size=3]故电离度[/size][/font][size=3][font=Times New Roman] [/font][/size][font=Times New Roman][size=3]2)[/size] [/font][size=3][font=宋体]滴定前溶液酸度计所指示的[/font][font=Times New Roman]pH[/font][sub][font=宋体]初[/font][/sub][font=宋体]为[/font][font=Times New Roman][H[/font][sub][font=宋体]总[/font][/sub][font=Times New Roman][sup]+[/sup]][/font][font=宋体]的负对数[/font][font=Times New Roman],[/font][font=宋体]即[/font][/size][font=Times New Roman][size=3] [/size][/font][size=3][font=宋体]。[/font][/size][font=宋体][size=3]故:[/size][/font][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]3[/font][font=宋体])滴定至终点[/font][font=Times New Roman]pH =8.2[/font][font=宋体]时根据等物质量反应原则得[/font][font=Times New Roman]:[/font][/size][size=3][font=Times New Roman][/font][/size][font=宋体][size=3]即[/size][/font][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]4[/font][font=宋体])结合[/font][font=Times New Roman]1), 2), 3)[/font][font=宋体]中的计算式可计算出[/font][font=Times New Roman][H[/font][sub][font=宋体]矿[/font][/sub][font=Times New Roman][sup]+[/sup]],[/font][font=宋体]即游离矿酸浓度[/font][font=Times New Roman]([/font][font=宋体]以氢离子浓度计[/font][font=Times New Roman])[/font][/size][font=Times New Roman][size=3]3.[/size] [/font][size=3][font=宋体]试验[/font][/size][font=Times New Roman][size=3]1)[/size] [/font][size=3][font=宋体]仪器[/font][font=Times New Roman]:[/font][/size][size=3][font=Times New Roman]pHS-3C[/font][font=宋体]型酸度计[/font][font=Times New Roman] [/font][font=宋体]磁力搅拌器[/font][/size][font=Times New Roman][size=3]2)[/size] [/font][size=3][font=宋体]试剂:[/font][/size][font=宋体][size=3]①pH=4.00标准缓冲液;[/size][/font][font=宋体][size=3]②pH=6.86标准缓冲液;[/size][/font][size=3][font=宋体]③0.1mol/L的氢氧化钠标准溶液;[/font][/size][font=Times New Roman][size=3]3)[/size] [/font][size=3][font=宋体]试验方法:[/font][/size][size=3][font=Times New Roman]pHS-3C[/font][font=宋体]型酸度计用[/font][font=Times New Roman]pH[/font][font=宋体]=[/font][font=Times New Roman]6.86[/font][font=宋体]和[/font][font=Times New Roman]pH[/font][font=宋体]=[/font][font=Times New Roman]4.00[/font][font=宋体]的标准缓冲液校正正常待用。吸取[/font][font=Times New Roman]10.0mL[/font][font=宋体]样品于[/font][font=Times New Roman]100mL[/font][font=宋体]容量瓶中,加蒸馏水至刻度,混匀。吸取[/font][font=Times New Roman]20.0mL[/font][font=宋体],置于[/font][font=Times New Roman]200mL[/font][font=宋体]烧杯中,加[/font][font=Times New Roman]60.0mL[/font][font=宋体]蒸馏水,开动磁力搅拌器,读取被测溶液的[/font][font=Times New Roman]pH[/font][font=宋体]初;然后,用氢氧化钠标准溶液滴定至[/font][font=Times New Roman]pH[/font][font=宋体]=[/font][font=Times New Roman]8.2[/font][font=宋体];记录消耗氢氧化钠标准溶液的滴定数[/font][font=Times New Roman]V[sub]NaOH[/sub][/font][font=宋体]。[/font][/size][font=Times New Roman][size=3]4.[/size] [/font][size=3][font=宋体]计算公式:[/font][/size][align=center][size=3][/size][/align][font=宋体][size=3]式中:[/size][/font][size=3][/size][size=3][/size][size=3][/size][size=3][/size][size=3][/size][size=3][/size][size=3][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]二、[/font][font=宋体]方法讨论:[/font][/size][size=3][font=宋体]当用百里草酚蓝试纸和甲基紫试纸检测食醋中的游离矿酸时,若试纸呈现出阳性,为了防止出现假阳性,还须对样品进行定量试验,才可判定是否有游离矿酸。本文选取几个典型的样品用国标[/font][font=Times New Roman]GB/T5009.31-2003[/font][font=宋体]:百里草酚蓝试纸和甲基紫试纸法与用本文电位滴定法检测数值比较见下表:[/font][/size][align=center][size=3][font=宋体]表:国标[/font][font=Times New Roman]GB/T5009.31-2003[/font][font=宋体]法与电位滴定法比较[/font][/size][/align][table=623][tr][td=1,1,79][size=3][font=宋体]食醋样品[/font][/size][/td][td=1,1,264][size=3][font=宋体]国标[/font][font=Times New Roman]GB/T5009.31[/font][font=宋体]检测结果[/font][/size][/td][td=1,1,160][size=3][font=宋体]电位滴定法检测数值[/font][/size][/td][td=1,1,120][size=3][font=宋体]样品真实情况[/font][/size][/td][/tr][tr][td=1,1,79][size=3][font=Times New Roman]**[/font][font=宋体]白醋[/font][/size][/td][td=1,1,264][size=3][font=宋体]用百里草酚蓝试纸呈现出假阳性:即其黄色变为浅红色[/font][/size][/td][td=1,1,160][size=3][font=宋体]<[/font][font=Times New Roman]0[/font][font=宋体](即未检出)[/font][/size][/td][td=1,1,120][size=3][font=宋体]未检出[/font][/size][/td][/tr][tr][td=1,1,79][size=3][font=Times New Roman]**[/font][font=宋体]白醋[/font][/size][/td][td=1,1,264][size=3][font=宋体]用百里草酚蓝试纸呈现出假阳性:即其黄色变为浅红色[/font][/size][/td][td=1,1,160][size=3][font=宋体]<[/font][font=Times New Roman]0[/font][font=宋体](即未检出)[/font][/size][/td][td=1,1,120][size=3][font=宋体]未检出[/font][/size][/td][/tr][tr][td=1,1,79][size=3][font=Times New Roman]**[/font][font=宋体]白醋[/font][/size][/td][td=1,1,264][size=3][font=宋体]用百里草酚蓝试纸呈现出浅红色[/font][/size][/td][td=1,1,160][size=3][font=Times New Roman]5mg/L[/font][/size][/td][td=1,1,120][size=3][font=宋体]有检出游离矿酸[/font][/size][/td][/tr][tr][td=1,1,79][size=3][font=Times New Roman]**[/font][font=宋体]陈醋[/font][/size][/td][td=1,1,264][size=3][font=宋体]用甲基紫试纸不易观察试纸颜色变化[/font][/size][/td][td=1,1,160][size=3][font=宋体]<[/font][font=Times New Roman]0[/font][font=宋体](即未检出)[/font][/size][/td][td=1,1,120][size=3][font=宋体]未检出[/font][/size][/td][/tr][tr][td=1,1,79][size=3][font=Times New Roman]**[/font][font=宋体]陈醋[/font][/size][/td][td=1,1,264][size=3][font=宋体]用甲基紫试纸不易观察试纸颜色变化[/font][/size][/td][td=1,1,160][size=3][font=Times New Roman]3 mg/L[/font][/size][/td][td=1,1,120][size=3][font=宋体]有检出游离矿酸[/font][/size][/td][/tr][/table][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][align=center][size=3][font=宋体]参考文献:[/font][/size][/align][size=3][font=宋体][1]GB/T5009.31-2003,[/font][font=宋体]《食品卫生检验方法 理化部分(一)》[S] [/font][/size][size=3][font=宋体][2][/font][font=宋体]食品理化检验方法指南, 叶世柏主编[M],北京大学出版社,2000,147-148 [/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size]
本人最近在做职业卫生草酸的方法验证,参考的标准是GBZ/T 300.114-2017,这个标准采用的色谱柱是阳[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱和邻苯二甲酸流动相,我们平时做环境中的草酸都是阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱,碳酸钠和碳酸氢钠流动相。大家做职业卫生的草酸的时候具体是怎么操作的?严格按照标准用阳[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱做?还是用阴离子做,再写一份方法偏离?先谢谢大家了!
[color=#3333ff]请问:[/color][color=#3333ff]日本药典标准里面的 醋酸羟丙甲纤维素琥珀酸酯 的质量标准中,(如下为标准的译文)[/color](2)游离醋酸以及游离琥珀酸 精密称量本品约0.1g,准确加入pH7.5的0.02mol/L磷酸盐缓冲液4mL,盖紧瓶盖,搅拌2小时。准确添加稀释后的磷酸(1→500)4mL,数次倒置振摇混合。对该溶液进行离心分离,取上清液作为供试溶液。另将20mL水放入100mL的量瓶中,精密称量其质量,加入2.0mL醋酸(100),精密称量其质量,计算出醋酸(100)的质量,再加入水,使其达到100mL。准确称量6mL该溶液,加水使其达到100mL,制成醋酸原液。接下来,精密称量大约0.13g的琥珀酸,溶解于水中,使之达到100mL,作为琥珀酸原液。准确称量4mL醋酸原液以及4mL琥珀酸原液,添加流动相,使之达到25mL,作为标准溶液。准确量取供试溶液以及标准溶液各10μL,在下述条件下根据液相色谱法进行试验,测定各个液体的醋酸以及琥珀酸的峰面积A[sub]TA[/sub]、A[sub]TS[/sub]以及A[sub]SA[/sub]、A[sub]SS[/sub],根据以下公式求出游离醋酸和游离琥珀酸的量,其总量不得超过1.0%。游离醋酸(C[sub]2[/sub]H[sub]4[/sub]O[sub]2[/sub])的量(%) =M[sub]SA[/sub]/M[sub]T [/sub]× A[sub]TA[/sub]/A[sub]SA [/sub]× 48/625游离琥珀酸(C[sub]4[/sub]H[sub]6[/sub]O[sub]4[/sub])的量(%) =M[sub]SS[/sub]/M[sub]T[/sub] × A[sub]TS[/sub]/A[sub]SS[/sub] ×32/25M[sub]SA[/sub]:醋酸(100)的称取量(mg)M[sub]SS[/sub]:琥珀酸的称取量(mg)M[sub]T[/sub]:换算成干燥品之后的本品的称取量(mg)[color=#3333ff]计算公式中的48/625和32/25是怎么得来的啊?[/color][color=#3333ff]请各位帮忙讨论一下,不甚感激。[/color]

[align=center][b][font=宋体]虫草浓缩液中虫草酸和虫草素测定方法[/font][/b][/align][size=18px][font=宋体]虫草浓缩液由虫草水提物制得,用于化妆品原料。客户想测虫草浓缩液中虫草酸和虫草素,虫草酸又名甘露醇。[/font][font='Times New Roman','serif']1 [/font][font=宋体]试剂:乙腈(色谱级),超纯水,甲醇(分析纯),虫草酸和虫草素均购置北京索莱宝公司。[/font][font='Times New Roman','serif']2 [/font][font=宋体]标准品配制:称取一定量的虫草酸,用纯水溶解,定容,得到浓度为[/font][font='Times New Roman','serif']150 μg/mL[/font][font=宋体],待测;[/font][font=宋体]虫草素,用甲醇溶解,定容,得到浓度为[/font][font='Times New Roman','serif']220 μg/mL[/font][font=宋体],待测;[/font][font='Times New Roman','serif']3 [/font][font=宋体]样品制备:[/font][font='Times New Roman','serif']3.1 [/font][font=宋体]精密量取[/font][font='Times New Roman','serif']0.5 mL[/font][font=宋体]虫草浓缩液,分别用水定容至[/font][font='Times New Roman','serif']10 mL[/font][font=宋体]测定虫草酸,用甲醇定容至[/font][font='Times New Roman','serif']10 mL[/font][font=宋体]测定虫草素,过[/font][font='Times New Roman','serif']0.45 μm[/font][font=宋体]滤膜,待测。[/font][font='Times New Roman','serif']4 [/font][font=宋体]虫草素[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]条件:[/font][font='Times New Roman','serif']LC-20AT[/font][font=宋体]配制紫外检测器,[/font][font=宋体]波长:[/font][font='Times New Roman','serif']260 nm [/font][font=宋体];进样量:[/font][font='Times New Roman','serif']5μL[/font][font=宋体];色谱柱型号:[/font][font='Times New Roman','serif']Agilent Zorbax SB-C18(4.6 mm×250mm, 5 μm)[/font][font=宋体];柱温:[/font][font='Times New Roman','serif']30.0 [/font][font=宋体]℃;流速:[/font][font='Times New Roman','serif']0.8 mL/min[/font][font=宋体];流动相条件如表[/font][font='Times New Roman','serif']1[/font][font=宋体]:[/font][/size][align=center][img=,551,185]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311641477076_4077_1858223_3.jpg!w551x185.jpg[/img][/align][font='Times New Roman','serif'] [/font][size=18px][font=宋体]虫草酸[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]条件:[/font][font='Times New Roman','serif']Angilent infinit1260[/font][font=宋体]配制示差检测器,进样量:[/font][font='Times New Roman','serif']5[/font][font=宋体]μ[/font][font='Times New Roman','serif']L[/font][font=宋体];色谱柱型号:[/font][font='Times New Roman','serif']Agilent Zorbax SB-C18(4.6 mm[/font][font=宋体]×[/font][font='Times New Roman','serif']250 mm, 5 μm)[/font][font=宋体];[/font][font=宋体]柱温:[/font][font='Times New Roman','serif']30.0 [/font][font=宋体]℃,;流动相条件乙腈:纯水[/font][font='Times New Roman','serif']=80:20[/font][font=宋体];流速:[/font][font='Times New Roman','serif']0.5mL/min[/font][font=宋体]。[/font][/size][align=center][img=,690,265]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311642440362_8441_1858223_3.jpg!w690x265.jpg[/img][/align][align=center][b][font=宋体]虫草素标准品色谱图[/font][/b][/align][align=center][img=,683,269]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311642555977_2623_1858223_3.jpg!w683x269.jpg[/img][/align][align=center][b][font=宋体]虫草浓缩液中虫草素色谱图[/font][/b][/align][b][font=宋体]结果:虫草浓缩液中虫草酸含量([/font]7.65 mg/mL [font=宋体]),虫草素含量([/font]2.65[/b][font='Times New Roman','serif']μg/mL[/font][b][font=宋体])。[/font][font=宋体]小结:测定虫草素的过程中发现流动相梯度洗脱,回到起始梯度是需要平衡时间久一些,虫草素含量较低,虫草酸含量比较高。示差检测器也是进样前需要稳定[/font]2[font=宋体]小时左右,才能保证实验数据稳定性。[/font] [/b]
加权最小二乘法建立豆制品中游离甲醛含量分析标准曲线的研究摘要化学分析工作中,两个变量之间的关系普通采用最小二乘法建立标准曲线,如果分析测定的变量范围宽,在低浓度区域则分析结果的相对误差较大,本文主要讨论了以加权最小二乘法建立标准曲线的优越性,并以DB35/T638-2005乙酰丙酮法测豆制品中游离甲醛为应用实例,介绍了加权最小二乘法的原理、计算公式、权重因子在提高低浓度测定相对误差的作用。关键词 加权最小乘法;标准曲线;权重因子;游离甲醛Weighted Least SquaresMethod to Establish Formaldehyde Content in Bean Products Analysis of Standard CurveZheng Jin-wen (Nanping Product Quality Inspection Institute, Fujian Nanping, 353000)AbstractIn chemical analysis, therelationship between the two variables, ordinary least squares method isadopted to establish the standard curve, if the analysis determination ofvariable scope wide, in low concentration region are the results of theanalysis of relative error is larger, this paper mainly discusses with theweighted least squares method to establish the superiority of the standardcurve, and acetyl acetone method DB35/T638 free formaldehyde in bean productsas an example, this paper introduces the principle of weighted least squaresmethod, calculation formula and weighting factor in low concentration bymeasuring relative error of the function. Keywords weighted least square; Standard curve;Weighting factor; Free formaldehyde 1 前言在豆制品制品的分析工作中,对其游离甲醛的含量进行定量分析一般是采用标准曲线法进行数据处理,通过对系列浓度的甲醛标准溶液依DB35/T638-2005 进行吸光度的测定,得到吸光度(Xi)与浓度(Yi)的对应数据,再运用最小二乘法进行回归运算,得到线性回归标准曲线方程。然而,在实际工作中,由于豆制品制品中游离甲醛含量变化大,需检测的浓度范围宽,若使用最小二乘法建立的回归标准曲线,会导致低浓度所得结果的相对误差较大。为解决这一问题,本文以豆制品制品中游离甲醛分析方法为例,讨论了加权最小二乘法在建立标准曲线(线性方程)中的应用。2 实验所得的相关原始数据依DB35/T638标准对系列已知浓度的游离甲醛浓度进行吸光度的测定,所得的相关数据见表1。

[align=left][size=4][font=宋体][color=#f10b00]维权声明:本文为abcdefghijkl123原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现的,均属侵权违法行为,我们将追究法律责任.[/color][b] 用电位滴定法对食醋中游离矿酸进行准确定量[/b][/font][/size][size=4][/size][/align][align=center][b][size=4][font=Times New Roman][/font][/size][/b][/align][align=center][b][size=4][font=Times New Roman][/font][/size][/b][/align][size=3][font=宋体]摘要:国标[/font][font=Times New Roman]GB/T5009.41-2003[/font][font=宋体]对食醋中游离矿酸的检测是采用百里草酚蓝试纸和甲基紫试纸检测。用指示剂法对食醋中游离矿酸的检测会存在着出现假阳性即误判的现象,尤其是当食醋中颜色呈琥珀色等深颜色用甲基紫试纸和白醋用百里草酚蓝试纸检测时均会有不同程度的干扰。因此,有必要对其定性的方法进行改进,本文采用电位滴定法对食醋中游离矿酸进行准确定量,并比较了两种方法对食醋的检测结果。[/font][/size][size=3][font=Times New Roman][/font][/size][size=3][font=宋体]关键词:食醋游离矿酸[/font][font=Times New Roman] [/font][font=宋体]假阳性[/font][font=Times New Roman] [/font][font=宋体]电位滴定法[/font][font=Times New Roman] [/font][font=宋体]准确定量[/font][/size][size=3][font=宋体]前言;食醋中游离矿酸的测定[/font][font=Times New Roman],[/font][font=宋体]依[/font][font=Times New Roman]GB/T5009.31-2003[/font][font=宋体]采用百里草酚蓝试纸和甲基紫试纸进行定性检测。用此法不易对食醋中游离矿酸进行准确的检测。本文介绍了用电位滴定法对食醋中游离矿酸进行准确定量的原理及方法。该法简单可行,可与食醋中的总酸同时进行测定。[/font][/size][size=3][font=Times New Roman][/font][/size][size=3][font=宋体]一、电位滴定法测游离矿酸[/font][/size][font=Times New Roman][size=3]1.[/size] [/font][size=3][font=宋体]定义:游离矿酸:指硫酸,硝酸,盐酸等无机酸。[/font][/size][font=Times New Roman][size=3]2.[/size] [/font][size=3][font=宋体]原理:[/font][/size][img]http://ng1.17img.cn/bbsfiles/images/2010/10/201010181502_252097_2961690_3.jpg[/img][size=3][font=Times New Roman]4[/font][font=宋体])结合[/font][font=Times New Roman]1), 2), 3)[/font][font=宋体]中的计算式可计算出[/font][font=Times New Roman][H[/font][sub][font=宋体]矿[/font][/sub][font=Times New Roman][sup]+[/sup]],[/font][font=宋体]即游离矿酸浓度[/font][font=Times New Roman]([/font][font=宋体]以氢离子浓度计[/font][font=Times New Roman])[/font][/size][font=Times New Roman][size=3]3.[/size] [/font][size=3][font=宋体]试验[/font][/size][font=Times New Roman][size=3]1)[/size] [/font][size=3][font=宋体]仪器[/font][font=Times New Roman]:[/font][/size][size=3][font=Times New Roman]pHS-3C[/font][font=宋体]型酸度计[/font][font=Times New Roman] [/font][font=宋体]磁力搅拌器[/font][/size][font=Times New Roman][size=3]2)[/size] [/font][size=3][font=宋体]试剂:[/font][/size][font=宋体][size=3]①pH=4.00标准缓冲液;[/size][/font][font=宋体][size=3]②pH=6.86标准缓冲液;[/size][/font][size=3][font=宋体]③0.1mol/L的氢氧化钠标准溶液;[/font][/size][font=Times New Roman][size=3]3)[/size] [/font][size=3][font=宋体]试验方法:[/font][/size][size=3][font=Times New Roman]pHS-3C[/font][font=宋体]型酸度计用[/font][font=Times New Roman]pH[/font][font=宋体]=[/font][font=Times New Roman]6.86[/font][font=宋体]和[/font][font=Times New Roman]pH[/font][font=宋体]=[/font][font=Times New Roman]4.00[/font][font=宋体]的标准缓冲液校正正常待用。吸取[/font][font=Times New Roman]10.0mL[/font][font=宋体]样品于[/font][font=Times New Roman]100mL[/font][font=宋体]容量瓶中,加蒸馏水至刻度,混匀。吸取[/font][font=Times New Roman]20.0mL[/font][font=宋体],置于[/font][font=Times New Roman]200mL[/font][font=宋体]烧杯中,加[/font][font=Times New Roman]60.0mL[/font][font=宋体]蒸馏水,开动磁力搅拌器,读取被测溶液的[/font][font=Times New Roman]pH[/font][font=宋体]初;然后,用氢氧化钠标准溶液滴定至[/font][font=Times New Roman]pH[/font][font=宋体]=[/font][font=Times New Roman]8.2[/font][font=宋体];记录消耗氢氧化钠标准溶液的滴定数[/font][font=Times New Roman]V[sub]NaOH[/sub][/font][font=宋体]。[/font][/size][font=Times New Roman][size=3]4.[/size] [/font][size=3][font=宋体]计算公式:[/font][/size][align=center][size=3][/size][/align][img]http://ng1.17img.cn/bbsfiles/images/2010/10/201010181503_252098_2961690_3.jpg[/img][size=3][font=Times New Roman]二、[/font][font=宋体]方法讨论:[/font][/size][size=3][font=宋体]当用百里草酚蓝试纸和甲基紫试纸检测食醋中的游离矿酸时,若试纸呈现出阳性,为了防止出现假阳性,还须对样品进行定量试验,才可判定是否有游离矿酸。本文选取几个典型的样品用国标[/font][font=Times New Roman]GB/T5009.31-2003[/font][font=宋体]:百里草酚蓝试纸和甲基紫试纸法与用本文电位滴定法检测数值比较见下表:[/font][/size][img]http://ng1.17img.cn/bbsfiles/images/2010/10/201010181505_252100_2961690_3.jpg[/img][align=center][size=3][font=宋体]参考文献:[/font][/size][/align][size=3][font=宋体][1]GB/T5009.31-2003,[/font][font=宋体]《食品卫生检验方法 理化部分(一)》[s] [/s][/font][/size][size=3][font=宋体][2][/font][font=宋体]食品理化检验方法指南, 叶世柏主编[M],北京大学出版社,2000,147-148 [/font][/size][size=3][font=Times New Roman][/font][/size][size=3][font=Times New Roman][/font][/size][size=3][font=Times New Roman][/font][/size][size=3][font=Times New Roman][/font][/size]
我们是用草酸酸化提取出土霉素。怎样测定药品中草酸残余量呢?我用的是高效液相色谱。用的是反向离子柱。
建立食品中草酸含量测定的新方法—间接[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]。样品经处理后,加入过量且定量的氯化钙,使其与草酸根离子生成草酸钙沉淀,经离心分离后再利用[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url](AAS)法定量测定上清液中剩余Ca2+ 的含量,间接计算出食品中草酸的含量。在最佳条件下,该法的线性范围为0~8.0mg/L,回收率为98.1%~98.4%。本方法精密度高、灵敏度高、检出限低,适用于食品中草酸含量的测定。
国标中的检测方法为:称取2 g试样,称准至0.01g ,溶于20ml不含二氧化碳的水(2.4.1.3)中,加2滴酚酞指示液(2.4.1.1),如溶液无色,加0.3 m l氢氧化钠标准溶液(2.4.1.2 ),应显粉红色;如溶液呈粉红色,加0.3 ml盛酸标准溶液(2.4.1.4),粉红色应退去。国标中没有给出相应的公式,请问,游离酸或碱是按酸碱反应计算出来的吗?因为即使是0.1M的盐酸或氢氧化钠,滴定用的量都很少,请问大伙怎么准确操作的呢,是在滴定管中滴定呢,还是用移液器调到小量程多次加的呢?针对于上面国标的方法,是只能检测出游离酸或游离碱吗?有没有可能里面既含游离酸又含游离碱呢?因为国标上最后列出来的指标是游离酸小于多少,游离碱小于多少。非常谢谢大家。
借用xuanleer的帖子提一下几个疑问:不知道从何说起,我们在做某些碱性化合物检测时,购买的标准品通常是盐酸盐、硫酸盐、草酸盐之类的,如下面的糠氨酸(二盐酸盐)以及莱克多巴胺盐酸盐、四环素盐酸盐等等,疑问:(1)想问下大家这类目标化合物在进(HPLC、GC)色谱分析时,(色谱峰)是以游离碱的形式(糠氨酸、莱克多巴胺、四环素)存在还是以游离碱盐酸盐的形式存在?(2)这类化合物不少选用酸性环境下进行HPLC/LC-MS分析,其原因是否是让目标化合物以游离碱的形式(糠氨酸、莱克多巴胺、四环素)存在? (3) 如果第(2)个问题是对的,哪进GC分析时得到色谱峰是以何种形式存在的?也是游离碱吗?欢迎各位老师专家解答啊!顺祝大家节日快乐!参考资料如下:糠氨酸的鉴定适用于《NYT 939-2005 复原乳的鉴定》,具体见附件。色谱柱:LAEQ-462572 CNW Athena C18-WP 液相色谱柱,4.6*250mm,5um流动相:A=0.1%三氟乙酸水溶液;B=0.1%三氟乙酸乙腈平衡:A:B=99:1梯度:0min:99%A/1%B,25min:79%A/21%B检测波长:280nm流速:1ml/min进样浓度:2ppm柱温:室温标准品:CDDD-SC494-10MG,糠氨酸(二盐酸盐),品牌 NeoMPS,现货供应。参考:http://bbs.instrument.com.cn/shtml/20120903/4223471/
借用xuanleer的帖子提一下几个疑问:不知道从何说起,我们在做某些碱性化合物检测时,购买的标准品通常是盐酸盐、硫酸盐、草酸盐之类的,如下面的糠氨酸(二盐酸盐)以及莱克多巴胺盐酸盐、四环素盐酸盐等等,疑问:(1)想问下大家这类目标化合物在进(HPLC、GC)色谱分析时,(色谱峰)是以游离碱的形式(糠氨酸、莱克多巴胺、四环素)存在还是以游离碱盐酸盐的形式存在?(2)这类化合物不少选用选型环境下进行HPLC/LC-MS分析,其原因是否是让目标化合物以游离碱的形式(糠氨酸、莱克多巴胺、四环素)存在? (3) 如果第(2)个问题是对的,哪进GC分析时得到色谱峰是以何种形式存在的?也是游离碱吗?欢迎各位老师专家解答啊!顺祝大家节日快乐!参考资料如下:糠氨酸的鉴定适用于《NYT 939-2005 复原乳的鉴定》,具体见附件。色谱柱:LAEQ-462572 CNW Athena C18-WP 液相色谱柱,4.6*250mm,5um流动相:A=0.1%三氟乙酸水溶液;B=0.1%三氟乙酸乙腈平衡:A:B=99:1梯度:0min:99%A/1%B,25min:79%A/21%B检测波长:280nm流速:1ml/min进样浓度:2ppm柱温:室温标准品:CDDD-SC494-10MG,糠氨酸(二盐酸盐),品牌 NeoMPS,现货供应。参考:http://bbs.instrument.com.cn/shtml/20120903/4223471/
主要是测血清中游离谷氨酸和天冬氨酸。。。磺基水杨酸去蛋白离心取上清,然后直接用PITC做衍生,反应一小时后用等体积的正己烷萃取,然后上柱检测。求助PITC衍生有什么注意事项吗??标准品可以走出峰来,但是样品总是做不出来,氨基酸出峰有很大的干扰,几乎看不到氨基酸的峰。请教有什么注意事项吗?或者有好的萃取小柱吗?目前样品都用磺基水杨酸处理过了[em0812]
求助各位大侠用PE8000无机进样系统测试二氟草酸硼酸锂中的杂质含量的测试。
草酸学名乙二酸,化学式HOOC-COOH。当我们从课本上了解了羧酸的化学性质,是不是也能推断出草酸的一般性质了?在我们身边,草酸一般用作除锈剂或者可以除去白衣衫上的墨水污迹,而它其实也是一种可以能致人死命的危险的化学物质。可是大家知道平时爱吃的巧克力中也含有草酸吗?不要慌张,这种危险情况极少出现。我们每天都通过许多不同渠道摄入草酸,草酸在很多食品中都有少量存在,而在少数食品中含量很高。可可就属于含量最高的食品之一,,每100克可可中含有500毫克草酸;绿色蔬菜中的草酸含量一般很高,每100克菠菜含600毫克,大黄含500毫克,甜菜、花生、茶中也有较多的草酸。平均一个人一天大约摄入150毫克草酸,而草酸的致死剂量是1500毫克左右。我们在普通的一天中会摄入这么多草酸吗?那么摄入草酸对我们人体有什么影响? 大黄在美国曾被称为“食用大黄”,在过去,人们常把它和糖放在一起炖了吃。大黄最出名的特性是治疗便秘,因为它能刺激肠道排出自然毒素——草酸。一碗炖烂的大黄里含有的草酸已经接近于使人中毒的剂量。第一次世界大战期间,由于有人把大黄叶当作蔬菜吃,以至于草酸中毒身亡。而吃巧克力则无须担心,无论你对巧克力多么喜爱,但巧克力中的草酸含量太低,就是你吃的无法下咽的时候,体内的草酸含量达不到让你腹泻的程度。 在大黄流行的时候,烹制大黄食品方法层出不穷,曾经使用铝锅来炖大黄,发现意想不到的好处:它能把铝锅“炖”的很干净。之所以有这样的效果,是因为草酸能把铝锅氧化膜和表面金属溶解掉。当然,这种方法还会使食者摄取铝元素造成潜在的危害。
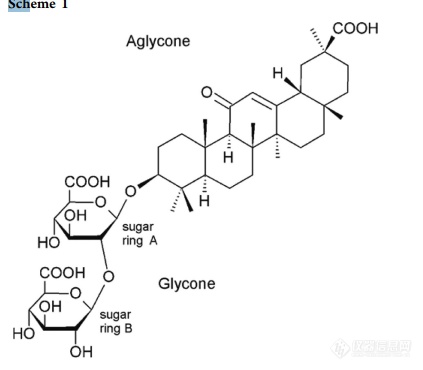
[align=center]CNS食品添加剂—甘草酸盐性质概述[/align] 杨勉疾[align=center]2021年 7 月[/align]1.甘草酸盐系列物质理化性质概述1.1 甘草酸理化性质 甘草入药史自古以来,是最为广泛的药用植物之一。其中甘草酸(CA)被认为是其提取物中最主要活性成分。甘草酸呈白色结晶性粉末,甜度约为蔗糖的200倍。显甜迟后,但留甜时间长;相对密度(d204):1.43;熔点在212-217℃左右;常压沸点972℃;闪点288℃;溶解性:难溶于冷水,易溶于热水,不溶于油脂,其热水溶液冷却后呈黏稠冻胶状。溶于丙二醇。 GA是一种单桥皂甙,其由三萜类疏水性苷元(18β甘草次酸)与亲水性二葡萄糖醛酸结合而成,GA的两亲性结构决定了其性能溶液中的物理性质。使得GA分子聚集水溶液中的表面活性化合物会导致聚集体、胶束的形成,并且在较高浓度下尤甚。其皂苷结构决定了GA许多特殊药理功能,调节其疏水分子形成水溶性复合物能力,可以用于调节其他物质化学稳定性,水溶性,生物利用度;以及在临床上应用于能性药物释放系统(DDS)。其有急性毒性:人体口经TDLo:280mg/kg/4W;小鼠口经LCLo:3gm/kg;小鼠腹经LCLo:2gm/kg;小鼠静脉LC:300mg/kg。在环境方面,甘草酸对水稍有危害,不可使未稀释或大量的产品接触地下水、水道或者污水系统。若无政府许可,不得排入周围环境。[1] 下图1.2分别为二维糖平台与三萜组成的基本结构单元透视图从两边伸出的部分;球和棍子(b)和空间填充(c)表示,显示由相互渗透的基本元素形成的通道单位(以浅灰色和深灰色显示的分子属于相邻单位)。通道约占晶体体积的42%。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/08/202108081544564157_4482_1608728_3.png[/img][/align][align=center]图 1甘草酸二维结构[size=16px][2][/size][/align][align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/08/202108081544567370_8_1608728_3.png[/img][/align][align=center]图 2 甘草酸三维立体结构[2][/align] 甘草酸作为一种多元酸,在碱性或离子液体内会不同程度脱质子成盐,在自然条件下,会和钾、钠离子结合存在。甘草酸盐是由甘草酸衍生的一系列盐类总称,包括甘草酸铵、甘草酸一钾及三钾、甘草甜素二钠等。1.2 甘草酸铵 甘草酸铵为白色粉末或淡黄色结晶型粉末,有强甜味,甜度约为蔗糖的200倍,溶于氨水,不溶于冰乙酸。应用于甜味剂,依照我国《食品添加剂使用卫生标准》,可按生产需要适量用于肉类罐头、调味品、糖果、饼干、蜜饯凉果、饮料等等。还可以用于进一步制备其他甘草酸盐类的中间物。 甘草酸单铵盐具激素样活性,但无激素的副作用,不仅对气管炎、支气管炎、咳嗽、哮喘等呼吸系统疾病有显著疗效。而且对消化道感染、乙肝、口腔溃疡、胃溃疡等也有奇效。对于多种毒素如白喉毒素、河月豕毒素、破伤风毒素和蛇毒等有着较强的解毒功效。同时还具有类似肾上腺皮质激素的作用。其毒理学半数致死量为10g/kg;经骨髓微核实验证实无致突变作用[3]。1.3 甘草酸一钾及三钾 甘草酸一钾及三钾类似白色或淡黄色粉末,无臭。有特殊甜味(甘草酸一钾为蔗糖的500倍;甘草酸三钾为蔗糖的150倍),甜味残留时间长,易溶于水,溶于稀乙醇、甘油、丙二醇,微溶于无水乙醇和乙醚。其同样应用于甜味剂,和甘草酸铵类似;毒理依据其半致死量为小鼠口服>10g/kg[4]。 在化妆品行业,可配制成护肤霜,祛斑霜高级珍珠膏等,既有美容护肤,又能消炎、抗变态反应,治疗皮肤病等作用;在医药行业,可用于眼药水、口腔炎的药膏;在日化行业,可用于牙膏。1.4 甘草酸二钠 甘草酸二钠又名甘草甜素二钠。为白色至淡黄色粉末,味极甜,稀释4000倍仍有甜味,甜度约为蔗糖的150-200倍,且甜味残留时间长。易溶于水,溶于稀乙醇、甘油、丙二醇,不溶于无水乙醇、乙醚、氯仿和油脂。用作甜味剂。日本限用于酱油(0.015g/L)和豆酱(0.03-0.07g/L)。毒性为半致死量5g/kg[5]。 由于其在水中非常易溶解,溶液澄清透明,无杂质和怪味,口感好,在食品添加剂方面具有低热能、安全无毒和较强的医疗保健功效,是高血压、肥胖症、糖尿病、心脏病患者使用的最理想甜味剂,有浓郁的甘草特殊香味,具有保健、解毒、护肝、消炎、增香等功效,是非常理想的纯天然甜味剂原料。2.甘草酸盐的制备及检测标准2.1 甘草酸生产方法及指标[6] 甘草酸以甘草为直接制备原料。将甘草的根茎干燥后粉碎至0.833mm的粉末(保留纤维部分)取粉末及纤维200kg,加水1200kg,在85-100℃下浸提2h。过滤后滤渣再用1000kg水提取2h,过滤后滤渣再重复浸提1次。合并3次滤液,在搪瓷蒸发器中浓缩至1/5体积。冷却后加入95%乙醇,使乙醇浓度达到65%,静置24h,过滤除去植物蛋白、多糖等杂质。滤液中加入硫酸,调节PH至甘草酸沉淀析出。过滤。洗涤后,加入3倍的丙酮,加热可回流3h,倾出提取液,残渣再反复回流提取2次。合并3次提取液,过滤后回收丙酮,浸湿甘草酸,与45℃干燥1h,缓缓升温至85-95℃,快烘干时,升至100-105℃烘干5min,经粉碎后即得成品。 此外,也可直接用氨水萃取,经浓缩后用硫酸沉淀,再用95%乙醇重结晶而得。 其质量指标需要符合中国企标:水分≤13%;灰分15%;熔点为220℃。2.2甘草酸二钠制备及质量标准[7] 甘草酸二钠一般由甘草酸为直接原料。其一由甘草甜素与钠碱进行部分中和而后精制而成。其二,由甘草粉加五倍水煮沸抽提,滤去固形物,加稀硫酸至呈弱酸性。室温下放置至析出物沉降,除去上澄清液,沉淀经水析出后用氨水中和、过滤、滤液加醋酸使甘草甜素铵析出,用70%-80%乙醇重结晶,按理论值加入碳酸钠水溶液,减压浓缩而得。 其质量指标参照日本标准,1999。包括含量95%-100%,溶液性状:10%水溶液应透明;5%溶液PH值5.5-6.5,氯化物(Cl-计)≤0.014%;水分≤13%;砷含量<4mg/kg;重金属<40mg/kg等等。相应的质量指标分析手段一般均通过标准试剂化学滴定得到。2.3甘草酸一钾及三钾制备方法及质量标准[8] 以甘草酸粗品(含量75%)为原料,在乙醇中用氢氧化钾中和而得。将100g甘草酸盐粗品加入400ml工业乙醇中国,在40-50℃下搅拌提取1h。抽滤后滤渣用200ml乙醇在同样的条件下提取1h,合并提取液,在搅拌下加入20%的KOH乙醇溶液至PH至7-8为止。静置片刻后分离得甘草酸三钾黄色结晶200g,将其放入80-90ml冰醋酸中,加热至75℃,保温几分钟使其转化为单钾盐,抽滤得近白色甘草酸单钾盐粗品,用少量工业乙醇洗涤一次,以出去黄酮类色素和甘草次酸等杂质。粗品用400ml乙醇冰醋酸混合液溶解,加入10g活性炭,在80℃下脱色0.5h。过滤后滤液放置结晶,得产品25-30g,收率约为70%。 其质量指标包括含量(UV法≥98%;HPLC≥85%);重金属≤0.001;砷盐≤0.0002;灰分≤9.63%;水中不溶物≤0.5%。2.4 间接甘草酸盐生产制备方法 为使甘草酸发挥更好的疗效和提高生产效率,非常需要实用性较强的制备甘草酸盐精品方法。 根据甘草酸易溶于热水,可溶于热稀醇,几乎不溶于无水乙醇和乙醚, 又可于水溶液中加稀酸游离液,又可于水溶液中加稀酸游离出来的性质,以及甘草酸锌盐、铁盐、铝盐及秘盐在热水中仅微溶或者不溶的性质,可以使甘草酸在水或稀醇溶液中与相应的无机盐水溶液反应制取需要的甘草酸盐。如果选用粗甘草酸溶液作原料,则得到甘草酸盐粗品,要制成精品往往需要反复多次精制,[font=times new roman][size=13px] [/size][/font]操作十分繁琐.如果选用甘草酸单按盐精品为原料,[font=times new roman][size=13px] [/size][/font]可以比较方便地制取草酸盐精品。在实际生产中,可以利用甘草或者甘草浸膏为原料,先制取甘草酸单按盐精品,然后再以甘草酸单按盐为原料制备甘草酸盐别的品种。在质量指标检测方面,甘草酸根含量测定可采用层析法,锌、秘、铝和铁的测定可采用容量分析或重量分析的方法。2.4.1甘草锌制备 取甘草酸单铁盐209溶于80%乙醇90ml中,加热回流,慢慢滴加予热至50℃的5%硫酸锌溶液80g,生成白色沉淀,加完硫酸锌溶液后,保温反应30min,之后降温至20℃,过滤,滤饼用6oml蒸馏水分三次清洗,滤尽母液,取出滤饼真空50℃干燥,得棕黄色甘草锌粉末19.69。测定甘草酸根含量87.6%,锌含为10.5%。2.4.2甘草酸秘制备 取甘草酸单铵盐溶于200ml热水中,于8℃在搅拌下慢慢滴加予热至60℃的10%的硝酸秘酸性溶509,需维持反应液为酸性(PH~3),生成白色沉淀,加完硝酸秘溶液后,保温反应30min,然后降温至30℃,过滤,滤饼用60rnl蒸馏水分三次清洗,滤尽母液,再以95%乙醇45ml分三次清洗,滤尽母液,在40~50℃真空干操,得白色甘草酸秘粉末21.39,测定甘草酸根含量82.2%,秘含量14%。3.甘草酸盐应用 邓淑华等人研究显示,甘草酸二钠、甘草酸二钾、甘草酸二铵在体外实验条件下,对金黄色葡萄球菌、白色葡萄球菌、大肠埃希氏菌、福氏志贺氏菌、乙型副伤寒沙门氏菌等细菌均表现了不同程度的抑菌作用。实验额外证实,甘草酸盐对乙型副伤寒沙门氏菌、金黄色葡萄球菌(附院)、福氏志贺氏菌等细菌具有一定的杀菌作用[9]。 甘草酸盐及甘草煎剂对杀虫双染毒的小鼠急性中毒不仅有顶防作用,而且甘草酸盐对急性中毒还有治疗作用,能明显降低杀虫双不同途径染毒之小鼠 、兔子的死亡率、其解毒机尚待进一步研究[10]。Francesco Maione[font=宋体]等人对单铵甘草酸盐抗炎抗伤害以小鼠实验进行以及生化和对接研究。在小鼠单次给药后的,一次腹腔注射AG对酵母多糖引起的足跖水肿和足跖肿胀均有抗炎作用腹膜炎。此外,在几种疼痛动物模型中,如扭体试验、福尔马林试验,酵母多糖诱发的痛觉过敏,试验前24小时给予AG可诱发痛觉过敏强烈的抗伤害作用。综上所述,所有这些发现都突出了AG在疼痛和或炎症相关疾病临床治疗中的潜在应用。AG与mPGES-2和COX-2的关键氨基酸相互作用。经过实验结果分析,甘草酸单铵的抗炎抗伤效应来自其与mPGES-2和COX-2的特异受体相互作用 。AG在结合处的定位较好COX-2与Trp387、Ser530(氢键)和Arg120等关键氨基酸相互作用时的囊袋。此外,通过结合刚性和柔性分子对接研究,两种可能的方法提出了AG与5-LO相互作用的机制:非氧化还原竞争结合和非氧化还原竞争结合Fe[/font][font=宋体]2+[/font][font=宋体]络合。而理论计算结果显示,前者结合能相对更低。[/font][font=宋体][11][/font]Carlotta Marianecci等人[font=宋体]研究表明甘草提取物可用于治疗皮炎、湿疹和银屑病,其疗效与皮质类固醇相当。在这项工作中,通过研究不同浓度的表面活性剂(吐温85和司班20)和胆固醇组成的囊泡在甘草酸铵(AG)释放中用于治疗各种炎症性疾病的效果。对囊泡进行了包括尺寸、ζ电位、各向异性、药物包封率、稳定性、细胞毒性评价和皮肤耐受性等方面的表征,证实纤维素膜在甘草酸铵囊泡的体外释药特性中作用[/font][font=宋体][12][/font][font=宋体]。[/font]甘草酸在大多数肝脏疾病的临床实践中用作肝脏保护剂。万荣等研究证实,甘草酸二铵减缓肝损伤并可阻止自然杀伤T细胞。其通过两种不同剂量甘草酸多铵给药对照试验,通过检测相应指标。得出预处理能显著降低血清ALT并改善cona诱导的自身免疫性肝组织损伤的结论。实验结果证实,DG预处理可下调攻击后的炎性细胞因子与Con A,并可以抑制胸腺T淋巴细胞凋亡。此外,甘草酸二铵还可有效地抑制CD4的增殖+CD25、CD69+、CD8+及CD69型+等外周血和脾脏的亚群,并显著下调NKT细胞的频率,同时上调树突状细胞的频率肝脏[13]。隋秀文等研究证明了甘草酸多铵盐和氯化锂共同作用抑制伪狂犬病病毒PrV感染,并可诱导PrV细胞凋亡。(PrV)是一种猪嗜神经性疱疹病毒与单纯疱疹病毒1型(HSV-1)有共同的基因组排列。其感染严重威胁畜牧业和人类健康。以甘草酸多铵盐为基底开发有效的抗病毒药物是减少PrV感染的重要策略之一[14]。李云等研究证实,甘草酸二铵(DG)具有抗炎和保肝药理作用。非酒精性脂肪肝(NAFLD),作为常见的慢性肝病,在世界范围内普遍存在。李云团队通过高脂饮食诱导的NAFLD模型小鼠实验,我们观察到DG可以减轻体重、肝脏脂肪变性以及肝脏炎症Illumina对16S rRNA的测序显示DG干预改变NAFLD小鼠肠道微生物群的组成,使得肠道菌群的丰富度显著增加。特别是DG降低了厚壁菌与拟杆菌的比率和产生内毒素的细菌(如脱硫弧菌)提高了益生菌如变形杆菌和乳酸杆菌的丰度。DG能增强短链蛋白的表达水平,如产脂肪酸(SCFA)的细菌、瘤胃科和漆树科,促进SCFA的产生。此外DG补充显著减轻了肠道低度炎症。促进细胞表达紧密连接蛋白、杯状细胞数量和粘蛋白分泌,从而增强肠屏障功能。因此,目前可以认为,DG对NAFLD的预防可能是通过调节肠道菌群和恢复肠道功能来实现的[15]。异甘草酸镁(MgIG)被广泛应用于慢性肝病的治疗。主要认为是通过作用于肝毒性诱导物质——甲氨蝶呤(MTX)诱导的肝毒性实现其效果。曹雨竹等人研究结果显示,预防性的给予小鼠MgIG(9和18mg/kg/天)可显著降低小鼠血液中血清天冬氨酸转氨酶和丙氨酸转氨酶的减少;MgIG还能减轻MTX诱导的肝纤维化。对MTX诱导的肝细胞损伤有较好的保护作用。此外,MTX还可诱导环氧合酶-2(COX-2)表达,给予MgIG后,肠道通透性和炎症减轻。总之,MgIG对甲氨蝶呤引起的肝毒性和肠道损伤有积极作用一种,是有可能缓解MTX肝脏和肠道副作用的药物[16]。4.总结甘草是一种豆科草本植物,其作史古已有之,必然意味着甘草所独具的 性质千百年来一直为人们所使用。而其主要活性成分甘草酸及其衍生盐类由于其甜度极高,且甜度留存时间长,主要用作甜味剂用于食品添加剂中。但都具有一定毒性,需要严格按照国家标准使用。此外,甘草酸盐还具有药理性质,在生物医药研究方面受到了学者的广泛关注,具有抗炎、保肝两方面的功能,因此也频繁应用与新型药物的开发,其价值也得到了更多的延伸。参考文献[1]甘草酸的制备及其在食品工业中的应用.食品工业,1994,(6);49~51[2]Tykarska E , Gdaniec M . Toward Better Understanding of Isomorphism of Glycyrrhizic Acid and Its Mono- and Dibasic Salts[J]. Crystal Growth & Design, 2013, 13(3):1301-1308.[3]郑国斌.从甘草酸粗品制取甘草酸单钾盐.中国医药工业杂志,1995,26(2);54[4-5,7-8]食品添加剂应用手册/孙平,张津凤主编.一北京:化学工业出版社,2010.10 ISBN978-7-122-09417-9[6]苌云玉.甘草酸盐制备方法研究[J].基层中药杂志,1995(04):33-34. [9]邓淑华,王晓斌,王鸿梅,刘艳华.甘草酸盐抗菌作用的实验研究[J].承德医 学院学报,2011,28(03):325-326.[10]黄能慧,曾样锬,刘季昆,夏炳南.甘草酸盐对农药(杀虫双)的解救作用[J].贵阳医学院学报,1982(03):21-22.[size=13px] [/size][11] Maione F , Minosi P , Giannuario A D , et al. Long-Lasting Anti-Inflammatory and Antinociceptive Effects of Acute Ammonium Glycyrrhizinate Administration: Pharmacological, Biochemical, and Docking Studies[J]. Molecules, 2019, 24(13)[12] [size=13px][color=#222222]Koide M , Takahashi M , Tamagaki S , et al. Catalytic effect of dipotassium glycyrrhizinate on the hydrolysis of nonionic ester surfactants[J]. Journal of the American Oil Chemists' Society, 1996, 73.[/color][/size][13]万荣, 刘莎, 范稚坚,等. Clinical Observation of Diammonium Glycyrrhizinate Enteric-coated Capsule in Preventing Liver Injury Induced by Anti-tuberculosis Drugs[J]. 大理学院学报, 2019, 004(004):45-47.[color=#222222][14] Sui X , Yin J , Ren X . Antiviral effect of diammonium glycyrrhizinate and lithium chloride on cell infection by pseudorabies herpesvirus.[J]. Antiviral Research, 2010, 85(2):346-353. [15][/color] [color=#222222]Li, Yun, Liu, et al. Diammonium Glycyrrhizinate Protects against Nonalcoholic Fatty Liver Disease in Mice through Modulation of Gut Microbiota and Restoration of Intestinal Barrier[J]. Molecular pharmaceutics, 2018.[/color][16] Marianecci C , Rinaldi F , Mastriota M , et al. Anti-inflammatory activity of novel ammonium glycyrrhizinate/niosomes delivery system: Human and murine models[J]. Journal of Controlled Release, 2012, 164(1):17-25.