最近在做食品中钙,1.曲线0-5mg/L,相关系数:0.9999,2.标准物质是GBW10018鸡肉,3.曲线和样品中镧含量都是4g/L,4.微波消解,消解程度:无肉眼可见物,溶液呈现浅黄色5.标准物质回收率只有50%6.通过稀释一倍来改变样品中镧的含量,都没有显著差异不知大家是否有经验传授,不胜感激!
最近在检测食品中钙,氧化镧的空白有点高,所以想用锶盐,不知道氯化锶多大的浓度呢?有做过的吗
新西兰修订2008年食品标准 新西兰近日发出G/SPS/N/NZL/411号通报,对2008年新西兰(农化物最大残留限量)食品标准进行了修订,拟将以下MRL(农化物最大残留限量)纳入2008年新西兰食品标准表1:葡萄内的啶酰菌胺3mg/kg及梨果内的啶酰菌胺0.05mg/kg,芸薹类植物内的异恶草松0.01mg/kg及萝卜内的异恶草松0.02mg/kg,核果(樱桃除外)0.02mg/kg内的嘧菌环胺,鳄梨内的埃玛菌素0.005mg/kg,芬苯哒唑:哺乳动物脂肪0.05mg/kg、哺乳动物肾0.05mg/kg、哺乳动物肝0.5mg/kg、哺乳动物瘦肉0.05mg/kg,双炔酰菌胺:球茎洋葱0.01mg/kg及绿葱0.2mg/kg,绵羊脂肪7mg/kg、绵羊肝5mg/kg、绵羊肾2mg/kg及绵羊瘦肉内的0.7mg/kg,1-萘乙酸:橘子0.01mg/kg,Oxfendazole:哺乳动物脂肪0.05mg/kg、哺乳动物肾0.05mg/kg、哺乳动物肝0.5mg/kg、哺乳动物瘦肉0.05mg/kg,葡萄内的唑菌胺酯2mg/kg。 2008年新西兰食品标准(农业化合物最大残留限量)还有特别规定:农业化合物残留达到但不超过国内MRL标准的食品、含不超过0.1mg/kg农残且新西兰未对该食品中的相关农业化合物做出规定的食品,可在新西兰销售。如进口食品符合以上条件之一,或含农业化合物残留不超过FAO/WHO CODEX发布的“食品内杀虫剂残留或食品内兽药残留”当前或补充版规定的该农业化合物在该食品(种、类、或等级)中的限量,可在新西兰销售。 该通报的拟批准日期为2008年10月22日,拟生效日期为2008年11月27日。信息来源:中国质量新闻网
[size=4] 近日,新西兰食品安全局(NZFSA)发布了对《新西兰(澳大利亚、新西兰食品标准法典)食品标准2002》的第31号修订案。[/size][size=4] 该修订案对《食品标准法典》作了第117号修订,主要内容如下:[/size][size=4] 1、允许在糖霜和糖粉中使用食用色素3号赤藓红;[/size][size=4] 2、允许使用由转基因玉米(耐除草剂)Line DP-098140-6加工的食品;[/size][size=4] 3、允许使用β-半乳糖苷酶作为加工助剂(酶);[/size][size=4] 4、允许使用麦芽四糖淀粉酶作为加工助剂(酶)。[/size][size=4] 该修订案将于2010年9月2日生效。[/size]
钾钠钙镁火焰原吸标准曲线很差小弟最近刚学习火焰原吸,用的仪器是普析通用ATS-990,做钾、钠、钙、镁火焰原吸的时候标准曲线很差,很难得到三个九,请问各位大侠是怎么做的?有普析通用ATS-990的吗?你们设的参数是多少? 我做的时候没有加锶盐、镧溶液消除干扰!
哪里可以买到蓝萼甲素标准品,做指纹图谱用。我在沈阳。
这个问题涉及到很多方面,故放在综合区,望版主谅解。近日在考察注射用盐酸阿糖胞苷是否可用USP37的标准。发现一个问题,USP37收载的该剂型的活性物质是阿糖胞苷,而不是盐酸阿糖胞苷;而在查阅国外的几个制药公司的该产品的说明书,注明的活性物质也是阿糖胞苷原型,而非盐酸盐。故在此想请教对药物化学和药物分析很了解的童鞋们几个问题:1、国外的该产品说明书上注明的是阿糖胞苷原型药,USP37收载的也是原型药,是否说明在国外该制剂采用的原料药是阿糖胞苷,而非其盐酸盐?2、国内的制药厂家的该产品说明书上注明的活性物质是盐酸阿糖胞苷,且中国药典收载的也是盐酸阿糖胞苷,毫无疑问说明原料药采用的是盐酸阿糖胞苷,为什么要用盐酸盐,而不跟国外一样采用原型药?是为了避开专利还是盐酸盐的形式更有利于人体吸收?3、USP37收载原型药,被检测的药物是盐酸盐,是否说明该药物不能用USP37的标准来检?4、在哪里可以查到国外药物的专利,及其详细信息,如药物的化学结构、化学式、其专利到期的时间等?5、如何可以准确地知道国外一些药品制剂所使用的原料的详细信息?尤其是理化方面的信息,这些信息在说明书上体现的很少。望高手不吝赐教!谢谢!
我们在编写标准时,关于专利的那句话是必须写的一个套话吗?如不是什么情况下写一般?谢谢
今天做食品中的钙,在仪器资料上看到,产生吸光度为0.2的溶液浓度为0.8mg/L。但是,在将仪器条件调节到最佳状态时,我做的标准曲线如下:C(mg/L)00.51.01.52.03.0A0.00270.02160.04020.05820.07850.1176 这样的话灵敏度下降了很多.后来看到资料上用的是笑气-乙炔火焰,我用的是空气-乙炔火焰,这会不会是原因呢?
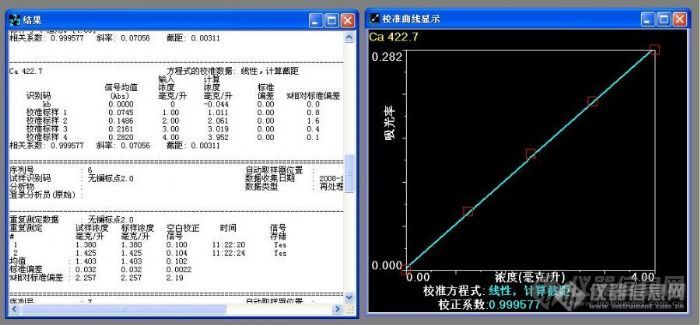
用[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]法测定钙元素时,由于铝、硫酸盐、磷酸盐和硅酸盐等能抑制钙的原子化,产生干扰,所以需要加入锶、镧或其他释放剂。该实验用[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]火焰法测定水中的钙镁元素,验证了一下镧盐在测定中的作用。实验参考方法是GB/T 8538-1985饮用天然矿泉水检验方法中钙镁的测定,测定采用的是PE700仪器的推荐条件,其中钙标准曲线浓度分别为1.00、2.00、3.00、4.00ppm,氯化镧溶液定容,试验空白为氯化镧溶液,曲线如图:[img]http://ng1.17img.cn/bbsfiles/images/2008/12/200812272218_126601_1626455_3.jpg[/img][img]http://ng1.17img.cn/bbsfiles/images/2008/12/200812272219_126602_1626455_3.jpg[/img]同时配制了一个浓度为2.0ppm的钙元素标点(没有加氯化镧),测定数值如上图,发现样品中不加镧盐测定数值偏低很多。同时做镁的标准曲线浓度为0.10、0.20、0.30、0.40ppm,加入了氯化镧溶液,曲线如图:[img]http://ng1.17img.cn/bbsfiles/images/2008/12/200812271807_126583_1626455_3.jpg[/img][img]http://ng1.17img.cn/bbsfiles/images/2008/12/200812271807_126584_1626455_3.jpg[/img]同样配制了一个浓度为0.2ppm的镁元素标点(没有加氯化镧),测定数值如上图,发现样品中不加镧盐测定数值没有太大的变化。最后得出结论,在进行水中钙元素的测定时,必须要加入镧盐,否则测定数值偏低,而镁元素的测定是否加入镧盐对实验结果影响不大。
[size=4][font=黑体]日前发表文章,介绍了近年来日本、韩国、美国、欧盟、加拿大、智利和澳大利亚对食品检测标准作出的一些新调整。现将文章主要内容转载如下: 日本通过立法对进口食品实施新贸易措施 日本《食品卫生法》及其修正案新的《食品卫生法》对不合格的进口食品采取更严厉的措施,增加了农残、药残的限制项目,修正案则进一步强化进口农产品检查制度,规定农产品只能使用108种农药。对多次检出不合格进口食品的地区将全面禁止进口。 《种苗修正案》该修正案规定,未经缴纳专利费、擅自利用日本植物种源生产或改良的农产品,个人侵权者处以300万日元以下罚金或3年以下有期徒刑;法人企业侵权最高处以1亿日元的罚金。该修正案已于2004年4月实施。 优良农产品认证制度最近,日本农林水产省决定在2005年前建立优良农产品认证制度,目前已开始对牛肉进行认证。[/font][/size]
[center]Gilead就HIV药品专利起诉Teva[/center]生物技术公司Gilead Sciences Inc.(GILD)表示,针对Teva Pharmaceutical Industries Ltd.(TEVA)生产Truvada仿制版本的举动,已向后者提起了一项专利侵权诉讼。Truvada是Gilead用于治疗艾滋病病毒(HIV)的全球畅销药。 Gilead表示,Teva生产Truvada仿制版本的计划将侵犯覆盖该药一种成分的两项专利。Gilead表示,该药受到10项专利的保护。该公司已向纽约联邦地区法院提交了诉状。 上个月,总部位于以色列的Teva请求美国食品与药品管理局(FDA)批准其研制的仿制版的Truvada。在那次申请中,该公司表示,保护Truvada的10项专利中的两项是无效的、不可执行的,或者不会被侵犯,如果Teva自己的版本获准上市的话。Gilead已经表示,此次诉讼涉及的这两项专利要到2021年才到期。 这两项专利都与Emtriva有关,后者是Truvada的两种成分之一。另一成分是Gilead生产的一种名为Viread的药物。Emtriva与Viread也是三合一的HIV治疗药Atripla,以及百时美施贵宝生产的Sustiva的关键成分。 Truvada第三季的销售额达到5.49亿美元,占Gilead当季营收的40%。 此次诉讼导致了FDA监管程序的暂停。该机构在最多30个月内、或者在法院就这两项专利的有效性作出裁决之前不会批准Teva的仿制版Truvada。信息来源:医药新闻网
据新西兰初级产业部(MPI)消息,针对新西兰牛奶中检出低含量双氰胺的报道,新西兰两家最大的肥料公司已暂停双氰胺的销售,新西兰初级产业部对两家公司采取的行动表示支持。 双氰胺是肥料辅助品,用于牧场可增加牧草的产量,还可防止肥料的副产品硝酸盐流入河流和湖泊,并减少温室气体的排放。 新西兰初级产业部表示,目前双氰胺在食品中的限量尚无国际标准,使用双氰胺不存在食品安全风险,而且双氰胺毒性较低,未发现高剂量使用会出现不良反应。 然而新西兰MPI担心,由于目前尚无国际标准,消费者不能接受牛奶中检出双氰胺的事实,这可能会对新西兰的乳品贸易产生影响。 原文链接:据了解,现在有很多第三方机构及政府机构提供双氰胺检测的方法有HPLC \LC-MS\LC-MS-MS ,后者居多,本机构也是提供LC-MS-MS 检测方法检测
因为职称的事情去找评委会咨询,咨询过后,评委会告诉我,这几年评职称的人业绩都很厉害,要不有专利,要不制定了行业标准。现在的职称评审好难啊,中级都要有标准了,高级更不用说了,平常只会默默工作的人,是不可能评上职称的。
某食品微生物检验室内有一冰箱,其上标识为待检样品,未见样品保存期间的温度监控记录。请问该食品微生物检验室做法是否符合相关标准文件要求?
[u]兰州市食品药品检验检测研究院[/u]招标项目的潜在投标人应在[u]兰州市公共资源交易中心网(http://lzggzyjy.lanzhou.gov.cn/)在线免费获取磋商文件[/u]获取招标文件,并于[u]2022-10-09 09:30[/u](北京时间)前递交投标文件。一、项目基本情况项目编号:206003JH035项目名称:兰州市食品药品检验检测研究院2022年下半年标准品试剂耗材等采购项目预算金额:210.0(万元)最高限价:210.0(万元)采购需求:详见招标文件,供应商只能中标其中一个包合同履行期限:根据采购人的通知时间,交货期为十个工作日本项目(是/否)接受联合体投标:否
做农残检验的朋友们,对于一个对日出口型企业来说,实验室该多少拥有农药标准品合适?以前参照一齐法,理论上应该具备200多种农药标准品,中国国标也有一次性检验400多种农药的记录,不知是不是我见识浅的问题,感觉一次性测那么多有点变态了,像那样的话,代价太大,一天搞定一个样就不错了,而且结果有时令人质疑。我现在对我每日需要测定的样品,一律用混合样建立农残数据采集方法,但是还是觉得不妥。那天借了本常用农药手册发现,有很多我公司加工用到的蔬菜(书上提到它们经常使用的农药我们这边都没有)你们说该咋整,单纯为了应付商检,又该备有哪些常用农药标准品!!!!!!!
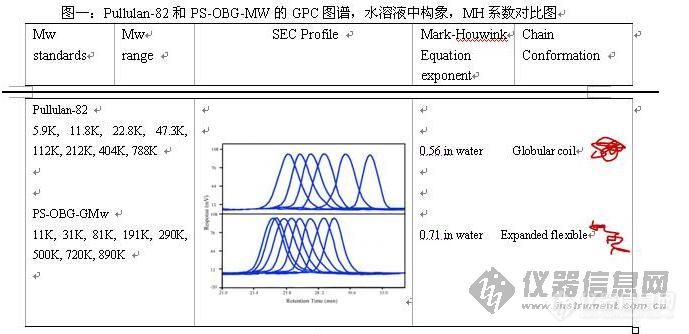
目前,高分子碳水化合物正被广泛应用于食品,啤酒,制药等行业,如香菇多糖,羧甲基纤维素,透明质酸,半乳甘露聚糖等,但对于不同分子量的碳水化合物来说,它们的作用都是不同的,因此在工业生产和科学研究中对于准确测定高分子碳水化合物的分子量就显的尤为重要。 目前,绝大数公司,高校和科研院所都使用凝胶渗透色谱(GPC)法来测定高分子物质分子量,这种方法相对于光散射法来说具有操作简单,经济快速等优点,因此在各行业得到广泛的使用。对于这种方法来说,在测定待测样品时,需要选择标准品来做标准曲线,因此对于准确测定高分子碳水化合物的分子量来说,标准品的正确选择就显得尤为重要。Pullulan和Dextran是两种从微生物中提取的多糖,主要被用于分子量的测定,但是通过研究我们发现这两种多糖在水溶液中的构象为一个球状线团,他们的MH系数α为0.5左右,而上面我们提到的香菇多糖,羧甲基纤维素,透明质酸,半乳甘露聚糖等高分子物质在水溶液中的结构为扩展性构象,因此当我们用Pullulan和Dextran作为标准品来测定这些具有扩展性链结构的大分子物质分子量时,是不是可以准确测定它们的分子量呢?为了进行对比研究,我们选择了另一种分子量测定标准品燕麦β葡聚糖(PS-OBG,来源于百特纯大分子有限公司),该标准品时从燕麦细胞壁中提取的,结构单元为葡萄糖,与Pullulan和Dextran相同,但它是由β-1,4和β-1,3键连接而成的线性结构,在水溶液中呈现扩展性构象,MH系数α为0.71.实验材料:待测样品:香菇多糖(PLE),羧甲基纤维素(CMC),半乳甘露聚糖(GG)葡聚糖标准品套盒:Shodex公司的pullulan-82(p-82),该套盒有8个点,分子量从5000到800000,百特纯大分子有限公司的通用分子量套盒(PS-OBG-GMw),该套盒有8个点,分子量从11000到89000实验方法:分别用GPC法和光散射(LLS)法来测定该样品的分子量试验结果:图一:Pullulan-82和PS-OBG-MW的GPC图谱,水溶液中构象,MH系数对比图表一:三种不同物质分子量的测定结果Samples Mw1 Mw2 Mw3PLE 707k 1160k 790kGG 122k 331k 112kCMC 130k 354k 148kMw1 : 用PS-OBG-GMw 套盒测定值Mw2: 用Pullulan-82 套盒测定值Mw3 : 用光散射测定值从表一中我们可以发现用pullulan-82来测定这些具有扩展性链结构的大分子物质时,会导致明显的过高测定,之所以会出现这样的情况,是因为对于同样分子量的标准品来说,球形线团结构在GPC柱子中流出时间要比扩展性结构的流出时间长,而用PS-OBG来测定的话,测定值则非常接近光散射值,因此在对于大多数植物及真菌类多糖和具有扩展性链结构的大分子物质来说,用PS-OBG来测定是非常适合的。http://ng1.17img.cn/bbsfiles/images/2017/01/201701191653_632709_1672347_3.jpg
今年6月底前后,跨国药企美国默克公司降胆固醇药舒降之(辛伐他汀)和全球药业老大辉瑞公司的抗抑郁药左洛复(舍曲林)先后失去专利保护权,去年这两种药品全球销量分别为44亿美元、34亿美元。同时,包括诺华的兰美抒、赛诺菲安万特的思诺思、百时美施贵宝的普拉固和葛兰素史克(GSK)的枢复宁等在内的全球多个重磅药品,均将在两年内结束其专利保护期。有数据显示,今年年内将有全球年销量约230亿美元的专利药专利到期,而到2008年之前,全球专利到期药品的总价值将超过800亿美元。 全球专利药的集中到期,将给以仿制药为主的中国药企提供巨大商机,国内药企无论在仿制药开发、原料供应还是制剂生产方面都面临很多机会。 研发机构、药企提前“盯”上到期专利药 美国一项名为《全球非专利处方药市场》的最新报告称,未来4年超过30种药物面临专利到期的命运,全球非专利处方药销售将快速上扬,从2005年的282亿美元增至2010年的480亿美元。2004年非专利处方药市场即达到253亿美元,2005年增长了11.2%.预计未来数年内该市场仍将以近似的增速稳定增长。在未来数月内,畅销药物如络活喜、帕罗西汀专利均将陆续到期。对于这一市场空间,业内分析,最先受益的将是靠开发仿制药生存的中国药品研发机构,他们的生意将显得日益兴隆。 “到期专利药的仿制开发在国内十分普遍,包括药厂自己的研究所在内,全国至少有6000个药品研发机构都提前在做类似的事情。”研发型企业广东固志医药科技有限公司总经理吴智南告诉记者,目前委托他们做这种开发的有10多家药企,他们正在对20多个专利即将到期的药品进行开发,主要是根据其已公开的专利技术知识,研究药物的合成路径。吴智南称,一般开发这样的药品要花9个月左右的时间,每个品种收取研发费用约50万元。 其实,与收益相对稳定的研发型企业相比,药厂面对的专利药到期市场无疑是一场苦战。“我现在主要还是生产抗菌类普药,暂且不会考虑去做到期专利药仿制。”广州诺贝华乐制药公司总经理许守良称,专利到期药的研发成本并不高,但报批手续特别烦琐,没有一定渠道很难拿到批文。“往往有上百家药厂去开发一个品种,国内厂商利润已非常低,竞争近乎惨烈。”做药品研发近20年的吴智南认为,这种过度竞争的模式他并不看好。 另外,不仅是仿制药企之间存在竞争,现在原研药厂家也开始介入这一场仿制药的争夺战。据悉,正是瞅准这一市场前景,制药巨头诺华去年已将其位居全球第二位的非专利药业务“山德士”引进中国,并在华积极寻求合作伙伴;而日前,就在美国一家仿制药宣布其生产的辛伐他汀将比默克“舒降之”价格低30%~50%之后,默克即与美国最大健康保险公司UnitedHealth达成协议,专利品牌药“舒降之”今后价格将比任何一家上市的辛伐他汀产品都低。 乙肝药仿制市场集中上演“血拼”大战 这么多“重磅炸弹”可以仿制,对于药企和研发机构而言,哪些品种对他们更有吸引力呢? 据了解,刚在美国专利到期的默克“舒降之”进中国11年并无专利保护,而辉瑞“左洛复”在华行政保护也在几年前到期,这两种药品的仿制品早就“遍地开花”了。业内人士分析,目前到期专利药的仿制大战中,最为激烈的恐怕是乙肝药市场的争夺了。据GSK相关人士介绍,现在国内已有几十家药厂把目光聚焦在专利即将到期的一线乙肝抗病毒药“贺普丁”(拉米夫定)。若以零售价计算,2005年贺普丁在中国销售收入约有10亿元。而今年9-10月,贺普丁在华专利保护就将到期。 最新资料显示,全球目前有4亿乙肝病毒感染者,而中国就占到1/3,慢性乙肝治疗等相关费用每人年均2万元左右,中国整个乙肝病市场至少有100亿元的容量。去年以来,GSK、施贵宝又先后向中国引进了贺维力、博路定两款乙肝新药,诺华公司乙肝新药也即将在华上市。与这些价格不菲的专利药相比,专利行政保护即将到期的贺普丁成了众多患者和药厂的“抢手货”。“目前,公司正在研发一系列抗病毒品种,包括拉米夫定在内总共有几十个品种。”上海新先锋药业副总经理李建文向记者表示,一般他们会提前两年就对将到期的目标药品合成路径及生产工艺进行研发,等到临过期时再开发,市场早就被别人抢走了。“研发费用本身并不贵,像开发拉米夫定一个品种约200万元,最头疼的事情是仿制厂家太多,市场竞争将十分激烈。”李建文称。 不过,对于国内正酝酿的拉米夫定仿制热潮,贺普丁生产商GSK有关人士则表示了不同意见。“贺普丁专利的行政保护权,确实将在2006年第四季度到期,但目前贺普丁在华仍有其他专利可保护。”负责贺普丁市场的GSK抗感染药高级经理黄怡峥向记者表示,贺普丁在华专利包括生产制备方法专利以及拉米夫定活性成分与药用载体相合成的方法专利,这几项专利将在2010年至2015年间到期。问及GSK乙肝新药贺维力与老药贺普丁会不会形成营销冲突,黄怡峥表示,两者可以互补,今后贺普丁也不会撤出中国市场。 专家说法 “首仿药”更应关注 一直以来,国内4500多家药企90%以上在做仿制药,而往往同一个品种集中了上百家甚至几百家药厂在生产,造成了严重的资源浪费和恶性竞争。有关专家据此认为,国内厂商与其一哄而上去拼抢在华专利到期的某一个品种,不如把精力投向已在国外上市却未进入中国市场的“首仿药”市场,虽说投入稍高,但回报将更为客观。 在美国,一旦某个药品专利到期,首家获得仿制权的药企在市场和定价上都有更多优先权。“目前,专利到期的舒降之已被全球最大非专利药公司以色列TEVA首家取得FDA仿制批文,TEVA将获得180天市场独占权”,默沙东(即美国默克)中国公司公共事务高级主任丁燕宁介绍。 今年3月初,国家发改委向相关企业下发了《药品定价方法》征求意见稿,首次提出“首仿药”概念,要求对首仿药(即“首先研究申报国外已上市而在国内未上市的药品”)给予定价优先。该方案称,国内首先仿制生产并上市销售的同种仿制药品的价格经专家论证后,允许在统一定价的基础上适当上浮,上浮范围不超过政府规定的最高上浮范围。 上海市食品药品监督管理局科技情报研究所主任干荣富向媒体表示,国家拟允许“首仿药”价格比同类产品上浮15-20个百分点,且享有一段时间的价格独享权,是国内制药企业不可错过的好机会。干荣富称,他汀类、普利类、沙坦类、抗抑郁药、抗溃疡药等特色原料药已给许多企业创造了利润,这些企业避开了专利,并且在国际上获得了注册、认证以及合同加工订单,特别是在2008-2010年前后,将有一批专利药到期,这会给一大批特色原料药创造巨大的市场需求。
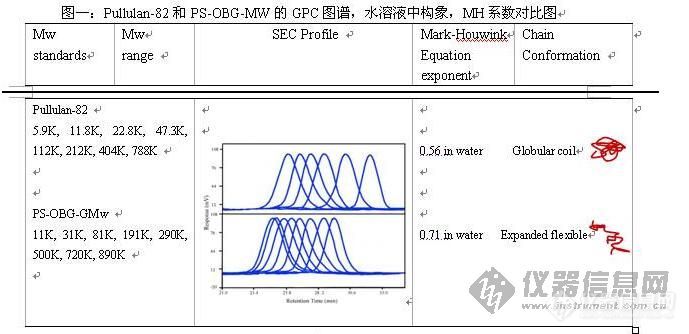
目前,高分子碳水化合物正被广泛应用于食品,啤酒,制药等行业,如香菇多糖,羧甲基纤维素,透明质酸,半乳甘露聚糖等,但对于不同分子量的碳水化合物来说,它们的作用都是不同的,因此在工业生产和科学研究中对于准确测定高分子碳水化合物的分子量就显的尤为重要。 目前,绝大数公司,高校和科研院所都使用凝胶渗透色谱(GPC)法来测定高分子物质分子量,这种方法相对于光散射法来说具有操作简单,经济快速等优点,因此在各行业得到广泛的使用。对于这种方法来说,在测定待测样品时,需要选择标准品来做标准曲线,因此对于准确测定高分子碳水化合物的分子量来说,标准品的正确选择就显得尤为重要。Pullulan和Dextran是两种从微生物中提取的多糖,主要被用于分子量的测定,但是通过研究我们发现这两种多糖在水溶液中的构象为一个球状线团,他们的MH系数α为0.5左右,而上面我们提到的香菇多糖,羧甲基纤维素,透明质酸,半乳甘露聚糖等高分子物质在水溶液中的结构为扩展性构象,因此当我们用Pullulan和Dextran作为标准品来测定这些具有扩展性链结构的大分子物质分子量时,是不是可以准确测定它们的分子量呢?为了进行对比研究,我们选择了另一种分子量测定标准品燕麦β葡聚糖(PS-OBG,来源于百特纯大分子有限公司),该标准品时从燕麦细胞壁中提取的,结构单元为葡萄糖,与Pullulan和Dextran相同,但它是由β-1,4和β-1,3键连接而成的线性结构,在水溶液中呈现扩展性构象,MH系数α为0.71.实验材料:待测样品:香菇多糖(PLE),羧甲基纤维素(CMC),半乳甘露聚糖(GG)葡聚糖标准品套盒:Shodex公司的pullulan-82(p-82),该套盒有8个点,分子量从5000到800000,百特纯大分子有限公司的通用分子量套盒(PS-OBG-GMw),该套盒有8个点,分子量从11000到89000实验方法:分别用GPC法和光散射(LLS)法来测定该样品的分子量试验结果:图一:Pullulan-82和PS-OBG-MW的GPC图谱,水溶液中构象,MH系数对比图表一:三种不同物质分子量的测定结果SamplesMw1Mw2Mw3PLE707k1160k790kGG122k331k112kCMC130k354k148kMw1 : 用PS-OBG-GMw 套盒测定值Mw2: 用Pullulan-82 套盒测定值Mw3 : 用光散射测定值从表一中我们可以发现用pullulan-82来测定这些具有扩展性链结构的大分子物质时,会导致明显的过高测定,之所以会出现这样的情况,是因为对于同样分子量的标准品来说,球形线团结构在GPC柱子中流出时间要比扩展性结构的流出时间长,而用PS-OBG来测定的话,测定值则非常接近光散射值,因此在对于大多数植物及真菌类多糖和具有扩展性链结构的大分子物质来说,用PS-OBG来测定是非常适合的。[img]http://ng1.17img.cn/bbsfiles/images/2008/12/200812160944_124361_1672347_3.jpg[/img]
美“生物仿制药途径”为药品专利博弈设新规 □毛黎 美国药品市场极大。据艾美仕市场研究公司最新统计,2009年全美药品总销售额达3003亿美元。在销售的药品中,大多高利润的药品受专利保护,价格低廉的仿制药必须在专利过期后才有机会进入美国市场。据报道,今后两年内,全球有20多个专利药的核心专利将过期,其销售额大约为690亿美元。这给全世界的仿制药生产商提供了机遇。 美国1984年通过的“药品价格竞争及专利补偿法案”(Drug Price and Patent Restoration Act,又称Hatch-Waxman法案),为由美国联邦食品、药品和化妆品法(Federal Food,Drug and Cosmetic Act)管辖的仿制药进入市场提供了简化申请程序,方便仿制药在专利过期后快速进入市场。 今年3月,美国总统奥巴马签署了医疗改革法案。此法案中一些条款制定了生物仿制药进入市场的简化申请途径,又称“生物仿制药途径”(Biosimilars Pathway),这无疑给生物仿制药提供了新的机遇。 首先,该法案定义“生物仿制”产品为与参照产品(如新药)“高度相似”的生物制品。“(生物仿制产品和参照产品)即使在临床上非活性的组分上可能有微小差别”,但“安全性、产品的纯度和效力在临床上并无有意义的差异”。 根据此法案,生物仿制药的申请人在新药获准销售的4年内不得向美国食品药品管理局(FDA)提交生物仿制药简化申请,而FDA不可在创新药品获准销售的12年内批准生物仿制药简化申请,从而保证新药的市场独占期最少为12年。 其次,“生物仿制药途径”制定了一个新药生产商与仿制药申请人之间相互交换有关专利信息的机制。根据Hatch-Waxman法案,新药的专利有效期和市场专营期都列在《经治疗等同性评价批准的药品》(橙皮书)上。与Hatch-Waxman法案不同,生物仿制药途径所适用的药品不列在橙皮书上,而是要求生物仿制药申请人在FDA接受申请之后20天内,向新药生产商提供一份申请的副本,并披露其生产流程。这些资料对外保密,但必须提供给新药生产商的律师。此外,如果新药生产商从第三方专利权人那里获取了生产新药的许可,而第三方专利权人保留了参与专利诉讼的权利,仿制药申请人则要向第三方专利权人提供同样的信息。 在收到这些信息60天内,新药生产商必须向仿制药申请人提供一份专利清单,列出所有被仿制药侵权的专利,并向对方指出愿意许可授权的专利。仿制药申请人在收到专利清单的60天内必须提供一份声明,根据“事实和法律”,详细说明为何专利清单所列专利无效,不可强制执行或将不会被仿制产品侵权,否则仿制药申请人必须声明在专利过期之前不会商业营销仿制药。针对仿制药申请人的声明,新药生产商必须在60天内,根据“事实和法律”,详细说明所列专利为何有效,可执行,且被仿制药侵权。法案要求双方进行有诚意的谈判,如果诉讼不可避免,法案则规定了对侵权诉讼和获取初步禁令的程序。 由此可见,新药生产商必须在60天时间里决定用哪些专利主张。仿制药申请人则必须在60天内决定是否挑战和如何挑战这些专利,其立场必须在随后的诉讼过程中经得起考验。由于新药生产商很可能会罗列许多专利,仿制药申请人若无准备,可能无法在规定的60天里完成所需的大量工作。所以,仿制药申请人需要在递交申请之前就预测对方会主张哪些专利,并准备好对策。 虽然新药生产商在接到申请书副本后有60天的时间来分析仿制药的生产工艺并选择专利主张,在接到仿制药申请人对其专利挑战后有60天作出回应,因而总计有120天制定主张策略,但如果事先对自身的专利不明了,也很可能措手不及。所以,新药生产商有必要针对其产品进行专利排查。 核心专利过期和“生物仿制药途径”为中国医药企业提供了打进美国市场的契机。但抓住这些机遇要求企业能很好地运用专利这一工具,这无疑再次凸显了知识产权的重要性。
[b][color=#cc0000][font=微软雅黑]问:[/font][font=微软雅黑]服装招标项目,在评分标准中,能否要求服装有专利工艺?[/font][font=微软雅黑]答:这个[/font][font=微软雅黑]属于以不合理的条件对供应商实行差别待遇或者歧视待遇。法律依据:《政府采购法实施条例》第二十条,采购人或者采购代理机构有下列情形之一的,属于以不合理的条件对供应商实行差别待遇或者歧视待遇:(六)限定或者指定特定的专利、商标、品牌或者供应商。[/font][/color][/b]
我这边依据GB 5009.92-2016 食品安全国家标准 食品中钙的测定来做样品加标,钙的回收率做到了300%,不知道是什么原因。想请各位老师给点指导意见。
我按照食品国标法,用PE-400做食品中钙的原子测定,可是测定结果不理想,请有经验的朋友发一份标准,谢谢
[color=#DC143C][B]贴几个相关文章,供大家浏览~~[/B][/color][color=#6495ED][B]标准”不应成壁垒 [/B][/color]在当前国际贸易中,几乎所有工业产品都得遵守进口国的标准,否则将难以进入相关市场。但是,目前世界上绝大多数的国际标准均是由发达国家确定和控制的,而在目前复杂的国际标准背后,实际上充斥了大量由发达国家公司或个人所持有的专利。因此,一旦某项标准获得国际认可,则其背后相关的各类专利便成为了悬在国际标准遵循者头上的达摩克利斯之剑。 以DVD行业为例,根据2002年的一项统计,我国企业负担的各种专利费用总计平均约19.7美元/台。在这样的情况下,我国DVD企业实际上几乎无利润可赚。 现有专利制度与产业标准结合的一个后果便是,如果领先厂商在行业标准竞争中占得先机,则网络效应会导致兼容性厂商和消费者没有其他选择的余地,领先厂商将按照现行专利制度提供的保护收取利益,而该专利的价格也必然是按照经济学的垄断定价原理制定,这必然导致社会生产效率的递减。为解决这个问题,发达国家在国内对此进行了限制和约束,在大量的司法实践中,专利的信息披露义务、专利应用中的RAND原则以及专利拥有者的反垄断义务逐渐在发达国家被人们接受和采纳。 然而,该问题一旦进入国际层面,则由于大量的国际标准及其背后的知识产权均属于发达国家,而标准及其专利的使用者往往都是后进的发展中国家,由此发达国家又换成了另一副面孔———或对损害发展中国家生产效率的行为视而不见、或亲自出面要求发展中国家接受自己制定的国际标准,或者全力迫使国际社会接受单方面的知识产权规则却不提如何限制知识产权的滥用———以上行为的最终后果,使得发达国家与发展中国家在国际标准应用上的收益严重的不对等。 基于上述现状,2005年6月,中国在世贸组织的技术性贸易壁垒委员会(TBT委员会)会议上正式提交了一个提案“标准化中的知识产权问题”。该提案引起了广泛的国际反响。外电报道,这是中国第一次在国际会议上提出自己在知识产权方面的主张,并且涉及到了知识产权与国际标准的关系这一敏感问题。 在该提案中,中国认为,国际标准制定和采用中的知识产权问题已对各成员根据TBT协定要求采用国际标准、便利国际贸易造成阻碍。WTO应该考虑到该问题对多边贸易的消极影响,并就与该问题相关的多边贸易政策进行探讨。中国并不认为TBT委员会应对上述所有的问题负责。但因为TBT鼓励成员们采用国际标准,而上述问题对国际标准制定的效率和质量以及成员采用国际标准的效果有重要意义,因此,“标准化中的知识产权问题”与TBT密切相关。 鉴于此,中国政府建议,TBT委员会应利用其三年审议的工作优势就该问题进行讨论,寻求解决这一问题的方法和政策,以便推动国际标准的制定和实施,从而促进TBT的实施。“标准化中的知识产权问题”有重要的“发展”内涵。TBT委员会应当彻底讨论该问题,这将有助于增强发展中成员参与国际标准化活动和国际贸易。发展中成员面临的困难及他们在技术援助和能力建设方面的需要等,在委员会就该问题的讨论中应被给予充分的关注。 在今年11月形成TBT三年审议报告时,美国等成员以该问题与TBT不相关等理由反对将该问题纳入报告。中国等成员据理力争,经过密集、激烈的磋商,成员同意中方在报告体现“标准化中的知识产权问题”提案的要求。“标准化中的知识产权问题”在WTO历史上第一次被写入WTO文件。 与此同时,我们应该看到,“标准化中的知识产权问题”是一个敏感和复杂的问题,今后的工作还很艰巨。中国政府将以负责任的态度,积极推动这个对发展中国家和发达国家都具有重要性意义的议题的进展。
2011年8月9日消息,印度标准局(BIS)日前更新了限制玩具中邻苯二甲酸盐(phthalates)含量的要求,以配合包括美国、加拿大及各欧盟成员国在内的30多个国家对邻苯二甲酸盐的限制。印度此项举措将紧跟由美国消费品安全委员会(CPSC)提出的指导方针,根据该方针规定,儿童玩具及儿童护理用品中各类禁止的邻苯二甲酸盐的含量不得超过0.1% 在此之前,印度标准局已规定玩具中邻苯二甲酸盐的总量不得超过0.1%;但是该规定指的是三类邻苯二甲酸盐的总和,其中包括邻苯二甲酸二辛(DEHP)、邻苯二甲酸二癸酯(DDP)、邻苯二甲酸二丁酯(DBP)或邻苯二甲酸二异壬酯(DINP、邻苯二甲酸二异癸酯(DIDP)和邻苯二甲酸二正辛酯(DNOP),而不是指每一项不超过0.1%。 印度玩具协会于7月在新德里举办了第5届国际玩具博览,而印度此次决定正是继美国玩具产业协会(TIA)和印度标准局在此博览会上讨论所决定的。玩具产业协会技术部副总裁Alan Kaufman曾与印度标准局的VijayMalik博士谈及印度邻苯二甲酸盐的规定,称此项举措有助于在全球范围内设立玩具安全标准。AlanKaufman还指出,印度修订了邻苯二甲酸盐的限制要求,意味着印度在玩具安全方面的努力又向前迈进了一步,希望通过对邻苯二甲酸盐的限制,玩具公司能开发出更安全的产品,并且更顺利地走出国门开拓新的市场。
原标题:药品专利集中到期,中国化学药企业市场份额提升仍艰难中国化学药企业以生产仿制药为主,且经过多年发展,国产仿制药整体产能规模已居世界前列,但由于研发投入低、研发能力弱及政策支持力度小,行业整体仍处于产业链低端,原料药产品以大宗原料药为主,制剂药产品中蛋白类普药和抗生素占比较高,企业间产品同质化竞争严重。相较外资药企,中国化学药企业占中国医药市场的份额处于较低水平。 伴随全球药品专利集中到期,一方面,专利药品在高端医院市场的份额下降,为仿制药产品的进入腾出空间;另一方面,中低端市场上新仿制药品种类大幅增加,用药人群也大幅上升,中低端市场有望扩容。整体上,仿制药市场呈持续扩大趋势。 但从中国化学药行业看,由于行业集中度低,行业内企业规模普遍较小,研发费用占销售收入的比重较低,避专利工艺开发能力较弱,实现过期专利药品首仿难度较大,而过期后的专利药品在中国市场仍享受单独定价权,在现行的“药品加成”政策背景下,定价较高的原研药在高端医院市场较仿制药竞争优势明显。同时,为减缓专利药品到期对盈利的影响,跨国专利药企业开始向仿制药领域延伸,并加快了在中国市场的布局。在具有较强的技术研发体系、学术推广能力和品牌优势的跨国专利药企业竞争下,中国化学药企业在中低端市场份额的扩大也存在较大阻力。 整体看,全球药品专利集中到期的背景下,中国化学药企业整体市场份额的提升仍比较艰难。
[font=宋体][size=3]百灵威整合国际资源为烟草行业提供品类齐全的烟草成分分析标准品。产品涵盖烟草分析所用到的各类代谢物、衍生物、农药及香精香料标准品。可以满足烟草行业各类分析实验需求。[/size][/font]
受委托检测一批亚硝酸盐的样品,给的样品包含酱腌菜,豆制品,银耳等。但是GB 2760-2011 《食品安全国家标准 食品添加剂使用标准》(含增补公告)GB 2762-2005 《食品中污染物限量》中只提到了熏肉腊肉,酱腌菜,新鲜粮食蔬菜肉类的限量,没有豆制品银耳等的限量~那我该参考什么呢。这样看的话前段时间传的沸沸扬扬的血燕亚硝酸盐超标是参考的那个指标呢?
请问哪里可以买到敌鼠钠盐标准品和氟乙酸标准品啊?