我需要D5-莱克多巴胺标准品,发现只有D5-莱克多巴胺盐酸盐标准品,测食品中残留量是不是一样的用
我们参与能力验证用[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]法测定金属元素Cu和Pb,Cu样品介质为盐酸5%溶液,Pb样品介质为硝酸5%溶液,那么配制标准系列时Cu和Pb也分别是5%盐酸和5%硝酸?平时我们一般是0.2%硝酸.总之标准系列的酸度要和样品一致吗?
哪位大侠知道哪里有卖孔雀石绿的盐酸盐标准品的?谢谢![em23] [em27]
盐酸副玫瑰苯胺比色法测定亚硫酸盐方法的要点及改进 盐酸副玫瑰苯胺比色法测定食品中的亚硫酸盐残留量是食品卫生理化国标检验方法中的第一法( GB/ T5009. 34 -1996) ,它灵敏、准确,但是它对于水不溶性样品检测时间太长,同时方法未给出关键试剂盐酸副玫瑰苯胺溶液中盐酸浓度范围等,给实际操作带来很大的不便。相据笔者的摸索及实践经验,进行了改进。现报告如下:1 水不溶性固体样品的前处理前处理时间按标准规定水不溶性的固体样品粉碎研磨浸泡至少4h 后才能过滤测定(以使二氧化硫完全被吸收) ,整个实验过程最短也要5h 以上,如果能将水不溶性的固体样品的前处理方法加以改进,实验时间将会大大缩短。笔者用振荡法或超声波法对几种水不溶性固体样品进行不同时间的处理,同时与浸泡法进行了对比,结果见表1。表1 不同前处理方法测定亚硫酸盐残留量(以SO2 计,g/ kg) 结果对比样品名称浸泡5h 超声40min 振荡50min话梅1. 27 1. 28 1. 29情人梅1. 71 1. 75 1. 72话梅肉0. 67 0. 65 0. 69山楂糕0. 12 0. 13 0. 11冬瓜蜜饯0. 77 0. 79 0. 75银耳6. 02 6. 00 5. 95竹笋4. 23 4. 18 4. 20竹荪9. 29 9. 34 9. 32干辣椒0. 080 0. 078 0. 069 对表1 中数字进行统计学处理,浸泡5h 与超声40min 两方法之间经t 检验, P 0. 05 ,两法测定的结果无显著性差异 同时浸泡5h 与振荡50min 两方法之间经t 检验, P 0. 05 ,两法结果也无显著性差异。所以,对于水不溶性的固体样品,可以用超声法(40min) 、或振荡法(50min) 来代替浸泡法进行样品前处理。2 实验关键试剂盐酸副玫瑰苯胺比色法涉及的试剂有多种,其中盐酸副玫瑰苯胺和二氧化硫标准是两个最关键的试剂。2. 1 二氧化硫标准液 二氧化硫标准液容易氧化变质,经实验,新标定的1. 142mg/ ml 二氧化硫标准溶液避光存放冰箱的条件下,可稳定一个月,一个月后必须重新标定。实验结果见表2。表2 二氧化硫标准贮备液存放时间对吸光度值的影响时间1μgSO2标准吸光度2μgSO2标准吸光度4μgSO2标准吸光度一个月前配制0. 002 0. 030 0. 076新配制0. 034 0. 067 0. 1412. 2 盐酸副玫瑰苯胺溶液 盐酸副玫瑰苯胺溶液中的盐酸浓度对实验结果影响非常大,酸度大,比色颜色浅,灵敏度低 酸度低,比色颜色深,灵敏度高,同时空白值也高。但标准方法中未给出调节盐酸副玫瑰苯胺溶液颜色的盐酸用量范围,仅仅指出用肉眼观察颜色变化(由红变黄) ,在实际操作中笔者曾几次因显色剂酸度问题导致实验失败。所以有必要找到一个合适的盐酸副玫瑰苯胺溶液盐酸酸度范围,使实验空白值低、灵敏度又满足要求,为此笔者进行了不同盐酸浓度下标准和空白吸光度值的对比实验,结果见表3 和图1。表3 盐酸副玫瑰苯胺溶液中盐酸的浓度与吸光度的关系盐酸浓度(mol/ L)显色剂颜色空白吸光度4.μgSO2标准吸光度减空白后吸光度0. 20 浅黄色0. 298 0. 459 0. 1610. 30 黄色0. 338 0. 372 0. 0340. 40 黄色0. 251 0. 303 0. 0520. 50 黄色0. 089 0. 254 0. 1650. 60 黄色0. 076 0. 230 0. 1540. 70 黄色0. 062 0. 202 0. 1400. 80 黄色0. 054 0. 186 0. 1320. 90 黄色0. 046 0. 168 0. 1221. 00 黄色0. 043 0. 158 0. 115 注:表2 中盐酸的浓度是指加到盐酸副玫瑰苯胺溶液中盐酸的用量换算之后的浓度。图1 中标准吸光度为减去空白吸光度后的值。图1 不同酸度的盐酸副玫瑰苯胺溶液对空白和标准吸光度值测定的影响0 6 7 中国卫生检验杂志2003 年12 月第13 卷第6 期 Chinese Journal of Health Laboratory Technology 20031December1131No16© 1995-2005 Tsinghua Tongfang Optical Disc Co., Ltd. All rights reserved.2. 2. 1 从图表中可以看出盐酸副玫瑰苯胺溶液中盐酸介质的浓度在0. 50mol/ L、0. 60mol/ L 时灵敏度高,但空白值也高(0.089、0. 076) ,盐酸副玫瑰苯胺溶液中盐酸介质的浓度在0.70mol/L - 1. 0mol/ L 之间空白吸光度较低(0. 062 - 0. 043) 并且灵敏度较高,所以配制0. 02 %的盐酸副玫瑰苯胺使用溶液时,可吸取0. 1 %盐酸副玫瑰苯胺溶液20ml 后直接加入一定量的(1/ 1) 盐酸使盐酸的浓度为0. 70mol/ L - 1. 0mol/ L 之间即可使用。实践证明使用同一个合适酸度的盐酸副玫瑰苯胺溶液,用新标定的标准溶液做标准曲线,环境条件、仪器条件相对稳定的前提下,可以使用相对较长一段时间(更换盐酸副玫瑰苯胺溶液时,再重新标定标准溶液,绘制新的标准曲线) 。2. 2. 2 0. 20mol/ L 空白及标准吸光度较0. 30mol/ L 的空白及标准吸光度高,是因为在反应体系中由于酸度的降低,盐酸副玫瑰苯胺本身结构改变颜色发生变化所致。3 标准曲线线性范围国标方法中规定标准曲线的线性范围是从0 - 4μg 二氧化硫,经过实验线性范围可延伸到10μg 二氧化硫,结果见表3。表3 盐酸副玫瑰苯胺比色法测定二氧化硫残留量标准曲线标准含量(μg) 0. 00 0. 40 0. 80 1. 20 1. 60 2. 00 3. 00 4. 00 6. 00 8. 00 10. 00吸光度值0. 000 0. 012 0. 027 0. 040 0. 061 0. 067 0. 107 0. 141 0. 222 0. 292 0. 368 线性范围的扩大对于高含量样品可减少稀释带来的误差。本文根据笔者的实际经验和摸索,对盐酸副玫瑰苯胺比色法测定食品中的亚硫酸盐残留量提出了改进意见,会给实际操作者带来一定的益处。参考文献[1 ] 中华人民共和国国家标准,食品卫生检验方法,理化部分,食品中亚硫酸盐残留量的测定方法GB/ T5009. 32 - 1996.(收稿日期:2003206230)
请教硫酸、盐酸浓度测定的国家标准为什么
硫氰酸汞测空气中盐酸标准曲线不好,可能是什么原因?
按照国标法进行总氮的测定时,为什么要在碱性溶液中进行消解,如果采用酸性(硫酸调节酸度)可以吗?消解完毕后,为什么要用盐酸调节酸度然后在进行比色?用硫酸调节酸度可以吗?敬请各位专家赐教!
酸度(盐酸或硝酸超过50%对火焰测守有影响吗
现在很多目标物买的标准品都是对应的盐酸盐,除了标品制备更稳定外,还出于什么目的?在[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]中目标物和对应的盐酸盐为何保留时间无区别,另外如果在质谱中,盐酸盐的标品和目标物是否会有区别
食品安全国家标准 食品营养强化剂 L-盐酸赖氨酸
在兽药残留检测时,有时只能找到盐形式的标准品,有时盐形式的标准品比较便宜,这种情况下有用盐形式的标准品的想法。举两个个例子:例1:沙丁胺醇,分子量:239.31,CAS:18559-94-9,100mg,4320元 沙丁胺醇硫酸盐,分子量:337.39,CAS:51022-70-9,100mg,510元例2:莱克多巴胺,分子量:301.38,CAS:97825-25-7,主要供应商均无此标准品 盐酸莱克多巴胺,分子量:337.84,CAS:90274-24-1,100mg,945元问题1:如果用沙丁胺醇硫酸盐替代沙丁胺醇,是否可以得到一致的保留时间?问题2:如果用沙丁胺醇硫酸盐替代,最终结果是否需要折算?问题3:如果需要折算,沙丁胺醇硫酸盐的折算系数是否为239.31/337.39=70.93%?
测蛋白时,用盐酸标准溶液滴定好,还是选择硫酸标准溶液合理?
酸度计标准操作规程1 目的建立酸度计操作规程,使质检人员能正确使用,确保酸度计测定数据的准确性。2 适用范围适用于各类原辅料、中间体、成品、水质及缓冲溶液的PH值测定。3 责任者:操作人员4 操作规程4.1 基本操作4.1.1 接通电源,打开开关钮。4.1.2 标准温度 检测所测样品温度与PH计温度设定值是否一致。若不同,输入被测样品溶液的温度值。4.1.3 电极准备 将保护帽从电极头处取下,并将橡皮帽从填液孔上打开,先用蒸馏水冲洗,后再用标准缓冲液冲洗电极头,最后用滤纸将水吸干。4.1.4 核对电极 使用与被测样品PH值接近的缓冲液定位,再用PH值个差约3个的标准缓冲液核对一次,误差应不超过±0.02PH单位。4.1.5 使用电极前 需用纯化水冲洗,再用供试液冲洗电极,最后用滤纸将水吸干。4.1.6 样品测定 将供试品溶液(若是固体需溶解),移至小烧杯中,将电极插入烧杯溶液中。4.1.7 使用后清洗电极 取出电极并用纯化水洗涤,然后用滤纸将水吸干。4.1.8 存放电极 将电极头套入保护帽中,然后打开填液孔上的橡皮帽,将电极插入填液孔中。4.1.9 关闭开关钮,拔出电源。4.2 注意事项4.2.1 新电极必须在PH=4或PH=7缓冲液中过液。4.2.2 用滤纸吸干电极时,勿擦拭电极,以免产生极化和迟缓现象。4.2.3 小心使用电极,勿当搅拌器用,取放勿接触电极膜。4.2.4 测定小体积样品时,确保液体能否浸没电极头。4.2.5 勿使电极保护液干涸。4.2.6发现缓冲液有浑浊、长霉、沉淀现象和超过保持期时,勿继续使用。另外用过的溶液禁止倒回瓶中。4.2.7 配制标准缓冲液与供试品溶液,应使用新沸过的冷蒸馏水配制。4.2.8 实验完毕后,填好酸度计操作使用表。若出现异常,在操作使用表上写明,向负责人报告并处理。酸度计使用登记表日期操作人部 门检测物质名称PH值仪器状况备 注酸度计操作原始记录表日 期操 作 人部 门检测物质测量结果备注: 部门负责人: 报告人:
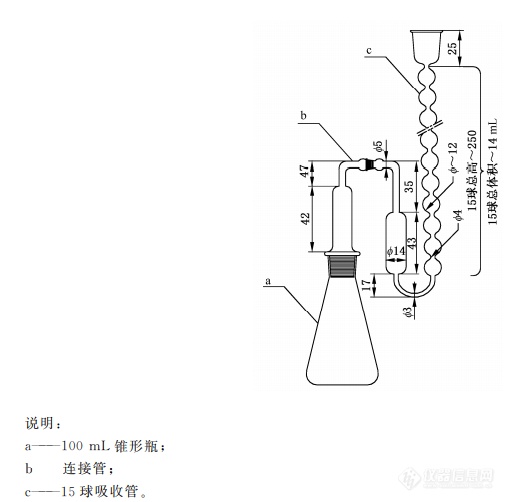
[align=center][font='calibri'][size=29px]浅析食品级盐酸[/size][/font][/align][align=center][font='calibri'][size=18px]范紫嫣[/size][/font] [/align]摘要:盐酸作为传统的无机化合物,除了实验室、工业生产中的应用外,在食品领域也可作为添加剂使用。本文针对盐酸的理化性质、杂质、应用等方向进行了简要的讨论。关键词:食品级盐酸 理化性质 应用 食品安全是民生首要大事。随着生活水平的提高,人们的健康意识不断增强,“绿色食品”、“无添加食品”等概念逐渐流行。2013年12月23日召开的中央农村工作会议上,习近平总书记在会上强调:“能不能在食品安全上给老百姓一个满意的交代,是对执政能力的重大考验”。16世纪利巴菲乌斯正式记载了氯化氢的制备方法后,在工业革命期间,盐酸开始大量生产。作为人们谈之色变的化学物质,它在食品添加剂中常作为酸度调节计、合成原料出现。本文就盐酸的理化性质、杂质检测、应用等方面对食品级盐酸展开讨论。[font='calibri'][size=21px]1[/size][/font][font='calibri'][size=21px] [/size][/font][font='calibri'][size=21px]盐酸[/size][/font][font='calibri'][size=18px]1[/size][/font][font='calibri'][size=18px].1 [/size][/font][font='calibri'][size=18px]盐酸的理化性质[/size][/font]盐酸的分子式为HCl,在常温下为无色或浅黄色的透明液体,常由氯气与氢气合成制得,由于装置的开停车及工艺控制条件的变化,造成成品酸中杂质含量的变化。根据国家标准规定,各杂质含量须在表1规定内才为食品级盐酸。[align=center][size=12px]表1[/size][font='宋体'][size=12px][1][/size][/font][size=12px] [/size][size=12px]理化指标[/size][/align][table][tr][td][align=center]项目[/align][/td][td][align=center]要求[/align][/td][td][align=center]指标[/align][/td][/tr][tr][td][align=center]铁(以Fe计),/%[/align][/td][td][align=center]≤[/align][/td][td][align=center]0.0005[/align][/td][/tr][tr][td][align=center]硫酸盐(以SO4计), /%[/align][/td][td][align=center]≤[/align][/td][td][align=center]0.007[/align][/td][/tr][tr][td][align=center]游离氯(以Cl计), /%[/align][/td][td][align=center]≤[/align][/td][td][align=center]0.003[/align][/td][/tr][tr][td][align=center]还原物(以SO3计), /%[/align][/td][td][align=center]≤[/align][/td][td][align=center]0.007[/align][/td][/tr][tr][td][align=center]不挥发物, /%[/align][/td][td][align=center]≤[/align][/td][td][align=center]0.05[/align][/td][/tr][tr][td][align=center]砷(mg/kg), mg/kg[/align][/td][td][align=center]≤[/align][/td][td][align=center]1.0[/align][/td][/tr][tr][td][align=center]重金属(以Pb计),mg/kg[/align][/td][td][align=center]≤[/align][/td][td][align=center]5[/align][/td][/tr][/table]当前,随着合成食品加工业的迅速发展,对食品酸的需求日益增加。与之相反的是国内工业酸市场销售状况时好时坏,滞销、积压时常出现。因此,工业酸经除铁、脱色后制成食品酸的工艺也逐渐发展起来。福州第二化工厂的陈允翼等[font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]2][/size][/font]使用RT型离子交换树脂,处理含铁量过高的工业酸能得到符合要求的食品级盐酸,该方法路线简单,操作方便,对设备、管道材质亦无特殊要求。[font='calibri'][size=18px]1.2 [/size][/font][font='calibri'][size=18px]盐酸的鉴别实验[/size][/font] 量取1 mL试样于50 mL水中,滴加硝酸银溶液,即产生白色乳状沉淀。能在氨溶液中溶解而不在硝酸中溶解。或量取1 mL试样于100 mL水中,加两滴甲基橙溶液,溶液为红色,则该水溶液为强酸性[font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]1][/size][/font]。[font='calibri'][size=18px]1.3 [/size][/font][font='calibri'][size=18px]总酸度的测定[/size][/font] 以溴甲酚绿为指示剂,用氢氧化钠标准滴定溶液滴定盐酸待测液至由黄色变为蓝色。可由下列公式计算得盐酸的总酸度(以HCl计),取平行测定结果的算术平均值为测定结果,平行测定结果的绝对差值不大于0.2%。其中:V——滴定中消耗的NaOH标准滴定溶液的体积,mL;c——NaOH标准滴定溶液的浓度,mol/L;m[font='宋体'][size=13px]1[/size][/font]——试样的质量,g;[font='calibri'][size=18px]1[/size][/font][font='calibri'][size=18px].3 [/size][/font][font='calibri'][size=18px]检验规则[/size][/font][font='calibri'][size=18px][[/size][/font][font='calibri'][size=18px]3][/size][/font] 食品添加剂盐酸应由生产厂的质量监督检验部门进行检验,每批出场的该产品都必须符合国家标准的要求,并附有一定格式的质量证明书。内容包括:生产厂名、厂址、产品名称、等级、净重、批号、生产日期、食品卫生许可证号、生产许可证号、产品质量符合本标准的证明及本标准编号。使用单位有权按照国标的规定对食品添加剂盐酸产品进行验收。当检验结果如果有一项不符合本标准规定,应重新自两倍量的包装中重新取样进行核验,检验结果即使有一项不符合国标的要求,则整批产品判为不合格。在运输过程中,需要专用槽车、食品包装用聚乙烯塑料桶、玻璃钢衬里的容器或以专用陶瓷坛包装。 食品添加剂盐酸储存时不得与有毒、有害物品混储。保存期为两年,逾期重新检验,合格仍可使用。[font='calibri'][size=21px]2[/size][/font][font='calibri'][size=21px] [/size][/font][font='calibri'][size=21px]杂质的测定[/size][/font][font='calibri'][size=18px]2[/size][/font][font='calibri'][size=18px].1 [/size][/font][font='calibri'][size=18px]铁含量(以[/size][/font][font='calibri'][size=18px]F[/size][/font][font='calibri'][size=18px]e计)的测定[/size][/font]工业上生产盐酸常在钢管中制备、运输盐酸,在反应时铁可能与氯气反应生成FeCl[font='宋体'][size=13px]3[/size][/font],从而使得盐酸溶液呈现黄色。而人体长期摄入铁元素会导致慢性铁中毒,表现出肝硬化、骨质疏松、生殖器官发育障碍、凝血障碍等症状。因此,检测并除去食品级盐酸中的铁是制备工艺中最重要的一步。[size=16px]2[/size][size=16px].1.1 [/size][size=16px]盐酸羟胺还原法[/size]试样中的Fe[font='宋体'][size=13px]3+[/size][/font]能被盐酸羟胺还原成Fe[font='宋体'][size=13px]2[/size][/font][font='宋体'][size=13px]+[/size][/font],在pH为4.5缓冲溶液体系中,Fe[font='宋体'][size=13px]2+[/size][/font]与1,10-菲啰啉反应生成橙红色络合物,用分光光度计测定吸光度。反应式如下:通过测定波长为510 nm处的溶液吸光度,绘制以铁含量为横坐标,吸光度为纵坐标的标准工作曲线法测得铁元素的含量。由下式可算得:式中:m[font='宋体'][size=13px]2[/size][/font]——试样的质量,g;10[font='宋体'][size=13px]-6[/size][/font]——换算系数;m[font='宋体'][size=13px]3[/size][/font]——由标准曲线查得或线性回归方程计算的试样中铁的质量,μg;——换算系数取平行测定结果的算术平均值为报告结果,平行测定结果之差的绝对值不大于0.0001%。反应涉及酸碱调节以及化学显色反应,实验操作干扰因素较多,耗时较长。[size=14px]2[/size][size=14px].1.2 [/size][size=14px]电感耦合等离子体原子发射光谱法[/size]ICP-AES具有简便快速、干扰少、重现性高、分析准确度和精密度较高的优点,一般情况下其相对标准偏差≤10%,当分析物浓度超过100倍检出限时,相对标准偏差≤1%。王洪涛等[font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]4][/size][/font]选择238.204 nm的分析谱线进行测定,配制标准曲线,结果与国标标准测定方法基本一致。[size=18px]2[/size][size=18px].2 [/size][size=18px]硫酸盐(以S[/size][size=18px]O[/size][font='宋体'][size=18px]4[/size][/font][size=18px]计)的测定[/size]利用硫酸高沸点原理制得易挥发盐酸是实验室常见的盐酸制取方法,尽管在工业生产中较少使用,但国标也给出了硫酸盐的规定浓度。在大量摄入硫酸盐后出现的最主要生理反映是腹泻、脱水和胃肠道紊乱。将试样蒸发干后,用盐酸溶液溶解残渣,用甘油-乙醇混合液做稳定剂,加入氯化钡制得悬浮液,用分光光度计测定悬浮液吸光度,即可测定硫酸盐的含量。 按表2量取0.1 g/L硫酸盐标准溶液分别置于7个50 mL容量瓶中。向每个容量瓶中加入3 mL1 mol/L盐酸溶液,和5 mL甘油-乙醇混合液,用水稀释至刻度,摇匀后转移至盛有0.3 g BaCl[font='宋体'][size=13px]2[/size][/font]2H[font='宋体'][size=13px]2[/size][/font]O的干燥烧杯中,以2 r/s 的速度摇动2 min,在室温下静置10min。在波长450 nm处测定溶液吸光度。以硫酸盐含量(mg)为横坐标,对应的吸光度为纵坐标绘制标准曲线。[align=center][size=12px]表2[/size][font='宋体'][size=12px][1][/size][/font][size=12px] [/size][size=12px]硫酸盐标准工作曲线[/size][/align][table][tr][td][align=center]硫酸盐标准溶液体积/mL[/align][/td][td][align=center]对应的硫酸盐质量/mg[/align][/td][/tr][tr][td][align=center]0[/align][/td][td][align=center]0[/align][/td][/tr][tr][td][align=center]2.5[/align][/td][td][align=center]0.25[/align][/td][/tr][tr][td][align=center]5.0[/align][/td][td][align=center]0.50[/align][/td][/tr][tr][td][align=center]7.5[/align][/td][td][align=center]0.75[/align][/td][/tr][tr][td][align=center]10.0[/align][/td][td][align=center]1.00[/align][/td][/tr][tr][td][align=center]15.0[/align][/td][td][align=center]1.50[/align][/td][/tr][tr][td][align=center]20.0[/align][/td][td][align=center]2.00[/align][/td][/tr][/table]称取约20 g试样置于蒸发皿中,在水浴上蒸发至干,冷却至室温,加入3 mL盐酸溶液溶解残留物,全部移入50 mL容量瓶中,加入5 mL甘油-乙醇混合液,用水稀释至刻度,摇匀。将试样小心移入盛有0.3 g BaCl[font='宋体'][size=13px]2[/size][/font]2H[font='宋体'][size=13px]2[/size][/font]O的干燥烧杯中,以2 r/s的速度摇动2 min,在室温下静置10 min。在波长450 nm处测定溶液吸光度。同时,要按照与测定试样完全相同的分析步骤、试剂和用量进行空白试验。由下式计算可得:式中:m[font='宋体'][size=13px]5[/size][/font]——由标准曲线查得或线性回归方程计算的试样中硫酸盐的质量,mg;——换算系数;m[font='宋体'][size=13px]4[/size][/font]——试样的质量,g; 取平行测定结果的算术平均值为报告结果,平行测定结果之差的绝对值不大于0.0001%。[size=18px]2[/size][size=18px].3 [/size][size=18px]游离氯(以Cl计)的测定[/size] 当盐酸中含有游离氯(次氯酸、次氯酸根离子,溶解的单质氯)时,使用或处理这类盐酸时,会使其散发出来,增加了生产成本和资源消耗,又对环境造成了污染。 试样溶液加入碘化钾溶液,析出碘,以淀粉为指示剂,用硫代硫酸钠标准滴定溶液滴定游离出来的碘。反应式如下:量取约50 mL试样,置于内装约100 mL水并已称量(精确到0.01 g)的锥形瓶中,冷却至室温,称量(精确到0.01 g)。向试样中加入7 mL碘化钾溶液,塞紧瓶塞摇动,在暗处静置2 min。加入1 mL淀粉指示剂,用硫代硫酸钠标准滴定溶液滴定至溶液蓝色消失为终点。同时,用等量的盐酸替代试样,采用与测定试样完全相同的分析步骤、试样和用量,进行空白试验。由下列公式可得:其中:V[font='宋体'][size=13px]1[/size][/font]——试样滴定消耗的硫代硫酸钠标准滴定溶液的体积,mL;V[font='宋体'][size=13px]0[/size][/font]——空白滴定消耗的硫代硫酸钠标准滴定溶液的体积,mL;1000——换算系数;c——硫代硫酸钠标准滴定溶液的浓度,mol/L;m[font='宋体'][size=13px]6[/size][/font]——试样的质量,g 取平行测定结果的算术平均值为报告结果,平行测定结果之差的绝对值不大于0.001%。 该方法是一种限量分析方法,经典的碘量法测定高纯盐酸中的游离氯误差较大。还可以采用比色法来测定[font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]5][/size][/font]。利用酸性溶液中,游离氯与联邻甲苯胺生成黄色化合物。通过颜色的色度依样品中的游离氯的多少而变化,但目视法误差也较大。[size=18px]2.4 A[/size][size=18px]s的测定[/size] 日常生活中,人们可能通过食物、水源、大气摄入砷。砷及其化合物具有毒性,过量的砷会干扰细胞的正常代谢,损伤小动脉和毛细血管壁,加重脏器损害。由于盐酸生产过程中工艺流程,其中会有少量砷存在。 在酸性介质中,用碘化钾与氯化亚锡将As[font='宋体'][size=13px]5+[/size][/font]还原为As[font='宋体'][size=13px]3+[/size][/font],加锌粒与酸作用,产生新生态氢,使As[font='宋体'][size=13px]3+[/size][/font]进一步还原为砷化氢,被二乙基二硫代氨基甲酸银[Ag(DDTC)]吡啶溶液吸收,生成紫红色胶体溶液,用分光光度计测定吸光度。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107161916577801_1661_1608728_3.png[/img][/align][align=center][size=12px]图1[/size][font='宋体'][size=12px][1][/size][/font][size=12px] [/size][size=12px]定砷器示意图[/size][/align] 按表3量取0.1 g/L硫酸盐标准溶液分别置于6个100 mL容量瓶中。向每个锥形瓶中加入10 mL盐酸,加水至约40mL。量取5mL二乙基二硫代氨基甲酸银吡啶溶液置于图1的c中,并将图1的c与事先放入乙酸铅棉花的b连接好。向每个锥形瓶中依次加入2 mL碘化钾溶液和2 mL氯化亚锡盐酸溶液,混匀后,静置 15min。再加5 g锌粒,每更换一批锌粒或新配制一次二乙基二硫代氨基甲酸银吡啶溶液,应重新绘制标准曲线。按图1迅速连接好仪器,反应45min。在波长540nm处,测定溶液吸光度,以砷含量([font='symbol']?[/font]g)为横坐标,与其对应的吸光度为纵坐标绘制标准曲线。量取10.0 mL试样,称量(精确到0.01g),移至图1a中,加水至约40 mL,进行同样的测定。[align=center][size=12px]表3[/size][font='宋体'][size=12px][1][/size][/font][size=12px] [/size][size=12px]砷标准工作曲线浓度表[/size][/align][table][tr][td][align=center]砷标准溶液体积/mL[/align][/td][td][align=center]对应的砷质量/[font='symbol']?[/font]g[/align][/td][/tr][tr][td][align=center]0[/align][/td][td][align=center]0[/align][/td][/tr][tr][td][align=center]1.0[/align][/td][td][align=center]2.5[/align][/td][/tr][tr][td][align=center]2.0[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]4.0[/align][/td][td][align=center]10[/align][/td][/tr][tr][td][align=center]6.0[/align][/td][td][align=center]15[/align][/td][/tr][tr][td][align=center]8.0.0[/align][/td][td][align=center]20[/align][/td][/tr][/table]由下式计算可得砷的质量分数[font='宋体'][size=13px]6[/size][/font]:其中: m[font='宋体'][size=13px]10[/size][/font]——由标准曲线上查得的或回归方程计算的试样中砷的质量,μg;m[font='宋体'][size=13px]9[/size][/font] ——试样的质量,g;10[font='宋体'][size=13px]6[/size][/font]——换算系数 取平行测定结果的算术平均值为报告结果。平行测定结果之差的绝对值不大于0.00005%。 也可以采用氢化物原子荧光光度法检测[font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]6][/size][/font],通过调节仪器条件,选择适合的参数,通过配置标准曲线,也可得到精确度高的结果。 除上述所提到的杂质检验,国标中还给出了重金属、不溶物的测定。可以看出,国家标准对食品级盐酸的要求之高,这在另一方面也证明国家在食品安全领域的重视程度之高。[font='calibri'][size=21px]3[/size][/font][font='calibri'][size=21px] [/size][/font][font='calibri'][size=21px]应用[/size][/font] 在国际标准分类中,食品级盐酸涉及到纺织产品、饲料、药品、食品原料等方面。盐酸以及其他无机酸口感较苦涩,应用范围相较有机酸较窄。[size=18px]3.1 [/size][size=18px]酸度调节剂[/size] 酸度调节剂,亦称pH调节剂,是用以维持或改变食品酸碱度的物质,具有增进食品质量的许多功能特性,例如改变和维持食品的酸度并改善其风味、增进抗氧化作用、与重金属离子络合组织氧化或褪变反应。根据食品安全国家标准及食品添加剂使用标准中[font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]7][/size][/font]规定,食品级盐酸可用于蛋黄酱、沙拉酱中,最大使用量根据生产需要适量使用。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107161916581277_8632_1608728_3.jpeg[/img][/align][align=center]图2 蛋黄酱[/align][size=18px]3[/size][size=18px].2 [/size][size=18px]食品原料[/size] 食品级盐酸常作为甜味剂原料,比如在阿斯巴甜、果糖、葡萄糖的制备中使用[font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]8][/size][/font]。例如,陈金龙[font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]9][/size][/font]提出一种从甲酸出发的N羰基酸酐法,加入浓盐酸使甜味的α-异构体结晶析出,调节pH后可得到阿斯巴甜。将大豆、玉米等煮沸后,加入盐酸降解,再通过氢氧化钠中和的产品,富含谷氨酸等带有鲜味的氨基酸,可作为许多食品的增味剂[font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]10][/size][/font]。相较于酶解法水解速度较慢、长时间在作用最适温度(40~50℃)下水解、难免污染杂菌,导致水解液变质发臭。而盐酸催化水解则无此类问题,常见工艺为加压法及常压法。在食品添加剂中常用的柠檬酸在酸水解植物蛋白以及酸法水解淀粉制糖方面的应用就逊色于盐酸。[size=18px]3[/size][size=18px].3 [/size][size=18px]药物合成[/size] 盐酸盐药物在日常生活中十分常见。许多药物含有碱性基团,在水中的溶解度与pH有关,用药部位pH值的变化会影响到药物的溶出与吸收,。与盐酸形成盐类化合物后,在一定pH范围内,盐的溶解度是不变的,这样药物才能发挥出确切的疗效。因为盐酸盐具有在各种盐中的溶解度高,氯离子毒性低,成盐后还能改善药物分子的微环境,提高药物的稳定性等优点。同时因为其便宜易得,易于放大生产,所以食品级盐酸常用于药物合成中。[size=18px]3[/size][size=18px].4 [/size][size=18px]盐酸湿法磷酸工艺[/size][font='宋体'][size=18px][[/size][/font][font='宋体'][size=18px]11][/size][/font] 磷酸是一种重要的化工原料,食品级磷酸常用于制备食品添加剂、饲料添加剂、牙膏摩擦剂等方面。自二十世纪60年代初,以色列矿业工程公司提出IMI湿法磷酸工艺,实现了盐酸法湿法磷酸工艺的工业化。李军[font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]12][/size][/font]等利用食品级盐酸分解磷矿,并进行一系列后处理,浓缩制得的H3PO4品质高,无需净化既可用于食品工业。[size=18px]4[/size][size=18px] [/size][size=18px]总结[/size] 本文针对食品级盐酸的理化性质、杂质的检测、应用等方面进行了讨论,可以发现盐酸由于酸性强、腐蚀性强的特性,单独作为食品添加剂较少,但在药物合成、磷酸工业中应用广泛。近年来,我国氯碱工业发展迅速,副产品盐酸供大于求,因此如何解决盐酸应用问题是解决我国产能问题的一大关键。[font='arial'][size=18px][color=#000000]参考文献:[/color][/size][/font][font='times new roman'][size=12px][color=#000000][[/color][/size][/font][font='times new roman'][size=12px][color=#000000]1]GB 1886.9-2016 [/color][/size][/font][font='times new roman'][size=12px][color=#000000]食品安全国家标准 食品添加剂 盐酸[/color][/size][/font][font='times new roman'][size=12px][color=#000000][2]陈允冀,卓秀容.工业级盐酸用离子交换法提纯成食品级盐酸[J].中国氯碱,1994(12):26-27.[/color][/size][/font][font='times new roman'][size=12px][color=#000000][[/color][/size][/font][font='times new roman'][size=12px][color=#000000]3]GB 1897-1995 [/color][/size][/font][font='times new roman'][size=12px][color=#000000]食品添加剂 盐酸[/color][/size][/font][font='times new roman'][size=12px][color=#000000][4]汪洪涛,朱婕妤,洪华.电感耦合等离子体原子发射光谱法在工业用合成盐酸中铁元素测定中的应用[J].江苏科技信息,2021,38(16):51-53.[/color][/size][/font][font='times new roman'][size=12px][color=#000000][5]姜新其.高纯盐酸中游离氯测定方法比较[J].中国氯碱,2003(08):31-33+44.[/color][/size][/font][font='times new roman'][size=12px][color=#000000][6]朱国英.AFS-3100型原子荧光光谱仪测定食品中的砷[J].现代农业科技,2016(10):261-262.[/color][/size][/font][font='times new roman'][size=12px][color=#000000][[/color][/size][/font][font='times new roman'][size=12px][color=#000000]7] GB 2760-2014 食品安全国家标准 食品添加剂使用标准[/color][/size][/font][font='times new roman'][size=12px][color=#000000][[/color][/size][/font][font='times new roman'][size=12px][color=#000000]8] [/color][/size][/font][url=https://baike.baidu.com/item/%E5%B7%A5%E4%B8%9A%E7%9B%90%E9%85%B8/1151658][font='times new roman'][size=12px][color=#000000]https://baike.baidu.com/item/%E5%B7%A5%E4%B8%9A%E7%9B%90%E9%85%B8/1151658[/color][/size][/font][/url][font='times new roman'][size=12px][color=#000000][9]陈金龙. 阿斯巴甜的合成[D].浙江工业大学,2006.[/color][/size][/font][font='times new roman'][size=12px][color=#000000][10][/color][/size][/font][url=http://wiki.cnki.com.cn/HotWord/5618241.htm][font='times new roman'][size=12px][color=#000000]http://wiki.cnki.com.cn/HotWord/5618241.htm[/color][/size][/font][/url][font='times new roman'][size=12px][color=#000000][11]王斌,张宗凡,罗康碧,罗珍.盐酸法湿法磷酸工艺研究现状[J].化学工程师,2014(08):46-49.[/color][/size][/font][font='times new roman'][size=12px][color=#000000][12]李军,金央,罗建洪,周堃,唐湘,王涛,李维. 盐酸分解中低品位磷矿制备工业级和食品级磷酸的方法[P]. 四川:CN101774556A,2010-07-14.[/color][/size][/font]
[color=#444444]请问[/color][color=#444444]GB/T5009.84-2003 [/color][color=#444444]食品中硫胺素(维生素[/color][color=#444444]B1[/color][color=#444444])的测定中所用的硫胺素标准品指的是硝酸硫胺素还是盐酸硫胺素?这两种标准品都有的卖。[/color][color=#444444]但就是找不到[/color][color=#444444]“[/color][color=#444444]硫胺素[/color][color=#444444]”[/color]
[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]检测环丙沙星,但标准品买的是盐酸环丙沙星,在配置时需要扣掉盐酸的质量吗?另外我用乙腈溶解发现溶解后的溶液白色浑浊,很多白色的悬浮物,加100ul甲酸后仍然浑浊,老师们有遇到过这种情况吗?
请教一下大家,原子荧光做锡的话酸度影响大吗,还有用盐酸跟硫酸有很大区别吗,我看国标里面几乎不加酸的啊
实验室要用ICP-MS测食品中的铝,我找到了一瓶水中铝的单标,发现瓶上注明基质5%盐酸,考虑盐酸对ICP-MS有影响,于是我就降低酸度用2%的盐酸配制了标准溶液,划完曲线线性系数3个9,不知道这样做到底对不对?
我们参加能力验证 元素铜(Cu)[size=3][font=宋体],样品介质为盐酸([/font][/size][size=3][font='Times New Roman']HCl[/font][/size][size=3][font=宋体])[/font][/size][size=3][font='Times New Roman']5%[/font][/size][size=3][font=宋体]溶液,而我们的标准储备液是1000mg/L,1%硫酸.用它分析[size=2][font=Arial]能力验证样品影响大吗?[/font][/size][/font][/size]
大家好 请教个问题 我做液相色谱分析标准曲线,用邻氯苯胺盐酸盐做标准曲线,但是样品是邻氯苯胺硫酸盐,怎么计算邻氯苯胺的含量?谢谢
今天带新人做实验,标定硫代硫酸钠溶液,结果浓度为0.25mol/L,不是配制的0.1mol/L,称量肯定没有问题。分析原因:硫代硫酸钠用量偏低,造成的原因应该是碘没有完全析出。因为称量没有问题,那只能是酸度不够。一看他给我的标准附录,盐酸前后浓度不对,应该是1mol/L,他按0.1mol/L配制的。下面是我截选的标准附录部分------------------------------------------------------------------------------------附录A硫代硫酸钠标准溶液制备及标定方法 A.1.2 0.1mol/L盐酸溶液:量取82ml浓盐酸加水稀释至1000ml。 ---------------------------------------------------------------------------------------分析:量取82ml浓盐酸加水稀释至1000ml,其浓度应该为:82*1.15*(36%~38%)/36.5=(0.93~0.98)mol/L
各位老师,关于71-3中0.07mol/L 的盐酸标定,有国标标准时说关于盐酸标定的么?
我们实验室有一台雷磁PHSJ-3F型实验室pH计,以前工作一切正常。最近不知怎么回事,使用新配制的缓冲溶液校准时出了毛病。使用pH为4.00的缓冲液校准时,屏幕显示4.25~4.30;使用pH为9.18的缓冲液校准时,屏幕显示9.27~9.35;斜率为98.6%,无论过多长时间,校准的数值都在以上范围内,按下确定键后,数值回到4.00(即校准时显示4.30,按下确定后显示4.00,同理9.35时按下确定后显示9.18)校准以后,回过头来测量pH为4.00的缓冲液时,测量值为4.00.pH为9.18的缓冲液测量值为9.18.请问这台酸度计出了什么毛病?如果这台酸度计测量pH时,测量的结果是偏高还是偏低?怎么才能让它回到正常状态?另:使用此酸度计测量pH时,比如说我需要把溶液调至2.50,测量值为2.17,于是向溶液中加盐酸或硝酸,边搅拌,边测量。搅拌的时候酸度计显示为2.50时,停止搅拌,静止以后,却下降到2.30左右。请问在这种情况下到底是以搅拌时测得的pH为准还是静止时测得的pH为主?实验室用水为(一次蒸馏水)
谁有YS/T 239.5-1994 三硫化二锑化学分析方法 重量法测定盐酸不溶物标准,请上传一下进行分享。
一 酸度调节剂Acidity regulator酸度调节剂,或PH值控制剂,是用来调整或保持PH值(酸或碱)的一种食品添加剂。酸度调节剂可以是有机酸或无机酸、碱、中和剂或缓冲剂。酸度调节剂由其E编码标识,如E260(乙酸),或列在“食品酸度剂”下。经常使用的酸度调节剂是柠檬酸,乙酸和乳酸。碳酸钠、碳酸钾可用于面制食品中,盐酸、氢氧化钠属于强酸、强碱性物质,其对人体具有腐蚀性,只能用作加工助剂,要在食品完成加工前予以中和。简介 酸度调节剂亦称pH调节剂,是用以维持或改变食品酸碱度的物质。它主要用以控制食品所有需的酸化剂、碱剂以及具有缓冲作用的盐类。 酸化剂具有增进食品质量的许多功能特性,例如改变和维持食品的酸度并改善其风味;增进抗氧化作用,防止食品酸败;与重金属离子络合,具有阻止氧化或褐变反应、稳定颜色、降低浊度、增强胶凝特性等作用。酸化剂均有—定的抗微生物作用,尽管单独用酸来抑菌,防腐所需浓度太大,影响食品感官特性,难以实际应用,但是当以足够的浓度,选用一定的酸化剂与其他保藏方法如冷藏、加热等并用,可以有效地延长食品的保存期。至于对不同酸的选择、取决于酸的性质及其成本等。 酸味的刺激阈值用pH值来表示,无机酸的酸味阈值在3.4~3.5左右,有机酸的酸味阈值在3.7~4.9之间。大多数食品的pH值在 5~6.5之间,虽为酸性,但并无酸味感觉,若pH值在3.0以下,则酸味感强,难以适口。 酸度调节剂其有效应用主要受食品所需特性控制,通常以有机酸及具有缓冲作用的盐为主。又由于很多有机酸都是食品的正常成分,或参与人体正常代谢,因而安全性高,使用广泛。我国批准许可使用的酸度调节剂品种不少。但是,与国外许可使用的同类品种相比尚有一定差距。主要是缺少各种有机酸的盐。不过,当前重要的是加强应用开发,应尽量利用现有品种,针对不同食品原料,研制出具有各自不同风味特点而受人欢迎的食品。基本介绍 酸度调节剂为增强食品中酸味和调整食品中pH或具有缓冲作用的酸、碱、 盐类物质总称。规定允许使用的酸度调节剂有柠檬酸、柠檬酸钾、乳酸、酒石酸等17种,其中柠檬酸为广泛应用的一种酸味剂。柠檬酸、乳酸、酒石酸、苹果酸、柠檬酸钠、柠檬酸钾等均可按正常需要用于各类食品。 酸度调节剂亦称pH调节剂,是用以维持或改变食品酸碱度的物质。它主要有用以控制食品所需的酸化剂、碱剂以及具有缓冲作用的盐类。酸化剂具有增进食品质量的许多功能特性,例如改变和维持食品的酸度并改善其风味;增进抗氧化作用,防止食品酸败;与重金属离子络合,具有阻止氧化或褪变反应、稳定颜色、降低浊度、增强胶凝特性等作用。酸均有一定的抗微生物作用,尽管单独用酸来抑菌,防腐所需浓度太大,影响食品感官特性,难以实际应用,但是当以足够的浓度,选用一定的酸化剂与其他保藏方法如冷藏、加热等并用,可以有效地延长食品的保存期。至于对不同酸的选择,取决于酸的性质及其成本等。 酸度调节剂除可使用的酸度调节剂品种不少。但是,与国外许可使用的同类品种相比尚有一定差距,主要是缺少各种有机酸的盐。不过,当前重要的是加强应用开发,应尽量利用现有品种,针对不同食品原料,研制出具有各自不同风味特点,受人欢迎的加工食品。酸度调节剂除可调节食品的pH、控制酸度、改善风味之外,尚有许多其他功能特性。其有效应用主要受食品所需特性控制,通常以有机酸及具有缓冲作用的盐为主。又由于很多有机酸都是食品的正常成分,或参与人体正常代谢,因而安全性高,使用广泛。性质介绍 又称pH值调节剂。是用以维持或改变食品酸碱度的物质。主要有用以控制食品所需的酸化剂、碱剂以及具有缓冲作用的盐类。酸化剂具有增进食品质量的特性,如改变和维持食品的酸度并改善其风味;增进抗氧化作用,防止食品酸败;与重金属离子络合,具有阻止氧化或褐变反应、稳定颜色、降低浊度、增强胶凝特性等作用。酸均有一定的抗微生物作用,选用一定的酸化剂与其他保藏方法如冷藏、加热等并用,可以有效地延长食品的保质期。种类介绍 已批准许可使用的酸度调节剂有: 卫生标准 酸度调节剂 范围 本标准规定了食品添加剂的品种,使用范围及使用量。 酸度调节剂原理本标准适用于1995年、1996年度申请单位申报的新增食品添加剂的使用卫生标准以及某些现有品种的扩大使用范围。 标准为GB2760—1996《食品添加剂使用卫生标准》的续篇。 引用标准 下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。本标准出版时,所示版本均有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。 GB2760一1996食品添加剂使用卫生标准 GBl2493—1990食品添加剂分类和代码 GBl4880—1994食品营养强化剂使用卫生标准 编辑本段实际运用 南京国海生物工程有限公司作为全国最大的DL-苹果酸制造商,市场份额占66%,产品技术指标达到甚至部分指标优于国际相关标准规定,但由于种种原因,在去年国家标准化管理委员会公布的国家标准立项计划中,《食品添加剂DL-苹果酸》国家标准话语权“花落旁家”,国海生物公司无缘参与。标准话语权的丧失将对国海生物公司的技术研发、生产控制、成品质量和销售等造成严重影响,很大程度制约着企业发展。得知消息后,标准化处与六合分局第一时间深入企业分析原因、查找问题,多次与全国有机化学标准化技术委员会协调沟通,并率企业赴北京向国家标准委和行业主管部门汇报情况、积极磋商,取得了国标委和行业的了解和支持,国海生物公司被批准为《食品添加剂DL-苹果酸》国家标准主导研制单位。6月19日,该国家标准行业预审会在六合成功举行,标志着我市又一重点项目关键技术夺回标准话语权。 随着《食品添加剂DL-苹果酸》国家标准的研制成功,DL-苹果酸作为食品添加剂中的一种酸度调节
实验室盐酸标准溶液通常都是用玻璃瓶来装的,如果配好的标准溶液需要搬到其它实验室用,为了搬运过程安全,可以用塑料壶来装吗?
原料药盐酸米多君标准(国内:YBH09452006),5-氨基乙酰丙酸盐酸盐标准。若有特殊要求也可站内信息联系!有国外标准也行。
原子荧光测镉时使用液稀释问题镉储备液用盐酸稀释会有很大影响吗?镉在高盐酸酸度下会不会形成不易生成氢化物的化合物那?镉在什么介质中即稳定有益与原子荧光的发生?
标定盐酸标准滴定溶液的不确定度分析 作者:吴文英 张春雨 唐惠兰 来源:中华医学研究杂志 在理化分析过程中,一切测量结果都不可避免地具有不确定度。盐酸标准溶液是常用化学定量参比物质,其标定值的准确性直接影响常规分析质量。笔者以GB/T601《滴定分析(容量分析)用标准液的制备》为依据配制并标定盐酸根据JJF1059-1999《测定不确定度评定与表示》分析其测量不确定度。简述由标定过程中得到的不确定度。 1 实验部分 1.1 测定方法[1,2] 准确称量270℃~300℃干燥至恒重的基准碳酸钠(99.95%~100.05%)约0.2g左右,电子分析天平(精度为0.1mg),置于三角瓶中,加入50ml水使之溶解,加指示剂,用盐酸标准液滴定至终点同时作试剂空白实验。 1.2 主要计量仪器与试剂 电了分析天平:AG204;酸式滴定管:50ml A级。 1.3 建立数学模型 C=m (V1-V2)×0.05300 式中 C:盐酸标准滴定溶液的浓度(mol/L);m:基准无水碳酸钠的质量(g);V1:盐酸标准滴定溶液用量(ml);V2:试剂空白实验中盐酸标准滴定溶液用量(ml);0.05300:与1.00ml盐酸标准溶液[C(HCl)=1.000mol/L]相当于以克表示的无水碳酸钠的质量。 1.4 盐酸标准滴定溶液的标定结果 为获得标准溶液重复测量的不确定度分量,对同一标准溶液进行8次独立的标定。测定数据见表1。 表1 盐酸标准滴定溶液的标定结果 略 2 测量不确定度来源 从检测过程和数学模型分析,标定盐酸标准溶液的不确定度主要来源,由四个方面所引起。(1)测量的重复性(A类不确定度);(2)基准无水碳酸钠的纯度;(3)测量使用的电子分析天平及量具;(4)其他相关常数。 3 测量不确定度分析 3.1 A类不确定度的分析 利用表1中的测量结果,按照A类评定测量重复性的标准不确定度。具体计算过程:重复测量的平均值计算式:=1 n∑8 i=1xi=0.09951mol/L 单次测量的标准差按贝塞尔公式计算s(x)为 s(x)=∑8 i=1(xi-)2 n-1=0.0001555mol/L 的标准差s()为 s()=s(x) n=0.000155 8=0.0000548mol/L=5.48×10-5mol/L 由测量重复性引起的相对标准不确定度为U(x):0.0000548/0.09951=0.055%。 3.2 B类不确定度分析 3.2.1 基准碳酸钠的纯度 基准碳酸钠的纯度为1.0000±0.0005,视为矩形分布0.00053=0.00029,则标准不确定度为:由基准碳酸钠的纯度引入的相对不确定度u(p)为:0.029%。 3.2.2 天平称量所引入的标准不确定度 干燥器与天平称量仓内均放置同质硅胶,视为相同湿度,称量时无吸潮。电子天平检定证书标出线性为上0.2mg;可视为矩形分布,则标准不确定度为:因为称量采用的是减量法,故称量的标准不确定度为0.2mg /3=0.12mg:因为称量采用的是减量法,故称量的标准不确定度为:2×0.122=0.17mg,则由称量引入的相对标准不确定度u(m)为:0.17mg/0.2018g=0.084%。 3.2.3 标定体积的不确定度 (1)滴定管的校准:滴定使用50ml酸式滴定管(A级),按照检定规程,其最大允许误差为±0.05ml,相对允许误差为±0.1%,按照矩形分布,则滴定体积的相对标准不确定度u(V)为:u(V)=0.1%/3=0.0577%。(2)环境温度:实验环境在空调条件下,室温近似20℃。温度在20℃左右,标准溶液的温度补正值非常小,对实验结果影响可忽略不计,所以在不确定度分析中不把一温度影响引起的不确定度列入考虑范围。(3)滴定终点的判断:终点时的误差±0.05ml(1滴的体积),两点分布,现由终点分布判断引入的标准不确定度为0.05ml:相对标准不确定度为0.05ml/38.32ml=0.13%标定体积的影响引入相对标准不确定度U(V)为0.0572+0.132=0.142%。 3.2.4 其他常数 基准无水碳酸钠摩尔质量引起的标准不确定度很小,可以忽略。 4 合成标准不确定度 测量重复性、基准无水碳酸钠的纯度、天平称量、标定体积等的不确定度相互独立,故将上述数据合成得盐酸的相对合成标准不确定度U(C)为0.0552+0.0292+0.0842+0.1422=0.176%。 5 扩展不确定度 实验测得盐酸标准溶液浓度为0.09951mol/L,则测量结果的合成标准不确定度U(C)=0.09951mol/L×0.176%=0.000175mol/L。若取包含因子K=2,得测量结果的扩展不确定度U=2U(C)=0.00035mol/L。 6 测量结果的表示 盐酸标准滴定溶液的浓度可表示为:(0.09951±0.00035mol/L,K=2)。 【参考文献】 1 姚正堂,将已峰.奶制品中蛋白质测定的不确定度分析.中华医学研究杂志,2005,5(6):6. 2 国家技术监督局.JJF1059-1999测量不确定度与表示.北京:中国计量出版社,1997,81. 作者单位: 214171 江苏无锡,无锡市惠山区疾病预防控制中心
1.我在容量瓶里面加入了10ml盐酸,定容25ml,然后高温煮到还剩下1ml,这个时候盐酸都被浓缩了吗?我在定容25ml,还是跟之前一样的酸度吗?不太懂酸度的概念……2.我溶解样品的时候用了10ml盐酸,定容100ml,那我标准曲线也是加入10ml盐酸定容比较好吗?