请问各位高手有没有叔丁醇锂的国标,行业标准也行,谢谢!
哪位知道国产的异丁醇,异戊醇标准品哪有?
各位大大,本人现在正在做一个冻干制剂的叔丁醇残留检测,标准上规定用PEG20000为固定液的柱子,但未指定品牌和型号,我这里刚好有一根HP-INNOWAX的柱子,就试着做了一下,结果发现出峰时间在1分半钟左右,而且进的几个不同叔丁醇标准液的浓度和它们的峰面积基本呈线性。但是我觉得保留时间这么短,又有些担心,比如死时间出峰什么的。所以想问下各位,有没有人做过类似叔丁醇残留测定的,柱子是HP-INNOWAX或者DB-WAX的,这么短的保留时间能不能用。还有个问题,标准上规定的载气流量是以“毫升每分钟”记的,但是我们这的岛津GC上面只有载气压力显示,要是想换算成流量,应该怎么弄啊。 (本人是新手,还请各位多多帮忙,谢谢)
[color=#444444]本人现在正在做一个冻干制剂的叔丁醇残留检测,标准上规定用PEG20000为固定液的柱子,但未指定品牌和型号,我这里刚好有一根HP-INNOWAX的柱子,就试着做了一下,结果发现出峰时间在1分半钟左右,而且进的几个不同叔丁醇标准液的浓度和它们的峰面积基本呈线性。但是我觉得保留时间这么短,又有些担心,比如死时间出峰什么的。所以想问下各位,有没有人做过类似叔丁醇残留测定的,柱子是HP-INNOWAX或者DB-WAX的,这么短的保留时间能不能用。还有个问题,标准上规定的载气流量是以“毫升每分钟”记的,但是我们这的岛津GC上面只有载气压力显示,要是想换算成流量,应该怎么弄啊。[/color]
【求助】GC测定叔丁醇残留用什么气相色谱柱各位大大,本人现在正在做一个冻干制剂的叔丁醇残留检测,标准上规定用PEG20000为固定液的柱子,但未指定品牌和型号,我这里刚好有一根HP-INNOWAX的柱子,就试着做了一下,结果发现出峰时间在1分半钟左右,而且进的几个不同叔丁醇标准液的浓度和它们的峰面积基本呈线性。但是我觉得保留时间这么短,又有些担心,比如死时间出峰什么的。所以想问下各位,有没有人做过类似叔丁醇残留测定的,柱子是HP-INNOWAX或者DB-WAX的,这么短的保留时间能不能用。还有个问题,标准上规定的载气流量是以“毫升每分钟”记的,但是我们这的岛津GC上面只有载气压力显示,要是想换算成流量,应该怎么弄啊。 (本人是新手,还请各位多多帮忙,谢谢)
本人要测定叔丁醇中的纯度,找了很久都有找到如题标准,那位好心人支持一下,万分感谢!
三氧化二铝柱能不能进醇类?我想知道丁醇在三氧化二铝柱中的出峰位置,怎么实现?
分析二甲基丁醇,三甲基丁醇,样品浓度大约为99%。请教分析方法及使用何种色谱柱?谢谢了!![em58]
测四氟丙醇中的杂质叔丁醇的含量。因为现有两台[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]GC979/GC1690,手动进样0.8UL,都是FID。柱子都是兰化所的1701毛细柱。分析同一个样品,总峰面积1690为1080W,9790的为998W,结果1690那台叔丁醇的含量是9790的两倍,做了3次试验都是一样情况。两台色谱的载气,空气,氢气的流速都一样。不知道怎样才能确定哪个是准确的。是不是用内标?本人接触色谱不久对内标不是很懂,对叔丁醇选什么内标物好?内标物是不是要特别买?我看试剂的含量都是个范围。

目前,许多国家规定,凡结构中具有不对称因素的药物,即“手性药物”,必须拆分其相应的立体异构体,并分别研究其药理、毒理和药物代谢性质。对已上市的消旋体药物,要重新评价其光学异构体的性质。对新申报的药品,一开始就要合成其光学异构体。这就要求我们在产品质量控制过程中,开发相应的光学异构体分离方案。 现大家常用HPLC来进行分离,色谱柱是一部分因素,但是色谱条件的选择,对分离的影响非常大。通常会首先正相条件来进行分离,使用的流动相含有烷烃(正己烷、正戊烷)以及醇类(异丙醇、乙醇、甲醇、叔丁醇),现通过一个案例看叔丁醇在手性分离中的应用。 项目名称是:[b][i]替格瑞洛[/i][/b],结构式分别如下:[img=,416,254]http://ng1.17img.cn/bbsfiles/images/2017/08/201708222022_01_1708019_3.png[/img][img=,374,252]http://ng1.17img.cn/bbsfiles/images/2017/08/201708222023_01_1708019_3.png[/img][img=,388,272]http://ng1.17img.cn/bbsfiles/images/2017/08/201708222023_02_1708019_3.png[/img] 接下来的就是选柱子、选方法了: 当然,开始从正相条件入手,选择了常规的两款多糖涂覆型手性柱:[b]月旭Ultimate Cellu-D(4.6×250mm,5μm)与月旭Ultimate Amy-D(4.6×250mm,5μm)[/b]开始测试。流动相选择了:[b]正己烷:乙醇=90:10[/b],测试效果如下: [img=,690,299]http://ng1.17img.cn/bbsfiles/images/2017/08/201708222030_01_1708019_3.png[/img] [img=,690,301]http://ng1.17img.cn/bbsfiles/images/2017/08/201708222031_01_1708019_3.png[/img] 结果分离效果均不理想,接下来用这两款柱子,醇类选择异丙醇和乙醇按不同比例来测试,均达不到分离要求,但是明显在[b] [/b]Amy-D的分离效果更好,所以后续方法的调整均在Amy-D柱上进行测试; 接下来怎么办呢,试试两种醇混合使用,看看效果: [img=,690,289]http://ng1.17img.cn/bbsfiles/images/2017/08/201708222036_01_1708019_3.png[/img] 上图是使用流动相:[b]正己烷:甲醇:乙醇=90:10:10[/b]来进行分离,结果三个物质均露面了,但是但是还是达不到分离要求,而且降低醇类的比例,也无法实现分离; 哎,看来正相体系是没有办法了,只能再试试模式了。现在[b]极性溶剂模式[/b]也是常用的一种模式,这种模式是使用100%的醇类或两种醇类混合使用,通常用于常规模式分离不理想的时候的一种选择吧!!! 先用[b]甲醇:异丙醇=80:20[/b]开始,出图先: [img=,690,192]http://ng1.17img.cn/bbsfiles/images/2017/08/201708222043_02_1708019_3.png[/img] 分离不开,不行再来,用[b]甲醇:乙醇=90:10:[/b] [img=,690,241]http://ng1.17img.cn/bbsfiles/images/2017/08/201708222045_01_1708019_3.png[/img] 结果三个物质均出现,两个杂质分别在主峰的前后,也达不到基线分离。 继续:100%甲醇、100%乙醇、100%乙腈。。。。。。还是分离不开,咋办。唉这时候已经想选择放弃,通过两个方法,杂质A与杂质B分别控制。 听说有些极端情况下,可以试试叔丁醇呢,那加点叔丁醇试试吧,结果在[b]甲醇:叔丁醇 = 78 : 22[/b]条件下,使用[b]Amy-D(4.6×250mm,5μm)[/b]分析,各个物质均达到基线分离,且杂质A与杂质B均在主峰之前出峰,是不是都是我们希望的,按照要求配置一个系统适应性溶液测试: [img=,690,321]http://ng1.17img.cn/bbsfiles/images/2017/08/201708222048_01_1708019_3.png[/img] 分析条件初步完成,接下来么,就是方法验证了,就不再一一列举了。 所以在进行手性分析时,当遇到分离度不合适,或者样品在烷烃中的溶解性不好以及难以洗脱的样品时,可以试试极性溶剂模式来进行分离,同时因为手性分离,不同醇类,会出现不同的分离效果,而甲醇、叔丁醇也可以当做添加剂的形式,配合其他醇类用于手性分离,有时候会出现意想不到的效果。
同为极性柱子,为什么乙醇叔丁醇在PEG20M的柱子上乙醇出峰在前,FFAP的柱子顺序相反呢?
叔丁醇锂游离碱分析方法我要分析叔丁醇锂游离碱含量,请问有谁知道,请赐教
[em0808] 我做了个酯化反应,正丁醇和乙酸的,然后想用GC-MS检测它们反应进行的程度我用的是外标法,然后刚才结果出来了,连续三个小时内,正丁醇峰面积几乎没有变化,但是产物确实越来越多,怎么会这样?理论上正丁醇峰也该减少才是。另外,我在做标准样品时,用的配比就是反应初始配比5ml:32ml=乙酸:正丁醇。但是这个标样的峰面积也会变化,上周测的都在4,000,000左右,这周测的几个都在4,650,000左右。。。这是为什么呢?
安捷伦7890A,顶空自动进样器,19091S-510色谱柱检测乙醇,叔丁醇內标,以前都正常乙醇保留时间为1.2分钟,叔丁醇3.3分钟,现在突然叔丁醇0.6分钟就出峰了,请问一下是什么原因呢?
(应助版友在其他版面的标准求助)GB 10618-1989 食品添加剂 正丁醇1990-02-01实施,改号调整为HG 2926-1989。HG 2926-1989(1997年确认) 食品添加剂 正丁醇1990-02-01实施,现行有效。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=118515]GB 10618-1989 食品添加剂 正丁醇(调整为HG 2926-1989)[/url]GB 11962-1989 食品添加剂 丁酸1990-09-01实施。改号调整为QB/T 2796-2006。QB/T 2796-2006 食品添加剂 丁酸2006-10-11实施,现行有效。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=118516]GB 11962-1989 食品添加剂 丁酸(调整为QB/T 2796-2006)[/url]
正丁醇部位的分离是天然药物化学专业分离较难的部分,但分到有价值的东西几率较大,所以值得我们为之一搏。 一般来说,正丁醇部位常含有单糖、二糖等小分子糖,多种酚类化合物,以及苷类化合物,极性较大,在硅胶柱上吸附较多,成点性差,分离效果不好。因此,一般说来,对于正丁醇部位可采取以下方法: 1. 大孔树脂柱砍段。 样品水溶解后上样,依次用水,30%、60%、95%乙醇溶液洗脱,分别合并、收集。一般说来目标化合物多在60%段,水,30%段多为一些水溶性单糖、二糖及多酚类化合物,可以考虑弃去。而95%部分多和乙酸乙酯部位大极性段重叠,可以乙酸乙酯部位合并处理。 2. 反相柱分段。 如果正丁醇部位量不是太大,或者课题组有大反相柱,可以考虑用反相柱砍段。本课题组就有一根500g的反相柱,专门用于砍段,效果比正相柱好了许多。唯一需要提醒注意的是,由于我们一般是用正相硅胶板检测化合物分离情况,所以反相柱 砍段后往往各组份在硅胶板上看起来比较混乱,不如硅胶柱砍段后那么直观,一定要小心对比,否则会越分越乱。 3.正相柱分配色谱层析。 如果正丁醇部位量太大,或者课题组没有大的相柱用来分段,那么可以考虑氯仿:甲醇:水 体系来砍段。我一般用8:2:1、7:3:1以及6.5:3.5:1依次洗脱,效果不会很好,但两到三次反复上柱后各部分还是可以看得到点的。这时再会反相柱细分,拿十到二十个点应该没问题的。 总体来说,这部分较难,但等你分到好东西了,难也值得,小小经验和大家分享,祝大家实验顺利!
[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]校验时精密度太差是什么原因,FID检测器,PEG-20M柱,标准品异丁醇浓度1mg/ml
用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]检测叔丁醇中水,怎么配置标液
五种混标用二硫化碳溶解,毛细管柱为安捷伦DB1701,进样口温度250,检测器250,柱温35,程序升温至150,结果只检出甲醇,正丁醇,异戊醇。而乙二醇,异丙醇未检出,是我的仪器条件设置问题吗?求教!
各位大神好,大家有用GC-MS测试叔丁醇的吗?色谱柱如何选择?[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]和质谱条件设定要注意些什么?谢谢!
最近接到任务要检测公司一产品中过氧化叔丁醇残余量,本人接触色谱时间不长,知识有限,感觉无从下手,请各位大虾给些指导,不胜感激。
水、叔丁醇、己烷的分离条件是什么?用什么色谱柱比较合适呢?
国标乳品中碘的测定中,在硫酸条件下碘与丁醇反应生成丁醇与碘的衍生物,到底此衍生为何物?
我用的极性柱测甲醇丁醇乙醇异丙醇只出三个峰,50度的程序升温,这是什么原因呢
请问,有没有人用Q柱测过叔丁醇,水,我这边测试只出水峰,检测器是TCD,是水,正己烷,仲丁醇,叔丁醇的混合物
问题描述:本人新买了有机锡的标准品一氯三丁基锡 CISn(C4H9)3,配制成工作液后加内标衍生,衍生产物为乙基三丁基锡C2H5Sn(C4H9)3 (TBT),走GC-MS,发现会出二乙基二丁基锡 (C2H5)2Sn(C4H9)2 (DBT).疑问:1:这个标准是不是存在分解,如果存在,分解发生在那个步骤,是标准配制还是要衍生或是进样口。2:因为多出的目标物(DBT)也是我们的检测目标物,这样就存在定量的问题,TBT偏小。DBT偏高。我把谱图发上来大家看下
请问各位老师,《环境空气和废气 臭气的测定 三点比较式臭袋法》里面的臭气浓度为20.3、305、2000的正丁醇统一样品,其几个浓度是怎么配制出来的?
正丁醇和丁醇是一样的吗?
[size=5]GB 10618-89 食品添加剂 正丁醇[/size]
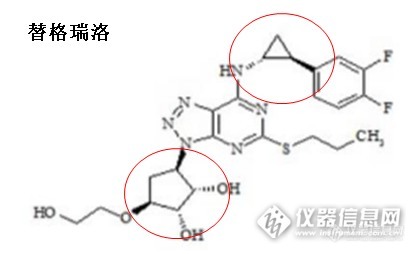
目前,许多国家规定,凡结构中具有不对称因素的药物,即“手性药物”,必须拆分其相应的立体异构体,并分别研究其药理、毒理和药物代谢性质。对已上市的消旋体药物,要重新评价其光学异构体的性质。对新申报的药品,一开始就要合成其光学异构体。这就要求我们在产品质量控制过程中,开发相应的光学异构体分离方案。 现大家常用HPLC来进行分离,色谱柱是一部分因素,但是色谱条件的选择,对分离的影响非常大。通常会首先选择正相条件来进行分离,使用的流动相含有烷烃(正己烷、正戊烷)以及醇类(异丙醇、乙醇、甲醇、乙腈),现通过一个案例看叔丁醇在手性分离中的应用。 项目名称是:替格瑞洛,结构式分别如下: [img=,286,223]http://ng1.17img.cn/bbsfiles/images/2017/08/201708250816_01_1708019_3.png[/img] [img=,297,222]http://ng1.17img.cn/bbsfiles/images/2017/08/201708250817_01_1708019_3.png[/img] [img=,310,222]http://ng1.17img.cn/bbsfiles/images/2017/08/201708250818_01_1708019_3.png[/img] 接下来就是选柱子,选方法了: 当然,开始先从正相条件入手,选择了常规的两款多糖涂覆型手性柱:月旭Ultimate Cellu-D(4.6×250mm,5μm)与月旭Ultimate[b] [/b]Amy-D(4.6×250mm,5μm)开始测试。流动相选择了:正己烷:乙醇=90:10,测试效果如下:[img]http://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img] [img=,690,299]http://ng1.17img.cn/bbsfiles/images/2017/08/201708250820_01_1708019_3.png[/img] [img=,690,301]http://ng1.17img.cn/bbsfiles/images/2017/08/201708250820_02_1708019_3.png[/img] 结果分离效果均不理想,接下来用这两款柱子,醇类选择异丙醇和乙醇按不同比例来测试,均达不到分离效果,但是明显在Amy-D柱上的分离效果更好,所以后续方法的调整均在Amy-D柱上进行测试; 再接下来怎么办呢,试试两种醇混合使用,看看效果: [img=,690,289]http://ng1.17img.cn/bbsfiles/images/2017/08/201708250821_01_1708019_3.png[/img] 上图是使用流动相:正己烷:甲醇:乙醇=90:10:10来进行分离,结果三个物质均露面了,但是但是还是达不到分离的要求,而且降低醇类的比例,也无法实现完全分离。 哎,看来正相体系是没有办法了,只能再试试别模式了。现在极性溶剂模式也是常用的一种模式,这种模式是使用100%的醇类或两种醇类混合使用,也算是常规模式分离不理想情况下的一种选择吧!!! 先用甲醇:异丙醇=80:20开始,出图先: [img=,690,192]http://ng1.17img.cn/bbsfiles/images/2017/08/201708250822_01_1708019_3.png[/img][img]http://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img] 分离不开,不行再来,试试甲醇:乙醇=90:10: [img=,690,241]http://ng1.17img.cn/bbsfiles/images/2017/08/201708250823_01_1708019_3.png[/img][img]http://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img] 三个物质均出现,两个杂质分别在主峰前后,也达不到基线分离。 继续:100%甲醇、100%乙醇、100%乙腈。。。。。。还是分离不开,咋办。唉,这时候已经想选择放弃,通过两个方法来,分别监控杂质A与杂质B的含量。 嗯,听说有些极端情况下,可以试试叔丁醇呢,那加点叔丁醇试试吧,结果在甲醇:叔丁醇 = 78 : 22条件下,使用Amy-D(4.6×250mm,5μm)分析,各个物质均达到基线分离,且杂质A与杂质B均在主峰之前出峰,是不是都是我们希望的,按照要求配置一个系统适应性溶液测试: [img=,690,321]http://ng1.17img.cn/bbsfiles/images/2017/08/201708250823_02_1708019_3.png[/img][img]http://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img] 分析条件的筛选初步完成,接下来么,就是方法验证了,就不再一一列举了。 所以在进行手性分析时,当遇到分离度不合适,或者样品在烷烃中的溶解性不好以及难以洗脱时,可以试试极性溶剂模式来进行分离,同时因为手性分离,不同醇类,会出现不同的分离效果,而甲醇、叔丁醇也可以当作添加剂的形式,配合其他醇类用于手性分离,有时候会出现意想不到的效果。