质子传递反应质谱电离技术重大突破—新型1,4-二氟苯前驱体研发与应用
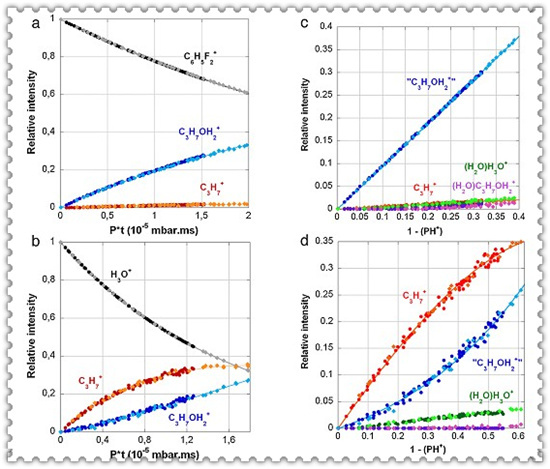
质谱法是利用带电粒子在磁场或电场中的运动规律,然后按照质量或荷质比实现分离分析的技术。早在1898年,W.维恩用电场和磁场使正离子束发生偏转时发现,电荷相同时,质量小的离子偏转得多,质量大的离子偏转得少。1913年J.J.汤姆孙和F.W.阿斯顿用磁偏转仪证实氖有两种同位素。阿斯顿于1919年制成一台能分辨一百分之一质量单位的质谱计,用以测定同位素的相对丰度,成功鉴定了多种同位素。质谱计的发展也从只用于气体分析和测定化学元素的稳定同位素到后来用于对石油馏分中的复杂烃类混合物进行分析,并证实了复杂分子能产生确定的能够重复的质谱之后,才将质谱法用于测定有机化合物的结构,开拓了有机质谱的新领域。 图1. 图左为英国物理学家J.J.汤姆孙,图右为诺贝尔化学奖获得者F.W.阿斯顿 质子传递反应质谱(Proton Transfer Reaction- Mass Spectrometry)是分析挥发性有机物(VOCs)的一种新的先进分析手段。该技术具有检测速度快、灵敏度高、无需内标定量测量等优点,特别适合挥发性有机物的实时在线监测与预警。基于多年挥发性有机物在线分析质谱研究经验,法国AlyXan公司研发的质子传递反应-傅里叶变换离子回旋共振质谱(BTrap)通过运用先进的傅里叶变换离子回旋共振质谱技术,使仪器的质量分辨率高达10000,成为质量分辨率高的质子传递反应质谱。BTrap具有高质量分辨率,高度与稳定性、低离子碎片、高灵敏度高、低检测限等诸多优势,可用于材料,环境,汽车工业,化工等多领域的气体组分在线监测分析,适应各种复杂实验气候与环境。 质子传递反应质谱一般采用质子(H3O+ )作为电离源,该技术的原理是大多数VOCs的质子亲和能高于水而低于高聚水,可以跟质子反应而被电离。但对醇,醛与长链烷烃类化合物,该方法的应用会受到很大限制。如正丁醇在正常测试条件下,不能测到分子离子峰,只能测到脱去羟基的丁烯的峰,为正丁醇的测试带来的很大困难。针对此类问题,法国AlyXan公司研发了一种全新的前驱体——1,4-二氟苯(C6H4F2)[1]。1,4-二氟苯的质子亲合能为718.7 kJ/mol,介于691到750 kJ/mol。因此C6H5F2+可以与大多数VOCs反应,同时产生更少的碎片,可以作为更加温和的质子转移试剂。同时1,4-二氟苯分子非常稳定,生成离子只会发生质子转移反应,不会参与其他反应。分子量比质子大,具有更小的质量歧视效应。 如图2所示,以正丙醇分子为例。在1.26×10-5 mbar的压力下,(a)采用C6H5F2+作为电离源,分子离子(C3H7OH2+)强度非常高,而脱羟基产物(C3H7+)的峰浓度一直维持再非常低的浓度;(b)采用H3O+作为电离源,脱羟基产物将为主要离子,分子离子峰为次要离子。说明有大量分子离子峰发生脱羟基反应,生成C3H7+离子。(c) 在更高的压力7.34×10-5 mbar下, 采用C6H5F2+作为电离源,分子离子峰(C3H7OH2+)依然为主要离子,脱羟基产物,水合离子及高聚水离子的含量非常少;(d) 采用H3O+作为电离源, 脱羟基产物为主要离子,分子离子峰为次要离子,同时有大量水合离子及高聚水离子生成。 图2. 以正丙醇为样品,离子相对强度图 1.26×10-5 mbar压力下, (a)C6H5F2+作为电离源,(b)H3O+作为电离源 7.34×10-5mbar压力下 (c)C6H5F2+作为电离源,(d)H3O+作为电离源。 从下表数据中可以发现,在其他有机物中可以有效重复试验结果,新型前躯体产生的C6H5F2+可以与大多数VOCs反应,并产生少的碎片信号。 除此之外,很多测试实例也证实了质子传递反应-傅里叶变换离子回旋共振质谱技术的先进性和可靠性,1,4-二氟苯作为一种新型的前驱体,有效解决了醇、醛及长链脂肪烃的测定难题,为质子传递反应质谱分析提供了突破性的解决方案。参考文献:[1] Latappy, H. Lemaire, J. Heninger, M. Louarn, E. Bauchard, E. Mestdagh, H. International Journal of Mass Spectrometry 2016, 405, 13.质子传递反应质谱;1,4-二氟苯;VOCs;高分辨率;少碎片相关产品:法国Alyxan公司高分辨质子传递反应质谱(BTrap):http://www.instrument.com.cn/netshow/C247308.htm