大家好!我是个新手,我现在在做一个化学品——3-环已胺基丙胺的含量分析我用的是标准样品,可是我所采用的方法在我们公司的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]上打不出原有浓度,所以求助大家给点宝贵意见。谁能提供一下关于该化学品——3-环已胺基丙胺的含量分析方法
γ-氨基丁酸和α-羟基丙酸氢键核磁峰位置大概是多少?
大家好。我想问一下。 我的做1,4-对氨基苯与FITC(异硫氰酸荧光素)反应的时候。其条件完全是按照蛋白质的氨基与FITC 的条件。即氨基与异硫氰根的反应条件进行的。但是却标记不上。不知道是不是苯环上的氨基具有惰性?还是反应条件不适合?有哪位高手指教一下!谢谢啊
[em09509]各位大虾,小弟用HPLC做邻氨基对叔丁基苯酚的分析,发现基本上只有一个峰,杂质基本上不出峰,大哥大姐们谁做过啊?能不能给个分析方法啊?或者有什么好的建议啊? 谢谢啊!!
在用氨基键合丙基硅胶SPE柱处理蔬菜、水果样品检测氨基甲酸酯类农药时它主要去除的是样品中的那类干扰物质。谢谢那
氨基柱是同时可以用于正相条件和反相条件的,但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,对这一点的忽略可能会带给使用者一些麻烦。对于新购买到的柱子,首先请注意打开分析测试说明书,了解柱子的保存溶剂。如果保存溶剂与你将要使用的流动相极性不同不会互溶,请先用异丙醇过渡。 过渡过程中注意因异丙醇粘度较大,会导致柱压很高,适当调低流速即可。如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。☆ 柱效检测:这是判断一个用户是否有经验的指标之一,是用户是否习惯配制一些柱效检测标准溶液。说到柱效检测,可以向大家提供一个方法,而且很通用,你也可以用同样的标准溶液和流动相来检测硅胶柱和氰基柱。流动相:10%乙酸乙酯+90%正己烷流速1.0标准溶液:乙苯(如乙苯找不到就用甲苯代替呗)+苯甲酸甲酯检测波长254nm这个方法特别适用于新购柱子(新购柱子往往保存在正相溶剂中)时即进行检测,也适合在柱子在准备放置相当长一段时间之前进行充分清洗后进行检测作为记录留档。在平常的使用过程中,如果分析物是固定重复的,我们当然可以从对分析物的分离分析情况来作出判断;但如果分析物和分析条件不同时,定期检测柱效可以避免柱效下降导致分离不佳再分析查找原因这样浪费人力物力的过程。不过特别要注意的是,当氨基柱(或氰基柱)在反相条件中使用时,如用该条件检测,请注意流动相的换相过渡问题。 ☆ 氨基柱的使用:需要注意的是,氨基柱的键合官能团氨丙基要比C18,C8柱的键合官能团C18,C8要容易水解,所以首先要做好其使用寿命稍逊的心理准备,特别是当你的使用条件是反相条件下时。反相条件下使用时,要特别注意控制PH值范围,PH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。所以,在使用后以及准备长时间放置该柱时,必要的清洗和将氨基柱保存于纯的有机溶剂中是很好的保养措施。有一种情况是,当使用氨基柱进行酸性物质如果汁的分析时(分析其中的糖份),酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。这时,Kromasil专家所给的建议是:用5-10倍的柱体积的含0.5-1.0%NH3的50-50乙腈-水溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。☆ 氨基柱的清洗:简单说起来,正相条件下使用的氨基柱你就参照硅胶柱的清洗方法;反相条件下使用的氨基柱你就参照C18的清洗方法。※ 平时在正相条件下使用:首先用50倍柱体积的异丙醇清洗,因异丙醇粘度较大可适当放低流速;之后,用50倍的甲醇清洗;之后,用异丙醇过渡回到平常使用的正相流动相,即可。※ 平时在反相条件下使用:缓冲盐应及时冲洗,以及不能直接用纯甲醇冲洗缓冲盐等,属常识就不作特别交待了。用50倍纯甲醇冲洗;之后,用异丙醇过渡后,用二氯甲烷冲洗色谱柱;之后,再用异丙醇过渡回来到甲醇条件下。这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等。
我的做1,4-对氨基苯与FITC(异硫氰酸荧光素)反应的时候。其条件完全是按照蛋白质的氨基与FITC的条件。即氨基与异硫氰根的反应条件进行的。但是却标记不上。不知道是不是苯环上的氨基具有惰性?还是反应条件不适合?有哪位高手指教一下!谢谢啊
用氨基酸自动分析仪测定氨基酸含量,配制不同pH的柠檬酸钠缓冲液的作用是什么?是淋洗不同的氨基酸?如果用732阳离子树脂吸附氨基酸,用氨水来淋洗,测定氨基酸总量,原理上可行吗?谢谢!
我的做1,4-对氨基苯与FITC(异硫氰酸荧光素)反应的时候。其条件完全是按照蛋白质的氨基与FITC的条件。即氨基与异硫氰根的反应条件进行的。但是却标记不上。不知道是不是苯环上的氨基具有惰性?还是反应条件不适合?有哪位高手指教一下!谢谢啊
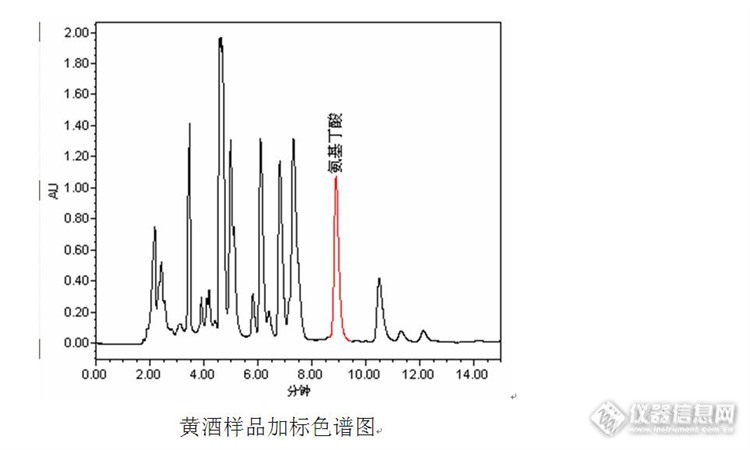
黄酒中γ-氨基丁酸含量测定的辛酸历程 近日实验室收到一批黄酒样品,该批黄酒是用发芽糙米为原料酿造而成,客户要求测定黄酒中的γ-氨基丁酸含量。由于之前实验室以丹磺酰氯为衍生试剂,建立了高效液相色谱法测定发芽糙米中γ-氨基丁酸含量的实验方法,并对实验方法的线性、精密度以及回收率进行了确认,均可以满足发芽糙米中γ-氨基丁酸含量测定要求,因此拿到黄酒样品后直接按照发芽糙米的前处理方法和色谱方法进行分析。链接如下:http://bbs.instrument.com.cn/shtml/20141226/5591256/。然而事与愿违,在测定的液相色谱图中压根就没有见到γ-氨基丁酸的色谱峰,反而在11.5min左右有个小的色谱峰,其峰高与发芽糙米中γ-氨基丁酸峰高有点相似,初步怀疑是保留时间发生了漂移,与发芽糙米样品色谱图对比后发现,在发芽糙米样品色谱图中该保留时间处也出现了一个相似的小峰,因此将该色谱峰是γ-氨基丁酸的可能性排除。http://ng1.17img.cn/bbsfiles/images/2014/12/201412311333_530568_1669358_3.jpghttp://ng1.17img.cn/bbsfiles/images/2014/12/201412311334_530570_1669358_3.jpg 原本该实验到此结束,准备将实验结果反馈给客户:黄酒中γ-氨基丁酸的检测结果为“未检出”。为了保证数据的准确性和可靠性,在黄酒样品中进行加标实验,结果在加标的色谱图中也未在相应的保留时间出峰,而且11.5min左右的色谱峰也没有增大,因此决定先将“未检出”的结果搁置,并对实验方法进行分析。 经过对样品前处理过程和色谱方法的分析,觉得可能造成加标样品中γ-氨基丁酸未检出的原因可能有:(1)保留时间漂移。由于流动相需要调节pH值,同时样品前处理过程中也涉及到酸、碱溶液的使用,怀疑是流动相或者样品pH的改变导致保留时间的漂移,从而未在原有的保留时间出现应有的色谱峰。然而重新配制流动相和前处理样品,加标样品测定结果依然是“未检出”,对比加标和不加标样品的色谱图,两者几乎一样,也没有峰面积或峰高变化明显的色谱峰;(2)衍生试剂失效。丹磺酰氯对光和湿敏感,不稳定,放置时间久了会生产二氯亚砜并继续分解成其他物质,影响其在有机溶剂中的溶解度,也会影响结果。可是为了排除衍生试剂的问题,重新打开一瓶刚购置不久的丹磺酰氯试剂,并重新试验,结果仍然不理想;(3)衍生条件控制不当。之前用相似的方法测定牛磺酸含量以及测定发芽糙米中γ-氨基丁酸含量时曾出现过衍生过程条件控制不当造成衍生不完全或者不能衍生的情况,可是与黄酒样品同一批处理的γ-氨基丁酸标准溶液和发芽糙米样品均能衍生成功,并正常出峰,为何唯独黄酒样品不出峰呢?在百思不得其解之际,看到同事在滴定黄酒中总酸,忽然间若有所悟:黄酒中的γ-氨基丁酸需要在碱性条件下才能与丹磺酰氯发生衍生反应,而黄酒是酸性介质,pH值一般在3~5之间,同时黄酒为酿造产物,对酸碱性具有一定的缓冲能力。http://ng1.17img.cn/bbsfiles/images/2014/12/201412311336_530572_1669358_3.jpg 通过比较发现:黄酒为酸性样品,缓冲能力较强,按照发芽糙米样品前处理方法直接加入0.5mL 碳酸钠(pH9.8)可能不能达到合适的衍生反应条件,最终导致黄酒样品中γ-氨基丁酸“未检出”。 找到问题后调整实验方案,先将黄酒样品调整至中性,然后再按照发芽糙米样品方法进行前处理。调整实验方案后,黄酒样品中γ-氨基丁酸测定的色谱图如下图。从色谱图中可以发现,经过实验方案的调整黄酒样品中检出了γ-氨基丁酸的存在。http://ng1.17img.cn/bbsfiles/images/2014/12/201412311337_530573_166
大家好。我想问一下。 我的做1,4-对氨基苯与FITC(异硫氰酸荧光素)反应的时候。其条件完全是按照蛋白质的氨基与FITC的条件。即氨基与异硫氰根的反应条件进行的。但是却标记不上。不知道是不是苯环上的氨基具有惰性?还是反应条件不适合?有哪位高手指教一下!谢谢啊
氨基柱在含水量多的情况下是很不稳定的,也不宜在强酸的环境下使用。缓冲液则先用水/乙腈清洗再用乙腈,氨基柱其本质属于正相柱,使用氨基柱除了采用正相系统作为流动相以外,一般还采用乙腈-水作为流动相,但是要求乙腈的含量不得低于80%,含水过多的流动相对氨基柱有损害,一般尽量不要用含水过多流动相。建议用小流速的异丙醇冲洗过夜试试。 氨基柱是同时可以用于正相条件和反相条件的,这一点很多用户都已经知道。但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,对这一点的忽略可能会带给使用者一些麻烦。NH2柱是在硅胶上键合一个5碳NH2;CN柱是在硅胶上键合一个5碳CN基;NH2.CN都为两相柱。 对于新购买到的柱子,首先请注意打开分析测试说明书,了解柱子的保存溶剂。如果保存溶剂与你将要使用的流动相极性不同不会互溶,请先用异丙醇过渡。过渡过程中注意因异丙醇粘度较大,会导致柱压很高,适当调低流速即可。如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。反相条件下使用时,要特别注意控制pH值范围,pH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。所以,在使用后以及准备长时间放置该柱时,必要的清洗和将氨基柱保存于纯的有机溶剂中是很好的保养措施。
苯丙氨酸的boc氨基保护,除了生成N-boc苯丙氨酸,还生成什么?是二氧化碳和叔丁醇吗?
求3-氨基-5正丙胺基-1,2,4-三氮唑标准品,CS号也不知道是多少
我先介绍下我们实验室使用氨基柱的姻缘,早在两年前,领导突然要求检测制剂药品中门冬氨酸辅料的含量,于是乎从网上找了一篇文献是关于做门冬氨酸的,看了看色谱柱:氨基柱,没用过的新柱子;找供应商买了一款氨基柱(phenomenex家的),一开始由于没有经验,就只是把它当普通的色谱柱来用,用着用着发现,一个月用个2-3次,柱子就用坏了;然后就找厂家的技术支持要资料,自己也上网查资料,总结了一下氨基柱的使用与维护,现在分享给大家:我们实验室采购的是phenomenex LunaNH2氨基柱([color=#ff0000]色谱柱耐受pH 1.5-11.0[/color])(我想其他品牌的氨基柱应该是有相同的共性的,希望有用过的大家补充补充)1. 氨基柱是一款既可以正相使用,也可以反相使用,但是我们要注意到的是:正相溶剂和反相溶剂往往是不互溶的,正常情况新氨基柱出厂时保存在正相环境中,而Luna的 氨基柱查找说明书是保存在正己烷-乙腈(99:1)中。2. 如果大家是用于正相的体系:2.1 推荐先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再根据流动相选用极性相近的氯仿或二氯甲烷以相同的流速冲10倍柱体积,最后换成你实验的流动相2.2 正相使用时,不宜分析含醛基、羰基的化合物,不可用于还原糖的分析;流动相要彻底脱气,并不得含有羰基化合物和过氧化物(质量不好的乙醚、四氢呋喃含有少量)2.3 [color=#ff0000]任何时候更换流动相时都要确保新流动相与柱子原保存液可互溶[/color]3. 如果大家用于反相的体系:3.1 由于新的氨基柱保存在正己烷-乙腈(99:1)中,与反相流动相是不互溶的,因此如果使用反相的方法,必须用至少10倍柱体积的异丙醇冲洗过渡(约2h,0.5mL/min),以除去正相保存溶液。过渡过程中注意因异丙醇粘度较大,会导致柱压很高,适当调低流速即可。3.2 再用至少10倍柱体积95%水-5%乙腈(或甲醇)冲洗(不含缓冲盐的流动相可省去)过渡,最后用流动相平衡。3.3 用完后洗柱时,必须先用95%水冲洗至少10倍柱体积,除去所用缓冲盐(不含缓冲盐的流动相可省去)。然后保存于乙腈/水(80:20)溶液([color=#ff0000]一个月内[/color])中。长期不用的话,建议用异丙醇保存[color=#ff0000](一个月以上)。[/color]3.4 新柱子一定要置换掉保存溶液,用异丙醇保存的柱子在使用前也需要花一定的时间给置换掉。3.5 反相条件下使用时,要特别注意控制pH值范围(根据你色谱柱耐受使用pH),pH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。3.6 还有一种情况是,当使用氨基柱进行酸性物质的分析时,酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。---------建议用10-15倍的柱体积的为pH=11 NH3的乙腈-水(50:50)溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。3.7 柱子再生:以0.5ml/min的流速用30倍柱体积的pH10.0的氨水或氢氧化钠水溶液冲柱子(注意pH值切不可超过11.0),立即用水(0.5ml/min的流速,30倍柱体积)冲洗,再乙腈/水(80:20)溶液冲洗保存。最后谈一下平衡的问题,我们用的最多的是反相体系,正相体系不是很清楚(见谅);一开始我们以为2-3小时就可以稳定了,其实不然,后来经过不断的折腾,发现至少12个小时,你的系统才能稳定下来(我们碰到过平衡时间不够,进了几十针标准品,样品出峰时间以0.02min/针的形式,从最初的12.8min漂移到15.2min)。希望对广大用氨基柱的论友们有所帮助!
(2S,3S)-3-氨基-2-甲基-4-氧代氮杂环丁烷-1-磺酸(2S,3S)-3-amino-2-methyl-4-oxoazetidine-1-sulfonic acid谁有这个液相的检测纯度的方法,是氨曲南的起始物料N-氮杂环丁烷???
氨基柱的使用和保养氨基柱是同时可以用于正相条件和反相条件的这一点很多用户都已经知道;但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,对这一点的忽略可能会带给使用者一些麻对于新购买到的柱子,首先请注意打开分析测试说明书,了解柱子的保存溶剂。如果保存溶剂与你将要使用的流动相极性不同不会互溶,请先用异丙醇过渡。过渡过程中注意因异丙醇粘度较大,会导致柱压很高,适当调低流速即可。如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。柱效检测:我用于判断一个用户是否有经验的指标之一,是用户是否习惯配制一些柱效检测标准溶液。说到柱效检测,我可以向大家提供一个方法,而且很通用,你也可以用同样的标准溶液和流动相来检测硅胶柱和氰基柱。流动相:0%乙酸乙酯+90%正己烷 流速1.0标准溶液:乙苯(如乙苯找不动就用甲苯代替呗)+苯甲酸甲酯检测波长:254nm这个方法特别适用于新购柱子(新购柱子往往保存在正相溶剂中)时即进行检测,如有问题,可及时与供应商沟通。也适合在柱子在准备放置相当长一段时间之前进行充分清洗后进行检测作为记录留档。在平常的使用过程中,如果分析物是固定重复的,我们当然可以从对分析物的分离分析情况来作出判断;但如果分析物和分析条件不同时,定期检测柱效可以避免柱效下降导致分离不佳再分析查找原因这样浪费人力物力的过程。不过特别要注意的是,当氨基柱(或氰基柱)在反相条件中使用时,如用该条件检测,请注意流动相的换相过渡问题。 氨基柱的使用:需要注意的是,氨基柱的键合官能团氨丙基要比C18,C8柱的键合官能团C18,C8要容易水解,所以首先要做好其使用寿命稍逊的心理准备,特别是当你的使用条件是反相条件下时。反相条件下使用时,要特别注意控制PH值范围,PH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。所以,在使用后以及准备长时间放置该柱时,必要的清洗和将氨基柱保存于纯的有机溶剂中是很好的保养措施。有一种情况是,当使用氨基柱进行酸性物质如果汁的分析时(分析其中的糖份),酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。这时,Kromasil专家所给的建议是:用5-10倍的柱体积的含0.5-1.0%NH3的50-50乙腈-水溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。氨基柱的清洗简单说起来,正相条件下使用的氨基柱你就参照硅胶柱的清洗方法;反相条件下使用的氨基柱你就参照C18的清洗方法。平时在正相条件下使用:首先用50倍柱体积的异丙醇清洗,因异丙醇粘度较大可适当放低流速;之后,用50倍的甲醇清洗;之后,用异丙醇过渡回到平常使用的正相流动相,即可。平时在反相条件下使用:缓冲盐应及时冲洗,以及不能直接用纯甲醇冲洗缓冲盐等,属常识就不作特别交待了。用50倍纯甲醇冲洗;之后,用异丙醇过渡后,用二氯甲烷冲洗色谱柱;之后,再用异丙醇过渡回来到甲醇条件下。这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等Ultimate氨基柱的使用方法1.氨基柱既可以正相使用,也可以反相使用,但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,正常情况新氨基柱保存在正相环境中,例如LUNA 氨基柱保存在正己烷-乙腈(99:1)中。2. 正相使用2.1 新柱子可直接用流动相。推荐先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再根据流动相选用极性相近的氯仿或二氯甲烷以相同的流速冲10倍柱体积,最后换成流动相。2.2 正相使用时,不宜分析含醛基、羰基的化合物,不可用于还原糖的分析;流动相要彻底脱气,并不得含有羰基化合物和过氧化物(质量不好的乙醚、四氢呋喃含有少量)。2.3 任何时候更换流动相时都要确保新流动相与柱子原保存液可互溶。3 反相使用3.1 先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再依次以相同的流速相同的用量用氯仿、异丙醇、甲醇、甲醇-水(50:50)冲柱子。3.2 以0.5ml/min的流速用30倍柱体积的pH11.0的氢氧化钠(LUNA)水溶液冲柱子(注意pH值切不可超过11.0),立即用水(0.5ml/min的流速,30倍柱体积)冲洗,再换成流动相。3.3 配制流动相时,应各组分分别量取,比例较小的组分要精密量取,需调pH值时要精密到0.1。3.4 反相条件下使用时,要特别注意控制pH值范围,pH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。最理想的pH范围在pH 3.0-7.03.5 如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。3.6 有一种情况是,当使用氨基柱进行酸性物质的分析时,酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。建议:用5-10倍的柱体积的含0.5-1.0%NH3的乙腈-水(50:50)溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。4 色谱柱的冲洗:简单说起来,正相条件下使用的氨基柱就参照硅胶柱的清洗方法;反相条件下使用的氨基柱就参照C18的清洗方法。5 色谱柱的保存5.1 正相使用时,将柱子冲洗干净后,用正己烷-乙腈(99:1)保存。5.2 反相使用时,如短期不用,可用甲醇或乙腈保存;长期不用时需将甲醇依次用异丙醇、氯仿置换,最后用正己烷保存。6 色谱柱的再生6.1 方案1:依次用甲醇、异丙醇、氯仿、正己烷、氯仿、异丙醇、甲醇冲柱子(各以0.5ml/min的流速,20倍柱体积),再换流动相。这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等。6.2 方案2:NH2柱用于反相条件时,NH2键会水解,尤其是在该柱子pH范围以外,在极端酸性和碱性条件下柱寿命会下降很快,如果在这个条件下使用需要清洗一下,需要用10倍柱体积溶液冲洗,如下:95%水/5%乙腈THF四氢呋喃95%乙腈/5%水并保持95%乙腈/5%水继续冲洗,以低流速0.2-0.5mL/min过夜冲洗。6.3 方案3:柱子使用一定时间后,柱效下降,老化,也可清洗一下柱子恢复柱性能,清洗时依次用10倍柱体积的下列溶液冲洗:95%水/5%乙腈THF四氢呋喃95%乙腈/5%水再走流动相即可
氨基柱是同时可以用于正相条件和反相条件的这一点很多用户都已经知道;但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,对这一点的忽略可能会带给使用者一些麻烦。对于新购买到的柱子,首先请注意打开分析测试说明书,了解柱子的保存溶剂。如果保存溶剂与你将要使用的流动相极性不同不会互溶,请先用异丙醇过渡。过渡过程中注意因异丙醇粘度较大,会导致柱压很高,适当调低流速即可。如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。柱效检测:我用于判断一个用户是否有经验的指标之一,是用户是否习惯配制一些柱效检测标准溶液。说到柱效检测,我可以向大家提供一个方法,而且很通用,你也可以用同样的标准溶液和流动相来检测硅胶柱和氰基柱。流动相:10%乙酸乙酯+90%正己烷 流速1.0标准溶液:乙苯(如乙苯找不动就用甲苯代替呗)+苯甲酸甲酯检测波长254nm这个方法特别适用于新购柱子(新购柱子往往保存在正相溶剂中)时即进行检测,如有问题,可及时与供应商沟通。也适合在柱子在准备放置相当长一段时间之前进行充分清洗后进行检测作为记录留档。在平常的使用过程中,如果分析物是固定重复的,我们当然可以从对分析物的分离分析情况来作出判断;但如果分析物和分析条件不同时,定期检测柱效可以避免柱效下降导致分离不佳再分析查找原因这样浪费人力物力的过程。不过特别要注意的是,当氨基柱(或氰基柱)在反相条件中使用时,如用该条件检测,请注意流动相的换相过渡问题。氨基柱的使用:需要注意的是,氨基柱的键合官能团氨丙基要比C18,C8柱的键合官能团C18,C8要容易水解,所以首先要做好其使用寿命稍逊的心理准备,特别是当你的使用条件是反相条件下时。反相条件下使用时,要特别注意控制PH值范围,PH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。所以,在使用后以及准备长时间放置该柱时,必要的清洗和将氨基柱保存于纯的有机溶剂中是很好的保养措施。有一种情况是,当使用氨基柱进行酸性物质如果汁的分析时(分析其中的糖份),酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。这时,Kromasil专家所给的建议是:用5-10倍的柱体积的含0.5- 1.0%NH3的50-50乙腈-水溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。氨基柱的清洗简单说起来,正相条件下使用的氨基柱你就参照硅胶柱的清洗方法;反相条件下使用的氨基柱你就参照C18的清洗方法。平时在正相条件下使用:首先用50倍柱体积的异丙醇清洗,因异丙醇粘度较大可适当放低流速;之后,用50倍的甲醇清洗;之后,用异丙醇过渡回到平常使用的正相流动相,即可。平时在反相条件下使用:缓冲盐应及时冲洗,以及不能直接用纯甲醇冲洗缓冲盐等,属常识就不作特别交待了。用50倍纯甲醇冲洗;之后,用异丙醇过渡后,用二氯甲烷冲洗色谱柱;之后,再用异丙醇过渡回来到甲醇条件下。这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等LUNA氨基柱的使用方法1.氨基柱既可以正相使用,也可以反相使用,但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,正常情况新氨基柱保存在正相环境中,例如LUNA氨基柱保存在正己烷-乙腈(99:1)中。2. 正相使用2.1新柱子可直接用流动相。推荐先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再根据流动相选用极性相近的氯仿或二氯甲烷以相同的流速冲10倍柱体积,最后换成流动相。2.1正相使用时,不宜分析含醛基、羰基的化合物,不可用于还原糖的分析;流动相要彻底脱气,并不得含有羰基化合物和过氧化物(质量不好的乙醚、四氢呋喃含有少量)。2.3 任何时候更换流动相时都要确保新流动相与柱子原保存液可互溶。3 反相使用3.1先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再依次以相同的流速相同的用量用氯仿、异丙醇、甲醇、甲醇-水(50:50)冲柱子。3.2以0.5ml/min的流速用30倍柱体积的pH11.0的氢氧化钠(LUNA)水溶液冲柱子(注意pH值切不可超过11.0),立即用水(0.5ml/min的流速,30倍柱体积)冲洗,再换成流动相。3.3 配制流动相时,应各组分分别量取,比例较小的组分要精密量取,需调pH值时要精密到0.1。3.4反相条件下使用时,要特别注意控制pH值范围,pH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。最理想的pH范围在pH3.0-7.03.5如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。3.6有一种情况是,当使用氨基柱进行酸性物质的分析时,酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。建议:用5-10倍的柱体积的含0.5-1.0%NH3的乙腈-水(50:50)溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。4色谱柱的冲洗:简单说起来,正相条件下使用的氨基柱就参照硅胶柱的清洗方法;反相条件下使用的氨基柱就参照C18的清洗方法。5 色谱柱的保存5.1 正相使用时,将柱子冲洗干净后,用正己烷-乙腈(99:1)保存。5.2反相使用时,如短期不用,可用甲醇或乙腈保存;长期不用时需将甲醇依次用异丙醇、氯仿置换,最后用正己烷保存。6 色谱柱的再生6.1 方案1:依次用甲醇、异丙醇、氯仿、正己烷、氯仿、异丙醇、甲醇冲柱子(各以0.5ml/min的流速,20倍柱体积),再换流动相。这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等。6.2方案2:NH2柱用于反相条件时,NH2键会水解,尤其是在该柱子pH范围以外,在极端酸性和碱性条件下柱寿命会下降很快,如果在这个条件下使用需要清洗一下,需要用10倍柱体积溶液冲洗,如下:95%水/5%乙腈THF四氢呋喃95%乙腈/5%水并保持95%乙腈/5%水继续冲洗,以低流速0.2-0.5mL/min过夜冲洗。6.3方案3:柱子使用一定时间后,柱效下降,老化,也可清洗一下柱子恢复柱性能,清洗时依次用10倍柱体积的下列溶液冲洗:95%水/5%乙腈THF四氢呋喃95%乙腈/5%水再走流动相即可
氨基柱是同时可以用于正相条件和反相条件的这一点很多用户都已经知道;但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,对这一点的忽略可能会带给使用者一些麻烦。对于新购买到的柱子,首先请注意打开分析测试说明书,了解柱子的保存溶剂。如果保存溶剂与你将要使用的流动相极性不同不会互溶,请先用异丙醇过渡。过渡过程中注意因异丙醇粘度较大,会导致柱压很高,适当调低流速即可。如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。柱效检测:我用于判断一个用户是否有经验的指标之一,是用户是否习惯配制一些柱效检测标准溶液。说到柱效检测,我可以向大家提供一个方法,而且很通用,你也可以用同样的标准溶液和流动相来检测硅胶柱和氰基柱。流动相:10%乙酸乙酯+90%正己烷 流速1.0标准溶液:乙苯(如乙苯找不动就用甲苯代替呗)+苯甲酸甲酯检测波长254nm这个方法特别适用于新购柱子(新购柱子往往保存在正相溶剂中)时即进行检测,如有问题,可及时与供应商沟通。也适合在柱子在准备放置相当长一段时间之前进行充分清洗后进行检测作为记录留档。在平常的使用过程中,如果分析物是固定重复的,我们当然可以从对分析物的分离分析情况来作出判断;但如果分析物和分析条件不同时,定期检测柱效可以避免柱效下降导致分离不佳再分析查找原因这样浪费人力物力的过程。不过特别要注意的是,当氨基柱(或氰基柱)在反相条件中使用时,如用该条件检测,请注意流动相的换相过渡问题。 氨基柱的使用:需要注意的是,氨基柱的键合官能团氨丙基要比C18,C8柱的键合官能团C18,C8要容易水解,所以首先要做好其使用寿命稍逊的心理准备,特别是当你的使用条件是反相条件下时。反相条件下使用时,要特别注意控制PH值范围,PH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。所以,在使用后以及准备长时间放置该柱时,必要的清洗和将氨基柱保存于纯的有机溶剂中是很好的保养措施。有一种情况是,当使用氨基柱进行酸性物质如果汁的分析时(分析其中的糖份),酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。这时,Kromasil专家所给的建议是:用5-10倍的柱体积的含0.5-1.0%NH3的50-50乙腈-水溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。氨基柱的清洗简单说起来,正相条件下使用的氨基柱你就参照硅胶柱的清洗方法;反相条件下使用的氨基柱你就参照C18的清洗方法。平时在正相条件下使用:首先用50倍柱体积的异丙醇清洗,因异丙醇粘度较大可适当放低流速;之后,用50倍的甲醇清洗;之后,用异丙醇过渡回到平常使用的正相流动相,即可。平时在反相条件下使用:缓冲盐应及时冲洗,以及不能直接用纯甲醇冲洗缓冲盐等,属常识就不作特别交待了。用50倍纯甲醇冲洗;之后,用异丙醇过渡后,用二氯甲烷冲洗色谱柱;之后,再用异丙醇过渡回来到甲醇条件下。这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等LUNA氨基柱的使用方法1. 氨基柱既可以正相使用,也可以反相使用,但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,正常情况新氨基柱保存在正相环境中,例如LUNA 氨基柱保存在正己烷-乙腈(99:1)中。2. 正相使用2.1 新柱子可直接用流动相。推荐先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再根据流动相选用极性相近的氯仿或二氯甲烷以相同的流速冲10倍柱体积,最后换成流动相。2.2 正相使用时,不宜分析含醛基、羰基的化合物,不可用于还原糖的分析;流动相要彻底脱气,并不得含有羰基化合物和过氧化物(质量不好的乙醚、四氢呋喃含有少量)。2.3 任何时候更换流动相时都要确保新流动相与柱子原保存液可互溶。3 反相使用3.1 先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再依次以相同的流速相同的用量用氯仿、异丙醇、甲醇、甲醇-水(50:50)冲柱子。3.2 以0.5ml/min的流速用30倍柱体积的pH11.0的氢氧化钠(LUNA)水溶液冲柱子(注意pH值切不可超过11.0),立即用水( 0.5ml/min的流速,30倍柱体积)冲洗,再换成流动相。3.3 配制流动相时,应各组分分别量取,比例较小的组分要精密量取,需调pH值时要精密到0.1。3.4 反相条件下使用时,要特别注意控制pH值范围,pH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。最理想的pH范围在pH 3.0-7.03.5 如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。3.6 有一种情况是,当使用氨基柱进行酸性物质的分析时,酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。建议:用5-10倍的柱体积的含0.5-1.0%NH3的乙腈-水(50:50)溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。4 色谱柱的冲洗:简单说起来,正相条件下使用的氨基柱就参照硅胶柱的清洗方法;反相条件下使用的氨基柱就参照C18的清洗方法。5 色谱柱的保存 5.1 正相使用时,将柱子冲洗干净后,用正己烷-乙腈(99:1)保存。5.2 反相使用时,如短期不用,可用甲醇或乙腈保存;长期不用时需将甲醇依次用异丙醇、氯仿置换,最后用正己烷保存。6 色谱柱的再生6.1 方案1:依次用甲醇、异丙醇、氯仿、正己烷、氯仿、异丙醇、甲醇冲柱子(各以0.5ml/min的流速,20倍柱体积),再换流动相。这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等。6.2 方案2:NH2柱用于反相条件时,NH2键会水解,尤其是在该柱子pH范围以外,在极端酸性和碱性条件下柱寿命会下降很快,如果在这个条件下使用需要清洗一下,需要用10倍柱体积溶液冲洗,如下:95%水/5%乙腈THF四氢呋喃95%乙腈/5%水并保持95%乙腈/5%水继续冲洗,以低流速0.2-0.5mL/min过夜冲洗。6.3 方案3:柱子使用一定时间后,柱效下降,老化,也可清洗一下柱子恢复柱性能,清洗时依次用10倍柱体积的下列溶液冲洗:95%水/5%乙腈THF四氢呋喃95%乙腈/5%水再走流动相即可
[color=#444444]在利用液相色谱分析检测氨基甲酸乙酯的时候,总是有丙氨酸的干扰,而且两者的出峰时间较为接近,丙氨酸很容易将后面出来的氨基甲酸乙酯的峰重叠掉,试了很多方法都没办法改变,请求各位支招,万分感谢![/color]
氨基甲酸酯类农药是在有机磷酸酯之后发展起来的合成农药,在水中溶解度较高。氨基甲酸酯类农药一般无特殊气味,在酸性环境下稳定,遇碱性环境分解。大多数品种毒性较有机磷酸酯类低。 酒精饮品中的各种物质及其分解物经发酵过程后均可产生氨基甲酸酯。这些物质(如尿素、氰酸酯和瓜氨酸)与乙醇发生化学作用,在酒精饮品中产生氨基甲酸酯,进而其被广泛运用到农业生产上。氨基甲酸酯类农药大多数为结晶低熔点固体,而产生的数量取决于熵曲线和温度两大要素。 氨基甲酸酯类农药几乎没有气味,味道苦且有冰冷感觉。 氨基甲酸酯类农药并不是剧毒化合物,但具有致癌性。另外,氨基甲酸酯类可入药,但约50%的患者表现出恶心和呕吐,长时间使用会导致胃肠道出血。大鼠,小鼠和仓鼠的研究已经表明,把氨基甲酸酯类 口服,注射,或涂在皮肤上会导致癌症,因此,国际癌症研究机构在2007年把氨基甲酸酯类列为2A类致癌物。含酒精的农作物,特别是某些食材水果白酒和威士忌,往往含有低浓度的氨基甲酸酯类农药。 在日本(2000)和香港(2009)的研究概括了在日常生活中的氨基甲酸酯类农药的累积暴露的程度。一些发酵食品,如酱油,泡菜,大酱,面包,面包卷,馒头,饼干,豆腐,加上酒,清酒和梅酒等亚洲传统食物中有较高的氨基甲酸酯类农药水平。 联合国粮食及农业组织及世界卫生组织与联合食品添加剂专家委员会(专家委员会)曾在2005年进行有关氨基甲酸酯类农药评估,认为经食物(不包括酒精饮品)摄入的氨基甲酸酯类农药分量,对健康的影响并不大,但经食物和酒精饮品摄入的氨基甲酸酯类总量,则可能对健康构成潜在的风险。专家委员会建议采取措施,减少一些农作物氨基甲酸酯类的含量。
丙酮氨基海因的 检测方法 现在条件是 波长 210 流动相 10:90 乙腈:0.003磷酸溶液 保留时间 4.2 一直有拖尾的肩峰现在流动相的极性乙腈这么大了 请问还有这么方法可以把肩峰 区分开来
求助:最近要检测5-氨基乙酰丙酸(固体)含量,可是找不到药典中的检测方法,希望高手帮忙,没有药典,有企业标准也行谢谢找了一篇国标,测尿液中的5-氨基乙酰丙酸,不知道用来测定固体的含量可不可靠,有没有可信度谢谢
氨基柱是同时可以用于正相条件和反相条件的这一点很多用户都已经知道;但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,对这一点的忽略可能会带给使用者一些麻烦。 对于新购买到的柱子,首先请注意打开分析测试说明书,了解柱子的保存溶剂。如果保存溶剂与你将要使用的流动相极性不同不会互溶,请先用异丙醇过渡。过渡过程中注意因异丙醇粘度较大,会导致柱压很高,适当调低流速即可。如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。 柱效检测: 我用于判断一个用户是否有经验的指标之一,是用户是否习惯配制一些柱效检测标准溶液。说到柱效检测,我可以向大家提供一个方法,而且很通用,你也可以用同样的标准溶液和流动相来检测硅胶柱和氰基柱。 流动相: 10%乙酸乙酯+90%正己烷 流速1.0 标准溶液: 乙苯(如乙苯找不动就用甲苯代替呗)+苯甲酸甲酯 检测波长254nm 这个方法特别适用于新购柱子(新购柱子往往保存在正相溶剂中)时即进行检测,如有问题,可及时与供应商沟通。也适合在柱子在准备放置相当长一段时间之前进行充分清洗后进行检测作为记录留档。在平常的使用过程中,如果分析物是固定重复的,我们当然可以从对分析物的分离分析情况来作出判断;但如果分析物和分析条件不同时,定期检测柱效可以避免柱效下降导致分离不佳再分析查找原因这样浪费人力物力的过程。不过特别要注意的是,当氨基柱(或氰基柱)在反相条件中使用时,如用该条件检测,请注意流动相的换相过渡问题。 氨基柱的使用: 需要注意的是,氨基柱的键合官能团氨丙基要比C18,C8柱的键合官能团C18,C8要容易水解,所以首先要做好其使用寿命稍逊的心理准备,特别是当你的使用条件是反相条件下时。 反相条件下使用时,要特别注意控制PH值范围,PH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。所以,在使用后以及准备长时间放置该柱时,必要的清洗和将氨基柱保存于纯的有机溶剂中是很好的保养措施。 有一种情况是,当使用氨基柱进行酸性物质如果汁的分析时(分析其中的糖份),酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。这时,Kromasil专家所给的建议是:用5-10倍的柱体积的含0.5-1.0%NH3的50-50乙腈-水溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。 氨基柱的清洗 简单说起来,正相条件下使用的氨基柱你就参照硅胶柱的清洗方法;反相条件下使用的氨基柱你就参照C18的清洗方法。 平时在正相条件下使用: 首先用50倍柱体积的异丙醇清洗,因异丙醇粘度较大可适当放低流速;之后,用50倍的甲醇清洗;之后,用异丙醇过渡回到平常使用的正相流动相,即可。 平时在反相条件下使用: 缓冲盐应及时冲洗,以及不能直接用纯甲醇冲洗缓冲盐等,属常识就不作特别交待了。 用50倍纯甲醇冲洗;之后,用异丙醇过渡后,用二氯甲烷冲洗色谱柱;之后,再用异丙醇过渡回来到甲醇条件下。 这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等 LUNA氨基柱的使用方法 1. 氨基柱既可以正相使用,也可以反相使用,但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,正常情况新氨基柱保存在正相环境中,例如LUNA 氨基柱保存在正己烷-乙腈(99:1)中。 2. 正相使用 2.1 新柱子可直接用流动相。推荐先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再根据流动相选用极性相近的氯仿或二氯甲烷以相同的流速冲10倍柱体积,最后换成流动相。 2.1 正相使用时,不宜分析含醛基、羰基的化合物,不可用于还原糖的分析;流动相要彻底脱气,并不得含有羰基化合物和过氧化物(质量不好的乙醚、四氢呋喃含有少量)。 2.3 任何时候更换流动相时都要确保新流动相与柱子原保存液可互溶。 3 反相使用 3.1 先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再依次以相同的流速相同的用量用氯仿、异丙醇、甲醇、甲醇-水(50:50)冲柱子。 3.2 以0.5ml/min的流速用30倍柱体积的pH11.0的氢氧化钠(LUNA)水溶液冲柱子(注意pH值切不可超过11.0),立即用水( 0.5ml/min的流速,30倍柱体积)冲洗,再换成流动相。 3.3 配制流动相时,应各组分分别量取,比例较小的组分要精密量取,需调pH值时要精密到0.1。 3.4 反相条件下使用时,要特别注意控制pH值范围,pH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。最理想的pH范围在pH 3.0-7.0 3.5 如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。 3.6 有一种情况是,当使用氨基柱进行酸性物质的分析时,酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。建议:用5-10倍的柱体积的含0.5-1.0%NH3的乙腈-水(50:50)溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。 4 色谱柱的冲洗:简单说起来,正相条件下使用的氨基柱就参照硅胶柱的清洗方法;反相条件下使用的氨基柱就参照C18的清洗方法。 5 色谱柱的保存 5.1 正相使用时,将柱子冲洗干净后,用正己烷-乙腈(99:1)保存。 5.2 反相使用时,如短期不用,可用甲醇或乙腈保存;长期不用时需将甲醇依次用异丙醇、氯仿置换,最后用正己烷保存。 6 色谱柱的再生 6.1 方案1:依次用甲醇、异丙醇、氯仿、正己烷、氯仿、异丙醇、甲醇冲柱子(各以 0.5ml/min的流速,20倍柱体积),再换流动相。这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等。 6.2 方案2:NH2柱用于反相条件时,NH2键会水解,尤其是在该柱子pH范围以外,在极端酸性和碱性条件下柱寿命会下降很快,如果在这个条件下使用需要清洗一下,需要用10倍柱体积溶液冲洗,如下: 95%水/5%乙腈 THF四氢呋喃 95%乙腈/5%水 并保持95%乙腈/5%水继续冲洗,以低流速0.2-0.5mL/min过夜冲洗。 6.3 方案3:柱子使用一定时间后,柱效下降,老化,也可清洗一下柱子恢复柱性能,清洗时依次用10倍柱体积的下列溶液冲洗: 95%水/5%乙腈 THF四氢呋喃 95%乙腈/5%水 再走流动相即可
[color=#3e3e3e]在我做技术支持过程中发现用户对氨基柱的了解不是很多,这里我愿意把我对氨基柱的一点点了解与大家分享,有不对或遗漏之处,欢迎更正补充。[/color][color=#3e3e3e]1.氨基柱是同时可以用于正相条件和反相条件的,这一点很多用户都已经知道;但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,对这一点的忽略可能会带给使用者一些麻烦。[/color][color=#3e3e3e][/color][color=#3e3e3e]2.对于新购买到的柱子,首先请注意打开分析测试说明书,了解柱子的保存溶剂。如果保存溶剂与你将要使用的流动相极性不同不会互溶,请先用异丙醇过渡。过渡过程中注意因异丙醇粘度较大,会导致柱压很高,适当调低流速即可。如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。[/color][color=#3e3e3e] 柱效检测:[/color][color=#3e3e3e][/color][color=#3e3e3e] 我用于判断一个用户是否有经验的指标之一,是用户是否习惯配制一些柱效检测标准溶液。说到柱效检测,我可以向大家提供一个方法,而且很通用,你也可以用同样的标准溶液和流动相来检测硅胶柱和氰基柱。[/color][color=#3e3e3e] 流动相:10%乙酸乙酯+90%正己烷 流速1.0[/color][color=#3e3e3e][/color][color=#3e3e3e] 标准溶液:乙苯(如乙苯找不动就用甲苯代替呗)+苯甲酸甲酯[/color][color=#3e3e3e][/color][color=#3e3e3e] 检测波长254nm[/color][color=#3e3e3e] 这个方法特别适用于新购柱子(新购柱子往往保存在正相溶剂中)时即进行检测,如有问题,可及时与供应商沟通。也适合在柱子在准备放置相当长一段时间之前进行充分清洗后进行检测作为记录留档。在平常的使用过程中,如果分析物是固定重复的,我们当然可以从对分析物的分离分析情况来作出判断;但如果分析物和分析条件不同时,定期检测柱效可以避免柱效下降导致分离不佳再分析查找原因这样浪费人力物力的过程。不过特别要注意的是,当氨基柱(或氰基柱)在反相条件中使用时,如用该条件检测,请注意流动相的换相过渡问题。[/color][color=#3e3e3e] 氨基柱的使用:[/color][color=#3e3e3e][/color][color=#3e3e3e] 需要注意的是,氨基柱的键合官能团氨丙基要比C18,C8柱的键合官能团C18,C8要容易水解,所以首先要做好其使用寿命稍逊的心理准备,特别是当你的使用条件是反相条件下时。[/color][color=#3e3e3e] 反相条件下使用时,要特别注意控制PH值范围,PH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。所以,在使用后以及准备长时间放置该柱时,必要的清洗和将氨基柱保存于纯的有机溶剂中是很好的保养措施。[/color][color=#3e3e3e] 有一种情况是,当使用氨基柱进行酸性物质如果汁的分析时(分析其中的糖份),酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。这时,Kromasil专家所给的建议是:用5-10倍的柱体积的含0.5-1.0%NH3的50-50乙腈-水溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。[/color]
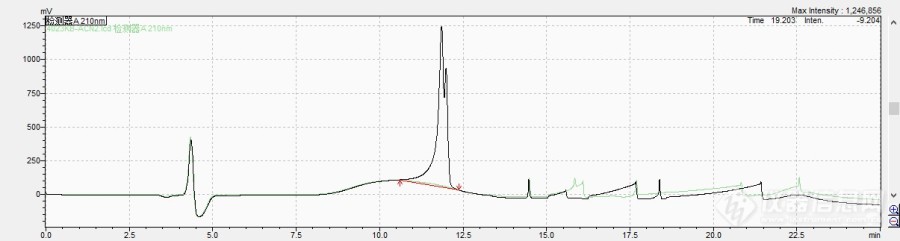
CAS:283159-95-5我用C18的柱子,流动相A、B分别是0.05%TFA的纯水、0.05%TFA的乙腈,流动相B的梯度是初始10%,5min升到60%并保持10min,15min后降到10%保持5min,谱图主峰分叉。[img=,690,184]https://ng1.17img.cn/bbsfiles/images/2024/01/202401271531592473_6839_4185279_3.jpg!w690x184.jpg[/img]请问(S)-3-氨基-3-(4-氯苯基)丙酸甲酯是手性化合物吗,需要什么类型色谱柱和流动相条件分析?
氨基丙氟灵的分析可以用气相色谱做吗?我现在用液相做,流动相是乙腈:水=8:2(调ph=6.8)柱子是XB-C18,总感觉重现性不是很好,心里没有底师兄,师姐们,帮下后进学弟吧

研究概况 物质的相平衡数据测定及其相平衡研究是化工热力学的一个重要分支,固液相平衡是化工分离的理论基础。固液平衡的研究为结晶分离过程规定了分离极限,并为设备结构尺寸的设计和操作条件的确定提供基础数据,是实现化工生产的重要前提。实验测定固液平衡不仅是工程设计必不可少的基础数据,也是进行理论研究的基础。固液平衡的数学模型参数需要由实验数据来回归,数学模型的准确性需要用实验数据来检验。通过对固液平衡实验数据的处理,找出其内在规律,提出符合溶解行为的数学模型。 4-二甲氨基吡啶(简称DMAP)结构上有共电子的二甲氨基与吡啶环的共振,强烈的激活了环上的氮原子进行亲核取代,明显催化高位阻、低反应性的醇或胺的酰化(磷酰化、磺酰化)反应,其活性为吡啶的106倍。1967年,Litvinenko和Kirichenko用间氯苯胺进行苯甲酰化动力学研究,以4-二甲氨基吡啶代替吡啶,发现其反应速率增加约1万倍。Steglich、Hassner等人开始着手于研究DMAP作为催化剂催化酰化反应,酰化反应应用于醇、胺、酚和烯醇盐,尤其是存在空间位阻的仲醇、叔醇等。至今,DMAP在酰化反应催化剂中,具有反应速度快、副反应少、溶剂选择范围广、反应条件温和、反应温度低、催化剂量少、对空间位阻大与活性低的醇类酰化催化效果明显的特点,被称为“超级催化剂”。 美、欧、日等国家早已实现DMAP的工业化生产与应用研究,广泛地应用于医药、高分子、精细化工等行业中,我国从90年代初开始DMAP的合成与应用研究,目前,在化学制药领域上取得了成功的应用及良好的效益,如乙(丙)酞螺旋霉素、青篙素唬拍酸酷等原料药的生产;农药领域上在胺菊酯的合成已通过中试并投产。1.实验部分1.1实验试剂4-二甲氨基吡啶 (1) DMAP的物性:白色结晶性粉末,溶于水、乙醇、丙酮、苯、甲苯、二甲苯、二氯乙烷、氯仿、乙酸、乙酐、乙酸乙酯、已烷、四氢呋喃、三乙胺、吡啶、DMF 等溶剂。DMAP的分子结构,如图1-1。http://ng1.17img.cn/bbsfiles/images/2015/09/201509272125_568160_2423358_3.jpg1.2实验试剂规格及来源实验试剂规格及来源,均符合分析化学实验的要求,可以保证实验的进行。表1-2 实验所用试剂 试剂名称 生产厂家分子量规格和品级质量分数% DMAP 北京华威锐科化工有限公司122.17分析纯99.00 乙醇 北京化工厂46.07分析纯99.70 正丙醇 天津市福晨化学试剂厂60.10分析纯99.80 异丙醇 北京化工厂60.10分析纯99.70 正丁醇 北京化工厂74.12分析纯99.00 异丁醇 天津市福晨化学试剂厂74.12分析纯99.00 乙酸甲酯 天津市光复精细化工研究所74.08分析纯98.00 乙酸乙酯 北京化工厂88.11分析纯99.50 乙酸丙酯 天津市光复精细化工研究所102.13分析纯98.00 乙酸异丙酯 天津市光复精细化工研究所102.13分析纯99.00 乙酸丁酯 北京化工厂116.16分析纯99.00 乙酸异丁酯 天津市光复精细化工研究所116.16分析纯98.501.3实验装置表1-3 实验的仪器设备 设备名称 型号 生产厂家 精密温度计 制冷和加热循环槽 0-50℃ MPG-10C型 上海精密科学仪器厂 上海一恒科技仪器有限公司 电子分析天平 Sartorius CP124S型 德国Sartorius公司 磁力搅拌器 85-1A型 巩义市于华仪器有限责任公司 激光发射器 JDW-3型激光电源 北京大学物理系 夹套溶解釜 定制 北京化工大学仪器厂 本实验用到的仪器设备列于表1-3。 实验装置主要包括激光监视系统、夹套溶解釜、磁力搅拌器、电子分析天平、制冷和加热循环槽等。激光监视系统是发射激光、接受激光、记录仪等组成的,激光具有单色性好、相干性高、方向性强的特点,应用到测定溶解度,可减少因人为目测试样溶解情况带来的误差。夹套溶解釜是一个双层玻璃的瓶子,外层接通循环水,使内层试样升温或降温,还具有保温功能,内层装实验试样,内层上方有两个瓶口,大瓶口以插有温度计的塞子为塞子,大瓶口加入溶剂或溶质,小瓶口接冷凝管,冷却逸出液面到达瓶口处的试样,减少试样的挥发。磁力搅拌器充分搅拌瓶内试样,加快溶质的溶解。电子分析天平用来称量溶剂、溶质的质量。制冷和加热循环槽是一个超级恒温水浴系统,通过设定循环槽的温度调整溶解釜的温度,确保在加入溶质的实验过程中为恒定温度下。http://ng1.17img.cn/bbsfiles/images/2015/09/20150927212
[b][color=#3e3e3e]氨基柱的使用[/color][color=#3e3e3e]和保养[/color][/b][color=#3e3e3e]按柱子说明书的方法去做即可,进口柱一般都有详细说明。不同品牌的柱子可能不尽相同。我的phenomenex色谱柱说明书上把氰基柱列为正相柱(其实也可用于反相色谱),保存时用异丙醇或正己烷。柱效下降时的清洗程序为:用做正相柱时其清洗过程为氯仿、异丙醇、二氯甲烷10倍柱体积依次冲洗;用做反相柱时其清洗过程为5%乙腈水溶液、四氢呋喃、95%乙腈10倍柱体积依次冲洗。[/color][b][color=#3e3e3e]氨基柱的使用:[/color][/b][color=#3e3e3e]需要注意的是,氨基柱的键合官能团氨丙基要比C18,C8柱的键合官能团C18,C8要容易水解,所以首先要做好其使用寿命稍逊的心理准备,特别是当你的使用条件是反相条件下时。反相条件下使用时,要特别注意控制PH值范围,PH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。所以,在使用后以及准备长时间放置该柱时,必要的清洗和将氨基柱保存于纯的有机溶剂中是很好的保养措施。有一种情况是,当使用氨基柱进行酸性物质如果汁的分析时(分析其中的糖份),酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。这时,Kromasil专家所给的建议是:用5~10倍的柱体积的含0.5~1.0%NH[/color][sub][color=#3e3e3e]3[/color][/sub][color=#3e3e3e]的50-50乙腈-水溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。[/color][b][color=#3e3e3e]氨基柱的清洗:[/color][/b][color=#3e3e3e]简单说起来,正相条件下使用的氨基柱你就参照硅胶柱的清洗方法;反相条件下使用的氨基柱你就参照C18的清洗方法。[/color][b][color=#3e3e3e]平时在正相条件下使用:[/color][/b][color=#3e3e3e]首先用50倍柱体积的异丙醇清洗,因异丙醇粘度较大可适当放低流速;之后,用50倍的甲醇清洗;之后,用异丙醇过渡回到平常使用的正相流动相,即可。[/color][b][color=#3e3e3e]平时在反相条件下使用:[/color][/b][color=#3e3e3e]缓冲盐应及时冲洗,以及不能直接用纯甲醇冲洗缓冲盐等,属常识就不作特别交待了。[/color][color=#3e3e3e]用50倍纯甲醇冲洗;之后,用异丙醇过渡后,用二氯甲烷冲洗色谱柱;之后,再用异丙醇过渡回来到甲醇条件下。[/color][color=#3e3e3e]这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等。[/color][color=#3e3e3e]其他一些通用小技巧如调转柱子低流速冲洗,在污染物累积在柱头时是比较有效的,不再赘述。[/color][color=#3e3e3e]最后,仍然建议:在实验室中做好定期柱效检测工作,是重要而有意义的。[/color]
氨基柱的维护保养,你做到了吗?在我做技术支持过程中发现用户对氨基柱的了解不是很多,这里我愿意把我对氨基柱的一点点了解与大家分享,有不对或遗漏之处,欢迎更正补充。 1.氨基柱是同时可以用于正相条件和反相条件的,这一点很多用户都已经知道;但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,对这一点的忽略可能会带给使用者一些麻烦。 2.对于新购买到的柱子,首先请注意打开分析测试说明书,了解柱子的保存溶剂。如果保存溶剂与你将要使用的流动相极性不同不会互溶,请先用异丙醇过渡。过渡过程中注意因异丙醇粘度较大,会导致柱压很高,适当调低流速即可。如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。 柱效检测: 我用于判断一个用户是否有经验的指标之一,是用户是否习惯配制一些柱效检测标准溶液。说到柱效检测,我可以向大家提供一个方法,而且很通用,你也可以用同样的标准溶液和流动相来检测硅胶柱和氰基柱。 流动相:10%乙酸乙酯+90%正己烷 流速1.0 标准溶液:乙苯(如乙苯找不动就用甲苯代替呗)+苯甲酸甲酯 检测波长254nm