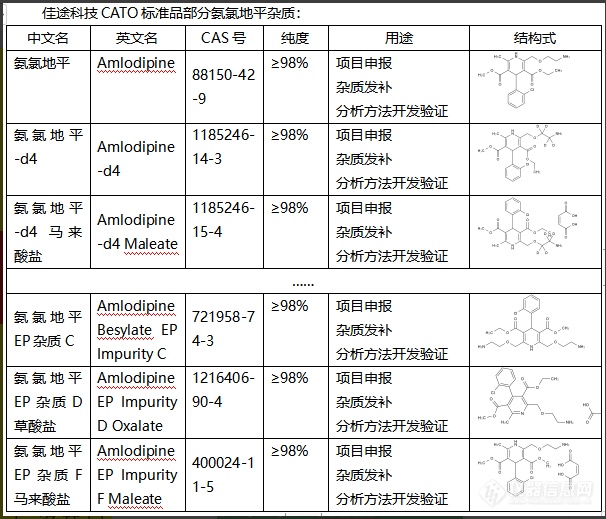
氨氯地平是一种常用的抗高血压药物,对于其中的杂质,氨氯地平杂质其作用主要体现在以下几个方面:1. 质量影响:杂质会影响氨氯地平的纯度和稳定性,可能会导致药品质量下降。2. 安全性影响:杂质可能会产生一些未知的副作用和毒性反应,影响药品的安全性。3. 药效影响:杂质可能会干扰氨氯地平的药效,使得药物的治疗效果降低。4. 法规因素:食品药品监管部门对药品中的杂质有严格的限制标准,过多的杂质可能会导致药品不能上市。CATO标准品对于氨氯地平这类药物的生产,控制和降低杂质的含量是非常注重的。[img=,606,519]https://ng1.17img.cn/bbsfiles/images/2024/02/202402041354066781_2922_6381668_3.png!w606x519.jpg[/img]
如题,俺第一次测盐酸左氧氟沙星,做有关物质时杂质A与左氧保留时间完全重叠,排除了乙酸铵、高氯酸钠等试剂滴原因,实在没辙咧,请教大虾帮忙。盐酸左氧氟沙星有关物质测定方法(来源:中国药典2010年版第一增补本): 有关物质 取本品,精密称定,加0.lmol/L盐酸溶液溶解并定量稀释制成每1ml中约含1.2mg的溶液,作为供试品溶液,精密量取适量,用0.1mol/L盐酸溶液定量稀释制成每1ml中含2.4ug的溶液,作为对照溶液。另精密称取杂质A对照品约18mg,置100ml量瓶中,加6mol/L氨溶液1ml与水适量使溶解,用水稀释至刻度,摇匀,精密量取2ml,置100ml量瓶中,用水稀释至刻度,摇匀,作为杂质A对照品溶液。照高效液相色谱法(附录V D)测定,用十八烷基硅烷键合硅胶为填充剂;以醋酸铵高氯酸钠溶液(取醋酸铵4.0g和高氯酸钠7.0g,加水1300ml使溶解,用磷酸调节pH值至2.2)-乙腈(85 :15)为流动相A,乙腈为流动相B;按下表进行线性梯度洗脱。柱温为40°C;流速为每分钟1ml。称取左氧氟沙星对照品、环丙沙星对照品和杂质E对照品各适量,加0.1mol/L盐酸溶液溶解并稀释制成每1ml中约含左氧氟沙星1.2mg、环丙沙星和杂质E各6ug的混合溶液,取10ul注人液相色谱仪,以294nm为检测波长,记录色谱图,左氧氟沙星峰的保留时间约为15分钟。左氧氟沙星峰与杂质E峰和左氧氟沙星峰与环丙沙星峰的分离度应分别大于2.0与2.5。量取对照溶液10ul注人液相色谱仪,以294mn为检测波长,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的20%。精密量取供试品溶液、对照溶液和杂质A对照品溶液各10ul,分别注人液相色谱仪,以294nm和238nm为检测波长,记录色谱图。供试品溶液色谱图中如有杂质峰,杂质A(238nm检测)按外标法以峰面积计算,不得过0.3%。其他单个杂质(294nm检测)峰面积不得大于对照溶液主峰面积(0.2%),其他各杂质(294nm检测)峰面积的和不得大于对照溶液主峰面积的2.5倍(0.5%)。供试品溶液色谱图中任何小于对照溶液主峰面积0.1倍的峰可忽略不计。时间(分钟) 流动相A(%) 流动相B(%) 0 100 0 18 100 0 25 70 30 39 70 30 40 100 0 50 100 0
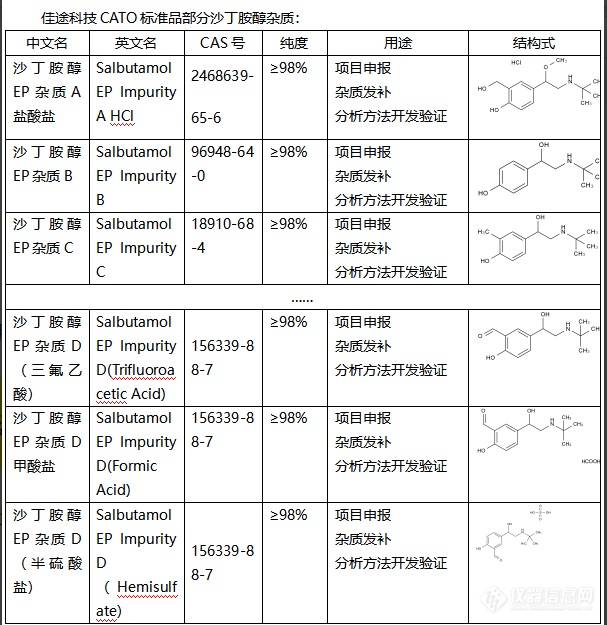
沙丁胺醇是一种药物,主要用于治疗哮喘和慢性阻塞性肺病等呼吸系统疾病。在药品制备过程中,可能会产生一些不同结构的化合物,这些化合物就被称为杂质。杂质可能会对药品的品质、安全性、效力和稳定性等产生影响。根据产生的差异,杂质的作用可以具体表现如下:1. 影响药品的稳定性:杂质可能导致药品在贮存过程中发生化学变化,从而影响药品的稳定性。2. 影响药品的安全性:如果杂质对人体有毒性,那么杂质的存在可能降低药品的安全性。3. 影响药品的效力:杂质可能与药品的有效成分发生竞争,导致药品的效力降低。4. 影响药品的品质:杂质可能改变药品的外观、颜色、溶解性等物理性质,影响药品的品质。CATO标准品制药行业对药品的杂质进行严格控制,保障药品的质量和患者的用药安全。[img=,607,625]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021631332927_8650_6381668_3.png!w607x625.jpg[/img]
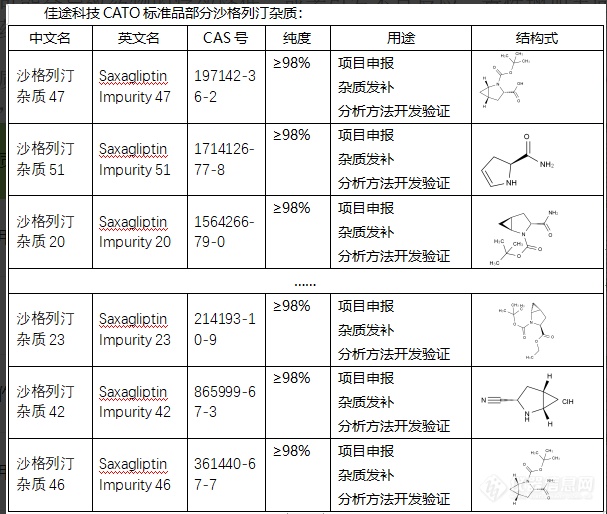
沙格列汀杂质可能是由制药过程中的化学反应产生,也可能是原料中的不纯物。当杂质的总量超过了允许的范围,可能会对药品的质量、安全性和疗效产生影响。例如,部分杂质可能会导致药物的疗效降低,或者引发不良反应、毒性增加等问题。因此,对于沙格列汀这类药物,对其杂质进行严格的检测和控制是保证药品质量的重要环节。只有将杂质控制在安全的范围内,才能保证药物的有效性和安全性。CATO标准品对沙格列汀杂质的研究也能帮助优化制药流程,找出产生过多杂质的环节,从而改进工艺,提高药品的质量和疗效。沙格列汀杂质可能是由制药过程中的化学反应产生,也可能是原料中的不纯物。[img=,607,514]https://ng1.17img.cn/bbsfiles/images/2024/02/202402052059405101_6177_6381668_3.png!w607x514.jpg[/img]
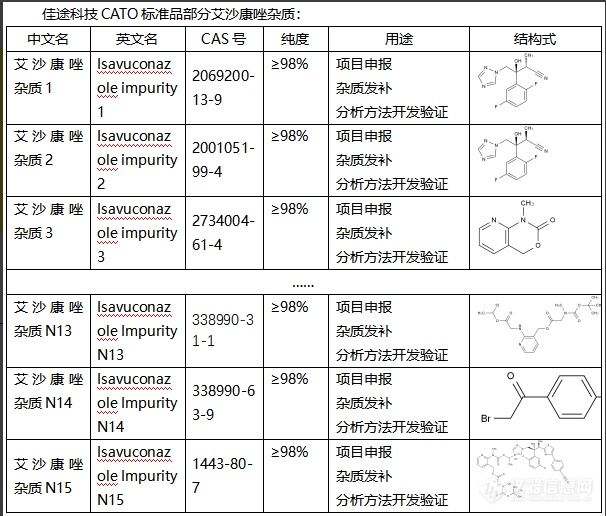
艾沙康唑是一种广谛抗真菌药,用于治疗各种真菌感染。然而,任何药物的生产过程中都可能会有杂质产生。艾沙康唑杂质的作用主要取决于杂质的性质。一些杂质可能无害,而一些杂质可能有害。有害的杂质可能会干扰艾沙康唑的抗真菌效果,增加药物的毒性,或引起不良反应。因此,药物生产中对杂质的控制是非常重要的。药品工艺需要设计成尽可能减少杂质的生成,并需要检测和控制杂质的含量,以确保药物的质量和安全。在药品注册时,也需要提交关于杂质的详细信息和控制策略。总的来说,艾沙康唑杂质对于药物的质量、疗效和安全性等都有重要影响,CATO标准品在药品的研发和生产过程中给予了足够的关注和控制。[img=,606,516]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021705445515_9017_6381668_3.png!w606x516.jpg[/img]
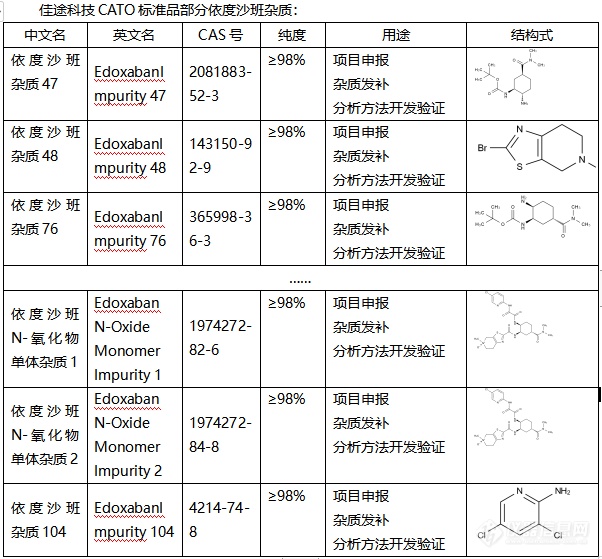
依度沙班,作为一种抗凝药物,被广泛应用于预防和治疗血栓形成。然而,与其他药物一样,依度沙班在生产过程中也可能产生杂质。这些杂质的存在可能会影响药物的安全性和有效性。为了确保依度沙班的质量,科学家们引入了CATO标准进行杂质分析。CATO标准是一种先进的分析方法,可以帮助研究人员准确地检测和衡量依度沙班中的杂质。通过对比和分析,我们可以清楚地了解杂质的种类、数量以及可能对药物产生的影响。这一标准的应用,不仅提高了依度沙班的生产质量,也为我们提供了一种有效的质量控制手段。在实际应用中,CATO标准品发挥着重要的作用。首先,它能够准确鉴定和量化依度沙班中的杂质,为药物的质量控制提供科学依据。其次,通过与标准品的比对分析,研究人员可以深入了解杂质的来源和性质,从而优化生产工艺,降低杂质的产生。此外,CATO标准品还可以用于评估杂质的毒性和风险,为药物的安全性评价提供有力支持。随着研究的深入,CATO标准在依度沙班杂质分析中的应用将不断优化和完善。通过科学的分析和严格的控制,我们能够确保依度沙班的安全性和有效性,为患者的健康提供更好的保障。同时,这也将推动药物生产的科技进步,造福更多患者。[img=,602,559]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021907159831_6894_6381568_3.png!w602x559.jpg[/img]广州佳途科技股份有限公司是一家专业的CATO标准品生产厂家,目前公司库存有全套乐伐替尼杂质,能够提供相应的系列图谱和产品COA证书,并且支持买家溯源。

[font=宋体]莫西沙星是一种广谱的抗生素,被广泛用于治疗很多种的细菌感染。莫西沙星杂质会影响到药物的安全性和有效性。[/font][font=宋体][/font][font=宋体][/font][font=宋体]1. 影响药物的安全性:如果莫西沙星中的杂质过多或是有毒性较高的杂质,可能会导致药品的毒副作用增加,影响到药品的安全应用。[/font][font=宋体][/font][font=宋体][/font][font=宋体]2. 影响药物的有效性:有一些杂质可能会与莫西沙星发生化学反应,改变其化学结构,从而降低其抗菌活性,影响治疗效果。[/font][font=宋体][/font][font=宋体][/font][font=宋体]3. 影响药物的稳定性:某些杂质可能会影响莫西沙星的稳定性,导致药物质量的降低。[/font][font=宋体][/font][font=宋体][/font][font=宋体]因此,对莫西沙星的杂质进行控制是非常重要的,相关监管部门也对其中的含量有着严格的标准。[/font][font=宋体][font=Calibri]CATO[/font][font=宋体]标准品[/font][/font][font=宋体]在药品的生产过程中,对杂质进行定期的检测和控制,以确保药品的质量。[img=,600,610]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021649392583_1508_6381668_3.png!w600x610.jpg[/img][/font]
工业生产中,采用甲醛与液氨反应,生成乌洛托品。再经结晶、离心机分离、干燥得到乌洛托品成品。已知甲醛会带入微量的甲酸及少量的甲醇,液氨中也有0.2%左右的油性杂质。成品中除了有小于0.5%的水份外,还含有什么杂质啊?
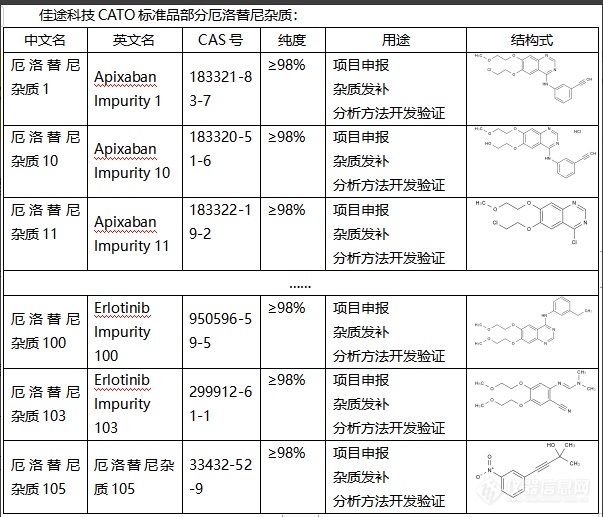
厄洛替尼杂质是药物制备过程中的副产品或污染物,可能会影响药物的安全性和有效性。常见的杂质有重金属、溶剂残留、有毒化合物等。对于厄洛替尼来说,杂质可能会影响其药效和安全性。一方面,杂质可能降低药物的纯度,从而降低其抑制肿瘤生长的效果。另一方面,某些杂质可能具有毒性或致敏性,可能导致患者出现不良反应。因此,对厄洛替尼的杂质进行检测和控制是药品质量控制的重要环节。这需要使用一种或多种分析方法,如高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法、[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法、质谱法等,以检测并定量药物中的杂质。CATO标准品针对可能的杂质源(如起始材料、反应条件、催化剂、溶剂等)进行控制,可以有效地减少杂质的生成。[img=,603,517]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021655361773_9862_6381668_3.png!w603x517.jpg[/img]
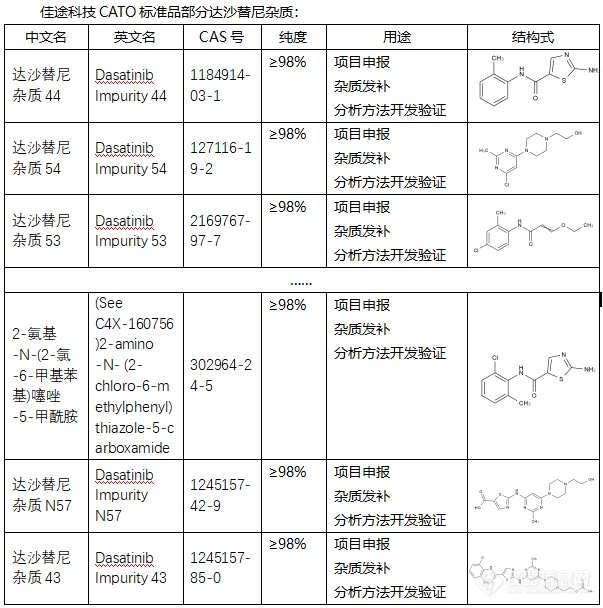
[font=宋体]◇达沙替尼[/font][font=宋体]杂质[/font][font=宋体] 达沙替尼[/font][font=宋体],[/font][font=宋体]其英文名为[/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]Dasatinib[/back][/color][/font][font=宋体][color=#05073b][back=#fdfdfe],)是一种创新的第二代双重酪氨酸激酶抑制剂(TKI),也被称作DASA锡IB或商品名SPRYCEL(施达赛)。[/back][/color][/font][font=宋体]达沙替尼[/font][font=宋体][font=宋体]杂质过抑制[/font][font=Calibri]BCR-ABL[/font][font=宋体]蛋白的活性来发挥治疗作用。达沙替尼能够与[/font][font=Calibri]BCR-ABL[/font][font=宋体]蛋白结合并抑制其激酶活性,从而阻断白细胞的异常增殖,并促进正常白细胞的生成。[/font][/font][font=宋体][font=Calibri] CATO[/font][font=宋体]标准品提供的达沙替尼杂质用途主要是用于分析化学物质和质量控制的化学物质。[img=,603,608]https://ng1.17img.cn/bbsfiles/images/2024/02/202402062123365450_9441_6381607_3.png!w603x608.jpg[/img][/font][/font][font=宋体][font=宋体] 广州佳途科技股份有限公司,[/font][font=Calibri]CATO[/font][font=宋体]标准品厂家,提供达沙替尼全套[/font][/font][font=宋体]的[/font][font=宋体]杂质,通过全面的检测、高效的沟通、专业的服务和完善的售后,确保所有产品均能现货供应[/font][font=宋体],[/font][font=宋体]致力于为客户提供高质量的产品和优质的服务,以满足客户在药物研发和质量控制方面的需求。[/font]
高纯石英沙99.996%以上的样品,如何检测杂质含量,如Fe、Cu、mg、Ni、Na、Co等元素
[B][center]药物中杂质的来源及杂质限量检查[/center] [/B]药物只有合格品与不合格品;一般化学试剂分为4个等级(基准试剂、优级纯、分析纯、化学纯) [B]药物中一般杂质检查 [/B][B]氯化物为一指示性杂质。[/B] 通过对氯化物的控制,可同时控制与氯化物结合的一些阳离子以及某些同时生成的副产物。可从氯化物检查结果显示药物的纯度,间接考核生产、贮藏过程是否正常。 1. 原理 药物中微量的氯化物在硝酸酸性条件下与硝酸银反应,生成氯化银的胶体微粒而显白色浑浊,与一定量的标准氯化钠溶液在相同条件下产生的氯化银浑浊程度比较,判定供试品中氯化物是否符合限量规定。 Ag+ + Cl- → AgCl ↓ [B]硫酸盐检查法 [/B] 1. 原理 药物中微量的硫酸盐在稀盐酸酸性条件下与氯化钡反应,生成硫酸钡的微粒而显白色浑浊,与一定量的标准硫酸钾溶液在相同条件下产生的硫酸钡浑浊程度比较,判定供试品中硫酸盐是否符合限量规定。 [B]铁盐检查法 [/B]硫氰酸盐法 巯基醋酸法 砷盐检查法 1. 古蔡氏法 1. 原理 金属锌与酸作用产生新生态的氢,与药物中微量砷盐反应生成具挥发性的砷化氢,遇溴化汞试纸产生黄色至棕色的砷斑,与同条件下一定量标准砷溶液所生成的砷比较斑,判断砷盐的含量。 [B]硒、氟及硫化物检查法 [/B]1. 氧瓶燃烧法 适用于以共价键结合的卤素、硫、硒的有机药物。 本法系将有机药物防入充满氧气的密闭燃烧瓶中进行燃烧,将燃烧所产生的欲测组分吸收于适当的吸收液中,然后根据欲测组分的性质,选用合适的分析方法进行鉴别、检查或含量测定。 [B]注意事项及讨论 [/B]1. 根据被燃烧分解的样品量选用适宜大小的燃烧瓶。 2. 测定氟化物时应改用石英燃烧瓶。 1. 硒检查法 (1). 操作方法 样品与对照品液,调节Ph2.0±0.2,加盐酸羟胺,二氨基萘,比色。 [B]硫化物检查法 [/B] 方法同砷盐检查第一法,不装醋酸铅棉花,以醋酸铅试纸代替溴化汞试纸。 标准液取1ml 5/ml [B]澄清度检查法 [/B]将一定浓度的供试品溶液与浊度标准液分别置于配对的比浊用玻璃管,同置黑色背景上,在漫射光下观察。浊度标准液 硫酸肼与乌洛托品溶液混合分五个等级,未超过0.5等级即为澄清。BP98规定未超过1等级即为澄清。 [B]溶液颜色检查法 [/B]CHP2000 [B]1. 比色法[/B] 色调标准贮备液 黄色液 重铬酸钾液(BP98用氯化铁) 红色液 氯化钴液 蓝色液 硫酸铜液 配成各种色调色号标准比色液共50种。 [B]2. 分光光度法 [/B] [B]易碳化物检查法 [/B]检查药物中含有的遇硫酸易碳化或易氧化而呈色的有机杂质。 对照品液 样品液 加硫酸5后,加供试品。 [B]炽灼残渣检查法[/B] 取供试品1.0~2.0g或个药品项下规定的重量,置已炽灼至恒重的坩埚中,精密称定,缓缓炽灼至完全碳化,放冷至室温;除另有规定外,加硫酸使湿润,低温加热至硫酸蒸气除尽后,在700~800炽灼使完全灰化,移至干燥器内,放冷至室温,精密称定,再在700~800炽灼至恒重,即得。残渣限量一般为0.1~0.2% 一般应使炽灼残渣量为1~2mg 若需将炽灼残渣留作重金属检查时,炽灼温度必须控制在500~600。 [B]干燥失重测定 [/B]1. 常压恒温干燥法 2. 干燥剂干燥法 3. 减压干燥法 [B]水分测定法 [/B][B]费休氏法 [/B] 本法是根据碘和二氧化硫在吡啶和甲醇溶液中能与水起定量反应的原理以测定水分。 [B]甲苯法[/B] 在加热状态下,甲苯夹带着水分蒸出,收集蒸出的水分测定。 [B]药物中特殊杂质检查 [/B] [B]一、物理法 [/B] [B]二、化学反应法 [/B](一)容量分析法 (二)重量分析法 (三)比色法和比浊法 [B]三、色谱法 [/B]1.纸色谱法 薄层色谱法 TLC是药典中最常用的特殊杂质限量检查方法。 1.在一定供试品及检查条件下,不允许有杂质斑点存在 2.以待测杂质对照品检测 3.将供试品稀释到适当浓度作为杂质对照品溶液 4.选用质量符合规定的与供试品相同的药物作为杂质对照品 [B]高效液相色谱法 [/B] [B][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法 [/B] 1.面积归一化法 2.主成分自身对照法 3.内标法测定 4.内标法加校正因子法 5.外标法 有机溶剂残留量测定法 [B]分光光度法 紫外分光光度法 比色法 [url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度法[/B]
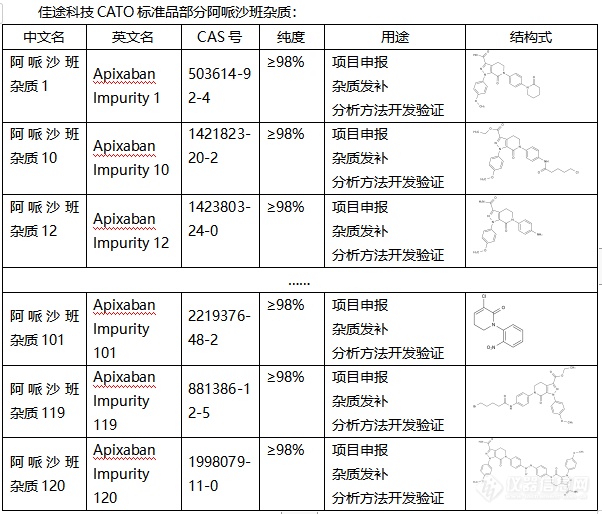
◇关于阿哌沙班杂质 阿哌沙班杂质是用于髋关节或膝关节择期置换术的成年患者,预防静脉血栓栓塞的杂质,阿哌沙班是一种结构新颖的中性双环吡唑,分子量为459.5 g/mol,水溶性为 40–50 μg/mL,Caco-2细胞渗透率为0.9?×?10?6 cm/s。阿哌沙班是通过抑制凝血因子Xa来发挥抗凝作用,阿哌沙班杂质的吸收主要发生在小肠。与其它的杂质相比,阿哌沙班杂质疗效更好,安全性更高。[font=UICTFontTextStyleBody]CATO[/font]标准品提供的[font=宋体]阿哌沙班杂质[/font][font=宋体],是抗凝[/font][font=宋体][font=宋体]剂领域的[/font]“领头羊”[/font][font=宋体]。[img=,602,514]https://ng1.17img.cn/bbsfiles/images/2024/02/202402040843332660_3775_6381607_3.png!w602x514.jpg[/img][/font]
机械杂质就是指存在于润滑油中不溶于汽油、乙醇和苯等溶剂的沉淀物或胶状悬浮物。机械杂质来源于润滑油的生产、贮存和使用中的外界污染或机械本身磨损,大部分是砂石和积碳类,以及由添加剂带来的一些难溶于溶剂的有机金属盐。 机械杂质的测定按GB/T 511-83石油产品和添加剂机械杂质测定法(重量法)进行。其过程是:称取100g的试油加热到70℃到80℃,加入2-4倍的溶剂,在已衡重的空瓶中的纸上过滤,用热溶剂洗净滤纸瓶再称重,定量滤纸的前后重量之差就是机械杂质的重量,由此求出机械杂质的质量分数。 机械杂质和水分、灰分、残炭都是反映油品纯洁性的质量指标,反映油品精制的程度。一般来讲润滑油基础油的机械杂质的质量分数都应该控制在0.005%以下(机械杂质在此以下认为是无),加剂后成品油的机械杂质一般都是增大,这是正常的。对用户来讲,测定机械杂质也是必要的,因为润滑油在使用、存储、运输中混入灰尘、泥沙、金属碎屑、铁锈及金属氧化物等,这些杂质的存在,将加速机械设备的磨损,严重时堵塞油路、油嘴和滤油器,破坏正常润滑。另外金属碎屑在一定的温度下,对油起催化作用,应该进行必要的过滤。但是,对于一些加有 添加剂油品的用户来讲,机械杂质的指标表面上看是大了一些(如一些的内燃机油),但其杂质主要是加入了多种添加剂后所引入的溶剂不溶物,这些胶状的金属有机物,并不影响使用效果,用户不应简单地用“机械杂质”的大小去判断油品的好坏,而是应分析“机械杂质”的内容,否则,就会带来不必要的损失和浪费
9种水中的杂质( 1、微粒物质(Particulate Matter)包括泥沙、铁锈、藻类、悬浮物、微纤维等微粒杂质,肉眼可见。这些微粒常常悬浮在水流之中,水产生的浑浊现象。这些微粒很不稳定,可以通过沉淀和过滤而除去。水在静置的时候,重的微粒(主要是砂子和粘土一类的无机物质)会沉下来。轻的微粒(主要是动植物及其残骸的一类有机化合物)会浮于水面上,用预沉,过滤等分离方法可以除去。 微粒物质是造成浊度、色度、气味的主要来源。自来水、二次供应的自来水、江河湖泊水中均可能存在。 2、胶体物质 胶体物质是比离子物质大而比颗粒物质小、直径在10-4~10-6mm之间的微粒。胶体是许多分子和离子的集合物。天然水中的无机矿物质胶体主要是铁、铝和硅的化合物。水中的有机胶体物质主要是植物或动物的肢体腐烂和分解而成的腐殖物。其中以湖泊水中的腐殖质含量最多,因此常常使水呈黄绿色或褐色。 胶体颗粒不能藉重力自行沉降而去除,一般是在水中加入药剂破坏其稳定,使胶体颗粒增大而沉降予以去除。 地表水或地下水都可能存在胶体物质。 3、离子物质(Ionic material) 包括:阳离子、阴离子。阳离子如钙离子、镁离子、铁离子等;阴离子氯离子、硫酸盐离子、磷酸盐离子等。 离子物质通常易溶于水中,溶解物质可以用离子交换或除盐等方法予以去除。 4、不反应的溶解气体 如空气中的氮气等。 5、可反应的溶解气体 天然水中常见的溶解气体有氧气(O2)、二氧化碳(CO2)、有时还有硫化氢(H2S)、二氧化硫(SO2)、氮气(N2)和氨 (NH3)等。这些溶解于水中的气体,大都对金属有腐蚀作用,是引起水系统金属腐蚀的重要因素。 空气中的CO2对纯水影响最大。CO2存在于空气中并很容易溶于水中,使水质呈酸性,即PH值低于7。水质越纯,越易受空气的影响,影响主要表现为PH值、电导(阻)率。 6、微生物 主要指水中的细菌含量。中国自来水的常规细菌允许含量<100cfu/ml;纯水的常规细菌允许含量<1cfu/ml。 7、热源 热源又称细菌内毒素,主要用于医药用水特别是注射用水时需考量热源的含量控制。实验室中有细胞培养等生物方面的应用时,对热源用含量控制要求。 8、有机物质 水中的有机物质主要是指腐殖酸、生活污水和工业废水的污染物。腐殖物质是水生生物一类的生命活动过程的产物。这些有机物污染着水体,并使水质恶化。 水中的有机物有个共同特点,就是要进行生物氧化分解,需要消耗水中的溶解氧,而导致水中缺氧。同时会发生腐败发酵,使细菌滋长,恶化水质,破坏水体;工业用水的有机污染,还会降低产品的质量。有机物是引起水体污染的主要原因之一。 地表水中有机物含量通常高于地下水中的含量。 9、残留消毒剂 自来水公司为控制水中的细菌含量,会添加消毒剂来控制总细菌数。常用的消毒剂为含氯制剂,当氯加到水中会产生含氧化性极强的化合物如余氯,起到消毒杀菌的作用。 对于采用反渗透技术的水处理设备而言,氧化性极强的余氯会对RO膜造成很大的损伤,因此在预处理中必须严格去除。常用活性碳吸附去除。
作者:李寅;陈凤仪;张国添;杨辉;黄玉玲;谢清春;钟鸣; (广州市番禺区中心医院;广东药学院药物研究所;广州汉方现代中药研究开发有限公司;)摘要:目的:测定厄贝沙坦在人血浆中的蛋白结合率。方法:采用HPLC法测定厄贝沙坦的浓度。采用平衡透析法测定厄贝沙坦的人血浆蛋白结合率。结果:以Diamonsil C18(4.6 mm×250 mm,5μm)为色谱柱,以乙腈-0.02 mol/L磷酸二氢钾水溶液(磷酸调pH至2.6)(45∶55)为流动相,检测波长为245 nm,血浆样品中其他成分不干扰厄贝沙坦的测定,厄贝沙坦的线性范围为0.10~10.40μg/ml,定量下限为0.10μg/ml。厄贝沙坦的低、中、高浓度的蛋白结合率分别为93.0%、91.5%、92.3%。结论:厄贝沙坦具有较强的蛋白结合率。谱图:无
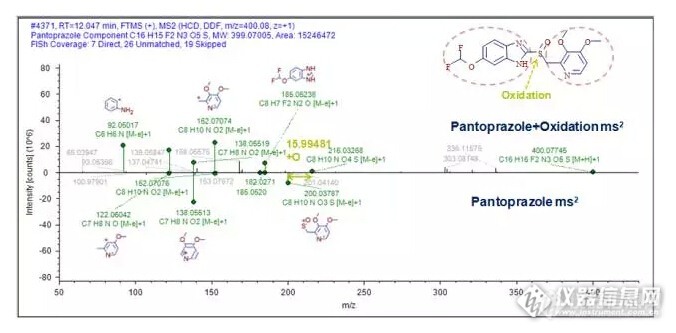
药物杂质是药物活性成分(原料药)或药物制剂中不希望存在的化学成分,会对用药的安全性和有效性带来隐患,因此杂质的检测是保证药物质量至关重要的部分,FDA、EMEA、PMDA、CFDA等各国药品监管部门制定了相应的指导原则对其进行严格管控。http://ng1.17img.cn/bbsfiles/images/2015/12/201512141737_577892_3005330_3.jpg 独有的四极杆静电场轨道阱Q Exactive™ Focus高分辨液质联用技术,凭其高灵敏度、高专属性和高准确性的分析能力,可对样品中药物杂质进行全面的信息采集。结合新一代的智能小分子化合物鉴定软件Compound Discoverer™,以高度灵活的自定义方式制定分析工作流程,对数据中的目标和非目标杂质进行提取、比对及鉴定,工作流程如下:http://ng1.17img.cn/bbsfiles/images/2015/12/201512141737_577893_3005330_3.jpg 通过软件对样品数据的分析和提取,在Compound Discoverer中可以直观、便捷的查看和筛选预期和未知的杂质分析结果,从结果界面中可获得不同条件下样品杂质的变化情况,获得所有杂质保留时间、一级质谱、同位素和二级质谱等丰富信息:http://ng1.17img.cn/bbsfiles/images/2015/12/201512141738_577894_3005330_3.jpg 在获得母药和杂质的一级和二级质谱信息后,软件将调用碎裂数据库(Fragmentation Library)快速的对泮托拉唑的碎片结构进行归属,该数据库几乎涵盖了所有已发表的文献,保证了碎片解析的准确性。在此研究结果之上,通过软件对杂质与母药二级质谱信息之间的比对,可进一步对杂质变化位点进行推测。在本例中,通过152、185等共有碎片和200、216等特征差异碎片的比对,推测出该杂质为泮托拉唑砜:http://ng1.17img.cn/bbsfiles/images/2015/12/201512141738_577895_3005330_3.jpg 基于新一代四极杆-静电场轨道阱质谱Q Exactive Focus和新一代小分子化合物分析软件Compound Discoverer,建立了药物杂质鉴定的新流程。无论是优质数据的有效获取,还是获取后对已知和未知杂质的分析鉴定,该工作流程都可以完美的实现。在本例中,共鉴定到泮托拉唑杂质15个,其中可能的降解杂质9个,可能的工艺杂质6个,为药物杂质的质量控制、安全性评估提供了富有价值的信息。(分享)
莫西沙星有关物质分析方法采用USP43制剂方法测定,色谱柱:Inertsil Phenyl 4.0*250mm,5μm,其中杂质A的校正因子0.70,药典方法1.89.相差很大,大家有没有遇到这个问题?
求助:给位大侠,有没有做过氧氟沙星氯化钠注射液的??我一直弄不明白2010药典对杂质的计算,各位如果做过,麻烦发一张积分图谱,如果有数据报告最好,谢谢注:双波长的转换我会做,就是不知道哪个是我所需要的峰?
石油产品机械杂质测定的作用及意义1、什么叫做试油的机械杂质?答:试油中的机械杂质是指存在于油品中所有不溶于溶剂(汽油,苯)的沉淀状或悬浮状物质。这些杂质多由砂子,粘土、铁屑粒子等组成。现行方法测出的杂质也包括了一些不溶于溶剂的有机成份,如碳青质和碳化物等。2、油品中机械杂质对机组运行以下危害:(1)可引起调速系统卡涩和机组的转动部分磨损等潜在故障。(2)引起绝缘油的绝缘强度、介质损耗因数及体积电阻率等电气性能下降。(3)影响汽轮机油的乳化性能和分离空气的性能。。(4)堵塞滤油器和滤网,影响油箱油位的显示,磨损油泵齿轮。(5)影响变压器散热,引起局部过热故障
石油产品机械杂质测定的作用及意义1、什么叫做试油的机械杂质?答:试油中的机械杂质是指存在于油品中所有不溶于溶剂(汽油,苯)的沉淀状或悬浮状物质。这些杂质多由砂子,粘土、铁屑粒子等组成。现行方法测出的杂质也包括了一些不溶于溶剂的有机成份,如碳青质和碳化物等。2、油品中机械杂质对机组运行以下危害:(1)可引起调速系统卡涩和机组的转动部分磨损等潜在故障。(2)引起绝缘油的绝缘强度、介质损耗因数及体积电阻率等电气性能下降。(3)影响汽轮机油的乳化性能和分离空气的性能。。(4)堵塞滤油器和滤网,影响油箱油位的显示,磨损油泵齿轮。(5)影响变压器散热,引起局部过热故障。
氟康唑杂质可能来自原料药、副反应产物或分解产物,以及其在存储过程中可能发生的变化。这些杂质如果未被及时检测和控制,可能对药物的效力和安全性产生影响,包括药效降低、不良反应增加等。因此,检测和控制氟康唑中的杂质是药品生产过程中的重要环节,对药物质量、安全性以及疗效的保证至关重要。研究分析这些杂质,还可以优化生产工艺,减少杂质产生,提高药物的质量和疗效。CATO标准品对沙格列汀杂质的研究也能帮助优化制药流程,找出产生过多杂质的环节,从而改进工艺,提高药品的质量和疗效。[img=,603,570]https://ng1.17img.cn/bbsfiles/images/2024/02/202402052101491000_1515_6381668_3.png!w603x570.jpg[/img]
如何除石油产品中的杂质 石油里的成分主要是碳氢化合物,但同时还有不少含有硫、氮和氧的化合物,以及微量的金属。它们大多是有害物质。含硫的化合物中有的本身就具有腐蚀性。而它燃烧后生成的二氧化硫和三氧化硫遇水会变成亚硫酸和硫酸。它们更是强腐蚀性物质。石油中的含氧化物大多带有酸性,尽管石油酸有特殊的用途,但是在石油产品中还是属于有害成分。石油中的含氮化合物则多半带有碱性,会使有些催化剂中毒。此外,轻油中的砷以及重油中的镍、钒等也都是对催化剂有害的物质,均属于要脱除的物质。 所以,这些杂质是非要除掉不可的。目前,普遍采用的精制方法是加氢精制。所谓加氢精制是指在较高的压力和温度下,使石油产品中的硫、氮、氧与外加的氢气反应,生成气态的硫化氢、氨和水,从而得到比较干净的液体石油产品。通过加氢,同时还可以除去油中的金属杂质。 加氢精制技术的核心是它所用的催化剂。此类催化剂的品种很多,性能有别、牌号各异,但是万变不离其宗。其活性组分都离不开钴、钼、镍、钨这几种元素,同时一般都是以氧化铝为载体,有时也加入一些分子筛。 有些原油中硫含量高,近年来对汽油等燃料的质量要求越来越高,对含硫量的限制越来越严,所以加氢精制已是必不可少的步骤。有些原油含氮较多,可是脱除氮要比脱除硫更困难些。为此,我国专门研制出了脱氮性能优越的加氢精制催化剂。 加氢精制的操作条件得根据原料所含杂质的性质和数量以及对产品质量的要求来确定。其反应温度的范围很宽,在300摄氏度至400摄氏度,而压力的范围更宽,低的只有十几个大气压(约1兆帕),高的会达100多个大气压(约10兆帕),几乎相差十倍之多。
不能的X射线管有不同的杂质线,大家结合各类X射线管讨论一下不同的X射线管有哪些杂质线,方便我们分析这些元素,注意背景的扣除。
ICP--AES法测定仲钨酸铵中杂质元素 张云芒 仲钨酸铵的成品纯度要求较高,其杂质含量通常在0—0.1%之间。因杂质含量较低,而仲钨酸铵的含量较高,样品溶液进入ICP—AES之后,钨产生的谱线对被测元素干扰较大,其信号强度甚至超过被测元素本身所产生的。因而,需要除去钨,鉴于钨酸的特性,综合考虑采用沉淀分离法使基体钨酸从溶液中分离出来。分离效果较为明显。实验部分一, 仪器与设备(1) ICP—1000II(北京豪威量科技有限公司);a功率:1000w;b阳压:2460v;c阳流:0.74A;d栅流:0.16A;e等离子:800L/H;f雾化气:0.16MPa(2) 分析天平:精确度达到 0.0001g。 (3) 玻璃棒,烧杯,漏斗,定量滤纸,聚四氟烧杯。容量瓶:50ml,100ml。移液管。所有的器皿在使用前都应用 10% (v/v )的硝酸清洗。(4) 可调节电热炉。二, 试剂1,水:蒸馏水。2,硝酸:ρ(HNO3 ) = 1.42 g/mL。优级纯。 3,盐酸:ρ(HCl) = 1.19 g/mL。 优级纯。4,氨水(氢氧化铵):25%—28%,优级纯。5,过氧化氢:30%,优级纯。 6,定量滤纸。三, 样品处理准确称取样品1.0000g,并作平行样。置于标记的聚四氟乙烯坩埚中,加氨水15ml。盖坩埚盖,室温下放置4h以上。加上过氧化氢10ml,盖上坩埚盖,将坩埚放到垫有耐火的电热板上加热使其微沸30分钟左右。取下,加过氧化氢10ml,盖盖,继续微沸30分钟,使样品分解完全。除去坩埚盖,加入盐酸或硝酸5ml,加热蒸至近干,再加入盐酸5ml,加热取下。加入沸水20ml,搅拌均匀。过滤,用水洗涤沉淀若干次,弃去滤渣。将滤液冷却至室温,定容至50ml容量瓶中,备用。(注:由于容量瓶小,所以洗涤沉淀用水要多次少量。) 四, 标准制备配制标准溶液如下,单位mg/ml元素 P Sn As Si Cu Mg Mo标准1 20 20 20 20 8 8 8标准2 4 4 4 4 1.6 1.6 1.6标准3 1 1 1 1 0.4 0.4 0.4在计算机输入时,其换算结果如下:A称样1.0000g,定容至50ml容量瓶中。其浓度为:20mg/ml元素 P Sn As Si Cu Mg Mo标准1 0.1% 0.1% 0.1% 0.1% 0.04% 0.04% 0.04%标准2 0.02% 0.02% 0.02% 0.02% 0.008% 0.008% 0.008%标准3 0.005% 0.005% 0.005% 0.005% 0.002% 0.002% 0.002%五, 测试样品开机后,调试仪器各个条件如“一”中。建立方法,吸取“四”中所配置的系列标准液制作标准曲线。然后,一次吸入样品,测得结果打印。如下:单位:%,即样品中的百分含量。 P As Sn Si Mg Cu Mo36(1) 0.0041 0.0027 0.0000 0.0020 0.0013 0.0004 0.000136(2) 0.0042 0.0027 0.0000 0.0021 0.0013 0.0003 0.000112(1) 0.0034 0.0026 0.0000 0.0024 0.0018 0.0004 0.000012(2) 0.0034 0.0026 0.0000 0.0025 0.0018 0.0004 0.0000六, 总结本次测试,样品处理是关键,处理起来需要耐心仔细。结果回传送样方,其结果基本与第三方检测基本吻合。实验人:张云芒
各位大佬,求助!!今天遇到过ICP测杂质铁的时候,结果偏高的情况,259.940谱线左背景有较大干扰峰,设置了不带入计算,那么左边背景还会对结果有影响吗?要想解决这个问题有什么好的建议吗?
ICP--AES法测定仲钨酸铵中杂质元素 张云芒 仲钨酸铵的成品纯度要求较高,其杂质含量通常在0—0.1%之间。因杂质含量较低,而仲钨酸铵的含量较高,样品溶液进入ICP—AES之后,钨产生的谱线对被测元素干扰较大,其信号强度甚至超过被测元素本身所产生的。因而,需要除去钨,鉴于钨酸的特性,综合考虑采用沉淀分离法使基体钨酸从溶液中分离出来。分离效果较为明显。实验部分一, 仪器与设备(1) ICP—1000II(北京豪威量科技有限公司);a功率:1000w;b阳压:2460v;c阳流:0.74A;d栅流:0.16A;e等离子:800L/H;f雾化气:0.16MPa(2) 分析天平:精确度达到 0.0001g。 (3) 玻璃棒,烧杯,漏斗,定量滤纸,聚四氟烧杯。容量瓶:50ml,100ml。移液管。所有的器皿在使用前都应用 10% (v/v )的硝酸清洗。(4) 可调节电热炉。二, 试剂1,水:蒸馏水。2,硝酸:ρ(HNO3 ) = 1.42 g/mL。优级纯。 3,盐酸:ρ(HCl) = 1.19 g/mL。 优级纯。4,氨水(氢氧化铵):25%—28%,优级纯。5,过氧化氢:30%,优级纯。 6,定量滤纸。三, 样品处理准确称取样品1.0000g,并作平行样。置于标记的聚四氟乙烯坩埚中,加氨水15ml。盖坩埚盖,室温下放置4h以上。加上过氧化氢10ml,盖上坩埚盖,将坩埚放到垫有耐火的电热板上加热使其微沸30分钟左右。取下,加过氧化氢10ml,盖盖,继续微沸30分钟,使样品分解完全。除去坩埚盖,加入盐酸或硝酸5ml,加热蒸至近干,再加入盐酸5ml,加热取下。加入沸水20ml,搅拌均匀。过滤,用水洗涤沉淀若干次,弃去滤渣。将滤液冷却至室温,定容至50ml容量瓶中,备用。(注:由于容量瓶小,所以洗涤沉淀用水要多次少量。) 四, 标准制备配制标准溶液如下,单位ug/ml元素 P Sn As Si Cu Mg Mo标准1 20 20 20 20 8 8 8标准2 4 4 4 4 1.6 1.6 1.6标准3 1 1 1 1 0.4 0.4 0.4在计算机输入时,其换算结果如下:A称样1.0000g,定容至50ml容量瓶中。其浓度为:20mg/ml元素 P Sn As Si Cu Mg Mo标准1 0.1% 0.1% 0.1% 0.1% 0.04% 0.04% 0.04%标准2 0.02% 0.02% 0.02% 0.02% 0.008% 0.008% 0.008%标准3 0.005% 0.005% 0.005% 0.005% 0.002% 0.002% 0.002%五, 测试样品开机后,调试仪器各个条件如“一”中。建立方法,吸取“四”中所配置的系列标准液制作标准曲线。然后,一次吸入样品,测得结果打印。如下:单位:%,即样品中的百分含量。 P As Sn Si Mg Cu Mo36(1) 0.0041 0.0027 0.0000 0.0020 0.0013 0.0004 0.000136(2) 0.0042 0.0027 0.0000 0.0021 0.0013 0.0003 0.000112(1) 0.0034 0.0026 0.0000 0.0024 0.0018 0.0004 0.000012(2) 0.0034 0.0026 0.0000 0.0025 0.0018 0.0004 0.0000六, 总结本次测试,样品处理是关键,处理起来需要耐心仔细。结果回传送样方,其结果基本与第三方检测基本吻合。实验人:张云芒
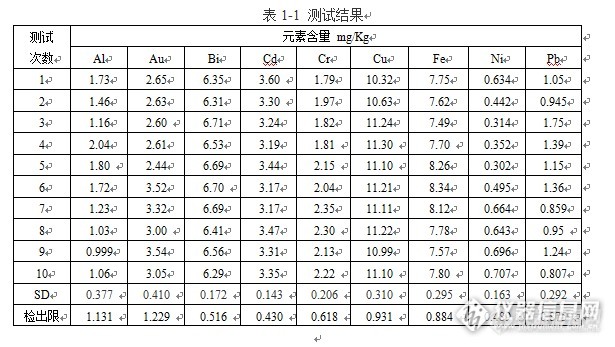
[align=center][b]火花直读光谱法测定银中杂质元素的检出限探讨[/b][/align][align=center]张帆(南京质检院NQI)[/align][color=#333333] 火花[url=https://baike.so.com/doc/6549047-6762794.html][color=#333333]直读光谱仪[/color][/url]以其分析速度快,准确度高,适用波长范围较宽,可在同一分析条件下对样品中多种元素同时进行分析测试,并且线性范围宽,可做高含量分析而在金属材料生产和检测企业受到广泛的应用,随着银饰品由以前的作坊式生产逐渐变成企业量化生产,应用火花直读光谱进行银料的测试越来越受到银饰品生产企业的青睐。[/color]本文通过实验给出了火花直读光谱仪检测银中杂质元素的检出限,并探讨了检出限的影响因素,为银中杂质元素的检测提供数据基础。 实验使用德国AMETEK SPECTRO火花直读光谱仪,型号:LAB LAVM11。外部配有稳压器及氩气净化装置,检测波长范围:120nm-780nm。分光装置为帕邢-龙格装置。光学系统为密封充氩自循环系统。采用火花倍增管与CCD结合的检测器。 火花直读光谱分析曲线采用基体元素银为内标元素,根据其他元素干扰情况和浓度灵敏度选择分析线,检出限的测定方法为:使用银含量﹥99.99%的样品重复测定10次,计算其标准偏差(SD),用3倍的标准偏差做为检出限。样品检测结果见表1-1及1-2。由实验结果可知,银中杂质元素的检出限在0.311mg/Kg-1.229mg/Kg之间,铝、金和铂的检出限略高,金的检出限略高是由于火花台底座受到金基体样品污染所致。[img=,690,337]http://ng1.17img.cn/bbsfiles/images/2017/08/201708251438_01_3048281_3.png[/img][img=,682,339]http://ng1.17img.cn/bbsfiles/images/2017/08/201708251438_02_3048281_3.png[/img] 检出限的影响因素。[color=#333333]要获得较低的检出限,首先需要火花直读光谱仪具有较好的稳定性,其稳定性影响因素主要有:[/color][color=#333333]1.[/color][color=#333333]此型号火花直读光谱的光室要求工作温度较低,为[/color][color=#333333]17℃[/color][color=#333333],虽然仪器内部配有空气冷却系统,但室内温度过高会导致制冷用压缩机超负荷工作,温度过高也会导致光室温度不能降到工作温度,无法测试,因此夏季应注意仪器室内温度最好控制在[/color][color=#333333]25℃[/color][color=#333333]以下,避免阳光直射在设备上,且保持室内温度稳定,以免由于光室温度不稳定影响数据的稳定性;[/color][color=#333333]2.[/color][color=#333333]仪器最好保持开机状态,如果必须要关机,则再开机后需等待[/color][color=#333333]4[/color][color=#333333]小时以上,待仪器状态稳定再进行测试。除了仪器要有较好的稳定性,测定检出限的样品也要满足以下几点:[/color][color=#333333]1.[/color][color=#333333]样品表面应平整、激发时不漏气;[/color][color=#333333]2.[/color][color=#333333]样品表面无其它杂质污染;[/color][color=#333333]3[/color]样品中元素分布均匀性越高越好,分布不均会导致检出限偏高;4.样品应选择基体纯度高且含有所需的杂质元素,并且每种元素含量较低为佳。为获得准确的检出限还应注意,不同基体单独使用一套配件,更换基体配件时,要彻底清洁干净,避免不同基体样品间相互污染的问题。
我做的产品的峰背上出现了一个杂质小峰,浓度都缩小时两个峰之间有一分钟的差距,但是产品的浓度要是变大的话,杂质就在产品的背上出峰,流动相的比例,波长之间能改的都改了,都不行,求助一下哥哥姐姐,我要用什么型号的柱子才能将它分开????
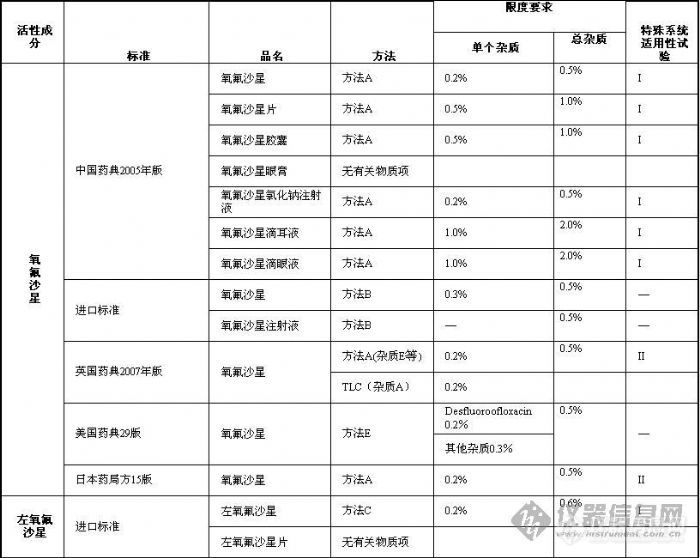
作者 张立雯 成海平 正文内容 【摘要】本文总结了国家标准中氧氟沙星、左氧氟沙星、盐酸左氧氟沙星、乳酸左氧氟沙星、甲磺酸左氧氟沙星系列药物的有关物质控制方法,分析了该类药物注册申报中有关物质控制存在的问题,希望能为研发者提供帮助。 【关键词】氧氟沙星、左氧氟沙星、有关物质一、概况 氧氟沙星(Ofloxacin)为合成的第三代广谱氟喹诺酮类抗菌药,对大多数革兰氏阳性菌和革兰氏阴性菌均有明显的抑制作用。临床上主要用于敏感菌所致的呼吸系统感染、泌尿生殖系统感染。氧氟沙星由日本第一制药株式会社研发,于1985年在日本、德国上市,制剂为口服片剂、注射剂等。目前国内已上市的氧氟沙星制剂有片剂、胶囊剂、颗粒剂、缓释制剂、小针、葡萄糖注射液和氯化钠注射液等。 左氧氟沙星(Levofloxacin)为氧氟沙星的左旋体,具有抗菌谱广、抗菌作用强的特点。日本第一制药株式会社于1993年在日本上市销售左氧氟沙星原料及片剂,并现已在英国、美国等多国上市。目前国内上市的左氧氟沙星制剂主要有片剂、小针、葡萄糖注射液和滴眼剂等。另外,国内已批准上市的左氧氟沙星还有其盐酸盐、乳酸盐和甲磺酸盐,三种加酸根的左氧氟沙星均有片剂、胶囊剂、注射制剂等多种剂型上市。二、国家标准中有关物质控制方法比较 氧氟沙星系列药物的有关物质测定国家标准大多采用HPLC法,列表比较见表1。 表1 氧氟沙星系列药物的有关物质测定方法与限度的比较 这些方法有很多相似的地方,如均采用ODS柱,色谱条件与含量测定色谱条件相同,按照主成分自身稀释对照法定量等。但也有一些不同的地方值得关注,作者从以下三个方面来对这些国家标准方法的不同之处进行比较。1、流动相 按照流动相的不同,作者将有关物质测定方法分为六种,具体如下: 方法A:醋酸铵高氯酸钠溶液(取醋酸铵4.0g和高氯酸钠7.0g,加水1300ml使溶解,用磷酸调节pH至 2.2)-乙腈(85∶15)为流动相,在294nm下检测; 方法B:略; 方法C:略; 方法D:己烷磺酸钠[取己烷磺酸钠0.98g,加磷酸盐缓冲溶液(取磷酸二氢钾6.8g,加水溶解并稀释至 1000ml,加0.05mol/L磷酸约500ml,使pH为2.4)]-甲醇(3∶1)为流动相,在293nm下检测; 方法E:磷酸缓冲溶液(溶解27.2磷酸二氢钾在1000ml水中,用磷酸调节pH至2.4)-乙腈(90∶10)为流动相,在294nm下检测; 方法F:己烷磺酸钠[取己烷磺酸钠0.98g,加磷酸盐缓冲溶液(取磷酸二氢钾6.8g,加水溶解并稀释至 1000ml,加0.05mol/L磷酸约500ml,使pH为2.4)]-甲醇(65∶35)为流动相,在230nm下检测。 六种流动相的共同特点是:组成均是酸性缓冲溶液加有机溶剂(甲醇或乙腈)。方法A、B、E未加表面活性剂,方法C、D加有表面活性剂己烷磺酸钠。除方法F在230nm下检测外,其他方法均在294或293nm下检测。2、主要杂质 英国药典收载了氧氟沙星杂质A、B、C、D、E、F共6个已知杂质,依次分别为去哌嗪环、去羧基、去氟、氟取代位置不同、去甲基以及氮氧化的化合物物。英国药典氧氟沙星原料药采用TLC法控制杂质A,采用HPLC法控制其他已知和未知杂质。美国药典重点关注了杂质desfluoroofloxacin,日本药局方重点关注了ofloxacin demethyl substance,均与英国药典的杂质E相同,是氧氟沙星的去甲基化合物,该化合物为氧氟沙星的主要降解产物,光照下极易产生。美国药典给出了desfluoroofloxacin的相应因子为1.13。中国药典没有明确已知杂质,但有关物质检查时采用以下光照降解法进行特殊系统适用性试验,光照试验中产生的杂质即为氧氟沙星、左氧氟沙星的主要杂质。 美国药典中desfluoroofloxacin按加校正因子的主成分自身稀释对照法定量,美国药典氧氟沙星其他杂质和其他国家标准中氧氟沙星或左氧氟沙星所有杂质按不加校正因子的主成分自身稀释对照法定量。有关物质限度的要求详见表1。3、特殊系统适用性试验 氧氟沙星、左氧氟沙星及其盐的含量测定和有关物质检查方法的系统适用性试验除通常的进样精密度、记录时间、理论塔板数等的要求外尚有一项较为特殊的系统适用性试验,其他标准方法采用I法,日本药局方采用II法,详述如下: 特殊系统适用性试验I(光照降解法):取供试品溶液于无色试管中,用日光灯(2500lux或3500lux)或紫外灯(254nm)照射1小时或3小时或4小时,取此液注入液相色谱仪,记录色谱图,相对保留时间约为主峰1.2处应能检测出色谱峰。 特殊系统适用性试验II(杂质对照品法):氧氟沙星和杂质E(ofloxacin impurity E CRS,英国药典)或氧氟沙星的去甲基物(ofloxacin demethyl substance)分离度不得低于2.0或2.5。 由于缺少杂质对照品,国内氧氟沙星系列药物的有关物质测定系统试验常常是采用光照降解法。也正是因为缺少杂质对照品,系统适用性试验才显得尤为重要,是考察系统分离能力的重要指标。 另外,左氧氟沙星及其盐的原料和制剂均需检查右旋异构体,方法基本相同,均是采用硫酸铜-L异亮氨酸溶液-甲醇或硫酸铜-D苯丙氨酸溶液-甲醇为手性流动相检测,限度要求不得过0.8%或1.0%。在此就不详加讨论。三、注册申报中存在问题与探讨1、不重视系统适用性试验 氧氟沙星系列药物的特殊系统适用性试验常常被忽视,其实却非常重要。若不做该项试验,就不能保证所采用的系统能将最难分离的相对保留时间1.2倍的色谱峰分离出来,就有可能得到错误的结果。 审评中曾发现申报盐酸左氧氟沙星注射液的某厂家自测盐酸左氧氟沙星含量较药检所检验结果高约5%(含量测定色谱条件与有关物质检查一致)。仔细审查其图谱,发现未按盐酸左氧氟沙星注射液的已有国家标准用光照降解法进行系统适用性试验,且色谱峰明显拖尾。其测定结果偏高很可能是紧随主峰之后的杂质峰包裹进了主峰。 申请人往往会留意进样精密度、理论塔板数这样的常规系统适用性试验,却常常忽略了光照降解系统适用性试验,此种现象在申报资料中占很大比例。究其原因,是试验人员没有理解到此项系统适用性试验的目的和重要性,希望提醒申请人提高对系统适用性试验的重视程度。2、没有杂质个数与含量的详细对比 申报资料中杂质对比研究通常的做法就是按照国家标准方法检验一下自制品和已上市对照药品,若都在标准规定范围内,就认为自制品与已上市药品质量相当。其实这样的做法是对杂质对比的目的和比什么不甚明了的表现。杂质对比一方面要了解自己的产品与已上市品杂质有哪些不同,另一方面要了解制剂过程中有没有新产生的杂质,若有新产生的杂质,应加以控制。所以比较就要落到列表对比杂质的个数与含量上,泛泛地比较杂质总量是不足以说明问题的。 例如,申报盐酸左氧氟沙星、乳酸左氧氟沙星的注射剂采用方法D测定的较为多见。在该色谱条件下,相对保留时间为0.23、0.43、1.2左右的杂质峰较常见,其中相对保留时间为1.2的色谱峰是稳定试验中含量有所增加的主要杂质。 另外,统计杂质的个数时要注意“忽略限度”。英国药典氧氟沙星有关物质项下明确规定:Disregard any peak with an area less than 0.1 times the area of the principal peak in the chromatogram obtained with reference solution (a),即忽略面积小于对照溶液主峰面积0.1倍的色谱峰(0.02%)。中国药典没有这么详细的规定,但从实际操作来看,为增强方法的严谨性和数据的可比性,建议申请人在统计杂质个数时应明确忽略限度。3、强力破坏试验降解程度不合适 有关物质检查方法学验证的重要项目就是通过强力破坏试验考察方法的专属性,但强力破坏试验破坏程度的掌握不尽合理。较容易出现的情况是破坏太轻微,酸、碱、氧化、光照破坏均几乎未产生可检测的杂质,这样就无法判断所采用的色谱条件分离能力是否符合要求,破坏试验失去意义。另一种极端是破坏过度,主峰降解了大半,产生大量重叠的杂质色谱峰,这样很难找到合适的色谱条件将所有的降解产物分离。个人认为,适度的破坏应是采用比贮藏中可能遇到的最强条件稍强烈的条件降解,产生比贮藏中可能产生的稍多杂质,若所选色谱条件能将这些杂质都分离,就是专属性符合要求的。 以上问题是氧氟沙星系列药物审评中经常遇到的问题,希望能为研发者提供帮助,共同努力提高我国仿制药的研发水平。 [img]http://ng1.17img.cn/bbsfiles/images/2009/07/200907202227_160694_1612824_3.jpg[/img][img]http://ng1.17img.cn/bbsfiles/images/2009/07/200907202231_160696_1612824_3.jpg[/img]