GB 26400-2011 食品安全国家标准 食品添加剂 二十二碳六烯酸油脂(发酵法)
一、案例近年来,被消费者争先购买的“深海鱼油”之类的营养品,其标签上往往可看到“DHA”和“EPA”这两类成分,DHA为二十二碳六烯酸,EPA为二十碳五烯酸,均属于多不饱和脂肪酸,深海鱼油中DHA和EPA含量较高。EPA和DHA能促进神经系统的发育,乳粉中加入EPA可抑制脂质在小肠的吸收和胆汁酸的吸收,抑制肝脏脂质和脂蛋白合成,促进胆固醇排泄,降低血液中的甘油三酯、VLDL、LDL和胆固醇含量,同时增高有益的HDL含量,有效防止高脂血症的发生,并可抑制血小板凝聚,减少血栓的形成,DHA和EPA还可以有效增强记忆力,预防老年性痴呆,延缓衰老,改善视力。二、选用的国家标准GB/T 5009.168--2003食品中二十碳五烯酸和二十二碳六烯酸的测定——气相色谱法。三、测定方法1.皂化取鱼油制品或经过处理的鱼油脂lg于50mL具塞容量瓶中,加入10mL正己烷轻摇使之溶解,并定容,然后吸取1.00~5.OOmL于另一10mL具塞比色管中,再加入2mol/L氢氧化钠一甲醇溶液lmL,振荡lOmin,置于60~C水浴中加热1~2min,皂化完全后,冷却到室温。2.甲酯化将皂化后的样品加入2m01/L盐酸一甲醇溶液2mL,振荡10min,于50℃水浴中加热2min,进行甲酯化,弃去下层液体,再加约2mL蒸馏水洗净并除去水层,用滴管吸出正己烷层,移至另一装有无水硫酸钠的漏斗中脱水,将脱水后的溶液在70℃水浴上加热浓缩,定容至lmL,待上机测试用。标准溶液系列:准确吸取配制好的标准溶液(此溶液含EPA和DHA各0.50mg/mL)1.0mL、2.0mL、5.0mL分别移入lOmL具塞比色管中,再加入2mol/L盐酸甲醇溶液2mL,充分振荡10min,以下步骤同上处理后,此系列标准溶液中EPA或DHA的浓度依次为0.5mg/mL、1.0mg/mL、2.5mg/mI。待上机测试用。3.气相色谱分析色谱柱:玻璃柱lm×4mm(id),填充涂有10%DEGS/Chromosorb W DMCS80~100目的载体。气体及气体流速:氮气50mL/min、氢气70mL/min、空气100mL/min。系统温度:色谱柱185℃、进样口 210℃、检测器210℃。4.测定(1)标准曲线的制作 分别吸取处理后的标准溶液1.0μL,注入色谱仪,测得不同浓度EPA甲酯、DHA甲酯的峰高,以浓度为横坐标,相应峰高响应值为纵坐标,得标准曲线。(2)测定样液把处理后的样品溶液1.0~5.OμL注入气相色谱仪,以保留时间定性,以测得的峰高响应值与标准曲线比较定量。5.结果计算X=A*V3*V1/m*V2式中 X——试样中二十碳五烯酸或二十二碳六烯酸的含量,mg/g;A——被测定样液中二十碳五烯酸或二十二碳六烯酸的含量,mg/mL;V1一鱼油或海鱼类试样皂化前定容体积,mL;V2——鱼油或海鱼类试样用于皂化样液体积,mL;V3——样液最终定容体积,mL;m——样品的质量,g。6.试剂①正己烷。②甲醇。③2mol/L氢氧化钠一甲醇溶液:称取8g氢氧化钠溶于lOOmL甲醇中即可。④2mol/L。盐酸一甲醇溶液:把浓硫酸小心滴加在约lOOg氧化钠上,把产生的氯化氢气体通入事先量取好的约470mL甲醇中,按质量增加量换算,调制成2mol/L盐酸一甲醇溶液,密封保存在冰箱中。⑤二十碳五烯酸和二十二碳六烯酸标准溶液:精密称取EPA、DHA各50.0mg,加入正己烷溶解并定容至100mL,此溶液含EPA和DHA各0.50mg/mL。7.仪器①气相色谱仪(附有氢火焰离子化检测器)。②索氏提取器。③氯化氢发生系统(启谱发生器)。④刻度试管(带分刻度):2mL、5mL、10mL。⑤组织捣碎机。⑥旋涡式振荡混合器。⑦旋转蒸发仪。
卫生部关于发布《食品添加剂二十二碳六烯酸油脂(发酵法)》等7项食品安全国家标准的公告(2011年第7号) 中 华 人民 共 和 国 卫 生 部公 告2011年 第7号根据《中华人民共和国食品安全法》和《食品安全国家标准管理办法》的规定,经食品安全国家标准审评委员会审查,现发布《食品添加剂二十二碳六烯酸油脂(发酵法)》(GB 26400-2011)等7项食品安全国家标准。其编号和名称如下:GB 26400-2011食品添加剂 二十二碳六烯酸油脂(发酵法)GB 26401-2011食品添加剂 花生四烯酸油脂(发酵法)GB 26402-2011食品添加剂 碘酸钾GB 26403-2011食品添加剂 特丁基对苯二酚GB 26404-2011食品添加剂 赤藓糖醇GB 26405-2011食品添加剂 叶黄素GB 26406-2011食品添加剂 叶绿素铜钠盐添加剂标准文本特此公告。二○一一年三月十五日
[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]分析脂肪酸甲酯标准品,怎样处理标准品?用什么溶剂稀释?
我们实验室是检测饲料和原料含量的,以前别人介绍用过中国农业科技院分析检测中心研制的氨基酸分析用校核标准品(参比物),名字我忘记了,只记得有代号,1#、2#、3#、4#、5# 这5种。有知道的老师们请帮帮忙!
http://file1.foodmate.net/file/upload/201202/01/09-19-48-90-410687.jpg 中国食品安全标准屡遭舆论批评。近两年来,从面粉增白剂风波,到乳制品标准争议,无论是标准本身的科学性还是标准制定程序的公正性等,均面临大量质疑。日前,卫生部发出关于公开征求《食品安全国家标准“十二五”规划(征求意见稿)》意见的函,意见征集截止到2012年2月28日。这意味着,在“十二五”期间,中国食品安全的数千条标准有望重新洗牌。 标准清理整合至关重要 该征求意见稿提出,“十二五”期间,食品安全国家标准方面的主要目标包括清理整合现行食品标准,加快制定、修订食品安全国家标准,完善食品安全国家标准管理机制,强化标准宣传贯彻和实施工作。 《征求意见稿》称,“十二五”期间,要清理现行食用农产品质量安全标准、食品卫生标准、食品质量标准以及行业标准中强制执行内容,解决标准间交叉、重复、矛盾等问题。 对此,中国工程院院士陈君石表示,现阶段,对食品安全标准的清理整合至关重要,“比补充更新重要得多”。他指出,由于长期以来多头管理,中国很多食品存在多重标准,且多为强制性标准,这些标准往往交叉、重复、矛盾,对食品安全监管颇为不利。“中国是世界上唯一一个有着多套强制性标准的国家”。 食品风险评估亟待加强 在谈到当前存在的问题和制约因素时,征求意见稿指出,目前,“食品安全国家标准的基础研究滞后,风险评估工作尚处于起步阶段,食品安全暴露评估等数据储备不足,监测评估技术水平有待提高。”对此,南开大学副教授宋华琳也指出,“风险评估”缺乏,一直是我国食品标准以及其他食品安全的软肋之一。 宋华琳指出,食品安全监管具备典型的风险监管的特征,因此需要通过食品安全风险评估制度这一组织形式和程序装置,将相关的化学、毒理学、营养学和微生物学等专业知识加以整合,将诸多科学和技术信息加以整合,通过对数据的分析与推演,来评估食品安全风险,并将其作为制定食品安全标准的基础。但宋华琳指出,目前在制度、能力、人才和技术体系等诸多方面,我国食品安全风险评估制度都与发达国家有较大差距。 对此,本次征求意见稿也强调,将“以风险评估为科学基础”作为食品安全标准制定的基本原则之一。即,“食品安全国家标准要以食品安全风险评估为基础,以对人体健康可能造成食品安全风险的因素为重点,科学合理设置标准内容,提高标准的科学性和实用性。” 制定标准程序要透明 食品安全标准制定过程中的程序正义问题始终备受关注。本次规划对此亦有所涉及。其主要任务中提到,完善食品安全国家标准管理制度。即“按照食品安全国家标准要科学合理、安全可靠的要求,进一步完善食品安全国家标准管理制度和工作程序”。 征求意见稿规定,2012年底前,公布食品安全国家标准跟踪评价规范等相关法规。2013年底前,完善食品安全国家标准制定、修订、征求意见、标准审评、审评委员会委员管理、标准公布等管理制度和工作程序,实现标准工作的公开、透明。 宋华琳建议,应建立审评专家的动态更新机制。这有助于防止审评专家过于固定,防止产业界和审评专家之间形成不当的联系;通过建立审评专家的进入与退出机制,从而将真正活跃在食品标准和食品安全科学研究第一线的专家,及时充实到食品安全国家标准审评专家的队伍之中。此外,他强调,未来还应以制度化的方式对待食品安全标准审评专家的利益冲突问题。 进度表 到2013年底,要基本完成对现行1900项食品国家标准和3000余项食品行业标准中强制执行内容的清理,2015年底前基本完成相关标准的整合和废止。
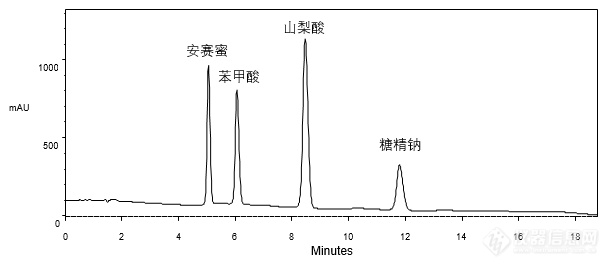
[align=center][b]GB 5009.28-2016食品安全国家标准 食品中苯甲酸、山梨酸和糖精钠的测定[/b][/align][align=center][b] ——标准品与乳品实际样品的分析[/b][/align][align=center][/align][align=left]本实验按照《GB5009.28-2016 食品安全国家标准食品中苯甲酸、山梨酸和糖精钠的测定》方法,分别对安赛蜜、苯甲酸、山梨酸、糖精钠的标准品混合溶液及加标乳品样品进行了分析。首先,使用CAPCELL PAK C[sub]18[/sub] MG S5 4.6 mm i.d. × 150mm色谱柱,对标准品混合溶液进行分析,如图1,安赛蜜、苯甲酸、山梨酸、糖精钠标准品均得到了良好的分析结果。[/align][align=left][/align][align=center][img=,611,268]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221532276656_9890_2222981_3.png!w611x268.jpg[/img][/align][align=center]图1 标准品混合溶液分析色谱图[/align][img=,400,200]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221532280132_6863_2222981_3.png!w400x200.jpg[/img][align=left][/align][align=left]其次,对乳品加标样品进行分析,如图2,糖精钠(Rt 12 min)与其后杂质峰之间未能取得基线分离,分离度仅为1.02。[/align][align=left][/align][align=center][img=,668,335]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221533054905_2223_2222981_3.png!w668x335.jpg[/img][/align][align=center]图2 加标乳品样品分析色谱图[/align][align=left][img=,406,203]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221533317202_2333_2222981_3.png!w406x203.jpg[/img][/align][align=left][/align][align=left]为改善糖精钠与杂质间的分离,在国标方法基础上,将流动相由[b]乙酸铵 / 甲醇 = 95 / 5[/b]调整为[b][b]乙酸铵 / 甲醇[/b][color=red]([/color][color=red]2 mmol/L [/color][color=red]甲酸)[/color]= 92 / 8[/b],再次对混合标准溶液和加标样品进行分析,结果如图3所示。[/align][align=left][/align][align=center][img=,690,545]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221534141056_4073_2222981_3.png!w690x545.jpg[/img][/align][align=center]图3 混标与加标乳品样品分析色谱图[/align][align=left][img=,464,171]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221535548985_7176_2222981_3.png!w464x171.jpg[/img][/align][align=left][/align][align=left]如图3,在酸性条件下,出峰顺序发生了变化,安赛蜜保留时间略有缩短,糖精钠保留时间明显缩短,由12 min缩短至8 min,苯甲酸和山梨酸保留时间分别延长至2 min和6 min;在分离度方面,糖精钠与苯甲酸之间分离度为2.79,苯甲酸与峰后杂质间分离度为2.04,所有色谱峰之间都达到了基线分离。[/align][align=left][/align][align=left]为使客户有更多选择,实验室又在国标原方法条件下继续筛选色谱柱,最终使用SUPERIOREX ODS S5 4.6 mm i.d. × 250 mm色谱柱时,仅微调有机相比例即可实现加标乳品样品的良好分析结果。如图4,杂质峰与糖精钠之间分离度达到2.48,达到基线分离要求。[/align][align=left][/align][align=center][img=,580,332]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221537130173_1058_2222981_3.png!w580x332.jpg[/img][/align][align=center]图4 加标乳品样品分析色谱图[/align][align=left]*注:峰上标所示数字由下至上依次为分离度与不对称因子。[/align][align=left][img=,326,177]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221537540634_9437_2222981_3.png!w326x177.jpg[/img][/align][align=left][/align][align=left]综上所述,按照国标《GB 5009.28-2016 食品安全国家标准食品中苯甲酸、山梨酸和糖精钠的测定》方法进行分析,使用CAPCELL PAK C[sub]18 [/sub]MG色谱柱对标准品混合溶液能得到良好分析结果,但在对加标乳品样品进行分析时,糖精钠与样品中的杂质未能实现基线分离,通过在流动相中添加甲酸可实现安赛蜜、糖精钠、苯甲酸、山梨酸及杂质的基线分离;另一方面,使用SUPERIOREX ODS色谱柱,在原条件基础上微调即可实现乳品中安赛蜜、苯甲酸、山梨酸、糖精钠及杂质间的良好分离。[/align]
求助:原乙酸三甲酯分析方法或分析标准
标定盐酸标准滴定溶液的不确定度分析 作者:吴文英 张春雨 唐惠兰 来源:中华医学研究杂志 在理化分析过程中,一切测量结果都不可避免地具有不确定度。盐酸标准溶液是常用化学定量参比物质,其标定值的准确性直接影响常规分析质量。笔者以GB/T601《滴定分析(容量分析)用标准液的制备》为依据配制并标定盐酸根据JJF1059-1999《测定不确定度评定与表示》分析其测量不确定度。简述由标定过程中得到的不确定度。 1 实验部分 1.1 测定方法[1,2] 准确称量270℃~300℃干燥至恒重的基准碳酸钠(99.95%~100.05%)约0.2g左右,电子分析天平(精度为0.1mg),置于三角瓶中,加入50ml水使之溶解,加指示剂,用盐酸标准液滴定至终点同时作试剂空白实验。 1.2 主要计量仪器与试剂 电了分析天平:AG204;酸式滴定管:50ml A级。 1.3 建立数学模型 C=m (V1-V2)×0.05300 式中 C:盐酸标准滴定溶液的浓度(mol/L);m:基准无水碳酸钠的质量(g);V1:盐酸标准滴定溶液用量(ml);V2:试剂空白实验中盐酸标准滴定溶液用量(ml);0.05300:与1.00ml盐酸标准溶液[C(HCl)=1.000mol/L]相当于以克表示的无水碳酸钠的质量。 1.4 盐酸标准滴定溶液的标定结果 为获得标准溶液重复测量的不确定度分量,对同一标准溶液进行8次独立的标定。测定数据见表1。 表1 盐酸标准滴定溶液的标定结果 略 2 测量不确定度来源 从检测过程和数学模型分析,标定盐酸标准溶液的不确定度主要来源,由四个方面所引起。(1)测量的重复性(A类不确定度);(2)基准无水碳酸钠的纯度;(3)测量使用的电子分析天平及量具;(4)其他相关常数。 3 测量不确定度分析 3.1 A类不确定度的分析 利用表1中的测量结果,按照A类评定测量重复性的标准不确定度。具体计算过程:重复测量的平均值计算式:=1 n∑8 i=1xi=0.09951mol/L 单次测量的标准差按贝塞尔公式计算s(x)为 s(x)=∑8 i=1(xi-)2 n-1=0.0001555mol/L 的标准差s()为 s()=s(x) n=0.000155 8=0.0000548mol/L=5.48×10-5mol/L 由测量重复性引起的相对标准不确定度为U(x):0.0000548/0.09951=0.055%。 3.2 B类不确定度分析 3.2.1 基准碳酸钠的纯度 基准碳酸钠的纯度为1.0000±0.0005,视为矩形分布0.00053=0.00029,则标准不确定度为:由基准碳酸钠的纯度引入的相对不确定度u(p)为:0.029%。 3.2.2 天平称量所引入的标准不确定度 干燥器与天平称量仓内均放置同质硅胶,视为相同湿度,称量时无吸潮。电子天平检定证书标出线性为上0.2mg;可视为矩形分布,则标准不确定度为:因为称量采用的是减量法,故称量的标准不确定度为0.2mg /3=0.12mg:因为称量采用的是减量法,故称量的标准不确定度为:2×0.122=0.17mg,则由称量引入的相对标准不确定度u(m)为:0.17mg/0.2018g=0.084%。 3.2.3 标定体积的不确定度 (1)滴定管的校准:滴定使用50ml酸式滴定管(A级),按照检定规程,其最大允许误差为±0.05ml,相对允许误差为±0.1%,按照矩形分布,则滴定体积的相对标准不确定度u(V)为:u(V)=0.1%/3=0.0577%。(2)环境温度:实验环境在空调条件下,室温近似20℃。温度在20℃左右,标准溶液的温度补正值非常小,对实验结果影响可忽略不计,所以在不确定度分析中不把一温度影响引起的不确定度列入考虑范围。(3)滴定终点的判断:终点时的误差±0.05ml(1滴的体积),两点分布,现由终点分布判断引入的标准不确定度为0.05ml:相对标准不确定度为0.05ml/38.32ml=0.13%标定体积的影响引入相对标准不确定度U(V)为0.0572+0.132=0.142%。 3.2.4 其他常数 基准无水碳酸钠摩尔质量引起的标准不确定度很小,可以忽略。 4 合成标准不确定度 测量重复性、基准无水碳酸钠的纯度、天平称量、标定体积等的不确定度相互独立,故将上述数据合成得盐酸的相对合成标准不确定度U(C)为0.0552+0.0292+0.0842+0.1422=0.176%。 5 扩展不确定度 实验测得盐酸标准溶液浓度为0.09951mol/L,则测量结果的合成标准不确定度U(C)=0.09951mol/L×0.176%=0.000175mol/L。若取包含因子K=2,得测量结果的扩展不确定度U=2U(C)=0.00035mol/L。 6 测量结果的表示 盐酸标准滴定溶液的浓度可表示为:(0.09951±0.00035mol/L,K=2)。 【参考文献】 1 姚正堂,将已峰.奶制品中蛋白质测定的不确定度分析.中华医学研究杂志,2005,5(6):6. 2 国家技术监督局.JJF1059-1999测量不确定度与表示.北京:中国计量出版社,1997,81. 作者单位: 214171 江苏无锡,无锡市惠山区疾病预防控制中心
跪求有没有人有“硫酸银、碳酸银”分析标准啊?
GB 26400-2011 食品添加剂 二十二碳六烯酸油脂(发酵法)
食品分析中标准物的管理及其标准溶液的校正一、意义食品分析标准物质是分析方法质控的核心,是定性和定量的依据。标准物质以一定纯度和浓度配制的溶液称标准溶液,其稳定性受其自身降解、化学转化、溶质和溶剂挥发等内在因素的影响,又受其存放条件如温度、湿度、光线照射、存放时间、存放容器及其配制技巧等外界条件的影响。由于影响标准物及其标准液的因素较多,如果条件控制不当或管理不严密,标准物质浓度易发生变化,这是食品分析中难以进行质量控制的主要原因。以上原因也是实验室食品分析测定产生误差的最主要因素,要减小这些产生误差的主要因素,就要特别注重标准物管理,以及进行标准溶液的稳定性观察和校正工作,也是实验室质量控制关键工作之一。当标准溶液发生变化时就要重新配制,并找出变化原因,为分析工作积累经验,并可写入方法注释中。在食品分析质量控制中,准确度和精密度的提高,是以标准溶液稳定性和准确性为前提的,因此对于标准溶液稳定性和准确性的关键技术问题,是质量控制的核心问题。二、标准物质的管理 1、容量分析的基准物是标定其它标准溶液的基准,应购买基准试剂,它可以保证其纯度。另一个因素是水份的影响,用前应充分干燥和恒重,配制时量器要校正。溶剂要纯化,使用的容器要充分洗涤。最终目的都是防止基准物的化合损失。2、用于分光光度分析的标准物,分有机的和无机的标准物,无机标准稳定性好,但使用液浓度低时,极易被容器吸附,并与容器中离子进行交换,因此决定了其稀溶液使用时间短。玻璃容器在碱性介质中易溶出,塑料容器在成型时加入助剂时也含有不同金属杂质,容易溶出如Zn、Ca等金属离子。有机标准最好不放在塑料制容器中,因塑料在成型时加入的有成份比较复杂的助剂和增塑剂。标准使用液应现用现配为最佳。三、标准物存放使用1、无机的标准物要求在干燥并无化学干扰物的条件下存放,选择合适干燥剂如硅胶和分子筛。有机标准物最好分装封入安培瓶中低温避光保存。固体的多环芳烃可配制成溶液,再分装在安瓿瓶中保留溶剂封存,也可把溶剂挥掉后干燥封存,使用时再定容,后一种方法更为稳妥些。配制好一批标准溶液,再一支一支使用也是很方便的。如果液体的标准物特别是几种标准的混合物用于色谱分析同系物如醇类物质,可同时配制一批分装安瓿瓶低温存放,再一支一支使用,能避免溶剂挥发体积变化产生的误差。这种做法更适于实验室间的标准分发和校正工作。最难办的是气体,标准如氯乙烯、氟里昂,最好是钢瓶中存放,或配制钢瓶标准气。这些条件不具备时也可以选择高沸点溶剂,密封溶解这些气体,称量溶质重量,一次性使用。从这一事实出发,气体,测定误差可以稍加放宽,因为标准自身稳定性差。2、用于色谱分析的标准物要求色谱纯,其配剂溶液剂也要求色谱纯,准确配制前要在色谱上进行检查。特别是几种标准进行混合更应慎重,每种要严格检查否则给定性定量带来很多麻烦。如果纯度不够时可以纯化,再结晶或用制备色谱制备。勉强使用是无益的。四、标准溶液的校正1、从安瓿瓶分装标准溶液无论是有机的或是无机的用于校正是很方便的。如原子吸收测定金属,从安瓿瓶中取一定量配制浓度系列,再封存。每隔一段时间(1~2周)再用原溶液配制同样浓度系列,严格控制仪器条件来比较二次标准曲线的斜率,斜率下降时表明有损失。2、相同浓度同时配制的标准的几支安瓿瓶,先用打开的一支标准的测定值与间隔一段时间后打开的另一支标准的测定值进行比较,以此类推最后在一段时间内几支同时测定,其变异程度就是标准在这段时间稳定性变化程度。3、几个实验室用同一标准物分别配制相同浓度标准液,各自进行标准曲线的测定,再按规定交换该标准液再进行测定,比较测定结果差异来观察同一标准的时间和空间变异。如果标准液稳定,配制不准确的实验室很容易查出。配制都准确时,标准液若不稳定时,会使各实验室的测得值都偏低。4、同种标准物来源不同,也应采用分别配制交叉测定的办法来检查标准的纯度及配制是否准确。在食品分析中无论用何种手段分析样品,所使用的标准物应作统一的或确切的规定。例如:过硫酸铵测锰,用MnSO4·H2O作为标准使用,到底硫酸锰需要不需要烘烤呢?对于这个问题,在一部份的教科书中有规定烘烤的,也有不烘烤的。按照MnSO4·H2O的性质遇到空气可能吸潮或风化,如果直接称重计算Mn量,就有可能出现误差。用烘烤称重测得水分所含的量比理论值高1.6%,有同一硫酸锰配制锰标准溶液测一合成水样,使用烘烤后配制的锰标准溶液,测得的Mn含量为0.205mg/L,未烘烤过的则高达约2.3%,从中说明硫酸锰在配制标准溶液时应经过烘烤,使标准一致。
求助:在哪能买到环丙烯酸(又叫锦葵酸)标准品。
化验分析硅石标准品,怎样测铝的含量,标准品如何处理?
[font='Times New Roman']急需以下三个标准[/font][font='Times New Roman']GB/T 22661.1-2008 氟硼酸钾化学分析方法 第1部分:试样的制备和贮存[/font]GB/T 22661.3-2008 氟硼酸钾化学分析方法 第3部分:氟硼酸钾含量的测定 氢氧化钠容量法[font='Times New Roman']GB/T 22662.3-2008 氟钛酸钾化学分析方法 第3部分:氟钛酸钾含量的测定 硫酸高铁铵容量法[/font][font='Times New Roman'][/font]
谁有新的高纯碳酸锂分析标准?急用,谢谢
成分分析中硫酸法测定棉和聚酯纤维的含量时,标准要求1克样品200ML硫酸,这量比较大,大家有用100ML硫酸做过实验吗?
现我室来了批含量约30% (w/w)的硫酸氢钠NaHSO4试样,请教各位专业人士怎么分析其含量呀?或者谁能提供工业硫酸氢钠的执行标准?小弟先谢谢过!硫酸氢钠。。。。。。ZB G 12002-1987
最近发现用ICP分析Sb元素,弱酸介质下GBW配置的标准曲线分析的其他品牌的标准溶液回收率偏低。实验室用的仪器是瓦里安 ICP-720,标准曲线是使用国家计量院的GBW(E)080545锑单元素溶液标准物质,浓度100ug/mL,基体是5%HCl。作为交叉验证的CK是使用国家钢铁材料测试中心钢铁研究总院的GSB G 62043-90锑标准溶液,浓度500ug/mL,基体是25%硫酸。或者是ACCU的ICP-02N-1,浓度1000ug/mL,基体是2~5%HNO3。我发现使用弱酸基体(若0.07mol/L HCl或者5%HNO3)配置的标准曲线(使用计量院的Sb标准溶液配置),分析相同基体的CK(由另外品牌的Sb标准溶液配置),测量第一个CK时,Sb回收率只有70-85%(酸度越低,回收率越差),继续测量,回收率会慢慢增大。可是即使连续测量(不拔出进样管)10次以上,Sb的回收率也只有93-94%。而测量由计量院的Sb标准溶液配置的同样基体的Sb溶液,回收率却没有问题;若是使用浓酸基体(35%HNO3),两个品牌的标准溶液的回收率却又没有问题。我知道Sb会有残留,可是分析每一只样品(包括标准曲线的点),我都会快泵进样十几秒再分析溶液的,就算有残留,没道理厉害到分析了10多样品还有残留。母溶液的基体可能有影响,可是同一支溶液的其他元素的回收率都OK啊最近有支PT样(5%硝酸基体,什么品牌的母溶液配出来的就不知道了),就是因为这个原因,Sb的读数偏低了。现在要整改,可是什么原因都不知道……现在只好到论坛来求助各位老大了,希望各位能给点意见。先谢谢了。
药品分析中标准品和对照品有什么区别?
药品分析中标准品和对照品有什么区别?
目录 -------------------------------------------------------------------------------- 总则第一章 绪论第一节 食品分析的性质和任务第二节 食品分析的内容第三节 食品分析方法及发展趋势第四节 食品标准第五节 食品分析课程的学习要求思考题(一)第二章 样品的准备及结果的数据处理第一节 分析样品的准备第二节 分析结果的数据处理思考题(二)第三章 食品的感官分析第一节 感官分析概述第二节 感觉第三节 食品的感官检验第四节 食品感官分析常用的方法第五节 感官分析的应用及方法选择思考题(三)第四章 食品的物理检验法第一节 密度法第二节 折光法第三节 旋光法第四节 压力测定法第五节 固态食品的比体积思考题(四)第五章 物理化学分析法第一节 电化学分析法第二节 吸光光度法第三节 [url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度法思考题(五)第四节 色谱分析法思考题(六)第六章 食品的一般成分分析第一节 水分的测定思考题(七)第二节 灰分的测定思考题(八)第三节 酸度的测定思考题(九)第四节 脂类的测定思考题(十)第五节 碳水化合物的测定思考题(十一)第六节 蛋白质及氨基酸的测定思考题(十二)第七节 维生素的测定思考题(十三)第七章 食品添加剂的测定第一节 概述第二节 甜味剂——糖精钠的测定第三节 防腐剂的测定第四节 发色剂——硝酸盐与亚硝酸盐的测定思考题(十四)第五节 漂白剂 ——二氧化硫及亚硫酸钠的测定第六节 品质改良剂——磷酸及其盐类的测定第七节 抗氧化剂(BHA、BHT)的测定第八节 食品中色素的测定思考题(十五)第八章 食品中矿物质元素的测定第一节 概述第二节 矿物质微量元素的比色测定第三节 [url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度法测定食品中矿物质元素思考题(十六)第九章 食品中常见有害有毒物质的测定第一节 概述第二节 有机氯农药残留量的测定第三节 有机磷农药残留量的测定第四节 薄层色谱法测定食品中黄曲霉毒素第五节 液相色谱法测定食品中苯并(a)芘第六节 比色法测定食品中N-亚硝胺类思考题(十七)第十章 食品分析实验第一节 实验室安全要点第二节 实验室技术实验一 食品感官分析实验实验二 密度计的使用实验三 折光计的使用实验四 旋光计的使用实验五 碳酸饮料中CO2含量的测定实验六 固态食品比体积的测定实验七 全脂乳粉中水分含量的测定实验八 面粉中灰分含量的测定实验九 汽水中总酸及pH值的测定实验十 鲜乳中脂肪含量的测定实验十一 麦乳精中脂肪含量的测定实验十二 水果硬糖中还原糖量的测定实验十三 面粉中淀粉含量的测定实验十四 豆乳饮料中蛋白质含量的测定实验十五 酱油中氨基酸态氮含量的测定实验十六 新鲜果蔬中维生素C含量测定实验十七 饮料中山梨酸含量的测定实验十八 香肠中亚硝酸盐含量的测定实验十九 植物油中抗氧化剂的测定实验二十 罐头食品中锡含量的测定实验二十一 矿泉水中微量元素的测定实验二十二 乳品中残留农药的测定附录一、附表附表(一)部分元素相对原子质量表附表(二)常用酸和碱溶液的相对密度和浓度附表(三)排序检验法检验表(α=5%)附表(四)排序检验法检验表(α=1%)附表(五)χ2分布表附表(六)观测锤度温度改正表(标准温度20℃)附表(七)酒精计温度浓度换算表附表(八) 乳稠计读数变为温度15℃时的度数换算表附表(九)乳稠计读数变为温度20℃时的度数换算表附表(十)糖液折光锤度温度改正表(20℃)附表(十一)碳酸气吸收系数表附表(十二) 相当于氧化亚铜质量的葡萄糖、果糖、乳糖转化糖质量表二、浓度换算关系主要参考资料
药品分析中标准品和对照品有什么区别?
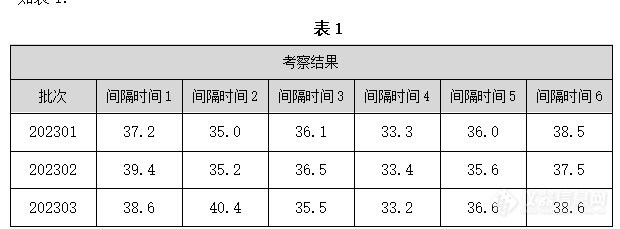
[align=center][b]食品叶酸检测分析[/b][/align][align=left][b]实验背景:[/b][font=宋体]检验过程中发现经过考察后,食品中叶酸检验结果有增长趋势,[/font][font=宋体]。[/font][font=宋体][b]对数据进行原因分析,结论为实验室之间检测误差导致。[/b][font=宋体]检验方法[/font][font=宋体]1.1仪器与用具:电热鼓风干燥箱、电子天平、旋涡混合仪、立式压力蒸汽灭菌器、紫外可见分光光度计、生物安全柜、生化培养箱、离心管、容量瓶、量筒、试管、[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url]。[/font][font=宋体][font=宋体]注:所用玻璃器皿使用前用盐酸浸泡液或月桂基磺酸钠洗涤剂清洗干净后,[/font][font=宋体]250℃干热1h~2h。[/font][/font][font=宋体]1.2试剂:20%乙醇溶液(2+8)、氢氧化钠乙醇溶液(0.01mol/L)、氢氧化钠溶液(1mol/L)。[/font][font=宋体]1.3培养基:琼脂培养基,叶酸测定培养基。[/font][font=宋体]1.4 标准品:叶酸标准品。[/font][font=宋体]1.5菌种的制备与保存:[/font][font=宋体]菌种:鼠李糖乳杆菌或等效菌株。[/font][font=宋体][font=宋体]储备菌种的制备:将菌种鼠李糖乳杆菌转接至菌种储备用琼脂培养基中,在[/font][font=宋体]36℃±1℃恒温培养箱中培养20h~24h,连续转种2代~3代。取出后放入2℃~4℃冰箱作为储备菌株保存。[/font][/font][font=宋体][font=宋体]实验前将储备菌株接种至菌种储备用琼脂培养基中,在[/font][font=宋体]36℃±1℃恒温培养箱中培养20h~24h以活化菌株,用于接种液的制备。[/font][/font][font=宋体][font=宋体]注:保存[/font][font=宋体]2周以上的储备菌种,不能立即用作接种液制备,实验前宜连续传种2代~3代以保证细菌活力。[/font][/font][font=宋体]1.6接种液的制备:实验前一天,取2mL叶酸标准工作液与4mL叶酸测定用培养基混匀,分装至2支试管中,于121℃(0.10MPa~0.12MPa)高压灭菌15min(或根据培养基标签标识进行灭菌)后即为种子培养液。冷却后用接种环将活化的菌株转种至2支种子培养液中,于36℃±1℃恒温培养箱中培养20h~24h。取出后将种子培养液混悬,无菌操作下吸取0.5mL转种至5mL不加叶酸标准工作液的无菌叶酸测定培养基中,于36℃±1℃再培养6h,以消耗种子培养液中残存在菌株中的多余叶酸,制成接种液。[/font][font=宋体]1.7分析步骤(所有操作均需避光进行)[/font][font=宋体][font=宋体]试样提取:准确称取液体试样[/font][font=宋体]0.5mL~2mL,精确至0.001g,转入锥形瓶中,加入80mL氢氧化钠乙醇溶液,具塞,超声振荡0.5h~4h至试样完全溶解或分散,转入100mL容量瓶中,用水定容至刻度。[/font][/font][font=宋体][font=宋体]稀释:根据试样中叶酸含量用水对试样提取液进行适当稀释,使试样稀释液中叶酸含量在[/font][font=宋体]0.2ng/mL~0.3ng/mL范围内。[/font][/font][font=宋体]1.8试样测定[/font][font=宋体][font=宋体]试样系列管:取[/font][font=宋体]3支试管,分别加入1.0mL、2.0mL、3.0mL试样稀释液(Vx),补水至5.0mL,混匀。每个梯度做2个平行。[/font][/font][font=宋体][font=宋体]标准系列管:取试管分别加入叶酸标准工作溶液[/font][font=宋体]0.00mL、0.25mL、0.50mL、1.00mL、1.50mL、2.00mL、2.50mL、3.00mL、4.00mL和5.00mL,补水至5.00mL,相当于标准系列管中叶酸含量为0.00ng、0.05ng、0.10ng、0.20ng、0.30ng、0.40ng、0.50ng、0.60ng、0.80ng和1.00ng,混匀。制备2套~3套标准系列管,绘制标准曲线时,以每个标准点平均值计算。[/font][/font][font=宋体][font=宋体]灭菌:将所有测定系列管、叶酸测定培养基于[/font][font=宋体]121℃(0.10MPa~0.12MPa)高压灭菌15min(或根据培养基要求进行灭菌)。[/font][/font][font=宋体][font=宋体]接种和培养:待测定系列管冷却至室温后,在无菌操作条件下,每[/font][font=宋体]10mL叶酸测定培养基加入接种液40μL,混匀,每支测定管中加入接种后的叶酸测定培养基5mL,混匀。置于36℃±1℃恒温培养箱中培养20h~40h,获最大混浊度时终止培养。另准备一支标准0管(含0.00ng叶酸)不接种作为0对照管。[/font][/font][font=宋体][font=宋体]测定:将培养好的标准系列管、试样系列管用旋涡混合仪混匀。用[/font][font=宋体]1cm比色杯,于540nm处,以未接种0对照管调节透光率为100%(或吸光度值为0),依次测定标准系列管、试样系列管的透光率(或吸光度值)。如果0对照管出现浑浊,说明可能有杂菌污染,需重做实验。[/font][/font][font=宋体][font=宋体]注:适宜的测定光谱范围为[/font][font=宋体]540nm~610nm。[/font][/font][font=宋体]1.9分析结果表述:[/font][font=宋体] [font=宋体]标准曲线:以标准系列管叶酸含量为横坐标,每个标准点透光率(或吸光度值)均值为纵坐标,绘制标准曲线。[/font][/font][font=宋体][font=宋体]试样结果计算:从标准曲线计算试样系列管中叶酸的相应含量([/font][font=宋体]cx),如果3支试样系列管中有2支叶酸含量在0.10ng~0.80ng范围内,且各管之间折合为每毫升试样提取液中叶酸含量的偏差小于10%,则可继续按式进行结果计算,否则需重新取样测定。[/font][/font][font=宋体] [/font][font=宋体]2.检验结果[/font][font=宋体]分析的数据,叶酸含量没有降解趋势,结果符合[/font][font=宋体]GB 29922-2013[/font][font=宋体][font=宋体]的规定,结果如表[/font][font=宋体]1:[/font][/font][img=,620,229]https://ng1.17img.cn/bbsfiles/images/2023/07/202307011003010672_7959_2227357_3.png!w620x229.jpg[/img][b]3.[font=宋体]原因分析[/font][/b][font=宋体]GB 5009.211-2014《[/font][font=宋体][font=宋体]食品安全国家标准[/font] [/font][font=宋体]食品中叶酸的测定[/font][font=宋体][font=宋体]》方法为微生物法,实验过程需要将鼠李糖乳杆菌接种至含有样品的培养液中,培养后测定其吸光值,根据含量与透光率的关系,绘制标准曲线并计算出试样中的叶酸含量,整个实验过程人员、所处的环境、菌液的生长差异、吸光值测定时设备台间差,都直接影响检验结果。考察期叶酸含量稳定没有增长[/font][font=宋体]/降解趋势;综合分析[/font][/font][font=宋体]叶酸检验结果有增长趋势,系实验室之间检测误差导致。[/font]实验也是解决问题的过程,持续改进方法,不断增强技术。[font=宋体][font=宋体][/font][/font][/font][/align]
食品安全现场快速检测分析方法 编号索引 标准溯源GB/T 中华人民共和国国家标准分析方法CDC/SB 中国疾病预防控制中心营养与食品安全所 现场快速检测分析方法CDC/SB 101 农药有机磷类(国内允许使用的30 多种)和氨基甲酸酯类(国内允许使用的10 多种)的快速检测:采用国家标准快速检测方法GB/T5009.199-2003。适用于蔬菜、水果以及其它食品中农药残毒的快速检测,也适用于食物中毒物质中农药的快速筛选定性。现场使用,20 分钟出结果。CDC/SB 102 鼠药毒鼠强的快速检测:中国疾病预防控制中心营养与食品安全所现场快速检测方法。主要用于预防性监测和中毒物的筛选、定性鉴别。检出限5ug/ml。现场使用,20 分钟出结果。CDC/SB 103 鼠药敌鼠钠盐的快速检测:中国疾病预防控制中心营养与食品安全所现场快速检测方法。主要用于预防性监测和中毒物的筛选、定性鉴别。检出限45ug/ml。现场使用,10 分钟出结果。CDC/SB 104 鼠药安妥的快速检测:中国疾病预防控制中心营养与食品安全所现场快速检测方法。主要用于预防性监测和中毒物的筛选、定性鉴别。检出限20ug/ml。现场使用,10 分钟出结果CDC/SB 105 鼠药氟乙酰胺的快速检测:中国疾病预防控制中心营养与食品安全所现场快速检测方法。主要用于预防性监测和中毒物的筛选、定性鉴别。检出限50ug/ml。现场使用,15 分钟出结果。CDC/SB 106 亚硝酸盐的快速检测:中国疾病预防控制中心营养与食品安全所现场快速检测方法。本方法是在国家标准GB/T5009.33-2003 盐酸萘乙二胺检测方法基础上改进的现场快速检测方法--速测管法。定性兼半定量检测。可用作卫生指标检测、投毒监测和食物中毒物质的快速筛选、定性定量。最低检出量为0.025mg/L。现场使用,15 分钟出结果。
老师同学们有无这样的经历?对已知化合物定量分析,标准品和质控样分别出自不同的厂商,皆在有效期内,定量过程线性良好,RSD合规,但是多种化合物合成的质控样一直有一个化合物无法进入合理区间范围?多次尝试无果?这个时候考虑标准品有问题还是指控样有问题?还是分析方法有问题?从哪里入手?类似问题咋解决???
求购 质谱分析的蛋白标准品,MALDI-TOF-MS上用的。 分子量在400--30000da 的或者接近这个质量范围的,如有请联系我。直接给我这个留言就可以,谢谢!
[font=宋体][size=3]百灵威整合国际资源为烟草行业提供品类齐全的烟草成分分析标准品。产品涵盖烟草分析所用到的各类代谢物、衍生物、农药及香精香料标准品。可以满足烟草行业各类分析实验需求。[/size][/font]
刚刚看到国标GB/T 22110-2008 食品中反式脂肪酸的测定-气相色谱法 中用到反-9、12、15十八碳三烯酸甲酯标准品(trans-9,trans-12,trans-15-Octadecatrienoic acid methyl ester),有谁买过,哪个品牌可以提供?谢谢!
求助GB/T 19281-2003 碳酸钙分析方法有谁有这个标准请给我好吗?