对羟基苯甲酸酯,俗称尼泊金酯是一类安全高效的防腐剂, 广泛用于食品、饮料、化妆品、医药等许多方面。在化妆品行业中,由于其安全、高效和广谱的特点,长期以来被用于各类产品中。 在中国,对羟基苯甲酸酯是经过卫生部批准的化妆品组分中的限用防腐剂,中国《化妆品卫生规范》(2007版)规定,单一酯和混合酯的限量分别为0.4%和0.8%。在规定的范围内适量添加防腐剂对于保护化妆品的产品质量是非常必要的,防腐剂的功能是使化妆品免受微生物的污染,确保消费者的使用安全。 此外,对羟基苯甲酸酯也是我国允许使用的食品添加剂,广泛用于酱油、醋、果酱、糕点馅、果汁和碳酸饮料等食品中,我国国家标准——《食品添加剂食用卫生标准GB 2760-2007》中规定最高使用浓度可以达到0.5g/kg (相当于500ppm)。 对羟基苯甲酸酯类在世界范围内得到了各国及国际性官方组织的认可。美国食品药品管理局(US FDA)批准对羟基苯甲酸酯类可以作为化妆品防腐剂使用,据统计截至到2006年,在美国仍有很高的使用频度。美国独立的化妆品原料安全性评价专家小组(Cosmetic Ingredient Review, CIR)也对对羟基苯甲酸酯类在化妆品中使用情况作了权威性结论,即按目前的使用惯例,对羟基苯甲酸酯类作为化妆品防腐剂成分是安全的。欧盟委员会也批准对羟基苯甲酸酯类作为化妆品防腐剂使用。联合国食品法典委员会(CODEX)批准其作为允许添加的食品防腐剂。 消费者应该对于化妆品、食品等日常消费品中的防腐剂有正确的认识,防腐剂对于保护产品、防止有害微生物滋生和最终保护消费者的健康是非常必要的,只要防腐剂添加的含量符合相关法规标准的要求,产品就是安全的,消费者尽可以放心使用。
石英玻璃中羟基含量检验方法[url]http://www.king-ber.com/Product_Show.asp?ID=755[/url] (红外分光光度计检测)GB/T 12442-901主题内容与适用范围 本标准规定了检验石英玻璃中羟基含量时试样的制备、试验用仪器、试验步骤 及结果处理。 本标准适用于透明石英玻璃中羟基含量的测定。 2引用标准 GB9657 半导体用透明石英玻璃管 GB9658 光源及真空仪表用透明石英玻璃管 JC426-91 无臭的氧石英玻璃管 3术语 3.1透过率或透射比:透过物体的光强度与入射光强度的比值,符号为T。 3.2光谱透过曲线:透过率或透射比随波长的分布曲线。 3.3光密度:衡量玻璃阻止光线透过的能力,符号为D,数值等于透过率倒数的常用对数。 3.4基线:光谱透过曲线上吸收峰两肩边的连线。 3.5零线:光谱透过曲线上透射比为零的线。 3.6摩尔吸收系数:浓度为1mol/L的单位光程长的吸光度,符号为ε。 4试验原理 根据石英玻璃中羟基含量与波长2.73μm处光吸收的线性关系进行定量测定。 5试验仪器 5.1可测波长范围为2.00 ̄3.30μm,测量精度为±1%T的红外分光光度计(TJ270-30A)。 5.2稳定精度为±0.5%的电了交流稳压器。 5.3精度为±0.01mm的千分尺,量度为0.02mm的游标卡尺。 5.4宽度为0.6 ̄1.0mm的长方形固定光栏一组(2个)。 6试样制备 6.1从外观质量符合GB9657、GB9658、JC126或相应标准规定的石英玻璃产品中选取待测样品。 6.2待测样品为块状时,将待测石英玻璃切割、研磨、抛光成镜面,制成25mm×12mm两面平行 厚度差小于或等于0.05mm)的透明试样两个,厚度为0.1 ̄10.0mm,其中人造石英玻璃厚度为0.1 ̄0.7mm,气炼玻璃厚度为0.8 ̄3.0mm,电熔石英玻璃厚度为1.6 ̄10.0mm。使试样在2.73 μm处的透过率在10% ̄80%(吸光度在1.0 ̄0.1)的范围内。 待测样品为管状时,将待测石英玻璃管切取长35 ̄40mm的管段二段,再分别沿管长方向切 取弦长为8 ̄15mm的弧形试样各一个。 6.3用千分尺或卡尺测量试样的厚度。 6.4将试样在器皿中用无水乙醇洗涤干净、晾干、待测。 7试验步骤 7.1开启并预热试验用仪器。当检测管状试样时,在样品光路和参考光路中分别装入长方形 固定光栏。 7.2用遮蔽物遮盖样品光路,盖上样品室的盖,检查并调整仪器零点。 7.3拿去遮蔽物,记录并调整仪器在2.00 ̄3.30μm范围内的100%基准线。 7.4将块状待测试样置于样品光路中,当检测管状样品时,将其试样固定在样品光路的固定 光栏架上,使其中心对准光栏。 7.5按动扫描进行扫描,记录试样在2.00 ̄3.30μm范围的光谱透过曲线。 7.6将试样上下位置对换,再记录一次光谱透过曲线。 8试验结果 8.1在记录的光谱曲线上,划出基线,分别测量出2.73μm处基线到零线和吸收峰到零线的距离。 8.2石英玻璃的羟基含量用下式计算: 1I0 C=96.5──lg──dI 式中:C──试样的羟基含量,ppm; d──试样厚度,cm; I0──2.73μm处基线到零线的距离,mm; I──2.73μm处吸收峰到零线的距离,mm。 本公式由中国建筑材料科学研究院石英玻璃所实测国产石英玻璃中羟基在2.73μm处的克分了 吸收系数ε=80.1L• moL[-1]• cm[-1],根据朗伯-比耳定律导出的。 8.3每个试样用两次计算结果的算术平均值作为该试样的羟基含量值。取两个试样的算术平均值 作为待测石英玻璃的羟基含量值。 8.4参考附录A(参考件)记录和报告试验结果。 附录A 试验记录和试验报告 (参考件) 试验中使用的试验条件应记录在光谱透过曲线的记录纸上,按下述格式和内容填写试验 记录和报告。 石英玻璃羟基含量试验记录 送样单位_____送样日期_____试样名称_____试样数量_____ 试验日期_____试验人员_____ 检验结果 试样编号试样名称试样厚度I0I羟基含量,ppm cmmm检测值平均值石英玻璃羟基含量试验报告 送样单位_____试样名称_____ 试验人员_____报告日期_____ 检验结果 试样编号称试样名称羟基含量,ppm附加说明: 本标准由国家建筑材料工业局提出。 本标准中国建筑材料科学研究院技术归口。 本标准由中国建筑材料科学研究院石英玻璃研究所负责起草并解释。 本标准起草人王明龙。
看到很多文献说羟基磷灰石在化妆品中可以作为添加剂,最近在合成载银的羟基磷灰石(Ag-HAP),对应用方面比较感兴趣。想请教一下对这方面了解的前辈啊。我自己目前的一些了解:载银HAP主要用做抗菌剂和抗菌添加剂,如抗菌塑料、抗菌陶瓷等。但化妆品方面的应用也有报道,但具体应用方式和前景都不太了解。好像目前国家规定不允许化妆品做抗菌抑菌的宣传,除非有卫消准字的产品。是不是这方面的规定限制了化妆品抗菌功能的开发?另外,化妆品使用过程中,有防微生物滋生和污染的需求,这方面应用主要是指化妆品防腐剂,主要好像是有机物比较多,无机物方面如载银HAP是否也可以应用到这类用途?对化妆品这行还了解不深入,还请大家指教。
[size=5]各位高手: 请问大家有没有丙醛、三羟基甲基乙烷的相关标准?我找了许多网站,都没有找到,有没有哪位高人有丙醛和三羟基甲基乙烷的企业标准、国内外的标准可以支援一下啊?谢谢帮忙,我将重谢![/size]
各位 谁有羟基柠檬酸钾的 质量标准 检测指标 操作规程 都可以 羟基柠檬酸钾里面含有羟基柠檬酸 羟基柠檬酸钠 羟基柠檬酸钙 等 如何检测?谢谢
请问糠氨酸标准品哪里有卖?麻烦告知糠氨酸的中英文化学名以及结构式。谢谢!
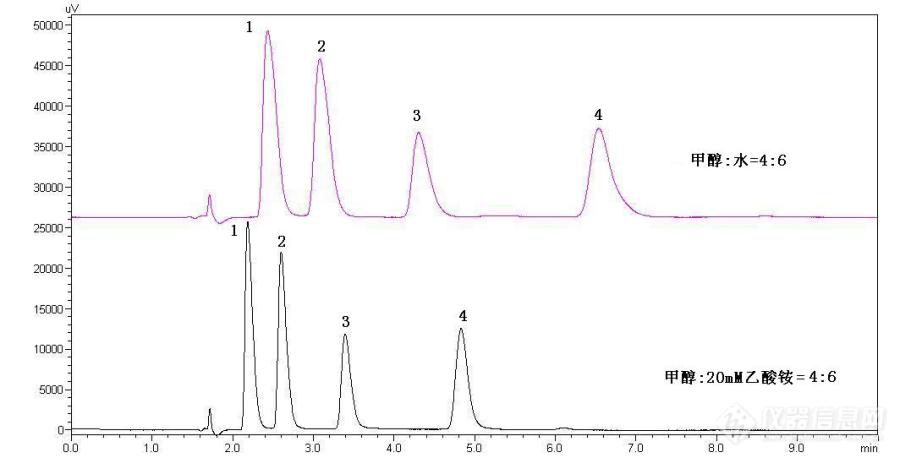
食品中对羟基苯甲酸酯类液相与[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法的测定方法比较摘要:本文详细讲述了液相色谱与[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定食品中对羟基苯甲酸酯类各自的优缺点,GB 5009.31-2016只收录了[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定标准的测定方法。关键词:对羟基苯甲酸酯类;液相色谱;[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url];优缺点;GB 5009.31-2016引言[font=黑体][size=18px][b] [/b][/size][/font][font=宋体][size=12px]食品中常见的对羟基苯甲酸酯类又称为对羟基安息香酸酯或尼泊尔金酯,包括对羟基苯甲酸甲酯、乙酯、丙酯、丁酯,是一类新一代高效低毒消毒杀菌防腐剂,它的抗菌能力、pH应用范围及用量比苯甲酸和山梨酸及其盐类广(见表1),且使用安全,经济方便,对人体刺激较小。在国外,已被广泛用于食品、饮料、化妆品和医药等方面。作为食品防腐剂,它可用于饮料、果蔬加工品、海产加工品、禽畜加工品、调味品、啤酒、米酒等加工品中,还可用于水果、蔬菜和海产品的防腐保鲜。它不但可完全替代苯甲酸钠和山梨酸钾,其使用范围比苯甲酸钠和山梨酸钾更广。在国外,已被广泛用于食品、饮料、化妆品和医药等方面。在日本,对羟基苯甲酸酯和山梨酸是主要的防腐剂产品。而我国,对羟基苯甲酸酯类防腐剂的用量也在逐年增加,成为防腐剂的第二个主要产品。[/size][/font][align=center]表1 GB2760-2014对羟基苯甲酸酯类限量要求[/align][img]https://ng1.17img.cn/bbsfiles/images/2020/08/202008192125459013_3455_2166779_3.png[/img]实验部分讨论液相色谱1.前处理及色谱分析条件称取5g(精确至0.01g)试样于50ml比色管中,加入15mL95%乙醇,混匀,超声波清洗器提取10min,冷却至室温后用95%乙醇定容至50mL刻度线,摇匀。静置分层,取上清液经0.22um微孔滤膜过滤后待测。色谱柱:C18柱,150×4.6 mm(i.d),5 μm,或性能相当者;流动相:甲醇(B)+20 mmol/L乙酸铵溶液(A) = 40+60(体积比);洗脱梯度见表2:[font=黑体]表2. 对羟基苯甲酸酯类的洗脱程序[/font][table][tr][td]时间/min[/td][td]2.00[/td][td]4.00[/td][td]12.00[/td][td]12.01[/td][td]15.00[/td][/tr][tr][td]B%[/td][td]40[/td][td]60[/td][td]60[/td][td]40[/td][td]stop[/td][/tr][/table]流速:1 mL/min;柱温:35 ℃;进样体积:10 μL;检测波长扫描范围:210 nm—390 nm,定量波长256 nm。由于对羟基苯甲酸酯在[font=times new roman]pH4~8的[/font]范围内稳定存在且有很好的抗菌效果,但水溶性较低,易溶于乙醇,而乙醇的毒性较甲醇低,所以采用乙醇做为标准使用液和样品提取液。大部分添加对羟基苯甲酸酯类的食品都具有含水性高、不易长期保存的特点,因此在取样时选择被测物稳定保存的状态,采用浸泡过夜、超声及振荡提取的方式,能达到较好的提取效果。2、色谱条件的选择及优化2.1 检测波长的选择以浓度为[font=times new roman]0.02 mg/ml的标准使用液依次在高效液相色谱—二极管阵列检测器190 nm-410 nm波长[/font]范围进行扫描,以确定被[font=times new roman]测物质的最大吸收波长,对羟基苯甲酸酯类的最大吸收波长均十分相似,在256nm处有紫外最大吸收峰,这是与自身具有苯环和羰基结构所决定,实验选择256nm为检测波长,能有效满足四种物质的分析检测。[/font] [size=12px] 2.2 分析条件的选择[/size]分别使用水和20mM乙酸铵做流动相在相同色谱条件下进行分析(见图2),UPLC(超高速液相)在5分钟内完全分离且重现性好,出峰顺序依次为对羟基苯甲酸甲酯、乙酯、丙酯、丁酯。由图可以看出在峰形和分析时间上利用缓冲盐做流动相要优于纯水,特别是面对食品样品的复杂性,选择20mM乙酸铵和甲醇作为流动相能有效排除基质干扰。[img]https://ng1.17img.cn/bbsfiles/images/2020/08/202008192125462304_3941_2166779_3.jpg[/img]图2 混合标准样品色谱图1.对羟基苯甲酸甲酯[font=arial][color=black];[/color][/font][font=times new roman]2.[/font]对羟基苯甲酸乙酯[font=arial][color=black];[/color][/font][font=times new roman]3.[/font]对羟基苯甲酸丙酯[font=arial][color=black];[/color][/font][font=times new roman]4.[/font]对羟基苯甲酸丁酯实验选择C18色谱柱进行分离,是根据尼泊尔金酯类的物理化学性质,在C18柱上具有良好的保留,当提高有机相甲醇的比例时,能快速得到洗脱。选择20m M乙酸铵作为流动相,能较好的平衡食品复杂基质的p H值,有效避免杂质干扰。实验尝试使用了日本岛津HPLC-20A,美国Grance Alltima 4.6mm×150mm C18色谱柱与日本岛津UPLC,shim-pack XR-ODS 3.0mm×75mm C18色谱柱对市售果蔬汁饮料、酱腌菜及酱油制品和糕点等所含的对羟基苯甲酸酯类进行比对分析,发现均能得到良好分离,且结果一致。在实验中发现,相同条件下,采用HPLC-20A,美国Grance Alltima 4.6mm×150mm C18色谱柱对酱腌菜类食品进行分析,在对羟基苯甲酸乙酯处会有干扰(见图3),通常情况下,改变流动相的比例能避免此类问题的发生,但若直接选用岛津UPLC,shim-pack XR-ODS 3.0 mm×75 mm C18色谱柱进行分析,则能有效避免(见图4)。考虑到两种C18柱的价格及维护费用,选择使用Grance Alltima 4.6mm×150mm C18进行大批量的实验分析,在保证实验数据的准确可靠前提下,能有效降低成本。[img]https://ng1.17img.cn/bbsfiles/images/2020/08/202008192125466015_1144_2166779_3.jpg[/img] [img]https://ng1.17img.cn/bbsfiles/images/2020/08/202008192125467275_3703_2166779_3.jpg[/img]图3 酱腌菜中对羟基苯甲酸酯类色谱图(HPLC-20A)峰序同图2 图4 酱腌菜中对羟基苯甲酸酯类色谱图(UPLC)2.3 基质的干扰与条件优化 [size=16px] [/size][size=12px]实验选择糕点、果蔬汁饮料及酱油及酱腌菜类为基质,采用上述方法进行前处理,岛津HPLC-20A,Grance Alltima 4.6mm×150mm C18进行分析检测,发现果蔬汁及饮料等,基质简单,峰形对称(见图5);在进行酿造酱油基质的加标回收分析时发现,甲酯由于出峰时间较早,容易被杂质峰包埋,致使检测的检出限降低(见图6);酱腌菜类食品由于基质复杂,特别是在腌制过程中产生的不明物质较多且各有差异,在实验中稍有不慎,极容易与对羟基苯甲酸乙酯、丙酯产生干扰(见图7),因此在进行分析过程中应注意色谱条件的选择,改变流动相中甲醇的比例能有效避免杂质的干扰。[/size][img=,690,331]https://ng1.17img.cn/bbsfiles/images/2020/08/202008192131109762_6420_2166779_3.png!w690x331.jpg[/img][img=,690,308]https://ng1.17img.cn/bbsfiles/images/2020/08/202008192131386200_7631_2166779_3.png!w690x308.jpg[/img][img=,690,325]https://ng1.17img.cn/bbsfiles/images/2020/08/202008192131527267_1909_2166779_3.png!w690x325.jpg[/img][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]国标GB5009.31-2016《食品安全国家标准 对羟基苯甲酸酯类的测定》检测范围为酱油、醋、饮料及果酱,采用GC酸化提取后进行分析检测,实验原理与本方法可互为验证和补充,但操作步骤复杂,耗时长,乙醚试剂消耗大,对检测人员伤害较大,且效率低,但基质处理的干净,不存在干扰而产生假阳性的情况。仪器条件:Agilent 7890 检测器:FID 进样量:1 μL 色谱柱:[color=black]HP-1(30m*320μm*0.25μm);HP-5(30m*320μm*0.25μm) ;DB-17 30m*320μm*0.25μm ; [/color][color=red]HP-5MS(30m*320μm*0.25μm)[/color][color=red] [/color]检测器温度:240[font=宋体]℃[/font] 进样温度:250[font=宋体]℃[/font]程序升温:100[font=宋体]℃[/font](1min) 20 [font=宋体]℃[/font]/min 160[font=宋体]℃[/font](3min) 15 [font=宋体]℃[/font]/min 250[font=宋体]℃[/font](3min)样品处理:取样5.0 g(±0.01 g)于50 mL塑料离心管中,加入1 mL盐酸(1:1)溶液酸化,再加入10 mL饱和氯化钠水溶液摇匀,分别每次30 mL乙醚提取三次,涡旋振荡4000 r/min离心,取上清液乙醚合并入250 mL分液漏斗中,先加入10 mL饱和氯化钠水溶液洗涤一次弃去水层,分别每次30 mL 1g/100mL的碳酸氢钠溶液洗涤洗三次 ,静置,弃去水层。过装有10 g无水硫酸钠的漏斗至鸡心瓶中,35[font=宋体]℃[/font]浓缩至干,用无水乙醇定容至2 mL上机测试。注释:[color=red](1)使用HP-5MS色谱柱主要是为了增加分离度,使得目标峰与分析纯乙醚中的干扰峰分离开。[/color](2)对羟基苯甲酸乙酯处有试剂干扰,来自乙醚。(3) 标准中使用125 mL的分液漏斗,实验室直接使用50mL的塑料离心管更易于提取。(4) 标准中用75 mL、50 mL、50 mL乙醚提取三次,实验室用离心管离心取上层乙醚层更方便,由于离心管容积只有50 mL,所以减少乙醚量,分别每次用20 mL乙醚提取三次。(5) 标准中用分液漏斗萃取,静置弃去水层,实验室用离心的方法分层,取上清液乙醚层。(6) 标准中在分液漏斗中加10 g无水硫酸钠于室温放置30 min脱水,实验室过装有10 g无水硫酸钠的漏斗脱水。色谱图分析比较:通过图8、图9([url=https://insevent.instrument.com.cn/t/Mp]气相[/url]法前处理)与图5~图7(液相法前处理)比较,[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]的图谱明显干净多了,而且不存在一点的基质干扰的现象。 [img]https://ng1.17img.cn/bbsfiles/images/2020/08/202008192125470058_269_2166779_3.png[/img] [img]https://ng1.17img.cn/bbsfiles/images/2020/08/202008192125470897_3417_2166779_3.png[/img]果酱食品基质加标(2ppm) b. 果酱类食品空白基质图8 果酱食品中对羟基苯甲酸酯类空白基质及基质加标(2ppm) [img]https://ng1.17img.cn/bbsfiles/images/2020/08/202008192125471786_7777_2166779_3.png[/img] [img]https://ng1.17img.cn/bbsfiles/images/2020/08/202008192125472549_3883_2166779_3.png[/img] a. [size=12px]果酱食品基质加标(2ppm) b. 果酱食品空白基质 [/size] [size=12px]图9 果酱食品中对羟基苯甲酸酯类空白基质及基质加标(2ppm) [/size]按国标GB5009.31-2016检测方法线性范围和测定低限:在1~500 μg/mL浓度范围内,以峰面积(y)与目标化合物浓度(x,μg/mL)绘制标准工作曲线。结果表明,在1.0~500 μg/mL质量浓度范围内,目标化合物良好线性关系,线性方程式、线性关系和测定低限(LOQ,S/N=10)见表2。表2 线性方程式、线性相关系数和定量限[table][tr][td][align=center]化合物[/align][/td][td][align=center]线性方程式[/align][/td][td][align=center]线性相关系数[/align][/td][td][align=center]定量限/(mg/kg)[/align][/td][/tr][tr][td][align=center]对羟基苯甲酸甲酯[/align][/td][td][align=center]Y=0.532847x-1.26878[/align][/td][td][align=center]0.99915[/align][/td][td][align=center]2.0[/align][/td][/tr][tr][td][align=center]对羟基苯甲酸乙酯[/align][/td][td][align=center]Y=0.563352x-1.13532[/align][/td][td][align=center]0.99972[/align][/td][td][align=center]2.0[/align][/td][/tr][tr][td][align=center]对羟基苯甲酸丙酯[/align][/td][td][align=center]Y=0.554134x-2.50160[/align][/td][td][align=center]0.99915[/align][/td][td][align=center]2.0[/align][/td][/tr][tr][td][align=center]对羟基苯甲酸丁酯[/align][/td][td][align=center]Y=0.530932x-4.29406[/align][/td][td][align=center]0.99971[/align][/td][td][align=center]2.0[/align][/td][/tr][/table] 回收率和精密度分别向空白蚝油中添加目标物,做空白添加回收试验,添加水平为2.0、5.0、50.0 mg/kg,各添加水平分别做6次平行试验。加标回收率为88.7%~108%,相对标准偏差(RSD)为1.3~5.2%,方法的精密度及回收率均满足定量测定的要求,试验结果见表3。[size=12px][font=times new roman] [img=,690,371]https://ng1.17img.cn/bbsfiles/images/2020/08/202008192133361979_6058_2166779_3.png!w690x371.jpg[/img][/font][/size] 总结: [font=宋体][size=12px]国标方法是用盐酸酸化样品,乙醚提取,浓缩后,用具有氢火焰离子化检测器的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]进行分离检测,外标法定量;耗时长、成本高、消耗大、毒性强、工作效率低等弱点,极大的限制了在食品检测过程中的广泛运用,优点是谱图干净,几乎没有基质干扰的现象。针对食品检测工作中样品量大、基质干扰多、成分复杂且易变质腐败等特点,在检测过程中也需要建立一种准确高效的检测方法运用于实际工作;液相法是一种快捷、准确、适用范围广的方法,以满足检测工作的需要,达到提高工作效率的目的。遇到有基质干扰,不合格的样品时改用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法进行准确定量检测。[/size][/font] [size=12px] [/size]
本人因论文需要求购以下农药标准品: 3-羟基克百威, 涕灭威, 涕灭威砜, 涕灭威亚砜, 丙硫克百威, 丁硫克百威, 硫双灭多威,残杀威, 苯恶威, 灭多威, 杀线威(以上最好是便宜的标准溶液).越便宜越好。希望尽快了解产品的包装规格,含量,价格等详细资料。多谢[em06]
光催化抗菌材料及制品抗菌性能的评价Photo-catalytic antimicrobial materials and products-Assessment for antimicrobial activity and efficacy 我现在只有国标,我需要一份其他相关的权威标准(美国等国家的标准)[em09501][em09501][em09511]非常感谢!!!yanxiali2009@yahoo.com.cn
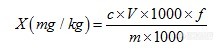
[align=center][b]对食品中羟基苯甲酸酯类的检测学习探讨[/b][/align][align=center][b] 西安国联质量检测技术股份有限公司[/b][/align][align=center][b] 食品事业部:牛晓[/b][/align][b]1.原理[/b] 试样经无水乙醇超声提取,采用高效液相色谱仪测定,保留时间定性,峰面积外标法定量。实验方法参考张艳达等食品中对羟基苯甲酸酯类的检测-高效液相色谱法(CumulativetyNO.272)[b]材料与方法[/b]2.1仪器设备与耗材高效液相色谱仪:配紫外检测器、0.45μm滤膜,有机系、分析天平:感量为0.0001g 、氮吹仪、组织捣碎机、超声波发生器。2.2试剂乙腈:色谱纯、甲醇:色谱纯、乙醇:分析纯。对羟基苯甲酸甲酯(1000.0μg/mL)标品。对羟基苯甲酸乙酯(1000.0μg/mL)标品。对羟基苯甲酸丙酯(1000.0μg/mL)标品。[b]试样提取[/b]3.1固体试样:准确称取样品5g(精确至0.01g),置于50mL比色管中,加入25mL无水乙醇,置超声波水浴中提取10min,取出4000r/min离心10min,上清液转入50mL容量瓶中,残渣再用20mL无水乙醇重复提取一次,合并上清液,用无水乙醇定容至刻度,过0.45μm滤膜过滤。供液相色谱分析。3.2液体试样:准确称取样品5g(精确至0.01g),置于50mL比色管中,加入25mL无水乙醇,置超声波水浴中提取10min,取出等冷却至室温时用无水乙醇定容至刻度,过0.45μm滤膜过滤。供液相色谱分析。3.3[b] 色谱条件:[/b]3.3.1色谱柱:C18柱,柱长250mm,内径4.6mm,粒径5μm;3.3.2流动相:水:乙腈=45:553.3.3流速:1mL/min ;3.3.4检测波长:254nm;3.3.5进样体积20μL。3.3.6柱温:25℃3.4外标法计算公式:[align=center][img=,224,50]http://ng1.17img.cn/bbsfiles/images/2017/09/201709080923_01_2904018_3.png[/img][/align]式中:C-由标准曲线所得样品溶液各组分浓度,μg/ mL;V-定容体积,mL;m-称样质量g;f-稀释倍数。 两次测试结果的相对误差小于10%即为测试平行[b]4实验结果[/b]4.1外标法标准曲线线性的确定分别精确吸取对羟基苯甲酸甲酯、对羟基苯甲酸乙酯和对羟基苯甲酸丙酯1000.0μg/mL的标准储备液5.0μL、12.5μL、25.0μL、40.0μL、50.0μL、125.0μL 、250.0μL于5 0mL容量瓶中,用无水乙醇配制成0.1、0.25 、0.5、0.8、1.0 、2.5 、5.0μg/mL标准溶液,按照上述已确定的色谱条件,进样20μL,测定对羟基苯甲酸酯类浓度与峰面积的相关性,确定相关系数及线性范围,标准曲线见图1。可见,对羟基苯甲酸甲酯、对羟基苯甲酸乙酯和对羟基苯甲酸丙酯在0.1[sub]~[/sub]5.0μg/mL范围内,含量与色谱峰面积呈显著的线性关系,可满足定量分析的需要。对羟基苯甲酸甲酯:[u]Y=73446.0X-3284.05 R2=0.9994227[/u][align=center][img=,583,392]http://ng1.17img.cn/bbsfiles/images/2017/09/201709080924_01_2904018_3.png[/img][/align]对羟基苯甲酸乙酯:[u]Y=120633X-637.664 R2=0.9998993[/u][align=center][img=,578,375]http://ng1.17img.cn/bbsfiles/images/2017/09/201709080924_02_2904018_3.png[/img][/align]对羟基苯甲酸丙酯:[u]Y=101679X+626.935 R2=0.9996277[/u][align=center][img=,584,385]http://ng1.17img.cn/bbsfiles/images/2017/09/201709080924_03_2904018_3.png[/img][/align] 图1 对羟基苯甲酸酯类标准曲线图4.2检出限取0.8μg/mL和1.0μg/mL标准溶液梯度稀释进样,至S/N=3±1,确定出对羟基苯甲酸甲酯和对羟基苯甲酸乙酯检出限为0.08μg/mL,对羟基苯甲酸丙酯检出限为0.1μg/mL。即本方法的对羟基苯甲酸甲酯和对羟基苯甲酸乙酯检出限为0.8mg/kg,对羟基苯甲酸丙酯检出限为1.0mg/kg。3.3加标回收及重复性 对样品进行加标回收实验,加标浓度设0.5μg/mL、0.8μg/mL、1.2μg/mL,回收率结果见表1,可见对样品进行三个浓度的加标回收率在90%[sub]~[/sub]112%之间。称取6个样品,分别对其进行5.0μg/mL加标,做准确度实验,重复性实验结果见表2,结果可见,对羟基苯甲酸酯类的平均回收率在98.0%~105%之间,RSD为对羟基苯甲酸甲酯2.44%、对羟基苯甲酸乙酯1.13%、对羟基苯甲酸丙酯0.49%由表1和表2结果表明本实验方法能够满足分析要求。[align=center] 表1对羟基苯甲酸酯类加标回收率结果[/align][align=center][img=,634,116]http://ng1.17img.cn/bbsfiles/images/2017/09/201709080926_01_2904018_3.png[/img][/align]样品图谱[align=center][img=,624,256]http://ng1.17img.cn/bbsfiles/images/2017/09/201709080926_02_2904018_3.png[/img][/align]加标0.5μg/mL即加标值4.97(mg/kg)图2[align=center][img=,614,261]http://ng1.17img.cn/bbsfiles/images/2017/09/201709080926_03_2904018_3.png[/img][/align]加标0.8μg/mL,即加标值7.95(mg/kg)图谱3[align=center][img=,623,251]http://ng1.17img.cn/bbsfiles/images/2017/09/201709080927_01_2904018_3.png[/img] [/align]加标1.2μg/mL,即加标值11.86(mg/kg)图谱4[align=center]表2对羟基苯甲酸酯类方法重复性实验[/align][align=center][img=,690,330]http://ng1.17img.cn/bbsfiles/images/2017/09/201709080927_02_2904018_3.png[/img][/align][align=center][img=,678,599]http://ng1.17img.cn/bbsfiles/images/2017/09/201709080928_01_2904018_3.png[/img][img=,649,293]http://ng1.17img.cn/bbsfiles/images/2017/09/201709080928_02_2904018_3.png[/img][/align][align=center][img=,637,530]http://ng1.17img.cn/bbsfiles/images/2017/09/201709080929_01_2904018_3.png[/img] [/align][align=center]加标重复性实验结果图5[/align][b]5.结论[/b]综上所述:苏打水中对羟基苯甲酸酯类方法学经从线性、重复性、回收率、准确度、最低检出限均符合分析要求。本方法的对羟基苯甲酸甲酯和对羟基苯甲酸乙酯检出限为0.8mg/kg,对羟基苯甲酸丙酯检出限为1.0mg/kg,本方法可以用于苏打水中对羟基苯甲酸酯类的测定。
求助:对羟基苯甲酸丁酯钠和对羟基苯甲酸丙酯钠的相关行业标准,国内、国外的标准都可以。
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=66614]羟基与萘甲酸生产标准 [/url]
各位同仁们帮个忙,谁有工业用对羟基苯甲酸国家标准,可不可以上传一个。谢谢大家的帮忙!
对羟基苯甲酸甲乙丙酯的标准溶液有很多杂峰正常吗?我感觉理论上应该是只有三个大的色谱峰,结果出了十多个[img]https://ng1.17img.cn/bbsfiles/images/2023/10/202310191022364344_1417_5979722_3.png[/img]
[align=center]邓 文 婷[/align][align=center]2021[font='华文中宋']年[font='华文中宋'] 7 [size=21px]月27日[/size][/font][/font][/align][align=center][/align][align=center][/align][align=center][size=21px]二丁基羟基甲苯[/size][/align][align=center][/align][摘要] 二丁基羟基甲苯是国内外广泛使用的油溶性抗氧化剂,主要应用于食用油脂、油炸食品、干鱼制品、饼干、方便面、速煮米、果仁罐头、腊制肉制品等,但长期过量食用含抗氧化剂的食品,对人体肝、脾、肺均有不利影响,因此各国对食用抗氧化剂都有严格的使用限量规定。本篇主要总结二丁基羟基甲苯的相关性质、标准、限量、检测方法以及其应用,供学习参考。[align=left][关键词] 二丁基羟基甲苯 检测方法 标准[/align][align=left][/align]二丁基羟基甲苯英文名:Butyl Hydroxy Toluene (Butylated Hydoxy Toluene),又名丁羟甲苯(dibutyl hydroxy toluene),别名 2,6-二叔丁基对甲酚、3,5-二叔丁基-4-羟基甲苯、BHT。分子式为C15H240,相对分子质量220.35,其结构式如图1所示。BHT可用于长期保存的油脂和含油脂较高的食品及饲料中和维生素中,可以单独使用,也可以与丁基羟基茴香醚(BHA)和特丁基对苯二酚(TBHQ)是混合使用,主要通过与油脂在自动氧化过程中所产生的过氧化物结合,形成氢过氧化物,从而阻止氧化过程的进行,形成抗氧化剂自由基,达到抗氧化、防酸败、防变色等效果。[1]但长期过量食用含抗氧化剂的食品,对人体肝、脾、肺均有不利影响,同时也会对水体有一定危害。为方便研究,本文主要总结BHT 的以下理化性质、应用、标准、限量及检测方法。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/08/202108042154569522_2600_1608728_3.png[/img][/align][align=center]1、 理化性质[/align]二丁基羟基甲苯为白色结晶或结晶性粉末,无味或稍有特殊性气味、可燃;熔点69~73℃,沸点265℃,相对密度 1.048g/cm3,折射率为1.4859,闪点为127℃;对热稳定,具有单酚型特征的升华性,遇光颜色变黄,并逐渐变深;与金属离子作用不会着色,是常用的油脂抗氧化剂;不溶于水、丙二醇、甘油及10% 烧碱溶液,易溶于酒精、甲醇、异丙醇、丙酮、甲乙酮、苯、甲苯、动植物油、石油醚、亚麻子油,常温下在下列溶剂中的溶解度:甲醇25%,乙醇25%~26%,异丙醇30%,矿物油30%,丙酮40%,石油醚50%,苯40%,猪油(40~50℃)40%~50%,玉米油及大豆油40%~50%。[align=center]2、 应用[/align]BHT虽毒性较大,但其抗氧化能力较强,耐热及稳定性好,既没有特异臭,也没有遇金属离子呈色反应等缺点,而且价格低廉,我国仍作为主要抗氧化剂使用。一般与BHA配合使用,并以柠檬酸或其他有机酸为增效剂。本品也具有一定的抗菌作用,但较BHA弱。[align=left](一)可作食品加工工业用的抗氧剂,用于含油脂较多的食品中。我国规定可用于食用油脂、油炸食品、饼干、方便面、速煮米、果仁罐头、干鱼制品和腌腊肉制品。[/align][align=left](二)可作为饲料抗氧化剂,保护饲料中的维生素,防止脂肪和蛋白质的氧化损失,也具有一定的抗菌作用。美、日和欧洲共同体都将BHT作为法定的饲料添加剂,欧洲共同体规定,在饲料中的最大用量为150ppm,可用于各种饲料。[/align](三)可作为通用型酚类抗氧剂,还广泛用于高分子材料、石油制品和食品加工工业中。本品是常用的橡胶防老剂。对热、氧老化有一定的防护作用,也能抑制铜害。单独使用没有抗臭氧能力,但与抗臭氧剂及蜡并用可防护天候的各种因素对硫化胶的损害。在丁苯胶中亦可作为胶凝抑制剂。在橡胶中一般用量为0.5~3份。BHT还可做为合成橡胶后的处理和贮存时的稳定剂,可用于丁苯橡胶、顺丁橡胶、乙丙橡胶、氯丁橡胶等胶种。抗氧剂264在一些高分子材料中是有效的抗氧剂。BHT在聚乙烯、聚氯乙烯(用量0.01~0.1%)及聚乙烯基醚中是有效的稳定剂。(四)也可用作化妆品、香料等的抗氧剂,另外还可用作润滑油及燃料油添加剂,提高油品稳定性。[2][align=center]3、 限量[/align](一)我国《食品添加剂使用卫生标准》(GB 2920-1996)规定:可用于油脂、油炸食品、干鱼制品、饼干、方便面、速煮米、干果罐头、腌腊肉制品,最大使用量为0.2g/kg。BHT与BHA混合使用时,总量不得超过0.2g/kg;BHT、BHA与没食子酸丙酯混合使用时,BHA、BHT总量不得超过0.1g/kg,没食子酸丙酯不得超过0.05g/kg,最大使用量以脂肪计。(二)我国台湾省《食品添加剂使用范围及使用量标准》(1986)规定:用于油脂、奶油、干鱼贝制品及腌制品,最大使用量为0.2g/kg以下;冷冻鲜贝类、冷冻鲸肉的浸渍液,最大使用量为0.1g/kg以下,口香糖,泡泡糖最大使用量0.75g/kg以下。并且规定,当混合使用抗氧化剂时,要用标准除使用量,其得数不得大于1。(三)日本规定:用于鱼贝冷冻品(生食用冷冻鱼贝及生食用冷冻牡蛎除外)、鲸鱼冷冻品的浸渍液(生食冷冻鲸鱼肉除外),最大使用量1g/kg;油脂、奶油、鱼贝干制品、鱼贝盐制品、干燥类淀粉,最大使用量0.2g/kg;口香糖,最大使用量0.75g/kg。(四)FAO/WHO(1984)规定:一般食用油脂单用BHT或与BHT、TBHQ、没食子酸酯类合用,最大使用量为0.2g/kg(其中没食子酸酯类不得超过100mg/kg);用于乳脂肪最大使用量为0.2g/kg;与BHA、没食子酸酯类合用总量为0.2g/kg,而没食子酸酯类不得超过10mg/kg,不得用于直接消毒,也不得用于调制奶及其制品;用于人造奶油,单用或与BHA、没食子酸酯类合用,最大使用量为0.1g/kg。(五)BHT也可加入焙烤食品、速冻食品及其他方便食品的包装纸或包装塑料中,使用量为0.2~1kg/t包装材料。[align=center]4、 标准[/align](1) GB 5009.32-2016 《食品安全国家标准 食品中9种抗氧化剂的测定》[3]本标准规定了食品中没食子酸丙酯(PG)、2,4,5-三羟基苯丁酮(THBP)、叔丁基对苯二酚(TBHQ)、去甲二氢愈创木酸(NDGA)、叔丁基对羟基茴香醚(BHA)、2,6-二叔丁基-4-羟甲基苯酚(1onox-100)、没食子酸辛酯(OG)、BHT、没食子酸十上酯(DG)9种抗氧化剂的5种测定方法—高效液相色谱法、液相色谱串联质谱法、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]质谱法、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法以及比色法。本标准液相色谱法适用于食品中PG、THBP、TBHQ、NDGA、BHA、BHT、lonox100、OG、DG的测定;液相色谱串联质谱法适用于食品中THBP、PG、OG、NDGA、DG的测定;[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]质谱法适用于食品中BHA、BHT、TBHQ、 lonox-100的测定;[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法适用于食品中BHA、BHT、TBHQ的测定;比色法适用于油脂中PG的测定。(2) GB 1900-2010《食品添加剂二丁基羟基甲苯》[4]本标准适用于以对甲酚、异丁醇为原料,以浓硫酸作为催化剂,氧化铝作为脱水剂,反应生成的食品添加剂BHT。[align=left]相关理化指标如标1所示。[/align][align=center]表1 GB 1900-2010《食品添加剂二丁基羟基甲苯》理化指标[/align][align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/08/202108042154571084_352_1608728_3.png[/img][/align][align=center][/align][align=center]5、 检测方法[/align]目前报道的BHT的检测方法主要有液相色谱法[5-8]、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法[9]、毛细管电泳法[10]、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱法[11]、荧光光谱法[12]等。(1) 、高效液相色谱法1、原理油脂样品经有机溶剂溶解后,使用凝胶渗透色谱(GPC)净化;固体类食品样品用正己烷溶解,用乙腈提取,固相萃取柱净化。高效液相色谱法测定,外标法定量。2、试剂和材料除非另有说明,本方法所用试剂均为色谱纯,水为GB/T 6682规定的一级水。(1)试剂甲酸(HCOOH)、乙腈(CH3CN)、甲醇(CH3OH)、正己烷(C6H14):分析纯,重蒸、乙酸乙酯(CH3COOCH2CH3)、环己烷(C6H12)、氯化钠(NaCl):分析纯、无水硫酸钠(Na2SO4):分析纯,650℃灼烧4h,贮存于干燥器中,冷却后备用。(2)试剂配制乙腈饱和的正己烷溶液:正己烷中加入乙腈至饱和。正己烷饱和的乙腈溶液:乙腈中加入正己烷至饱和。乙酸乙酯和环己烷混合溶液(1+1):取50mL乙酸乙酯和50mL环己烷混匀。乙腈和甲醇混合溶液(2+1):取100mL乙腈和50mL甲醇混合。饱和氯化钠溶液:水中加入氯化钠至饱和。甲酸溶液(0.1+9.9):取0.1mL甲酸移入100mL容量瓶,定容至刻度。(3)标准品2,6-二叔丁基对甲基苯酚:纯度≥98%(4)标准溶液配制2,6-二叔丁基对甲基苯酚标准物质混合储备液:准确称取0.1g(精确至0.1mg)固体2,6-二叔丁基对甲基苯酚标准物质,用乙腈溶于100mL棕色容量瓶中,定容至刻度,配制成浓度为1000mg/L的标准混合储备液,0℃~4℃避光保存。2,6-二叔丁基对甲基苯酚混合标准使用液:移取适量体积的浓度为1000mg/L的2,6-二叔丁基对甲基苯酚标准物质混合储备液分别稀释至浓度为20mg/L、50mg/L、100mg/L、200mg/L、400mg/L的混合标准使用液。(5)材料C18固相萃取柱:2000mg/12mL;有机系滤膜:孔径0.22μm。(6)仪器和设备离心机:转速≥3000r/min;旋转蒸发仪;高效液相色谱仪;凝胶渗透色谱仪;分析天平:感量为0.01g和0.1mg;涡旋振荡器。3、分析步骤(1)试样制备固体或半固体样品粉碎混匀,然后用对角线法取四分之二或六分之二,或根据试样情况取有代表性试样,密封保存;液体样品混合均匀,取有代表性试样,密封保存。(2)测定步骤1)提取a固体类样品:称取1 g(精确至0.01 g)试样于50 mL离心管中,加入5 mL乙腈饱和的正己烷溶液,涡旋1min充分混匀,浸泡10 min。加入5mL饱和氯化钠溶液,用5 mL正己烷饱和的乙腈溶液涡旋2 min,3000 r/min离心5min,收集乙腈层于试管中,再重复使用5 mL正己烷饱和的乙腈溶液提取2次,合并3次提取液,加0.1%甲酸溶液调节pH=4,待净化。同时做空白试验。b油类:称取1g(精确至0.01 g)试样于50mL离心管中,加入5 mL乙腈饱和的正己烷溶液溶解样品,涡旋1 min,静置10 min,用5 mL正己烷饱和的乙腈溶液涡旋提取2 min,3 000 r/min离心5min,收集乙腈层于试管中,再重复使用5 mL正己烷饱和的乙腈溶液提取2次,合并3次提取液,待净化。同时做空白试验。2)净化在C18固相萃取柱中装入约2 g的无水硫酸钠,用5 mL甲醇活化萃取柱,再以5 mL乙腈平衡萃取柱,弃去流出液。将所有提取液倾入柱中,弃去流出液,再以5 mL乙腈和甲醇的混合溶液洗脱,收集所有洗脱液于试管中,40℃下旋转蒸发至干,加2 mL乙腈定容,过0.22μm有机系滤膜,供液相色谱测定。3)凝胶渗透色谱法(纯油类样品可选)称取样品10g(精确至0.01 g)于100 mL容量瓶中,以乙酸乙酯和环己烷混合溶液定容至刻度,作为母液;取5 mL母液于10 mL容量瓶中以乙酸乙酯和环己烷混合溶液定容至刻度,待净化。取10 mL待测液加入凝胶渗透色谱(GPC)进样管中,使用GPC净化,收集流出液,40℃下旋转蒸发至干,加2 mL乙腈定容,过0.22μm有机系滤膜,供液相色谱测定。同时做空白试验。(3)液相色谱仪条件色谱柱:C18柱,柱长250mm,内径4.6mm,粒径5μm,或等效色谱柱流动相A:0.5%甲酸水溶液,流动相B:甲醇洗脱梯度:0-5min:流动相(A)50%,5min-15min:流动相(A)从50%降至20%,15min-20min:流动相(A)20%,20min-25min:流动相(A)从20%降至10%,25min-27min,流动相(A)从10%增至流动相50%,27min-30min:流动相(A)50%。柱温:35℃进样量:5μL检测波长:280nm。(4)标准曲线的制作将系列浓度的标准工作液分别注入液相色谱仪中,测定2,6-二叔丁基对甲基苯酚,以标准工作液的浓度为横坐标,以响应值(如:峰面积、峰高、吸收值等)为纵坐标,绘制标准曲线。(5)试样溶液的测定将试样溶液注入高效液相色谱仪中,得到相应色谱峰的响应值,根据标准曲线得到待测液中2,6-二叔丁基对甲基苯酚的浓度。(6)分析结果的表述试样中2,6-二叔丁基对甲基苯酚含量按式(1)计算:Xi=ρi×V/m……(1)式中:Xi-试样中2,6-二叔丁基对甲基苯酚含量,单位为毫克每千克(mg/kg);ρi-从标准曲线上得到的2,6-二叔丁基对甲基苯酚溶液浓度,单位为微克每毫升(μg/mL);V-样液最终定容体积,单位为毫升(mL);M-称取的试样质量,单位为克(g)。结果保留三位有效数字(或保留到小数点后两位)。(7)精密度在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%。(8)其他本方法的检出限为2,6-二叔丁基对甲基苯酚(BHT):4mg/kg,定量限为20mg/kg。(2) 、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]质谱法1、原理油脂样品经有机溶剂溶解后,使用凝胶渗透色谱(GPC)净化;固体类食品样品用正己烷溶解,用乙腈提取,固相萃取柱净化。[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱联用仪测定,外标法定量。2、试剂和材料试剂、试剂配制、标准品、材料基本同上,仪器将高效液相色谱仪换为[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]质谱联用仪。(1)标准溶液配制2,6-二叔丁基对甲基苯酚标准物质储备液:准确称取0.1g(精确至0.1mg)固体2,6-二叔丁基对甲基苯酚标准物质,用乙腈溶于100mL棕色容量瓶中,定容至刻度,配制成浓度为1000mg/L的标准混合储备液,0℃~4℃避光保存。2,6-二叔丁基对甲基苯酚混合标准使用液:移取适量体积的浓度为1000mg/L的2,6-二叔丁基对甲基苯酚标准物质储备液分别稀释至浓度为1mg/L、2mg/L、5mg/L、10mg/L、20mg/L、50mg/L、100mg/L、200mg/L的混合标准使用液。3、分析步骤试样制备、测定步骤、分析结果的表述、精密度同上。(1)[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]质谱仪条件色谱柱:5%苯基-甲基聚硅氧烷毛细管柱,柱长30m,内径0.25mm,膜厚0.25μm,或等效色谱柱;色谱柱升温程序:70℃保持1min,然后以10℃/min程序升温至200℃保持4min,再以10℃/min升温至280℃保持4min; 载气:氦气,纯度≥99.999%,流速1mL/min; 进样口温度:230℃; 进样量:1μL; 进样方式:无分流进样,1min后打开阀; 电子轰击源:70eV; 离子源温度:230℃;[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]-MS接口温度:280℃; 溶剂延迟8min;选择离子监测:每种化合物分别选择一个定量离子,2个-3个定性离子。每组所有需要检测离子按照出峰顺序,分时段分别检测。(2)定性测定在相同试验条件下进行样品测定时,如果检出的色谱峰的保留时间与标准样品相一致,并且在扣除背景后的样品质谱图中,所选择的离子均出现,而且所选择的离子丰度比与标准样品相一致(相对丰度50%,允许±20%偏差;相对丰度20%~50%,允许±25%偏差;相对丰度10%~20%,允许±30%偏差;相对丰度≤10%,允许±50%偏差),则可判断样品中存在2,6-二叔丁基对甲基苯酚。(3)标准曲线的制作将标准系列工作液进行[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]串联质谱仪测定,以定量离子对峰面积对应标准溶液浓度绘制标准曲线。(4)试样溶液的测定将试样溶液注入[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]质谱联用仪中,得到相应色谱峰响应值,根据标准曲线得到待测液中2,6-二叔丁基对甲基苯酚的浓度。 (5)其他本方法的检出限为2,6-二叔丁基对甲基苯酚(BHT):0.5mg/kg,定量限为1mg/kg。(3) 、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法 1、原理样品中的2,6-二叔丁基对甲基苯酚用有机溶剂提取、凝胶渗透色谱(GPC)净化后,用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]氢火焰离子化检测器检测,采用保留时间定性,外标法定量。2、试剂和材料除非另有说明,本方法所用试剂均为色谱纯,水为GB/T 6682规定的一级水。(1)试剂环己烷(C6H12);乙酸乙酯(CH3COOCH2CH3);石油醚:沸程30℃~60℃(重蒸);乙腈(CH3CN);丙酮(CH3COCH3)(2)试剂配制乙酸乙酯和环己烷混合溶液(1+1):量取50mL乙酸乙酯和50mL环己烷混匀。(3)标准品BHT标准品:纯度≥99.3%。BHT标准储备液:准确称取BHT标准品各50g(精确至0.1mg),用乙酸乙酯和环己烷混合溶液定容至50mL,配制成1mg/mL的储备液,于4℃冰箱中避光保存。BHT标准使用液:吸取标准储备液0.1mL、0.5mL、1.0mL、2.0mL、3.0mL、4.0mL、5.0mL于一组10mL容量瓶中,用乙酸乙酯和环己烷混合溶液定容,此标准系列的浓度为0.01mg/mL、0.05mg/mL、0.1mg/mL、0.2mg/mL、0.3mg/mL、0.4mg/mL、0.5mg/mL,现用现配。(4)材料有机系滤膜:孔径0.45μm。(5)仪器和设备[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]([url=https://insevent.instrument.com.cn/t/Mp]gc[/url]):配氢火焰离子化检测器(FID)。凝胶渗透色谱仪(GPC),或可进行脱脂的等效分离装置。 分析天平:感量为0.01g和0.1mg。旋转蒸发仪;涡旋振荡器;粉碎机。3、分析步骤试样制备、分析结果的表述、精密度同上。(1)试样处理1)油脂样品混合均匀的油脂样品,过0.45μm滤膜后,准确称取0.5 g(精确至0.1 mg),用乙酸乙酯和环己烷的混合溶液准确定容至10.0 mL,混合均匀待净化。2)油脂含量较高或中等的样品(油脂含量15%以上的样品)根据样品中油脂的实际含量,称取5 g混合均匀的样品,置于250 mL具塞锥形瓶中,加入适量石油醚,使样品完全浸没,放置过夜,用快速滤纸过滤后,旋转蒸发回收溶剂,得到的油脂用乙酸乙酯和环己烷混合溶液准确定容至10.0 mL,混合均匀待净化。3)油脂含量少的试样(油脂含量15%以下的样品)和不含油脂的样品(如口香糖等)同法一中固体类样品处理步骤。(2)净化处理得到的试样经凝胶渗透色谱装置净化,收集流出液蒸发浓缩至近干,用乙酸乙酯和环已烷混合溶液定容至2mL,进[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]分析。不同试样的前处理需要同时做试样空白试验。(3)色谱参考条件色谱柱:5%苯基-甲基聚硅氧烷毛细管柱,柱长30m,内径0.25mm,膜厚0.25μm,或等效色谱柱; 进样口温度:230℃; 升温程序:初始柱温80℃,保持1min,以10℃/min升温至250℃,保持5min; 检测器温度:250℃;进样量:1μL;进样方式:不分流进样;载气:氮气,纯度≥99.999%,流速1mL/min。(4)标准曲线的制作将标准系列工作液分别注入[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]中,测定2,6-二叔丁基对甲基苯酚,以标准工作液的浓度为横坐标,以响应值(如:峰面积、峰高、吸收值等)为纵坐标,绘制标准曲线。(5)试样溶液的测定将仪中试样溶液注入[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]谐,得到BHT的响应值,根据标准曲线得到待测液中2,6-二叔丁基对甲基苯酚的浓度。 (6)其他本方法的检出限为2,6-二叔丁基对甲基苯酚(BHT):2mg/kg,定量限为5mg/kg。(4) 、荧光光谱法1、原理在酸性条件下,高锰酸钾能氧化二丁基羟基甲苯,其产物具有良好的荧光特性,且测得产物的荧光强度与二丁基羟基甲苯的量呈良好的线性关系,在优化反应条件的基础上,可用来测定 BHT 。2、试剂和材料 荧光分光光度计;高功率数控超声波清洗器;pH 计;电子分析天平;数显恒温水浴锅。BHT(分析纯)储备液:称取0.2204 g BHT用无水乙醇溶解,移至100 mL容量瓶中,用无水乙醇稀释至刻度,配成 1.0×10-3mol/L的BHT储备液。高锰酸钾(分析纯);其他试剂均为分析纯,实验用水为二次蒸馏水。 3、实验方法在25 mL比色管中,分别依次加入不同体积2.2mg/L的 BHT标准溶液、2.0 mL pH 2.0的盐酸和2.0 mL1.0×10-4 mol/L KMnO4溶液,用95%乙醇稀释10 mL,振荡均匀,在75℃的水浴锅中加热50 min后取出,冷却至室温,测定荧光强度,记录数据绘制标准曲线。样品按照同样的实验方法反应后测定荧光强度再比对标准曲线便可得到BHT浓度。4、方法分析特性方法的检出限(S/N=3)为0.01 mg/L。该法文献并不多,可靠性不是很强,但是可以为检测BHT提供一种新的思路。[align=center]6、 结语[/align]食品中BHT的检测方法虽然在研究较多,但各类分析方法都具有一定的适用范围,同时分析多种不同基质食品中BHT的报道较少,而且仍然存在着样品前处理过程复杂、溶剂消耗多、耗时长、选择性不好、灵敏度不高等问题,无法满足含BHT食品的市场监管和进出口贸易要求,因而对于BHT的研究仍有待深入。参考文献[align=left][1]冯楠,李淑娟,蔡会霞,李建中,安娟,李刚.[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱法同时测定食品中3种脂溶性抗氧化剂[M].北京:中国卫生检验杂志,2008:1742-1743.[/align][2]李永强,陈福新,陈琦.食品级抗氧化剂BHT国内市场应用情况[J].现代食品,2020 ( 9) : 68-69.[3]中华人民共和国国家市场监督管理总局,中国国家标准化管理委员会.中华人民共和国国家标准 食品安全国家标准 食品中9种抗氧化剂的测定:GB 5009.32-2016[s].[/s]北京:中国标准出版社,2016. [4]中华人民共和国国家市场监督管理总局,中国国家标准化管理委员会.中华人民共和国国家标准 食品安全国家标准 食品添加剂二丁基羟基甲苯:GB 1900-2010[s].[/s]北京:中国标准出版社,2010. [5]续颖,刘雪莹,伍蓥,麦亨,黄秋娜,何聪容.高效液相色谱法测定食用植物油中TBHQ、BHA、BHT含量[M].安徽:安徽农业科学,2017:89-90.[6]现代测量与实验室管理,食品中叔丁基羟基茴香醚(BHA)与2,6-二叔丁基对甲酚(BHT)测定方法:GB/T5009.30—2003[s].2012[/s].[7]周惠惠,胡立学,刘佳佳,梅兴国.HPLC法测定维生素D3软胶囊中抗氧剂二丁基羟基甲苯的含量[J].中国民族民间医药,2021,30(8):26-29.[8]宋阳,管咏仪,邹志飞,等. 植物油中的丁基羟基茴香醚和二丁基羟基甲苯的超高效合相色谱测定法[J].职业与健康,2016(3):328-331.[9]陈集元.[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法检测水产配合饲料中的合成抗氧化剂[J].福建分析测试,2018,27(5):47-53.[10]毛江胜,陈子雷,杜红霞,等.毛细管[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定食用油中的酚类抗氧化剂BHA、BHT、TBHQ[J].化学分析计量,2006,15(6):11一12.[align=left][11]鞠福龙,李东刚,李春娟. [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]-MS-SIM法同时分析饮料中防腐剂和抗氧化剂[J]. 现代科学仪器,2010,1: 77-79.[/align][align=left][12]张蔚,冯娜,李满秀.荧光光谱法测定食品中二丁基羟基甲苯[J].食品安全质量检测学报,2015 ,6(8):3283-3286.[/align]
大家有没有用过中检所的抗生素标准品的?如头孢氨苄、阿莫西林等,我正在用,结果用液质联用检测出两个色谱峰,质谱结果显示,这两个峰都是同一种物质,猜测标准品不纯,是同分异构体的混合物,大家有没有类似的遭遇?
PBDE固体标准品哪里有啊?我们要过CMA评审,PBDE很难做,怕现场试验过不了啊,所以哪里有PBDE固体标准品,请喊一声,拜托了!
PBDE固体标准品哪里有啊?我们要过CMA评审,PBDE很难做,怕现场试验过不了啊,所以哪里有PBDE固体标准品,请喊一声[em0806],拜托了!
深圳福田区法院日前审结了一起案件,认定徐福记芒果酥、芝麻香酥沙琪玛含有国家规定不得在糕点或糖果类食品中添加的抗氧化剂,该行为已经构成对消费者的欺诈,必须作出赔偿。今年8月28日,广东一消费者在深圳家乐福商业有限公司购买了三款徐福记食品,其中一款是芒果酥,生产日期为2012年7月18日;另一款是芝麻香酥沙琪玛,净含量为35克,生产日期为2012年7月22日;还有一款落花生酥心糖,生产日期为2012年1月12日。 该消费者称,其在购买食品后才发现,徐福记的上述食品存在违规添加食品添加剂问题——在徐福记的上述食品产品标签中,标注含有食品添加剂TBHQ、BHT。而根据国家标准GB2760相关规定,特丁基对苯二酚(简称“TBHQ”)和二丁基羟基甲苯(简称“BHT”)两种食品添加剂不能添加到糕点或糖果类食品中,“TBHQ和BHT属于食品添加剂中的抗氧化剂,能防止或延缓油脂或食品成分氧化分解、变质,提高食品稳定性的物质。按照卫生部卫政申复2139号《政府信息公开告知书》,上述二种食品添加剂不能添加在糕点或糖果类食品里。”徐福记方面解释:涉案产品中的TBHQ和BHT并非人为添加,而是食品原料带入的。===================================================================================讨论:1、食品安全,原料带入与人为添加有依据判定吗?原料带入就能否定责任?2、征集食品中丁基羟基茴香醚(BHA)、二丁基羟基甲苯(BHT)与特丁基对苯二酚(TBHQ)的检测方法3、你检测过食品中抗氧化剂吗?都是什么食品呢?谈谈你的检测经验吧4、鼓励分享食品中抗氧化剂的检测原创分享,除了可以参加原创大赛,还可以获得100个积分奖励哦!!!*****************检测标准:GB T 23373-2009 食品中抗氧化剂丁基羟基茴香醚(BHA)、二丁基羟基甲苯(BHT)与特丁基对苯二酚(TBHQ)的测定
本标准代替GB 1916-1980本标准规定了食品添加剂叔丁基-4-羟基茴香醚的技术要求、试验方法、检验规则、标志、包装、运输、贮存及保质期。
各位老师,GB5009.31-2016是检测食品中对羟基苯甲酸酯。标准中检测原理是:试样酸化后,对羟基苯甲酸酯类用乙醚提取,浓缩近干用乙醇复溶,并利用氢火焰离子化检测器[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法进行分离测定,保留时间定性,外标法定量。我想请教的是为什么要酸化,酸化的作用是什么?是让目标成分都以酯的形式存在吗?
求助:12羟基硬脂酸 的羟值 用什么标准, 需要注意哪些事项, 在羟值计算时注意哪些问题? 反应机理是啥啊? 呼呼,求助!!!!!!
近期想购买一些标准品,做液相用;但对市场行情不甚了解,望知情的大虾不吝告知一下以下几个标准品的大致合理价格,3Q!丁香酸(syringic acid)香草酸(vanillic acid)对-羟基苯甲酸(p-hydroxybenzoic acid)香豆酸(coumaric acid)
[align=center][font=SimHei]食品安全标准[/font][/align] [b]第十八条[/b] 制定食品安全标准,应当以保障公众身体健康为宗旨,做到科学合理、安全可靠。 [b]第十九条[/b] 食品安全标准是强制执行的标准。除食品安全标准外,不得制定其他的食品强制性标准。 [b]第二十条[/b] 食品安全标准应当包括下列内容: (一)食品、食品相关产品中的致病性微生物、农药残留、兽药残留、重金属、污染物质以及其他危害人体健康物质的限量规定; (二)食品添加剂的品种、使用范围、用量; (三)专供婴幼儿和其他特定人群的主辅食品的营养成分要求; (四)对与食品安全、营养有关的标签、标识、说明书的要求; (五)食品生产经营过程的卫生要求; (六)与食品安全有关的质量要求; (七)食品检验方法与规程; (八)其他需要制定为食品安全标准的内容。
有高手用液谱做过食品中的对羟基苯甲酸酯的测定吗?我们现在做标准曲线,发现4个标准品的峰出峰不是很好,1,4个峰分得很开,各有各的时间段。2,每个峰分得不是太清晰,旁边都有杂峰3,要出第三个峰或者第四峰前,基线下降有高手做过的请指教!国标法是用气相的,但山东省有个标准是用液相,二极管检测器(DB37/T1100-2008),因为有甲乙丙丁四酯,这个标准上图谱是有的,但没指明各个是哪个峰。我怀疑,DB这个标准上标准溶液没指明有什么溶剂配制,我们就用水配制,但样品是用甲醇定容取上清液的,有做过的高手请说一下经验!
韩国拟定修改健康或功能食品标准和禁用成分相关法规来源:中国技术性贸易措施网 2009年10月12日,韩国发布通报:韩国食品药物管理局拟定修改健康/功能食品标准规范。本拟定法规制定和增加包括食物纤维在内的32种健康/功能食品吸收成分提示的相关规定。它还制定了卵磷酯、瓜尔胶/瓜尔胶水解物、葡甘露聚糖、阿拉伯树胶及聚葡萄糖内的铅含量规范,增加了瓜尔胶/瓜尔胶水解物及抗麦芽糖糊精的功效要求。此外,准许蜂胶提取物成品制成软胶囊。 韩国食品药物管理局拟定修改健康/功能食品禁用成分相关法规。 本拟定法规扩大健康/功能食品禁用植物成分的范围。本拟定措施还将减肥药、糖尿病药物及其它同类物质纳入健康/功能食品禁用植物成分清单。
[align=center][font='楷体'][size=21px]李敬贤[/size][/font][/align][align=center][font='黑体'][size=34px]《丁基羟基茴香醚及其检测》[/size][/font][/align]摘要:丁基羟基茴香醚是在食品中常用的氧化剂。2017年,世界卫生组织下属机构,国际癌症研究中心发布了致癌物清单,其中丁基羟基茴香醚被列为2B类。这意味着虽然它对人体致癌的证据有限,但仍然留有对人类致癌的可能。同时,有一系列证据显示,作为常用私聊添加剂的丁基羟基茴香醚,对鼠、家禽类有致突变作用。[1]所以,在食品检测时,对其进行定性定量的检测是必要。而为了探究其毒性来源于何处,我们有必要探究其作为抗氧化剂的抗氧化机理,以及合成路线,以分析排除其他因素致毒的干扰。最后,我们将从分析化学手段分析如何对丁基羟基茴香醚进行检测。[size=21px]一、丁基羟基茴香醚[/size][size=18px]1. [/size][size=18px]基本性质[/size][size=16px]丁基羟基茴香醚是白色或为黄色蜡状晶体粉末,带有酚类的特异臭气和刺激性气味,如下图所示,一般由两种异构体混合物组成(3[/size][size=16px]-BHA/2-BHA[/size][size=16px])。[/size][align=center][size=13px]图1[/size][size=13px] [/size][size=13px]构成[/size][size=13px]BHA[/size][size=13px]的两种混合异构体[/size][/align] [size=16px]其熔点由于是混合物的原因,通常随混合比的不同而出现波动,比如3[/size][size=16px]-BHA[/size][size=16px]占9[/size][size=16px]5%[/size][size=16px]的B[/size][size=16px]HA[/size][size=16px]熔点为6[/size][size=16px]2[/size][size=16px]℃。总的来说,丁基羟基茴香醚的熔点在5[/size][size=16px]7~65[/size][size=16px]℃之间。而由于相同原因,B[/size][size=16px]HA[/size][size=16px]沸点大致在2[/size][size=16px]64~270[/size][size=16px]℃之间。同时,B[/size][size=16px]HA[/size][size=16px]不溶于水,在常见溶剂和油脂中的溶解度大致在几十克每毫升,比如在花生油中为4[/size][size=16px]0 g/100 mL[/size][size=16px]。[/size][size=16px]作为一种带有酚羟基的抗氧化剂,在被提取出来时具有单酚型特征的挥发性。但对热很稳定,对光则容易被氧化,外观上看起来则是颜色加深,在弱碱性条件下较稳定。[/size][size=16px]与[/size][size=16px]2-BHA[/size][size=16px]相比,3[/size][size=16px]-BHA[/size][size=16px]的抗氧化性随着异丁基对酚羟基位置更远,自由基抗氧化作用也随之强化,增强的倍数大致在1[/size][size=16px].5~2[/size][size=16px]倍之间。同时,二者混用可以增强抗氧化性能。对食品来说,用量控制在0[/size][size=16px].02%[/size][size=16px]比控制在0[/size][size=16px].01%[/size][size=16px]抗氧化效果增强1[/size][size=16px]0[/size][size=16px]倍。但是用量增加超过0[/size][size=16px].02%[/size][size=16px]后抗氧化效果反而会下降。[[/size][size=16px]3][/size][size=18px]2[/size][size=18px]. [/size][size=18px]国家标准[/size][size=16px]根据我国《食品添加剂使用卫生标准》(GB2760-1996)中规定:二丁基羟基甲苯可用于食用油脂、油炸食品、干鱼制品、饼干、方便面、速煮米、果仁罐头、腌腊肉制品、早餐谷类食品,最大食用量为0.2g/kg。BHT与BHA混合使用时,总量不得超过0.2g/kg;BHT和BHA与PG(没食子酸丙酯,[/size][size=16px]P[/size][size=16px]roply [/size][size=16px]G[/size][size=16px]allate)混合使用时,BHA、BHT(2,6-二丁基羟基甲苯)总量不得超过0.1g/kg,PG不得超过0.05g/kg。最大使用量以脂肪计。此外,也可用于胶姆糖配料。[/size][size=18px]3. [/size][size=18px]应用范围[/size][size=16px] [/size][size=16px]丁基羟基茴香醚作为脂溶性抗氧化剂,适宜油脂食品和富脂食品。由于其热稳定性好,因此可以在油煎或焙烤条件下使用。另外丁基羟基茴香醚对动物性脂肪的抗氧化作用较强,而对不饱和植物脂肪的抗氧化作用较差。丁基羟基茴香醚可稳定生牛肉的色素和抑制酯类化合物的氧化。[/size][size=16px]丁基羟基茴香醚与三聚磷酸钠和抗坏血酸结合使用可延缓冷冻猪排腐败变质。丁基羟基茴香醚可稍延长喷雾干燥的全脂奶粉的货架期、提高奶酪的保质期。丁基羟基茴香醚能稳定辣椒和辣椒粉的颜色,防止核桃、花生等食物的氧化。将丁基羟基茴香醚加入焙烤用油和盐中,可以保持焙烤食品和咸味花生的香味。延长焙烤食品的货架期。丁基羟基茴香醚可与其他脂溶性抗氧化剂混合使用,其效果更好。如丁基羟基茴香醚和二丁基羟基甲苯配合使用可保护鲤鱼、鸡肉、猪排和冷冻熏猪肉片。丁基羟基茴香醚或二丁基羟基甲苯、没食子酸丙酯和柠檬酸的混合物加入到用于制作糖果的黄油中,可抑制糖果氧化。[[/size][size=16px]3][/size][size=16px] [/size][size=16px] [/size][size=16px]丁基羟基茴香醚一直作为常用抗氧化剂使用是因为相比于其他抗氧化剂,它具有自己的优势。它不像没食子酸丙酯会与金属离子配合,不想二丁基羟基甲苯一样不溶于丙二醇。同时,丁基羟基茴香醚除了抗氧化作用还有很强的抗菌力,用质量分数为0[/size][size=16px].015%[/size][size=16px]的丁基羟基茴香醚即可一直金黄色葡萄球均,用量达到0[/size][size=16px].028%[/size][size=16px]即可阻止寄生曲霉孢子生长,进而阻碍黄曲霉素的生成。[/size][size=16px]BHA对动物脂肪的抗氧化作用较强,对不饱和的植物油的抗氧化性较弱。BHA可以在油煎或烘烤的温度下使用,并在此过程中随油进入食品,从而对食品起到抗氧化作用。BHA具有一定的熏蒸性,因此它可以通过加到食品包装中而对食品起抗氧化作用。BHA可单独使用,也可与其他抗氧化剂共同使用。单独用于起酥油,其效果不如BHT、TBHQ,但在乳剂中效果比BHT好。[/size][size=21px]二、丁基羟基茴香醚的合成与作用机理[/size][size=18px]1. [/size][size=18px]丁基羟基茴香醚的合成[/size][size=16px]丁基羟基茴香醚的合成主要来自于苯的对二取代物。[/size][size=16px](1)对苯二酚路线[/size][size=16px]用对苯二酚和叔丁醇,以磷酸为催化剂,在101℃下反应,制的中问体叔丁基对苯二酚,然后再以叔丁基对苯二酚与硫酸二甲酯在氮气氛中,加热回流反应18小时,冷却后用苯提取,苯提取液用热水洗涤,蒸除苯后,得粗品,减压蒸馏,得丁基羟基茴香醚。[/size][size=16px](2)对氯苯酚路线[/size][size=16px]以对氯苯酚为原料,将其与异丁烯混合,在磷酸存在的条件下反应。得到产品为[/size][size=16px]2,4[/size][size=16px],6[/size][size=16px]-C[/size][size=16px]l(Me[/size][font='times new roman'][size=16px]3[/size][/font][size=16px]C[/size][size=16px])[/size][font='times new roman'][size=16px]2[/size][/font][size=16px]C[/size][font='times new roman'][size=16px]6[/size][/font][size=16px]H[/size][font='times new roman'][size=16px]3[/size][/font][size=16px]OH和[/size][size=16px]2[/size][size=16px],[/size][size=16px]4-C[/size][size=16px]l(Me[/size][font='times new roman'][size=16px]3[/size][/font][size=16px]C[/size][size=16px])C[/size][font='times new roman'][size=16px]6[/size][/font][size=16px]H[/size][font='times new roman'][size=16px]3[/size][/font][size=16px]OH的混合物,前者与甲醇钠在甲醇溶液中发生Williamson反应,即得产品3-BHA。[/size][size=16px](3)对甲氧基苯酚路线[/size][size=16px]对甲氧基苯酚的合成关键在于叔丁基与苯环的结合,因此缩合催化剂的选择最重要,比较早前的工艺中使用质子酸作为催化剂,如浓硫酸、磷酸、氢氟酸等,但反应条件较为苛刻,而且需要较高的温度。据日本专利报道以离子交换树脂为催化剂,反应温度65~75℃,总产率可达到68.5%,其中3-BHA的含量为51.8%,所得产品中3-BHA为90%。据另一日本专利报道,3-BHA的含量高达82.3%,对甲氧基苯酚的转化率为87%,这是一般无机酸催化剂所不能达到的。[/size][size=16px](4)对氨基苯甲醚路线[/size][size=16px]先合成对羟基苯甲醚即对甲氧基苯酚,然后再通过烷基化反应,制备BHA。具体工艺如下:在冰浴搅拌下,加入对氨基苯甲醚和亚硝酸钠(摩尔比1[/size][size=16px]:[/size][size=16px]1[/size][size=16px].[/size][size=16px]15),在硫酸存在下进行重氮化反应,反应完成后保温过滤,将滤液滴加于热的水解反应液中水解,生成对羟基苯甲醚。然后即可用蒸汽提馏出来,冷凝下来的对羟基苯甲醚溶液用有机溶剂进行萃取,经浓缩蒸馏除去溶剂,可得对羟基苯甲醚,平均收率为84.7%。[/size][size=16px](5)对羟基苯甲醚路线[/size][size=16px]将对羟基苯甲醚、叔丁醇和溶剂加热溶解,再将此混合试剂加入到事先预热好的催化剂中,在混合良好的反应器中进行反应,15min后反应完毕。取样用高效液相色谱测定未反应的叔丁醇,当取样化验结果合格,反应即可停止。静置分层,收集有机物,然后采用蒸馏的方法除去有机溶剂,在经高真空减压蒸馏,得BHA产品,收率为77.8%。[[/size][size=16px]3][/size][size=18px]2[/size][size=18px]. [/size][size=18px]丁基羟基茴香醚的抗氧化机理[/size][size=16px]天然油脂暴露在空气中会自发地发生氧化反应,生成低级脂肪酸、醛、酮等, 产生恶劣的酸臭和口味变坏等,是油脂及含油食品败坏变质的主要原因。油脂的自动氧化遵循自由基反应机制,首先脂肪分子被热、光或金属离子等自由基引发剂活化后,分解成不稳定的自由基R[/size][size=16px]和H[/size] [size=16px]。当有分子氧存在时,自由基与O[/size][font='times new roman'][size=16px]2[/size][/font][size=16px]反应生成过氧化物自由基,此过氧化物自由基又和脂肪分子反应,生成氢过氧化物和自由基R[/size][size=12px] [/size][size=16px],通过自由基R[/size][size=16px]的链式反应又再传递下去,直到自由基和自由基或自由基和自由基失活剂相结合,产生稳定化合物时,反应才结束。此过程中产生许多短链羰基化合物, 如醛、酮、羧酸等,是产生酸败和劣味的主要物质, 而大量过氧化物的存在,对人体也会产生不良结果。[[/size][size=16px]4][/size][size=16px]丁基羟基茴香醚除了可以与自由基发生反应,还可以螯合金属离子(如铜离子和铁离子)进而延缓脂肪氧化,使肉制品具有稳定的货架期。[[/size][size=16px]5][/size][size=16px] [/size][size=16px] [/size][size=21px]三、毒性研究[/size][size=16px]对食品安全的影响一般认为BHA毒性很小,较为安全。根据以上文献,我们发现丁基羟基茴香醚虽然被分为2[/size][size=16px]B[/size][size=16px]类致癌物,对人体致癌证据尚不完全,但从自由基机理我们不难怀疑当大量使用时,作为自由基链式反应的转移终止中间体,可能会延长自由基寿命。在人体以外的动物实验中,丁基羟基茴香醚同样表现出了各种各样的毒性,这样的毒性不仅会影响农渔业生产,其自由基反应的难代谢产物同样会因为富集作用对人类健康产生影响。[/size][size=16px]比如,对小鼠(雄)经口LD50为1.1g/kg,对大鼠经口LD50为2.09/kg。日本于1981年用含2%BHA料喂大白鼠两年,发现其前胃发生扁平上皮癌,故自1982年5月限令只准用于棕榈油和棕榈仁油中,其他食品禁用。[[/size][size=16px]3][/size][size=16px]故以下将丁基羟基茴香醚对动植物毒性影响的文献稍作整理:[/size][size=18px]1[/size][size=18px]. [/size][size=18px]丁基羟基茴香醚对剑尾鱼的毒性[/size][size=16px]BHA试验分别设置5个间隔较大的浓度梯度和空白对照组。试验在1L的烧杯中进行, 内盛800 mL试验液, 每个浓度设3个平行, 每只烧杯中放4尾鱼, 雌、雄鱼各2条。实验开始后第0、24、48、72、96 h时观察并记录各容器实验鱼的存活情况。[/size][size=16px]结果,BHA在预试验中96 h内使剑尾鱼100[/size][size=16px] [/size][size=16px]%死亡的浓度为5 mgL[/size][font='times new roman'][size=16px]-1[/size][/font][size=16px],因此, BHA属于高毒, 对剑尾鱼产生急性毒性。[[/size][size=16px]6][/size][size=18px]2[/size][size=18px]. [/size][size=18px]大口黑鲈对丁基羟基茴香醚的耐受性评价[/size][size=16px]本试验依据农业部《饲料原料和饲料添加剂水产靶动物耐受性评价试验指南( 试行) 》进行。在大口黑鲈的基础饲料中分别添加0、150、300、1 500 mg / kg的BHA ,其中150 mg / kg为最高推荐添加剂量,而300和1500 mg /kg分别是它的2和10倍,制成4种直径为2[/size][size=16px].[/size][size=16px]0 m[/size][size=16px]m[/size][size=16px]的硬颗粒料,自然晾干后备用。本试验设计4个组,对应饲喂4种试验饲料,每组6个重复(桶),每桶30尾鱼。试验鱼每天表观饱食投喂2 次,投喂时间分别为08: 00和16: 00。定期检测水质,水质条件保持在溶氧(DO)浓度 7. 0 mg /L,氨氮( NH[/size][font='times new roman'][size=16px]4+[/size][/font][size=16px]-N ) 浓度 0. 3 mg /L,pH 7[/size][size=16px].[/size][size=16px]5 ~ 8.5,水温(23±1)℃ 。养殖试验从2014年7月15日到2014年9月23日,共70 天。[/size][size=16px]抗氧化测试通过试剂盒进行,按照说明书测定血浆及各组织中抗氧化指标,所用试剂盒均购自南京建成生物工程研究所。桶随机取5 尾鱼,采血制备血浆并取肝脏、心脏和肌肉,放在-80℃待测。[/size][size=16px]结果表面,饲料中添加150 mg /kg的BHA对大口黑鲈具有一定的脂肪代谢促进作用和抗氧化保护功能,且对大口黑鲈是安全的,安全系数为10 倍。同时,本试验中D1500 组血浆中GSH-Px活性最高,可能原因是高剂量的BHA对GSH具有显著诱导作用,促进GSH-Px与底物GSH和H2O2反应生成水和氧化型谷胱甘肽( GSSG) 。[[/size][size=16px]7][/size][size=18px]3[/size][size=18px]. [/size][size=18px]对各种生物的LD50(半数致死量)[/size][size=16px]小鼠口服1100mg/kg(bw)(雄性),小鼠口服1300mg/kg(bw)(雌性);大鼠口服2000mg/kg(bw),大鼠腹腔注射200mg/kg(bw);兔口服2100mg/kg(bw)。[/size][size=21px]四、丁基羟基茴香醚的检测[/size][size=16px]丁基羟基茴香醚([/size][size=16px]BHA[/size][size=16px])一般同时与同属于抗氧化剂,并且经常混合使用的2,6-二叔丁基对甲酚(N[/size][size=16px]HT[/size][size=16px])和特丁基对苯二酚(T[/size][size=16px]BHQ[/size][size=16px])同时测定。目前已经建立起了测定食品中抗氧化剂叔丁基羟基茴香醚 (BHA),2, 6-二叔丁基对甲酚 (BHT) 和特丁基对苯二酚 (TBHQ)的液相色谱法和[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法。[/size][size=16px]而随着国家近几十年对食品安全越来越重视,对丁基羟基茴香醚等一系列食品抗氧化剂的检测都提出了明确而合理的检测手段。国家标准从[/size][size=16px]GB/T 23373-2009[/size][size=16px]更新到了[/size][size=16px]GB 5009.32-2016[/size][size=16px]。说明随着技术手段的发展,高效液相[/size][size=16px]/[/size][size=16px]气象色谱的普及,国家标准同样也在更新。同时,在学术领域,对丁基羟基茴香醚的测定同样也在不断进行深化探究。[/size][size=18px]1[/size][size=18px]. [/size][size=18px]方法一[/size][size=16px]方法先用石油醚提取食品中的油脂, 油脂中抗氧化剂用13ml甲醇提取后, 离心, 重复两次, 合并提取液, 旋蒸浓缩到5ml, 定容至10ml, 冷冻1h,上清液分别注入到条件优化好的液相色谱和[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]中进行色谱分析。结果液相测定BHA、BHT和TBHQ的定量下限分别为0.002、0.010和0.002 g/kg,[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]测定BHA的定量下限分别为0.003、0.002和0.005g/kg, 两个方法的加标回收率为82.8%~109.0%。两种仪器分析方法结果比对差异无显著性。结论所建立的前处理方法简单、可操作性强, 两种仪器方法的比对结果一致。[[/size][size=16px]8][/size][size=18px]2. [/size][size=18px]方法二[/size][size=16px]样品前处理称取2 g(精确至0.01g)油样或提取的脂肪置于离心管中, 加入10 mL甲醇, 在旋涡混合器上振荡提取1min,5000 r/mi[/size][size=16px]n[/size][size=16px]离心3 min, 吸取甲醇层置于第二支离心管中, 如上操作分别用5.0 mL提取两次, 合并甲醇层置于第二支离心管中, 混匀后, 置于-18℃冷冻半小时, 取出后立刻过0.45[/size][size=16px] [/size][size=16px]μm[/size][size=16px]有机相滤膜, 滤液待上机测定。[[/size][size=16px]9][/size][size=18px]3[/size][size=18px]. [/size][size=18px]方法三(P[/size][size=18px]SE-HPLC[/size][size=18px])[/size][size=16px]该方法采用正交试验对影响PSE萃取效率的温度、压力、萃取溶剂、萃取时间进行优化,联合HPLC进行测定,并确定分别以BHA提取量、BHT提取量以及总量为评价指标的最优条件。结果:PSE-HPLC法测定BHT和BHA的相对标准偏差(RSD)为0.5%~3.1%,并且在1.0~200.0[/size][size=16px] [/size][size=16px]μg/mL[/size][size=16px]范围内色谱峰面积与组分质量浓度均有很好的线性相关性(r≥0.9997),检出限为0.05[/size][size=16px] [/size][size=16px]μ[/size][size=16px]g/mL,在最优条件下的回收率为92.60%~97.80%。结论:PSE-HPLC法简便、快速、效率高,方法的重现性、线性相关性以及检出限理想,适用于食品中BHT和BHA含量及两者总量的同时快速检测。[[/size][size=16px]10][/size][size=18px]4[/size][size=18px]. [/size][size=18px]加压毛细管电色谱法[/size][size=16px]称取25 mg丁基羟基茴香醚,移入25mL棕色容量瓶中,以乙腈定容至刻度,制成1mg/m L的标准贮备液,低温保存。用乙腈溶液将上述标准储备液逐级稀释为2、5、10、50、100、200μg/m L的系列标准混合溶液,置于冰箱保存备用。准确称取大豆油5[/size][size=16px] [/size][size=16px]g(精确至0.001[/size][size=16px] [/size][size=16px]g),置于具塞离心管中,加入8[/size][size=16px] [/size][size=16px]mL甲醇,漩涡混合3[/size][size=16px] [/size][size=16px]min,静置2[/size][size=16px] [/size][size=16px]min,以3000[/size][size=16px] [/size][size=16px]r/min离心5[/size][size=16px] [/size][size=16px]min,用微量[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液器[/color][/url][/color][/url]取出上清液,残余物每次用8[/size][size=16px] [/size][size=16px]mL甲醇提取2次,合并上清液与甲醇提取液,用氮吹仪于50[/size][size=16px] [/size][size=16px]℃下浓缩至近干,以适量甲醇溶解并定容至5[/size][size=16px] [/size][size=16px]mL容量瓶。[/size][size=16px]加压毛细管电色谱分离体系中需要添加可导电的酸、碱或者缓冲盐溶液,以保证施加电压后形成稳定的电场及电渗流,实验中分别考察了三氟乙酸、甲酸以及醋酸铵改性剂等对分离的影响。结果表明,三氟乙酸以及醋酸铵缓冲溶液体系下,色谱峰的响应值变低,且加电后的电流值过高,容易引起焦耳热效应,造成基线噪声较大 而添加甲酸后,可有效改善色谱峰形,减少拖尾,在施加电场后,电流稳定,基线平稳。同时注意到,添加过量的甲酸会造成流动相体系的pH过低,不利于电渗产生,所以本实验最终选择甲酸的浓度为0.05%。[/size][size=16px]以加压毛细管电色谱法(pCEC)为平台,在8[/size][size=16px] [/size][size=16px]min内可以完成4种抗氧化剂的同时测定。该方法简单快速,准确可靠,借助pCEC电渗流和压力流的双重推动力,能将丁基羟基茴香醚中的杂质与主成分分开,提高了分析速度和分离效能。pCEC作为一种微分离技术,实际分析流速只在微升级甚至纳升级,且样品用量只有几纳升,大大节省了检测成本,具有实用推广价值。[/size][size=21px]*参考文献:[/size][size=16px][1][/size][size=16px]世界卫生组织国际癌症研究机构致癌物清单, 2B类致癌物, 2017[/size][size=16px][2][/size][size=16px]李毅民,胡燕平,李彦红.叔丁基-4-羟基茴香醚致突变性研究[J].癌变.畸变.突变,2000(01):34-36.[/size][size=16px][3][/size][size=16px]周家华,崔英德,曾颢等编著.食品添加剂 (第二版):化学工业出版社,2008:55-57[/size][size=16px][4][/size][size=16px]李银聪,阚建全,柳中.食品抗氧化剂作用机理及天然抗氧化剂[J].中国食物与营养,2011,17(02):24-26.[/size][size=16px][5][/size][size=16px]刘立群,喻倩倩,刘毅,戴瑞彤.天然抗氧化剂作用机理及在肉类制品中的应用研究进展[J].肉类研究,2017,31(06):45-50.[/size][size=16px][6][/size][size=16px]梁惜梅,鹿金雁,聂湘平,王翔,李凯彬.饲料添加剂叔丁基对羟基茴香醚和抗生素诺氟沙星对剑尾鱼的毒性效应[J].环境科学学报,2010,30(01):172-179.[/size][size=16px][7][/size][size=16px]于利莉,薛敏,王嘉,韩芳,郑银桦,吴秀峰,吴立新.大口黑鲈对饲料中丁基羟基茴香醚的耐受性评价[J].动物营养学报,2016,28(03):747-758.[/size][size=16px][8][/size][size=16px]杨杰,方从容,杨大进.液相色谱法和[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定食品中抗氧化剂叔丁基羟基茴香醚、2,6-二叔丁基对甲酚和特丁基对苯二酚的研究和比对[J].卫生研究,2013,42(01):114-118.[/size][size=16px][9][/size][size=16px]陈秀明,林海丹,梁小茹.食品中叔丁基羟基茴香醚(BHA)与2,6-二叔丁基对甲酚(BHT)的测定[J].现代测量与实验室管理,2012,20(01):16-18.[/size][size=16px][10][/size][size=16px]林太凤,刘阳,王慧琴,郑大威,罗云敬,张淑芬.PSE-HPLC法测定食品中叔丁基羟基茴香醚和2,6-二叔丁基羟基甲苯[J].食品科学,2010,31(14):254-257.[/size][size=16px][11][/size][size=16px]王晓曦,王彦,李静,茹鑫,闫超.加压毛细管电色谱法同时测定植物油中4种抗氧化剂[J].食品工业科技,2015,36(09):273-277.[/size]
需要辉瑞的伏立康唑原料标准,英文的也可以,谢谢

联合用药血浆样品中抗真菌药物的快速同时测定 真菌感染是临床上表现严重的而且难攻可的难题,而且发病率高可导致死亡。抗真菌药伏立康唑,泊沙康唑,伊曲康唑以其广谱抗菌性是临床上被广泛地用于抗真菌感染的三唑类抗真菌药。伊曲康唑的主要代谢产物羟基伊曲康唑的抗菌活性与伊曲康唑相媲美,三唑类抗真菌药的药理和毒理与其药物浓度存在浓度-效应关系。它们在血液中的浓度以及吸收、代谢、消除以及合并用药均存在差异。所以对这些药物的临床药物监测对于增强临床效果降低毒副作用有很重要的意义。三唑类抗真菌药的临床检测需要快速简便的分析手段来分析血浆中的血药浓度,同时测定人体血浆中伏立康唑,泊沙康唑,伊曲康唑的分析方法多采用液相色谱 - 质谱(LC-MS)或LC-串联质谱法(LC-MS / MS)的方法,LC-MS/MS是近年来用于生物样品中药物定量测定的有力手段,然而,LC-MS/MS系统由于其昂贵价格导致普及性并不高,本实验开发了一种简单、快速、可靠而且普适性的高效液相色谱同时测定伏立康唑,泊沙康唑,伊曲康唑以及代谢产物羟基伊曲康唑的方法,适合普遍的临床及实验室。高效液相色谱法通常需要复杂的样品前处理,如液-液萃取、固液-萃取、以及血浆的处理,这些过程不仅需要试剂更耗时严重,本实验中对方法进行了简化,一步除蛋白,样品离心后可直接上样。材料和方法:伏立康唑,泊沙康唑、伊曲康唑、羟基伊曲康唑标准品及药品,萘普生标准品,甲醇、乙腈(色谱纯)、实验室自制试验用水。色谱条件:安捷伦1200,安捷伦 SB-Phenyl色谱柱(150mm×4.6mm×5μm),检测波长260nm,流动相A 0.01M的磷酸盐缓冲液(pH3.5)流动相B(95%乙腈的水溶液),梯度洗脱情况如下:http://ng1.17img.cn/bbsfiles/images/2014/10/201410281127_520414_2206101_3.jpg标准储备溶液配制:伏立康唑和泊沙康唑均配置成1.0mg/ml(以游离碱计)的甲醇溶液,伊曲康唑制备成0.4mg/ml的甲醇溶液,羟基伊曲康唑配制成0.1mg/ml的甲醇溶液,内标溶液为0.6mg/ml萘普生甲醇溶液,皆4度保存备用。标准曲线::伏立康唑、泊沙康唑、伊曲康唑、羟基伊曲康唑标准曲线绘制通过向空白血清中加入标准溶液来获得,浓度范围0.05-100mg/L。样品制备:取100ul 10ug/ml的内标普萘生溶液分别加入100ul的空白、标准溶液、以及样品血浆中。混匀,加入25ul的1.0M的高氯酸是样品酸化,加入400ul的甲醇使蛋白质沉淀析出,离心2000转/min(5min),取上清液30ul进样。结果与讨论1、本实验建立了一种高效液相色谱法同时快速检测人体血浆中伏立康唑、泊沙康唑、伊曲康唑以及伊曲康唑的代谢产物羟基伊曲康唑。2、方法中使用了1.0M的高氯酸和甲醇作为蛋白质沉淀的方法,简单、快速。经过离心后,上层离心液经0.45um滤膜过滤后直接进样分析。3、为了达到最佳的分离效果,我们比较了各种色谱柱,流动相我们对0.01M的磷酸盐缓冲液和不同浓度的甲醇、乙腈进行比较,得到优化的色谱条件:Phenyl色谱柱(150mm×4.6mm,5μm)上使用0.01M的磷酸盐缓冲液(pH3.5)、乙腈流动相梯度洗脱,波长260nm下进行检测。在该条件下:伏立康唑、萘普生、泊沙康唑、羟基伊曲康唑、伊曲康唑的保留时间及色谱图如下:http://ng1.17img.cn/bbsfiles/images/2014/10/201410281128_520415_2206101_3.jpghttp://ng1.17img.cn/bbsfiles/images/2014/10/201410281128_520416_2206101_3.jpg4、标准曲线在0.05-10mg/L范围内线性良好(r2=0.99,浓度范围0.05-10mg/L),日内和日间变化系数10%。5 为了找到最简便快速的沉淀方法,对于沉淀剂进行了选择优化(甲醇乙腈高氯酸等),用乙腈和高氯酸沉淀效果皆很好,但综合考虑回收率高氯酸最优。
对羟基苯甲酸甲酯,又叫尼泊金甲酯,白色结晶粉末或无色结晶,易溶于醇,醚和丙酮,极微溶于水,沸点270-280℃。主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂。 由于它具有酚羟基结构,所以抗细菌性能比苯甲酸、山梨酸都强。其作用机制是:破坏微生物的细胞膜,使细胞内的蛋白质变性,并可抑制微生物细胞的呼吸酶系与电子传递酶系的活性。它属酚类防腐剂,对各种霉菌、酵母菌、细菌有效,但尼泊金酯的杀菌力低,通常与尼泊金乙酯混合使用,具有良好的加成性和协同性。添加量0.1%~1.0%。防腐活性与溶液ph值有关,当ph值为7时,其活性为原有活性的2/3;如ph值为8.5,则降低为原有活性的一半。会被一些高分子化合物如甲基纤维素、明胶蛋白质等束缚而使其失去防腐活性。在《化妆品卫生规范》(2007版)里面对其限制使用,要求不得高于0.4%,检测方法为用甲醇提取样品以后,用液相色谱法检测。