[size=20px][color=#93c6bc][b]鉴别[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体](1)本品叶表面观:叶上表皮细胞多角形,细胞壁连珠状增厚;叶下表皮细胞多角形,垂周壁波状弯曲,略呈连珠状增厚,气孔平轴式或[color=var(--weui-LINK)]不定式[i][/i][/color]。黑色腺点由一团分泌细胞组成,细胞内容物红色;半透明腺点为分泌囊结构,由1层上皮细胞包围圆形腔隙构成,内含油状物。[/font] [font=宋体](2)取本品粉末0.1g,加甲醇10ml,超声处理10分钟,滤过,滤液蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。另取贯叶金丝桃对照药材0.1g,同法制成对照药材溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各2[/font][font=宋体]μ[/font][font=宋体]l[/font][font=宋体],分别点于同一硅胶G薄层板上,以乙酸乙酯-甲酸(25:1)为展开剂,展开,取出,立即置紫外光灯(365nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点。[/font] [font=宋体](3)取[color=var(--weui-LINK)]金丝桃苷[i][/i][/color]对照品、芦丁对照品,分别加甲醇制成每1ml各含0.5mg的溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取〔鉴别〕(2)项下的供试品溶液和上述对照品溶液各2[/font][font=宋体]μ[/font][font=宋体]l[/font][font=宋体],分别点于同一硅胶G薄层板上,以乙酸乙酯-甲酸-水(8:1:1)为展开剂,展开,取出,晾干,喷以5%三氯化铝乙醇溶液,置紫外光灯(365nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点。[/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [size=20px][color=#93c6bc][b]检查[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [font=宋体][/font] [font=宋体][/font] [b][font=宋体][/font][/b] [font=宋体][/font] [font=宋体][/font] [font=宋体][b]水分[/b] 不得过12.0%(通则0832第二法)。[/font] [b][font=宋体]【含量测定】[/font][/b][font=宋体] 照高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法(通则0512)测定。[/font] [b][font=宋体]色谱条件与系统适用性试验[/font][/b][font=宋体] [/font][font=宋体]以[color=var(--weui-LINK)]十八烷基硅烷键合硅胶[i][/i][/color]为填充剂;以乙腈-0.1%磷酸溶液(16:84)为[color=var(--weui-LINK)]流动相[i][/i][/color];检测波长为360nm。理论板数按金丝桃苷峰计算应不低于3000。[/font] [b][font=宋体]对照品溶液的制备[/font][/b][font=宋体] [/font][font=宋体]取金丝桃苷对照品适量,精密称定,加甲醇制成每1ml含32[/font][font=宋体]μ[/font][font=宋体]g[/font][font=宋体]的溶液,即得。[/font] [b][font=宋体]供试品溶液的制备[/font][/b][font=宋体] [/font][font=宋体]取本品粉末(过三号筛)约0.4g,精密称定,置具塞锥形瓶中,精密加入60%乙醇50ml,称定重量,加热回流1小时,放冷,再称定重量,用60%乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。[/font] [b][font=宋体]测定法[/font][/b][font=宋体] [/font][font=宋体]分别精密吸取对照品溶液与供试品溶液各10[/font][font=宋体]μ[/font][font=宋体]l[/font][font=宋体],注入[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url],测定,即得。[/font] [font=宋体]本品按干燥品计算,含金丝桃苷(C[sub]21[/sub]H[sub]20[/sub]O[sub]12[/sub])不得少于0.10%。 [/font] [font=宋体] [/font]
[b][font='Times New Roman']1[/font][font=宋体]溶液的制备[/font][/b][align=left][b][font=宋体]对照品溶液的制备[/font][font='Times New Roman'] [/font][/b][/align][align=left][font=宋体]精密称取芦丁对照品[/font][font='Times New Roman']12.75mg[/font][font=宋体],置于[/font][font='Times New Roman']50mL[/font][font=宋体]量瓶中,加[/font][font='Times New Roman']80%[/font][font=宋体]乙醇超声溶解,并稀释至刻度,摇匀,即得浓度为[/font][font='Times New Roman']255.0 [/font][font=Symbol]m[/font][font='Times New Roman']g[/font][font='Times New Roman']/mL[/font][font=宋体]的芦丁对照品贮备溶液。精密吸取[/font][font='Times New Roman']2.5mL[/font][font=宋体]芦丁对照品贮备溶液,置于[/font][font='Times New Roman']50mL[/font][font=宋体]量瓶中,加[/font][font='Times New Roman']80%[/font][font=宋体]乙醇稀释至刻度,摇匀,即得浓度为[/font][font='Times New Roman']12.75 [/font][font=Symbol]m[/font][font='Times New Roman']g[/font][font='Times New Roman']/mL[/font][font=宋体]的芦丁对照品溶液。[/font][/align][align=left][b][font=宋体]供试品溶液的制备[/font][/b][font='Times New Roman'] [/font][/align][align=left][font=宋体]取贯叶金丝桃药材,粉碎,过三号筛。精密称取贯叶金丝桃药材粉末[/font][font='Times New Roman']25mg[/font][font=宋体],置于[/font][font='Times New Roman']10mL[/font][font=宋体]量瓶中,加[/font][font='Times New Roman']80%[/font][font=宋体]乙醇适量([/font][font='Times New Roman']5mL[/font][font=宋体]),超声提取[/font][font='Times New Roman']1h[/font][font=宋体],放冷,[/font][font='Times New Roman']80%[/font][font=宋体]乙醇稀释至刻度,摇匀,[/font][font='Times New Roman']0.45 [/font][font=Symbol]m[/font][font='Times New Roman']m[/font][font=宋体]微孔滤膜滤过,取续滤液,即得药材供试品溶液。[/font][/align][align=left][font=宋体]称取贯叶连翘提取物粉末[/font][font='Times New Roman']5mg[/font][font=宋体]于[/font][font='Times New Roman']10mL[/font][font=宋体]量瓶中,加[/font][font='Times New Roman']80%[/font][font=宋体]乙醇适量([/font][font='Times New Roman']5mL[/font][font=宋体]),超声溶解,用[/font][font='Times New Roman']80%[/font][font=宋体]乙醇稀释至刻线,摇匀,静置。[/font][font='Times New Roman']0.45 [/font][font=Symbol]m[/font][font='Times New Roman']m[/font][font=宋体]微孔滤膜滤过,取续滤液,即得提取物供试品溶液。[/font][/align][b][font='Times New Roman']2 [/font][font=宋体]显色方法选择[/font][/b][align=left][font=宋体]对黄酮类物质的含量测定多采用紫外[/font][font='Times New Roman']-[/font][font=宋体]可见分光光度法,常用芦丁为对照品,经[/font][font='Times New Roman']NaNO[sub]2[/sub]- A1(NO) [sub]3[/sub]-NaOH[/font][font=宋体]显色后用比色法测定,也有用[/font][font='Times New Roman']AlCl[sub]3[/sub]-[/font][font=宋体]醋酸缓冲液[/font][font='Times New Roman'](pH4.5)[/font][font=宋体]显色测定的。本研究分别从方法的稳定性、准确性方面比较了两种测定方法,结果显示亚硝酸钠法测定值偏高,考虑到贯叶金丝桃药材中含有鞣质、绿原酸、咖啡酸等具有邻二酚羟基结构的非黄酮类成分物质,会发生假阳性反应,因此选择三氯化铝显色法。[/font][/align][b][font='Times New Roman']3 [/font][font=宋体]含量测定方法[/font][/b][align=left][font=宋体]分别精密量取供试品溶液及对照品溶液各[/font][font='Times New Roman']1.5 mL[/font][font=宋体],置于[/font][font='Times New Roman']10mL[/font][font=宋体]量瓶中,各精密加[/font][font='Times New Roman']0.1mol/L[/font][font=宋体]三氯化铝溶液[/font][font='Times New Roman']1.0mL[/font][font=宋体],使混匀,再分别加入[/font][font='Times New Roman']80%[/font][font=宋体]乙醇稀释至刻度,摇匀,室温放置[/font][font='Times New Roman']20min[/font][font=宋体],以试剂为空白,按紫外[/font][font='Times New Roman']-[/font][font=宋体]可见分光光度法规定进行检查,在[/font][font='Times New Roman']410nm[/font][font=宋体]波长处测定吸收度,以标准曲线法计算,即得。[/font][/align][align=left][font=宋体][b][font='Times New Roman']4 [/font][font=宋体]含量测定[/font][/b][font=宋体]制备含量测定药材供试品溶液。按含量测定方法项下操作,在[/font][font='Times New Roman']410 nm[/font][font=宋体]波长处测定吸收度值,采用标准曲线法按质量百分比计算样品中黄酮类成分的含量,结果见表[/font][font='Times New Roman']1[/font][font=宋体]。[/font][font=宋体]由表[/font][font='Times New Roman']1[/font][font=宋体]可知,[/font][font='Times New Roman']10[/font][font=宋体]批不同产地的贯叶金丝桃药材中黄酮类成分的含量测定结果范围为[/font][font='Times New Roman']2.91%[/font][font=Symbol]~[/font][font='Times New Roman']4.17 %[/font][font=宋体]。[/font][/font][/align][align=center][b][font='Times New Roman']Tab. 1Contents of [/font][font='Times New Roman']flavonoids[/font][font='Times New Roman'] in [/font][i][font='Times New Roman']Hypericumperforatum [/font][/i][font='Times New Roman']fromdifferent sources[/font][/b][/align] [table][tr][td] [align=center][font='Times New Roman'][color=black]No.[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]Sources[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]Contents[/color][/font][font=宋体][color=black]([/color][/font][font='Times New Roman'][color=black]%[/color][/font][font=宋体][color=black])[/color][/font][/align] [/td][/tr][tr][td] [align=center][font='Times New Roman'][color=black]S1[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]Sichuan[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]3.33[/color][/font][/align] [/td][/tr][tr][td] [align=center][font='Times New Roman'][color=black]S2[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]Sichuan[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]2.98[/color][/font][/align] [/td][/tr][tr][td] [align=center][font='Times New Roman'][color=black]S3[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]Gansu[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]3.2[/color][/font][/align] [/td][/tr][tr][td] [align=center][font='Times New Roman'][color=black]S4[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]Gansu[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]3.47[/color][/font][/align] [/td][/tr][tr][td] [align=center][font='Times New Roman'][color=black]S5[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]Jiangsu[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]2.91[/color][/font][/align] [/td][/tr][tr][td] [align=center][font='Times New Roman'][color=black]S6[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]Jiangsu[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]3.54[/color][/font][/align] [/td][/tr][tr][td] [align=center][font='Times New Roman'][color=black]S7[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]Jiangsu[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]3.42[/color][/font][/align] [/td][/tr][tr][td] [align=center][font='Times New Roman'][color=black]S8[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]Jiangsu[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]3.01[/color][/font][/align] [/td][/tr][tr][td] [align=center][font='Times New Roman'][color=black]S9[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]Shanxi[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]2.95[/color][/font][/align] [/td][/tr][tr][td] [align=center][font='Times New Roman'][color=black]S10[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]Shanxi[/color][/font][/align] [/td][td] [align=center][font='Times New Roman'][color=black]4.17[/color][/font][/align] [/td][/tr][/table]
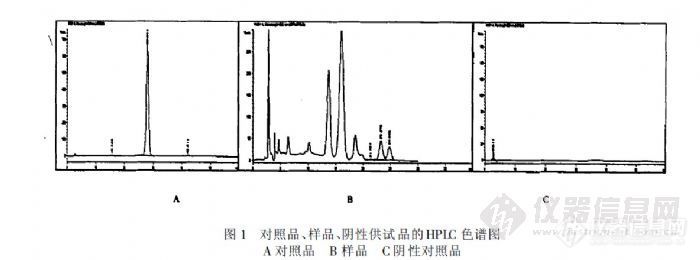
在薄层色谱定性时,对照品、供试品和对照药材在相同的问题显相同颜色的斑点即可。对照品和对照药材定性有何区别?为什么两个要同时做呢?
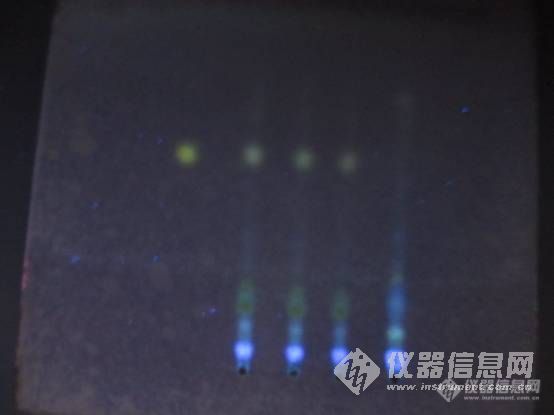
研究中药复方制剂中各味药材的鉴别药典中鉴别乌梅药材,选择“熊果酸”为对照乌梅含有熊果酸,大枣也含有熊果酸,请问那我做制剂中乌梅药材鉴别时,是不是就不能以熊果酸作对照了,因为怕大枣会有干扰?这种情况,乌梅该选择什么组分作为对照?实验结果显示,乌梅阴性并没有干扰,我能以“熊果酸”作为对照鉴别乌梅吗,虽然明知大枣也含熊果酸。乌梅阴性没有干扰,会不会是点样量少的问题?http://ng1.17img.cn/bbsfiles/images/2012/11/201211010017_400582_1872149_3.jpg1. 熊果酸;2-4. 样品;5. 阴性
[size=20px][color=#93c6bc][b]鉴别[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size][font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [b][font=宋体][/font][/b] [font=宋体][/font][font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体](1)本品表面观:上、下表皮细胞多角形,垂周壁平直,表面有颗粒状角质纹理;气孔平轴式。[/font] [font=宋体]本品横切面:表皮细胞扁平,外壁突起。叶两面均具[color=var(--weui-LINK)]栅栏组织[i][/i][/color],上表皮内栅栏细胞多为2列,下表皮内多为1列,细胞极短,海绵组织细胞2~4列,含棕色物。主脉维管束双韧型,维管束周围和韧皮部散有[color=var(--weui-LINK)]乳汁管[i][/i][/color]。[/font] [font=宋体](2)取本品粉末1g,加乙醚50ml,加热回流1小时,放冷,滤过,弃去乙醚液,药渣加水25ml,加热回流1小时,放冷,滤过,滤液用乙酸乙酯振摇提取2次,每次20ml,合并乙酸乙酯液,蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。另取罗布麻叶对照药材1g,同法制成对照药材溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各3[/font][font=宋体]μ[/font][font=宋体]l[/font][font=宋体],分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇-水(13:7:2)10℃以下放置过夜的下层溶液为展开剂,展开,取出,晾干,喷以3%[color=var(--weui-LINK)]三氯化铝[i][/i][/color]乙醇溶液,在105℃加热至斑点显色清晰,置紫外光灯 (365nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点。[/font] [font=宋体](3)取本品粉末0.5g,加80%甲醇50ml,加热回流1小时,放冷,滤过,滤液蒸干,残渣加水20ml使溶解,用乙醚振摇提取2次,每次20ml,弃去乙醚液,水液加盐酸5ml,加热回流1小时,取出,立即冷却,用乙醚振摇提取2次,每次20ml,合并乙醚液,用水10ml洗涤,弃去水液,乙醚液用铺有适量无水硫酸钠的滤纸滤过,滤液挥干,残渣加乙醇1ml使溶解,作为供试品溶液。另取[color=var(--weui-LINK)]槲皮素[i][/i][/color]对照品、山柰酚对照品,分别加乙醇制成每1ml各含0.5mg的溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取供试品溶液5[/font][font=宋体]μ[/font][font=宋体]l[/font][font=宋体]、两种对照品溶液各2[/font][font=宋体]μ[/font][font=宋体]l[/font][font=宋体],分别点于同一硅胶G薄层板上,以正己烷-乙酸乙酯-甲酸(7:5:0.8)为展开剂,展开,取出,晾干,喷以3%三氯化铝乙醇溶液,在105℃加热至斑点显色清晰,分别置日光和紫外光灯(365nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点或荧光斑点。[/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [size=20px][color=#93c6bc][b]检查[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [b][font=宋体][/font] [font=宋体][/font][/b] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][b]水分[/b] 不得过11.0%(通则0832第二法)。[/font] [b][font=宋体]总灰分[/font][/b][font=宋体] [/font][font=宋体]不得过12.0%(通则2302)。[/font] [b][font=宋体]酸不溶性灰分[/font][/b][font=宋体] [/font][font=宋体]不得过5.0%(通则2302)。[/font] [b][font=宋体]【浸出物】[/font][/b][font=宋体] 照醇溶性浸出物测定法(通则2201)项下的热浸法测定,用75%乙醇作溶剂,不得少于20.0%。[/font] [b][font=宋体]【含量测定】[/font][/b][font=宋体] 照高效液相色谱法(通则0512)测定。[/font] [b][font=宋体]色谱条件与系统适用性试验[/font][/b][font=宋体] [/font][font=宋体]以[color=var(--weui-LINK)]十八烷基硅烷键合硅胶[i][/i][/color]为填充剂;以乙腈-0.2%磷酸溶液(15:85)为流动相;检测波长为256nm。理论板数按金丝桃苷峰计算应不低于6000。[/font] [b][font=宋体]对照品溶液的制备[/font][/b][font=宋体] [/font][font=宋体]取金丝桃苷对照品适量,精密称定,加甲醇制成每1ml含36[/font][font=宋体]μ[/font][font=宋体]g[/font][font=宋体]的溶液,即得。[/font] [b][font=宋体]供试品溶液的制备[/font][/b][font=宋体] [/font][font=宋体]取本品粉末(过三号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入50%甲醇50ml,密塞,称定重量,加热回流30分钟,放冷,再称定重量,用50%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。[/font] [b][font=宋体]测定法[/font][/b][font=宋体] [/font][font=宋体]分别精密吸取对照品溶液与供试品溶液各10[/font][font=宋体]μ[/font][font=宋体]l[/font][font=宋体],注入液相色谱仪,测定,即得。[/font] [font=宋体]本品按干燥品计算,含金丝桃苷(C[sub]21[/sub]H[sub]20[/sub]O[sub]12[/sub])不得少于0.30%。[/font] [font=宋体][/font]
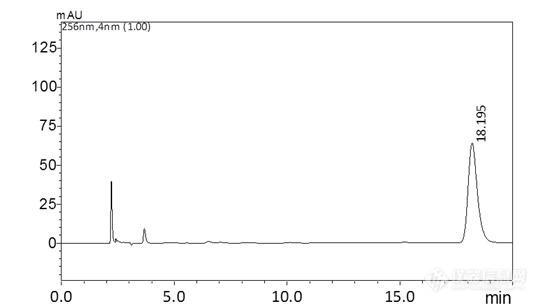
[align=center][font=宋体]中药材罗布麻叶测定注意事项[/font][/align][font=宋体]罗[/font][font=宋体]布麻叶经过提取杂质较多色素类物质较多,在测定罗布麻叶时候流动相应该在实验中注意的问题做一下讨论:[/font][font='Times New Roman', serif]1 [/font][font=宋体]材料[/font][font=宋体]罗布麻叶药材(送检样);乙腈(色谱级),甲醇、磷酸(分析纯);金丝桃苷对照品(购自中检院)。[/font][font='Times New Roman', serif]2 [/font][font=宋体]仪器与设备[/font][font=宋体]岛津[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url][/font][font='Times New Roman', serif]LC-20AT[/font][font=宋体]配制[/font][font='Times New Roman', serif]UV/DAD[/font][font=宋体]检测器,安家[/font][font='Times New Roman', serif]Eclipse XDB C18[/font][font=宋体]色谱柱[/font][font='Times New Roman', serif](250mm*4.6μm*5μm)[/font][font=宋体],超声波清洗器。[/font][font='Times New Roman', serif]3 [/font][font=宋体]实验方法[/font][font='Times New Roman', serif]3.1 [/font][font=宋体]色谱条件[/font][font=宋体]流动相(参照中国药典[/font][font='Times New Roman', serif]2020[/font][font=宋体]年第一部):乙腈[/font][font='Times New Roman', serif]-0.2%[/font][font=宋体]磷酸水为流动相进行洗脱;检测波长[/font][font='Times New Roman', serif]256nm[/font][font=宋体];柱温:[/font][font='Times New Roman', serif]35[/font][font=宋体]℃[/font][font=宋体];流速:[/font][font='Times New Roman', serif]1.0 mL/min[/font][font=宋体],进样量:[/font][font='Times New Roman', serif]10μL[/font][font=宋体]。[/font][font='Times New Roman', serif]3.2[/font][font=宋体]对照品溶液制备[/font][font='Times New Roman', serif] [/font][font=宋体]取金丝桃苷对照品适量,精密称定,加甲醇制成每[/font][font='Times New Roman', serif]1ml[/font][font=宋体]含[/font][font='Times New Roman', serif]36μg[/font][font=宋体]的溶液,即得。[/font][align=center][img=,539,304]https://ng1.17img.cn/bbsfiles/images/2022/09/202209010926295172_7098_1858223_3.jpg!w539x304.jpg[/img][/align][align=center][/align][font=宋体][/font][align=center][font=宋体]图[/font][font='Times New Roman', serif]1 [/font][font=宋体]金丝桃苷标准品色谱图[/font][/align][font='Times New Roman', serif]3.3 [/font][font=宋体]供试品溶液的制备[/font][font='Times New Roman', serif] [/font][font=宋体]取本品粉末(过三号筛)约[/font][font='Times New Roman', serif]0.5g[/font][font=宋体],精密称定,置具塞锥形瓶中,精密加入[/font][font='Times New Roman', serif]50%[/font][font=宋体]甲醇[/font][font='Times New Roman', serif]50ml[/font][font=宋体],密塞,称定重量,加热回流[/font][font='Times New Roman', serif]30[/font][font=宋体]分钟,放冷,再称定重量,用[/font][font='Times New Roman', serif]50%[/font][font=宋体]甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。[/font][align=center][img=,527,310]https://ng1.17img.cn/bbsfiles/images/2022/09/202209010927277774_606_1858223_3.jpg!w527x310.jpg[/img][/align][align=center][font=宋体]图[/font]2 [font=宋体]罗布麻叶样品色谱图[/font][/align][align=left][font=宋体]讨论:([/font][font='Times New Roman', serif]1[/font][font=宋体])罗布麻叶中含有色素类物质较多,提取溶液颜色较重,在实验处理过程中要注意滤膜选择[/font][font='Times New Roman', serif]0.22μm[/font][font=宋体]滤膜过滤干净之后上机检测,防止堵塞色谱管道,做叶子类物质也建议使用色谱柱保护预柱,防止污染色谱柱;[/font][/align][align=left][font='Times New Roman', serif](2)[/font][font=宋体]我们从样品的色谱图可以看出在金丝桃苷目标峰出现之后[/font][font=宋体]后面还有很多杂质出现,所以我们在目标峰出现后,设置一个梯度洗脱,以免影响下一个样品出峰,同时也能保护柱子的使用寿命。[/font][/align]

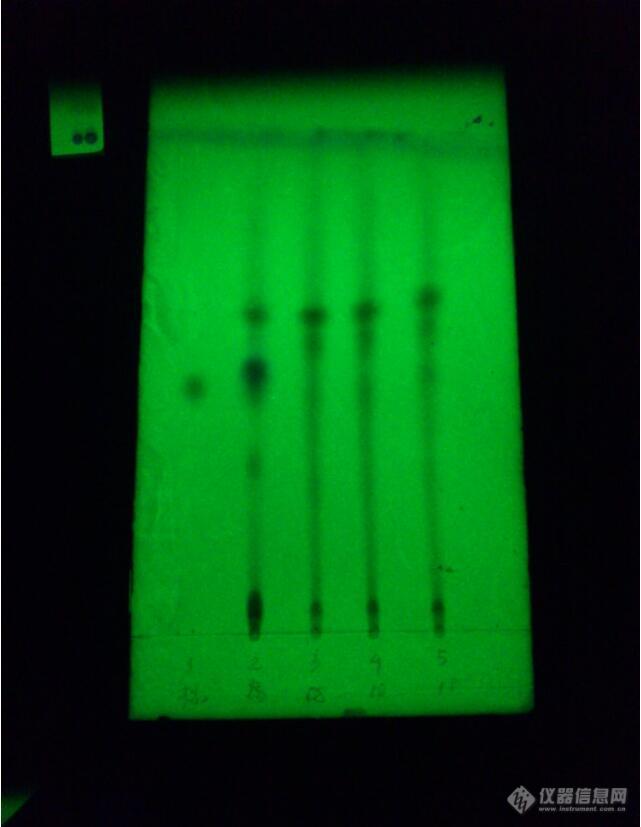
请各位老师帮忙看看,不知荆芥对照药材(右边一个为对照药材,左边三个为制剂样品——含荆芥)本身就这样,还是我做的不好,斑点不清晰。多谢![img=,690,517]https://ng1.17img.cn/bbsfiles/images/2019/07/201907171127582678_7811_1825519_3.jpg!w690x517.jpg[/img]

问题:千柏鼻炎胶囊中金丝桃苷的检测药典要求理论板数按金丝桃苷峰计算应?答案:不低于7000【活动奖励】幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币mengzhaocheng(ID:mengzhaocheng)dyd3183621(注册ID:dyd3183621)ZHAOGUANGXI(注册ID:ZHAOGUANGXI)http://ng1.17img.cn/bbsfiles/images/2016/02/201602241517_585010_1610895_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/02/201602241517_585011_1610895_3.png积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。======================================================================= 千柏鼻炎胶囊中金丝桃苷的检测样品制备 制备方法1. 对照品:取金丝桃苷对照品适量,精密称定,加流动相制成每1 mL含15 μg的溶液,即得。2. 供试品:取装量差异项下的本品内容物,研细,取约0.5 g,精密称定,精密加入75%甲醇25 mL,称定重量,加热回流1小时,放冷,再称定重量,用75%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。分析条件 色谱柱Platisil ODS 150 x 4.6 mm,5 μm (Cat#:99501)流动相乙腈:0.2%冰醋酸溶液=15:85 流速1 mL/min柱温30 ℃检测器UV 360 nm进样量10 μL色谱图对照品(流动相溶解) http://ng1.17img.cn/bbsfiles/images/2016/02/201602241020_584970_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 23.282 715234 21365 11118.648 0.953 -- *药典要求理论板数按金丝桃苷峰计算应不低于7000供试品http://ng1.17img.cn/bbsfiles/images/2016/02/201602241020_584971_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 23.411 24797 927 17640.547 0.912 -- *药典要求理论板数按金丝桃苷峰计算应不低于7000本品种同时使用了Leapsil C18色谱柱,在药典规定条件下进行金丝桃苷的检测,满足药典要求。

问题:千柏鼻炎片中金丝桃苷的检测:用到了迪马哪几款色谱柱?答案:捌道巴拉巴巴巴(ID:v3082413)梧桐(ID:mengzhou)WUYUWUQIU(ID:wulin321)http://ng1.17img.cn/bbsfiles/images/2016/02/201602251657_585143_708_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/02/201602251657_585144_708_3.jpg【活动奖励】幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。千柏鼻炎片中金丝桃苷的检测样品制备 制备方法1. 对照品:取金丝桃苷对照品适量,精密称定,加甲醇制成每1 mL含20 μg的溶液,即得。2. 供试品:取本品20片,糖衣片除去包衣,精密称定,研细,取适量(约相当于2片重量),精密称定,精密加入75%甲醇25 mL,称定重量,加热回流1小时,放冷,再称定重量,用75%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。分析条件 色谱柱Platisil ODS 150 x 4.6 mm,5 μm (Cat#:99501)流动相乙腈:0.2%冰醋酸溶液=15:85 流速1 mL/min柱温30 ℃检测器UV 360 nm进样量10 μL色谱图对照品(流动相溶解)http://ng1.17img.cn/bbsfiles/images/2016/02/201602251145_585066_708_3.png 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 23.282 715234 21365 11118.648 0.953 -- *药典要求理论板数按金丝桃苷峰计算应不低于7000供试品http://ng1.17img.cn/bbsfiles/images/2016/02/201602251145_585067_708_3.png 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 23.397 60226 1941 12868.432 0.973 -- *药典要求理论板数按金丝桃苷峰计算应不低于7000本品种同时使用了Leapsil C18色谱柱,在药典规定条件下进行金丝桃苷的检测,满足药典要求。

黄连上清片高温灭菌后,黄连对照药材薄层鉴别的点变红是怎么回事?[img=,690,388]https://ng1.17img.cn/bbsfiles/images/2019/07/201907101138123673_5943_1782490_3.jpg!w690x388.jpg[/img]
白芷的荧光鉴别白芷是与肉桂、红花、川乌、草乌、荆芥、防风、干姜、金银花、当归、三棱、莪术混提,用水煎煮提取2次,每次2小时,成品中有白芷的薄层鉴别,与白芷对照药材在紫外下观察荧光。我已经做了多批,都看不到荧光斑点,很困惑,请有经验的老师帮忙指导。

中药制剂中木瓜的薄层鉴别:供试品与对照药材处相应的点颜色不同是为什么?狗脊的薄层鉴别也是一样,提取时处理方法是一样的图1前三供试品(绿色),中二木瓜对照药材(蓝色),后二阴性对照图2前二供试品(亮的点蓝色),中二狗脊对照药材(绿色),后二阴性对照不知道该怎么办,诚请各位大师解答,谢谢[img=,690,459]https://ng1.17img.cn/bbsfiles/images/2019/08/201908061329352099_2969_1816508_3.jpg!w690x459.jpg[/img][img=,380,362]https://ng1.17img.cn/bbsfiles/images/2019/08/201908061329533546_2463_1816508_3.jpg!w380x362.jpg[/img]
天麻对照品天麻素和对羟基苯甲醇保留时间分别是11和22分钟,天麻药材出峰时间是15和26分钟,且时间还比较稳定,后面更换了新柱子,把柱温箱温度从30度调到35度,把泵从B泵更换到A泵,重新配流动相,供试品,发现还是一样漂移。而且之前做的特征图谱保留时间又对的上。流动相过滤了也超声了。真的不知道该咋办了??
求贯叶连翘中的金丝桃素的提取和检测方法,谢谢!
西青果的薄层图?按药典方法提取展开,对照药材也没有斑点。是否有其他可行的方法?
药材样品溶液和对照品在聚酰胺板跑,但样品与对照总是不一致,这个成分在样品中含量约0.06%左右,样品称的是2g,最后溶解于2ml的EP管中,点样量5μL。后来把样品称到5g,但最后无法全部洗脱于2ml的EP管中,由于太浓稠了,点样量只是点了一下。但还是一样。 药材为叶类药材
延胡索薄层样品比对照药材多了一个点,怎么回事?
[size=20px][color=#93c6bc][b]鉴别[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [font=宋体][/font] [font=宋体][/font][b][font=宋体][/font][/b] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [b][font=宋体][/font][/b][font=宋体][/font] [font=宋体]本品粉末灰绿色。上表皮细胞表面观多角形,外壁乳头状或短绒毛状突起,呈双圆圈状;断面观长方形,外壁呈乳头状突起;气孔[color=var(--weui-LINK)]不定式[i][/i][/color],副卫细胞5[/font][font=&]~[/font][font=宋体]8[/font][font=宋体]个。下表皮细胞表面观垂周壁略波状弯曲,有时可见连珠状增厚。[color=var(--weui-LINK)]草酸钙簇晶[i][/i][/color]多见,直径约至40μm。[/font] [font=宋体](2)[/font][font=宋体]取本品粉末1g,加浓氨试液1ml润湿,加二氯甲烷40ml,超声处理30分钟,滤过,滤液回收溶剂至干,残渣加甲醇1ml使溶解,作为供试品溶液。另取荷叶对照药材1g,同法制成对照药材溶液。再取荷叶碱对照品,加甲醇制成每1ml含1mg的溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取上述供试品溶液和对照药材溶液各15μl,对照品溶液5μl,分别点于同一硅胶G薄层板上,以二氯甲烷-乙酸乙酯甲醇-水(3:4:2:1)的下层溶液为展开剂,展开,取出,晾干,喷以碘化铋钾试液,置日光下检视。供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上,显相同颜色的斑点。[/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font][font=宋体][/font] [font=宋体] [/font] [size=20px][color=#93c6bc][b]检查[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [font=宋体][/font] [b][font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体]水分 [/font][/b][font=宋体] 不得过15.0%(通则0832第二法)。[/font] [b][font=宋体]总灰分[/font][/b][font=宋体] [/font][font=宋体]不得过12.0%(通则2302)。[/font] [b][font=宋体]【浸出物】[/font][/b][font=宋体] 照醇溶性浸出物测定法(通则2201)项下的热浸法测定,用70%乙醇作溶剂,不得少于10.0%。[/font] [b][font=宋体]【含量测定】[/font][/b][font=宋体] 照高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法(通则0512)测定。[/font] [b][font=宋体]色谱条件与系统适用性试验[/font][/b][font=宋体] [/font][font=宋体]以[color=var(--weui-LINK)]十八烷基硅烷键合硅胶[i][/i][/color]为填充剂;以乙腈-水-三乙胺-冰醋酸(27:70.6:1.6:0.78)为[color=var(--weui-LINK)]流动相[i][/i][/color];检测波长为270nm。理论板数按荷叶碱峰计算应不低于2000。[/font] [b][font=宋体]对照品溶液的制备[/font][/b][font=宋体] [/font][font=宋体]取荷叶碱对照品适量,精密称定,加甲醇制成每1ml含16μg的溶液,即得。[/font] [b][font=宋体]供试品溶液的制备[/font][/b][font=宋体] [/font][font=宋体]取本品粗粉约0.5g,精密称定,置具塞锥形瓶中,精密加入甲醇50ml,称定重量,加热回流2.5小时,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液5ml,置10ml量瓶中,加水至刻度,摇匀,即得。[/font] [b][font=宋体]测定法 [/font][/b][font=宋体]分别精密吸取对照品溶液与供试品溶液各20μl,注入[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url],测定,即得。[/font] [font=宋体]本品按干燥品计算,含荷叶碱(C[sub]19[/sub]H[sub]21[/sub]NO[sub]2[/sub])不得少于0.10%。[/font] [font=宋体][/font]
[size=20px][b]性状[/b][/size][size=16px][color=#e2a4a4]|[/color][/size] [font=宋体][/font] [b][font=宋体][/font][/b][font=宋体][b][font=&][/font][/b][/font][b][font=宋体][/font][/b][font=宋体]本品为鳞片状集合体。呈不规则块状或碎片,碎片直径0.1~0.8cm;块状者直径2~10cm,厚0.6~1.5cm,无明显棱角。棕黄色或黄褐色,带有金黄色或银白色光泽。质脆,用手捻之,易碎成金黄色闪光小片。具滑腻感。气微,味淡。[/font][font=宋体][/font] [font=宋体][/font][font=宋体][/font] [font=宋体][/font][font=宋体][/font] [font=宋体][/font] [size=20px][color=#93c6bc][b]鉴别[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font]取本品碎片少量,置铁片上加热,即层裂或散裂,膨胀2~5倍,有的鳞片变成弯曲的蛭虫状;色泽变浅,重量减轻,可浮于水面。[font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [size=20px][color=#93c6bc][b]饮片[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [font=宋体][/font] [font=宋体][/font] [b][font=宋体][/font][/b] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][b]金礞石[/b] 除去杂石。[/font] [b][font=宋体]【性状】[/font][/b][font=宋体] 同药材。[/font] [b][font=宋体]煅金礞石[/font][/b][font=宋体] [/font][font=宋体]取净金礞石,照明煅法(通则0213)煅至红透。[/font] [b][font=宋体]【性状】 [/font][/b][font=宋体]呈不规则碎块状颗粒或鳞片状粉末。表面无明显棱角,棕黄色至金黄色,具金黄色光泽。碎块断面可见层纹。具滑腻感。质脆,易碎。气微,味淡。[/font] [font=宋体] [/font] [color=#93c6bc][size=20px][b]其他[/b][/size][/color][size=16px][color=#e2a4a4]|[/color][/size] [b][font=宋体][/font][/b][font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [b][font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体]【性味与归经】[/font][/b][font=宋体] 甘、咸,平。归肺、心、肝经。[/font] [b][font=宋体]【功能与主治】[/font][/b][font=宋体] 坠痰下气,平肝镇惊。用于顽痰胶结,咳逆喘急,癫痫发狂,烦躁胸闷,惊风抽搐。[/font] [b][font=宋体]【用法与用量】[/font][/b][font=宋体] 多入丸散服,3~6g;煎汤10~15g,布包先煎。[/font] [b][font=宋体]【贮藏】[/font][/b][font=宋体] 置干燥处。[/font] [font=宋体][/font]
维权声明:本文为yhc2004原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。有机氯农药是一类高效广谱杀虫剂,曾在世界各国广泛使用。我国虽已在1983年停止使用这类农药,但由于它具有化学性质稳定、不易分解,并通过生物链富集在动植物体内,造成了对自然环境的严重污染及对人体健康的极大危害。中药材种植期一般较长,尤其是多年生根类药材,更易受到有机氯农药的污染。我国中药材中的农药残留的污染,是造成中药材质量下降的重要原因,已成为制约我国中药材走向国际市场的主要障碍。因此,中药材中农药残留问题已经引起了国内外的普遍关注,建立和完善中药材中有机氯农药残留量的检测方法十分必要。 黄芪药材为豆科植物蒙古黄芪或膜荚黄芪的干燥根。呈圆柱形,表面淡棕黄色或淡棕褐色,有不整齐的纵皱纹或纵沟。质硬而韧,不易折断,断面纤维性强,并显粉性,皮部黄白色,木部淡黄色,具放射状纹理及裂隙,呈“菊花心状”。气微,味微甜。嚼之有豆腥味。性温,味甘。具有补气固表,利尿,托毒,排脓,敛创生肌之功效。主产于山西、黑龙江、内蒙古等省区。以栽培的蒙古黄芪质量为佳。至今为止,对其中有机氯农药六六六、滴滴涕残留测定的研究未见报道。本文建立了黄芪药材中9种有机氯农药超声提取,毛细管气相色谱检测的方法,为提高传统中药的质量、建立和完善中药产品中有机氯类农药残留量的测定的方法提供依据。 1 仪器与试剂1.1 仪器 THGC-2001气相色谱仪,电子捕获检测器,弹性石英毛细管柱 30m×0.32mm×0.25μm。800型离心机。1.2 试剂 丙酮(分析纯),石油醚(沸程60~90℃,分析纯),二氯甲烷(分析纯)无水硫酸钠(分析纯)硫酸(分析纯)有机氯农药六六六(BHC)(α-BHC,β-BHC,γ-BHC,δ-BHC)、滴滴涕(DDT)(PP΄-DDE, PP΄-DDD ,OP΄ -DDT,PP΄-DDT)及五氯硝基苯(PCNB)标准品(农业部农药检定所)2 方法与结果2.1 对照品的制备2.1.1 对照品储备液的制备精密称取六六六(BHC)(α-BHC,β-BHC,γ-BHC,δ-BHC)、滴滴涕(DDT)(PP΄-DDE, PP΄-DDD ,OP΄ -DDT,PP΄-DDT)及五氯硝基苯(PCNB)农药对照品适量,用石油醚(60~90℃)分别制成每1ml约含4~5µg的溶液,即得2.1.2 混合对照品储备液的制备 精密量取上述各对照品储备液0.5ml,置10ml量瓶中,用石油醚(60~90℃)稀释至刻度,摇匀,即得。2.1.3 混合对照品溶液的制备 精密量取上述混合对照品储备液,用石油醚(60~90℃)制成每1L分别含0µg、1µg、5µg、10µg、50µg、100µg、250µg的溶液,即得。 2.2 色谱条件 弹性石英毛细管柱 30m×0.32mm×0.25μm;进样口温度230℃,检测器温度300℃,不分流进样;流速为28ml/min;程序
[size=20px][color=#93c6bc][b]鉴别[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [font=宋体][/font] [font=宋体][/font] (1)本品叶片近基部横切面:上表皮细胞类方形,壁厚,外被厚的角质层,主脉处有单细胞非腺毛;下表皮细胞略小,可见气孔。[color=var(--weui-LINK)]栅栏组织[i][/i][/color]为2~4列细胞,海绵组织疏松;主脉处上、下表皮内为1至数列[color=var(--weui-LINK)]厚角细胞[i][/i][/color]。主脉维管束外韧型,其上、下方均具木化纤维群。叶缘表皮内常依次为厚角细胞和[color=var(--weui-LINK)]石细胞[i][/i][/color]半环带,再内为木化纤维群;叶缘近叶柄处仅有数列厚角细胞,近基部以上渐无[color=var(--weui-LINK)]厚角组织[i][/i][/color]。叶缘表皮内和主脉处下表皮内厚角组织中偶有石细胞,韧皮部下方的纤维群外亦偶见。[color=var(--weui-LINK)]薄壁组织[i][/i][/color]和下表皮细胞常含草酸钙簇晶。 [font=宋体](2)取本品粉末2g,加70%乙醇40ml,超声处理30分钟,滤过,滤液蒸干,残渣加水40ml使溶解,加三氯甲烷40ml振摇提取,弃去三氯甲烷液,水层加浓氨试液2ml,摇匀,再加水饱和的正丁醇40ml振摇提取,分取正丁醇液,浓缩至干,残渣加甲醇2ml使溶解,作为供试品溶液。另取枸骨叶对照药材2g,同法制成对照药材溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各1[/font][font=&]μ[/font][font=宋体]l[/font][font=宋体],分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-水(1:3:1:0.3)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点。[/font] [font=宋体][/font] [font=宋体] [/font] [font=宋体][/font] [font=宋体][/font] [size=20px][color=#93c6bc][b]检查[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [b][font=宋体][/font] [font=宋体][/font] [font=宋体]水分[/font][/b][font=宋体] [/font][font=宋体]不得过8.0%(通则0832第二法)。[/font] [b][font=宋体]总灰分[/font][/b][font=宋体] [/font][font=宋体]不得过6.0%(通则2302)[/font]
[font=宋体]茯苓载于《神农本草经》,列为上品,为多孔菌科真菌茯苓[/font][i]Poria cocos [/i](Schw.) Wolf[font=宋体]的干燥菌核,具有利水渗湿、健脾宁心之效[/font][sup][1][/sup][font=宋体]。茯苓被誉为中药四君八珍之一,是方剂配伍的要药及中成药的重要原料。在[/font]2019[font=宋体]年新型冠状病毒肺炎治疗方案中,由茯苓配伍的多个中药组方疗效显著[/font][sup][2][/sup][font=宋体]。茯苓多糖和三萜类化合物分别占菌核干质量的[/font]70%[font=宋体]~[/font]90%[font=宋体]和[/font]0.3%[font=宋体],为其主要活性成分,其药理活性较为丰富,具有抗肿瘤、抑菌抗炎、增强免疫和镇静等疗效[/font][sup][3-5][/sup][font=宋体]。[/font][font=宋体]此外,茯苓在食品和化妆品等行业相关产品均有[/font][font=宋体]应用,且市场需求较大。[/font] [font=宋体]茯苓需以松属植物的根部或木段为寄主完成生命过程,但持续增长的市场需求与松木资源的过度消耗形成严峻矛盾,因而推动了茯苓代料栽培和液体发酵等新技术的快速发展。不同的培养方式对茯苓产量、药材品质和推广应用均有不同的影响,目前未见对茯苓培养方式全面科学的评价论述。基于此,笔者提出药材“四性”特征,即临床疗效“三性”(安全性、有效性、质量可控性)及经济性,用于综合评价药材种植、药材品质和临床药效。其中安全性是中药材用于临床治疗的前提,指按规定的适应证、用法和用量使用药材及相关产品过程中或使用后人体产生不良反应的程度,而培养过程中的重金属、农药残留等环境障碍因子会影响药材的安全性;有效性则是药材及相关产品存在、应用和优劣的根据,即在药品规定的适应证、用法和用量的条件下,能满足预防、治疗、诊断疾病,有目的地调节人生理机能的性能;质量可控[/font][font=宋体]性是保证药品安全性和有效性的基础,即在生产过程中可以切实控制达到药品内在质量的一致,不同培养方式下药材的质量可控性差异较大;经济性则代表了药材及其相关产品在达到相同治疗[/font]/[font=宋体]保健等效果时的利润空间,涉及培养时期的成本投入、相关产品的推广应用等。因此,本文以茯苓药材“四性”特征与供需关系的现状为切入点,分析了其培养方式的发展动态及未来趋势,总结了不同培养方式对茯苓“四性”特征的影响情况,对缓解菌木矛盾、促进茯苓相关产业可持续发展具有重要的意义。[/font] 1 茯苓的应用历史及现状[font=宋体]茯苓最初以“服零”载于战国时期医学帛书《五十二病方》,与半夏、白附子、牡蛎等配伍治疗痰症[/font][sup][6][/sup][font=宋体];[/font][font=宋体]后载于《神农本草经》[/font][sup][7][/sup][font=宋体],谓:“气味甘、平、无毒。主胸胁气逆,忧恚,惊邪恐悸,心下结痛,寒热烦满,咳逆,口焦舌干,利小便。久服安魂养神,不饥延年。”至东汉时期,《伤寒论》所载茯苓相关的方剂共计[/font]15[font=宋体]首,以利水消肿、健脾渗湿、宁心安神功效为主。至唐朝时期,茯苓的临床应用愈加普遍,《备急千金要方》中所载茯苓方剂达[/font]465[font=宋体]首[/font][sup][8][/sup][font=宋体]。[/font][font=宋体]根据[/font]2022[font=宋体]年对全国[/font]18[font=宋体]个省份共约[/font]43[font=宋体]万张汤剂处方的数据统计分析得知,在常用的临床汤剂中药饮片排名中,茯苓位列第[/font]2[font=宋体],仅次于甘草,素有“十药九苓”之说。在常用的中药方剂中,茯苓配伍率高达[/font]70%[sup][9][/sup][font=宋体];在国家中医药管理局制定的[/font]100[font=宋体]首古代经典名方中,以茯苓为原料的经典名方占[/font]24%[sup][10][/sup][font=宋体]。茯苓的药用价值高、复方制剂适配广。此外茯苓是我国著名的食药两用真菌,于[/font]2002[font=宋体]年列入卫生部《既是食品又是药品的中药名单》[/font][sup][11][/sup][font=宋体],已逐渐被开发为保健品、面食、饼干、酸奶、保健醋、保健型饮料等,茯苓的市场需求急剧增加,对其培养要求亦相应提高。[/font]2 茯苓资源市场现状[font=宋体]随着茯苓从临床应用拓展到食品、保健品、药膳等多元化的产品,茯苓市场需求与日俱增,也推动了茯苓种植的发展。目前全国茯苓种植面积约有[/font]1.2[font=宋体]亿[/font]hm[sup]2[/sup][font=宋体],年产量达[/font]4[font=宋体]万[/font]t[font=宋体],并保持持续的增长态势。全国[/font]10[font=宋体]余个省已建立了[/font]150[font=宋体]多个茯苓规范化种植基地。国内的茯苓供给已难以满足需求,自[/font]2019[font=宋体]年起,欧洲和朝鲜半岛成为我国茯苓进口的主要国家和地区,主要进口省份是我国吉林、辽宁、安徽、江苏和河北[/font][sup][12][/sup][font=宋体]。中国乃至全球对茯苓的需求量均呈逐年递增的趋势,伴随着对松木消耗的大幅增长,茯苓培养方式的深入研究及变革势在必行。[/font]3 茯苓培养方式的沿革[font=宋体]茯苓药材最初依赖于野生资源,受气候、地域及无序采挖等因素影响,茯苓收获不稳定、品质差异大,且随着药用需求的增加,野生茯苓资源逐渐枯竭,遂开始了人工培养茯苓的探索。南北朝梁代的《本草经集注》记:“彼土人乃故斫松作之,形多小,虚赤不佳”[/font][sup][13][/sup][font=宋体],揭示了茯苓常以松木蔸或木段为寄主生长,开创了茯苓人工培养的先河。此培养方式一直延续至今,期间经过多年的探索和完善,技术逐渐规范化,产量和质量得以显著提高,在现阶段茯苓栽培中仍占有主导地位。然而该技术需要消耗大量的松木资源,约每生产[/font]1 t[font=宋体]茯苓需要消耗[/font]20 m[sup]3[/sup][font=宋体]的松木。[/font]2005[font=宋体]年,习近平主席提出“绿水青山就是金山银山”的发展理念,出台了限制砍伐森林原木的条例,茯苓生产与保护森林资源形成相互制约,菌林矛盾凸显。为缓解资源矛盾,协同发展,现代化培养技术逐步得到关注,如以木屑和各种农副产品为培养基开展茯苓的代料培养。该培养方式能大幅度减少对松木的消耗。但目前该技术尚不成熟,茯苓产量较低、生产成本较高,难以推广。在此两难之际,微生物发酵技术被引入茯苓生产,相较于茯苓固体培养技术易受环境和人为操作影响导致茯苓质量稳定性较差的缺点,液体发酵技术具有制备菌种周期快、菌龄齐的特点,制备得到的发酵茯苓质量稳定性高等优势;同时在短时间内可获得大量茯苓菌丝体和次生代谢产物,有利于茯苓功能型产品的开发,并较好地解决了茯苓质量稳定性差的难题。至此,茯苓的培养方式经历了野生培养、传统人工培养、现代培养(代料栽培和液体发酵)[/font]3[font=宋体]个重要变革阶段(图[/font]1[font=宋体])。如今茯苓固体栽培技术和液体发酵技术仍需深入研究,二类技术的共同发展,既能较好满足茯苓市场需求,又能保护松木资源,维护生态平衡。[/font]3.1 [font=黑体]野生培养[/font][font=宋体]我国幅员辽阔,松木资源丰富,生态多样性形成了优质的茯苓种质资源。其中黄河以南的安徽、云南、贵州、湖北、湖南、广西、四川、河南、浙江、山西、陕西等都有分布[/font][sup][14-16][/sup][font=宋体]。初期,茯苓药材完全依靠于采挖野生资源,但其野生资源分布零散,采收不宜;同时野生资源的无序开发导致其资源几近枯竭,无法满足临床用药需求。南宋时期,江苏一带开始对茯苓进行人工培养的探索。明代中期,浙江一带开展茯苓林下仿野生人工培养。经过长期探索,成功将野生茯苓转为家种,其生产规模不断扩大。至此,茯苓结束了源于野生资源的历史。[/font]3.2 [font=黑体]传统人工培养[/font]3.2.1 [font=宋体]传统人工培养的应用[/font] [font=宋体]人们对茯苓人工培养的探索始于《本草经集注》,发现松树是茯苓的重要寄主。其中郁洲即今江苏连云港云台山一带,描述了人们砍伐松树,开展人工培养茯苓的场景,但该方式生产的茯苓产量低、品质差。宋末元初《癸辛杂识》载:“择其小者,以大松根破而系于其中,而紧束之,使脂渗入于内,然后择其地之沃者,坎而瘗之”,出现“肉引”培养的雏形,开始了小范围的茯苓种植,但培养技术尚不成熟。茯苓人工培养虽有[/font]1 500[font=宋体]多年的历史,但直到[/font]19[font=宋体]世纪中后期,其人工培养技术才逐步成熟稳定,至此,茯苓才完全转变为人工培养。目前,茯苓的传统人工培养模式主要有段木培养和树蔸培养[/font]2[font=宋体]种形式[/font][sup][2,17-18][/sup][font=宋体]。湖北等地区主要以段木培养为主,即以松木段作为培养基,将人工培育的菌种接种于木段上,入窖后菌丝可在段木上结苓,此方法为“菌引法”。向亮[/font][sup][19][/sup][font=宋体]发现段木培养一般每窖[/font]15[font=宋体]~[/font]20 kg[font=宋体]段木采收鲜茯苓[/font]2.5[font=宋体]~[/font]15.0 kg[font=宋体],高产可达[/font]25[font=宋体]~[/font]40 kg[font=宋体],折干率为[/font]50%[font=宋体]左右。云南和四川等地区主要以树蔸培养为主,树蔸培养茯苓是利用松木砍伐后遗留的松树蔸培养茯苓,即直接将菌种接种在树蔸上结出茯苓菌核。廖盛祥[/font][sup][20][/sup][font=宋体]采用直径[/font]23 cm[font=宋体]以上松树蔸培养茯苓,年产茯苓可达[/font]7.5[font=宋体]~[/font]50.0 kg[font=宋体]。菌核质量因培养模式不同而有所差异,目前以段木窖栽为主。[/font]3.2.2 [font=宋体]传统人工培养的现状[/font] [font=宋体]茯苓段木培养方式存在松木消耗量大(约每生产[/font]1 t[font=宋体]茯苓需要消耗[/font]20 m[sup]3[/sup][font=宋体]松木)、茯苓菌种质量差异大、生产周期长和易受环境条件影响等不足,导致茯苓产量较低,品质不稳定。同时随着茯苓栽培需求增加,对松木资源的损耗也同比增长,从而引发松木过度砍伐、森林生态失衡、水土流失、连作障碍等问题。为解决松木资源保护与茯苓资源开发间的矛盾,现多地采用耕种[/font]1[font=宋体]年、休耕[/font]3[font=宋体]年,及松木林间伐等措施,既能解除连作障碍,又能给松木生长提供时间空间。但松木生长常需较长的时间,随着茯苓需求与日俱增,菌木矛盾仍旧凸显,严重地制约其产业的可持续发展,亟需探寻新的培养技术。[/font]3.3 [font=黑体]现代化培养[/font]3.3.1 [font=宋体]代料培养[/font] [font=宋体]([/font]1[font=宋体])[/font][font=宋体]代料培养的应用:为缓解茯苓人工培养中的菌木矛盾,[/font]21[font=宋体]世纪初人们尝试开展代料培养。茯苓代料培养以松木屑及其他粮食废料为培养基,将菌种接种于代料进行室内培养,结出茯苓菌核。食用菌和药用真菌所需营养主要是氮源和碳源。氮源可从麸皮、谷糠等有机氮和硫酸铵等无机氮中获得;由于茯苓不能直接利用无机碳源,其碳源全部来自于有机碳源,如葡萄糖、蔗糖等小分子有机物及纤维素、半纤维素、木脂素和果胶等高分子有机物。松木屑、木块等工业边角余料中含有丰富的纤维素、半纤维素、木脂素和果胶等物质。代料培养过程[/font][sup][21-24][/sup][font=宋体]主要是:代料制作[/font]→[font=宋体]苓场的选择和整理[/font]→[font=宋体]接种[/font]→[font=宋体]下窖与覆土[/font]→[font=宋体]管理[/font]→[font=宋体]采收。已有较多研究针对茯苓代料配方及其培养效果进行了探讨(表[/font]1[font=宋体]),多以菌丝存活率和产量作为基本指标,并比较了代料培养茯苓与段木培养茯苓活性成分(如总三萜、多糖等)的含量,发现代料培养方式有望替代段木培养。[/font][font=宋体]([/font]2[font=宋体])[/font][font=宋体]代料培养的现状:代料培养所需培养料均属于工业边角余料和农副产品,如松木屑、玉米芯和麸皮等,廉价易得;且进行代料室内培养不需要占用土地,其生长发育过程不受外界天气影响,有利于茯苓快速生长,也避免了连作障碍的发生。相较于传统人工培养,该法减少了松木消耗,简化了种植方法,提高了松木利用率。但由于目前茯苓的代料培养技术尚不成熟,其所培养的茯苓产量较低、成本较高,目前该培养方式还难以推广。[/font]3.3.2 [font=宋体]液体发酵[/font] [font=宋体]([/font]1[font=宋体])[/font][font=宋体]液体发酵的应用:液体发酵技术兴起于[/font]20[font=宋体]世纪[/font]80[font=宋体]年代,是微生物发酵技术的一种,指将培养物料制备成液态培养基灭菌后,再将微生物接入而产生的生物反应。该技术兴起之初主要用于食品和医药等领域,近年来,微生物发酵技术逐渐融入到食用菌和药用真菌产业中,其产业模式和效益等方面均有不同程度的提升。液体发酵的培养基由碳源、氮源、无机盐和微量元素等组成[/font][sup][28-31][/sup][font=宋体]。碳源主要包括葡萄糖、蔗糖、乳糖和甘油等;氮源分为蛋白胨、酵母浸粉等有机氮和[/font]NH[sub]4[/sub]Cl[font=宋体]、[/font](NH[sub]4[/sub])[sub]2[/sub]SO[sub]4[/sub][font=宋体]等无机氮[color=red]二[/color]类。碳氮比是药用真菌生物发酵过程的关键因素,不同种类药用真菌的最适碳氮比不同,同一种类药用真菌在发酵的不同时期适宜的碳氮比也有所差异。培养基中[/font]K[sub]2[/sub]HPO[sub]4[/sub][font=宋体]、[/font]KH[sub]2[/sub]PO[sub]4[/sub][font=宋体]、[/font]MgSO[sub]4[/sub][font=宋体]、[/font]NaCl[font=宋体]、[/font]KCl[font=宋体]等无机盐和磷、镁、钠、钾、铁和硫等微量元素对于维持真菌菌丝体的生长发育及相关蛋白稳定性具有重要作用。在整个液体发酵过程中除了菌丝及其孢子大量增殖外,还可产生三萜、多糖和氨基酸等多种活性成分,且部分活性成分高于传统培养茯苓[/font][sup][32][/sup][font=宋体]。其发酵过程主要是:液体种子培养基的制备[/font]→[font=宋体]接种[/font]→[font=宋体]液体发酵培养基的制备[/font]→[font=宋体]接种[/font]→[font=宋体]发酵[/font]→[font=宋体]发酵茯苓。[/font][font=宋体]邵伟等[/font][sup][33][/sup][font=宋体]使用单因素实验优化茯苓液体发酵条件,发现茯苓液体发酵的适用温度为[/font]26 [font=宋体]℃,摇瓶装量为[/font]150 mL/500 mL[font=宋体]三角瓶,摇瓶转速为[/font]100[font=宋体]~[/font]150 r/min[font=宋体],培养基初始[/font]pH[font=宋体]为[/font]5.0[font=宋体]~[/font]5.5[font=宋体]。课题组前期也通过响应面优化技术获得了茯苓液体发酵最适培养基,即葡萄糖[/font]-[font=宋体]酵母浸膏[/font]-[font=宋体]蛋白胨[/font]-K[sub]2[/sub]HPO[sub]4[/sub]- MgSO[sub]4[/sub]7H[sub]2[/sub]O[font=宋体]为[/font]30.0[font=宋体]∶[/font]3.9[font=宋体]∶[/font]5.1[font=宋体]∶[/font]1.0[font=宋体]∶[/font]0.5[font=宋体]([/font]w/w[font=宋体],[/font]1 L[font=宋体]);在此基础上得到的最佳培养条件是培养温度[/font]26 [font=宋体]℃,摇瓶装量[/font]60 mL/250 mL[font=宋体]三角瓶,转速[/font]150 r/min[font=宋体],培养基初始[/font]pH[font=宋体]值[/font]5.5[font=宋体],液体菌种菌龄[/font]2 d[font=宋体],液体菌种接种量[/font]6%[font=宋体],摇瓶培养[/font]7 d[sup][34-36][/sup][font=宋体]。[/font][font=宋体]([/font]2[font=宋体])[/font][font=宋体]液体发酵的优势[/font][font=宋体]:[/font]①[font=宋体]培养基成本低、来源广泛。工业葡萄糖和工业蔗糖等工业原料可作为液体发酵培养基的碳源;黄豆饼粉、蚕蛹粉、麸皮粉等农作物废料可作为液体发酵培养基的氮源。木材水解液、各种农作物深加工废水等工业废水也可作为代用品,其原料来源相当广泛。[/font]②[font=宋体]菌丝体生长速度快,生产周期短。茯苓菌丝体在液体培养基中发菌点多、萌发快,新陈代谢旺盛,生长分裂迅速,培养周期为[/font]7 d[font=宋体]。而固体培养时间较长,段木培养一般需要[/font]240[font=宋体]~[/font]300 d[font=宋体],代料培养一般需要[/font]180[font=宋体]~[/font]240 d[font=宋体]。[/font]③[font=宋体]短时间可积累大量代谢产物。茯苓菌丝体在液体发酵过程中能充分接触和吸收营养物质,在短时间内可以获得大量的菌丝体和茯苓多糖、三萜类等活性代谢产物。[/font]④[font=宋体]液体发酵工艺易于控制,菌龄整齐。在液体发酵过程中,可全程适时动态控制茯苓菌丝体所需营养物质和发酵参数,且液体培养基的营养成分分布均匀,培养得到的茯苓菌丝体菌龄较齐,有利于提高茯苓质量可控性。[/font][font=宋体]综上,茯苓的液体发酵技术具有培养周期短、工艺易调控、可有效减轻菌种退化和大规模工业化生产等优势。相较于茯苓的固体发酵(树兜、段木、代料培养),液体发酵的优势体现在生产周期较短、获得的茯苓产品品质稳定可控,不受环境气候影响等优点,可有效解决野生茯苓资源逐渐枯竭和固体培养过程中成本高、质量不稳定等难题,减少茯苓培养对生态环境的影响。从长远来看,液体发酵方式有广阔的发展前景。 [/font]4 基于药材“四性”不同培养方式茯苓的综合评价[font=宋体]为满足茯苓逐年增长的市场需求,研究者开展了多元化培养模式的探索,但目前尚缺少对中药材科学且全面的评价体系,笔者提出了药材“四性”特征概念,即临床药效“三性”(安全性、有效性、质量可控性)及经济性,[/font][font=宋体]用于对茯苓培养过程、药材品质、临床药效等方面的综合评价。 [/font]4.1 [font=黑体]安全性[/font][font=宋体]安全性是中药材药用、食用的前提。药食两用物质因使用量和使用频率明显高于中药材,其安全问题更应被关注。茯苓在野外人工培养过程中,常因白蚁危害等问题喷洒毒死蜱、吡虫啉和氰戊菊酯等防白蚁低毒农药,而导致农药残留问题突出[/font][sup][37-40][/sup][font=宋体]。同时,茯苓加工厂为杀灭微生物和增加茯苓饮片的美观度[/font][sup][41][/sup][font=宋体],在炮制加工时会对茯苓进行硫磺熏蒸,而过度硫磺熏蒸会导致茯苓二氧化硫残留超标,危害人体健康。而液体发酵工艺易于控制,培养过程完全转变为工厂化生产,可规避白蚁危害,能有效解决农药残留的问题。同时,在培养过程中,注重无菌操作,严格控制微生物限量,可避免微生物污染等情况。 [/font]4.2 [font=黑体]有效性[/font][font=宋体]有效性是中药材及相关产品优劣的直观指标。研究发现茯苓中活性成分包括三萜类、多糖类、甾醇类、氨基酸和脂肪酸等,主要发挥活性的成分为三萜和多糖,其中三萜类化合物约有[/font]80[font=宋体]种,多糖类化合物有[/font]60[font=宋体]余种[/font][sup][5,42-46][/sup][font=宋体]。茯苓中多糖成分主要存在于茯苓的细胞壁中,具有较强的调节免疫、抑制肿瘤、抗炎和保护肝脏等作用[/font][sup][47-48][/sup][font=宋体]。根据茯苓多糖溶解度的不同,又将其分为水溶性多糖和碱溶性多糖,主要成分为葡聚糖,由主链[/font]β-1,3-[font=宋体]葡糖聚及少量支链[/font]β-1,6-[font=宋体]葡糖聚组成[/font][sup][49-51][/sup][font=宋体]。茯苓三萜类成分广泛分布于茯苓皮与菌核中。茯苓三萜类成分以羊毛甾型三萜为主,如茯苓酸、茯苓新酸和依布里酸等[/font][sup][52-53][/sup][font=宋体]。其中,茯苓酸为茯苓特有成分,是评估茯苓质量的化学标志物。[/font][font=宋体]杨祺等[/font][sup][54-55][/sup][font=宋体]开展了代料茯苓与传统松木培养茯苓质量的对比研究,结果表明代料茯苓总多糖和总三萜含量普遍高于传统松木培养茯苓。刑康康等[/font][sup][56][/sup][font=宋体]发现室内袋料培养茯苓的产量、结苓率、茯苓多糖含量等多项测定指标优于段木培养茯苓。[/font]Wang[font=宋体]等[/font][sup][57][/sup][font=宋体]研[/font][font=宋体]究报道菌丝体中的水提多糖和三萜类物质显著高于茯苓菌核。课题组前期在粉末显微特征、三萜类、多糖类、灰分和氨基酸含量等方面,对液体发酵茯苓和天然茯苓展开研究,发现发酵茯苓的氨基酸含量远高于天然培养茯苓[/font][sup][58-61][/sup][font=宋体]。在研究中发现[/font]4[font=宋体]种培养方式茯苓的总多糖含量从高到低依次为代料茯苓、段木茯苓、野生茯苓和发酵茯苓,发酵茯苓总多糖显著低于其他[/font]3[font=宋体]种茯苓;水溶性多糖和三萜类含量从高到低依次为发酵茯苓、代料茯苓、段木茯苓和野生茯苓,其中发酵茯苓含量较其他培养方式茯苓含量均高出数倍,代料茯苓和段木茯苓成分含量接近,无显著性差异。分析其原因在于野生茯苓、段木茯苓和代料茯苓均为固体发酵,药用部位为菌核;而液体茯苓的培养基与其他[/font]3[font=宋体]种培养方式的培养基显著不同,且其药用部位为
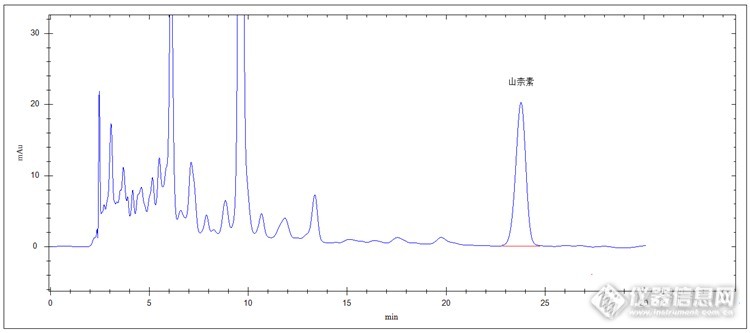
中药材红花高效液相色谱法检测 中药材红花为菊科植物红花的干燥花,夏季花由黄变红时采摘,阴干或晒干。 该药品具有活血通经、去瘀止痛、消肿润燥。用于治疗经闭、痛经、恶露不行、痈肿止痛、胸痹心痛、瘀滞腹痛,胸胁刺痛、跌打损伤、疮疡癥瘕、肌肉劳损、冠心病及多种妇科病等。 红花是生产多种药品的原材料,主要药物成分要严格控制。下面我们就采用高效液相色谱法对红花药材中重要成分羟基红花黄色素A和山柰素进行检测。 首先介绍下羟基红花黄色素A的检测。 对照品溶液制备:精密称取羟基红花黄色素A对照品5mg于50ml容量瓶中,加25%甲醇至刻度,配制成每0.1mg/ml羟基红花黄色素A对照品溶液,备用。 供试品溶液制备:取红花药材适量,充分粉碎后过三号筛(药典筛),精密称取过筛后粉末0.5g,置于具塞锥形瓶中,精密加入25%甲醇50ml,称定重量,超声处理40分钟,放冷,再次称定重量,用25%甲醇补足减少的重量,摇匀,0.45um有机相微膜滤过,待测。[/s
[size=20px][color=#93c6bc][b]鉴别[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [font=宋体][/font] [font=宋体]([/font]1[font=宋体])本品横切面:表皮细胞有时残留,[color=var(--weui-LINK)]木栓细胞[i][/i][/color]数列至[/font]10[font=宋体]余列。皮层由[/font]1[font=宋体]多层排列疏松的类圆形薄壁细胞组成。韧皮纤维断续排列成环。形成层明显。木质部射线单列;导管常单个散在,类圆形,呈放射状排列;木纤维较发达。髓部细胞壁略厚,木化。薄壁细胞含棕色物和[color=var(--weui-LINK)]草酸钙簇晶[i][/i][/color],簇晶棱角钝,直径[/font]18[font='MS Mincho']?[/font]80um[font=宋体]。[/font] [font=宋体]([/font]2[font=宋体])取本品粉末[/font]0. 5g[font=宋体],加乙醇[/font]30ml[font=宋体],加热回流[/font]1[font=宋体]小时,放冷,滤过,滤液浓缩至[/font]5ml[font=宋体],加水[/font]25ml[font=宋体],用乙酸乙酯振摇提取[/font]2[font=宋体]次,每次[/font]20ml[font=宋体],合并乙酸乙酯液,蒸干,残渣加甲醇[/font]1ml[font=宋体]使溶解,作为供试品溶液。另取桃枝对照药材[/font]0.5g[font=宋体],同法制成对照药材溶液。照薄层色谱法(通则[/font]0502[font=宋体])试验,吸取上述两种溶液各[/font]5[font='MS Mincho']?[/font]10μl[font=宋体],分别点于同一用[/font]4% [font=宋体][color=var(--weui-LINK)]醋酸钠溶液[i][/i][/color]制备的硅胶[/font]G[font=宋体]薄层板上,以甲苯[/font]-[font=宋体]乙酸乙酯[/font]-[font=宋体]甲酸([/font]5 : 4 : 1[font=宋体])为展开剂,展开,取出,晾干,喷以[/font]3%[font=宋体]三氯化铝乙醇溶液,置紫外光灯([/font]365nm[font=宋体])下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点。[/font] [font=宋体][/font] [size=20px][color=#93c6bc][b]检查[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [b][font=宋体][/font][/b] [color=black][b][/b][/color][b][font=宋体][color=black]水分[/color][/font][color=black] [/color][/b][color=black] [/color][font=宋体][color=black]不得过[/color][/font][color=black]15.0%[/color][font=宋体][color=black](通则[/color][/font][color=black]0832[/color][font=宋体][color=black]第二法)。[/color][/font] [b][font=宋体][color=black]总灰分[/color][/font][/b][color=black] [/color][font=宋体][color=black]不得过[/color][/font][color=black]2.0% [/color][font=宋体][color=black](通则[/color][/font][color=black]2302[/color][font=宋体][color=black])。[/color][/font] [font=宋体][color=black]【[b][color=var(--weui-LINK)]浸出物[i][/i][/color][/b]】[/color][/font][color=black] [/color][font=宋体][color=black]照醇溶性浸出物测定法(通则[/color][/font][color=black]2201[/color][font=宋体][color=black])项下的热浸法测定,用稀乙醇作溶剂,不得少于[/color][/font][color=black]5.0% [/color][font=宋体][color=black]。[/color][/font] [font=宋体][color=black] [/color][/font]
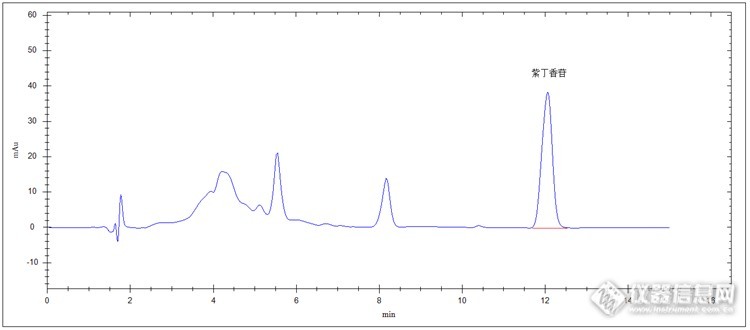
中药材刺五加检测 中药材刺五加为五加科植物刺五加的干燥根和根茎。可在春、秋二季采收,清水洗净,晒至干燥。 刺五加具有益气健脾、补肾安神、强身健体、补肾安神、延年益寿、安神醒脑功效。可用于治疗脾肺气虚、体虚乏力、食欲不振、腰膝酸软、肺肾两虚、久咳虚喘、腰膝酸痛、失眠多梦。另外对脑动脉硬化、脑血栓、脑栓塞、冠心病、神经衰弱、更年期等病症也有很好疗效。 刺五加药物功效很多,是很多药品生产的原材料,所以它中重要药物成分含量需要严格控制。下面我们介绍高效液相色谱法检测中药材刺五加中紫丁香苷含量实验。原理 取适量该粉末药材,加甲醇溶解,超声波超声提取,进样器进入高效液相色谱系统,由流动相带人C18色谱柱分离,紫外检测器检测,保留时间定性,峰面积定量(外标法)计算。仪器及试剂 仪器:高效液相色谱仪(紫外检测器+高压输液泵+柱温箱+自动进样器+在线脱气机等),超声波清洗仪,溶剂过滤器,电子天平,三号药典筛等。 试剂:甲醇(色谱纯),超纯水等。对照品溶液制备 精密称取紫丁香苷对照品2mg与25ml容量瓶中,加甲醇溶解并至刻度,配制成80μg/ml紫丁香苷对照品溶液,备用。供试品溶液制备 取刺五加药材适量,充分粉碎后过三号筛(药典筛),精密称取过筛后粉末2g于具塞锥形瓶中,精密加入甲醇25ml,称定重量,超声处理大约30分钟,放冷,再次称定重量,用甲醇补足减少的重量,摇匀,0.45um有机相微膜滤过,待测。色谱条件检测器:紫外检测器色谱柱:pGrandsil-STC-C18,4.6 X 250mm,5μm流动相:甲醇-水(25:75)检测波长:265 nm流速:1.0 mL/min柱温:30℃进样量:10ul对照品色谱图: http://ng1.17img.cn/bbsfiles/images/2014/12/201412282227_529738_2498430_3.png供试品色谱图:http://ng1.17img.cn/bbsfiles
【作者】 刘竹青; 张清波; 姜文红;【机构】 黑龙江省药品检验所; 黑龙江省药品检验所 黑龙江哈尔滨150001; 黑龙江哈尔滨150001;【摘要】 目的:建立通脉刺五加胶囊中金丝桃苷的高效液相含量测定的方法。方法:采用Diamonsil C18(250mm×4.6mm,5μm)色谱柱,流动相为乙腈-水-甲酸(16:84:0.5),检测波长360nm。结果:金丝桃苷在0.2008~2.008μg范围内有良好的线性关系(r=0.9998),平均回收率为97.3%。结论:本法操作简便、快速、准确,可用于通脉刺五加胶囊中金丝桃苷的含量测定。 更多还原【关键词】 通脉刺五加胶囊; 刺五加; 金丝桃苷; 高效液相; http://ng1.17img.cn/bbsfiles/images/2012/08/201208061734_381986_2352694_3.jpg
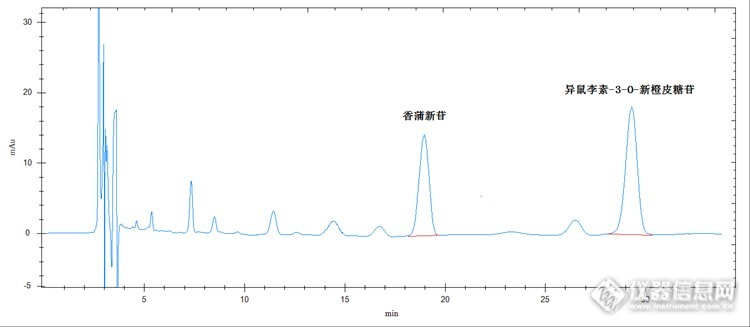
好药材不怕检,蒲黄药材接着检 蒲黄药材为香蒲科植物狭叶香蒲、宽叶香蒲、东方香蒲和长苞香的花粉,具有止血,化瘀,通淋功效。用于吐血,衄血,咯血,崩漏,外伤出血,经闭痛经,脘腹刺痛,跌扑肿痛,血淋涩痛效果较好。实验部分原理 取适量该药材,加甲醇溶解,加热回流或超声波提取,经进样系统进样,色谱柱分离,紫外检测器检测,保留时间定性,峰面积定量计算。仪器及试剂 仪器:高效液相色谱仪(紫外检测器),柱温箱,超声波清洗仪,溶剂过滤器,针筒式过滤器,加热回流装置,电子天平 试剂:甲醇(色谱纯),超纯水样品制备 对照品溶液的制备:精密称取异鼠李素-3-O-新橙皮糖苷、香蒲新苷对照品适量,加甲醇配制成浓度均为50μg/ml的对照品溶液,备用。 供试品溶液的制备:精密称取本品约0.5g,置具塞锥形瓶中,精密加入50ml甲醇后,称定重量并记录,冷浸12小时后加热回流1小时(或超声波超声30min),放冷,再次称定重量,用甲醇补足减少的重量,摇匀,滤过,待测。色谱条件检测器:紫外检测器色谱柱:C18,4.6 X 250mm,5μm流动相:乙腈:0.05%磷酸溶液=15:85(V:V)检测波长:254nm进样量20μl柱温:室温对照品色谱图:http://ng1.17img.cn/bbsfiles/images/2014/10/201410192152_519002_2498430_3.png供试品色谱图:http://ng1.17img.cn/bbsfiles/images/2014/10/201410192153_519003_2498430_3.png 从以上色谱图我们可以看出样品出峰时间很晚,峰形也较差。下面我们换用一根耐酸性色谱柱,效果我们请看色谱图。对照品色谱图:http://ng1.17img.cn/bbsfiles/images/2014/10/201410192153_519004_2498430_3.png供试品色谱图:http://ng1.17img.cn/bbsfiles/images/2014/10/201410192153_519005_2498430_3.png 换了这根色谱柱,色谱图的峰形好了很多,出峰时间也明显有所提前,但保留时间还是有点晚。下面我们又把色谱柱温度调整了一下,调到了40℃,效果接着往下看。对照品色谱图:http://ng1.17img.cn/bbsfiles/images/2014/10/201410192153_519006_2498430_3.png供试品色谱图:http://ng1.17img.cn/bbsfiles/images/2014/10/201410231859_519702_2498430_3.png 当然保留时间还可以再缩短缩短(通过增加流动相中甲醇含量,或提高高压泵流速,或换用更高效更短的色谱柱),但供试品中异鼠李素-3-O-新橙皮糖苷的附近有一个干扰物,为了保证分离度,这个分析时间已经比较合理,不要再缩短了。 检测蒲黄药材的这个方法到现在已经很完美了。但有几点事项需要注意。1.样品若采用超声波超声提取,为了保证提取效果有时得增加超声时间或超声波水域温度。2.检测这个样品最好要选择一款效果好的色谱柱,如耐酸性的色谱柱。3.为了缩短检测时间我们可以升高色谱柱的温度,对于这个样品效果就挺好。当然适当增加流动相中甲醇含量或增加高压泵流速,或换用更高效更短的色谱柱也能达到比较理想的效果。
按照药典规定的,展开剂:氯仿-醋酸乙酯-丙酮-甲酸=6:2.5:2.5:0.21为原儿茶酸对照品2药材对照品3、4、5均为制成的中药制剂供试品。我已经增大浓度试过了,色谱图无差异[img=,641,827]https://ng1.17img.cn/bbsfiles/images/2019/08/201908140947125804_8826_1791505_3.jpg!w641x827.jpg[/img]
建立一种新的中药材鉴定与分析方法,我们采用粉末X射线衍射分析技术,分别对19个不同来源的栀子样品进行实验分析研究。利用粉末X射线衍射傅立叶(Fourier)指纹图谱分析方法,获得栀子与水栀子等中药材的各自对照衍射图谱和特征标记峰值。使用对照衍射图谱和特征标记峰值可以很好地区分道地中药材栀子、药材栀子变种-水栀子及地方习用品-黄花栀子。分析结果表明,粉末X射线衍射Fourier指纹图谱分析方法可以用于传统中药材的鉴定与质量控制。
问题: 麻烦各位大师,药典上要求一个药材两个波长,检测两个对照品混合液。计算的时候应该怎么计算?回复: 分别各个波长的处理图谱,分别算