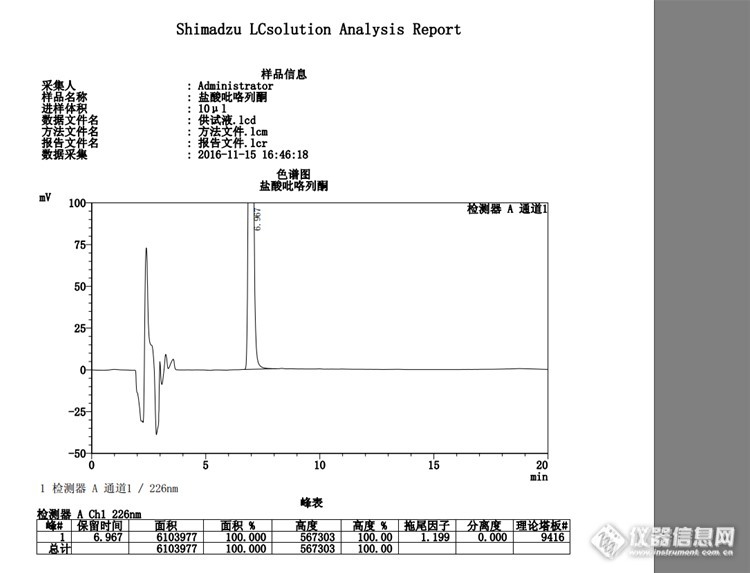
迎接2017年,原创1-Welchrom® C18测定盐酸比格列酮有关物质色谱柱sn:W13211841,pn:00310-02041(5μm,150mm×4.6mm)色谱条件自拟:流动相为乙腈-0.1M醋酸铵溶液(50:50),用醋酸调节pH值至5.0,检测波长为226nm,进样量为10μl,分析时间约为20分钟。操作:取本品适量置20ml容量瓶中,加流动相适量使溶解并稀释制成每1ml约含盐酸比格列酮0.5mg的溶液作为供试液,精密量取1ml,置100ml量瓶中,加流动相稀释至刻度,摇匀,作为对照溶液。本品空白溶剂为流动相。盐酸比格列酮简介药品名称: 盐酸吡格列酮别名:安可妥;盐酸匹格列酮;盐酸吡格列酮;盐酸皮格列酮;匹格列酮盐酸盐英文: Pioglitazone Hydrochloride;ACTOS中文化学名(±)5-苄基]-2,4-噻烷二酮盐酸盐剂型: 原料药性质:外观 白色晶体粉末熔程 193-194℃可溶性:在甲醇中溶解,在乙醇、氯仿中微溶分子式:C19H20N2O3S·HCl分子量:392.90CAS号:112529-15-4用途:新一代二型糖尿病治疗药,副作用小。本品主要成分是盐酸吡格列酮,其化学名称为(±)-5--苯甲基]噻唑烷-2,4-二酮单盐酸盐结构式:[url=http://p1.qhmsg.com/t01f3c03f21df4dc8b0.jpg][img]http://p1.qhmsg.com/dr/220__/t01f3c03f21df4dc8b0.jpg[/img]分子式:C19H20N203S·HCl分子量:392.90本品主要检测有关物质:其典型色谱图如下:空白溶剂:[img=,690,597]http://ng1.17img.cn/bbsfiles/images/2017/01/201701012253_01_1621890_3.png[/img]对照溶液:[img=,690,640]http://ng1.17img.cn/bbsfiles/images/2017/01/201701012254_01_1621890_3.png[/img]供试液:[img=,690,527]http://ng1.17img.cn/bbsfiles/images/2017/01/201701012256_01_1621890_3.png[/img]总结:现在该药品正在处于摸索阶段,结果显示本品较为“干净”,到底干净是否,要等组织长期的调查,我们相信群众的眼睛的,目前色谱数据较为理想,月旭的色谱柱的柱效较高均达到了9000,拖尾因子均小于1.3。一般我们在进行新的项目摸索方法的时候也在摸索色谱柱,初步确认该品种用月旭这款色谱柱较为理想。
三黄片的实验条件:乙腈:水(1:1)(每1000ml中加磷酸二氢钾3.4g,十二烷基硫酸钠1.7g)流动相,波长265nm,对照品的峰面积不稳定,每五针的RSD值大于2%。且样品的峰面积稳定是什么原因?对盐酸小檗碱发生变化。对照品的溶剂是甲醇。
方法:HPLC基质:标准溶液应用编号:103771化合物:盐酸曲唑酮固定相:Platisil ODS色谱柱/前处理小柱:Platisil ODS 5u 250 x 4.6 mm样品前处理:供试品:0.1g+60mL溶剂,震摇30min,溶剂定容到100mL。对照:供试品用溶剂稀释500倍。 注:溶剂为水:乙腈:二乙胺=650:350:0.4色谱条件:色谱柱: Platisil ODS 250*4.6 mm,5 μm(Cat#:99503) 流动相: 水:乙腈:二乙胺=320:680:0.4 流速: 1.5 mL/min 柱温: 40℃ 检测器: 254nm 进样量: 20μL文章出处:天津应用实验室关键字:盐酸曲唑酮、Platisil ODS、HPLC摘要:Platisil ODS检测盐酸曲唑酮。谱图:http://www.dikma.com.cn/u/image/2016/08/25/1472109147984782.pnghttp://www.dikma.com.cn/u/image/2016/08/25/1472109151321447.png
做个试验 想要盐酸贝那普利的对照品图,还有说两个光谱一致的依据是什么,全波数都对上? 包括指纹区?
有谁跑过盐酸组氨酸的薄板,对照溶液为自身样品溶液(50mg/ml)稀释而成(0.1mg/ml),以正丁醇-丙酮-浓氨溶液-水(10:10:5:2)为展开剂。显色后发现对照的斑点位置高于供试品。按说自身对照的话,Rf值应该是一样的啊,请问各位大虾,这是怎么回事啊?[em53] [em53]
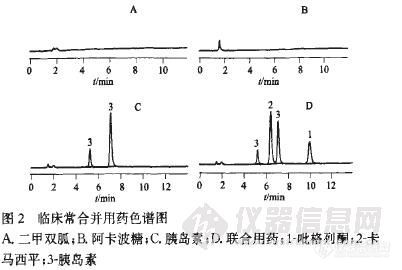
【作者】 方昱; 张虹; 李英;【机构】 同济大学附属同济医院;【摘要】 目的:建立高效液相色谱法测定人血浆中盐酸吡格列酮浓度的方法。方法:以卡马西平为内标,血浆样品用醋酸乙酯萃取,采用Diamonsil(TM)C18柱(250mm×4.6mm,5μm)分析。流动相为乙腈-0.05mol.L-1磷酸二氢钾(pH6.5)(42∶58),流速1.2mL.min-1,检测波长229nm,柱温35℃。结果:本法在0.025~4.0mg.L-1间线性关系良好,r=0.999 9,RSD为2.08%,(n=6),最低检测质量浓度为0.02mg.L-1。日内、日间精密度RSD均小于10%,低、中、高浓度的提取回收率均大于99%(n=5)。结论:此方法灵敏度高、重复性好,尤其适用于临床治疗合并用药时的药物浓度监测。【谱图】
如题,俺第一次测盐酸左氧氟沙星,做有关物质时杂质A与左氧保留时间完全重叠,排除了乙酸铵、高氯酸钠等试剂滴原因,实在没辙咧,请教大虾帮忙。盐酸左氧氟沙星有关物质测定方法(来源:中国药典2010年版第一增补本): 有关物质 取本品,精密称定,加0.lmol/L盐酸溶液溶解并定量稀释制成每1ml中约含1.2mg的溶液,作为供试品溶液,精密量取适量,用0.1mol/L盐酸溶液定量稀释制成每1ml中含2.4ug的溶液,作为对照溶液。另精密称取杂质A对照品约18mg,置100ml量瓶中,加6mol/L氨溶液1ml与水适量使溶解,用水稀释至刻度,摇匀,精密量取2ml,置100ml量瓶中,用水稀释至刻度,摇匀,作为杂质A对照品溶液。照高效液相色谱法(附录V D)测定,用十八烷基硅烷键合硅胶为填充剂;以醋酸铵高氯酸钠溶液(取醋酸铵4.0g和高氯酸钠7.0g,加水1300ml使溶解,用磷酸调节pH值至2.2)-乙腈(85 :15)为流动相A,乙腈为流动相B;按下表进行线性梯度洗脱。柱温为40°C;流速为每分钟1ml。称取左氧氟沙星对照品、环丙沙星对照品和杂质E对照品各适量,加0.1mol/L盐酸溶液溶解并稀释制成每1ml中约含左氧氟沙星1.2mg、环丙沙星和杂质E各6ug的混合溶液,取10ul注人液相色谱仪,以294nm为检测波长,记录色谱图,左氧氟沙星峰的保留时间约为15分钟。左氧氟沙星峰与杂质E峰和左氧氟沙星峰与环丙沙星峰的分离度应分别大于2.0与2.5。量取对照溶液10ul注人液相色谱仪,以294mn为检测波长,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的20%。精密量取供试品溶液、对照溶液和杂质A对照品溶液各10ul,分别注人液相色谱仪,以294nm和238nm为检测波长,记录色谱图。供试品溶液色谱图中如有杂质峰,杂质A(238nm检测)按外标法以峰面积计算,不得过0.3%。其他单个杂质(294nm检测)峰面积不得大于对照溶液主峰面积(0.2%),其他各杂质(294nm检测)峰面积的和不得大于对照溶液主峰面积的2.5倍(0.5%)。供试品溶液色谱图中任何小于对照溶液主峰面积0.1倍的峰可忽略不计。时间(分钟) 流动相A(%) 流动相B(%) 0 100 0 18 100 0 25 70 30 39 70 30 40 100 0 50 100 0
不知哪位做过半胱氨酸盐酸盐的其他氨基酸。供试品溶液的制备 :取本品,加2%N-乙基顺丁烯二酰亚胺溶液制成每1ml中含4mg的溶液,作为供试品溶液;对照液的制备:另精密称取胱氨酸对照品10mg,加0.1mol/L盐酸溶液3ml,超声,加水适量使溶解,并加水使成100ml,摇匀,精密量取1ml,加2%N-乙基顺丁烯二酰亚胺溶液4ml,摇匀,作为对照品溶液。这里要问为什么对照液不直接拿供试品溶液稀释呢?而用胱氨酸对照品呢??不明白[em06] [em06]
http://www.greenherbs.com.cn/bbs/dispbbs.asp?boardid=2&Id=7691601521 二类残留溶剂-1,4-二氧;六环 Residual Solvent Class 2 - 1,4-Dioxane 对照品/标准品1601500 二类残留溶剂-N,N-二甲基酰胺 Residual Solvent Class 2 - N,N-Dimethylformamide 对照品/标准品1601485 二类残留溶剂-N,N-二甲基乙酰胺 Residual Solvent Class 2 - N,N-Dimethylacetamide 对照品/标准品1601463 二类残留溶剂-1,2-二甲氧基乙烷 Residual Solvent Class 2 - 1,2-Dimethoxyethane 对照品/标准品1601441 二类残留溶剂-二氯甲烷 Residual Solvent Class 2 -Methylene Chloride 对照品/标准品1601420 二类残留溶剂- 1,2- 二氯乙烯 Residual Solvent Class 2 - 1,2-Dichloroethene 对照品/标准品1601408 二类残留溶剂-环己烷 Residual Solvent Class 2 - Cyclohexane 对照品/标准品1601383 二类残留溶剂-氯仿 Residual Solvent Class 2 -Chloroform 对照品/标准品1601361 二类残留溶剂-氯苯 Residual Solvent Class 2 - Chlorobenzene 对照品/标准品1601340 二类残留溶剂-乙腈 Residual Solvent Class 2 -Acetonitrile 对照品/标准品1601306 二类残留溶剂-混合物 C Residual Solvent Class 2 - Mixture C 对照品/标准品1601292 二类残留溶剂-混合物 B Residual Solvents Class 2 - Mixture B 对照品/标准品1601281 二类残留溶剂-混合物 A Residual Solvents Class 2 Mixture A 对照品/标准品1601226 一类残留溶剂- 1,1,1- 三氯乙烷 Residual Solvent Class 1 -1,1,1 对照品/标准品1601204 一类残留溶剂- 1,1- 二氯乙烯 Residual Solvent Class 1 -1,1-Dichlo 对照品/标准品1601180 一类残留溶剂- 1,2- 二氯乙烷 Residual Solvent Class 1 -1,2-Dichlo 对照品/标准品1601168 一类残留溶剂-四氯化碳 Residual Solvent Class 1 -Carbon Tetrachloride 对照品/标准品1601146 一类残留溶剂-甲苯 Residual Solvent Class 1- Benzene 对照品/标准品1601102 一类残留溶剂混合物 Residual Solvents Mixture Class 对照品/标准品1601000 利血平 Reserpine 对照品/标准品1600846 瑞格列奈杂质C Repaglinide Related Compound C 对照品/标准品1600835 瑞格列奈杂质B Repaglinide Related Compound B 对照品/标准品1600824 瑞格列奈杂质A Repaglinide Related Compound A 对照品/标准品1600813 瑞格列奈 Repaglinide 对照品/标准品1600121 瑞鲍迪甙 A Rebaudioside A 对照品/标准品1599500 红车轴草提取粉 Powdered Red Clover Extract 对照品/标准品1599000 萝芙碱 Rauwolfia Serpentina 对照品/标准品1598802 树莓酒 Raspberry Alcohol 对照品/标准品1598700 雷尼替丁杂质C Ranitidine Related Compound C 对照品/标准品1598609 雷尼替丁杂质B Ranitidine Related Compound B 对照品/标准品1598507 雷尼替丁杂质A Ranitidine Related Compound A 对照品/标准品1598450 雷尼替丁分离度用混合物 Ranitidine Resolution Mixture 对照品/标准品1598405 盐酸雷尼替丁 Ranitidine Hydrochloride 对照品/标准品1598347 雷米普利杂质D (二酮哌嗪雷米普利)Ramipril Related Compound D 对照品/标准品1598338 雷米普利杂质C Ramipril Related Compound C 对照品/标准品1598323 雷米普利杂质B Ramipril Related Compound B 对照品/标准品1598314 雷米普利杂质A Ramipril Related Compound A 对照品/标准品1598303 雷米普利 Ramipril 对照品/标准品1598201 盐酸雷洛昔芬 Raloxifene Hydrochloride 对照品/标准品1598008 3- 奎宁环基 3-Quinuclidinyl Benzilate 对照品/标准品1597504 奎宁酮 Quininone 对照品/标准品1597005 硫酸奎宁 Quinine Sulfate 对照品/标准品1596807 二水合盐酸奎宁 Quinine Hydrochloride Dihydrate 对照品/标准品1595509 硫酸奎尼丁 Quinidine Sulfate 对照品/标准品1595000 葡萄糖酸奎尼丁 Quinidine Gluconate 对照品/标准品1594506 金鸡纳酸 Quinic Acid 对照品/标准品1594007 喹乙宗 Quinethazone 对照品/标准品1593423 喹那普利杂质 B Quinapril Related Compound B 对照品/标准品1593412 喹那普利杂质 A Quinapril Related Compound A 对照品/标准品1593401 盐酸喹那普利 Quinapril Hydrochloride 对照品/标准品1593004 盐酸米帕林 Quinacrine Hydrochloride 对照品/标准品1592409 槲皮素 Quercetin 对照品/标准品1592227 夸西泮杂质 A Quazepam Related Compound A 对照品/标准品1592205 夸西泮CIV Quazepam CIV 对照品/标准品1592001 恩波吡维铵 Pyrvinium Pamoate 对照品/标准品1589109 丙酮酸 Pyruvic Acid 对照品/标准品1589007 乙胺嘧啶 Pyrimethamine 对照品/标准品1588004 马来酸吡拉明 Pyrilamine Maleate 对照品/标准品
请问谁做过这个药品的含量,谁知道为什么要用氮气吹干呀,没有氮气自然干燥给以吗???[font=SimSun][size=4][size=2][font=宋体] 色谱条件与系统适用性试验 用十八烷基硅烷键合硅胶为填充剂;以0.01mol/L磷酸氢二铵溶液(用磷酸调节pH值至7.O)-乙腈(50:50)为流动[/font][/size][/size][font=SimSun][size=3]相;检测波长为248nm。取盐酸氨溴索对照品约5mg,加甲醇0.2ml溶解,再加甲醛溶液(1→100)401,摇匀,置60℃加热5分钟,氮气吹干。残渣用水5ml溶解,再加流动相稀释至20ml,取20靗注入液相色谱仪,盐酸氨溴索与杂质B(相对保留时间约为0.8)的分离度应大于4.0。[/size][/font][/font][size=3][font=SimSun][size=2][font=宋体] 测定法 取本品20片,精密称定,研细,精密称取适量,加流动相溶解并定量稀释制成每lml中约含盐酸氨溴索30[/font][/size][size=2][font=宋体]靏[/font][/size][size=2][font=宋体]的溶液,滤过,精密量取续滤液[/font][/size][size=2][font=宋体]20[/font][/size][size=2][font=宋体]靗[/font][/size][size=2][font=宋体]注入液相色谱仪,记录色谱图;另取盐酸氨溴索对照品适量,精密称定,用流动相溶解并定量稀释制成每lml中约含30[/font][/size][size=2][font=宋体]靏[/font][/size][size=2][font=宋体]的溶液,同法测定。按外标法以峰[/font][/size][/font][size=2][font=宋体][font=SimSun]面积计算,即得。[/font][/font][/size][/size]
国家食药总局:警惕部分食品中违法添加“盐酸西布曲明”和“酚酞”一、背景信息 近期,食品药品监管部门发现有减肥类产品添加“盐酸西布曲明”和“酚酞”的违法行为,并对该违法行为进行了查处。“盐酸西布曲明”和“酚酞”究竟是什么?是否可添加到食品中?有何相关标准和法规?本期为您解读。 二、专家观点 (一)盐酸西布曲明曾为处方药,但目前已在全球大多数国家停止使用。 盐酸西布曲明(Sibutramine Hydrochloride)是西布曲明(Sibutramine)的氯化物,是一种中枢神经抑制药物,曾用于肥胖症的治疗。 盐酸西布曲明曾于1997年经美国食品药品监督管理局(FDA)批准上市,随后在欧盟、澳洲、加拿大、日本等多个国家获得批准上市,2000年在我国上市。 2009年12月,欧洲药品管理局(EMEA)发布研究报告显示,与安慰剂对照组相比,服用盐酸西布曲明的患者发生严重、非致死性心血管事件的风险增加。欧盟、英国等国家和地区先后停止使用盐酸西布曲明类药品。原国家食品药品监督管理局也组织相关专家对西布曲明在我国使用的安全性进行了评估,认为其减肥治疗的风险大于效益,并于2010年10月通知要求停止生产销售使用西布曲明制剂及原料药。目前盐酸西布曲明作为减肥药已在全球大多数国家停止使用。
所用对照品批号为110713-200911使用前无需任何处理,按含C20H18ClNO4为86.8%计,而我所检测的产品是以C20H18ClNO4.2H2O计,是不是最后结果得以1.097来折算??? http://bbs.sdatc.com/image/post/smile/26.gif
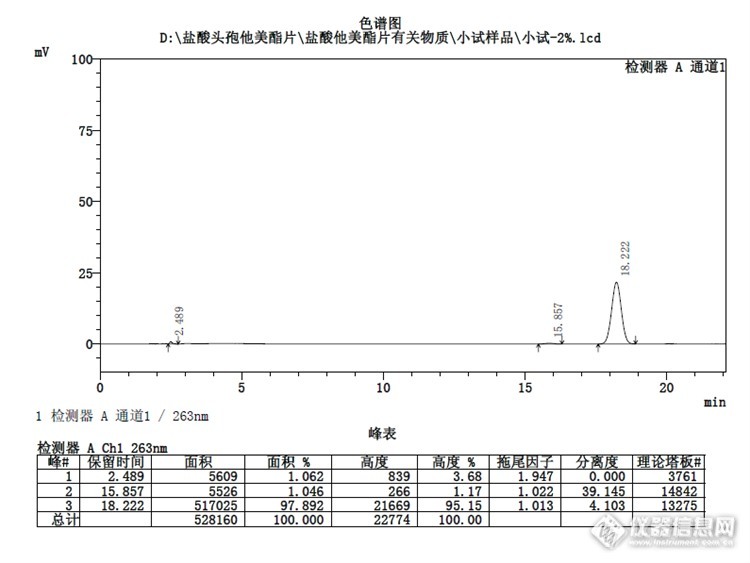
盐酸头孢他美酯是种广谱抗生素,可用于对它敏感细菌感染所引起的炎症。该产品为口服用。化学名:(6R,7R)-3-甲基-7-结构式:http://ng1.17img.cn/bbsfiles/images/2014/03/201403302127_494735_1621890_3.gif 英文名:Cefetamet Pivoxil Hydrochloride Tablets 药物别名:威锐片 成份:本品主要成分为盐酸头孢他美酯 性状:本品为薄膜衣片,除去包衣后呈白色、类白色,有引湿性。 药代动力学:本品单一剂量和多剂量的药代动力学参数基本一致。本品口服后,经过肠黏膜或首次经过肝脏时盐酸头孢他美酯被迅速代谢,在体内转变为头孢他美而发挥作用。本品随食物口服后,平均约55%的剂量转变为头孢他美。口服本品500mg后3~4小时,血药浓度达峰值4.1±0.7mg/L,分布容积为0.29L/kg,与细胞外水平一致。约22%头孢他美与清蛋白结合。年龄、肾脏及肝脏疾病对盐酸头孢他美酯的生物利用度无影响。抗酸剂(镁、铝、氢氧化物等)或雷尼替丁不改变本品生物利用度。本品90%以头孢他美形式随尿液排出,清除半衰期为2~3小时。肾衰竭患者,头孢他美的清除情况同肾功能成正比。 适应症:本品适用于敏感菌引起的下列感染:1.耳、鼻、喉部感染,如中耳炎、鼻窦炎、咽炎、扁桃体炎等。2.下呼吸道感染,如慢性支气管炎急性发作、急性气管炎、急性支气管炎等。3.泌尿系统感染,如非复杂性尿路感染、复杂性尿路感染(包括肾盂肾炎)、男性急性淋球菌性尿道炎等。注意事项 1.对青霉素类药物过敏者慎用。 2.若发生严重过敏反应,应立即停药,并紧急治疗。 3.在使用本品期间,由于肠道微生物的改变,可能导致伪膜性肠炎。若发生假膜性肠炎,应积极治疗(推荐使用万古毒素)。 4.本品应放到儿童触及不到的地方。 孕妇及哺乳期妇女用药:1.由于缺乏有关人类胎儿的临床数据,妇女妊娠期间,不推荐使用本品。若有对该药敏感的微生物严重感染时,必须充分权衡利弊。2.在乳汁中尚未发现本品的代谢物。 儿童用药:本品对新生儿的有效性和安全性尚无可靠的临床数据。 药物相互作用: 抗酸剂,H2受体拮抗剂对本品的药代动力学无影响。目前尚未见到本品对实验室检测值和/或方法有影响的报道,也未观察到伴随利尿药治疗的患者在使用本品时对肾功能的损伤。 药物过量: 若过量服用,发生严重反应,应洗胃,并采取对应治疗。 贮藏:遮光、密封、在干燥处保存。详见:http://baike.so.com/doc/6048874.html该品种国内批准文号有40个,见国家药监局网。截图如下:http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_646694_1621890_3.png试验条件:主要参照中国药典2010年版二部。用十八烷基硅烷键合硅胶为填充剂;以乙腈-甲醇-水-磷酸盐缓冲液(取无水磷酸氢二钠5.8g与磷酸二氢钾3.5g,加水溶解并稀释成1000ml)(360:95:500:45)为流动相;检测波长为263nm。取头孢他美酸和头孢他美酯对照品适量,用乙腈溶液(9→20)溶解并稀释制成每1ml中约含头孢他美酸0.05mg和含头孢他美酯1.4mg的混合溶液,取10μl注入液相色谱仪,头孢他美酯峰与头孢他美酸峰的分离度应不小于28.0,头孢他美酯峰与其相对保留时间约为0.9和1.1处杂质峰的分离度均应大于于2.0,理论板数按头孢他美酯峰计算不低于3000。取本品的细粉适量,加乙腈溶液(9→20)溶解并定量稀释制成每1ml中约含头孢他美1.0mg的溶液,滤过,取续滤液作为供试品溶液;精密量取供试品溶液适量,用乙腈溶液(9→20)定量稀释制成每1ml中约含头孢他美20μg的溶液,作为对照溶液。照含量项下的色谱条件,取对照溶液10μl注入液相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的25%;再精密量取供试品溶液与对照溶液各10μl,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的4.5倍。供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积(2.0%),各杂质峰面积的和不得大于对照溶液主峰面积的2.5倍(5.0%)。色谱柱信息:月旭Welchrom C18, 5μm, 4.6×250mm(货号:00310-02043;序列号:w13211564)试验图谱:1.系统适用性溶液:http://ng1.17img.cn/bbsfiles/images/2014/03/201403302057_494730_1621890_3.png2.供试品溶液:http://ng1.17img.cn/bbsfiles/images/2014/03/201403302112_494732_1621890_3.png3.对照溶液:http://ng1.17img.cn/bbsfiles/images/2014/03/201403302121_494734_1621890_3.png
我用高效液相色谱法测盐酸赖氨酸含量时,色谱柱:Agilent 氨基键合硅胶柱 250×4.6mm, 5μm,以0.05mol/L磷酸二氢钾溶液-乙腈溶液〔乙腈-水(10:1)〕(30:70)为流动相,检测波长为203nm,对照品不出峰,有经验的同学指导下啊!
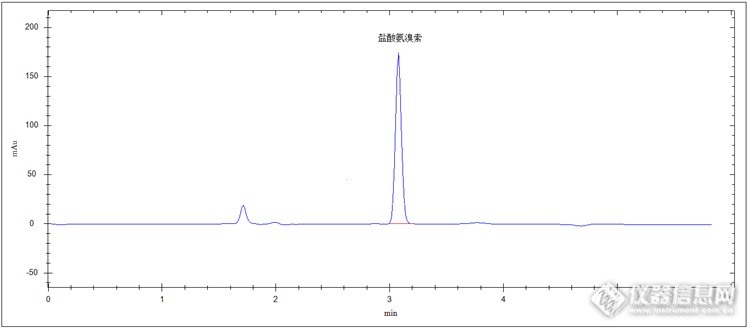
盐酸氨溴索片超快速检测 盐酸氨溴索片是一种良好的祛痰药,具有促进粘液排除作用及溶解分泌物的特性,有良好的祛痰及润滑呼吸道功效,并可促进肺表面物质的活性等药效。对于咳嗽、痰多、急慢性呼吸道疾病、支气管分泌异常等症状的治疗效果显著。 盐酸氨溴索片中主要药物成分为盐酸氨溴索,药物的品质和该物质在该药物中的含量有着直接的关系,所以该药品中该药物成分的检测不可小觑。 下面我们就来介绍高效液相色谱法检测盐酸氨溴索片中盐酸氨溴索含量。 对照品溶液的制备: 精密称取盐酸氨溴索对照品7.5mg于具塞离心管中,加甲醇0.2ml溶解,再加甲醛溶液40μl,摇匀,置于60℃恒温水域中加热5分钟,氮吹仪吹干。残渣用5ml水充分溶解,后置于25ml容量瓶中,加流动相稀释至刻度,制成300μg/ml对照品溶液,备用。 准确量取盐酸氨溴索对照品溶液2.5ml于25ml容量瓶中,加流动相溶解至刻度,制成30μg/1ml对照品溶液(命名为工作液),备用。 供试品溶液的制备: 取该样品适量,充分研碎,精密称取1.5mg于50ml容量瓶中,加流动相溶解并定容至刻度,0.45μm微膜滤过,待测。色谱条件:检测器:紫外检测器色谱柱:pGrandsil-STC C18,4.6 X 150mm,5μm检测波长:248nm流动相:0.01mol/L磷酸氢二铵溶液(用磷酸调节pH值至7.0)-乙腈(40:60)流速:1.0 mLmin
[size=3]以下是2010年版药典二部中关于盐酸小檗碱中有关物质检查的描述:[检查]有关物质 取本品适量,精密称定,加流动相溶解并定量稀释制成每1ml中含1mg的溶液,作为供试品溶液;另取盐酸药根碱对照品和盐酸巴马汀对照品适量,精密称定,加流动相溶解并定量稀释制成每1ml中含0.1mg的溶液,分别作为对照品溶液(1)和(2);精密量取供试品溶液2ml和对照品溶液(1)和(2)各10ml,置100ml量瓶中,用流动相稀释至刻度,摇匀,作为对照溶液;取对照品溶液(2)1ml,用供试品溶液稀释至10ml,摇匀,作为系统适用性试验溶液。照高效液相色谱法(附录V D)试验,用十八烷基硅烷键合硅烷为填充剂;以0.01mol/L磷酸二氢铵溶液(用磷酸调节pH值至2.8)-乙腈(75:25)为流动相;检测波长为345nm。取系统适用性试验溶液10ul,注入液相色谱仪,巴马汀峰与小檗碱峰间的分离度应符合要求。另取对照溶液10ul,注入液相色谱仪,调节检测灵敏度,使小檗碱色谱峰的峰高约为满量程的25%。精密量取对照溶液与供试品溶液各10ul,分别注入液相色谱仪,记录色谱图至主成分色谱峰保留时间的2倍。供试品溶液的色谱图中,如有与药根碱峰和巴马汀峰保留时间一致的色谱峰,按外标法以峰面积计算,均不得过1.0%;[color=#fe2419]其他杂质峰面积的和不得大于对照溶液中小檗碱峰的峰面积(2.0%)。[/color]我的问题是:最后一句是什么意思?为什么供试品溶液色谱图中的其他杂质峰与对照溶液色谱图中的小檗碱峰面积进行比较?而不在一张色谱图内比较?如果按上面说,我们的结果是50%以上;而最后的括号中的2.0%是什么意思?[/size]
HPLC法测定盐酸小檗碱时含量偏高,请教盐酸小檗碱含量对照品的处理方法及纯度!!!
益母草与川芎是中药成方制剂中配伍应用频率较高的药对,益母草主要含水苏碱等生物碱类活性成分,川芎主要含阿魏酸等活性成分。对益母草药材及其制剂《中国药典》常以雷氏盐剩余比色法测定益母草总碱含量。在对含益母草及川芎这一药对的制剂进行质量控制时,由于川芎所含生物碱也能与雷氏盐反应生成沉淀,且雷氏盐剩余比色法本身重现性较差,故不宜采用该法。为此,本实验建立了以薄层扫描法测定益母草与川芎合煎液中盐酸水苏碱含量的方法,为制订含有益母草与川芎药对制剂的质量标准提供参考。 1 仪器与试药 CS-9000型双波长薄层扫描仪(日本岛津):939薄层制板器(重庆南岸贝尔德仪器技术厂);定量毛细管(Drummond USA)。盐酸水苏碱对照品(中国药品生物制品检定所,712200105);益母草、川芎(购于安徽毫州)。硅胶G(化学纯,青岛市北区海化干燥剂厂);强酸性阳离子交换树脂(732型,上海化学试剂采购供应站);其余试剂均为分析纯。 2 方法与结果 2.1 益母草与川芎合煎液的制备 取药材100g(益母草-川芎:1:1),加水煎煮2次,每次2h,每次加12倍量水,合并煎液,滤过,滤液浓缩并定容至100mL,即得合煎液样品。 2.2 对照品溶液的制备 取105℃干燥至恒重的盐酸水苏碱对照品适量,精密称定,加乙醇溶解定容,制成1.2mg/mL的对照品溶液。 2.3 供试品溶液的制备 取合煎液样品适量,离心(4O00r/min)5min后,精密量取上清液lmL置小烧杯中,加蒸馏水1OmL,用稀盐酸调pH 1~2,通过已处理好的强酸性阳离子交换树脂柱(内径1cm,长1Ocm)用水洗至流出液无色,弃去水液,再以乙醇-氨水(8:2)150mL洗脱,收集洗脱液,蒸干,残渣加乙醇溶解,定量转移并定容于lmL容量瓶中,摇匀,作为供试品溶液。 2.4 薄层色谱与扫描条件 吸附剂:硅胶G-O.5%CMC-Na薄层板(厚约0.5mm,105℃活化lh,置干燥器中备用):展开剂:丙酮可-无水乙醇-盐酸(10:6:1) :显色剂:喷以改良碘化铋钾-1%FeC13无水乙醇液(5:1)。,冷风吹至斑点显色清晰。 描方式:双波长反射式锯齿扫描:检测波长:λs=525nm,λR=660nm:狭缝:0.4mm×0.4mm: 线形参数SX=3。 2.5 标准曲线的制备 分别精密吸取盐酸水苏碱对照品溶液4.0、6.0、8.0、10.0、12.0μL,分别点于同一薄层板 ,依上述条件展丌,显色,在薄层板上覆盖同样大小的玻璃板,周围用胶布吲定,然后扫描测定各斑点的峰面积积分值。以峰面积积分值(A)对点样量(C)进行回归,得回归方程:A=-37152.7+7579.18C‘r=O.9986。表明在4.8~14.4μg范围内盐酸水苏碱斑点峰面积积分值与点样量呈良好的线性关系。 2.6 稳定性考察 取供试品溶液5μL点样,依上述条件展开,显色,在1h内每隔10min扫描测定1次,结果斑点峰面积积分值RSD为4.6%(n=6),表明斑点在显色后1h内基本稳定。 2.7 精密度考察 精密吸取供试品溶液在同一薄层板上点相同量5点,每点5μL,按上述条件展开,显色,扫描测定,斑点峰面积秋分值RSD为1.33%(n=5),对其中一点连续扫描测定5次,斑点峰面积积分值RSD为0.62%(n=5),表明同板精密度和仪器精密度较好。 2.8 异板精密度试验 取薄层板3块,在每1块薄层板二分别点对照品溶液4、6μL及供试品溶液5μL,依法展开,显色,扫描测定,采用外标两点法计算含量。结果测得供试品溶液中水苏碱含量为1.1308 mg/mL(RSD=3.01%)。 2.9 回收率测定 精密量取已知含量的合煎液样品0.5mL,加入盐酸水苏碱对照品溶液0.5mL,混匀后,按2.3项方法制备供试品溶液。精密吸取供试液5μL,对照品溶液4、6μL,变又点样于同一薄层板上,按上述条件展开、显色、扫描测定,用外标两点法计算。 2.10 样品测定 取合煎液样品,按2.3项 方法制备供试品溶液。精密吸取供试品溶液5μL,对照品溶液4、6μL,分别交叉点于同一薄层板上,按上述条件展开,显色,扫描测定,用外标两点法计算样品中盐酸水苏碱的含量。 3 讨论 在供试品溶液制备中,以甲醇-氨水(8:2) 或乙醇-氨水(8:2) 作洗脱剂,提纯效果均较好。因乙醇比甲醇价廉且安全,建议采用乙醇-氨水(8:2)作为洗脱剂。本实验对洗脱剂用量考察结果表明,用14OmL即可将盐酸水苏碱洗脱完全。为了保证洗脱充分,本实验中确定用150mL洗脱。 盐酸水苏碱为水溶件物质,在薄层板上显色时受湿度影响很大。通过实验考察,优选出其较好的显色方式为:展开后,取出,晾干,丁105℃烘lOmin,再喷显色剂,冷风吹至斑点色清晰。 益母草有效成分水苏碱含量较低且波动大,容易造成含益母草的制剂有效成分低、产品质量不稳定 ,应增加水苏碱含量控制项目。本实验建立的含量测定方法可为制订含益母草及川芎制剂中水苏碱的定量标准提供参考。参考文献:[1]国家药典委员会.中国药典(一部)[S].北京:化学工业出版社,2000.237,455,564.[2]张玲,时延增,于宗渊,等.舣波长薄层扫描法测定益母草LJ服液中水苏碱的含量[J].中国药科大学学报,1996,27(1):16—18.[3]张玲, 宗渊,李国宝,等.7种含益母草中成药中水苏碱的含量测定[J].药物分析杂志,1996,16(3):181—183.
好长一段时间都买不到硫酸、盐酸和丙酮了,说是世博和亚运的原因。没有这些,实验室怎么做实验啊?其他实验室有没有出现这种情况呢?
盐酸二甲双胍格列本脲胶囊I有关物质按照15版药典配制双氰胺,三聚氰胺,和二甲双胍的出峰时间顺序是什么,求分享
前几天定的盐酸但拿到的送货单上却写着硝酸,想弱问下盐酸是管禁品吗?
盐酸应该怎么保存才是最好的呢?我们实验室条件有限,空间较小,只能与其它药品一同放在药品柜里。但我认为盐酸挥发性极强,容易污染其它药品,而且也容易腐蚀药品柜。大家是否有更好的保存方法呢?
求助,配制盐酸表小檗碱和盐酸黄连碱对照液时,发现其很难溶解,文献中溶剂用的甲醇或甲醇-盐酸,我试了,也很难溶,超声加热溶解性也不好,有什么办法可以帮助溶解啊?

盐酸二甲双胍格列本脲胶囊I有关物质按照2015版药典配制,三聚氰胺不出峰,色谱柱用的资生堂的。求各位大神指点一下[img]https://ng1.17img.cn/bbsfiles/images/2019/05/201905021326407220_6369_3384811_3.jpg[/img]
求助,配制盐酸表小檗碱和盐酸黄连碱对照液时,发现其很难溶解,文献中溶剂用的甲醇或甲醇-盐酸,我试了,也很难溶,超声加热溶解性也不好,有什么办法可以帮助溶解啊?
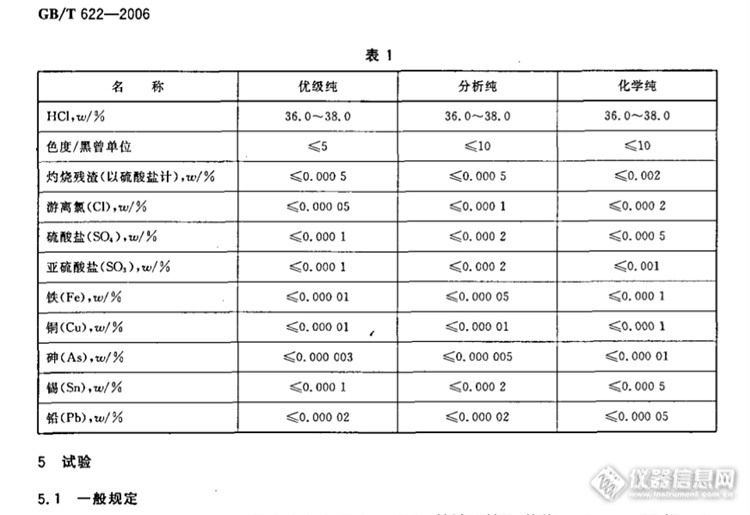
化学试剂盐酸与食品添加剂盐酸,如果从这两个名称来看,大家觉得哪一种盐酸会更好呢?或者说哪一种会更纯正一些呢?哪一个指标会更严格一些呢?不管你有答案,还是没答案,你看一下下面两个图的区别,或许你自己就找到答案了。http://ng1.17img.cn/bbsfiles/images/2014/03/201403151047_493283_1950135_3.jpghttp://ng1.17img.cn/bbsfiles/images/2014/03/201403151052_493286_1950135_3.jpg
哪位老师帮忙解答哈黄柏的供试品和对照药材不出点的问题啊?没有盐酸黄柏碱对应的点,急! [img=,690,920]https://ng1.17img.cn/bbsfiles/images/2021/02/202102281401144420_8460_4147998_3.png[/img]

盐酸多西环素注射液(IV)含量的测定实验部分:原理:精密量取处理好的样品及对照品,稀释后注入高效液相色谱系统,C18色谱柱分离,紫外检测器检测,外标法(保留时间定性、峰面积定量)计算,得出该样品中多西环素的含量。仪器及试剂仪器:安捷伦1100高效液相色谱仪,配置紫外检测器+等度泵+柱温箱+在线脱气机等电子天平(万分之一)试剂甲醇:色谱级 已睛:色谱级 草酸铵,二甲基甲酰胺,磷酸氢二铵,氨水,盐酸均为分析纯标准物质土霉素对照品(中国兽医药品监察所生产)土霉素(化学对照品)(中国食品药品检定研究所生产)美他环素(化学对照品)(中国食品药品检定研究所生产)-多西环素(化学对照品)(中国食品药品检定研究所生产)多西环素(化学对照品)(中国食品药品检定研究所生产)色谱条件:流动相:0.05mcl/l草酸铵溶液:二甲基甲酰胺:0.2mcl/l磷酸氢二铵溶液=65:30:5(ph=8.0)柱温:35℃ 检测波长:280nm流速:1.0ml/min进样量:20um对照品及样品的制备系统性试验:称取土霉素、美他霉素、-多西环素、多西环素对照品适量,加0.01mcl/l盐酸溶液溶解并稀释制成每1ml含土霉素、美他环素、多西环素及多西环素均加0.08mg的混合溶液。上机测定:理论塔板数n不低于1500,分离度R大于1.5样品的配制1.1盐酸多西环素注射液(IV)10ml:0.5g精密量取供试品1ml,置于50ml量瓶,加0.01mcl/l盐酸溶液溶解并稀释至刻度,摇匀。精密量取2ml,置于25ml量瓶中,加0.01 mcl/l盐酸溶液溶解并稀释至刻度,摇匀。1.2对照品溶液的制备(多西环素对照品含量为85.2%)精密称取多西环素对照品约25mg,置于25ml量瓶中,加入,加0.01 mcl/l盐酸溶液溶解并稀释至刻度,摇匀。精密量取2ml,置于25ml量瓶中,加0.01 mcl/l盐酸溶液溶解并稀释至刻度,摇匀色谱图系统性试验溶液色谱图 :http://ng1.17img.cn/bbsfiles/images/2015/09/201509281558_568305_2315779_3.pnghttp://ng1.17img.cn/bbsfiles/images/2015/09/201509281559_568307_2315779_3.pnghttp://ng1.17img.cn/bbsfiles/images/2015/09/201509281604_568308_2315779_3.pnghttp://ng1.17img.cn/bbsfiles/images/2015/09/201509281604_568309_2315779_3.png 图2标准品色谱图http://ng1.17img.cn/bbsfiles/images/2015/09/201509281607_568311_2315779_3.pnghttp://ng1.17img.cn/bbsfiles/images/2015/09/201509281607_568312_2315779_3.png 图3 被测样品色谱图计算及结果 样品中被测物含量计算公式:标示量%=http://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gifA—供试品中被测物峰面积值As—对照品中被测物峰面积值Ms—对照品的重量。单位为g.M—供试品的取样量。单位为mlCs—对照品的含量。85.2%。Ds—对照品的稀释倍数。D—供试品的稀释倍数。B—样品的标示量。经计算该兽药中多西环素含量为99.7%,含量合格,符合药典规定。 结论该方法对药典方法略作修改,得到不错的检测效果。由图1可以看出,该方法的系统实验,理论塔板数为1883,分离度为4.4,满足检测条件。
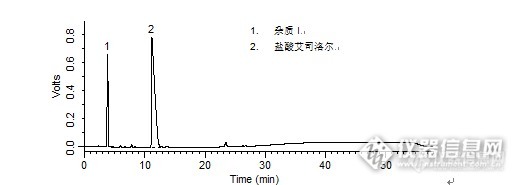
1. 杂质I2. 盐酸艾司洛尔 盐酸艾司洛尔样品制备 制备方法有关物质衍生溶液:取盐酸艾司洛尔对照品约10 mg,置10 mL量瓶中,加入1 mol/L盐酸溶液1 mL,放置30分钟,加1 mol/L的氢氧化钠溶液1 mL使中和,用流动相A 稀释至刻度,摇匀。分析条件 色谱柱Diamonsil C18(2) 250 x 4.6 mm,5 μm (Cat#:99603)流动相流动相A:乙腈:甲醇:磷酸盐缓冲液(取磷酸二氢钾3.0 g,加水至650 mL)=15:20:65流动相B:甲醇梯度流速1 mL/min柱温30 ℃检测器UV 222 nm进样量20 μL 色谱图有关物质衍生溶液http://ng1.17img.cn/bbsfiles/images/2016/04/201604211737_591070_708_3.png 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数 N USP拖尾因子 分离度 1 3.842 6280189 655879 2747.059 0.670 -- 2 11.157 29271705 784686 1512.532 5.026 10.154 本品种同时使用了SpursilC18色谱柱,在药典规定条件下进行检测,满足药典要求。
铜粉加入稀盐酸中,加热无现象,这时加入一种盐则铜粉溶解而溶液变蓝,同时有气体放出,这种盐是 ?