请问在哪能买到烷基葡糖苷:例如十二烷基葡糖苷?
请问十二烷氧基葡糖苷、十二烷基葡糖苷、聚乙二醇葡糖苷性能有什么不同?
本人对酶这种物质不甚了解http://simg.instrument.com.cn/bbs/images/brow/emyc1010.gif,特求助各位大侠?http://simg.instrument.com.cn/bbs/images/brow/em09511.gif应用搜索引擎没有找到β-葡糖醛酸糖苷酶,想知道这种酶是否还有别的名字?目前有β-葡糖苷酶(cas:9001-22-3),是否同一种酶?
β-Glucuronidase/aryl sulfatase β-葡萄糖醛酸酶\芳香基硫酸酯酶( 葡萄糖苷酸酶/硫酸芳酯酶 ) 标准品——检瘦肉精等用的除了北京希凯创新科技有限公司提供,还可以从哪里购买么?
β-Glucuronidase/aryl sulfatase β-葡萄糖醛酸酶\芳香基硫酸酯酶( 葡萄糖苷酸酶/硫酸芳酯酶 ) 标准品MERCK 1041140002
求助,我不太懂酶单位活性计算,我们需要30U/ml的溶液,之前买了2ml装的b-葡糖酸苷肽酶/芳基磺酸酯酶,使用时要不要稀释?
请问葡萄糖苷酶(EC3.2.1.21)和葡萄糖苷酸酶(EC3.2.1.31)有什么区别?分别的用途是什么?谢谢!
各位老师: 最近要检测绿咖啡豆中绿原酸,但是能够检测单绿原酸,不知道总绿原酸增么检测,是否可以使用单一的标准品定量所有的绿原酸吗?
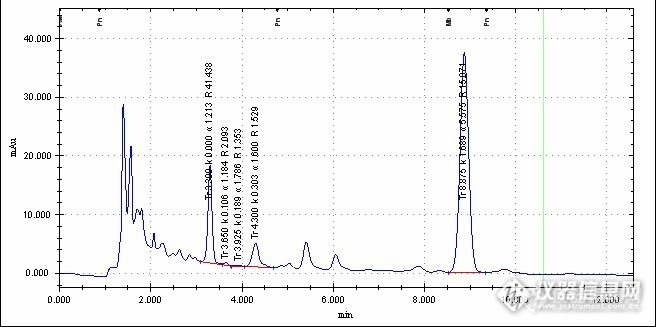
1 引言根据我国食品卫生法(1995年)的规定,食品添加剂是为改善食品色、香、味等品质,以及为防腐和加工工艺的需要而加入食品中的人工合成或者天然物质。苯甲酸可以用作食品、饲料、乳胶、牙膏的防腐剂。在酸性条件下,对霉菌、酵母和细菌均有抑制作用,但对产酸菌作用较弱。苯甲酸分子态的抑菌活性较离子态高,故PH小于4时,抑菌活性高,抑菌的最适pH值为2.5~4.0,一般以低于pH值4.5~5.0为宜。由于苯甲酸对水的溶解度低,故实际多是加适量的碳酸钠或碳酸氢钠,用90℃以上热水溶解,使其转化成苯甲酸钠钠后才添加到食品中。若必须使用苯甲酸,可先用适量乙醇溶解后再应用。由于苯甲酸对水的溶解度比苯甲酸钠低,因此在酸性食品中使用苯甲酸钠时,要注意防止由于苯甲酸钠转变成苯甲酸而造成沉淀和降低其使用效果。苯甲酸在酱油、清凉饮料中可与对-羟基苯甲酸酯类一起使用而增效。糖精,曾是一种饱受争议的甜味剂。研究人员曾对它做过一些动物实验,实验结果表明该物质具有致癌作用,因此FDA于1977年明令禁用该物质。但因餐饮行业(以及节食者)的坚持,糖精至今仍在市场上出售。但到了20世纪90年代末,包含糖精的产品包装上均贴有警告标签,指出糖精对实验室动物具有致癌作用。而美国热量控制委员会指出,人们不会像老鼠一样患上膀胱癌,因此,应该除去这个警告标签。在2000年,美国国会废除了相关法规,糖精产品不必进行健康警告标签。安赛蜜是一种食品添加剂,是化学品,类似于糖精,易溶于水,增加食品甜味的,没有营养,口感好,无热量,具有在人体内不代谢、不吸收(是中老年人、肥胖病人、糖尿病患者理想的甜味剂),对热和酸稳定性好等特点,是当前世界上第四代合成甜味剂。它和其它甜味剂混合使用能产生很强的协同效应,一般浓度下可增加甜度30%~50%。安赛蜜具有强烈甜味,甜度约为蔗糖的130倍,呈味性质与糖精相似。高浓度时有苦味。安赛蜜为人工合成甜味剂,经常食用合成甜味剂超标的食品会对人体的肝脏和神经系统造成危害,特别是对老人、孕妇、小孩危害更为严重。如果短时间内大量食用,会引起血小板减少导致急性大出血。咖啡因是一种黄嘌呤生物碱化合物,是一种中枢神经兴奋剂,能够暂时的驱走睡意并恢复精力,临床上用于治疗神经衰弱和昏迷复苏。有咖啡因成分的咖啡、茶、软饮料及能量饮料十分畅销,因此,咖啡因也是世界上最普遍被使用的精神药品。2 材料与方法2.1 材料2.1.1 材料与试剂空白可乐样品: 可口可乐原味(无咖啡因)(美国可口可乐公司); 样品: 可口可乐。苯甲酸钠; 糖精钠; 安赛蜜; 咖啡因;甲醇; 乙酸铵。2.1.2 仪器与设备Agilent 1260 高效液相色谱仪(美国安捷伦公司);天平; 离心机。2.2 实验方法2.2.1 标准品(1)标准储备液的配制精密称取苯甲酸钠、糖精钠、安赛蜜和咖啡因标准物质60、65、50、50 mg(精确至0.1 mg),分别置于50 mL 容量瓶中, 用水溶解并稀释至刻度,摇匀, 得到相应标准储备液, 4℃冰箱保存。(2)混合标准中间溶液的配制精密量取苯甲酸钠、糖精钠、安赛蜜和咖啡因标准储备液2.0 mL, 置同一10 mL 容量瓶中, 用水稀释至刻度, 摇匀, 得到混合标准中间溶液, 临用新制。(3)混合标准工作溶液的配制精密量取标准中间溶液适量, 置于10 mL 容量瓶中, 用水稀释至刻度, 摇匀, 配制成系列线性标准工作溶液, 供高效液相色谱仪测定。2.2.2 样品处理样品经超声脱气后, 精密量取1 mL 至2 mL 容量瓶中, 加水稀释至刻度, 摇匀, 经0.45 μm 滤膜过滤, 滤液供高效液相色谱仪测定。2.2.3 液相色谱条件色谱柱为月旭色谱柱,Ultimate XB-C18 4.6 x250,5um(part Number 00201-31043 Serial Number 211302350 Lot Number 2101.77)流动相A: 乙酸铵缓冲液(0.02mol/L), 流动相B: 甲醇, 梯度洗脱程序: 0~0.5 min, 流动相B 5%;0.5~6.0 min,5%~10%; 6.0~9.0 min, 10%~20%, 20%维持2min;11.0~16.0 min, 20%~75%, 75% 维持3min,19.0~20.0 min, 75%~5%, 5%维持7 min。流速1.0mL/min;进样量为20 μL; 柱温30 ℃; 检测波长230 nm 和272 nm。3 结果与分析3.1 方法的线性范围和检出限将 2.2.1(3)系列线性标准工作溶液(浓度范围为2.0~200 μg/mL)在2.2.3 仪器条件下进行分析, 建立标准曲线, 苯甲酸、糖精钠、安赛蜜和咖啡因的相关系数r 均大于0.999。以逐渐降低样品中标准溶液添加量的方法进行实验, 以峰面积相当于基线噪音的3倍(S/N=3)计算检出限。苯甲酸钠、糖精钠、安赛蜜和咖啡因的保留时间、检测波长、检测限等见表1。表1 检测波长、检出限、相关系数 化合物 检测波长 (nm) [alig
请教下各位老师,我们目前在用GB/T22250-2008保健食品中绿原酸的测定检测生咖啡豆中绿原酸的含量,按照标准使用70%甲醇超声30min,然后过膜HPLC检测,经过检测发现系统残留很严重,进样后再运行空针柱子中仍有很高的杂质峰和目标峰出来,不知有没有好的处理方法可以介绍下,谢谢!
锁阳咖啡中咖啡因含量的测定锁阳咖啡以天然锁阳为基础,配以速溶咖啡,是近几年涌现出的一种新型的固体饮料。锁阳主产于甘肃、青海、内蒙,其中以甘肃嘉酒地区的锁阳产量最大、质地最优。锁阳可调节生理机能、均衡营养、促进血液循环、滋肝健肾。锁阳咖啡是锁阳和咖啡的有机结合,越来越受到消费者的青睐。但是人们在饮用锁阳咖啡的同时却容易忽略咖啡的品质,咖啡因是咖啡中的一种重要成分,也是衡量其质量的一项重要指标,作为一种中枢兴奋剂,能兴奋大脑皮层,但易上瘾,因而国家对其制定了相应的标准。本实验用SN/T 1391-2004 《进出口速溶咖啡检验规程》中速溶咖啡中咖啡因的测定方法测定锁阳咖啡中咖啡因的含量。http://ng1.17img.cn/bbsfiles/images/2013/07/201307291536_454526_2764104_3.jpg1.方法提要样品用水溶解过滤后,用配有紫外检测器的高效液相色谱(HPLC)测定咖啡因,外标法定量。2.试剂和材料所有试剂除特殊注明外,均为分析纯,水为超纯水。2.1 乙睛:色谱纯;2.2 咖啡因标准品:纯度≥99%;2.3 标准储备液(100m g/L),准确称取 。0.0100 g 咖啡因标准品于100m L容量瓶中,用水溶解并定容至刻度,作为标准储备液。根据需要再用水将标准储备液稀释成适当浓度的标准工作液。3.仪器和设备3.1高效液相色谱仪配紫外检测器。3.2超声波振荡器。4.测定步骤4.1 提取称 取 0.1g(准确至 0.0001 g )均匀试样于 100m L容量瓶中,加人 80m L水,置超声波振荡器中超声20 min,冷却后用水定容至刻度并混匀,过0.45滤膜后,供HPLC测定。4.2 测定4 .2 .1 色谱条件a) 液 相色谱仪,配紫外检测器,检测波长273n m;b) 色 谱柱:C,。柱(25cm×4.6m mID,5um)柱或相当柱;c) 流 动相:乙睛一水一乙酸(16+83十1);d) 流 速 0.5 m L/min;e) 进 样 量 5uL4.2.2 色谱测定根据样液中咖啡因的含量情况,选定峰面积相近的标准工作溶液。标准工作溶液和样液中的咖啡因的响应值均应在仪器的检测线性范围内对标准工作溶液和样液等体积参插进样测定。在上述色谱条件下,咖啡因的保留时间约为9min。 http://ng1.17img.cn/bbsfiles/images/2013/07/201307291536_454528_2764104_3.jpg 标准溶液色谱图 http://ng1.17img.cn/bbsfiles/images/2013/07/201307291537_454529_2764104_3.jpg 标准曲线 http://ng1.17img.cn/bbsfiles/images/2013/07/201307291537_454530_2764104_3.jpg 样品色谱图 4.2.3[/size
?F42果葡糖浆国家行业标准 干物质大于71%,果糖占干物质大于42%,葡萄糖+果糖占干物质大于92%,PH值3.3-4.5,色度小于50RBU,不溶性颗粒物小于6.0mg/kg,硫酸灰分小于0.05%,透射比大于96%.????F42果葡糖浆是以碎米为原料,经酶法水解转化,异构,精制提取而制成的含果糖42%以上的淀粉糖产品,甜度与蔗糖相同,但口感优于蔗糖,目前己替代蔗糖广泛应用.其为无色或淡黄色,清亮透明的粘稠液体,甜味柔和,无异味.广泛应用于饮料,果汁,焙烤食品,糕点,罐头,乳制品,冷饮等行业.。

今天和同事收到了订购的咖啡,处于好奇,对两种咖啡的添加剂做了一下对比。一种是麦斯威尔的,一种是雀巢的。麦斯威尔的配料,还看明白几个,但是雀巢的就不懂了。说啥也没看的直观,发上来给大家看看。http://ng1.17img.cn/bbsfiles/images/2012/04/201204061114_359433_2471340_3.jpg两种咖啡的全景图(都是原味咖啡)http://ng1.17img.cn/bbsfiles/images/2012/04/201204061114_359435_2471340_3.jpg雀巢的配料(白砂糖、植脂末(葡萄糖浆,氢化植物油,稳定剂(340ii、331ii、452i),酪蛋白(含牛奶蛋白),乳化剂(471、472e),食用香精,抗结剂(551)),速溶咖啡)http://ng1.17img.cn/bbsfiles/images/2012/04/201204061121_359440_2471340_3.jpg麦斯威尔的配料(植脂末、白砂糖、速溶咖啡,食品添加剂)植脂末是做什么用的?麦斯威尔的植脂末中,有许多都是食品添加剂,比如二氧化硅,单硬脂酸甘油酯、干嘛还要和食品添加剂区分出来呢?
茶 咖啡碱测定 中华人民共和国国家标准 GB 8312-87 Tea-Determination of caffeine content 本标准适用于茶叶中咖啡碱的测定。 在茶叶水浸出物中除去叶蛋白、茶多酚等物质后,留下的生物碱其测定波长为274nm者,均称茶叶咖啡碱。1 原理 茶叶中的咖啡碱易溶于水,除去干扰物质后,用特定波长测定其含量。 2 仪器和用具 实验室常规仪器及下列各项:2.1 紫外分光光度仪。 2.2 分析天平: 感量0.0001g。 3 试剂和溶液 本标准所用试剂,除另有规定外,均为分析纯(AR) 水为蒸馏水。3.1 碱性乙酸铅溶液: 称取50g碱性乙酸铅(HG 3-1396-81),加水100mL,静置过夜。 3.2 盐酸(GB 622-77): 0.01N溶液,取0.9mL盐酸,用水稀释1L,摇匀。 3.3 硫酸(GB 625-77): 9N溶液,取硫酸250mL,用水稀释至1L,摇匀。 3.4 咖啡碱标准液: 称取100mg咖啡碱(纯度不低于99%)溶于100mL水中,作为母液,准确吸取5mL加水至100mL作为工作液(1mL含咖啡碱0.05mg)。 4 操作方法 4.1 取样 按GB 8302-87《茶 取样》的规定取样。4.2 试样的制备 按GB 8303-87《茶 磨碎试样的制备及其干物质含量测定》的规定,制备试样。4.3 测定步骤 4.3.1 试液的制备 按GB 8305-87《茶 水浸出物测定》中3.4.1的规定,制备试液。 4.3.2 测定 用移液管准确吸取试液(4.3.1)20mL移入250mL容量瓶中,加入10mL0.01N盐酸(3.2)和 2mL碱性乙酸铅溶液(3.1),用水准确稀释至刻度,充分混匀,静置澄清过滤,准确吸取滤液 50mL,注入100mL容量瓶中,加入0.2m19N硫酸溶液(3.3),加水稀释至刻度,混匀,静置澄清过滤。用10mm比色杯,在波长274nm处,以试剂空白溶液作参比,测定吸光度(A)。 4.3.3 咖啡碱标准曲线的制作 分别吸取0、5、10、15、20、25、30mL咖啡碱工作液(3.4)于一组100mL容量瓶中,各加入4.0mL盐酸溶液(3.2),用水稀释至刻度,混匀,用10mm石英比色杯,在紫外分光光度仪上选择狭缝0.1~0.18mm,在波长274nm处,以试剂空白溶液作参比,测定吸光度(A)。将测 得的吸光度与对应的咖啡碱浓度绘制标准曲线。 5 结果计算 5.1 计算方法和公式 茶叶中咖啡碱含量,以干态质量百分率表示,按下式计算: C 250 100 ──×L1×──×── 1000 20 50 咖啡碱(%)=───────────×100 M×m 式中:C--根据试样测得的吸光度(A),从咖啡碱标准曲线上查得的咖啡碱相应含量,mg/mL L1--试液总量,mL M--试样用量,g m--试样干物质含量百分率。如果符合重复性(5.2)的要求,取两次测定的算术平均值作为结果。 5.2 重复性 同一样品的两次测定值之差,每100g试样不得超过0.2g。 6 结果报告 试验报告应包括下列内容: a. 使用的方法 b. 测定的结果(取小数点后一位) c. 本标准中末规定的或另加的操作 d. 试样的名称和产地 e. 试验日期,操作人员。附加说明: 本标准由全国食品工业标准化技术委员会提出。 本标准由中国农业科学院茶叶研究所、商业部杭州茶叶加工研究所和上海进出口商品检验局负责起草。 本标准主要起草人李名君、钟萝、严家辉、程坤、郭雯飞、王济安。 中华人民共和国商业部1987-11-19批准 1988-07-01实施
有没有检测糖苷和氨基酸的液相柱?
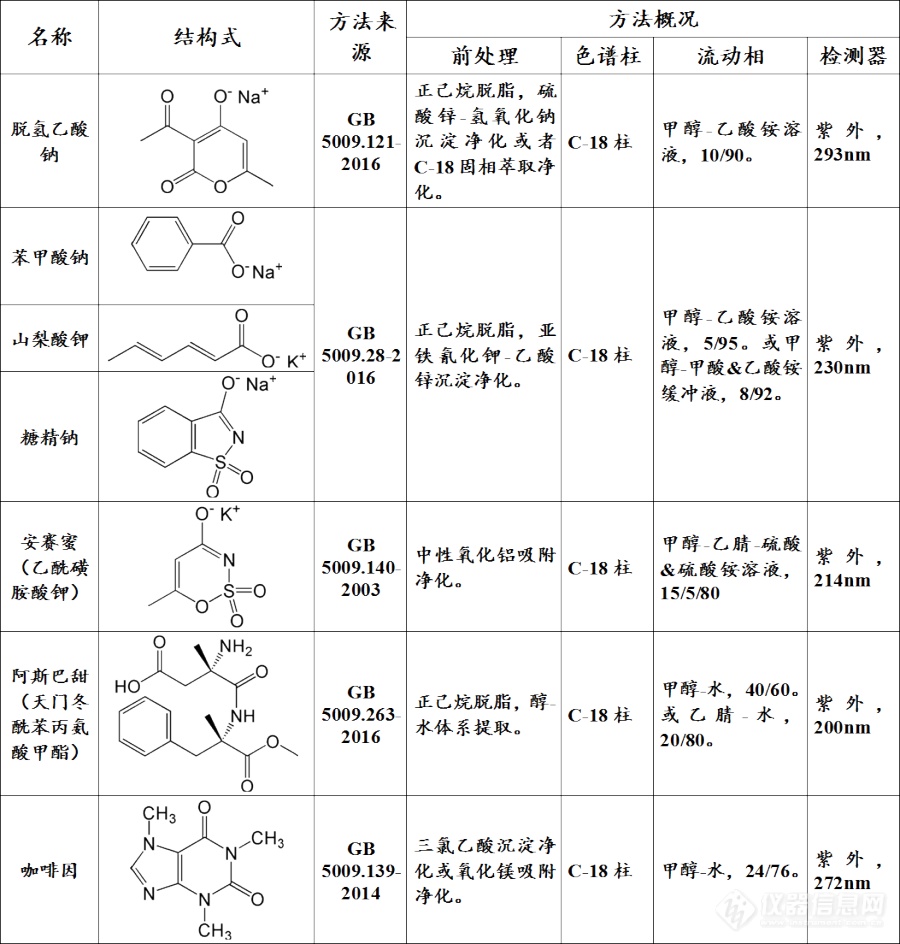
[b]1、引言[/b] 糖精钠、安赛蜜、阿斯巴甜是常用的甜味剂,苯甲酸钠、山梨酸钾、脱氢乙酸钠是常用的防腐剂。按GB 2760-2014,上述6种添加剂在诸多种类食品中都可使用。咖啡因也是一种常见的食品添加剂,并且在含茶、咖啡、可可的饮料和糕点中广泛存在。在实际生产实践中,对上述7种添加剂的测定属于常规需求,实施较为频繁。 按GB 5009系列标准,上述项目均有标准方法,但较为分散。整理如下表[img=,690,753]https://ng1.17img.cn/bbsfiles/images/2020/08/202008291644476781_2922_2204387_3.png!w690x753.jpg[/img] 上述7个项目隶属于5个不同的方法,需要分别测定,这就带来了诸多不便。考虑到五个标准方法由较多的相似性,只要确定了合适的色谱分离条件,上述7个项目完全可以整合到一个方法中进行测定。虽然有文献报道了相关的尝试([color=#33ccff]见:卫星华,李荣,董曼曼,艾芸,张亚锋,高安成.高效液相法同时测定饮品中8种食品添加剂[J].食品研究与开发,2017,38(24):137-140.[/color]),但是开发的方法需要梯度洗脱,单次分析需要40分钟以上,且每次进样之后需重新平衡。其他学者也进行了类似的研究,同样存在梯度洗脱时间长的问题([color=#33ccff]例如:姚浔平,李小平,姚珊珊,金米聪.高效液相色谱法同时测定食品中10种添加剂[J].中国卫生检验杂志,2009,19(01):9-11.[/color])。使用超高效液相色谱法可以显著提高分析速度([color=#33ccff]见:高敬铭,刘莹,姬建生,符锋.超高效液相色谱法同时测定食品中5种添加剂[J].理化检验(化学分册),2016,52(01):29-32.[/color]),但是仪器要求提高,目前尚不普及。 本文的主要目的是通过简便的等度洗脱方法实现上述7个目标物的快速分离,从而实现这7个项目同时测的,提高工作效率。.[b]2、实验方法[/b][align=left][b][font='Times New Roman']2.1 [/font][font=宋体]材料与试剂[/font][/b][/align][font='Times New Roman'] [/font][font=宋体]安赛蜜、糖精钠、苯甲酸、山梨酸、脱氢乙酸、咖啡因、阿斯巴甜标准品纯度均不低于[/font][font='Times New Roman']99.5% [/font][font=宋体]上海阿拉丁公司;甲醇(色谱纯)、磷酸二氢铵(分析纯)、氨水(分析纯)[/font][font='Times New Roman'] [/font][font=宋体]上海国药试剂公司;实验用水为二次蒸馏水。[/font][align=left][b][font='Times New Roman']2.2 [/font][font=宋体]仪器与设备[/font][/b][/align][font='Times New Roman'] iChrom 5100[/font][font=宋体]色谱系统,配[/font][font='Times New Roman']D5115[/font][font=宋体]二极管阵列检测器([/font][font='Times New Roman']DAD[/font][font=宋体])[/font][font='Times New Roman'] [/font][font=宋体]大连依利特公司;[/font][font='Times New Roman'] S210-B pH[/font][font=宋体]计、[/font][font='Times New Roman']XP6[/font][font=宋体]微量天平[/font][font='Times New Roman'] [/font][font=宋体]瑞士梅特勒公司;[/font][font='Times New Roman'] L400[/font][font=宋体]离心机[/font][font='Times New Roman'] [/font][font=宋体]湖南长沙湘仪公司。[/font][b][font='Times New Roman']2.3 [/font][font=宋体]方法[/font][font='Times New Roman']2.3.1 [/font][font=宋体]样品处理[/font][/b][font='Times New Roman'] [b]液体样品(饮料类)[/b]:[/font][font=宋体]准确称取试样[/font][font='Times New Roman']1.000 g[/font][font=宋体]置于[/font][font='Times New Roman']15 mL[/font][font=宋体]离心管中,加入[/font][font='Times New Roman']0.1 mol/L[/font][font=宋体]硫酸锌溶液[/font][font='Times New Roman']5 mL[/font][font=宋体]、[/font][font='Times New Roman']0.2 mol/L[/font][font=宋体]氨水[/font][font='Times New Roman']5 mL[/font][font=宋体],先机械振荡混匀,然后超声[/font][font='Times New Roman']5 min[/font][font=宋体],[/font][font='Times New Roman']4000 r/min[/font][font=宋体]离心[/font][font='Times New Roman']5 min[/font][font=宋体]。将上清液过滤到[/font][font='Times New Roman']25 mL[/font][font=宋体]容量瓶中,沉淀加色谱流动相(见[/font][font='Times New Roman']2.3.2[/font][font=宋体])洗涤[/font][font='Times New Roman']2[/font][font=宋体]次、每次[/font][font='Times New Roman']8mL[/font][font=宋体],洗涤液也滤到同一容量瓶中,用流动相定容。[/font] [b]固体样品(糕点类)[/b]:称取食品试样20~50g(精确至0.01g) ,加水100~200g(精确至0.1g) ,用高速匀浆机充分破碎混匀。然后按液体样品同样方法处理。 [b]含油脂较多的样品[/b]:先按固体试样相同方法进行匀浆。称取匀浆后的样品1.0~2.0g(精确至0.001g)置于15 mL离心管中,加氨水(0.2mol/L)5mL、乙醇0.5mL,混匀后再加正己烷5mL,加盖后剧烈震荡5min,然后4000 r/min离心5 min使样品分层。用吸管吸出大部分正己烷弃去,然后再加正己烷5mL重复萃取一次 。弃去正己烷相,水相用氮气吹扫使残余的正己烷挥发,然后加入硫酸锌溶液(0.1 mol/L)5 mL,混匀并剧烈振荡5 min。4000 r/min离心5 min分离沉淀,将上清液过滤到25 mL容量瓶中,沉淀加色谱流动相洗涤2次、每次8mL,洗涤液也滤到同一容量瓶中,用流动相定容,待色谱测定。[font='Times New Roman'][b]2.3.2 色谱条件[/b][/font][font='Times New Roman'] [/font][font=宋体]色谱柱:[/font][font='Times New Roman']Thermo Hypersil C18 (4.6 mm × 200 mm, 5 μm)[/font][font=宋体];流动相:甲醇[/font][font='Times New Roman']/[/font][font=宋体]磷酸盐缓冲液体积比为[/font][font='Times New Roman']20/80[/font][font=宋体],其中磷酸盐缓冲液为[/font][font='Times New Roman']0.1 mol/L[/font][font=宋体]磷酸二氢铵溶液用氨水调节至[/font][font='Times New Roman']pH = 5.5[/font][font=宋体];等度洗脱,流速为[/font][font='Times New Roman']1.000 mL/min[/font][font=宋体];柱温为[/font][font='Times New Roman']30.0 ℃[/font][font=宋体];进样体积为[/font][font='Times New Roman']10.00 μL[/font][font=宋体]。使用[/font][font='Times New Roman']DAD[/font][font=宋体]检测器,检测波长分别为:安赛蜜[/font][font='Times New Roman']225 nm[/font][font=宋体],糖精钠[/font][font='Times New Roman']210 nm[/font][font=宋体],苯甲酸[/font][font='Times New Roman']222 nm[/font][font=宋体],山梨酸[/font][font='Times New Roman']250 nm[/font][font=宋体],脱氢乙酸[/font][font='Times New Roman']228 nm[/font][font=宋体],咖啡因[/font][font='Times New Roman']272 nm[/font][font=宋体],阿斯巴甜[/font][font='Times New Roman']210 nm[/font][font=宋体]。[/font][b][font='Times New Roman']2.3.3 [/font][font=宋体]定性与定量方法[/font][/b][font='Times New Roman'] [/font][font=宋体]分别精确称量各标准品[/font][font='Times New Roman']10.00 mg[/font][font=宋体],定容至[/font][font='Times New Roman']10 mL[/font][font=宋体],制得浓度分别为[/font][font='Times New Roman']1.000 g/L[/font][font=宋体]的单标储备液,其中安赛蜜、糖精钠、阿斯巴甜的溶剂为纯水,其余的溶剂为甲醇。[/font] 依次准确吸取一定体积的单标储备液混合并用流动相(见1.3.2)稀释至1.00 ~ 50.0 mg/L的浓度范围,得到标准溶液系列。将标准溶液系列按相同色谱条件进行测定,以保留时间和DAD光谱匹配进行定性,以峰面积外标法建立工作曲线进行定量。.[b]3、问题讨论3.1 色谱流动相选择[/b] 原有方法测定7种目标物均采用反相色谱模式、C-18柱,本方法仍然选用C-18柱进行分离,因此实现分离的关键在于流动相的选择。 首先进行了改变有机相比例的实验,但这方面对分离效果的优化并不明显。提高有机相比例时,各目标物的保留时间均减小,分离度也随之减小。降低有机相比例时分离度增加,但各目标物的保留时间都显著延长,总体分析时间太长,不实用。 pH是影响这7种目标物分离的最重要因素。其中[font=宋体]安赛蜜、糖精钠均为强酸盐、苯甲酸钠、山梨酸钾、脱氢乙酸钠均为弱酸盐,咖啡因是弱碱,阿斯巴甜属于两性物质,随着流动相pH的变化,其存在形式会有显著不同,保留能力也随之变化明显。有不少文献也考查了pH的分离的影响([color=#33ccff]例如:方晓丽.超高效液相色谱同时测定饮料中5种食品添加剂[J].食品工业,2018,39(12):314-318.| 汪辉,曹小彦,陈利国,黄秀明.高效液相色谱法同时测定蜜饯中5种常见食品添加剂[J].分析试验室,2007(11):119-122.| 尤妍,潘辉国,陈盼盼,董琴芳,章萍萍.高效液相色谱法同时测定饮料中5种添加剂[J].食品研究与开发,2016,37(04):164-166.| 姚浔平,李小平,姚珊珊,金米聪.高效液相色谱法同时测定食品中10种添加剂[J].中国卫生检验杂志,2009,19(01):9-11.[/color]),但是数据较为零散,并没有揭示出有用的变化规律,因此缺乏指导意义,实验结果也不易重复。本研究在较宽的范围内考查了各目标物保留时间的变化趋势,并对各目标峰的相对位置进行了对比,结果如下图:[/font][font=宋体].[/font][align=center][font=宋体][color=#ff0000][img=,690,540]https://ng1.17img.cn/bbsfiles/images/2020/08/202008291807280222_7045_2204387_3.png!w690x540.jpg[/img][/color][/font][/align][align=center][color=#ff0000]流动相pH对7种目标物保留时间的影响(流动相为甲醇/缓冲液=20/80)[/color][/align][align=left].[/align][align=left] 糖精钠和安赛蜜都是强酸盐,相当于非常弱的碱,咖啡因本身就是极弱的碱,因此他们在弱酸性范围内存在形式不会有显著变化。只有在pH小于2之后,其保留时间才会水pH显著变化,但是通常色谱柱不能承受强酸,因此对pH小于2的情况不予考虑。阿斯巴甜是两性物质,在等电点附近呈分子内电离的形态,是保留最弱的。当pH增大或者减小时,其电离程度都是减小,保留时间都会表现为增大,但pH大于8是通常色谱柱不能承受的,因此也不予考虑。苯甲酸、山梨酸、脱氢乙酸都是羧酸,pKa均在5左右,因此其存在形式在pH从4到6变化时会显著不同,其保留时间在这个pH范围内也是变化最为显著的。pH减小时,羧酸形式存在占主导,因此其保留时间变大;pH增大时,盐形式存在的比例变多,因此保留时间减小;并且对于酸性强度不同的物质,其变化幅度和变化发生的pH范围也是显著不同的。相关理论在众多色谱专著中均有讨论([color=#33ccff]参见:Lloyd R.Snyder,Joseph J.Kirkland ,John W.Dolan,(译者:陈小明 唐雅妍[font=arial, &][/font]),现代液相色谱技术导论,人民卫生出版社,2012.[/color])。[/align][align=left] 上述讨论也说明,对于酸类物质的色谱分析,一定要精确控制流动相的pH。有些标准中对流动相pH未作明确的说明,这是极为不妥的,试剂的微小差异就会导致分析结果显著不同。例如GB 5009.28-2016中只规定了流动相加入乙酸铵,但实际购买的乙酸铵试剂pH可在6.5~7.5范围内变化,有时候就会导致苯甲酸与糖精钠的峰位置前后互换。[/align][align=left] 在明确了上述变化规律之后,流动相pH选择的问题也迎刃而解:显然在pH=5.5附近对于分离是最为有利的,不仅各目标物分离度较高,而且总的分析时间不太长,只需约15分钟。需要指出的是,由于pH计往往存在误差,实际配置缓冲液时并不一定按图中数值,而需要根据实际情况进行微调。若实测中发现脱氢乙酸与咖啡因分离度较低,说明配置的缓冲液pH略有偏低,应适当调高pH(通常调高0.1单位即可改善);若实测中发现脱氢乙酸与山梨酸分离度较低,说明配置的缓冲液pH略有偏高,应适当调低pH(通常调低0.1单位即可改善)。[/align][align=left] 在上述讨论的最佳流动相条件下,标样和实际样品的分离效果都很好,见下图:[/align][align=center][img=,690,719]https://ng1.17img.cn/bbsfiles/images/2020/08/202008291903133024_5403_2204387_3.png!w690x719.jpg[/img][/align][align=center][color=#ff0000]标样和实际样品的色谱图(流动相为甲醇/缓冲液=20/80,缓冲液为0.1M磷酸二氢铵溶液用氨水调节至pH5.5)[/color][/align][align=center][color=#ff0000].[/color][/align][align=left] 另外要补充说明的是,虽然标准方法中使用的缓存盐常常是乙酸或者甲酸体系,但实际上并不是最佳选择。因为有机酸本身会产生一定的背景吸收,在低波长下尤其明显。而磷酸盐体系的背景吸收要小得多,这对减小背景干扰和基线漂移是有利的。[/align][align=left][b]3.2 检测波长选择[/b][/align][align=left] 7种目标物的的吸收波长各不相同,用DAD检测器可较好解决问题,并且有助于通过吸收光谱图定性。若没有配备DAD检测器,可用一般可变波长紫外检测器的“波长时间程序”功能。[/align][align=left] 通过较高浓度标样测得7种目标物的色谱-光谱图如下,其紫外吸收谱图和最大吸收波长可供参考。[/align][align=left][img=,690,1127]https://ng1.17img.cn/bbsfiles/images/2020/08/202008291912345152_2614_2204387_3.png!w690x1127.jpg[/img][/align][align=left] 需要说明的是,糖精钠和阿斯巴甜的最大吸收波长都在较低波段,易受到背景吸收和样品基体的干扰,因此实际选用的是210nm进行检测,灵敏度虽然有所降低,但干扰也明显减轻。实际应用中发现,少数情况下,糖精钠仍然会受到基质干扰,此时可进一步将其检测波长降低到215~220nm,基质干扰基本上就减小到可忽略的程度了。[/align][align=left] 另外,不同文献中报道的各种目标物的最大吸收波长有一些出入,这一方面与不同仪器的波长误差有关,更重要的是因为目标物的离解程度随pH变化,不同pH下测得的最大吸收波长会有明显差异。[/align][align=left][b]3.3 样品前处理[/b][/align][align=left] 本方法参考现有方法,采用了锌盐沉淀的吸附和絮凝作用来净化除杂,但是未使用亚铁氰化钾和乙酸锌,也未采用三氯乙酸沉淀蛋白。因为这几种物质都有末端吸收,在接近210nm处产生的紫外吸收较为明显,而其色谱流出的时间又都与安赛蜜、糖精钠等物质接近(例如,三氯乙酸的流出时间与糖精钠几乎相同)。本方法采用氨水和硫酸锌生成氢氧化锌絮状沉淀,其吸附与絮凝效果与亚铁氰化钾-乙酸锌体系较为接近,同时不引入干扰离子。[/align][align=left] 对于含油脂较多的试样,本方法仍采用正己烷萃取除脂,与常规方法基本一致。[/align][align=left][b]3.4 方法验证[/b][/align][align=left] 对方法的重现性、线性范围、加标回收率进行了验证,详细数据较多,这里从略,主要结果如下:[/align][align=left] (1)标样7次重复测定的重现性很好,RSD均小于1%。但样品处理的重现性略差,同一样品匀浆后分别进行7次净化和测定,RSD在1%~3%。[/align][align=left] (2)7种目标物在1~50mg/L范围内线性相关系数均大于0.999,以取样1.0g计,测定范围相当于0.025~1.25g/Kg。考虑到添加剂的实际使用情况,未对更高含量水平进行验证。[/align][align=left] (3)按三倍信噪比估算,检出限均低于0.1mg/L,远低于常规检测范围,故未进一步对验证检出限。[/align][align=left] (4)进行了1g/Kg和0.1g/Kg两个水平的加标实验,阿斯巴甜的回收率略低,分别为94.1%和95.7%,其余目标物的回收率均在98%~101%之间。推测可能是阿斯巴甜容易被氢氧化锌沉淀吸附,导致回收率略低。[/align][align=left].[/align][align=left][b]4、结论[/b][/align][align=left] (1)使用C-18色谱柱,使用甲醇与pH=5.5的磷酸盐缓冲液按20/80比例作为流动相,可以在等度洗脱条件下实现[font='Times New Roman'] [/font][font=宋体]安赛蜜、糖精钠、苯甲酸、山梨酸、脱氢乙酸、咖啡因、阿斯巴甜等[/font]7种物质的完全分离,分析时间约15分钟。[/align][align=left] (2)基于上述色谱分离方法,可以实现7种常见食品添加剂的同时测定,结果较为准确,可以用于生产实践。[/align]
用反相高效色谱仪同时测定咖啡因和绿原酸含量的方法,在咖啡豆中提取绿原酸了,希望用反相高效色谱仪同时测定提取液中咖啡因和绿原酸的含量
有没有人做咖啡因的啊?现在我们公司想买咖啡因标准品,但是问了好几个地方,都说管制的,没法买。想问问大家哪里买的
咖啡因会刺激胃酸分泌,增加胃酸浓度,不建议空腹喝咖啡。喝之前最好吃些富含碳水化合物的食物,如面包、包子及各种饼类等。早上10点左右来杯咖啡,可以达到很好的提神效果。
作者:金智利; 袁文婧;哈药集团三精制药股份有限公司;摘要:目的:建立高效液相色谱法测定金银花连翘提取物中绿原酸、咖啡酸的的含量。方法:采用迪马(钻石)C18(250mm×4.6mm,5μm)色谱柱,流动相为甲醇-水-冰乙酸(20:80:1),流速1.0ml/min,检测波长:324nm。结果:金银花连翘提取物中绿原酸、咖啡酸能达到有效分离,绿原酸在9.44μg/ml~141.60μg/ml范围内,浓度同峰面积呈良好的线形关系,仪器精密度RSD为0.03%,方法的重复性RSD=0.24%。咖啡酸在5.36μg/ml~80.40μg/ml范围内,咖啡酸峰面积值与浓度有良好的线性关系,仪器精密度RSD为0.03%,方法的重复性RSD=0.33%。结论:该方法简便、准确、可行。可用于金银花连翘提取物的质量控制。
有参加2015年 辽宁检验检疫 CNAS PT0005 果汁中苯甲酸、糖精钠、山梨酸、咖啡因的检测能力验证的吗?大家比对下啊
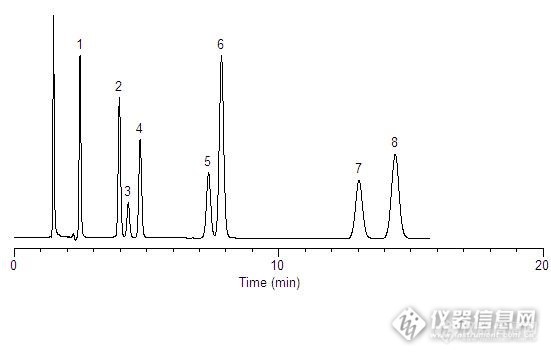
http://www.cheminlife.com/zb_users/upload/2013/4/2013040680891057.jpg 作为世界三大饮料之一的咖啡,其香浓醇厚的口感赢得了全世界人民的深深喜爱,更微妙的是,咖啡还具有提神的功效。随着生活节奏的日益加快,高强度的工作压力要求上班族们必须时刻保持清醒、精力充沛。如今,咖啡已成不少白领们每日不可少的饮品,由于既可使消费者方便购买到口味正宗的咖啡,也能让他们在品尝时拥有一个环境优雅的谈话、休憩场所,星巴克、上岛等连锁咖啡品牌日渐炙手可热。 环球时报讯:研究发现,过度饮用咖啡导致幻听。如果你总是幻听,可能是因为咖啡喝太多。研究人员称,一天5杯咖啡就能让你的耳朵不灵便。咖啡营养成分有哪些?为什么可以提神?又为什么会有苦味? 每100克咖啡豆中含水分2.2克、蛋白质12.6克、脂肪 16克、糖类46.7克、纤维素9克、灰分4.2克、钙120毫克、磷170毫克、铁42毫克、钠3毫克、维生素B2 0.12克、烟酸3.5毫克、咖啡因1.3 克、单宁 8 克。 咖啡所有成份中最为引人注目的是咖啡因,它属于植物黄质的一种,也叫三甲基黄嘌呤、咖啡碱、甲基可可碱,分子式为C8H10N4O2 。性质和可可内含的可可碱、绿茶内含的茶碱相同。适量的咖啡因能够刺激大脑皮层,促进感觉判断、记忆、感情活动,让心肌机能变得较活泼,血管扩张血液循环增强,并提高新陈代谢机能,咖啡因也可减轻肌肉疲劳,促进消化液分泌。咖啡中的苦味也是来源于咖啡因,烘焙过程对咖啡因破坏极小,约2个小时左右即可被排泄掉,不会聚积在体内。下图是使用Diamonsil C18(2)检测咖啡因的代谢物的谱图色谱柱:Diamonsil C18(2), 150 × 4.6 mm 5 μm 流动相:甲醇: 0.1%甲酸水溶液=10: 90流速:1.0 mL/min柱温:室温检测器:UV 254 nm样品: 1. 黄嘌呤(Xanthine) 2. 7-甲基黄嘌呤(7-Methylxanthine) 3. 1-甲基尿酸(1-Methyluric acid) 4. 3-甲基黄嘌呤(3-Methylxanthine) 5. 1, 3-二甲基尿酸(1, 3-Dimethyluric acid) 6. 可可碱(Theobromine) 7. 1, 7-二甲基黄嘌呤(1, 7-Dimethylxanthine) 8. 茶碱(Theophylline)http://ng1.17img.cn/bbsfiles/images/2015/01/201501141546_532264_1610895_3.jpg咖啡可以作为早餐么?咖啡也会上瘾?每天喝多少咖啡可算作过量饮用?后果如何? 早餐中加一杯咖啡可以提神醒脑、精力充沛,但空腹饮用咖啡往往会引起胃酸、胃痛,原因是咖啡因能使胃酸增多,持续的高剂量摄入会导致消化性溃疡,糜烂性食道炎和胃食管反流病。故胃肠功能不好者不适宜常饮咖啡,尤其是有胃溃疡的人更应谨慎。 通常所说的适量摄取咖啡,是维持在一天不超过2杯的水平上。但不少的青少年由于过量饮用咖啡,已经有“成瘾”的反应,每天都必须饮下大剂量的咖啡,不饮则会失眠、焦虑。在长期摄取的情况下,大剂量的咖啡因是一种毒品,能够导致“咖啡因中毒”。咖啡因中毒包括上瘾和一系列的身体与心理的不良反应,一旦停用会出现比如神经过敏、易怒、焦虑、震颤、肌肉抽搐(反射亢进)、失眠心悸、精神萎顿、浑身困乏疲软等各种戒断症状。虽然其成瘾性较弱,戒断症状也不十分严重,但由于药物的耐受性而导致用药量不断增加时,咖啡因就不仅作用于大脑皮层,还能直接兴奋延髓,引起阵发性惊厥和骨骼震颤,损害肝、胃、肾等重要内脏器官,诱发呼吸道炎症、妇女乳腺瘤等疾病。
最近在开展氨基糖苷类(包括卡那霉素\庆大霉素\链霉素\双氢链霉素\新霉素\安普霉素等)的检查,虽然有国标使用c18在做,但考虑到七氟丁酸容易污染到质谱,很是怕怕,所以就选择了hilic色谱柱。第一次接触hilic色谱柱,遇到了以下问题:现象:1. 使用等度洗脱,乙腈:水=90:10,所有项目的保留时间都在2.6min附近。2. 使用梯度洗脱,流动相还是乙腈:水,每个项目出现了两个保留时间,一个还是在2.6min附近,另一个在9min附近,两个保留时间都是在乙腈比例最高的时候出现。3.怀疑出现的峰是色谱柱被洗脱掉的物质,使用空白水进行测试(以上标准品使用水溶解),未出峰。排除是色谱柱及液相系统的问题,说明这些峰应该是想要的标准品峰。4.从论坛资料查询到的,有人说是用乙酸铵或甲酸铵可以,经测试,加入铵后,标准品不出峰或惨不忍睹。我使用的是10mM的浓度,不清楚是否是浓度太高的问题,但我觉得可能性不大。疑问:1。所有的标准品保留时间一样,非常奇怪,很是怀疑这到底是不是我要的标准品峰。2。跑标准曲线,不成线性,甚至部分项目低浓度的感度高于高浓度的,郁闷。。。3。保留时间无法再向后拖了,因为乙腈的比例够高了,应该再怎样改变保留时间呢?自己也搜索了一些资料,可是还没有一个比较完善的关于HILIC色谱柱的使用方法的资料,论坛中有人说使用HILIC是可以分析这些物质的,但给出的资料或说明又难以让人信服。所以,希望对HILIC了解或正在使用HILIC的大侠多多给点意见,如果有人确实在做这几种物质的话(使用HILIC),小生那更是感激不尽了。。。。欢迎大家在此热烈讨论。。。更新:在论坛上搜到了个HILIC方法开展指南,给大家分享下。欢迎继续探讨,希望这个帖子能够成为hilic开展方法的探讨贴。。。更新: 看了些资料,hilic色谱柱使用需要以下注意事项:1。流动相至少需要5%的极性溶剂(如水,甲醇等)2。流动相需要不低于40%的有机相(如乙腈)3。使用甲酸铵或乙酸铵能得到较好的重现性。4。定溶液不能使用100%的水5。平衡时间比较长,一般需要10倍以上的柱体积平衡更新: 经过一段时间的测试,通过使用hilic色谱柱目前还没有得到良好的效果。使用资生堂的一款链霉素专用色谱柱,保留特性不错,只是感度还有点差,需要再进行优化。由于最近忙于粘杆菌素的开展,氨基糖苷类的测试需要拖一拖了,如果,谁也在做粘杆菌素,不妨也来讨论下。
[align=center][size=21px]氨基糖苷[/size][size=21px]类药物检测国内标准比较解读[/size][/align][size=18px]氨基糖苷类[/size][size=18px]药物[/size][size=18px]是一类抑制革兰氏阴性菌的抗生素,其[/size][size=18px]分子结构[/size][size=18px]中含有氨基糖苷键和氨基环己醇,[/size][size=18px]本身不具有发色基团,只有通过与衍生试剂反应才能用紫外或荧光检测,[/size][size=18px]由于其极性很强,分析时需要加离子对试剂才能在反相色谱柱上保留,可以使用高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法活[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱法检测,现将[/size][size=18px]国内[/size][size=18px]氨基糖苷类[/size][size=18px]药物相关[/size][size=18px]主要[/size][size=18px]检测方法标准[/size][size=18px]总结如下[/size][size=18px]:[/size][table][tr][td]序号[/td][td]标准名称[/td][td]检测原理[/td][td]药物数量、种类[/td][/tr][tr][td]1[/td][td]GB/T 21323-2007 动物组织中氨基糖苷类药物残留量的测定 高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-质谱/质谱法[/td][td]试样用含0.4 mmol/L EDTA和2%三氯乙酸的磷酸盐缓冲溶液提取,经C18固相萃取柱净化,浓缩后使用七氟丁酸作为离子对试剂,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定。[/td][td]10 种:壮观霉素、潮霉素B、双氢链霉素、链霉素、丁胺卡那霉素、卡那霉素、安普霉素、妥布霉素、庆大霉素、新霉素[/td][/tr][tr][td]2[/td][td]GB/T 22995-2008 蜂蜜中链霉素、双氢链霉素和卡那霉素残留量的测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法[/td][td]试样用 0.2 mol/L的磷酸盐缓冲溶液提取,用HLB和羧酸型固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定。[/td][td]3 种:链霉素、双氢链霉素、卡那霉素[/td][/tr][tr][td]3[/td][td]GB/T 21164-2007 蜂王浆中链霉素、双氢链霉素残留量测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法[/td][td]试样用庚烷磺酸钠-磷酸钠混合缓冲溶液提取,用C18固相萃取柱净化,高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]荧光法检测。[/td][td]2 种:链霉素、双氢链霉素[/td][/tr][tr][td]4[/td][td]GB/T 22945-2008 蜂王浆中链霉素、双氢链霉素和卡那霉素残留量的测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法[/td][td]试样用5%磷酸溶液提取,三氯乙酸沉淀蛋白,用苯磺酸型和羧酸型固相萃取小柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱测定。[/td][td]3 种:链霉素、双氢链霉素、卡那霉素[/td][/tr][tr][td]5[/td][td]农业部1077号公告-3-2008 水产品中链霉素残留量的测定 高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法[/td][td]试样5%三氟乙酸溶液提取,用C18固相萃取小柱净化,高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]荧光法检测。[/td][td]1 种:链霉素[/td][/tr][tr][td]6[/td][td]SN/T 1925-2007 进出口蜂产品中链霉素、双氢链霉素残留量的检测方法 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法[/td][td]试样用pH=2的磷酸溶液提取,用阳离子交换柱和HLB固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱测定。[/td][td]2 种:链霉素、双氢链霉素[/td][/tr][tr][td]7[/td][td]SN/T 4778-2017 出口花粉中链霉素和双氢链霉素的测定方法 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-质谱/质谱法[/td][td]用庚烷磺酸钠-磷酸钠混合缓冲溶液提取,三氯乙酸沉淀蛋白,用C18固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱测定。[/td][td]2 种:链霉素、双氢链霉素[/td][/tr][tr][td]8[/td][td]SN/T 5117-2019 进出口食用动物、饲料 链霉素类(链霉素、二氢链霉素)药物残留测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-质谱/质谱法[/td][td]试样用含0.4 mmol/L EDTA和2%三氯乙酸的磷酸二氢钾缓冲溶液提取,经HLB固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定,外标法定量。[/td][td]2 种:链霉素、双氢链霉素[/td][/tr][/table][size=18px]通过比较这些方法标准发现,由于氨基糖苷类药物极性强,水溶性好,一般用磷酸溶液等无机溶液提取;试样中的蛋白等杂质一般通过加入三氯乙酸及SPE法去除(HLB、C[/size][size=18px]18[/size][size=18px]小柱等)[/size][size=18px],[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]方法检测时要特别注意七氟丁酸等离子对试剂的使用,浓度不能过高,使用后要用大量水冲洗管路,否则出现残留后会对仪器灵敏度产生较大影响。[/size]
熊陈思慧等建立了超高效液相色谱_线性离子阱/静电场轨道阱高分辨质谱法同时测定化妆品中的22种功效成分,样品采用甲醇超声提取C18 色谱柱 (100mm *2.1 mm,1.8μm)分离,以0.1% (v/v)甲酸水溶液和乙腈为流动相进行梯度洗脱 在正离子模式下以保留时间和一级母离子精确质量数进行定量分析以高能碰撞诱导解离获得的二级碎片离子精确质量数进行确证结果表明该方法线性关系良好检出限LOD 为 0.003~2.01mg/kg,定量限LOQ 为 0.02~4.36mg/kg水乳霜 种基质中 个添加水平的回收率范围为63.2%~125.1%相对标准偏差为0.18%~10.9%对标示含有烟酰胺抗坏血酸葡糖苷咖啡因泛醇及甘草类光果甘草根茎叶甘草根胀果、甘草根、麦冬根人参根黄芪根虎杖根苦参根地黄根积雪草茶叶提取物的54批样品进行检测标示单体功效成分的样品均有检出标示不同植物提取物的46批样品中24批检出植物提取物的功效成分,该方法简便快速定性定量可靠适用于化妆品中22种功效成分的定量测定。 文章具体内容见附件
前阵子有版友讨论了咖啡因对人体的危害。咖啡因来源有咖啡豆和茶,咖啡豆又是其中主要的来源。危害1、心脏。咖啡因以两种方式作用于心脏:除了影响调节心血管系统的大脑中枢,也直接对心脏产生作用。高剂量的咖啡因能使不耐受咖啡因的人每分钟增加 10~20 次心跳,并且可能使某些人短暂心律不齐。因此,适度饮用含咖啡因(平均每天最多 500 毫克)的饮品,不会大幅提高心脏疾病风险,但超过这个剂量可能会增加患心肌梗死的风险。2、肾脏。早上喝咖啡后爱上厕所,是许多人经常遇到的事。这是因为咖啡因会影响肾脏的腺苷受体,起到类似利尿剂的作用。咖啡因也可能减缓大脑释放一种减少尿液生成的抗利尿激素。3、消化系统。咖啡中的酸质、油脂及咖啡因都可能刺激胃黏膜,并促进胃酸分泌,长期大量饮用含有咖啡因的饮品,会导致胃病。4、呼吸系统。咖啡因及类似药物对于呼吸有两种影响,一是增加呼吸速率。此外,咖啡因可使气管周围的平滑肌放松,因而使气管扩张,增加呼吸量。但咖啡因不可以作为药物用于临床来治疗哮喘。警惕喝咖啡5大禁忌1、切记咖啡不宜与茶同服。茶和咖啡中的鞣酸可使铁的吸收减少75%。宜用温开水送服。2、茶叶和咖啡中的单宁酸,会让钙吸收降低。所以,喝茶和喝咖啡的时间,最好是选在两餐当中。3、含咖啡因的饮料和食品,被孕妇大量饮用后,会出现恶心、呕吐、头痛、心跳加快等症状。咖啡因还会通过胎盘进入胎儿体内,影响胎儿发育。4、不少医生认为,孕妇每天喝1~2杯(每杯6~8盎司)咖啡、茶或碳酸类饮料,不会对胎儿造成影响。但为慎重起见,孕妇最好禁用。咖啡因可导致流产率上升,所以应喝不含咖啡因的饮料。5、儿童不宜喝咖啡。咖啡因可以兴奋儿童中枢神经系统,干扰儿童的记忆,造成儿童多动症。你平时会喝咖啡么?喝多了是否对你有影响?
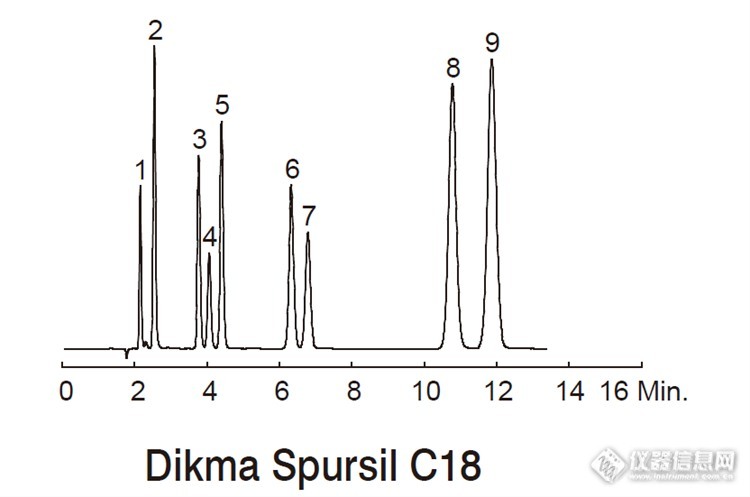
咖啡的主要成分是咖啡因,可以作用于神经细胞中一种叫做腺嘌呤核苷的化学物质,是一种中枢神经兴奋剂,能够暂时的驱走睡意并恢复精力。 不过,咖啡对有些人是有好处的,但是对某些人却产生负面影响,这主要是与咖啡因的在不同人的代谢能力有关的。 咖啡因在肝脏中被分解产生三个初级代谢产物副黄嘌呤,可可碱,茶碱。咖啡因在摄取后45分钟内被胃和小肠完全吸收。吸收后它会分布于身体的所有器官之中,转化过程符合化学动力学一级反应,这些化合物进一步代谢,最终通过尿液排泄。 如果某些人的这个酶的代谢比较快,摄入的咖啡因很快就会被清除出体外,因此咖啡因起作用的效果就很有限,不能令人产生特别明显的兴奋感。而对于另一些人,他们这个酶代谢速度慢,咖啡因在体内的清除速度很慢,起作用时间也就较长,这样的人往往一杯咖啡就会令他们夜不能寐,有的还会影响食欲,呕吐和痉挛,也可能出现胃炎或心脏病等不良反应。 所以这也解释了一般人普遍担心的咖啡会影响睡眠问题,其实和你对咖啡因的代谢力有很大的关系。由于每个人对咖啡因代谢的能力不同,平均来说,咖啡因在体内的运作,大约能维持3~4个小时,所以即使在晚餐后饮用,也不至于造成太大的困扰。但有些人的代谢力较差,可能会持续作用8~12个小时;或者体质对咖啡因比较敏感,就得特别注意喝咖啡的时间,避免影响作息,因为不论是多喝开水或是增加运动,都无法有效的促使咖啡因快速代谢。*********************************** 以上对咖啡因的代谢方面做了简单的科普,可如何对咖啡因代谢物进行检测呢?由于咖啡因代谢物从化学结构上来看,这一类化合物具有相似的母体结构,不同之处在于甲基的位置,属于位置异构体。(见下图)http://ng1.17img.cn/bbsfiles/images/2016/01/201601071109_581149_2452211_3.png 对于分离这些代谢物来说,对色谱柱的分离能力要求比较高,下面我们看看使用迪马Spursil色谱柱分离9种咖啡因代谢物的分离效果情况色谱柱:Spursil C18规格:150 x 4.6 mm, 5 μm流动相:甲醇/ 水+1% 乙酸=10/90流速:1.0 mL/min柱温:室温检测器:UV 254 nm样品:1. 尿酸2. 黄嘌呤3. 7- 甲基黄嘌呤4. 1- 甲基尿酸5. 3- 甲基黄嘌呤6. 1,3- 二甲基尿酸7. 可可碱8. 1,7- 二甲基黄嘌呤9. 茶碱http://ng1.17img.cn/bbsfiles/images/2016/01/201601071110_581151_2452211_3.png总结:Spursil 色谱柱能够在13分钟之内将它们全部分开且达到基线分离~棒棒哒http://simg.instrument.com.cn/bbs/images/default/em09505.gif
咖啡作为一种广受欢迎的饮品,除了单独饮用外,在食品工业中也有多种用途。咖啡可以为食品带来独特的风味,并且在不同的食品类别中发挥不同的功能。以下是咖啡在食品中的几种常见应用: 1. 饮品 - **即饮咖啡**:市场上有许多预包装的即饮咖啡产品,包括冷萃咖啡、拿铁、摩卡等。 - **咖啡混合饮料**:咖啡与其他饮料如茶、果汁或牛奶混合制成的饮品。 - **功能性饮料**:一些功能性饮料会添加咖啡提取物以提供额外的能量或提神效果。 2. 糕点和烘焙 - **咖啡蛋糕**:咖啡可以作为蛋糕的调味料,增加独特的风味。 - **咖啡面包**:在面团中加入咖啡粉或浓缩咖啡液,制成带有咖啡香味的面包。 - **咖啡饼干**:咖啡饼干是利用咖啡的苦甜味与饼干的酥脆口感相结合的美味小食。 3. 冰淇淋和甜品 - **咖啡冰淇淋**:经典的咖啡口味冰淇淋深受人们喜爱。 - **提拉米苏**:意大利经典甜品之一,用浸泡过咖啡的手指饼干与马斯卡彭奶酪层层叠放而成。 - **咖啡布丁**:利用咖啡的香气制作成布丁,提供不同于传统布丁的独特风味。 4. 糖果和巧克力 - **咖啡糖**:含咖啡成分的硬糖或软糖。 - **咖啡巧克力**:咖啡与巧克力结合的产品,如咖啡豆包裹巧克力、咖啡味巧克力等。 5. 酱料和调味品 - **咖啡酱**:咖啡可以用于制作甜酱或咸酱,用于搭配各种甜点或肉类菜肴。 - **咖啡腌料**:咖啡还可以作为腌料的一部分,为肉类增添风味。 6. 肉类加工 - **咖啡烤肉**:咖啡粉或咖啡液可用于制作烤肉的腌料,增加一种独特的焦香味道。 - **咖啡风味香肠**:一些特色香肠中会加入咖啡成分,使其具有特殊的风味。 注意事项 - **咖啡因含量**:使用咖啡制作食品时需要注意产品的咖啡因含量,尤其是针对儿童和敏感人群的产品。 - **口味平衡**:咖啡的味道比较强烈,因此在食品配方中需要与其他成分平衡好,以达到理想的口感。 - **食品法规**:在不同国家和地区,食品中咖啡成分的使用可能受到不同的法规限制,比如标签要求、成分声明等。 总的来说,咖啡在食品工业中有广泛的用途,可以为各种食品增添独特的风味。然而,在开发新产品时,需要考虑到目标消费者的偏好以及相关法律法规的要求。
目前在检测咖啡中的奎宁酸物质,使用普通C18柱子不知道能不能检测,问下老师们,希望得到解答,谢谢。
请问哪里能检测油菜籽中芥酸和硫代糖苷?最好在北方。谢谢!