均多相融合选择性催化制备生物基可降解聚酯单体——岛津XPS用户成果分享
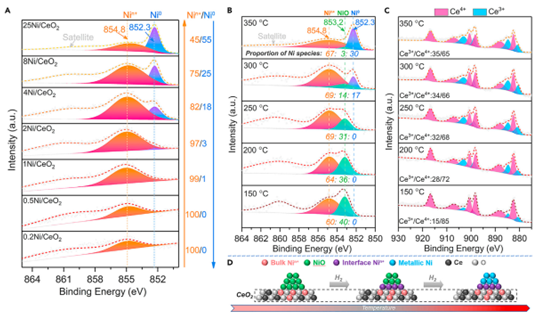
团队介绍:李福伟研究员团队李福伟老师现任中国科学院兰州化学物理研究所研究员,博士生导师,中科院特聘研究员,国家优秀青年基金获得者。2005年于中科院兰州化学物理研究所夏春谷研究员组获物理化学博士学位,随后在中科院过程工程研究所张锁江院士研究组从事绿色化工研究,2006年4月-2009年12月在新加坡国立大学化学系贺子森教授(Professor Andy Hor, 现香港大学副校长)研究组开展博士后研究。2010年入选中科院“百人计划”并于同年获择优支持,在兰州化学物理研究所开始独立研究工作,研究领域为面向清洁能源和先进合成的绿色催化,主要开展功能含氮杂环化合物的高效催化合成以及可再生碳资源(生物质、二氧化碳)的增值催化转化研究。已发表研究论文80余篇,论文H因子30,其中2011年以来以通讯作者在Chem. Rev., Nat. Commun., Angew. Chem. Int. Ed., ACS Catal., J. Catal., Appl. Catal. B: Environ., Green Chem.等期刊上发表50余篇论文。编著中英文专著2个章节,申请授权中国发明专利10余项。曾获中国化学会催化委员会首届“中国催化新秀奖”(2012)、中科院院长优秀奖(2005)等。2015年获国家自然科学基金“优秀青年基金”资助。均多相融合选择性催化制备生物基可降解聚酯单体羟基脂肪酸酯(PHA)是制备生物可降解聚酯高分子材料的重要单体, 现有制备方法存在催化效率和选择性低等不足。从可再生的生物基碳氧资源出发,发展简便、高效、高选择性的催化制备生物基羟基烷酸酯聚酯单体技术具有重要意义和潜在应用价值。中科院兰州化学物理研究所李福伟研究员团队从半纤维素下游产品糠醇出发,发现Pd与具有一定咬角结构的双膦配位后能够高效、高选择性地实现均相催化切断糠醇的羟基C-O键,插入制备PHA所需要的羧酸酯官能团,催化转化数(TON)高达104以上。减压蒸馏出呋喃乙酸酯产物后,催化剂可以循环使用二十次而不失活,为生物质的“量体裁衣”增碳提供了一个新的方法。图1 利用原位XPS分析xNi/CeO2催化剂中Ni物种的结构特点及演变规律Science Technology 以糠醛衍生物呋喃乙酸的C-O键氢解制备6-羟基羧酸酯为例,开发制备了非贵金属催化剂Ni/CeO2,并表现出高的催化活性和稳定性;如图1所示,利用in situ XPS技术详细分析了xNi/CeO2催化剂中Ni物种的结构特点及Ni物种在制备过程中的演变规律,结果显示8Ni/CeO2中存在金属Ni0物种和界面Nin+-VO-Ce物种。研究了Ni/CeO2表界面Ni物种类型及相对含量,发现催化剂界面Ni物种主要为Ni0和Niδ+,结合动力学分析,推断Ni0是C=C加氢的活性中心,而Niδ+是C-O氢解的活性中心。通过改变Ni负载量优化Ni0和Niδ+相对含量,实现C=C加氢和C-O氢解反应速率的动力学匹配,获得理想催化性能。相较于传统的石油基制备方法而言,其合成策略显示出:高的原子经济性,高能源利用率,原料来源可持续,并避免了易爆过氧化物的使用。参考文献Zelun Zhao, Guang Gao, Yongjie Xi, Jia Wang, Peng Sun, Qi Liu, Wenjun Yan, Yi Cui, Zheng Jiang, Fuwei Li*, Chem, 2022, 8, 1034-1049.本文内容非商业广告,仅供专业人士参考。