请教大家,标准品有没有必要进行受控号的标识?我理解就是给标准品归类为设备,给与受控号进行管理,但是这个受控号只体现在出入库记录里面,原始记录里面体现的还是批号。这样的管理溯源的时候好像管理编号也没啥用。同理还有试剂的管理,有没有必要进行编号管理?谢谢。
原标准被新规范替代,作废原标准,新规范的受控编号可以沿用作废的旧标准编号吗?
标准物质证书还需要做内部受控发放吗?
背景: cma认证参数表各参数均一 一对应方法标准,代表本检测机构的检测能力。观点一:检测机构标准管理时仅和参数表对应,对方法标准按照流程进行识别和受控管理,对于判定标准则无需纳入受控文件管理。判定标准时合同评审时与客户约定的内容,且判定标准可以是国、行、地、企四类标准,也可以为非现行有效的标准版本,判定标准与检测机构能力之间无必然联系,因此判定标准可不纳入标准受控范围。观点二:尽管目前参数表中均使用方法标准,但是作为判定的标准也应该受控,因为判定标准也需要检测机构对其现行有效性进行必要的分析,判定标准可以不按标准管理流程进行分析、识别、受控;但是也应该按照文件管理进行必要控制。观点三:将现有标准进行分类管理,分为“受控标准”和“受控资料”;方法标准视为“受控标准”适用《标准管理程序》需要进行分析、识别、受控,并加盖受控章,保准受控状态并动态更新。判定标准“受控资料”适用《文件管理程序》识别机构现有版本与官方版本的一致性后即加盖“资料章“。请坛内各位大佬各抒己见,学生拜谢。
非受控文件一定需要加盖非受控章吗
各位老师,关于实验室分析用标准能否如下操作?将所有标准进行分类装订,编写目录,编制封面,在封面盖受控章,侧面骑缝受控章,编排受控编号。例如,将[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]、重金属、[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]所用标准分别归类装订,编写目录表明所含标准,封面写明类别和适用范围。期间有标准更新时,更换相关标准,并更新目录。这样可以吗?
能否将环保不下载下来的标准(发布稿)作为内部受控标准,盖上受控章后使用(ps:发布稿的标准上写着“本电子版为发布稿。请以中国环境出版社的正式标准文本为准”)?还是一定要正式版本?请问哪里可以购入或者下载正式版本?有没有什么相关的文件规定依据可供参考的?
实验室正在准则CMA认证,购买了五十多份标准,以后扩项,可能会有几百份标准,标准如何受控,便于管理、归档、查找,复印之后下发要写分发号,正版标准盖受控章之后,复印件不需要该受控章了吧,望大家一起指导?
一般试验室受控的标国家标准都是从标准出版社买的正规标准文件。如果现在随意在网上下载试验用的国家标准,盖上受控章就可以当做受控文件吗??
请教各位同行,关于受控标准中引用或者关联的下一级标准该怎么管理,需要受控吗?举例,标准A是按照17025受控的,但是A又引用了B1,B2,B3,那B1,B2,B3怎么管理?thanks!
如果是不在CMA中批准的检测技术标准,还需要受控吗?如果有评价业务,相关的评价标准需要受控吗?
原始记录、委托单中标准年号发生变化,修订表格的时候需要改受控编号吗?
替诺福韦杂质是一种化学物质,它是替诺福韦的同分异构体或相关化合物。替诺福韦是一种核苷酸逆转录酶抑制剂,用于治疗HIV和乙型肝炎。COTO标准品是一种高纯度的标准物质,用于测定替诺福韦及其杂质的纯度、含量和化学性质。通过与COTO标准品进行对比和分析,可以确定替诺福韦及其杂质的结构、组成和含量,从而保证替诺福韦的质量和安全性。在药物研发和生产过程中,COTO标准品的使用非常重要。它可以提供可靠的参照物,用于质量控制、药物分析和化学计量学研究。通过使用COTO标准品,可以确保替诺福韦及其杂质的准确性和可靠性,为药物的安全性和有效性提供保障。总的来说,COTO标准品在替诺福韦杂质的研究和控制中具有重要作用。通过使用COTO标准品,可以更好地了解替诺福韦及其杂质的性质和含量,从而确保药物的安全和有效性。同时,也需要加强生产过程中的管理和监督,加强质量标准和监管措施的执行力度,确保药物质量和安全。
[align=center][font=宋体][color=#4B2C4F]诺码标准[/color][/font][font=Arial][color=#4B2C4F]——[/color][/font][/align][align=left][font=宋体][color=#404040]是一个国际标准物质平台 [/color][/font][font=Arial][color=#404040], [/color][/font][font=宋体][color=#404040]是由美国 [/color][/font][font=Arial][color=#404040]NORMACCURATE [/color][/font][font=宋体][color=#404040]公司与北京诺码标准技术有限公司共同建立的集研发、生产、销售、服务为一体的标准物质服务企业 。[/color][/font][/align][align=left][font=宋体][color=#404040]诺码标准[/color][/font][font=宋体][color=#404040]严格执行[/color][/font][font=Arial][color=#404040]ISO17034[/color][/font][font=宋体][color=#404040]的标准物质生产体系,可在更短时间内为客户提供[/color][/font][font=宋体][color=#404040]优质准确[/color][/font][font=宋体][color=#404040]的标准物质。[/color][/font][/align][align=left][font=宋体][color=#404040]目前公司产品涵盖常用的农药残留标准物质、兽药残留标准物质、无机金属液标、阴离子液标、食品添加剂标准物质、环境化学类标准物质、生物毒素类标准物质、食品类基体质控样品、环境类基体质控样品等,主要应用于食品检测、环境化工、医药生物等多个行业领域。[/color][/font][/align][align=left][font=宋体][color=#404040]旗下子公司天津检通生物技术有限公司主要生产供应各类食品安全快速检测试剂产品、快速检测仪器和标准气体等产品。[/color][/font][/align][align=left][font=宋体][color=#404040]我们[/color][/font][font=宋体][color=#404040]致力于为客户的需求和使用着想,为各类检测单位用户[/color][/font][font=宋体][color=#404040]提供可靠和快速的产品和服务。[/color][/font][/align]
最近整理实验室资料,随手都看到很多国家标准方法,有最新的也有过期的,给人感觉很随意,难道外来文件不用受控吗?质量手册写得很好,但是实际上感觉流于形式了。你觉得是否要受控?还是谁都可以到处拿出一份方法标准什么的来?
实验室的受控标准可以直接从网络上下载电子版的吗,这种从网上下载的标准是否可以作为实验室的受控标准?
1、标准无受控编号,标准变更后无法全部追溯变更,有错用废旧标准的风险。2、标准长时间无查新,标准废替新发不掌握,更新不及时有错用废旧标准的风险。3、废旧标准无收回或无加盖"作费"章,有误用可能。4、现行有效标准没有购买正式板本,有文本错误的可能。5、新标准无宣贯记录,无法保证所有相关人员准确掌握。6、新标准启用无审批程序和记录,技术负责人责任不到位。7、标准物质与其它试剂混存,有交叉污染的风险。8、标准物质无期间核查记录,标准质量不掌控,对检测结果有影响。9、标准物质无法定证书,标准质量不保证,有结果失真风险。10、用容量瓶贮存标准物质,有测量准确性下降的风险。实例~?标物没有定值证书?标物存储温湿度等条件不适合?标物排放回收不符合要求?标物无使用购买记录?标准没有定期跟踪查新?标准没有统一受控管理?标准没有发放回收记录?标准没有修订日期,实施发布日期等信息受控清单?标准未能更新保持现行有效欢迎补充讨论!!
在内审中,试验工程师有受控标准,在工作中使用了自行打印的检测标准,如何进行原因分析,和制定整改措施。请大神赐教!
最近在整理文件,整理到外部文件,我们实验室用的标准是国际版,这个国际版的标准有中文翻译版,我原版已经受控,这个翻译版我是否也能够受控呢?纠结呢,总感觉中文翻译版不算正式批准的标准。
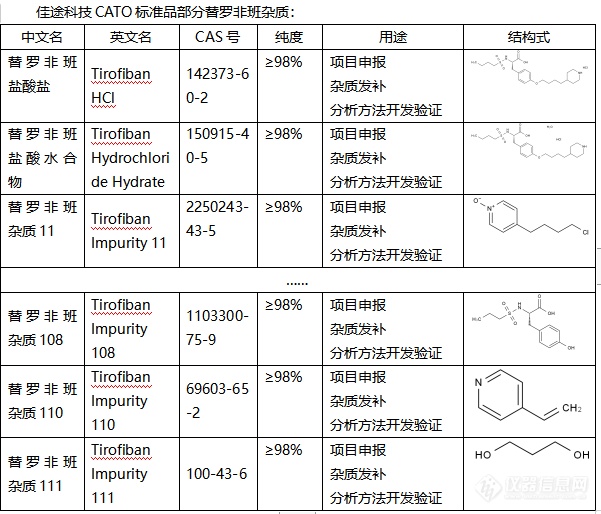
在当今的医疗领域,药物的质量控制至关重要,直接关系到患者的生命健康。替罗非班是一种广泛应用于心血管疾病治疗的药品,其质量控制尤为重要。而杂质分析作为药物质量控制的关键环节,能够准确评估药物的安全性和有效性。本文将重点探讨替罗非班杂质分析与CATO标准品应用研究的重要性。首先,杂质分析是确保药物质量的重要手段。在替罗非班的制备过程中,可能会产生一系列杂质,这些杂质的存在可能对药物的疗效和安全性产生不良影响。CATO标准品作为一种有效的分析工具,能够准确鉴定和量化替罗非班中的杂质,为药物的质量控制提供科学依据。其次,CATO标准品的应用有助于深入了解杂质的来源和性质。通过与标准品的比对分析,研究人员可以追溯杂质的产生途径,从而优化生产工艺,降低杂质的产生。此外,CATO标准品还可以用于评估杂质的毒性和风险,为药物的安全性评价提供有力支持。此外,CATO标准品在指导药物生产和改进方面也具有重要意义。通过对替罗非班中杂质的准确分析,生产商可以针对性地优化生产工艺、加强质量控制,从而提高药物的纯度和安全性。这不仅有助于保障患者的用药安全,还有助于提升企业的生产效益和市场竞争力。综上所述,替罗非班杂质分析与CATO标准品应用研究在药物质量控制中发挥着关键作用。通过深入研究替罗非班中的杂质,并借助CATO标准品这一强大工具,我们能够更好地了解杂质的来源、性质和影响,从而优化药物的生产工艺、提升药物的安全性和有效性。[img=,601,514]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021849065001_3752_6381568_3.png!w601x514.jpg[/img]欢迎有需要的各位联系
受控的文件是否一定要盖“受控”印章?——受控文件是否必须加盖“受控文件”印章,应视文件的受控管理方式和文件的实际用途而定。文件管理部门对提供实验室内部人员使用的实施修改受控的文件,应加盖“受控文件”章,其中包括对文件管理员本人使用的文件。“受控文件”印章中,可以包括受控级别、受控编号、受控起始时间、作废时间等项目。对实施检索受控管理的各类记录、档案,如原始记录、报告/证书副本、设备档案、人员技术档案、计量标准档案等,则应按照档案管理办法进行编目归档,不需要在每份文件上加盖“受控文件”章。 记录格式虽实施修改受控,一般不需加盖“受控文件”章。有的实验室在备案的记录格式上加盖“样张”,作为可对照的样板。当修改标准/规范或其他原因需要更新记录格式时,则应废除旧格式,并在发放新的记录格式的同时回收作废的记录格式,这需要履行一个更改申请、更改批准、有效表格发放、作废表格回收的程序,而不能图省事随意更改记录格式,实验室应做好发放文件的备案登记,以便于今后查找核对。有关人员在收取记录时,要识别记录格式是否为有效版本。记录格式的识别一般靠格式版本号或启用日期。 对不作为检测/校准依据,而仅作为文献资料提供技术人员查阅的规程汇编或标准汇编,不作受控管理,为防止误用,有的实验室给这类文件加盖了“参考资料”章。如果作为检测/校准依据,则应对其中作废的规程/标准作出明显的作废标记。
受控的文件是否一定要盖“受控”印章? 答:受控文件是否必须加盖“受控文件”印章,应视文件的受控管理方式和文件的实际用途而定。文件管理部门对提供实验室内部人员使用的实施修改受控的文件,应加盖“受控文件”章,其中包括对文件管理员本人使用的文件。“受控文件”印章中,可以包括受控级别、受控编号、受控起始时间、作废时间等项目。对实施检索受控管理的各类记录、档案,如原始记录、报告/证书副本、设备档案、人员技术档案、计量标准档案等,则应按照档案管理办法进行编目归档,不需要在每份文件上加盖“受控文件”章。记录格式虽实施修改受控,一般不需加盖“受控文件”章。有的实验室在备案的记录格式上加盖“样张”,作为可对照的样板。当修改标准/规范或其它原因需要更新记录格式时,则应废除旧格式,并在发放新的记录格式的同时回收作废的记录格式,这需要履行一个更改申请、更改批准、有效表格发放、作废表格回收的程序,而不能图省事随意更改记录格式,实验室应做好发放文件的备案登记,以便于今后查找核对。有关人员在收取记录时,要识别记录格式是否为有效版本。记录格式的识别一般靠格式版本号或启用日期。对不作为检测/校准依据,而仅作为文献资料提供技术人员查阅的规程汇编或标准汇编,不作受控管理,为防止误用,有的实验室给这类文件加盖了“参考资料”章。如果作为检测/校准依据,则应对其中作废的规程/标准作出明显的作废标记。
一般要加以控制的文件是指标准9001第4.2.1条要求的文件。那么,组织中非受控的文件有哪些呢?或者什么样的文件可以不加以控制呢?请随意发表意见和看法。
[size=18px][b]实验室或者说检验检测机构为了省事,能否在网上下载相关工作用到的标准(国家标准企业标准等等)然后纳入外来文件受控范围,打印出来盖“受控”标识这样是否会牵涉到一些问题会让CMA,CNAS评审组老师觉得做不行,不符合什么相关规定。因为我跟人觉得,日常实际工作中无论是用真金白银买来的正版还是网络资源下载的电子版,怎么来都完全无所谓,我主要是从评审角度去考虑 的,怕遗漏了去考虑其他因素。[/b][/size]
你们的标准查新都是从哪些渠道获得的?有受控吗?
现行环保有效受控标准及规范一览表
实验室把标准算是外来文件,这样的话是否都需要盖受控章呢
环境检测,需要采购纸质标准作为受控文件。现采购回来的一批标准,纸质版的 有的加了水印,有的加了防伪码标识,有的两种都有,是不是都可以用呢?还有电子版的 ,有的没有防伪码也没有水印,这种可以吗??
如题,大家受控文件目录中的受控文件有哪些?如何填写?这是我们的一个样子,如下:受控文件名称\文件编号\分发号\数量\存放地点\保管人质量手册 SC-2007 01 1 办公室 geniusiam程序文件 CX-2007 03 1 业务室 genius质量表格 GJ-2007 05 1 检测室 geniusiamnot作业指导书 ZY-2007 08 1 办公室 geniusiamnot质量手册 SC-2007 4 档案室 姜维这样填写有没有问题?问题1:质量手册存档的有4本,没有分发,是不是不用写分发号? 2:我觉得质量计划\内审管理评审报告\标准\外来文件\内部文件也该列入受控文件目录,对吗? 3:不管是手写的受控文件目录,还是打印的受控文件目录的更改、增加、作废也应按文件申请审批手续走.作废的盖作废章?4:外来文件(通知、通告等)什么时候、什么情况算作废?欢迎回帖!
标准和标准物质的问题与风险1、标准无受控编号,标准变更后无法全部追溯变更,有错用废旧标准的风险。2、标准长时间无查新,标准废替新发不掌握,有错用废旧标准的风险。3、废旧标准无收回或无加盖"作费"章,有误用可能。4、现行有效标准没有购买正式板本,有文本错误的可能。5、新标准无宣贯记录,无法保证所有相关人员准确掌握。6、新标准启用无审批程序和记录,技术负责人责任不到位。7、标准物质与其它试剂混存,有交叉污染的风险。8、标准物质无期间核查记录,标准质量不掌控,对检测结果有影响。9、标准物质无法定证书,标准质量不保证,有结果失真风险。10、用容量瓶贮存标准物质,有测量准确性下降的风险。欢迎老师补充