高效液相色普法测定甘草酸苷含量,甘草酸苷对照品峰面积与之前相比较偏高,导致含量偏高,请问有可能是哪些原因?

问题:四君子颗粒中甘草苷、甘草酸铵的检测对照品分析中甘草苷与甘草酸铵的分离度是?答案:62.445【活动奖励】因zgx3025(注册ID:v2844608)的答案不正确,所以取消本次获得的钻石币幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币mengzhaocheng(注册ID:mengzhaocheng)莫名其妙(注册ID:moyueqiu)http://ng1.17img.cn/bbsfiles/images/2016/03/201603031621_585902_1610895_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/03/201603031621_585903_1610895_3.png积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================四君子颗粒中甘草苷、甘草酸铵的检测样品制备制备方法1. 对照品:取甘草苷对照品、甘草酸铵对照品适量,精密称定,加甲醇制成每1 mL分别含甘草苷20 μg、甘草酸铵0.2 mg溶液,即得(甘草酸重量=甘草酸铵重量/1.0207)。2. 供试品:取本品装量差异项下的内容物3 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,密塞,称定重量,超声处理(功率250 W,频率40 KHz)30分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液15 mL,蒸干,残渣加甲醇使溶解,移至5 mL量瓶中,加甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。分析条件色谱柱Platisil ODS 250 x 4.6 mm,5 μm (Cat#:99503)流动相A:乙腈 B:0.05%磷酸溶液 梯度流速1.0 mL/min柱温30 ℃检测器UV 237 nm 进样量10 μL 色谱图对照品http://ng1.17img.cn/bbsfiles/images/2016/03/201603031020_585805_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 15.739 771814 49202 22131.352 0.998 -- 2 36.170 766340 93054 391608.534 1.043 62.445 *药典要求理论板数按甘草苷峰计算应不低于5000供试品http://ng1.17img.cn/bbsfiles/images/2016/03/201603031021_585807_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 15.784 475765 27766 18773.718 0.973 -- 2 36.033 152478 18510 403100.536 0.997 58.879 *药典要求理论板数按甘草苷峰计算应不低于5000本品种同时使用了Diamonsil C18、DiamonsilC18(2)两款色谱柱,在药典规定条件下进行甘草苷、甘草酸铵的检测,均满足药典要求。
建立食品中草酸含量测定的新方法—间接[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]。样品经处理后,加入过量且定量的氯化钙,使其与草酸根离子生成草酸钙沉淀,经离心分离后再利用[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url](AAS)法定量测定上清液中剩余Ca2+ 的含量,间接计算出食品中草酸的含量。在最佳条件下,该法的线性范围为0~8.0mg/L,回收率为98.1%~98.4%。本方法精密度高、灵敏度高、检出限低,适用于食品中草酸含量的测定。
[b]Q:四君子颗粒中甘草苷、甘草酸铵的检测,供试品溶液的前处理步骤是?A:供试品溶液:取本品装量差异项下的内容物3g,精密称定,置具塞锥形瓶中,精密加入甲醇25ml,密塞,称定重量,超声处理(功率250W,频率40KHz)30分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液15ml,蒸干,残渣加甲醇使溶解,移至5ml量瓶中,加甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。===============================================================【活动内容】1、每个工作日上午10:00左右发布一个关于应用数据库的应用问答题,版友根据题目给出自己理解的答案。2、每个工作日下午15:10公布参考答案。【活动奖励】幸运奖:抽奖软件,当天随机抽取3个或5个回答正确的版友ID号(最后一个ID号,截止至下午15:00),每人奖励[color=#ff0000]2钻石币[/color](抽奖人数≤10,抽取3个版友;抽奖人数>10,抽取5个版友);莫名其妙(注册ID:moyueqiu)999youran(注册ID:999youran)yy_0324(注册ID:yy_0324)大川之子,纵横四海(注册ID:chuangu120)dahua1981(注册ID:dahua1981)[img=,690,387]https://ng1.17img.cn/bbsfiles/images/2018/12/201812171515416757_7540_1610895_3.png!w690x387.jpg[/img][img=,690,387]https://ng1.17img.cn/bbsfiles/images/2018/12/201812171516149100_7965_1610895_3.png!w690x387.jpg[/img]积分奖励:所有回答正确的版友奖励[color=#ff0000]10个积分[/color](幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次[/b][align=left][color=#ff0000][b]PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。[/b][/color][/align][align=left][color=#ff0000][b] 下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。[/b][/color][/align][align=center]=======================================================================[/align]方法:HPLC基质:药品应用编号:103534化合物:甘草苷、甘草酸铵色谱柱:[url=http://www.dikma.com.cn/product/details-855.html]Platisil ODS 5μm 250 x 4.6mm[/url]样品前处理:1、对照品溶液:取甘草苷对照品、甘草酸铵对照品适量,精密称定,加甲醇制成每1ml分别含甘草苷20μg、甘草酸铵0.2mg溶液,即得(甘草酸重量=甘草酸铵重量/1.0207)。2、供试品溶液:取本品装量差异项下的内容物3g,精密称定,置具塞锥形瓶中,精密加入甲醇25ml,密塞,称定重量,超声处理(功率250W,频率40KHz)30分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液15ml,蒸干,残渣加甲醇使溶解,移至5ml量瓶中,加甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。色谱条件:色谱柱: Platisil ODS 250*4.6 mm,5 μm(Cat#:99503)流动相: A:乙腈 B:0.05%磷酸溶液流速: 1.0 mL/min柱温: 30 ℃检测器: UV 237 nm进样量: 10 μL文章出处:天津应用实验室关键字:四君子颗粒、甘草苷、甘草酸铵、Platisil C18、HPLC、2015药典摘要:Platisil C18检测四君子颗粒中甘草苷、甘草酸铵。图谱:[img]http://www.dikma.com.cn/u/image/2015/08/04/1438671548996616.png[/img][img]http://www.dikma.com.cn/u/image/2015/08/04/1438671551486259.png[/img][img]http://www.dikma.com.cn/u/image/2015/08/04/1438671554462333.png[/img]
甘草提取液,同样的条件,在Agilent ZOBAX Eclipse plus C18 和迪马铂金C18上跑出来的图相比,前者就硬是差一个最大的峰----甘草酸,用对照品进样也发现在前者上不出峰,后用100%乙腈冲很久才出来一大堆杂质峰,应该是吸附在柱子上了。请问这2种都是C18的柱子,为什么会有如此大的差别,前者为什么会产生强吸附?谢谢
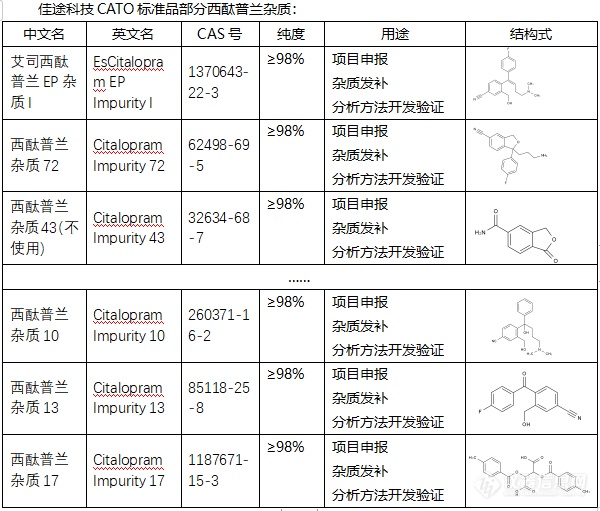
[font=宋体]◇关于西酞普兰杂质[/font][font=Helvetica][color=#333333][back=#f5f5f5]西酞普兰[/back][/color][/font][font=宋体][color=#333333][back=#f5f5f5],[/back][/color][/font][font=宋体][color=#333333][back=#f5f5f5]它[/back][/color][/font][font=Helvetica][color=#333333][back=#f5f5f5]是一种选择性5-羟色胺再摄取[/back][/color][/font][font=宋体][color=#333333][back=#f5f5f5]的[/back][/color][/font][font=Helvetica][color=#333333][back=#f5f5f5]抑制剂,[/back][/color][/font][font=宋体][color=#333333][back=#f5f5f5]它[/back][/color][/font][font=微软雅黑][color=#666666]作用[/color][/font][font=微软雅黑][color=#666666]主要在于[/color][/font][font=微软雅黑][color=#666666]中枢神经系统,[/color][/font][font=Helvetica][color=#333333][back=#f5f5f5]选择性地抑制5-HT转运体,[/back][/color][/font][font=宋体][color=#333333][back=#f5f5f5]从而阻止并且切断[/back][/color][/font][font=Helvetica][color=#333333][back=#f5f5f5]突触前膜对5-HT的再摄取[/back][/color][/font][font=宋体][color=#333333][back=#f5f5f5],[/back][/color][/font][font=微软雅黑][color=#666666][font=微软雅黑]增加突触间隙中[/font]5-羟色胺的浓度,从而起到改善情绪的作用[/color][/font][font=Helvetica][color=#333333][back=#f5f5f5]。[/back][/color][/font][font=宋体][color=#333333][back=#f5f5f5]西酞普兰不仅可以[/back][/color][/font][font=宋体][color=#333333][back=#f5f5f5]促进胃肠蠕动,主要是[/back][/color][/font][font=宋体][color=#333333][back=#f5f5f5]通过作用于胃肠道内的D2受体,使胃肠更快的蠕动;西酞普兰还可以刺激胃肠道内的5-HT4受体,使胃肠道液体分泌得更多,让肠胃消化和吸收更快。[/back][/color][/font][font=宋体][font=Calibri]CATO[/font][font=宋体]标准品提供的西酞普兰杂质[/font][/font][font=宋体]用途主要[/font][font=微软雅黑]是[/font][font=微软雅黑]用于分析[/font][font=微软雅黑]和质量控制的化学物质。[img=,600,511]https://ng1.17img.cn/bbsfiles/images/2024/02/202402051926582339_6789_6381607_3.png!w600x511.jpg[/img][/font][font=宋体][font=宋体]广州佳途科技股份有限公司,[/font][font=Calibri]CATO[/font][font=宋体]标准品厂家,提供西酞普兰[/font][/font][font=宋体]的全套[/font][font=宋体]杂质[/font][font=宋体],[/font][font=微软雅黑][color=#222222]严格的[/color][/font][font=微软雅黑][color=#222222]控制[/color][/font][font=微软雅黑][color=#222222]质量,通过全面的检测[/color][/font][font=微软雅黑][color=#222222],[/color][/font][font=微软雅黑][color=#222222]所有产品均能现货供应[/color][/font][font=微软雅黑][color=#222222]。[/color][/font]
最近做小儿七星茶颗粒甘草酸的测定时遇到了很奇怪的问题:对照品有峰,样品却只出杂质峰,开始怀疑是样品没有含量,可是拿以前做过的有含量的样品再做,却没峰了;后来吸一半对照品一半样品进样就出峰了,可是加对照品到样品中一起按标准处理后就又没有峰出来,怎么想都不明白问题出在哪里。所用的试剂换了好几次,也换人配了,结果还是一样没有,会不会是超声引起的呢,因为我们的超声机的功率只有80瓦,不过以前也做得出啊,大家帮帮忙,下面是标准【含量测定】 照高效液相色谱法(中国药典2005年版一部附录VI D)测定。 色谱条件与系统适用性试验 以十八烷基硅烷键合硅胶为填充剂;以甲醇-0.2mol/L醋酸铵溶液—冰醋酸(65:35:1)为流动相;检测波长为250nm。理论板数按甘草酸峰计算应不低于2000。 对照品溶液的制备 取甘草酸铵对照品适量,精密称定,加流动相制成每1ml含16μg的溶液,即得(折合甘草酸为15.672μg)。 供试品溶液的制备 取装量差异项下的本品内容物,混匀,研细,取约7g,精密称定,置50ml量瓶中,加流动相约45ml,超声处理(功率300W,频率40kHz)30分钟,放冷,加流动相至刻度,摇匀,滤过,取续滤液,即得。 测定法 精密吸取对照品溶液与供试品溶液各20μl,注入液相色谱仪,测定,即得。
摘要:建立胡黄连中香草酸和桂皮酸的含量测定方法。方法用双波长扫描法测定胡黄连中香草酸和桂皮酸的含量。结果香草酸。桂皮酸斑点峰面积3Il内稳定,香草酸回收率为103.86%,RSD=1.33%,桂皮酸回收率为103.16%,RSD=1.28%。结论该方法稳定,可行。具有实用性。 关键词:胡黄连 薄层扫描法 香草酸 桂皮酸 胡黄连具有保肝利胆、抗炎、抗真菌等药理作用。胡黄连含胡黄连素、胡黄连苷(I II III)、D-甘露醇、香草酸、肉桂酸、胡黄连醇成分。香草酸和桂皮酸是其中的两种抗菌成分。我们对胡黄连中香草酸、桂皮酸含量建立了薄层扫描法,以达到控制胡黄连的质量,从而为临床疗效提供保证。 1 仪器与试剂 药材:胡黄连,太原市药材公司;仪器:日本岛津CS--9301PC薄层扫描仪;手提式荧光灯(上海固村电光仪器厂);对照品:香草酸对照品(中国药品生物制品检定所);桂皮酸对照品溶液(省药检所提供e=0.604mg/50ml);硅胶GF254(青岛海洋化工厂)所用试剂均为分析纯。 2 实验条件 2.l 薄层层析条件:分别以石油醚-氯仿-丙酮-冰醋酸(10:4.4:10.1);正己烷-乙醚-冰醋酸(5:5:0.1);正己烷-氯仿-乙醚-冰醋酸(5:3:2:0.1)以及氯仿:甲醇(2:1)展开,多次比较发现正己烷。氯仿-乙醚-冰醋酸(5:3:2:0.4)分离效果好。 2.2 测定波长及主要扫描参数,分别对香草酸,桂皮酸对照品斑点在200nm-370nm扫描,在290nm处有最大吸收,350nm处无吸收,固定350nm为参比波长,290nm为测定波长。
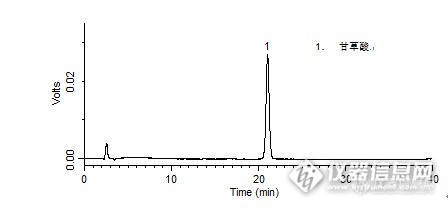
问题:玄麦甘桔含片中甘草酸的检测:USP拖尾因子是多少呢答案:1.009活动奖励:zengzhengce163(ID:zengzhengce163)sixingxing(ID:v2889187)千层峰(ID:jxyan)http://ng1.17img.cn/bbsfiles/images/2015/12/201512231541_579203_708_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/12/201512231541_579204_708_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/12/201512231542_579205_708_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/12/201512231542_579206_708_3.jpg【活动奖励】幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。玄麦甘桔含片中甘草酸的检测样品制备 制备方法对照品:取甘草酸对照品适量,精密称定,加80%甲醇制成每1 mL含0.2 mg的溶液。分析条件 色谱柱Platisil ODS 250 x 4.6 mm,5 μm (Cat#:99503)流动相乙腈:0.1%磷酸溶液=37:63 流速1 mL/min柱温30 ℃检测器UV 250 nm进样量5 μL色谱图对照品http://ng1.17img.cn/bbsfiles/images/2015/12/201512231017_579120_708_3.png 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 21.026 694197 26857 15108.406 1.009 -- *药典要求理论板数按甘草酸峰计算应不低于4000本品种同时使用了Leapsil C18色谱柱,在药典规定条件下进行甘草酸的检测,满足药典要求。

问题:玄麦甘桔胶囊中甘草酸的检测对照品分析中甘草酸的理论塔板数是?答案:15108.406【活动奖励】幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币捌道巴拉巴巴巴(注册ID:v3082413)翠湖园(注册ID:hhx050)m3071659(注册ID:m3071659)http://ng1.17img.cn/bbsfiles/images/2016/03/201603171519_587237_1610895_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/03/201603171519_587238_1610895_3.png积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================玄麦甘桔胶囊中甘草酸的检测样品制备 制备方法1. 对照品:取甘草酸对照品适量,精密称定,加80%甲醇制成每1 mL含0.2 mg的溶液。2. 供试品:取装量差异项下的本品内容物,研细,混匀,取约1 g,精密称定,置具塞锥形瓶中,精密加入80%甲醇25 mL,称定重量,超声处理(功率250 W,频率33 kHz)30分钟,放冷,再称定重量,用80%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。分析条件 色谱柱Platisil ODS 250 x 4.6 mm,5 μm (Cat#:99503)流动相乙腈:0.1%磷酸溶液=37:63 流速1 mL/min柱温30 ℃检测器UV 250 nm进样量5 μL色谱图对照品http://ng1.17img.cn/bbsfiles/images/2016/03/201603170956_587210_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 21.026 694197 26857 15108.406 1.009 -- *药典要求理论板数按甘草酸峰计算应不低于4000供试品http://ng1.17img.cn/bbsfiles/images/2016/03/201603170956_587211_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 22.033 991915 35292 14188.640 1.081 -- *药典要求理论板数按甘草酸峰计算应不低于4000本品种同时使用了Leapsil C18色谱柱,在药典规定条件下进行甘草酸的检测,满足药典要求。
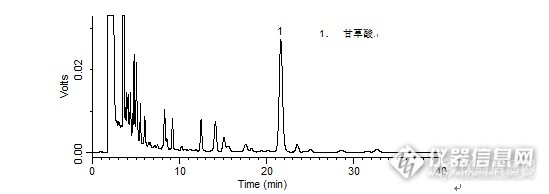
问题:玄麦甘桔颗粒中甘草酸的检测:用到了迪马哪几款色谱柱?答案:Platisil ODS,Leapsil C18获奖名单:WUYUWUQIU(ID:wulin321)m3071659(ID:m3071659)sixingxing(ID:v2889187)http://ng1.17img.cn/bbsfiles/images/2016/03/201603231529_587978_708_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/03/201603231529_587979_708_3.jpg【活动奖励】幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。玄麦甘桔颗粒中甘草酸的检测样品制备 制备方法1. 对照品:取甘草酸对照品适量,精密称定,加80%甲醇制成每1 mL含30 μg的溶液,摇匀,即得。2. 供试品:取装量差异项下的本品内容物,研细,混匀,取约1 g,精密称定,置具塞锥形瓶中,精密加入80%甲醇25 mL,称定重量,超声处理(功率250 W,频率33 kHz)30分钟,放冷,再称定重量,用80%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。分析条件 色谱柱Platisil ODS 250 x 4.6 mm,5 μm (Cat#:99503)流动相乙腈:0.1%磷酸溶液=37:63 流速1 mL/min柱温30 ℃检测器UV 250 nm进样量5 μL色谱图对照品http://ng1.17img.cn/bbsfiles/images/2016/03/201603230951_587901_708_3.png 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 21.299 413351 15834 15232.463 1.016 -- *药典要求理论板数按甘草酸峰计算应不低于4000供试品http://ng1.17img.cn/bbsfiles/images/2016/03/201603230951_587902_708_3.png 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 21.607 706476 26568 14700.090 1.065 -- *药典要求理论板数按甘草酸峰计算应不低于4000本品种同时使用了Leapsil C18色谱柱,在药典规定条件下进行甘草酸的检测,满足药典要求。
我们是用草酸酸化提取出土霉素。怎样测定药品中草酸残余量呢?我用的是高效液相色谱。用的是反向离子柱。
各位大虾:请教个问题,草酸与乙醛酸含量大概在1-4%之间的水溶液,怎么分析草酸与乙醛酸的含量?新建项目,用原来的色谱条件分不开,向各位讨教讨教。
草酸学名乙二酸,化学式HOOC-COOH。当我们从课本上了解了羧酸的化学性质,是不是也能推断出草酸的一般性质了?在我们身边,草酸一般用作除锈剂或者可以除去白衣衫上的墨水污迹,而它其实也是一种可以能致人死命的危险的化学物质。可是大家知道平时爱吃的巧克力中也含有草酸吗?不要慌张,这种危险情况极少出现。我们每天都通过许多不同渠道摄入草酸,草酸在很多食品中都有少量存在,而在少数食品中含量很高。可可就属于含量最高的食品之一,,每100克可可中含有500毫克草酸;绿色蔬菜中的草酸含量一般很高,每100克菠菜含600毫克,大黄含500毫克,甜菜、花生、茶中也有较多的草酸。平均一个人一天大约摄入150毫克草酸,而草酸的致死剂量是1500毫克左右。我们在普通的一天中会摄入这么多草酸吗?那么摄入草酸对我们人体有什么影响? 大黄在美国曾被称为“食用大黄”,在过去,人们常把它和糖放在一起炖了吃。大黄最出名的特性是治疗便秘,因为它能刺激肠道排出自然毒素——草酸。一碗炖烂的大黄里含有的草酸已经接近于使人中毒的剂量。第一次世界大战期间,由于有人把大黄叶当作蔬菜吃,以至于草酸中毒身亡。而吃巧克力则无须担心,无论你对巧克力多么喜爱,但巧克力中的草酸含量太低,就是你吃的无法下咽的时候,体内的草酸含量达不到让你腹泻的程度。 在大黄流行的时候,烹制大黄食品方法层出不穷,曾经使用铝锅来炖大黄,发现意想不到的好处:它能把铝锅“炖”的很干净。之所以有这样的效果,是因为草酸能把铝锅氧化膜和表面金属溶解掉。当然,这种方法还会使食者摄取铝元素造成潜在的危害。
对 草酸分析求救贴:http://www.instrument.com.cn/bbs/shtml/20080509/1256137/的回答: 草酸是一种常见的有机酸,分析方法很多,不同的样品和含量有对应不同的检测方法。在色谱法普及前,用酸碱滴定,氧化还原法,以及比色法都是有的,但这些一般适合常量分析,如果有干扰的,分析是很不准确的。从现在分析角度来看,色谱法是最佳的分析方法,分析简单,快速,但不同是色谱方法之间有很大的差异。现在色谱方法很多,都可以分析草酸,但要区别来看。簿层色谱法和纸色谱法是可以分析草酸的,但目前只能用于特定的范围,定量也不准确,操作相对繁琐。 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法直接分析草酸有点勉强,因为有二个羧基,沸点高。但可以用衍生的方法来分析草酸,这样的文献也不少,操作也是繁琐一些,也不是最佳的方法。 液相色谱法分析草酸是比较好的手段,根据不同的分离机理,有不同的类型:1反相色谱法:在酸抑制条件下,采用C18柱分析草酸这样的有机酸是有成功的报道,如果用纯水柱则效果更好,波长在210nm,其灵敏度因其有二个羧基响应是很大的,远高于其它有机酸。2离子交换法:采用液相的SAX柱,也可以分析草酸,不过淋洗盐的浓度要比较低,另外在SAX中出峰还是比较快的,复杂样品不是很适合。3离子对色谱法:从理论上讲采用离子对试剂是可以分析草酸的,但由于一般的离子对试剂的纯度问题,低紫外的吸收很高,而且试剂浓度不低,这样基线噪音会很大,对复杂样品不是很理想,而且TBA效果不好,应采用更高碳数的试剂,成本较高,灵敏度低。4离子排斥法:这种方法比较经典,采用专用的有机酸柱(就是离子排斥柱)有很多的文献报道,只是有这种柱子的人很少,我曾试分析过草酸,一般分析时间比C18柱长多了,草酸的保留时间长,但柱效不如C18的柱子,这种柱子用于分析混合有机酸是比较常见的。因为其流动相是很低浓度的稀硫酸,水不溶的样品不适合这种柱子。[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法:分析草酸比较方便的方法是用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法,灵敏度高,选择性好。[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]有碳酸盐体系和OH体系二种柱子,对于复杂化合物用OH体系柱子比较好,可以进行梯度分析,但要注意如果硫酸根离子浓度很高的话,对草酸测定会带来很大干扰。戴安另外还有一种离子排斥的抑制色谱法可测定有机酸。毛细管电泳,也有用于分析有机酸成功的报道,分析速度快,灵敏度高,但目前实用性不强,准确性欠佳。综上所述,草酸可用[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]的衍生法、液相的反相酸抑制法及离子排斥法以及抑制电导[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定相对比较合适和可靠。
各位大侠:草酸可以用色谱分析吗?用什么柱子可以啊,条件是什么啊?谢谢
目前我们分析草酸钴的杂质先将草酸钴在400度氧化,再加盐酸硝酸溶解试样,程序比较麻烦,而且易污染,有谁知道更简洁的处理样品的方法?
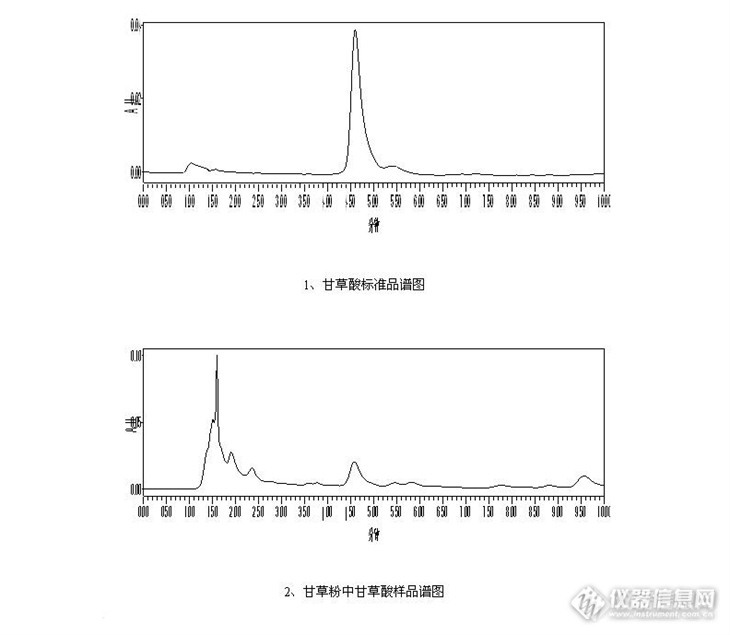
高效液相色谱法测定甘草制品中甘草酸的含量前言甘草酸是一味常用的中药,目前有关甘草的研究很多,甘草具有清热解毒,润肺止咳之功效。同时,我们也要注意甘草的副作用,过量的甘草会使到尿量及钠的排出减少,身体会积存过量的钠(盐分)引起高血压;水分储存量增加,会导致水肿。同时过多血钾流失引起的低血钾症,导致心律失常,肌肉无力。所以有高血压症状的人是不能食用甘草的,我们的父母有一种误区,觉得食用甘草可以清热解毒,殊不知其副作用也同样可怕。中药无毒论确实非常可怕啊!闲话少说,回到正题。http://ng1.17img.cn/bbsfiles/images/2013/09/201309190950_465407_2428063_3.jpg甘草切片的图片甘草的主要成分为甘草酸、甘草次酸和甘草苷等。甘草酸是最主要的有效成分。目前,我们使用的检测方法为高效液相色谱法,同时又该方法又有等度高效液相法和梯度高效液相色谱法。1、如果单纯检测甘草酸,我建议使用普通的高效液相色谱法,本单位所使用色谱柱为:Sunfire TM C18色谱柱,填料为5um,规格为4.6*150mm。所使用的仪器为Waters 2695,配备了2887 PDA全波段紫外检测器,可以根据需要提取不同波长的色谱图。如下为:甘草酸的色谱分离条件甲醇-0.2mol醋酸铵-冰醋酸(66:33:1) 检测波长为250nm 流速为1mL/min样品提取过程称取0.2克样品,加入1:1的甲醇水溶液,超声波提取20分钟,然后定容到100mL的容量瓶中。http://ng1.17img.cn/bbsfiles/images/2013/09/201309190952_465408_2428063_3.jpg2、本人查询了最新的2010版药典,发现检测的方法发生了变化,其核心变化就是检测的物质多了一个甘草苷,可以同时实现两种物质的分离,从分离学上来讲是非常有意义的。但是如果单纯的测定甘草酸,我觉得还是使用2005版药典的方法更好。以前的方法5分钟左右就可以出峰,10分钟就可以完成检测。但是采用新方法以后,一针样品要运行1个小时,对色谱柱和时间都是极大的浪费,当然在检测过程中,我们可以进行适当的优化,但是无疑是很劳民伤财的。

[align=center][b][font=宋体]虫草浓缩液中虫草酸和虫草素测定方法[/font][/b][/align][size=18px][font=宋体]虫草浓缩液由虫草水提物制得,用于化妆品原料。客户想测虫草浓缩液中虫草酸和虫草素,虫草酸又名甘露醇。[/font][font='Times New Roman','serif']1 [/font][font=宋体]试剂:乙腈(色谱级),超纯水,甲醇(分析纯),虫草酸和虫草素均购置北京索莱宝公司。[/font][font='Times New Roman','serif']2 [/font][font=宋体]标准品配制:称取一定量的虫草酸,用纯水溶解,定容,得到浓度为[/font][font='Times New Roman','serif']150 μg/mL[/font][font=宋体],待测;[/font][font=宋体]虫草素,用甲醇溶解,定容,得到浓度为[/font][font='Times New Roman','serif']220 μg/mL[/font][font=宋体],待测;[/font][font='Times New Roman','serif']3 [/font][font=宋体]样品制备:[/font][font='Times New Roman','serif']3.1 [/font][font=宋体]精密量取[/font][font='Times New Roman','serif']0.5 mL[/font][font=宋体]虫草浓缩液,分别用水定容至[/font][font='Times New Roman','serif']10 mL[/font][font=宋体]测定虫草酸,用甲醇定容至[/font][font='Times New Roman','serif']10 mL[/font][font=宋体]测定虫草素,过[/font][font='Times New Roman','serif']0.45 μm[/font][font=宋体]滤膜,待测。[/font][font='Times New Roman','serif']4 [/font][font=宋体]虫草素[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]条件:[/font][font='Times New Roman','serif']LC-20AT[/font][font=宋体]配制紫外检测器,[/font][font=宋体]波长:[/font][font='Times New Roman','serif']260 nm [/font][font=宋体];进样量:[/font][font='Times New Roman','serif']5μL[/font][font=宋体];色谱柱型号:[/font][font='Times New Roman','serif']Agilent Zorbax SB-C18(4.6 mm×250mm, 5 μm)[/font][font=宋体];柱温:[/font][font='Times New Roman','serif']30.0 [/font][font=宋体]℃;流速:[/font][font='Times New Roman','serif']0.8 mL/min[/font][font=宋体];流动相条件如表[/font][font='Times New Roman','serif']1[/font][font=宋体]:[/font][/size][align=center][img=,551,185]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311641477076_4077_1858223_3.jpg!w551x185.jpg[/img][/align][font='Times New Roman','serif'] [/font][size=18px][font=宋体]虫草酸[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]条件:[/font][font='Times New Roman','serif']Angilent infinit1260[/font][font=宋体]配制示差检测器,进样量:[/font][font='Times New Roman','serif']5[/font][font=宋体]μ[/font][font='Times New Roman','serif']L[/font][font=宋体];色谱柱型号:[/font][font='Times New Roman','serif']Agilent Zorbax SB-C18(4.6 mm[/font][font=宋体]×[/font][font='Times New Roman','serif']250 mm, 5 μm)[/font][font=宋体];[/font][font=宋体]柱温:[/font][font='Times New Roman','serif']30.0 [/font][font=宋体]℃,;流动相条件乙腈:纯水[/font][font='Times New Roman','serif']=80:20[/font][font=宋体];流速:[/font][font='Times New Roman','serif']0.5mL/min[/font][font=宋体]。[/font][/size][align=center][img=,690,265]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311642440362_8441_1858223_3.jpg!w690x265.jpg[/img][/align][align=center][b][font=宋体]虫草素标准品色谱图[/font][/b][/align][align=center][img=,683,269]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311642555977_2623_1858223_3.jpg!w683x269.jpg[/img][/align][align=center][b][font=宋体]虫草浓缩液中虫草素色谱图[/font][/b][/align][b][font=宋体]结果:虫草浓缩液中虫草酸含量([/font]7.65 mg/mL [font=宋体]),虫草素含量([/font]2.65[/b][font='Times New Roman','serif']μg/mL[/font][b][font=宋体])。[/font][font=宋体]小结:测定虫草素的过程中发现流动相梯度洗脱,回到起始梯度是需要平衡时间久一些,虫草素含量较低,虫草酸含量比较高。示差检测器也是进样前需要稳定[/font]2[font=宋体]小时左右,才能保证实验数据稳定性。[/font] [/b]
朋友们,帮帮我啊,草酸铜用碘量法做,不知是什么老是干扰终点,兰色老是回头,该选什么样的方法做呢?有没有这方面的分析标准,我怎么找也找不到
采用乙酸乙酯提取样品中的氟烯草酸,凝胶渗透色谱(GPC)净化,[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱联用仪测定,外标法定量。结果表明,本方法的线性浓度范围为0.05~1μg/ml,线性相关系数为0.9983,平均回收率在70.35%~95.24%之间,相对标准偏差在3.22%~6.69%之间,说明方法的可靠性和精密度良好,并且该方法的定量限为5μg/kg,完全可以达到日本肯定列表的检测要求。
今天拿草酸来做红外都得不到红外谱图,好像光透不来。用模具直接压和用KBr压片都不行。不知道是为什么。有谁做过草酸的红外啊,告诉要怎么 做。晕了。谢谢。

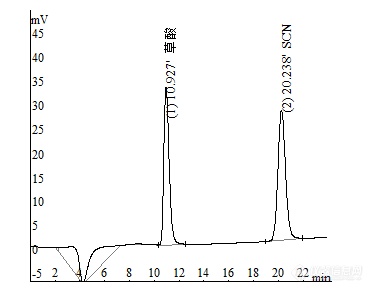
在一次失效分析的过程中,发现别的实验室在分析我们自己的日常样品中,有比较明显的草酸的结果显示,但是自己内部的测试结果没有很好地显示出来。因为之前没有需要报告草酸这个项目,所以也没有买过草酸的标准溶液。为了研究内部是否可以测试草酸,需要另外购买草酸的标准液(Fig-1)。[align=center] [img=,435,422]https://ng1.17img.cn/bbsfiles/images/2023/09/202309011031011657_3849_2942222_3.jpg!w435x422.jpg[/img][/align] 等草酸标液到了之后,开始配置不同浓度的标液,从低到高开始尝试进样,但是都没有在谱图上发现明显的出峰。到了150ppm仍然没有检测到很明显的峰,这是比较不正常的。在观察谱图时,发现在22分钟左右有一个翘起来的部分,有点像峰(Fig-2)。但是因为之前的程序设定了运行时间都是22分钟,是不是因为运行时间太短,导致草酸的峰还没有出来呢。[align=center] [img=,690,357]https://ng1.17img.cn/bbsfiles/images/2023/09/202309011031471109_959_2942222_3.jpg!w690x357.jpg[/img][/align] 经过更改程序文件,把出峰时间改到26分钟,在22-23分钟左右看到一个非常明显的草酸出峰(Fig-3),果然是之前的运行时间太短了,导致草酸不能够显示出来。[align=center][img=,690,213]https://ng1.17img.cn/bbsfiles/images/2023/09/202309011032034570_2099_2942222_3.jpg!w690x213.jpg[/img][/align] 为了进一步,进行了草酸的标准曲线验证。在新程序条件运行下,草酸在不同浓度都可以显示出来,可以得到一个非常好标准曲线,R2的值达到0.99以上(Fig-4)。[align=center][img=,690,468]https://ng1.17img.cn/bbsfiles/images/2023/09/202309011032193998_3826_2942222_3.jpg!w690x468.jpg[/img][/align][align=center]另外,有继续进行了草酸的回收率实验。把草酸标准溶液加入到正常的7个阴离子溶液中,草酸能够明显检测出来(Fig-5),回收率大概是107%。[/align][align=center][img=,690,328]https://ng1.17img.cn/bbsfiles/images/2023/09/202309011032369340_1786_2942222_3.jpg!w690x328.jpg[/img][/align] [font=等线]在新程序下运行,发现在日常的产品中也可以明显检测出草酸(Fig-6)。这证明了的确是之前的运行时间太短,导致草酸检测不出来.[/font][align=center][img=,690,502]https://ng1.17img.cn/bbsfiles/images/2023/09/202309011032564960_9557_2942222_3.jpg!w690x502.jpg[/img][/align] 经过这次的草酸寻峰计,还得出了一个教训。在以后研究新的物质时,要提前好好查下相关的文献,因为不同的柱子和淋洗方法都会影响到物质的出峰。如果没有资料可查,需要尝试在尽可能的运行时间去检测,以免有峰遗漏。
[font=宋体][size=13px]中[/size][/font][font=宋体][size=13px][color=#444444][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定尿液中草酸和硫氰酸盐[/color][/size][/font][align=center]黄选忠[/align][align=center](湖北兴山县疾病预防控制中心,湖北兴山,443711)[/align]摘要:【目的】建立以SH-AC-3型阴离子交换柱为分离柱,[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url][font=times new roman][size=18px]-[/size][/font]抑制电导检测法同时测定尿样中草酸和硫氰酸盐的新方法。【方法】研究用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定尿液中草酸和硫氰酸盐的可能性,通过试验优化确定了各项色谱条件。【结果】以SH-AC-3型阴离子交换柱为分离柱,以10.0mmol/LNa2CO3为淋洗液,流量为1.0mL/min,等度洗脱可将草酸和硫氰酸盐与尿液中大量共存的氯化物、磷酸盐和硫酸盐等常见阴离子完全分离,通过抑制电导检测,草酸和硫氰酸盐的峰面积、峰高均与其浓度在0.20~30.0mg/L范围内呈良好的线性关系,相关系数[size=13px][i]r[/i][/size]在0.9991~0.9999,方法应用于尿液中草酸和硫氰酸盐的同时测定,加标回收率在93.2%~105.2%[size=13px]和95.3%~99.8%,[/size], 5次平行测定的相对标准偏差(RSD)小于5%(n=5)。【结论】本方法可用于尿液中草酸和硫氰酸盐的同时测定。关键词:[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法;[font=times new roman][color=#444444]尿液[/color][/font];硫氰酸盐;草酸;中图分类号:O652.63 文献标识码: 文章编号:尿中硫氰酸盐(SCN-)含量是人体接触氰化物的一项生物接触指标[1],而SCN-又是致甲状腺肿物质,可阻滞甲状腺激素合成,尤其对胎儿和婴儿的智力和神经系统发育存在较大的风险[2],因此监测人血、尿等生物标本中的SCN-含量具有重要意义。目前,测定尿中微量SCN-的方法主要有分光光度法[3-5]、衍生-顶空[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法[6-7]等,其中分光光度法和[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法都存在氰化物的干扰问题。尿结石约70%为草酸钙结石,草酸代谢异常所引起的高含量草酸尿是泌尿系结石形成的主要原因[8]。因此准确测定尿中草酸含量对研究结石形成机理、结石的鉴别等均具有重要意义。目前测定尿中草酸的方法主要有光度法包括络合物褪色比色法[9]和催化光度法[10-11]、催化荧光法[12-13]、高效液相色谱法[14-15]和毛细管电泳法[16]等,而比色法、光度法、荧光法等光谱分析方法因特异性差样品要进行前处理,操作繁杂,高效液相色谱法和毛细管电泳法均需要专用仪器使其应用受限。[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法以其操作简便、试剂消耗少、可自动化和多组分同时测定的优势现已成为阴离子分析的首选方法[17],并成功应用于尿液中草酸[17-18]和SCN- [19-20]的分别测定,用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定尿液中草酸和SCN-似未见报道。本工作拟定的以SH-AC-3型阴离子交换柱为分离柱,10.0mmol/LNa2CO3溶液为淋洗液, 1.0mL/min的流量等度洗脱,[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]-抑制电导检测法同时测定尿液中草酸和硫氰酸盐的新方法,草酸和SCN-的含量均在0.20~30.0mg/L范围内与其峰高和峰面积呈良好的线性关系(相关系数r在0.9991~0.9999),方法应用于尿液中草酸和SCN-的同时测定,加标回收率分别为:95.0%~101.1%和95.5~100.5%,5次平行测定的相对标准偏差(RSD)小于3%,以3倍信噪比(3N/b)计算草酸和SCN-最低检出限分别为0.04mg/L和0.03mg/L。1、试验部分1.1主要仪器CIC-100型[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url](青岛盛瀚色谱公司,编号15601),抑制器:自再生抑制器,检测器:电导检测器,定量环体积为25μL;SHA—15自动进样器(青岛盛瀚色谱公司,编号AS1518050);SH-AC-3型阴离子交换柱(250×4.0mm i.d,青岛盛瀚色谱公司,批号:1602037);SH-AC-3型保护柱(50×4.0mm i.d,青岛盛瀚色谱公司,批号:1602037)。1.2 仪器工作条件及参数设置色谱仪:柱箱温度35℃,电流:75mA,量程:1档。自动进样器:全定量环取样,取样后清洗(每针之间),置换量70μL,取样量25μL,扎针深度4mm。1.3主要试剂草酸标准溶液:1000 mg/L,称取优级纯草酸(H2C2O42H2O)0.1401g用超纯水溶解定容至100mL;SCN-标准溶液:1000 mg/L,称取烘干的优级纯硫氰酸钾0.1673g用超纯水溶解定容至100mL。Cl-标准溶液:GBW(E)080268,1000 mg/L;SO4-2标准溶液:GBW(E)080266,1000 mg/L;H2PO4-标准溶液:1000 mg/L,称取分析纯磷酸二氢钾0.1402g用超纯水溶解定容至100mL。用前将各种标准溶液用纯水分别稀释成含草酸和SCN-10.0mg/L(A液)、100.0mg/L(B液)混合标准应用液备用。无水碳酸钠(分析纯,国药集团化学试剂有限公司),草酸(优级纯,国药集团化学试剂有限公司),硫氰酸钾(优级纯,国药集团化学试剂有限公司)。试验所用其他试剂均为AR级,试验用水为超纯水(18.2ΜΩcm)。1.4 试验方法1.4.1 标准曲线的绘制 取混合标准应用液(A液)0.20、0.50和1.00mL及B液0.50、1.0、1.50、2.00和3.00 mL于10mL容量瓶中加纯水至刻度,混匀,配制成含草酸和SCN-均为0.20~30.0 mg/L的标准系列,各管取1.5mL于样品瓶中,启动自动进样器进样分别测定各组分的峰面积(S)和峰高(H),以S及H对各组分浓度(C)绘制工作曲线。1.4.2尿样的采集 用清洗干净并干燥的聚乙烯瓶采集尿样50mL储存于4℃冰箱待测定。1.4.3 尿样测定 取新鲜尿样经8000转/min离心10min,取上清液用高纯水稀释10倍后分别用C18柱净化、用0.22μm滤膜过滤后取1.5mL于样品瓶中,启动自动进样器进样测定各组分的S和H,以标准曲线法定量,同时进行加标回收试验。2、结果与讨论2.1 色谱条件的选择2.1.1 淋洗液的选择 试验结果表明,当以SH-AC-3型阴离子交换柱为分离柱,以Na2CO3+NaHCO3溶液为淋洗液,其浓度配比在6 mmol/L+1 mmol/L~6 mmol/L+3 mmol/L时,均可将草酸和硫氰酸盐与尿液中的氯化物、磷酸盐和硫酸盐等常见阴离子完全分离,各组分的分离度R(相对于后续组分,如磷酸盐的R是相对于硫酸盐的,下同)可达1.5及以上,但硫氰酸盐的保留时间(T)长达24min以上,分析效率低下。为缩短硫氰酸盐的T提高分析工作效率,以洗脱能力较强的Na2CO3溶液进行了淋洗试验,结果显示当Na2CO3溶液浓度分别为8.0、10.0和12.0 mmol/L时,硫氰酸盐的T分别缩短至21、20和19分多钟,且草酸和硫氰酸盐与尿液中的磷酸盐和硫酸盐等阴离子完全分离,试验结果见表1。考虑到Na2CO3溶液浓度大,相应的抑制电流也高,不利于抑制器的使用[17],在保证适宜的R和较短的T的情况下,试验选择10.0mmol/LNa2CO3溶液为淋洗液。[align=center]表1 Na2CO3溶液浓度选择试验结果(流量1.0 ml/min)[/align][table][tr][td=1,2][align=center]组分[/align][/td][td=2,1][align=center]8.0mmol/L[/align][/td][td=2,1][align=center]10.mmol/L[/align][/td][td=2,1][align=center]12.0mmol/L[/align][/td][/tr][tr][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][/tr][tr][td][align=center]SO4-2[/align][/td][td][align=center]10.245[/align][/td][td][align=center]3.07[/align][/td][td][align=center]8.606[/align][/td][td][align=center]2.60 [/align][/td][td][align=center]7.868 [/align][/td][td][align=center]2.34[/align][/td][/tr][tr][td][align=center]草酸[/align][/td][td][align=center]13.121[/align][/td][td][align=center]8.15[/align][/td][td][align=center]10.891[/align][/td][td][align=center]9.45[/align][/td][td][align=center]9.828[/align][/td][td][align=center]10.18 [/align][/td][/tr][tr][td][align=center]SCN- [/align][/td][td][align=center]21.665[/align][/td][td][align=center]/[/align][/td][td][align=center]20.151[/align][/td][td][align=center]/[/align][/td][td][align=center]19.177 [/align][/td][td][align=center]/[/align][/td][/tr][/table]2.1.2 色谱柱的选择 以10.0mmol/LNa2CO3溶液为淋洗液、流量1.0mL/min等度洗脱,考察了青岛盛翰色谱公司生产的SH-AC-1型和SH-AC-3型阴离子交换柱对草酸和硫氰酸盐与氯化物、磷酸盐和硫酸盐等常见阴离子的分离情况,结果表明,在此条件下SH-AC-1型柱虽能将草酸与常见阴离子完全分离,但硫氰酸盐至少在90min内未出峰,而SH-AC-3型柱不但可将草酸和硫氰酸盐与氯化物、磷酸盐和硫酸盐等常见阴离子完全分离,且硫氰酸盐的T在21min以内,故本试验选择SH-AC-3型阴离子交换柱为分离柱。2.1.3淋洗液流量的选择 对于相同浓度的淋洗液,不同的流量组分的T和R的将发生改变。试验结果表明,当淋洗液流量从0.8mL/min增加至1.2mL/min时,硫酸盐、草酸和硫氰酸盐的T逐渐变短,R逐渐变小,但硫酸盐和草酸的R远大于1.5达到完全分离的标准,见表2。在保证待测组分与干扰离子完全分离的前提下尽量使用较低的流量,以使系统有较低的压力,淋洗液流量选定为1.0mL/min。[align=center]表2 不同淋洗液流量试验结果(10.0mmol/LNa2CO3)[/align][table][tr][td=1,2][align=center]组分[/align][/td][td=2,1][align=center]0.8ml/min[/align][/td][td=2,1][align=center]1.0ml/min[/align][/td][td=2,1][align=center]1.2ml/min[/align][/td][/tr][tr][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][/tr][tr][td][align=center]SO4-2[/align][/td][td][align=center]10.471[/align][/td][td][align=center]2.65[/align][/td][td][align=center]8.726[/align][/td][td][align=center]2.54 [/align][/td][td][align=center]7.331 [/align][/td][td][align=center]2.46 [/align][/td][/tr][tr][td][align=center]草酸[/align][/td][td][align=center]13.856[/align][/td][td][align=center]9.34[/align][/td][td][align=center]11.097[/align][/td][td][align=center]9.24 [/align][/td][td][align=center]9.540 [/align][/td][td][align=center]8.95 [/align][/td][/tr][tr][td][align=center]SCN- [/align][/td][td][align=center]24.793[/align][/td][td][align=center]/[/align][/td][td][align=center]20.383[/align][/td][td][align=center]/[/align][/td][td][align=center]17.350 [/align][/td][td][align=center]/[/align][/td][/tr][/table]2.1.4 柱箱温度的确定 考察了柱温在30℃、35℃和40℃时各组分的分离效果,结果显示,在30℃~40℃范围内,草酸和硫氰酸盐均能与氯化物、磷酸盐和硫酸盐等常见阴离子完全的分离,且随着柱温的升高组分的T稍微缩短,R逐渐下降,草酸的S和H均随着柱温的升高而增长,从30℃上升35℃,增长10%左右,35℃上升40℃,增长6%左右;硫氰酸盐的S随着柱温的升高基本保持不变,而其H随着柱温的升高而增长,从30℃上升35℃,增长7%左右,35℃上升40℃,增长9%左右;在保证适宜的T和较高的R的情况下,尽量采用较低的柱温,本试验确定柱箱温度为35℃,这也是产品说明书推荐的柱箱温度。2.2标准曲线按照1.4.1配制标准系列,测定各管的峰面积(S)和峰高(H),以S、H对浓度(C)绘制标准曲线,其标准曲线的线性范围、回归方程、相关系数r(回归曲线的截距、斜率和r由仪器软件给出)列于表3。从表3可见,以峰面积计算的草酸标准曲线的线性优于峰高,硫氰酸盐则反之,同时分段计算的标准曲线的线性较好,故在计算结果时草酸和硫氰酸盐可分别用峰面积和峰高计,并根据样品浓度范围采用分段计算的回归方程来计算,以减少测量误差,尤其对低含量的样品。其中,含10.0mg/L的草酸和硫氰酸盐标准溶液色谱图见图1。[align=center]表3 标准曲线试验结果[/align][table][tr][td=1,2][align=center]组分[/align][/td][td=3,1][align=center]以峰面积计[/align][/td][td=2,1][align=center]以峰高计[/align][/td][/tr][tr][td][align=center]线性范围/mg/L[/align][/td][td][align=center]回归方程[/align][/td][td][align=center]相关系数/r[/align][/td][td][align=center]回归方程[/align][/td][td][align=center]相关系数/r[/align][/td][/tr][tr][td=1,3][align=center]草酸[/align][/td][td][align=center]0.20~10.0[/align][/td][td][align=center]S=96700C-17000[/align][/td][td][align=center]0.99957[/align][/td][td][align=center]H=3320C-770[/align][/td][td][align=center]0.99930 [/align][/td][/tr][tr][td][align=center]10.0~30.0[/align][/td][td][align=center]S=112800C-177600[/align][/td][td][align=center]0.99996[/align][/td][td][align=center]H=3862C-6116[/align][/td][td][align=center]0.99993[/align][/td][/tr][tr][td][align=center]0.20~30.0[/align][/td][td][align=center]S=107100C-53210[/align][/td][td][align=center]0.99929[/align][/td][td][align=center]H=3671C-1995[/align][/td][td][align=center]0.99928[/align][/td][/tr][tr][td=1,3][align=center]SCN- [/align][/td][td][align=center]0.20~10.0[/align][/td][td][align=center]S=114600C+621.7[/align][/td][td][align=center]0.99913[/align][/td][td][align=center]H=2718C-108.6[/align][/td][td][align=center]0.99999[/align][/td][/tr][tr][td][align=center]10.0~30.0[/align][/td][td][align=center]S=124700C-141500[/align][/td][td][align=center]0.99971[/align][/td][td][align=center]H=2934C-2787[/align][/td][td][align=center]0.99984[/align][/td][/tr][tr][td][align=center]0.20~30.0[/align][/td][td][align=center]S=119200C-22340[/align][/td][td][align=center]0.99949[/align][/td][td][align=center]H=2835C-609.3[/align][/td][td][align=center]0.99972[/align][/td][/tr][/table]2.3 方法的精密度和检出限对2种浓度的标准溶液各平行测定5次,计算各成分峰面积的RSD,同时测定仪器30min的基线噪声,以3倍基线噪声除以标准曲线(峰面积计)的斜率(3N/b)计算草酸和硫氰酸[align=center][img=,374,293]https://ng1.17img.cn/bbsfiles/images/2020/09/202009021441333779_9714_3389662_3.png!w374x293.jpg[/img][/align][align=center]图1 标准溶液色谱法图[/align]盐的检出限,5次平行测定的RSD在0.86%~2.26%,方法的重复性良好,方法的检出限分别为0.04 mg/L和0.03 mg/L,见表4。[align=center]表4 方法的精密度和检出限[/align][table][tr][td=1,2][align=center]组分[/align][/td][td=3,1][align=center]标液1[/align][/td][td=3,1][align=center]标液2[/align][/td][td][align=center]检出限/mg/L[/align][/td][/tr][tr][td]浓度/mg/L[/td][td]平均峰面积[/td][td][align=center]RSD/%[/align][/td][td][align=center]浓度/mg/L[/align][/td][td]平均峰面积[/td][td][align=center]RSD/%[/align][/td][/tr][tr][td][align=center]草酸[/align][/td][td][align=center]1.00 [/align][/td][td][align=center]78077.3[/align][/td][td][align=center]2.10[/align][/td][td][align=center]10.00 [/align][/td][td][align=center]955086.6[/align][/td][td][align=center]0.86 [/align][/td][td][align=center]0.04[/align][/td][/tr][tr][td][align=center]SCN- [/align][/td][td][align=center]1.00 [/align][/td][td][align=center]116110.4[/align][/td][td][align=center]2.26[/align][/td][td][align=center]10.00 [/align][/td][td][align=center]1146968.6[/align][/td][td][align=center]1.16 [/align][/td][td][align=center]0.03 [/align][/td][/tr][/table]2.4 [size=12px] [/size]共存阴离子及抗坏血酸的影响由于尿液中含有大量的有机物和氯化物、磷酸盐和硫酸盐等阴离子,尿样通过C18柱的净化可以消除有机物的影响,尿液经10倍稀释以降低氯化物、磷酸盐和硫酸盐的影响。考察了氯化物等3种阴离子对草酸和硫氰酸盐测定结果的影响,结果表明,氯化物、磷酸盐和硫酸盐的保留时间远小于草酸和硫氰酸盐,且500mg/L Cl-、300mg/L H2PO4-、SO4-2(H2PO4-、SO4-2完全分不开合并为一个峰)不影响50mg/L的草酸、3mg/L的测定,分离色谱图见图2。[align=center][img=,379,281]https://ng1.17img.cn/bbsfiles/images/2020/09/202009021441474631_778_3389662_3.png!w379x281.jpg[/img][/align][align=center]图2 常见阴离子与草酸和硫氰酸盐分离色谱图[/align]尿液中可能含有抗坏血酸,在碱性条件下,抗坏血酸易发生降解反应,而草酸是抗坏血酸的降解产物之一,影响草酸的准确测定,有研究显示在15.0mmol/LNaHCO3溶液(pH=8.3)中40mg/L的抗坏血酸在80min内未降解为草酸[17],本试验使用10.0mmol/LNa2CO3溶液(pH≈11.1)为淋洗液,pH值远大于8.3,样品从进样到草酸出峰需要11min多钟,这段时间尿液中的抗坏血酸可能降解生成草酸而影响其测定。试验用纯水配制30mg/L的抗坏血酸观察其降解情况,结果表明,本试验条件下30mg/L的抗坏血酸降解产生约0.3mg/L的草酸,试验采用亚硫酸盐(SO3-2)抑制抗坏血酸的降解,这与在易氧化药物制剂中加入亚硫酸盐以提高药物稳定性的方法有相似原理。[align=center][img=,517,262]https://ng1.17img.cn/bbsfiles/images/2020/09/202009021442032319_2305_3389662_3.png!w517x262.jpg[/img][/align][align=center]图3 抗坏血酸降解抑制试验结果[/align][align=center]曲线1、30mg/L抗坏血酸(黑色)2、1+50 mg/L的SO3-2(粉红色)[/align][align=center] 3、[size=12px]30mg/L抗坏血酸+10mg/L草酸(蓝色)4、3+50 mg/L的SO[/size][size=12px]3[/size][size=12px]-2[/size][size=12px](桔红色)[/size][/align]试验结果显示,50mg/L的SO3-2可抑制30mg/L抗坏血酸的降解,见图3,且至少在120min内30mg/L抗坏血酸对10.0mg/L的草酸的峰面积与峰高无明显影响(增加值5%)。同时50mg/L的SO3-2对草酸和硫氰酸盐的测定结果无明显影响(误差5%),见图4。[align=center][img=,565,254]https://ng1.17img.cn/bbsfiles/images/2020/09/202009021442164802_4125_3389662_3.png!w565x254.jpg[/img][/align][align=center]图4 50mg/L的SO3-2对草酸和硫氰酸盐测定结果的影响[/align][align=center]曲线1、10mg/L草酸和硫氰酸盐(蓝色)[/align][align=center] 2、1+50 mg/L的SO3-2(粉红色)[/align]2.5尿液测定及回收率试验结果按试验方法1.4.3的步骤操作取1.5mL样液于样品瓶中,启动自动进样器进样测定各组分的峰面积(S)和峰高(H),以标准曲线法定量,同时进行加标回收试验。3份尿液草酸和[align=center]表5 尿液测定及回收率试验结果(以峰面积计)[/align][table][tr][td=1,2][align=center]组分[/align][/td][td=3,1][align=center]尿液1[/align][/td][td=3,1][align=center]尿液2[/align][/td][td=3,1][align=center]尿液3[/align][/td][/tr][tr][td][align=center]本底/mg/L[/align][/td][td][align=center]加入量[/align][align=center]/mg/L[/align][/td][td][align=center]回收率/%[/align][/td][td][align=center]本底/mg/L[/align][/td][td][align=center]加入量/mg/L[/align][/td][td][align=center]回收率[/align][align=center]/%[/align][/td][td][align=center]本底[/align][align=center]/mg/L[/align][/td][td]加入量/mg/L[/td][td]回收率/%[/td][/tr][tr][td][align=center]草酸[/align][/td][td][align=center]4.71[/align][/td][td][align=center]10.0[/align][/td][td][align=center]101.1[/align][/td][td][align=center]6.21[/align][/td][td][align=center]5.0[/align][/td][td][align=center]97.0[/align][/td][td][align=center]14.83[/align][/td][td][align=center]2.0[/align][/td][td][align=center]95.0[/align][/td][/tr][tr][td][align=center]SCN-[/align][/td][td][align=center]0.21[/align][/td][td][align=center]10.0[/align][/td][td][align=center]100.5[/align][/td][td][align=center]0.45[/align][/td][td][align=center]5.0[/align][/td][td][align=center]97.2[/align][/td][td][align=center]0.72[/align][/td][td][align=center]2.0[/align][/td][td][align=center]95.5[/align][/td][/tr][/table]硫氰酸盐的测定结果分别在4.71mg/L~14.83mg/L和0.21mg/L~0.72mg/L,加标回收率分别为:95.0%~101.1%和95.5~100.5%,结果见表5。其中尿液2的加标色谱图见图5.[align=center][img=,574,253]https://ng1.17img.cn/bbsfiles/images/2020/09/202009021442298329_66_3389662_3.png!w574x253.jpg[/img][/align][align=center]图5 尿液2及其加标色谱图[/align]曲线1、尿液[align=center] 2、尿液加5mg/L草酸和硫氰酸盐[/align]3 小结本工作采用国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]设备,建立了以青岛盛翰色谱公司生产的SH-AC-3型阴离子交换柱为分离柱,10.0mmol/LNa2CO3为淋洗液、流量1.0mL/min等度洗脱,抑制电导检测-[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定尿液中草酸和硫氰酸盐的分析方法。方法具有良好的重现性和准确性,操作简便快速,尿样通过C18柱的净化可以消除有机物的影响,尿液稀释10倍后可降低氯化物、磷酸盐和硫酸盐的影响。方法以自动进样器进样,降低检验人员的工作强度,提高了工作效率,适用尿液中草酸和硫氰酸盐的同时测定。参考文献1)中华人民共和国卫生部.GBZ209-2008职业性急性氰化物中毒诊断标准.北京:人民卫生出版社,20082)顾 欣,黄士新,李丹妮,等.乳中硫氰酸盐对人类健康的风险评估[J],中国兽药杂志,2010,44(9):45-523)WS/T39-1996.尿中硫氰酸盐的吡啶-巴比妥酸分光光度测定方法.北京:中国标准出版社,19974)冯翠霞,林丽玲,黄辉涛.分光光度法测定尿中硫氰酸盐的异烟酸-吡唑酮[J],中国职业医学,2009,36(6):501,5045)黄选忠,汪 波,舒开继等.异烟酸-巴比妥酸分光光度法测定尿硫氰酸盐[J],山东化工,2019,48(20):106-107,1126)钟良康,方波. 超短柱顶空[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定尿中硫氰酸盐[J],中国卫生检验杂志,2005,15(5):568,6287)武和平,武景福.尿中硫氰酸盐的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]测定法[J],职业与健康,2005,21(1):40-418)马腾骧,孙 光. 现代泌尿外科学[M].天津:天津科学技术出版社,2000:587-5889)李桂兰.锆-偶氮胂Ⅲ络合物比色法测定尿草酸[J].临床检验杂志,1997,15(2):86-8710)张爱梅,贾丽萍,牛学丽.表面活性剂增敏阻抑动力学光度法测定痕量草酸[J].分析化学,2003,31(9):1115-111811)麻全生,杨文初.铬酸钾氧化甲基红催化光度法测定微量草酸[J].理化检验化学分册,1998,37(7):309-31012)冯素玲,陈小兰,樊 静,等.抑制动力学荧光法测定草酸[J].分析化学,2000,28(5):621-62313)陈兰化,赵丹华.催化荧光法测定痕量草酸[J].光谱学与光谱分析,2003,23(1):203-20414)廖贤平,宋光庆.HPLC法同时测定尿液中草酸和枸橼酸含量的方法学评价及临床应用[J].武警医学院学报,2010,19(1):47-5015)彭 婕,郭卫红,谈恒山,等.高效液相色谱法测定人尿液中草酸的含量[J].中国医院药学杂志,2006,26(3):299-30116)谈绮文,郭 玮,顾梅秀,等.高效毛细管电泳法测定尿液中微量草酸和柠檬酸[J].中华检验医学杂志,2014,37(4):281-28417)杭义萍,卢祝靓子,杨春英.抗坏血酸存在下[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法直接测定尿液中草酸含量的研究[J].分析科学学报,2014,33(11):1307-131118)颜金良,高 杰,颜勇卿,等.[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法快速测定人尿液中草酸含量研究[J],中国卫生检验杂志,2009,19(3):554-55519)郭爱华,袁 佗,王 玮.[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法快速测定人尿中的硫氰酸盐[J],环境与职业医学,2015,32(6):593-59620)何 漪,王 钟,刘月月,等.抑制电导检测-[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定人尿中硫氰酸盐[J].现代预防医学,2017,44(22):4165-4167
草酸亚铁的确定,是分析草酸根还是分析铁含量,那种分析方法更有效,如何分析?
有哪位老师有用HPLC成功检测样品中草酸残留的案例么?我目前在草酸检测过程中,采用通用的纯水柱时空白死体积处的未知峰对草酸有干扰,采用RP18时草酸的保留得到了改善,但是草酸峰拖尾,且调节方法无改善。谢谢
其实,下面这个应用确切说不应该说是“抢先看”了,因为前几天我们在微信中已经分享了。只是论坛上没有这些应用,于是赶紧发布一下,已经看过的,请飘过哈~~根据国家药典委员会官方网站发布的2015药典“四君子颗粒”公示方法,迪马科技率先进行了此项目的检测,详细应用如下:四君子颗粒中甘草苷、甘草酸铵色谱柱:Diamonsil Plus 5 μm C18, 250 x 4.6 mm流动相:A:乙腈 B:0.05% 磷酸溶液 梯度流速:1.0 mL/min柱温:30℃检测器:UV 237 nm进样量:10 μL对照品溶液http://mmbiz.qpic.cn/mmbiz/sZguaRbQouv2HerhsR5EcrFIEicAd5N1FlfbFzZ7gZibVYc7ZDiafy1aa3adeAXEcoxraNOckqsFwicNxia5F7HG6Gg/640?tp=webp&wxfrom=5药典要求理论塔板数按甘草苷峰计算应不低于5000,而Diamonsil Plus C18 检测的理论塔板数为10814.879,高出药典要求。供试品溶液http://mmbiz.qpic.cn/mmbiz/sZguaRbQouv2HerhsR5EcrFIEicAd5N1F5vNgwbQPicPicjVCqICzDtAZXejMEMxXUMd22ZgMoTXiaK5wFBSIWqdHw/640?tp=webp&wxfrom=5药典要求理论塔板数按甘草苷峰计算应不低于5000,而Diamonsil Plus C18 检测的理论塔板数为10042.045,也高出药典要求。
草酸测水分选用卡尔费休水分仪的时候草酸会干扰并且附着在电极上方,在测定过程吸水导致测定结果偏大;选用快速水分仪105℃测定时间5min草酸会升华。请教下各位这个草酸的水分测定是不是可以用快去水分仪降低温度去测定,又或者是使用减压干燥80℃消失的重量就是水分这种方式去测定?
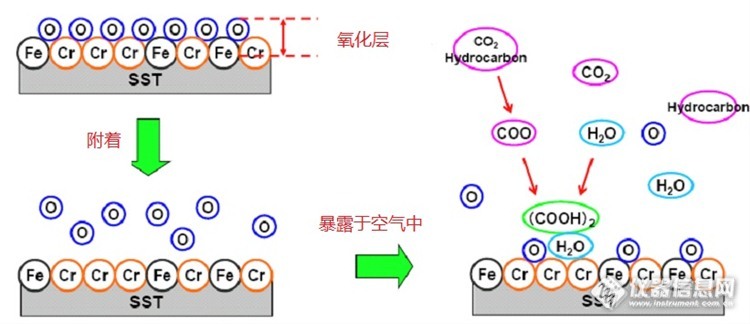
最近在某一产品的来料的离子色谱(IC型号:Dionex DX-500) 监控中发现阴离子的总数值有不断上升的趋势,且不断逼近规格线(spec)。按相关的文件规定,一旦这些监控数据超过规格线,这些来料是不能接收。当我们将这些异常情况反馈给供应商后,供应商查找了他们出货之前同一批的IC监控数据,没有发现异常。但是我们把这些样品返回给他们,他们测试的IC结果跟我们的测试结果很类似,都偏高。这些样品出了什么问题呢?难道是这批样品在转运或者保存时被污染了?我们决定努力去找这出其中的根源。 http://ng1.17img.cn/bbsfiles/images/2014/12/201412232237_528586_2942222_3.jpg 首先,我们对原始数据进行了分析。通过分析,发现这批样品中有个未知的离子的趋势跟总离子的趋势很类似,最近的走势也是不断往上扬。所以初步判断这个未知离子的增加可能是这批产品的总阴离子不断上升的原因。 http://ng1.17img.cn/bbsfiles/images/2014/12/201412232237_528587_2942222_3.jpg 那这个未知离子是什么呢?查阅相关的文献和结合这个未知离子的保留时间,怀疑这个未知离子可能是草酸(草酸盐)。我们找来草酸钠试剂,用UDI水溶解它,配成100ug/L的草酸钠溶液。当把配好的草酸钠溶液注射到离子色谱中,发现草酸根保留时间(10.237min)跟平时样品中未知离子保留时间(10.317min)很相近。所以基本确认这个未知离子就是草酸盐。 http://ng1.17img.cn/bbsfiles/images/2014/12/201412232238_528588_2942222_3.jpg 为了进一步确认这个未知离子就是草酸盐,我们还进行了加标实验。加标实验结果得到的重复回收率是103%。这就进一步证明了这个未知离子就是草酸(草酸盐)。 http://ng1.17img.cn/bbsfiles/images/2014/12/201412232238_528589_2942222_3.jpg 那这些草酸(盐草酸)是怎么来的呢?这些样品从供应商转运到我们的工厂,整个过程是用保鲜膜密封好的。整个运转过程没有拆包过程,所以这些样品是不会跟外界有任何的接触。按常理来说,这些样品应该不会受到污染的。通过与供应商的交流,了解到这些样品是在供应商那边储存了一段时间(~3个月),才运转到我们的公司。难道是供应商的存储地方有草酸盐,渗透到样品里而污染了样品?经过供应商的再三确认,他们存储样品的仓库是绝对没有草酸盐。那草酸盐是产品在自己存储的时候,自己产生的草酸盐? 我们测试了不同存储时间的产品,得到一个令人诧异的结果:这些样品的草酸值和总阴离子的值跟存储之间有着很好的关联。在前6个月里,草酸和总阴离子的值随着存储时间的增加而增加,但过了6个月之后基本趋于稳定。 http://ng1.17img.cn/bbsfiles/images/2014/12/201412232240_528590_2942222_3.jpg 产品在存储时是已经密封的,跟它接触的可能也就是从保鲜膜外面渗透进去的空气和水分,难道空气和水分会和这些产品发生反应而产生出草酸(草酸盐)吗?从上面的数据可以知道草酸(草酸盐)产生的过程应该是非常缓慢的。那怎么去验证这个猜测呢? 我们选了两个不同存储时间的2批(#1:存储时间不到一个月,#2存储时间~3个月)样品,放到恒温恒湿烘箱中进行测试(测试条件:温度85℃,湿度85%,持续时间100小时)。我们分别用离子色谱测量这2批样品的阴离子(经过恒温恒湿测试和没有测试各测试一组)的值。最后的结果显示:经过恒温恒湿测试后,草酸跟明显增加,但是其他离子却减少了。 http://ng1.17img.cn/bbsfiles/images/2014/12/201412232242_528591_2942222_3.jpg 这说明了在恒温恒湿测试过程中,其他离子因为水汽的冲洗而不断减少;但因为整个测试过程中因为发生了某些反应而产生了草酸(草酸盐),故草酸(草酸盐)没有减少反而增加了。 产品主要是有三个部件组合而成(#1:FX;#2:LB;#3:Baseplate);那草酸(草酸盐)是由哪个部件产生的呢?通过研究和实验,我们发现草酸跟增加主要是这个部件(#3:Base Plate)。 http://ng1.17img.cn/bbsfiles/images/2014/12/201412232243_528592_2942222_3.jpg 我们知道部件(Base Plate )的成份主要是不锈钢(Fe,Cr,Ni)。所以我们对草酸(草酸盐)产生的原理做了下面的推断:草酸(草酸盐)增加是由于在部件(Base Plate )的表面发生水解反应。整个化学反应过程是因为大气中的CO2和水汽在部件(Base Plate )的Fe,Cr的催化作用下发生了化学反应,不断产生草酸并附着在部件(Base Plate )的表面。 http://ng1.17img.cn/bbsfiles/images/2014/12/201412232243_528593_2942222_3.jpg

10,抽取5个版友);中奖名单:zgx3025(注册ID:v2844608)mengzhaocheng(注册ID:mengzhaocheng)千层峰(注册ID:jxyan)馨语(注册ID:huangdm)m3071659(注册ID:m3071659)http://ng1.17img.cn/bbsfiles/images/2017/02/201702281511_01_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2017/02/201702281511_02_1610895_3.jpg【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================天南星中草酸钙针晶的含量测定方法:HPLC基质:药品应用编号:102945化合物:草酸钙针晶固定相:Diamonsil C18(2)色谱柱/前处理小柱:Diamonsil 5μm C18(2), 250 x 4.6mm色谱条件:色谱柱:Diamonsil C18 250 mm× 4.6 mm, 5μm(Cat#:99603) 流动相: 0. 5% KH2PO4 -H3PO4水溶液( pH 2.3) 流速: 0.7 mL/min 柱温: 25 ℃ 进样量: 10 μL 检测器: UV 210 nm文章出处:中国实验方剂学杂志 2010, 16(11):30-31关键字:天南星, HPLC, 草酸钙针晶, Diamonsil C18, 钻石二代, 含量测定谱图:摘要:目的:建立天南星中的草酸钙针晶的含量测定方法。方法:采用HPLC法,Diamonsil C18柱(4.6 mm×250 mm,5μm)色谱柱;流动相0.5%KH2PO4-H3PO4水溶液(pH 2.3),流速0.7 L.min-1;检测波长210 nm;柱温28℃。结果:草酸在0.06~1.20μg线性关系良好(r=0.999 9)。平均回收率为100.89%(n=5),RSD为1.07%。结论:本法快速、灵敏、准确、可靠、重复性好,可用于天南星草酸钙针晶定量研究。http://www.dikma.com.cn/Public/Uploads/images/107-5.JPG