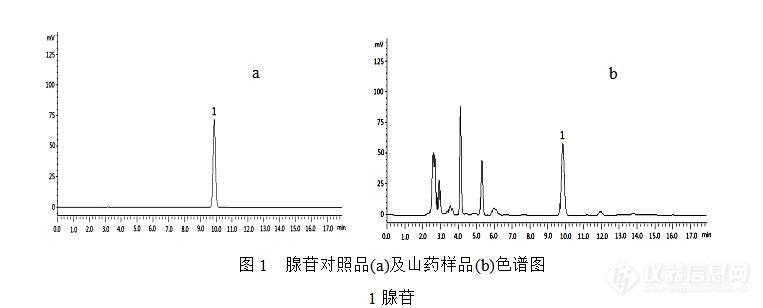
[align=center][b]HPLC测定不同来源山药中腺苷和脱氢表雄酮的含量[/b][/align] 山药(Dioscoreae Rhizoma)是薯蓣科植物薯蓣([i]Dioscorea opposita [/i]Thunb.)的干燥块茎,具有补脾养胃、生津益肺、补肾涩精的功能,是国家卫生部公布的药食两用的中药。然而在2015版《中国药典》一部中只收载了性状、鉴别、检查和浸出物等项目,缺少含量测定项指标,不足以对山药质量进行全面有效的控制。DHEA是人体肾上腺素的一种,国内外研究已经证实,DHEA对预防和治疗心血管疾病、增强免疫力、延缓衰老等均有一定效果,是山药中的重要活性成分之一。另外,腺苷具有舒张血管、降低血压、减慢心律、抑制血小板聚集、松弛血管平滑肌等生理活性。长期以来,由于对山药品种的评价和改良工作进展缓慢,目前仍然存在山药种植品种杂乱,缺乏综合性优良的品种。因此,本研究对包括野生山药在内的不同来源山药中的腺苷、DHEA含量进行测定,旨在为山药质量标准建立提供参考依据,也为山药品种驯化和选育提供一定的研究基础。[b][b]1 仪器和试药[/b][/b]LC-20AD高效液相色谱仪,配备紫外可见检测器(日本,岛津公司);ME204电子天平(德国Mettler Toledo公司),KQ-E型超声波清洗器(昆山市超声仪器有限公司)。脱氢表雄酮标准品(阿拉丁,批号为H1408213),腺苷标准品(中国食品药品检定研究院,批号为110879-200202);甲醇为色谱纯,水为娃哈哈纯净水,其他试剂均为分析纯。山药样品采自河南省温县山药种植基地。[b][b]2 方法与结果2.1标准储备溶液的制备[/b][/b]精密称取腺苷对照品6.61 mg置25 mL容量瓶中,加15 %甲醇溶解稀释至刻度,摇匀,配制成浓度为264.40 μgmL[sup]-[/sup][sup]1[/sup]的腺苷标准品储备溶液。精密称取DHEA对照品7.62 mg置50 mL容量瓶中,加甲醇溶解稀释至刻度,摇匀,配制成浓度为152.40 μgmL[sup]-[/sup][sup]1[/sup]的DHEA标准品储备溶液。[b][b]2.2样品的处理[/b][/b]2.2.1 腺苷样品的处理取本品粉末(过3号筛)约1.0 g,精密称定,置具塞锥形瓶中,精密加入15%甲醇l0 mL,密塞,摇匀,称定质量,超声处理30 min,放冷,再称定质量,用15%甲醇补足减失的重量,12000 rmin[sup]-[/sup][sup]1[/sup]离心15 min,取上清液,0.45 μm微孔滤膜滤过,取续滤液作为供试品溶液。2.2.2 DHEA样品的处理取本品粉末(过3号筛)约3.0 g,精密称定,置具塞锥形瓶中,精密加入甲醇l5 mL,密塞,摇匀,称定质量,超声处理1 h,放冷,再称定质量,用甲醇补足减失的重量,摇匀,0.45μm微孔滤膜滤过,取续滤液作为供试品溶液。[b][b]2.3 色谱条件[/b][/b]2.3.1 腺苷色谱条件:色谱柱:Aglient Extend XDB C18柱(4.6 mm×250 mm,5 μm);流动相:磷酸盐缓冲液(pH6.5) -甲醇(94:6,[i]v/v[/i]);流速:1 mLmin[sup]-[/sup][sup]1[/sup];柱温:30 °C; 检测波长:260 nm;进样量:10 μL。HPLC图见图1。2.3.2 DHEA色谱条件:色谱柱:Welch Ultimate XB-C18柱(4.6 mm×250 mm,5 μm);流动相:甲醇-水(62:38,[i]v/v[/i]);流速:0.6 mLmin[sup]-[/sup][sup]1[/sup];柱温:30 °C; 检测波长:204 nm;进样量:10 μL。HPLC图见图2。[img=,690,278]https://ng1.17img.cn/bbsfiles/images/2019/07/201907031540228286_5423_3451954_3.jpg!w690x278.jpg[/img][img=,690,300]https://ng1.17img.cn/bbsfiles/images/2019/07/201907031540280876_3707_3451954_3.jpg!w690x300.jpg[/img][b][b]2.4标准曲线的绘制[/b][/b]精密吸取腺苷标准品储备溶液0.5,1,3,5,8,10 mL分别置于10 mL量瓶中,加甲醇定容至刻度,摇匀,按上述色谱条件进样,以峰面积值 Y为纵坐标,腺苷浓度X为横坐标绘制标准方程为:[i]Y[/i]=34197.2[i] X[/i]+25515.1,[i]r[/i]=0.9999,表明腺苷在13.22 ~ 264.40 μgmL[sup]-[/sup][sup]1[/sup]浓度内与峰面积线性关系良好。精密吸取DHEA标准品储备溶液1 mL置于10 mL量瓶中,加甲醇定容至刻度,摇匀,得15.24 μgmL[sup]-[/sup][sup]1[/sup]的DHEA使用溶液。分别精密吸取DHEA使用溶液0.5,1,3,5,8,10 mL置于10 mL量瓶中,加甲醇定容至刻度,摇匀,按上述色谱条件进样,以峰面积值 Y为纵坐标,DHEA浓度X为横坐标绘制标准方程为:[i]Y[/i]=13042.7 [i]X[/i]-1836.3,[i]r[/i]=0.9999,表明DHEA在0.76 ~ 15.24 μgmL[sup]-[/sup][sup]1[/sup]浓度内与峰面积线性关系良好。[b][b]2.5 重复性试验[/b][/b] 取同一供试品粉末6份,精密称定,按“2.2”项下方法处理,按“2.3”项下色谱条件测定峰面积。结果腺苷和DHEA峰面积的RSD分别为1.87 %和1.91 % (n=6),表明方法重复性良好。[b][b]2.6 精密度试验[/b][/b]精密吸取同一供试品溶液10 μL,按上述色谱条件连续进样6次,测定腺苷、DHEA峰面积值,其RSD分别为0.92 %和1.03 % (n=6),表明仪器及进样精密度良好。[b][b]2.7 稳定性试验[/b][/b] 精密吸取同一供试品溶液,室温放置,分别在0,2,4,8,12,24,48 h进样分析。测定腺苷、DHEA峰面积值,其RSD分别为2.07 %和1.65 % (n=6),表明供试品溶液在48 h内稳定性良好。[b][b]2.8 回收率[/b][/b]分别称取已知含量的样品6份,精密称定,分别加入相当含量的腺苷和DHEA对照品溶液,按“2.2”项下供试品溶液的制备方法制备供试品溶液,分别进行测定,计算回收率。结果腺苷、DHEA平均加样回收率为98.10 % (RSD=1.40 %)和97.72 % (RSD=1.15 %),结果见表1、2。[align=center][b]表1 山药样品中腺苷的加样回收率实验结果(n=6)[/b][/align][table][tr][td][align=center]取样量/g[/align][/td][td][align=center]样品中量/mg[/align][/td][td][align=center]添加量/mg[/align][/td][td][align=center]测得量/mg[/align][/td][td][align=center]回收率/%[/align][/td][td][align=center]平均回收率/%[/align][/td][td][align=center]RSD/%[/align][/td][/tr][tr][td][align=center]0.5014[/align][/td][td][align=center]0.1604 [/align][/td][td][align=center]0.1586[/align][/td][td][align=center]0.3141[/align][/td][td][align=center]96.88 [/align][/td][td=1,6][align=center]98.10[/align][/td][td=1,6][align=center]1.40[/align][/td][/tr][tr][td][align=center]0.5011[/align][/td][td][align=center]0.1604 [/align][/td][td][align=center]0.1586[/align][/td][td][align=center]0.3201[/align][/td][td][align=center]100.72 [/align][/td][/tr][tr][td][align=center]0.4989[/align][/td][td][align=center]0.1596 [/align][/td][td][align=center]0.1586[/align][/td][td][align=center]0.3147[/align][/td][td][align=center]97.76 [/align][/td][/tr][tr][td][align=center]0.4997[/align][/td][td][align=center]0.1599 [/align][/td][td][align=center]0.1586[/align][/td][td][align=center]0.3141[/align][/td][td][align=center]97.22 [/align][/td][/tr][tr][td][align=center]0.5001[/align][/td][td][align=center]0.1600 [/align][/td][td][align=center]0.1586[/align][/td][td][align=center]0.3159[/align][/td][td][align=center]98.28 [/align][/td][/tr][tr][td][align=center]0.5012[/align][/td][td][align=center]0.1604 [/align][/td][td][align=center]0.1586[/align][/td][td][align=center]0.3154[/align][/td][td][align=center]97.74 [/align][/td][/tr][/table][align=center][b]表2 山药样品中DHEA的加样回收率实验结果(n=6)[/b][/align][table][tr][td][align=center]取样量/g[/align][/td][td][align=center]样品中量/mg[/align][/td][td][align=center]添加量/mg[/align][/td][td][align=center]测得量/mg[/align][/td][td][align=center]回收率/%[/align][/td][td][align=center]平均回收率/%[/align][/td][td][align=center]RSD/%[/align][/td][/tr][tr][td][align=center]1.5013[/align][/td][td][align=center]0.0293 [/align][/td][td][align=center]0.0305[/align][/td][td][align=center]0.0589[/align][/td][td][align=center]97.13 [/align][/td][td=1,6][align=center]97.72 [/align][/td][td=1,6][align=center]1.15 [/align][/td][/tr][tr][td][align=center]1.5024[/align][/td][td][align=center]0.0293 [/align][/td][td][align=center]0.0305[/align][/td][td][align=center]0.0591[/align][/td][td][align=center]97.72 [/align][/td][/tr][tr][td][align=center]1.4997[/align][/td][td][align=center]0.0292 [/align][/td][td][align=center]0.0305[/align][/td][td][align=center]0.0597[/align][/td][td][align=center]99.86 [/align][/td][/tr][tr][td][align=center]1.5001[/align][/td][td][align=center]0.0293 [/align][/td][td][align=center]0.0305[/align][/td][td][align=center]0.0589[/align][/td][td][align=center]97.21 [/align][/td][/tr][tr][td][align=center]1.4987[/align][/td][td][align=center]0.0292 [/align][/td][td][align=center]0.0305[/align][/td][td][align=center]0.0587[/align][/td][td][align=center]96.64 [/align][/td][/tr][tr][td][align=center]1.5011[/align][/td][td][align=center]0.0293 [/align][/td][td][align=center]0.0305[/align][/td][td][align=center]0.0591[/align][/td][td][align=center]97.80 [/align][/td][/tr][/table][b][b]2.9 结果分析[/b][/b]精密称取不同来源的山药粉末,按“2.2”项下方法制备供试品溶液,分别进样,记录峰面积积分值,外标法计算腺苷及DHEA的含量。结果如下表3所示。[align=center][b]表3 不同来源山药药材中腺苷及DHEA的含量([i]n[/i]=3)[/b][/align][table][tr][td][align=center]编号[/align][/td][td][align=center]样品来源[/align][/td][td][align=center]腺苷含量/%[/align][/td][td][align=center]DHEA含量/mg/kg[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]种植铁棍山药[/align][/td][td][align=center]0.032[/align][/td][td][align=center]19.50 [/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]野生山药1[/align][/td][td][align=center]0.027[/align][/td][td][align=center]5.38 [/align][/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]野生山药2[/align][/td][td][align=center]0.024[/align][/td][td][align=center]3.29[/align][/td][/tr][tr][td][align=center]4[/align][/td][td][align=center]驯化野生山药雌株[/align][/td][td][align=center]0.037[/align][/td][td][align=center]24.05 [/align][/td][/tr][tr][td][align=center]5[/align][/td][td][align=center]驯化野生山药雄株[/align][/td][td][align=center]0.040[/align][/td][td][align=center]62.25 [/align][/td][/tr][tr][td][align=center]6[/align][/td][td][align=center]紫山药[/align][/td][td][align=center]ND[/align][/td][td][align=center]ND[/align][/td][/tr][/table] 从测定结果看,不同来源山药中腺苷和DHEA含量差别较大,可能由于品种及生长环境的差异造成。研究表明,驯化野生山药雄株中腺苷和DHEA含量最高,显著高于野生山药中的含量,说明驯化过程对野生山药的改良起到了很好的积极作用。另外,驯化野生山药雄株中DHEA含量比公认的营养成分较高的铁棍山药高出3倍左右,进一步说明该山药品质的优异性。 另外,紫山药中并未检测到腺苷和DHEA两种成分的存在,这可能由于紫山药自身品种差异有关。[b][b]3 小结和讨论[/b][/b]3.1 DHEA提取条件优化 在DHEA测定前处理时,本实验曾根据李军等人的优化方法,采用甲醇-丙酮(6:4)超声提取、水浴蒸干、二氯甲烷多次萃取等主要工序对山药中DHEA进行提取,该方法提取效果较好,DHEA可以被较好的富集和检测。但是由于提取过程复杂,实验重复性和加样回收率较难控制。本实验采用甲醇、乙醇、甲醇-丙酮(1:1,[i]v/v[/i])等溶剂对山药样品进行超声1h提取,结果发现,四种溶剂提取效果没有明显差异,因此选用甲醇做为最终提取溶剂。 本实验采用的方法大大简化了山药中DHEA的提取过程,减少了有毒试剂的使用,缩短了提取时间,且提取率与李军的方法相比没有显著的差异。3.2 小结 本研究对山药中腺苷和DHEA成分的提取和测定条件进行优化,为山药质量标准建立和质量评价提供参考依据。另外,研究对包括野生、种植、驯化品种等不同来源山药中腺苷和DHEA指标含量进行测定,为山药品种的选育和驯化提供一定的研究基础。
5009.121-2016流动相用的是甲醇+0.02mol/L乙酸铵(10+90),标准溶液按照标准配置,发现峰形会有拖尾的现象。看了一些文献,有调节pH改善峰形的,但是有加酸调成酸性的,或者加碱调成碱性,请教大家在工作中怎么改善脱氢乙酸峰形?
我采用关松荫主编的《土壤酶及其研究方法》书中所述方法测量土壤中的脱氢酶,在绘制TTC还原产物TPF标准曲线的过程中遇到了难题。书中的方法是:“加NaHSO3(亚硫酸氢钠)还原TTC。”我加NaHSO3后溶液不显色。 试了几次仍然是不显色。 后来又查了些资料,用保险粉可以使TTC还原但是要用乙酸乙酯定容。试了一下保险粉果然可以显色,但是,当向显色后的溶液里加甲醇定容的时候,颜色又都消失了。现在这个很麻烦,向各位求助。
脱氢乙酸具有较强抑制细菌、霉菌及酵母菌发酵的作用,尤其对霉菌的抑制作用最强,是一种高效的防霉、防腐剂。其还具有脂溶性强、热稳定性高的特点,在摄氏120℃的杀菌温度下仍保持杀菌能力不变。国外曾广泛使用于食品、药品中,我国自上世纪70年代中其开始用于食品防腐,曾用于果汁、酱菜、腐乳、干酪、人造奶油、乳酸菌饮料、月饼、果酱等食品。而脱氢乙酸的缺点是毒性较强,目前我国允许在腐乳、酱菜、果蔬汁、肉类制品、糕点、月饼、焙烤馅料中作为防腐剂使用,最大使用量0.5克/公斤。 脱氢乙酸的国标检测方法为[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法,样品经过有机溶剂的萃取、净化、浓缩等步骤的复杂处理,并且脱氢乙酸在[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]条件下,色谱峰出现拖尾现象,使定性、定量影响较大。据报道利用高效液相色谱法食品中的脱氢乙酸,采用纯水、乙醇-水、碱性水对样品进行超声萃取处理,萃取液经过滤后上机检测。作者在试验中发现,利用脱氢乙酸难溶于水而易溶于甲醇、乙醇、乙腈等有机溶剂的特性,样品均浆后酸化处理,用乙腈提取,经微孔过滤后再用高效液相色谱进行定性、定量测定,方法的灵敏度、准确度和回收率高,精密度良好,重现性好,前处理简便快捷,更能满足样品分析要求。 实验样品材料采用一般市售的果汁、酱菜、腐乳、糕点等食品。果汁样品精确称取5.00 g于50 ml的离心管中;酱菜、腐乳、糕点等食品样品事先均匀,准确称取2.0~3.0 g于50ml的离心管中,加入5mL饱和氯化钠溶液和1ml盐酸溶液(1:1),用旋涡混合器混合1分钟,准确加入10mL乙腈,用旋涡混合器混合3分钟,3000转离心15分钟,取上清液经0.45μm过滤器过滤后供液相色谱测定。 按相应的色谱条件对样液进行分析,采用外标法,以保留时间定性,以峰面积定量,测定样液中脱氢乙酸的浓度(mg/ml)。 得到结果以下结果:一、根据扫描的结果,脱氢乙酸的最大吸收波长在230 nm和297 nm处,230 nm处吸收较强,但基体干扰较多,在波长297NM处基体干扰较少,故选取检测波长297NM。 二、动相为乙腈+水时,脱氢乙酸峰形拖尾,使用0.02 mol / L的乙酸铵代替水作流动相,峰形得到较大的改善。乙腈的比例影响出峰的时间和响应,乙腈的比例低,保留时间长,响应也会低,乙腈比例高时,出峰时间短,响应也较高。试验表明,当0.02 mol / L的乙酸铵―乙腈比例为85:15时效果较好。 三、脱氢乙酸难溶于水,易溶于苯、氯仿、乙醚。脱氢乙酸钠则易溶于水,选用水或氢氧化钠溶液、碳酸钠溶液提取,提取液须净化后方可使用。本方法选用乙腈作提取液,主要考虑到脱氢乙酸能溶液于乙腈,乙腈的水溶性有利于乙腈从酸性的样液中把脱氢乙酸完全溶解,同时乙腈可沉淀蛋白质,与脂肪不溶,离心分离得到干净的提取液。 四、在相应的色谱条件下测定,脱氢乙酸的保留时间为5.775min,峰形及组分分离效果好。 五、以70%乙腈水溶液为溶剂配制浓度0.01~0.1范围内的脱氢乙酸标准使用液。以峰面积对脱氢乙酸浓度进行回归分析得回归方程式Y=2.39X×108� 1.33×105,R=0.9997,线性良好。在对同一浓度标样连续进样5次,得到脱氢乙酸的峰面积和保留时间的RSD值分别为0.35%和0.24,方法的定性和定量准确度较高。 本文采用乙腈提取食品中脱氢乙酸,注入高效液相色谱进行测定,以保留时间定性,采用外标法定量。本方法的线性方程有良好的相关性,R=0.9997。方法加标回收率为96.2%~99.6%,变异系数RSD值为1.09%。该方法操作简便、准确,回收率高,精密度良好,重现性好,可用于优化食品中脱氢乙酸的测定。
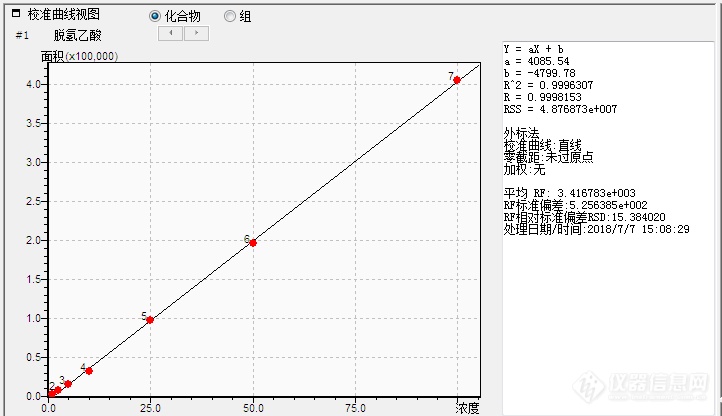
[align=center][b]食品中脱氢乙酸的测定 高效液相色谱法的方法验证报告[/b][/align][align=center][b]GB/T 23377-2009[/b][/align][align=center][b]牛晓[/b][/align]一、方法概述适用范围:本标准适用于黄油、酱菜、发酵豆制品、面包、糕点、培烤食品馅料、复合调味料、果蔬汁中脱氢乙酸含量的高效液相食品测定方法,其他食品可参照执行。原理:用氢氧化钠溶液提取式样中的脱氢乙酸,经脱脂、去蛋白处理后,用高效液相色谱紫外检测器测定,外标法定量。二、仪器与试剂1.仪器:1.1高效液相色谱仪:配有紫外检测器。仪器编号:UNQD-YQ-0961.2不锈钢高速均质器。1.3离心机。1.4 分析天平:感量0.0001g和感量0.01g。1.5超声波发生器:功率大于180W1.6涡旋混合器。1.7粉碎机。1.8 C[sub]18 [/sub]固相萃取柱:500mg,6mL(使用前用5mL的甲醇、10mL谁活化,使柱子保持湿润状态)。2. 试剂2.1甲醇:色谱纯2.2正己烷。2.3乙酸铵:优级纯。2.4甲酸溶液:10%。取10mL甲酸,加90mL水,混匀。2.5乙酸铵溶液:0.02mol/L。称取1.54g乙酸铵,用水溶解并定人至1L。2.6氢氧化钠溶液:20g/L.称取20.0g氢氧化钠,用水溶解并定人至1L.2.7硫酸锌溶液:120g/L。称取120g七水硫酸锌,用水溶解并定人至1L。2.8甲醇溶液:70%。取70mL甲醇,加30mL水,混匀。2.9脱氢乙酸标准品 来源:上海安谱 货号:CDAA-263002三、样品的制备与保存取具有代表性的样品粉碎均匀备用。四、分析步骤4.1、标准曲线绘制4.1.1脱氢乙酸标准品:脱氢乙酸含量≥98%4.1.2标准储备溶液:准确称取10.0mg脱氢乙酸标准品,用10mL20g/L氢氧化钠溶液溶解,用水定容至刻度。配成1000.0μg/mL的标准储备液。4.1.3标准工作液:准确移取标准储备0.01mL、0.025mL、0.05mL、0.10mL、0.25mL、0.50mL、1.0mL于10mL容量瓶中,用水稀释并定容至刻度,配成成浓度为1.0μg/mL、2.5μg/mL、5.0μg/mL、10.0μg/mL、25.0μg/mL、50.0μg/mL、100.0μg/mL系列工作液。[color=#ffc000] [/color]4.2样品的处理4.2.1提取:4.2.1.1果蔬汁:准确称取2g-5g式样,精确至0.01g,置于50mL容量瓶中,加入约10mL水,用氢氧化钠溶液调pH为7-8,加水稀释至刻度,摇匀,置于离心管中,4000r/minl离心10min,取20mL上清液用10%的甲酸调pH值至4-5,定容到25mL,取5mL过已经活化的固相萃取柱,用5mL水淋洗,用2mL70%的甲醇溶液洗脱,收集洗脱液,过0.45μm滤膜,供高效液相色谱测定。4.2.1.2酱菜、发酵豆制品:样品用不锈钢高速均质器均质,准确称取2g-5g均匀式样,精确至0.01g,置于25mL容量瓶中国,加入约10mL水、5mL硫酸锌溶液,用氢氧化钠溶液调pH为7-8,加水稀释至刻度,超声提取10min,取适量置于10mL离心管中,4000r/min离心10min,取上清液过0.45μm滤膜,供高效液相色谱测定。4.2.1.3黄油、面包、糕点、焙烤食品馅料、复合调味料:样品用粉碎机磨碎,准确称取2g-5g均匀式样,精确至0.01g,置于25mL容量瓶中,加入约10mL水、5mL硫酸锌溶液,用氢氧化钠溶液调pH为7-8,加水稀释至刻度,超声提取10min,转移到分液漏斗中,加入10mL正己烷,振摇1min,静置分层,弃去正己烷层,再加入10mL正己烷重复进行一次,取下层水相置于离心管中,4000r/min离心10min。取上清液过0.45μm滤膜,供高效液相色谱法测定,若高效液相色谱分离效果不理想时,可取20mL上清液,用10%的甲酸调pH至4-6,定容至25mL,取5mL过已经活化的固相萃取柱,用5mL水淋洗,用2mL70%的甲醇溶液洗脱,收集洗脱液,过0.45μm滤膜,供高效液相色谱测定。4.3.仪器测定条件4.3.1色谱柱:C18柱,柱长250mm,内径4.6mm,粒径5.0μm。4.3.2流动相:甲醇+0.02mol/L乙酸铵溶液=10+90,体积比4.3.3流速:1.0mL/min。4.3.4进样体积:1.0μL4.3.5柱温:30℃。4.3.6进样量:10μL。4.3.7检测波长:293nm。五、结果处理计算公式:[align=center][img=,275,96]http://ng1.17img.cn/bbsfiles/images/2018/07/201807281450143192_3078_2904018_3.png!w275x96.jpg[/img][/align]式中:X-样品中脱氢乙酸的含量,单位为g/kg C-由标准曲线查得试样中脱氢乙酸的浓度为μg/mL;C[sub]0[/sub]-由标准曲线查得空白试样中脱氢乙酸的浓度为μg/mL;V-试样溶的总体积,单位为mL f-过固相萃取柱换算系数(f=0.5) m-样品的质量,单位g。计算结果保留至小数点后3位。六、验证结果1.线性结果将混合标准系列工作溶液分别注入液相色谱仪中, 测定相应的峰面积,以混合标准系列工作溶液的质量浓度为横坐标,以峰面积为纵坐标,绘制标准曲线。同时做空白实验。[u]Y=4085.54X-4799.78R^2=0.9996307[/u][img=,690,397]http://ng1.17img.cn/bbsfiles/images/2018/07/201807281449566812_4874_2904018_3.png!w690x397.jpg[/img]以上结果表明脱氢乙酸在1.0μg/mL~100.0μg/mL范围内,R[sup]^2[/sup]=0.9996307,脱氢乙酸浓度和峰面积呈线性关系,线性良好,符合要求。2.检出限结果将5.0μg/mL标准溶液逐级稀释至S/N=9.50,得出脱氢乙酸的定量检出限为2.5mg/kg[color=#ff0000],[/color]此检出限结果小于国标GB/T 23377-2009的定量检出限5.0mg/kg,故此方法满足条件。七、方法精密度(重复性)对LBF180700281样品分别进行6次加标重复性的测定,测定结果如下:[table][tr][td][align=center]测定编号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][td][align=center]6[/align][/td][/tr][tr][td][align=center]质量(g)[/align][/td][td][align=center]5.0207[/align][/td][td][align=center]5.0300[/align][/td][td][align=center]5.0808[/align][/td][td][align=center]5.0251[/align][/td][td][align=center]5.0036[/align][/td][td][align=center]5.0087[/align][/td][/tr][tr][td][align=center]浓度(μg/mL)[/align][/td][td][align=center]25.428[/align][/td][td][align=center]24.875[/align][/td][td][align=center]25.920[/align][/td][td][align=center]25.525[/align][/td][td][align=center]25.558[/align][/td][td][align=center]25.351[/align][/td][/tr][tr][td][align=center]含量(mg/kg)[/align][/td][td][align=center]0.127[/align][/td][td][align=center]0.124[/align][/td][td][align=center]0.128[/align][/td][td][align=center]0.127[/align][/td][td][align=center]0.128[/align][/td][td][align=center]0.127[/align][/td][/tr][tr][td][align=center]平均值(mg/kg)[/align][/td][td=6,1][align=center]0.127[/align][/td][/tr][tr][td][align=center]RSD%[/align][/td][td=6,1][align=center]1.17[/align][/td][/tr][/table]本方法的精密度为1.17%,符合GB/T 23377-2009中给出试样测试结果的精密度要求,因此,本次测定均符合要求。八、准确度验证(加标回收)对LBF180700281样品加标,取1000.0 μg/mL的标液0.5mL、0.625 mL、0.8mL同样品同步处理后,结果见下表:[table][tr][td=2,1][align=center]测定编号[/align][/td][td=6,1][align=center]脱氢乙酸[/align][/td][/tr][tr][td][align=center]序号[/align][/td][td][align=center]m(g)[/align][/td][td][align=center]V(mL)[/align][/td][td][align=center]C(μg/mL)[/align][/td][td][align=center]脱氢乙酸含量(g/kg)[/align][/td][td][align=center]平均值(g/kg)[/align][/td][td][align=center]加标量(g/kg)[/align][/td][td][align=center]回收率%[/align][/td][/tr][tr][td][align=center]1#[/align][/td][td][align=center]5.0304[/align][/td][td][align=center]25.0[/align][/td][td][align=center]ND[/align][/td][td][align=center]ND[/align][/td][td=1,2][align=center]ND[/align][/td][td][align=center]/[/align][/td][td][align=center]/[/align][/td][/tr][tr][td][align=center]2#[/align][/td][td][align=center]5.0028[/align][/td][td][align=center]25.0[/align][/td][td][align=center]ND[/align][/td][td][align=center]ND[/align][/td][td][align=center]/[/align][/td][td][align=center]/[/align][/td][/tr][tr][td][align=center]加标1#[/align][/td][td][align=center]5.0255[/align][/td][td][align=center]25.0[/align][/td][td][align=center]17.581[/align][/td][td][align=center]0.087[/align][/td][td][align=center]0.087[/align][/td][td][align=center]0.099[/align][/td][td][align=center]87.9[/align][/td][/tr][tr][td][align=center]加标2#[/align][/td][td][align=center]5.0085[/align][/td][td][align=center]25.0[/align][/td][td][align=center]21.982[/align][/td][td][align=center]0.110[/align][/td][td][align=center]0.110[/align][/td][td][align=center]0.125[/align][/td][td][align=center]88.0[/align][/td][/tr][tr][td][align=center]加标3#[/align][/td][td][align=center]5.0068[/align][/td][td][align=center]25.0[/align][/td][td][align=center]32.028[/align][/td][td][align=center]0.160[/align][/td][td][align=center]0.160[/align][/td][td][align=center]0.175[/align][/td][td][align=center]91.4[/align][/td][/tr][/table]由上表可以看出脱氢乙酸在添加浓度5mg/kg-1000mg/kg范围内,回收率在80%-110%之间相对标准偏差为4.41%,小于国标要求应小于10%,符合规定要求。九、总结从检出限、线性范围、重复性、回收率测试结果可知,均符合方法要求,本实验方法符合GB/T 23377-2009的要求。
液相法测定脱氢乙酸标准GB/T23377-2009中,样品在用氢氧化钠溶液提取后的pH值为7-8,而对于果蔬汁及糕点调味料等样品,还多了一步固相萃取的步骤:用甲酸调pH到4-6后,经C18萃取后直接进样。 问题:为什么要调pH到4-6? 标准中脱氢乙酸标准溶液的配制看,有氢氧化钠参与,溶液应该是呈弱碱性的,这样的话,当样液经固相萃取后的pH(4-6)与标准溶液的pH不一样,是否会影响测定准确度?
想请教各位,甲醇中9种VOC混合系列溶液中,100和1000ug/ml证书上写的稀释倍数2是什么意思?是要自己稀释2倍后标准值才是100和1000吗?如果使用GB/T 18883-2002中TVOC的标准,那么用这个标液做的曲线可以用吗?
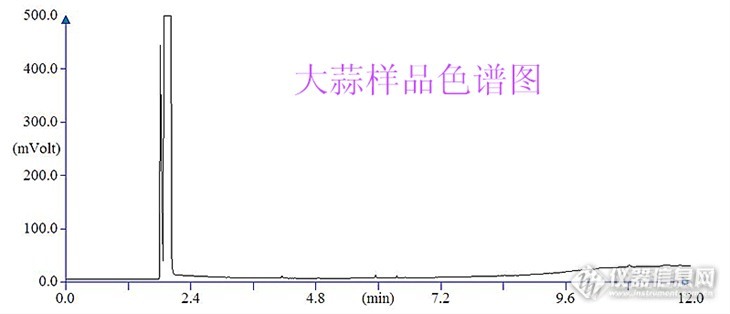
包装大蒜(酱菜)中脱氢乙酸的测定【生活中的仪器分析】食品安全——“菜”米油盐酱醋茶大检测本文采用气相色谱法对新疆某品牌大蒜(酱菜)中脱氢乙酸的含量进行分析测定,参考GB/T5009.121-2003国家标准,试验过程略加改动后,该方法在线性浓度范围内可准确用于食品中脱氢乙酸的测定。关键词:大蒜,脱氢乙酸,气相色谱-火焰离子化检测仪(GC-FID),前言:脱氢乙酸(DHA,Dehydroacetic),http://ng1.17img.cn/bbsfiles/images/2013/11/201311081643_475962_1634341_3.jpg别名二乙酰基乙酰乙酸,固态呈白色或淡黄色结晶粉末,无嗅、无味、熔点108~110℃,沸点270℃,是一种低毒高效防腐、防霉剂。在酸、碱条件下均有一定的抗菌作用,尤其对霉菌的抑制作用最强。我国《食品添加剂使用卫生(GB 2760-1996)规定:脱氢乙酸可用于腐乳、酱菜、原汁桔浆,最大使用量为0.30g/kg。(摘自百度百科)1试验材料材料:回民大蒜(新疆香儿纯实业有限公司)。化学试剂:丙酮(天津化学试剂研究所-色谱淋洗液);乙醚(天津化学试剂研究所-分析纯)硫酸(成都市科龙化工试剂厂)氯化钠、无水硫酸钠(天津光复精细化工研究所-分析纯)。仪器:天平(奥豪斯(上海)有限公司-AEL-160型0.01g);移液枪(BRAND-5mL、1mL、100uL);气相色谱仪(美国Thermo Finigan公司);旋转蒸发仪(上海爱郎仪器有限公司-EYELA SB-1100型);超声波清洗器(昆山市超声仪器有限公司)。2试验方法脱氢乙酸标准品配制:精密称取脱氢乙酸标准品100mg,丙酮定容至100mL的容量瓶中(母液浓度为1000mg/L)。标准曲线浓度:母液用丙酮稀释至10、20、[/
[size=5]用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定酒中甲醇含量,在配制甲醇标准溶液时,要用乙醇作溶剂,哪里可以买到不含甲醇的乙醇? 很困扰,请大家指点[/size]
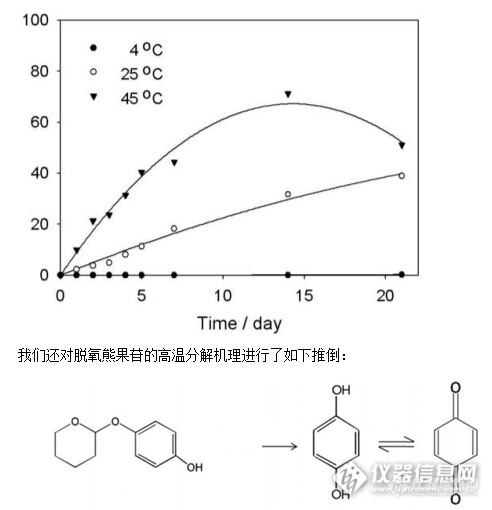
脱氧熊果苷在水溶液中热降解的高效液相色谱法测定 虽然人类的黑色素是皮肤抗紫外线伤害最重要的保障,然而黑色素堆积造成黝黑的皮肤造成了人类美容方面的困扰。黑色素水平的升高也是皮肤疾病,包括黄褐斑,晒斑,和炎症后色素沉着的一大特性。因此,人类越来越渴求一种用于皮肤美容美白兼具治疗作用的产品。酪氨酸是黑色素合成的前体,酪氨酸酶是人皮肤黑素细胞负责酪氨酸转化为黑色素的关键限速酶,通过竞争性抑制剂来降低酪氨酸酶的活性可以降低黑色素在人体黑素细胞内的合成。 经研究许多化合物包括氢醌,熊果苷和脱氧熊果苷能够结合酪氨酸酶的活性位点从而抑制黑色素合成。氢醌是最常规的皮肤增白剂,但其长期应用副作用也较多,包括刺激性皮炎,黑素细胞的破坏,接触性皮炎、褐黄病。熊果苷是熊果植物中一种糖基化的天然的对苯二酚,并且相比氢醌它更安全和较少的细胞毒性,但其在体内研究发现抑制黑色素产生的效率低下,脱氧熊果苷最新被报道是一种新型的皮肤美白剂,具更大的抑制酪氨酸酶活性,并且比对苯二酚和熊果苷更安全。http://ng1.17img.cn/bbsfiles/images/2014/12/201412302146_530363_2165260_3.jpg 熊果苷吸收到皮肤时在会原位产生氢醌,因此,在较高温度下它有潜在不稳定和由于氧化而易于改变其在制剂中颜色。由于脱氧熊果苷是熊果苷的衍生物,故在一些条件下也存在化合物稳定性的问题,这种稳定性问题会导致其在化妆品及医药产品中应用的问题。所以改善其稳定性是其未来应用的一个需要解决的问题。本实验中我们应用高效液相色谱法来分析其在水溶液中的稳定性。并研究了几个影响其降解的温度。材料与仪器:脱氧熊果苷、氢醌、色谱级甲醇、分析级丙二醇、去离子水;紫外可见分光光度计、安捷伦1100、菲罗门C18反相色谱柱、紫外检测波长280nm、流动相甲醇 - 水(60:40(V / V)、进样量20ul、流速1ml/min。结果与讨论:本实验的目的是探讨脱氧熊果苷在溶液中的热稳定性,所以我们首先确定了其溶解度及水溶液的紫外吸收图谱,其后建立了HPLC方法定量脱氧熊果苷,对熊果苷的热降解动力学进行了分析。脱氧熊果苷水溶液的制备--因为去除了葡萄糖侧链的羟基基团,脱氧熊果苷在室温下难溶于水,故采用丙二醇助溶,可将脱氧熊果苷的溶解度在丙二醇及丁二醇的助溶下达到13%(W / W)。美国食品和药物管理局(FDA)已经确定丙二醇是一种安全的成分可应用在化妆品、食品及药品中;世界卫生组织(WHO)也确定了它是安全可使用的。像水一样应用普遍的丙二醇常作为溶剂或湿润剂应用于化妆品中还有助溶的作用。虽然乙醇也可以起到助溶的作用,但考虑到其对皮肤的刺激性,我们采用了丙二醇作为脱氧熊果苷在水中的助溶剂。脱氧熊果苷的紫外吸收图谱:为确立脱氧熊果苷的紫外吸收情况,采用紫外可见风光光度计收集脱氧熊果苷水溶液的紫外吸收图谱,采用0.05 和 0.1 mM的脱氧熊果苷去离子水溶液(含10%的丙二醇),于石英池中200-400nm下进行测定。结果如下图:显示一个最小的248nm和两个232和283 nm的最大值。吸光度水平随浓度的增加而增加。http://ng1.17img.cn/bbsfiles/images/2014/12/201412302147_530364_2165260_3.jpghttp://ng1.17img.cn/bbsfiles/images/2014/12/201412302147_530365_2165260_3.jpg标准曲线浓度范围各为12-144mg/升,R2大于0.995。(其中下面为脱氧熊果酸,上面为氢琨)http://ng1.17img.cn/bbsfiles/images/2014/12/201412302148_530366_2165260_3.jpghttp://ng1.17img.cn/bbsfiles/imag
请问,哪里能买到甲醇中的苯标准溶液~可以给我留言给个联系方法。谢谢
我们做室内空气检测,需做苯标准曲线,所用的标准物质是GBW08703甲醇中苯溶液标准物质,该如何稀释,浓度是0.887mg/ml.
[b][font=宋体]问题描述:[/font][font=宋体]按照国标[/font]GB5009.121-2016[font=宋体]方法,以[/font]0.02mol/L[font=宋体]乙酸铵:甲醇([/font][i]V/V[/i][font=宋体])[/font]=90+10[font=宋体],流速[/font]1mL/min[font=宋体],可以检测脱氢乙酸,但在流动相中加入[/font]0.1%[font=宋体]的乙酸后,同样的分析时间内却检测不到脱氢乙酸色谱峰,这是为什么?[/font][font=宋体]解答:[/font][/b][font=宋体]([/font]1[font=宋体])脱氢乙酸是我国允许在食品生产加工中使用的一种化学合成防腐剂,在较高的[/font]pH[font=宋体]范围内保持良好的抗菌性。脱氢乙酸是极性化合物,因其含有双键具有紫外吸收,在[/font]C[sub]18[/sub][font=宋体]色谱柱有一定的吸附保留。在[/font]GB 5009.121-2016[font=宋体]《食品安全国家标准[/font] [font=宋体]食品中脱氢乙酸的测定》[/font] [font=宋体]液相色谱法中使用[/font]0.02mol/L[font=宋体]乙酸铵:甲醇([/font][i]V/V[/i][font=宋体])[/font]=90[font=宋体]:[/font]10[font=宋体]作为流动相,对脱氢乙酸作等度洗脱。[/font][font=宋体]([/font]2[font=宋体])通常可电离化合物而言,不同状的化合物态与[/font]C[sub]18[/sub][font=宋体]之间的作用力存在明显差异。脱氢乙酸[/font]p[i]Ka[/i][font=宋体]值为[/font]5.27[font=宋体],而[/font]0.02mol/L[font=宋体]乙酸铵:甲醇([/font][i]V/V[/i][font=宋体])[/font]=90[font=宋体]:[/font]10[font=宋体]流动相体系的[/font]pH[font=宋体]值在[/font]7~8[font=宋体],在此体系中,大部分脱氢乙酸处于离子态。当原有体系中加入乙酸酸化后,流动相体系的[/font]pH[font=宋体]值有利于脱氢乙酸从离子态向中性态转化,从而促使脱氢乙酸与[/font]C[sub]18[/sub][font=宋体]的作用力更强了,因此,相对而言,乙酸铵:甲醇([/font][i]V/V[/i][font=宋体])[/font]=90[font=宋体]:[/font]10[font=宋体]流动相洗脱能力变弱了,导致脱氢乙酸在[/font]C[sub]18[/sub][font=宋体]色谱柱上的保留时间更长,或长期保留在色谱柱上。只有延长酸化后流动相的洗脱时间,或增加酸化后流动相中有机相的比例,可将脱氢乙酸从色谱柱中洗脱出来。[/font][font='微软雅黑','sans-serif'][color=black][back=white]领取更多《实战宝典》请进:[url]http://instrument-vip.mikecrm.com/2bbmrpI[/url][/back][/color][/font][font='微软雅黑','sans-serif'][color=black][back=white] [/back][/color][/font]
为什么MS的标准溶液溶剂都是用甲醇呢?是因为出峰快,便于切除吗?用其他溶剂可以吗?如正己烷、二氯甲烷、丙酮.....有没有讲究?
[align=right][b]SGLC-GC-052[/b][/align][b]摘要:[/b]本文建立了脱氢乙酸的GC测定方法。参照国标GB 5009.121-2016中色谱条件,采用色谱柱SH-Polar D分析脱氢乙酸,脱氢乙酸峰形对称,理论塔板数按脱氢乙酸峰计算高于300000。此方法可为食品中脱氢乙酸含量测定提供参考。[b]关键词:[/b]脱氢乙酸 SH-Polar D GC[b]1. 实验部分1.1 实验仪器及耗材[/b]Shimadzu GC-2030[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url];色谱柱:SH- Polar D(30 m,0.32 mm × 0.25 μm;P/N:227-36321-02;S/N:1639516);SHIMSEN Arc Disc HPTFE针式过滤器(P/N:380-00341-05);[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GC-MS[/color][/url]认证样品瓶LabTotal Vial(P/N:227-34002-01);SHIMSEN Pipet[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url]:SHIMSEN Pipet PMII-10(P/N:380-00751-02);SHIMSEN Pipet PMII-100(P/N:380-00751-04);SHIMSEN Pipet PMII-1000(P/N:380-00751-06)。[b]1.2 标准工作溶液的制备[/b]分别精确吸取浓度为1.0 mg/mL的脱氢乙酸标准贮备液0.01 mL、0.1 mL、0.5 mL、1.0 mL、2.0 mL于10 mL容量瓶中,用乙酸乙酯稀释并定容,配制成浓度分别为1.0 μg/mL、10.0 μg/mL、50.0 μg/mL、100 μg/mL和200 μg/mL的标准工作液。[b]1.3 分析条件[/b]色谱柱:SH- Polar D(30 m,0.32 mm × 0.25 μm;P/N:227-36321-02;S/N:1639516)升温程序:初始温度60 ℃, 以每分钟20 ℃的速率升温至210 ℃,保持5分钟载气:N2进样口温度:240 ℃分流模式:分流(5:1)控制模式:恒流模式(2 mL/min)初始流速:2 mL/min检测器:FID,温度:250 ℃进样量:1 μL[b]2. 实验结果[/b]按照上述色谱条件(1.3)进行采集,标准溶液色谱图如下:[b]标准溶液[/b]/b[img=SHIMSEN Styra HLB]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-GC-052_01.png[/img][font=arial, &][size=12px][/size][/font][b]重现性[/b][img=SHIMSEN Styra HLB]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-GC-052_02.png[/img][img=SHIMSEN Styra HLB]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-GC-052_03.png[/img][font=arial, &][size=12px][/size][/font]标准曲线[img=SHIMSEN Styra HLB]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-GC-052_04.png[/img][font=arial, &][size=12px][/size][/font][b]3. 结论[/b]本文建立了脱氢乙酸的GC测定方法。结果表明,参照GB 5009.121-2016中色谱条件,采用色谱柱SH-Polar D分析脱氢乙酸,峰形对称,理论塔板数按脱氢乙酸峰计算高于300000。此方法可为食品中脱氢乙酸含量测定提供参考。
我用的是安捷伦1260液相色谱仪,sb c18柱,之前用分析纯甲醇配了一系列标准溶液采用液相检测能看到五种很明显的峰,检测条件是:t=0 水:甲醇=30:70t=5 水:甲醇=0:100t=10 水:甲醇=0:100t=15 水:甲醇=30:70波长225nm(275nm测出的峰高比225nm时低很多)但是过了两周用色谱纯甲醇新配了些标准溶液,测试发现无论是单标还是混标,在8分多钟有一个很高的尖峰,好像是和dehp重叠了,这时在用以前用分析纯配的标准溶液在测试也出现这种情况,把分析纯甲醇和色谱纯甲醇都进样也是出现很尖的峰,以前测试甲醇时都没出现过,不知道是不是溶液的问题?怎样才能去除干扰呢?数据处理我还不会,试着积分时发现提示在8分钟左右的位置有重叠峰,检测条件也是胡乱试的,也不懂梯度洗脱条件应该怎样来摸索,看理论的一些计算也不很明白,请高手帮我看一下是哪的问题啊?怎样能避免溶剂峰干扰dehp的峰呢?还有面积百分比报告我也看不懂,有谁能给解释下?谢谢了!第一次用这个仪器做毕业实验什么都不懂,请大家多帮帮忙,我要检测一些乳制品包装材料,学校的实验室只能用超声波或者水浴振荡器来做了,但是超声波提的时候瓶子不好固定,盖上盖子了溶液一加热也会把盖子顶开,损失了好多,而且好多论文中都用旋转蒸发浓缩,我试过一次,30毫升溶剂超声提取完后过滤,在用10毫升溶液润洗过滤,旋转蒸发一不小心就蒸发没了,在用色谱甲醇润洗出来定容到10毫升或者25毫升,光这个来回转移就损失好多,因为旋转蒸发瓶不能很好的把溶液直接转移到容量瓶里,于是我又先转到小烧杯里,然后在转到容量瓶里,这样来回用溶剂润洗,想定容成10毫升也很困难,只好把定容体积增大,麻烦大家说一下你们是如何用超声波等处理样品的?固相萃取等之类的就不要说了,我这也没有那些仪器,还有我这个实验老感觉没有什么创新行,课题组的老师都说检测增塑剂的国标也有了,我也没什么可做的了,就算是优化条件的话我们实验室的条件也不好,也谈不上什么优化了,麻烦大家给些建议,做些什么才能让这个实验显得量又大,又有点意义和创新行呢?先谢谢大家帮忙了
二氯甲烷从不同浓度的有机溶机水溶液(DMF, 甲醇,酸,碱)中萃取标准品,计算回收率,不知道大家有没有什么经验分享一下,由于水中有有机溶剂,不知道萃取效率能达到多少?有没有这方面资料可以参考呢?谢谢
配制0.002g/100ml的甲醇溶液,用气相色谱检测,所用标样为白酒13种混合标样建立的曲线和方法。现将具体配制方法描述:准备好60%的乙醇水溶液(优级纯乙醇),取100ml容量瓶,加入约30ml乙醇水溶液,然后置于分析天平上(0.1mg),清零,向其中滴入0.2g(实际称量0.2098g)的甲醇(色谱纯),定容,此时浓度为0.2098g/100ml。取1ml置于100ml容量瓶中,再定容,此时浓度为0.002g/100ml。色谱检测结果:1.0g/L,即10g/100ml。请高手指点配制或检测过程有无问题或其他的注意点,为什么检测出来的结果会出现数量级的区别呢。补充:FID检测器。甲醇标样浓度,0.3157g/L.
请教有经验的前辈,问题如主题,我买回两瓶甲醇中六六六,DDT混标溶液,但是发现用GC做六六六,DDT的标准曲线时,相关资料都是正乙烷或是异辛烷或是其他溶济中的标液,而没有甲醇作溶济的(听说甲醇作溶济做的效果很差)。但是买标准时研究所那边又说只有甲醇中的六六六,DDT混标,没有其他溶济中的这种混标了。我现在手上的这种标液该怎么用呢?能不能转成正乙烷为溶济的呢?
[align=center][b]多功能净化平台在脱氢乙酸检测前处理中的应用[/b][/align][align=center]武向勇,张佳佳,赵昀,封同月[/align][align=center](山西省食品质量安全监督检验研究院,山西太原 030012)[/align][b]摘要:[/b]建立了一种脱氢乙酸样品前处理的自动化净化方法,优化了自动化净化条件。制备后的样品液相色谱检测结果:脱氢乙酸的回收率为75% ~115%,精密度相对偏差小于6.0%。分析检测结果表明与国家标准方法比较,该前处理方法安全、环保、高效、可靠,提高了脱氢乙酸前处理的效率;分析检测结果的稳定性、准确度、精密度均有一定程度的提高。[b]关键词:[/b]多功能净化平台;脱氢乙酸;液相色谱 我国食品中脱氢乙酸的液相色谱检验方法是依据国家标准GB5009.121-2016第二法[sup][/sup]进行检测。样品前处理过程中,对C18固相萃取柱的净化方法为人工手动完成固相萃取柱的活化、上样、淋洗、洗脱等步骤。人工方法处理过程费时费力,稳定性欠缺,净化效果往往不是很好也不稳定,所用的有机溶剂易挥发,污染环境[sup][/sup],对操作人员的身体健康造成伤害。但目前自动化和高通量的样品前处理方法鲜见报道,笔者研究了多功能平台在脱氢乙酸的前处理中的净化条件,并与国家标准方法进行了比较,以期运用于自动化批量检测提供参考依据。[b]1 材料与方法1.1 仪器与试剂1.1.1 仪器设备[/b] 多功能进化平台:Freedom EVO 100-8 SPE型; 高效液相色谱仪:Agilent1260型; 数控超声波清洗器:KQ5200DE型; 高速离心机;TDL-5-A型; pH计:PHS-3C型; C18固相萃取柱:500mg,6mL。[b]1.1.2 试剂[/b] 脱氢乙酸标准品,纯度≥99.5%; 甲醇(色谱纯) 乙酸铵(分析纯) 氢氧化钠(分析纯) 甲酸(分析纯) 硫酸锌(分析纯) 脱氢乙酸标准储备液(1.0mg/mL)。[b]1.1 方法1.2.1 多功能净化平台对脱氢乙酸的前处理方法[/b] 准确称取2 g-5 g试样,置于50 mL容量瓶中,加入约10 mL水,用20g/L氢氧化钠溶液调pH值至7.5,加水稀释至刻度,摇匀,置于离心管中,4000 r/min离心10 min。取20 mL上清液用10 %甲酸溶液调pH值至5,定容到25 mL。分2次移取5mL待净化液,以17 μL/s的流速过已活化的固相萃取柱后,用2000 μL空气吹扫;分2次移取5 mL水,以17 μL/s的淋洗速度淋洗固相萃取柱后,用2000 μL空气吹扫;用2 mL 70 %甲醇溶液洗脱,以17 μL/s的洗脱速度进行洗脱后,用1000μL空气排干小柱,收集洗脱液2 mL,涡旋混合,过0.45μm有机滤膜,供高效液相色谱测定。[b]1.2.2 液相色谱测定[/b] 色谱柱:C18柱(4.6 mm×250 mm,5 μm);柱温:30 ℃;流动相:甲醇+乙酸铵溶液(体积比:10+90);流速: 1.0 mL/ min;波长:293 nm;进样量:10 μL。 根据保留时间定性,外标峰面积法定量。[b]1.2.3 试验设计[/b] 多功能净化平台可精确控制加液流速和空气吹扫体积,可以减少手动加液和吹扫带来的溶液交叉污染、净化淋洗洗脱不完全和时间的浪费,可以让净化、淋洗和洗脱三个步骤效率 达到最佳。由于多功能净化平台实际流速范围位4.17 μL/s ~ 4167 μL/s,选取8、17、35 μL/s三个加液流速进行选择。经过试验,选取1000μL、2000μL、3300μL三个空气吹扫体积进行选择。 本研究进行单因素试验,确定多功能净化平台的最佳净化条件。同时,进行此方法稳定性、精密度试验和与GB 5009.121-2016(第一法)前处理方法进行对比。[b]2 多功能净化平台条件的优化选择2.1 多功能净化平台加液流速的选择[/b] 称取四种类型试样各7份,每份5.0 g。每种试样中一份为本底样,三份为一组加入一种含量的脱氢乙酸标准溶液。每组试样在净化过程中只改变净化、淋洗、洗脱三步骤中的一个加液速度,其余过程按照多功能净化平台对脱氢乙酸的前处理方法处理。采用高效液相色谱仪测得脱氢乙酸含量并计算回收率。结果见表1。表1 不同加液流速下的脱氢乙酸回收率[table][tr][td=1,3][align=center]食品[/align][align=center]名称[/align][/td][td=1,3][align=center]加标量[/align][align=center](mg/kg)[/align][/td][td=3,1][align=center]待净化样液流速[/align][align=center](μL/s)[/align][/td][td=3,1][align=center]淋洗液流速[/align][align=center](μL/s)[/align][/td][td=3,1][align=center]洗脱液流速[/align][align=center](μL/s)[/align][/td][/tr][tr][td][align=center]8[/align][/td][td][align=center]17[/align][/td][td][align=center]35[/align][/td][td][align=center]8[/align][/td][td][align=center]17[/align][/td][td][align=center]35[/align][/td][td][align=center]8[/align][/td][td][align=center]17[/align][/td][td][align=center]35[/align][/td][/tr][tr][td=3,1][align=center]回收率(%)[/align][/td][td=3,1][align=center]回收率(%)[/align][/td][td=3,1][align=center]回收率(%)[/align][/td][/tr][tr][td=1,2][align=center]橙汁[/align][/td][td][align=center]20[/align][/td][td][align=center]92.1[/align][/td][td][align=center]93.2[/align][/td][td][align=center]75.2[/align][/td][td][align=center]93.2[/align][/td][td][align=center]91.2[/align][/td][td][align=center]80.6[/align][/td][td][align=center]91.2[/align][/td][td][align=center]90.4[/align][/td][td][align=center]83.1[/align][/td][/tr][tr][td][align=center]100[/align][/td][td][align=center]95.2[/align][/td][td][align=center]94.9[/align][/td][td][align=center]74.8[/align][/td][td][align=center]94.9[/align][/td][td][align=center]95.3[/align][/td][td][align=center]79.3[/align][/td][td][align=center]95.3[/align][/td][td][align=center]98.3[/align][/td][td][align=center]85.2[/align][/td][/tr][tr][td=1,2][align=center]糕点[/align][/td][td][align=center]40[/align][/td][td][align=center]93.2[/align][/td][td][align=center]95.8[/align][/td][td][align=center]78.1[/align][/td][td][align=center]95.8[/align][/td][td][align=center]94.9[/align][/td][td][align=center]82.1[/align][/td][td][align=center]94.9[/align][/td][td][align=center]94.3[/align][/td][td][align=center]83.7[/align][/td][/tr][tr][td][align=center]400[/align][/td][td][align=center]90.7[/align][/td][td][align=center]96.2[/align][/td][td][align=center]79.2[/align][/td][td][align=center]96.2[/align][/td][td][align=center]95.2[/align][/td][td][align=center]80.6[/align][/td][td][align=center]95.2[/align][/td][td][align=center]93.4[/align][/td][td][align=center]82.1[/align][/td][/tr][tr][td=1,2][align=center]桃罐头[/align][/td][td][align=center]100[/align][/td][td][align=center]96.7[/align][/td][td][align=center]95.6[/align][/td][td][align=center]73.8[/align][/td][td][align=center]95.6[/align][/td][td][align=center]97.1[/align][/td][td][align=center]75.4[/align][/td][td][align=center]97.1[/align][/td][td][align=center]95.3[/align][/td][td][align=center]80.7[/align][/td][/tr][tr][td][align=center]200[/align][/td][td][align=center]92.4[/align][/td][td][align=center]93.2[/align][/td][td][align=center]70.6[/align][/td][td][align=center]93.2[/align][/td][td][align=center]96.4[/align][/td][td][align=center]79.3[/align][/td][td][align=center]96.4[/align][/td][td][align=center]96.5[/align][/td][td][align=center]85.3[/align][/td][/tr][tr][td=1,2][align=center]酱腌菜[/align][/td][td][align=center]80[/align][/td][td][align=center]93.2[/align][/td][td][align=center]90.1[/align][/td][td][align=center]75.9[/align][/td][td][align=center]90.1[/align][/td][td][align=center]91.0[/align][/td][td][align=center]77.1[/align][/td][td][align=center]91.0[/align][/td][td][align=center]92.1[/align][/td][td][align=center]79.3[/align][/td][/tr][tr][td][align=center]200[/align][/td][td][align=center]91.7[/align][/td][td][align=center]90.7[/align][/td][td][align=center]76.8[/align][/td][td][align=center]90.7[/align][/td][td][align=center]89.9[/align][/td][td][align=center]72.6[/align][/td][td][align=center]89.9[/align][/td][td][align=center]94.2[/align][/td][td][align=center]84.5[/align][/td][/tr][/table] 由表1对比可得,加液流速太小,净化时间过长;加液流速太大,导致脱氢乙酸难以完全吸附在固相萃取柱上也不能完全洗脱下来。从实际检测和数据准确性考虑选择多功能净化平台加液流速控制均为17μL/s(相当于1mL/min)。[b]2.2 多功能净化平台吹扫空气体积的选择[/b] 称取四种类型试样各7份,每份5.0 g。每种试样中一份为本底样,三份为一组加入一种含量的脱氢乙酸标准溶液。每组试样在净化过程中只改变上样、淋洗、洗脱三步骤中的一个空气吹扫体积,其余过程按照多功能净化平台对脱氢乙酸的前处理方法处理。采用高效液相色谱仪测得脱氢乙酸含量并计算回收率。结果见表2。表2 不同空气吹扫体积下脱氢乙酸回收率[table][tr][td=1,4][align=center]食品[/align][align=center]名称[/align][/td][td=1,4][align=center] [/align][align=center]脱氢乙酸[/align][align=center]加标量[/align][align=center](mg/kg)[/align][/td][td=9,1][align=center]空气吹扫体积(μL)[/align][/td][/tr][tr][td=3,1][align=center]上样后[/align][/td][td=3,1][align=center]淋洗后[/align][/td][td=3,1][align=center]洗脱后[/align][/td][/tr][tr][td][align=center]1000[/align][/td][td][align=center]2000[/align][/td][td][align=center]3300[/align][/td][td][align=center]1000[/align][/td][td][align=center]2000[/align][/td][td][align=center]3300[/align][/td][td][align=center]1000[/align][/td][td][align=center]2000[/align][/td][td][align=center]3300[/align][/td][/tr][tr][td=9,1][align=center]回收率 (%)[/align][/td][/tr][tr][td=1,2][align=center]橙汁[/align][/td][td][align=center]20[/align][/td][td][align=center]75.4[/align][/td][td][align=center]85.3[/align][/td][td][align=center]86.3[/align][/td][td][align=center]85.3[/align][/td][td][align=center]91.0[/align][/td][td][align=center]83.4[/align][/td][td][align=center]93.5[/align][/td][td][align=center]90.4[/align][/td][td][align=center]90.1[/align][/td][/tr][tr][td][align=center]100[/align][/td][td][align=center]70.6[/align][/td][td][align=center]87.6[/align][/td][td][align=center]89.4[/align][/td][td][align=center]87.6[/align][/td][td][align=center]97.8[/align][/td][td][align=center]81.5[/align][/td][td][align=center]98.8[/align][/td][td][align=center]95.3[/align][/td][td][align=center]95.9[/align][/td][/tr][tr][td=1,2][align=center]糕点[/align][/td][td][align=center]40[/align][/td][td][align=center]69.4[/align][/td][td][align=center]82.4[/align][/td][td][align=center]81.0[/align][/td][td][align=center]82.4[/align][/td][td][align=center]92.6[/align][/td][td][align=center]79.6[/align][/td][td][align=center]96.4[/align][/td][td][align=center]94.3[/align][/td][td][align=center]92.1[/align][/td][/tr][tr][td][align=center]400[/align][/td][td][align=center]66.8[/align][/td][td][align=center]83.4[/align][/td][td][align=center]82.0[/align][/td][td][align=center]83.4[/align][/td][td][align=center]95.2[/align][/td][td][align=center]82.3[/align][/td][td][align=center]97.2[/align][/td][td][align=center]93.4[/align][/td][td][align=center]92.1[/align][/td][/tr][tr][td=1,2][align=center]桃罐头[/align][/td][td][align=center]100[/align][/td][td][align=center]70.1[/align][/td][td][align=center]85.1[/align][/td][td][align=center]86.1[/align][/td][td][align=center]85.1[/align][/td][td][align=center]96.1[/align][/td][td][align=center]83.4[/align][/td][td][align=center]98.1[/align][/td][td][align=center]95.3[/align][/td][td][align=center]94.1[/align][/td][/tr][tr][td][align=center]200[/align][/td][td][align=center]67.2[/align][/td][td][align=center]80.6[/align][/td][td][align=center]83.1[/align][/td][td][align=center]80.6[/align][/td][td][align=center]98.3[/align][/td][td][align=center]82.1[/align][/td][td][align=center]98.3[/align][/td][td][align=center]96.5[/align][/td][td][align=center]92.1[/align][/td][/tr][tr][td=1,2][align=center]酱腌菜[/align][/td][td][align=center]80[/align][/td][td][align=center]68.9[/align][/td][td][align=center]80.1[/align][/td][td][align=center]84.1[/align][/td][td][align=center]80.1[/align][/td][td][align=center]90.1[/align][/td][td][align=center]75.6[/align][/td][td][align=center]99.1[/align][/td][td][align=center]92.3[/align][/td][td][align=center]89.7[/align][/td][/tr][tr][td][align=center]200[/align][/td][td][align=center]72.3[/align][/td][td][align=center]82.1[/align][/td][td][align=center]83.1[/align][/td][td][align=center]82.1[/align][/td][td][align=center]94.9[/align][/td][td][align=center]79.4[/align][/td][td][align=center]96.9[/align][/td][td][align=center]94.2[/align][/td][td][align=center]94.8[/align][/td][/tr][/table] 由表2对比可得,上样和淋洗后空气吹扫体积太小和太大都导致脱氢乙酸不能完全吸附在固相萃取柱上或者净化不完全;洗脱后空气吹扫体积太大对脱氢乙酸的回收率没有太大影响。综合考虑,确定上样和淋洗后空气吹扫体积均为2000μL,淋洗后空气吹扫体积为1000μL。[b]2.3 方法与国标的符合性[/b] 多功能净化平台的最佳净化条件:加液速度为17μL/s,上样和淋洗后空气吹扫体积均为2000μL,淋洗后空气吹扫体积为1000μL。在此条件下,脱氢乙酸回收率在91%~99%之间,符合GB/T 27404-2008[sup][/sup]的要求。[b]3 多功能净化平台稳定性、精密度试验及与国家标准方法的比较试验3.1 多功能净化平台稳定性试验[/b] 多功能净化平台设备具有8个独立移液通道,所以选取4种不同基质的空白样品,向样品中加入相同含量脱氢乙酸标准溶液,提取后采用多功能净化平台进行前处理,测定脱氢乙酸含量并计算回收率,进行稳定性试验。结果见表3。表 3 同一时刻同一加标量的不同基质空白样品中脱氢乙酸回收率稳定性实验(n=6)[table][tr][td][align=center]脱氢乙酸加标量[/align][align=center]40mg/kg[/align][/td][td=2,1][align=center]苹果汁[/align][/td][td=2,1][align=center]橙汁[/align][/td][td=2,1][align=center]糕点[/align][/td][td=2,1][align=center]葡萄汁[/align][/td][/tr][tr][td=1,2][align=center]回收率(%)[/align][/td][td]38.2[/td][td][align=center]37.6[/align][/td][td]38.7[/td][td][align=center]38.1[/align][/td][td]36.1[/td][td]35.8[/td][td]36.9[/td][td]35.2[/td][/tr][tr][td]95.5[/td][td][align=center]94.0[/align][/td][td]96.8[/td][td][align=center]95.2[/align][/td][td]92.6[/td][td]89.5[/td][td]92.2[/td][td]88.0[/td][/tr][/table] 由表3可得,不同基质空白样品加标溶液中脱氢乙酸回收率均在80%以上,变化幅度很小,稳定性良好。[b]3.2 多功能净化平台准确度试验[/b] 选取不同类型的样品,加入不同含量的脱氢乙酸标准溶液,提取后采用多功能净化平台进行前处理,测定脱氢乙酸含量并计算回收率,进行准确度试验。结果见表4。表4 不同加标量的不同样品中脱氢乙酸回收率准确度实验(n=6)[table][tr][td][align=center]样品[/align][align=center]名称[/align][/td][td][align=center]脱氢乙酸含量[/align][align=center](mg/kg)[/align][/td][td][align=center]脱氢乙酸加标量[/align][align=center](mg/kg)[/align][/td][td][align=center]加标后测得脱氢乙酸含量[/align][align=center](mg/kg)[/align][/td][td][align=center]回收率(%)[/align][/td][/tr][tr][td=1,3][align=center]橙汁[/align][/td][td=1,3][align=center]0[/align][/td][td][align=center]20[/align][/td][td][align=center]18.2[/align][/td][td][align=center]91.1[/align][/td][/tr][tr][td][align=center]40[/align][/td][td][align=center]37.5[/align][/td][td][align=center]93.8[/align][/td][/tr][tr][td][align=center]100[/align][/td][td][align=center]98.4[/align][/td][td][align=center]98.4[/align][/td][/tr][tr][td=1,3][align=center]糕点[/align][/td][td=1,3][align=center]0[/align][/td][td][align=center]40[/align][/td][td][align=center]36.9[/align][/td][td][align=center]89.9[/align][/td][/tr][tr][td][align=center]200[/align][/td][td][align=center]198[/align][/td][td][align=center]99.1[/align][/td][/tr][tr][td][align=center]400[/align][/td][td][align=center]402[/align][/td][td][align=center]100.5[/align][/td][/tr][/table] 由表4可以看出,不同加标量的不同样品中脱氢乙酸回收率在89.9~100.5%之间,符合GB 5009.121-2016《食品安全国家标准 食品中脱氢乙酸的测定》在添加浓度2 mg/kg~10 mg/kg浓度范围内,回收率在80 %~110 %之间的要求。[b]3.3 与国家标准方法的精密度比较试验[/b] 为验证本方法的可行性、可靠性和准确性,选取了具有代表性的空白样品分别采用多功能净化平台的方法和国家标准方法进行了脱氢乙酸回收率与精密度比较试验,结果见表5。表5 采用多功能净化平台方法和国家标准方法的脱氢乙酸回收率及精密度比较实验(n=6)[table][tr][td=1,2][align=center]样品[/align][align=center]名称[/align][/td][td=1,2][align=center]加标量[/align][align=center](g/kg)[/align][/td][td=4,1][align=center]手动方法[/align][/td][td=4,1][align=center]多功能净化平台方法[/align][/td][/tr][tr][td][align=center]结果(n=6)[/align][/td][td][align=center]平均[/align][align=center]结果[/align][/td][td][align=center]回收率(%)[/align][/td][td][align=center]RSD(%)[/align][/td][td][align=center]结果(n=6)[/align][/td][td][align=center]平均[/align][align=center]结果[/align][/td][td][align=center]回收率[/align][align=center](%)[/align][/td][td][align=center]RSD[/align][align=center](%)[/align][/td][/tr][tr][td=1,12]面包[/td][td=1,6][align=center]0.3[/align][/td][td][align=center]0.27[/align][/td][td=1,6][align=center]0.24[/align][/td][td=1,6][align=center]80.0[/align][/td][td=1,6][align=center]8.5[/align][/td][td][align=center]0.26[/align][/td][td=1,6][align=center]0.27[/align][/td][td=1,6][align=center]90.0[/align][/td][td=1,6][align=center]5.5[/align][/td][/tr][tr][td][align=center]0.25[/align][/td][td][align=center]0.25[/align][/td][/tr][tr][td][align=center]0.24[/align][/td][td][align=center]0.29[/align][/td][/tr][tr][td][align=center]0.21[/align][/td][td][align=center]0.28[/align][/td][/tr][tr][td][align=center]0.26[/align][/td][td][align=center]0.27[/align][/td][/tr][tr][td][align=center]0.24[/align][/td][td][align=center]0.26[/align][/td][/tr][tr][td=1,6][align=center]0.5[/align][/td][td][align=center]0.46[/align][/td][td=1,6][align=center]0.45[/align][/td][td=1,6][align=center]90.0[/align][/td][td=1,6][align=center]5.62[/align][/td][td][align=center]0.46[/align][/td][td=1,6][align=center]0.48[/align][/td][td=1,6][align=center]96.0[/align][/td][td=1,6][align=center]2.82[/align][/td][/tr][tr][td][align=center]0.48[/align][/td][td][align=center]0.48[/align][/td][/tr][tr][td][align=center]0.41[/align][/td][td][align=center]0.49[/align][/td][/tr][tr][td][align=center]0.43[/align][/td][td][align=center]0.5[/align][/td][/tr][tr][td][align=center]0.46[/align][/td][td][align=center]0.48[/align][/td][/tr][tr][td][align=center]0.46[/align][/td][td][align=center]0.49[/align][/td][/tr][/table] 表5可以说明:两种方法均符合国家标准要求,但采用多功能进化平台的前处理方法得到的脱氢乙酸回收率均高于手动固相萃取净化方法,相对标准偏差均低于手动固相萃取净化方法。可见,本方法具有较高的精密度和可靠性,减少了偶然误差。[b]4 结论[/b] 多功能净化平台的最佳净化条件为:加液速度为17μL/s,上样和淋洗后空气吹扫体积为2000μL,洗脱后空气吹扫体积为1000μL。此条件下,样品中脱氢乙酸含量回收率为75%~115%,RSD小于6.0%。 与国家标准方法相比,采用多功能净化平台进行脱氢乙酸前处理,在符合国家标准GB 5009.121-2016(第一法)和GB/T 27404-2008要求的前提下,减少了试剂的交叉污染和净化洗脱效率的不完全不稳定,确保了脱氢乙酸含量回收率的稳定性、提高检测结果的准确度和精密度,缩短了约1/2的净化时间,提高了检验人员的工作效率并保障了检验人员的人身安全。[b]参考文献[/b](略)
[align=center][b]《GB/T 23377-2009 食品中脱氢乙酸的测定 高效液相色谱法》的分析——CAPCELL PAK C18 MG[/b][/align]脱氢乙酸无嗅、无味,作为一种广谱防腐剂,在酸、碱条件下,均有一定的抗菌作用,特别是对霉菌和酵母菌的抑菌能力强,被广泛应用于果汁、腐乳、酱菜、人造奶油、乳酸菌饮料、果酱、糕点、复合调味料等食物中。[align=center][img=,98,83]http://ng1.17img.cn/bbsfiles/images/2018/03/201803151201062706_4091_2222981_3.png!w98x83.jpg[/img][/align][align=center]脱氢乙酸[/align][align=center][/align]本次实验选用中等极性通用型CAPCELL PAK C[sub]18[/sub] MG S5 4.6mm i.d. × 250 mm色谱柱,按照国标方法《GB/T 23377-2009 食品中脱氢乙酸的测定高效液相色谱法》对脱氢乙酸标准品进行分析,得到结果如图1所示,脱氢乙酸保留时间为11min左右,理论塔板数为12400,色谱峰形略前延,不对称因子0.81。[align=center][img=,690,425]http://ng1.17img.cn/bbsfiles/images/2018/03/201803151201414841_7871_2222981_3.png!w690x425.jpg[/img][/align][align=center]图1 脱氢乙酸标准品分析图[/align][align=left]注:峰上标数字从下至上依次为理论塔板数和不对称因子。[/align][align=left][img=,437,175]http://ng1.17img.cn/bbsfiles/images/2018/03/201803151205221291_1773_2222981_3.png!w437x175.jpg[/img][/align][align=left][/align][align=center][img=,690,443]http://ng1.17img.cn/bbsfiles/images/2018/03/201803151202437604_2483_2222981_3.png!w690x443.jpg[/img][/align][align=center]附图:国标方法所附标准色谱图[/align]与国标方法所附标准色谱图对比可知,MG色谱柱分析所得结果分析时间更短,且峰形更佳。进一步,按照国标要求配制脱氢乙酸标准工作液,浓度分别为1.0 mg/L、10.0 mg/L、50 mg/L、100 mg/L、200 mg/L,进行线性考察实验。对各标准工作液按照国标方法进行分析,以浓度为横坐标,以峰面积为纵坐标绘制标准工作曲线,如图2所示,R[sup]2[/sup]=0.9992,得到良好线性结果。[align=left][/align][align=center][img=,690,413]http://ng1.17img.cn/bbsfiles/images/2018/03/201803151202301461_9895_2222981_3.png!w690x413.jpg[/img][/align][align=center]图2 脱氢乙酸标准曲线图[/align][align=center] [/align][align=left]为解决峰形前延的问题,在原方法基础上对液相方法进行调整,尝试将流动相中的0.02 mol/L乙酸铵溶液更换为0.1%磷酸水溶液,同时调整有机相比例。经过调整,最终结果如图3,脱氢乙酸峰形良好,不对称因子为1.00,理论塔板数为19428,峰形较原方法所得结果有明显改善。[/align][align=left][/align][align=left][/align][align=center][img=,690,421]http://ng1.17img.cn/bbsfiles/images/2018/03/201803151203319172_4111_2222981_3.png!w690x421.jpg[/img][/align][align=center]图3 脱氢乙酸标准品分析图(0.1%磷酸水:甲醇=45:55)[/align]注:峰上标数字从下至上依次为理论塔板数和不对称因子。[align=left][img=,473,169]http://ng1.17img.cn/bbsfiles/images/2018/03/201803151205040494_8042_2222981_3.png!w473x169.jpg[/img][/align][align=left][/align][align=left]继续按此方法对脱氢乙酸标准工作液进行线性考察,以浓度为横坐标,以峰面积为纵坐标绘制标准工作曲线,如图4所示,R[sup]2[/sup]=0.9944,得到良好线性结果。[/align][align=left][/align][align=center][img=,690,408]http://ng1.17img.cn/bbsfiles/images/2018/03/201803151206047125_66_2222981_3.png!w690x408.jpg[/img][/align][align=center]图4 脱氢乙酸标准曲线图(0.1%磷酸水 / 甲醇 = 45 / 55)[/align]综上,使用CAPCELL PAK C[sub]18[/sub] MG S5 4.6mm i.d. × 250 mm色谱柱,按照《GB/T 23377-2009 食品中脱氢乙酸的测定高效液相色谱法》对脱氢乙酸标准品进行分析,所得峰形略有前延,但线性良好,能够进行定量检测;同时,将流动相调整为磷酸水-甲醇体系后,峰形得到明显改善,最终得到良好分析结果。
想咨询如何用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]测定溶液中甲醇、甲酸、甲胺的方法。色谱仪的各种参数如何设置?以及标准溶液的配置。请详细回答,谢谢。
[color=#333333]紧急求助 22-脱氢赬桐甾醇的结构式怎么写和质谱数据。[/color]
【中文名称】脱氢醋酸;α,γ-二乙酰基乙酰乙酸【英文名称】dehydroaceticacid【结构或分子式】 http://ng1.17img.cn/bbsfiles/images/2012/02/201202191926_349889_1855403_3.jpg【熔点(℃)】108~110【沸点(℃)】270【性状】 白色或淡黄色结晶粉末。无臭,无味。【溶解情况】 难溶于水,在碱性水溶液中溶解度大(20℃时30%以上)。易溶于苯、乙醚、丙酮及热酒精。【用途】 是一种低毒、高效的广谱抗菌剂,在酸、碱条件下均有一定的抗菌作用。可用作食品和饲料的防腐剂。【制备或来源】 由乙酰乙酸乙酯经脱醇缩合而成,或由双乙烯酮缩合制得。【其他】 对光、热稳定。【生产单位】 江苏南通醋酸化工厂;江苏常熟防腐剂厂等
GB/T 394.2-94上提到甲醇标准溶液要用到基准乙醇(无甲醇乙醇)。请问那里可以购买此物。
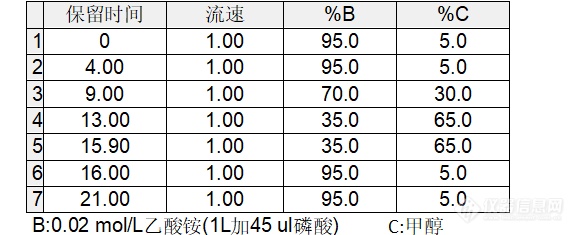
目前检测脱氢乙酸的国家标准方法为[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法,但该方法还存在一些不足,比如被测样品必须经过有机溶剂萃取,前处理过程过于繁杂。而液相色谱法在流动相及检测波长的选择方面也不够理想,色谱峰拖尾严重。本人对流动相的选择、检测波长进行了修改,有效解决脱氢乙酸拖尾的问题,在这里共享给大家。色谱柱:中谱红-RD-C18规 格:4.6*150 mm,5μm检测波长:230nm、293nm双波长检测(与其他添加剂一同检测,脱氢乙酸在293nm频道处出峰)流动相:A:0.02 mol/L乙酸铵(加磷酸调PH值) 、B:甲醇梯度方法:[img=,576,235]https://ng1.17img.cn/bbsfiles/images/2021/06/202106251024591636_4140_3979231_3.png!w576x235.jpg[/img]得到的分析图谱:[img=,690,689]https://ng1.17img.cn/bbsfiles/images/2021/06/202106251028159295_6694_3979231_3.png!w690x689.jpg[/img]
脱氢乙酸是一种用于食品中的防腐剂.我想找测定脱氢乙酸的国外标准,但是一个也查不到,难道国外没有用脱氢乙酸做防腐剂的吗?困惑中,55555555

10,抽取5个版友);中奖名单:WUYUWUQIU(注册ID:wulin321)莫名其妙(注册ID:moyueqiu)玲儿响叮当(注册ID:jshbhh)千层峰(注册ID:jxyan)吕梁山(注册ID:shih20j07)http://ng1.17img.cn/bbsfiles/images/2016/12/201612141537_01_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/12/201612141537_02_1610895_3.jpg【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================苯甲酸、山梨酸、糖精钠、安赛蜜、脱氢乙酸的测定方法:HPLC基质:标准溶液应用编号:101812化合物:苯甲酸、山梨酸、糖精钠、安赛蜜、脱氢乙酸固定相:Diamonsil C18(2)色谱柱/前处理小柱:Diamonsil 5μm C18(2), 250 x 4.6mm样品前处理:样品制备 制备方法: 分别取苯甲酸、山梨酸、糖精钠、安赛蜜、脱氢乙酸适量,用水溶解,配成浓度为0.02 mg/mL的混合标准溶液。色谱条件:分析条件 色谱柱: Diamonsil C18(2),250×4.6 mm,5 μm (Cat#:99603) 流动相: 甲醇:0.02 mol/L乙酸铵=6:94 流速: 1.0 mL/min 柱温: 30 ℃ 检测器: UV 230 nm 进样量: 10 μL文章出处:天津迪马实验室关键字:苯甲酸,山梨酸,糖精钠,安赛蜜,脱氢乙酸,Diamonsil C18(2),99603摘要:苯甲酸、山梨酸、糖精钠、安赛蜜、脱氢乙酸的测定谱图:http://www.dikma.com.cn/Public/Uploads/images/ansaimi3(1).PNG备注:1-安赛蜜 2-苯甲酸 3-山梨酸 4-糖精钠 5-脱氢乙酸
在室内空气中苯浓度分析,选用标液直接解吸进样的方法时,大家选择的标液是 甲醇中苯标准溶液 还是 二硫化碳中苯标准溶液?欢迎做这项分析的进来都能留个言!我们现在选用的是甲醇中苯标准溶液,用填充柱做的话,就有溶剂峰有很大的拖尾现象,峰形很不好看。买不到浓度合适的二硫化碳中苯标准溶液,我们都是自己配的,如哪位高人知道合适浓度的有证二硫化碳中苯标准溶液哪里有得买,也请指点!
各位老师好!今天用安捷伦1100做脱氢乙酸,用的是论坛上别人发的方法做的,发现脱氢乙酸确实是5分多钟就出峰了,高的那个峰是脱氢乙酸10ppm的,低的那个峰是脱氢乙酸1ppm的,单标都是用甲醇定容的,但是两个谱图在前面2~4分钟都会有相同的小杂峰,不知道是什么原因,请问有什么解决办法吗?[img]https://ng1.17img.cn/bbsfiles/images/2019/11/201911141544099843_9585_4026362_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2019/11/201911141544102579_611_4026362_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2019/11/201911141544105269_3851_4026362_3.png[/img]