GB/T5750.9-2006饮用水中666 DDT 标准溶液是环己烷中666,DDT。采购人员问了好几家标准物质卖家都没有,只有正己烷中666,DDT。那么我可以用正己烷中666,DDT标准品用环己烷稀释配制标准溶液吗?
先说结论:衍生化后的环己烷氨基磺酸钠标准溶液在25摄氏度下5个小时就会有变化,主色谱峰[font=&]环己醇的面积会变小,衍生物色谱峰环己醇亚硝酸酯的面积会变大(应该是两者面积和不会变化,理论上还是可以继续用来做标准曲线的)。而且低浓度的环己烷氨基磺酸钠标准溶液衍生化后的色谱峰环己醇的色谱峰会出现杂峰。 我猜测高浓度的环己烷氨基磺酸钠标准溶液衍生化后的色谱峰环己醇的色谱峰不会出现杂峰是因为主峰比较大,把杂峰包裹进去了。 [/font] 上午对环己烷氨基磺酸钠标准溶液进行衍生化处理,浓度分别是10μg/ml、50μg/ml、500μg/ml,处理完毕后立刻上机。一共是12个进样瓶,第一次上机最后一个样品跑完后,大概时间是中午12:30,然后等待下午2:30的时候,又重新上机。 每个进样瓶的信号采集时间大概是20分钟,这样第一个样品和最后一个样品间隔时间是20*11=220分钟,加上中午的2个小时,这样大概是5个小时。也就是说第一批和第二批进样中每个相同序号的进样瓶采集时间间隔是5小时 这次使用的环己烷氨基磺酸钠标准溶液有两种,分别是10个月前配置的标准溶液和新配置的标准溶液。 分别编号是10-1、50-1、500-1、10-2、50-2、500-2 下面是各个对比的色谱图,分别是上午的色谱图和下午的色谱图进行对比 10-1的对比,上午的色谱图几乎正常,下午再跑一次的色谱图,主色谱峰环己醇旁边出现了杂峰 [img=,690,373]https://ng1.17img.cn/bbsfiles/images/2024/09/202409181124064647_4366_5979722_3.png!w690x373.jpg[/img] 50-1的对比,上午的色谱图几乎正常,下午再跑一次的色谱图,主色谱峰环己醇面积明显变小了,衍生物色谱峰环己醇亚硝酸酯的面积明显变大了。 [img=,690,457]https://ng1.17img.cn/bbsfiles/images/2024/09/202409181124061287_876_5979722_3.png!w690x457.jpg[/img] 500-1的对比,上午的色谱图几乎正常,下午再跑一次的色谱图,500μg/ml的这个浓度上午和下午的色谱图区别不大 [img=,690,446]https://ng1.17img.cn/bbsfiles/images/2024/09/202409181124064695_5130_5979722_3.png!w690x446.jpg[/img] 10-2的对比,上午和下午的色谱图进行对比,环己烷氨基磺酸钠标准溶液的主色谱峰旁边出现了杂峰 [img=,690,413]https://ng1.17img.cn/bbsfiles/images/2024/09/202409181150579387_7325_5979722_3.png!w690x413.jpg[/img] 50-2的对比,上午的色谱图几乎正常,下午再跑一次的色谱图,主色谱峰环己醇面积明显变小了,衍生物色谱峰环己醇亚硝酸酯的面积明显变大了。 [img=,690,481]https://ng1.17img.cn/bbsfiles/images/2024/09/202409181150587943_3504_5979722_3.png!w690x481.jpg[/img] 500-2的对比,上午的色谱图几乎正常,下午再跑一次的色谱图,主色谱峰环己醇面积明显变小了,衍生物色谱峰环己醇亚硝酸酯的面积明显变大了。 [img=,690,509]https://ng1.17img.cn/bbsfiles/images/2024/09/202409181150579543_2309_5979722_3.png!w690x509.jpg[/img]
前两天在电冰箱看到了一个2023年11月16日配置的环己烷氨基磺酸钠标准溶液,浓度为1 mg/ml,距离现在已经有10个月了。理论上这个标准溶液应该是过期了,不可以使用了。在抛弃前,我决定检测一下这个环己烷氨基磺酸钠标准溶液的含量还有多少。 分别吸取指定体积的环己烷氨基磺酸钠标准溶液按照新国标进行衍生化处理,最终得到浓度分别是0.01ug/ml、0.02ug/ml、0.05ug/ml、0.1ug/ml、0.5ug/ml浓度的标准溶液。 然后上机检测,最终使用2024年3月份的环己烷氨基磺酸钠标准溶液制作的曲线来标定这几个色谱图。 但是这次色谱图不是很好,不知道是我衍生化污染了,还是本身保存了10个月的环己烷氨基磺酸钠标准溶液发生了分解。低浓度的溶液出现了杂峰,而且还干扰了主要的色谱峰,而且衍生物几乎没有色谱峰。高浓度标准溶液的色谱峰也不好,0.5ug/ml的标准溶液衍生物色谱峰过大。 大家可以看下面的色谱图,低浓度的色谱峰都存在问题,后面多少一些杂峰,这时候如果不积分这个杂峰,数据就明显偏低了,如果给杂峰积分,则数据还算是正常。但是这样明显不合理。 0.01ug/ml的标准溶液检测结果是0.0039ug/ml 0.02ug/ml的标准溶液检测结果是0.0124ug/ml 0.05ug/ml的标准溶液检测结果是0.0240ug/ml 这样看来,浓度都减半了。 过两天我准备重新配置环己烷氨基磺酸钠标准溶液,把新配置的标准溶液和这款过期的标准溶液一起进行衍生化处理,好好分析看一下到底什么情况,到时候我再把测试数据发到论坛上面。 [img=,682,558]https://ng1.17img.cn/bbsfiles/images/2024/09/202409031752042453_2355_5979722_3.png!w682x558.jpg[/img] 0.01ug/ml的标准溶液检测结果是0.0039ug/ml [img=,684,543]https://ng1.17img.cn/bbsfiles/images/2024/09/202409031752043985_5910_5979722_3.png!w684x543.jpg[/img] 0.02ug/ml的标准溶液检测结果是0.0124ug/ml [img=,674,540]https://ng1.17img.cn/bbsfiles/images/2024/09/202409031752045640_2049_5979722_3.png!w674x540.jpg[/img] 0.05ug/ml的标准溶液检测结果是0.024ug/ml [b][size=24px][color=#ff0000]这三个低浓度的都出现了拖尾峰,我没有计算 如果计算上拖尾峰,则结果还有高一些[/color][/size][/b] [img=0.01ug/ml的标准溶液检测结果是0.0039ug/ml,665,567]https://ng1.17img.cn/bbsfiles/images/2024/09/202409031755596696_8860_5979722_3.png!w665x567.jpg[/img] 0.01ug/ml的标准溶液检测结果是0.0091ug/ml [img=0.01ug/ml的标准溶液检测结果是0.0039ug/ml,674,532]https://ng1.17img.cn/bbsfiles/images/2024/09/202409031756234443_8618_5979722_3.png!w674x532.jpg[/img] 0.02ug/ml的标准溶液检测结果是0.017ug/ml [img=,690,527]https://ng1.17img.cn/bbsfiles/images/2024/09/202409031756562645_5411_5979722_3.png!w690x527.jpg[/img] 0.05ug/ml的标准溶液检测结果是0.0287ug/ml 再看看高浓度的标准溶液 [img=,683,571]https://ng1.17img.cn/bbsfiles/images/2024/09/202409031758376118_9242_5979722_3.png!w683x571.jpg[/img] 0.5ug/ml的标准溶液 [img=,690,547]https://ng1.17img.cn/bbsfiles/images/2024/09/202409031759031228_2645_5979722_3.png!w690x547.jpg[/img] 0.1ug/ml的标准溶液
为什么我配MIBK-环己烷溶液时,怎么用水洗都无法把PH洗到6以上?还有为什么要加酸洗PH呢,不洗行不行?不加酸直接用水洗PH都是3.9,这是为什么啊?这两天洗的都快奔溃了http://simg.instrument.com.cn/bbs/images/default/em09509.gif,求高手解答
[color=#444444]含环己烷1%的环戊烷溶液,用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分离,能看到环己烷的峰么?[/color]
因为没有[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]可以用,实验室只有waters 2695。用0.5M NaCl加环己烷搅拌后实验效果确实效果不一样,因为环己烷查着在水中微溶,NaCl溶液中不清楚,想要检测一下到底环己烷有没有溶解进去。我应该用什么柱子,什么检测器,流动相配比选和柱温有什么注意的么,感谢大佬
我按照中国药典2010版环己烷残留溶剂项实验,发现内标溶液的浓度只有0.04ug/ml,按此浓度进样,内标峰的峰面积非常小,基本上不能准确定量了,我不知道这个浓度是不是药典上打错了,实际上应该是0.04mg/ml,还是其它的什么问题?后续实验中,我把内标的浓度变为4ug/ml,峰面积就比较正常了。
请教各位大神,顶空气相做溶剂残留,正己烷和环己烷加样回收率只有70%,50%,样品处理为称0.1g样品加5ml50%(DMF:H20)稀释的混合标准溶液,至20ml顶空瓶,压盖,想请教下大家,做正己烷和环己烷回收率时有什么注意点,谢谢大家仪器:Agilent 7890A 7697A色谱柱:Elite-624 60meter,0.32mm ID,1.8um df进样方式:顶空,进样口温度:200 ℃,分流比10:1,柱温:程序升温,在40℃维持8分钟,再以每分钟10℃的升温速率升至150℃,维持13分钟,再以20℃每分钟的速率升至200℃,维持2分钟顶空瓶平衡温度:90 ℃,顶空瓶平衡时间:20 分钟加振摇,取样针温度:105 ℃,传输线温度:120 ℃检测器类型:FID,检测器温度:250 ℃气流条件:氢气 30.0 ml/min,空气 400.0 ml/min,氮气 2.0 ml/min
我们实验室需要买标准溶液,检测项目包括烷烃,苯类,农药类等等,很多有机物质,那么,我们需要买哪些标准溶液呢?例如,我们需要检测环己烷,是不是我们必须要买环己烷标准溶液呢?还是只买色谱纯的环己烷就可以了呢?谢谢
推翻上一次的结论,配置了10个月的环己烷氨基磺酸钠和刚配置的环己烷氨基磺酸钠没有区别 前段时间做了一个测试,配置了10个月的环己烷氨基磺酸钠标准溶液上机测试,感觉存在问题。 https://bbs.instrument.com.cn/topic/8404909_1_1_2_1_1 但是上次上机测试室存在问题,这次分别对10个月的环己烷氨基磺酸钠标准溶液和刚配置的环己烷氨基磺酸钠标准溶液进行衍生化处理。 浓度分别是10μg/ml、50μg/ml、500μg/ml 10个月的编号分别是10-1、50-1、500-1,新配置的编号是10-2、50-2、500-2 先看看浓度为10μg/ml的色谱图,蓝色的为10-2,黑色的为10-1,后面第三个小色谱峰为环己烷氨基磺酸钠的衍生物 这样看起来,新配置的标准溶液面积还要微微小于已经配置了10个月的环己烷氨基磺酸钠标准溶液。 [img=,690,371]https://ng1.17img.cn/bbsfiles/images/2024/09/202409181051539608_1886_5979722_3.png!w690x371.jpg[/img] 再看看浓度为50μg/ml的环己烷氨基磺酸钠的标准溶液色谱图 蓝色的为50-1,黑色的为50-2,后面第三个小色谱峰为环己烷氨基磺酸钠的衍生物 这样看起来,两个色谱峰相加后,看起来,新配置的标准溶液面积和10个月的环己烷氨基磺酸钠标准溶液的面积差不多,浓度也应该是相差不大。 [img=,690,364]https://ng1.17img.cn/bbsfiles/images/2024/09/202409181054148691_1246_5979722_3.png!w690x364.jpg[/img] 再看看浓度为500μg/ml的环己烷氨基磺酸钠的标准溶液色谱图 黑色的为500-1,蓝色的为50-2,后面第三个小色谱峰为环己烷氨基磺酸钠的衍生物 明显可以看出来,新配置的环己烷氨基磺酸钠标准溶液的面积要小于已经配置了10个月的环己烷氨基磺酸钠标准溶液面积,想当然的浓度也要小了。 [img=,690,414]https://ng1.17img.cn/bbsfiles/images/2024/09/202409181059211505_9762_5979722_3.png!w690x414.jpg[/img] 最后说一下,只所以新配置的环己烷氨基磺酸钠标准溶液的面积还小与10个月前的环己烷氨基磺酸钠标准溶液,应该是我配置新的标准溶液时,使用的50ml容量瓶,再往容量瓶加入10000μg/ml的环己烷氨基磺酸钠时,只从安剖瓶中吸取出了4.8ml,最终定容到50ml,相当于这个标准溶液最终浓度只是960μg/ml,因此用这个标准溶液配置的10、50、500的标准溶液使用液都会小一些,从而导致新的标准溶液要比10个月前的标准溶液浓度还要小。 但是我们可以得出最终的结论,正常2-8摄氏度冷藏保存,1000μg/ml的环己烷氨基磺酸钠标准溶液10个月是没有问题的,浓度几乎没有变化。

在5009.27《食品中苯并芘的测定》中第一法“荧光分光光度法”中,一开始是用二甲基甲酰胺萃取环己烷中的苯并芘,加入硫酸钠溶液后,就变成了环己烷提取二甲基甲酰胺中的苯并芘! 请高人指点下加入硫酸钠的作用是什么,谢谢!以下是标准中截取的片段,供参考。http://ng1.17img.cn/bbsfiles/images/2013/01/201301061002_418621_1633924_3.jpg
在做气项色谱分析时, 经常遇到这种情况,购买的标准物质的溶剂和检测样品时的萃取溶剂不一致,例如标准溶液是甲醇中的六六六,而样品萃取时需要用环己烷,那么进样时标准系列是甲醇溶的,样品是环己烷溶的,可以吗?影响定量吗?
啶虫脒在正己烷中的溶解度,到哪个网站去查,比较权威。啶虫脒在配标准溶液的时候,用丙酮定容好,还是用正己烷。
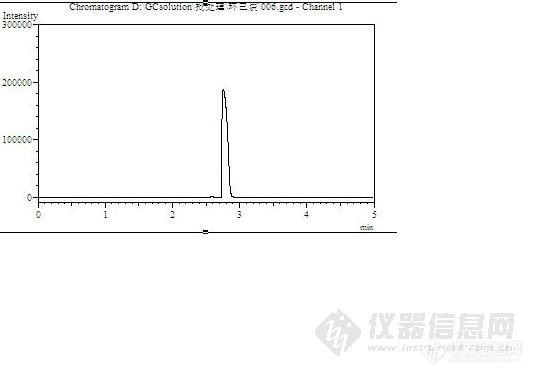
近日做工作场所空气中环己烷的测定。环己烷是有汽油气味的无色流动性液体。主要用于制备环己醇和环己酮,也用于合成尼龙6。在涂料工业中广泛用作溶剂。是树脂、脂肪、石蜡油类、丁基橡胶等的极好溶剂。取样后先是按照GBZ/T 160.41-2004方法规定的极性填充柱做,发现环己烷与溶剂二硫化碳分不开。后改用毛细柱OV-101分离的很好。 http://ng1.17img.cn/bbsfiles/images/2011/07/201107161544_305192_2103464_3.jpg上图是按照标准规定做的图。二硫化碳与环己烷峰重叠,改变条件也无法分离。经分析发现 :二硫化碳与环己烷均为非极性分子,环己烷沸点为80.7℃,二硫化碳沸点为 46.5℃两者极性相差很小,沸点相差很大。用非极性柱可以较好的分离,手头有一根非极性毛细柱OV101于是尝试用非极性毛细柱来做。http://ng1.17img.cn/bbsfiles/images/2011/07/201107161545_305195_2103464_3.jpg这是按照毛细柱做的图 分离的很好,理论板数45537 相关系数0.9999色谱条件: 岛津气相GC-2014C 带自动进样器AOC20+ 色谱柱:OV101 检测器: FID氢焰离子化检测器柱长:25 m 内径: 0.2 mm 膜厚: 0.25 μm 柱 温:50℃ 汽化室温度:140℃ 检测器温度160℃ 载气:18.0cm/s 氢气:40.0ml/min 空气:400.0ml/min 分流比 1 :50 试剂:二硫化碳(色谱纯) 环己烷(分析纯)标准溶液:在已含少量二硫化碳容量瓶中,称取环己烷,用二硫化碳稀释成1.0mg/ml的环己烷标准溶液。标准曲线的绘制: 用二硫化碳稀释标准溶液成 100、300、500ug/ml的环己烷标准系列。测定方法: 按GBZ/T 160.41-2004操作,1.0mL二硫化碳解吸,进 1μl标准与样品溶液,制得色谱图,以保留时间定性,外标法峰面积定量。http://ng1.17img.cn/bbsfiles/images/2011/07/201107161607_305200_2103464_3.jpg这是样品测定图,环己烷未检出。结论:对于非极性组分的分离一般选择非极性柱子,本法采用非极性毛细柱,不仅分离良好,而且有比填充柱高的多的柱效。对于工作场所空气中环己烷的测定定量准确,是对原方法的改进。
求环己烷国家标准,最新版的,拜托
请问,有人做过倍他环糊精中的环己烷吗?你们是怎么做的呀?我按照标准做的,对照品环己烷不溶,求解是怎么回事,谢谢
我用环己烷萃取培养基中的芘,比例是1:1,培养基主要有氯化铵,葡萄糖,吐温80、无机溶液和维生素溶液,培养基中的菌片用20mL环己烷和丙酮1:1 超声萃取,前段时间做实验上层是那种泡沫状,应该是乳化现象吧,很难分离,最近又出现上层有机相浑浊,放置很久还是很浑浊,尤其是第一次菌片的超声萃取很浑浊,是萃取剂的问题还是什么呢?
做航煤样中芳香族化合物的紫外谱图时,用正己烷稀释还是环己烷稀释,两者的区别大吗?我看资料一般芳香族化合物用的是环己烷做溶剂,我用了正己烷,不知道对结果的影响大不大?
正己烷的溶剂残留的方法学验证最近做正己烷的溶剂残留的方法学验证,用DMSO做溶剂,直接进样法,不知道什么原因,标准溶液中正己烷的峰面积呈下降的趋势。是标准溶液在放置过程中正己烷挥发了吗?
RT,有个产品用DMF溶就会出现三乙胺出峰变小甚至没有的问题,用咪唑啉酮溶解乙醇峰会变得很大,因为要测甲醇,乙醇,乙酸乙酯,三乙胺的残留,所以这些都不合适,用氢氧化钠溶液溶解,然后用环己烷萃取,结果乙醇还好,能出来大约一半的响应,甲醇才百分之三四的量,所以想用什么方法使甲醇萃取出来的多一点
用液相色谱做抗氧剂,流动相是甲醇,用甲醇溶的抗氧剂和环己烷溶的抗氧剂,跑出来的峰面积差距过大怎么回事呢?甲醇是3.7亿,环己烷是2.8亿左右。检测器是紫外的
ISO 2228-1972 工业用甲醛溶液 甲醇含量的测定 SH/T 1674-1999 工业用环己烷纯度及烃类杂质的测定 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法乙二醇三丁醚的含量测定求助标准,谢谢了。
实验条件:HP-1色谱柱,FID检测器,进样温度160,柱温40,检测器温度160,载气N2样品是甲苯和环己烷的甲醇溶液目前确定甲醇先出,对于甲苯和环己烷不知道沸点和极性哪个的影响大一点,谱图在附件同时还像请教下连续多次重复测定时,基线突然不平整是什么原因(区别是手动进样操作人不一样)
短链氯化石蜡标准溶液(100ppm)是存放在一个抽屉里,不知是什么时候泄露了,溶剂是环己烷,已经挥发了。是存放在一个抽屉里。应该怎么处理这个抽屉?会有毒吗?
车间空气中环己烷测定,用什么柱子好,标准所用柱子不能分离二硫化碳和环己烷,请教各位!
要从甲苯 正庚烷中分离提取甲基环己烷,可以按以下步骤进行:由于正庚烷是直链烷烃,沸点比那2个相同C原子数的烃类要高,所以先蒸馏蒸出甲苯和环己烷,然后在溶液中加入酸性KMnO4,甲苯变苯甲酸下沉,分液除去上层液体,然后再用乙醚萃取几次,再酸洗,碱洗,酸洗,干燥、蒸馏,得精品。还有其它的方法吗?
[align=center][img]https://img1.17img.cn/17img/images/201910/uepic/81ef7dca-16d8-4b3b-9f44-42d0cfba1c65.jpg[/img][/align]今天为大家带来食品中嘧霉胺、嘧菌胺、腈菌唑和嘧菌酯的测定。[b]适用范围[/b]适用于食品中嘧霉胺、嘧菌胺、腈菌唑和嘧菌酯的检测。(本实验样品采用菠菜和鳕鱼)。参考标准《GB 23200.46-2016 食品安全国家标准 食品中嘧霉胺、嘧菌胺、腈菌唑、嘧菌酯残留量的测定 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱法》[b]提取步骤一、菠菜:精确称取样品2.0g置于50mL的螺口尖底离心管[/b]1) 加入5mL丙酮和3g氯化钠,振荡1min,超声30min,移取上清液至另一个离心管中,用4mL丙酮分2次洗涤原离心管滤渣,合并上清液。2) 向上清液中加入5mL氯化钠溶液和6mL乙酸乙酯,振荡1min,静置分层(若乳化可4000rpm下离心5min),取上层有机相,向下层水相加4mL乙酸乙酯再次萃取,合并有机相,过5g无水硫酸钠,置于旋转蒸发瓶中,40℃水浴旋蒸至干,用1mL乙腈:甲苯(3:1)溶解待净化。[b]二、鳕鱼:精确称取样品2.0g置于50mL的螺口尖底离心管[/b]1) 加入5mL乙酸乙酯和3g氯化钠,振荡1min,超声30min,4000r/min离心5min,移取上清液过5g无水硫酸钠至旋转蒸发瓶中,再用4mL乙酸乙酯提取残渣,上清液过5g无水硫酸钠转至旋转蒸发瓶中,于40℃水浴旋蒸至干。2) 向旋转蒸发瓶中加入10mL乙腈饱和正己烷,转至50mL离心管中,再向旋转蒸发瓶中加入10mL正己烷饱和乙腈,转至同一50mL离心管中,振荡分层,乙腈层过5g无水硫酸钠转至原旋转蒸发瓶中;正己烷层再用5mL正己烷饱和乙腈振荡分层,弃去正己烷层,乙腈层过5g无水硫酸钠转至原旋转蒸发瓶中,于40℃水浴旋蒸至干,用1mL乙腈:甲苯(3:1)复溶待净化。注释:1) 正己烷饱和乙腈:100mL正己烷和100mL乙腈振荡,静置2h,下层为正己烷饱和乙腈。2) 乙腈饱和正己烷:100mL正己烷和100mL乙腈振荡,静置2h,上层为乙腈饱和正己烷。[b]SPE净化步骤SPE柱:[/b]月旭Welchrom Carb/NH2,规格:500mg/500mg/6mL。[b]活化:[/b]5mL乙腈:甲苯(3:1)活化,弃去;[b]上样:[/b]待净化液全部上样,控制流速,不宜过快,弃去;[b]淋洗:[/b]1mL乙腈:甲苯(3:1)洗涤旋转蒸发瓶,过柱弃去;[b]洗脱:[/b]精确移取8mL乙腈:甲苯(3:2)洗脱,抽干并收集于15mL离心管中;[b]复溶:[/b]将收集液体于45℃水浴氮吹至干,用丙酮-正己烷(1+1)定容至1mL,供检测。[b]色谱条件[/b][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]条件[b]色谱柱:[/b]WM-5MS 30m*0.25mm,0.25μm[b]进样口温度:[/b]250℃[b]升温程序:[/b]初始温度为100℃,保持1min;以10℃/min升温至210℃,保持2min;再以30℃/min升温至280℃,保持5min;最后以10℃/min升温至290℃,保持6min[b]载气:[/b]高纯氦气(纯度99.999%)[b]进样方式:[/b]不分流进样[b]恒流模式:[/b]1mL/min[b]进样量:[/b]2μL质谱条件[b]电离方式:[/b]电子轰击电离源(EI);[b]电离能量:[/b]70eV;[b]传输线温度:[/b]280℃;[b]离子源温度:[/b]230℃;[b]四极杆温度:[/b]150℃;[b]监测方式:[/b]选择离子扫描(SIM)1;[b]选择监测离子(m/z):[/b]嘧霉胺:定量 198;定性 199、188、184;嘧菌胺:定量 222;定性 223、208、181;腈菌唑:定量 179;定性 150、245、288;嘧菌酯:定量 344;定性 388、372、403;[b]溶剂延迟:[/b]8.0min。[b]谱图及数据[/b][align=center][img=,600,108]https://img1.17img.cn/17img/images/201910/uepic/d73f5e5c-38f2-4613-880d-600d23b097c2.jpg[/img][/align][align=center]图1.嘧霉胺等4种混合0.1mg/L标准图谱[/align][align=center][img=,600,108]https://img1.17img.cn/17img/images/201910/uepic/91db2d03-36df-4f5a-ab05-f0cba0c84633.jpg[/img][/align][align=center]图2.菠菜空白图谱[/align][align=center][img=,600,108]https://img1.17img.cn/17img/images/201910/uepic/eb79b4a7-3abe-42b5-be1f-6655a0983417.jpg[/img][/align][align=center]图3.菠菜样加标0.05mg/kg图谱[/align][align=center][img=,600,107]https://img1.17img.cn/17img/images/201910/uepic/b87e6d83-9431-40ce-a315-0d6a646f0180.jpg[/img][/align][align=center]图4.鳕鱼空白图谱[/align][align=center][img=,600,107]https://img1.17img.cn/17img/images/201910/uepic/773a1894-15ff-490b-84a0-39227e83107e.jpg[/img][/align][align=center]图5.鳕鱼样加标0.05mg/kg图谱[/align][align=center][img=,600,290]https://img1.17img.cn/17img/images/201910/uepic/473ef04c-9c09-42dd-8ba7-9d6e160f5539.jpg[/img][/align][b]相关产品信息[/b][align=center][img=,600,474]https://img1.17img.cn/17img/images/201910/uepic/cf428b91-631b-4d89-9f69-cd573bc29a3f.jpg[/img][/align]
环己烷能作溶剂进反向HPLC吗?流动相是甲醇:水=9:1柱子是C18环己烷在甲醇中的溶解度为:100份甲醇可溶解57份环己烷我看到有篇外文文献做PAH,浓缩后环己烷定容,进C18流动相为乙腈+水大家讨论一下吧,能用吗?会不会有溶剂效应呢?多谢大家
紫外法测油,正己烷参比和标准溶液的吸光度不停变低?我属于个例?紫外光的影响?挥发影响?
有人做过倍他环糊精残留溶剂没,怎么感觉环己烷不怎么溶于20%的二甲基亚砜,刚加进去的时候感觉像是油滴加进去似的,剧烈摇晃后感觉有点像乳化,在此请教给位老师是怎么回事。。。