水质样品检验与食品样品检验,如果同时是1/10稀释液平皿上未出现菌落生长,菌落总数结果报告有何区别?各如何(表述)报告结果呢?请连接:http://bbs.instrument.com.cn/shtml/20120104/3777936/“检验固体食品样品时,1/10稀释液平皿上未出现菌落生长,菌落总数应如何报告?”的话题。
检验固体食品样品时,1/10稀释液平皿上未出现菌落生长,菌落总数应如何报告?
[align=center]平皿计数法测菌落总数验证[/align][align=center]化工室:张苗苗[/align]一、 范围及定义1、范围 本标准规定了用平皿计数法测定生活饮用水及其水源水中的菌落总数。2、定义 菌落总数是指水样在营养琼脂上有氧条件下37℃培养24h后,所得1mL所含菌落的总数。二、仪器1、高压蒸汽灭菌器2、生化培养箱3、菌落计数器4、pH计或精密pH试纸5、灭菌试管、平皿,刻度吸管,采样瓶等。三、检验步骤1、以无菌操作方法用灭菌吸管吸取1mL充分混匀的水样,注入灭菌平皿中,倾注约15ml以融化并冷却到45℃左右的营养琼脂培养基,并立即旋摇平皿,使水样与培养基充分混匀。每次检验时应做一平行接种,同时另用一个平皿只倾注营养琼脂培养基作为空白对照。2、待冷却凝固后,翻转平皿,使底面向上,置于37℃培养箱培养24h,进行菌落计数,即为水样1mL中的菌落总数。四、菌落计数作平皿菌落计数时,可用菌落计数器检查,以防遗漏,在记下各平皿的菌落数后,应求出同稀释度的平均菌落数,供下一步计算时应用。再求同稀释度的平均数时,若其中一个平皿有较大片状菌落生长时,则不宜采用,而应以无片状菌落生长的平皿作为该稀释度的平均菌落数。若片状菌落不到平皿的一半,而其中一半中菌落数分布又很均匀,则可将此平皿计数后乘2以代表全皿菌落数。然后再求该稀释度的平均菌落数。五、计算和报告计数结果不同稀释度的选择1、首先选择平均菌落数在30~300之间者进行计算,若只有一个稀释度的平均菌落数符合此规范时,则将该菌落数乘以稀释倍数报告之(见表1中实例1) 2、若有两个稀释度,其生长的菌落数均在30~300之间,则视二者之比值来决定,若其比值小于2应报告两者的平均数(如表1中实例2)若其比值大于2应报告其中稀释度较小的菌落总数(如表1中实例3)。若等于2应报告其中稀释度较小的菌落数(如表1中实例4).3、 若所有的稀释度的平均菌落数均大于300,则应按稀释度最高的平均菌落数乘以稀释倍数报告之(见表1中实例5)4、 若所有的稀释度的平均菌落数均小于30,则应按稀释度最低的平均菌落数乘以稀释倍数报告之(见表1中实例6)5、 若所有的稀释度的平均菌落数均不在30~300之间,则应以最接近30或300的平均菌落数乘以稀释倍数报告之(见表1中实例7)6、 菌落计数的报告:菌落数在100以内时按实有数报告;大于100时,采用两位有效数字,在两位有效数字后面的数值以四舍五入方法计算。为了缩短数字后面的零数也可用10的指数来表示。 [b]表1 稀释度选择及菌落总数报告方式[/b][table][tr][td=1,2][align=center]实例[/align][/td][td=3,1][align=center]不同稀释度的平均菌落数[/align][/td][td=1,2][align=center]两个稀释度菌落数之比[/align][/td][td=1,2][align=center]菌落总数/(CFU/mL)[/align][/td][td=1,2][align=center]报告方式/(CFU/mL)[/align][/td][/tr][tr][td][align=center]10[sup]-1[/sup][/align][/td][td][align=center]10[sup]-2[/sup][/align][/td][td][align=center]10[sup]-3[/sup][/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]1365[/align][/td][td][align=center]164[/align][/td][td][align=center]20[/align][/td][td][align=center]-[/align][/td][td][align=center]16 400[/align][/td][td][align=center]16 000或1.6×10[sup]4[/sup][/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]2760[/align][/td][td][align=center]295[/align][/td][td][align=center]46[/align][/td][td][align=center]1.6[/align][/td][td][align=center]37 750[/align][/td][td][align=center]38 000或3.8×10[sup]4[/sup][/align][/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]2890[/align][/td][td][align=center]271[/align][/td][td][align=center]60[/align][/td][td][align=center]2.2[/align][/td][td][align=center]27 100[/align][/td][td][align=center]27 000或2.7×10[sup]4[/sup][/align][/td][/tr][tr][td][align=center]4[/align][/td][td][align=center]150[/align][/td][td][align=center]30[/align][/td][td][align=center]8[/align][/td][td][align=center]2[/align][/td][td][align=center]1 500[/align][/td][td][align=center]1 500或1.5×10[sup]3[/sup][/align][/td][/tr][tr][td][align=center]5[/align][/td][td][align=center]多不可计[/align][/td][td][align=center]1650[/align][/td][td][align=center]513[/align][/td][td][align=center]-[/align][/td][td][align=center]513 000[/align][/td][td][align=center]510 000或5.1×10[sup]5[/sup][/align][/td][/tr][tr][td][align=center]6[/align][/td][td][align=center]27[/align][/td][td][align=center]11[/align][/td][td][align=center]5[/align][/td][td][align=center]-[/align][/td][td][align=center]270[/align][/td][td][align=center]270或2.7×10[sup]2[/sup][/align][/td][/tr][tr][td][align=center]7[/align][/td][td][align=center]多不可计[/align][/td][td][align=center]305[/align][/td][td][align=center]12[/align][/td][td][align=center]-[/align][/td][td][align=center]30 500[/align][/td][td][align=center]31 000或3.1×10[sup]4[/sup][/align][/td][/tr][/table]对自来水的检测结果如下:[table][tr][td]接种量[/td][td]10[sup]-1[/sup][/td][td]10[sup]-2[/sup][/td][td]10[sup]-3[/sup][/td][td]10[sup]-1[/sup][/td][td]10[sup]-2[/sup][/td][td]10[sup]-3[/sup][/td][td]10[sup]-1[/sup][/td][td]10[sup]-2[/sup][/td][td]10[sup]-3[/sup][/td][/tr][tr][td]计数结果[/td][td]26[/td][td]10[/td][td]3[/td][td]23[/td][td]9[/td][td]3[/td][td]25[/td][td]10[/td][td]2[/td][/tr][tr][td]菌落总数CFU/mL)[/td][td=3,1]260[/td][td=3,1]230[/td][td=3,1]250[/td][/tr][/table]六、结论 此方法均符合GB/T5750.12-2006七、注意事项 1、所有玻璃器皿如试管、平皿,刻度吸管,采样瓶等都应灭菌。 2、做样品稀释的液体,每批都要有空白对照。 3、计数时应仔细观察
想请教一下有谁知道罗氏瓶是什么样的瓶子啊?实在不知道该在哪个版面求助,大家见谅啊~~~
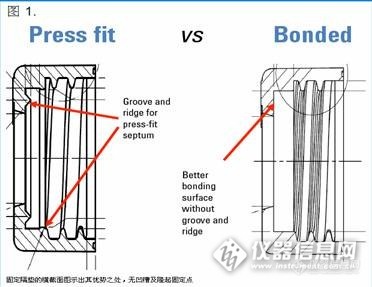
现场测试表明,在大多数情况下,安捷伦固定螺口盖的性能比标准非固定螺口盖好得多。使用非固定瓶盖的缺点浪费时间:需单独采购这些物品,到货后需将各组成部分组装起来可能发生错误:自行组装会引入污染、匹配不当以及将错误的瓶盖和错误的隔垫混在一起跟踪的负担:有相当多的部件号需要跟踪,同时还不能混淆库存其他潜在问题:隔垫被随机地推动、隔垫落入袋中、造成随后的分析时间损失安捷伦固定瓶盖的优点购买更少的部件:通常只有一半的部件号,再也无需购买单独的瓶盖或隔垫。安捷伦瓶盖始终具有固定在其上的隔垫无需预组装:降低产生问题的机会,如引入污染物、装配不当,以及将错误的瓶盖和错误的隔垫混在一起节省时间:减少订购、装配和故障排除的时间经济合算:价格与现有产品类似多种选择:从现有的螺口盖换为固定螺口盖,您可以通过九种选择轻易地实现先进的设计及测试安捷伦固定瓶盖的主要特点是将隔垫牢牢固定。这意味着隔垫在组装过程中不会夹在螺纹中,或在瓶盖拧紧时脱落。图 1 示出了与安捷伦固定隔垫出众的无缝固定相比,非固定隔垫老式的隆起和凹槽固定点的缺点。http://ng1.17img.cn/bbsfiles/images/2015/06/201506241021_551255_1601668_3.jpg我们在产品开发过程中进行了大量的正交试验,确保固定瓶盖在短期或长期内都没有缺点。我们未使用粘合剂或其他化学品将隔垫固定到瓶盖。因此,可以获得紧密、持久的贴合,并可防止污染物和/或浸出物进入样品。此外,我们进行了大量的化学品/材料测试,以确保额外的退火不会将可萃取物或浸出物从隔垫和/或瓶盖材料中释放到样品中。注意,安捷伦固定技术只适用于聚合物瓶盖,而不适用于与钳口盖、三层隔垫或夹层式隔垫。然而,无论您使用的是哪种瓶盖/隔垫组合,都不建议重复使用样品瓶和瓶盖。解决样品瓶瓶盖和隔垫的问题为了让您充分利用安捷伦固定隔垫的先进技术,我们提供了一些解决自动进样器中样品瓶瓶盖和隔垫常见问题的有用技巧(表 1)。问题现象分辨率碎屑进样针将硅胶撕裂了一块隔垫被刺穿,并落入样品瓶中确保针尖锋利,或更换针头/进样针粘连由于针粘连到隔垫上,造成针驻留在样品瓶内,使得自动进样器将样品瓶拉出样品盘此问题很少发生,但可以通过 Agilent G4513A 进样器 (A.10.09) 在 2014 年 6 月的固件更新得到解决隔垫被推入隔垫被推入样品瓶正确组装样品瓶和瓶盖十分必要,所以请在样品瓶顶部触及到隔垫后,将瓶盖拧至少四分之一圈。此外,请重新校准自动进样器,使进样针穿刺瓶盖的中心难以刺穿隔垫新隔垫很难被刺穿新隔垫较硬安捷伦每批隔垫的制造标准都秉持性能一致的要求。刚度或硬度与其他因素有关,如进样针或自动进样器装置进样针外径较大我使用的是大号进样针我使用的是液相色谱较大的进样针可能导致碎屑形成或隔垫被推入样品瓶中。安捷伦建议为较大的进样针使用固定瓶盖或预分体瓶盖表 1. 隔垫问题解决技巧
液氩气瓶与常规瓶装氩气瓶出口端的螺口相同吗?能用接液氩出瓶端口的接头去接瓶装氩气瓶出口端的接头吗?
喜炎平脉络宁注射液引起严重过敏2012年06月27日08:47新华网国家食品药品监督管理局26日发布通报,提示生产企业和医患人员关注喜炎平注射液和脉络宁注射液引起严重过敏反应的问题。据了解,喜炎平注射液的成分是穿心莲内酯磺化物,主要用于解热消炎。2011年,国家药品不良反应监测中心病例报告数据库有关喜炎平注射液的病例报告数共计1476例,其中涉及14岁以下儿童报告达1048例。主要不良反应表现为过敏样反应、过敏性休克、紫绀、呼吸困难等。脉络宁注射液是2009版国家基本药目录品种,其功能与主治为清热养阴、活血化瘀。用于血栓闭塞性脉管炎、动脉硬化性闭塞症、脑血栓形成及后遗症、静脉血栓形成等。2011年,国家药品不良反应监测中心病例报告数据库共收到有关脉络宁注射液药品不良反应病例报告1500例,其中严重病例报告189例。严重不良反应主要为呼吸系统损害、全身性损害和心血管系统损害等。国家食品药品监管局建议,由于这两种注射液易发生过敏反应,建议医护人员在用药前详细询问患者的过敏史,特殊人群和过敏体质者应慎重使用。使用时应严格按照说明书规定的用法用量给药,不得超剂量使用;谨慎联合用药。如确需联合使用其他药品时,应谨慎考虑与此两种药品的间隔时间以及药物相互作用等问题。对于药品生产企业,国家食品药品监管局建议,加强临床合理用药的宣传,确保产品的安全性信息及时传达给患者和医生;完善生产工艺、提高产品质量标准,开展相应安全性研究。(新华网)
大家好,使用GC2010气相色谱仪,顶空进样器如上。这种瓶子不知道大家有谁用过? 使用的原理 螺纹口旋塞是铁的那种,进样器依靠磁力作用将瓶子转移到agitator里面,保持恒定温度振荡,吸取样品后,再将瓶子吸到样品架上。 因为瓶子是玻璃的,螺纹口旋塞是铁皮的,所以拧的过程中经常出现玻璃螺纹被拧碎掉,这样一来对实验不准,二来也造成一定的浪费。但是拧瓶盖这种力气活也没有一种标准,感觉拧紧了就可以了大家有碰到这种比较尴尬的情况没有啊? 上次做一批样品,就拧坏了5个20ml 的玻璃样品瓶 碰上这种事情真够郁闷的

严格来说,这个也不算是特殊的样品瓶,但是国内用的还相对较少,所以也拉出来单独介绍下!http://ng1.17img.cn/bbsfiles/images/2012/02/201202271712_351313_2067003_3.jpg这种顶空瓶最大的好处就在于——方便、安全!使用方便,无需钳口工具进行处理,避免了错误钳口的风险;螺纹口技术更方便和更容易打开和拧紧,样品可在现场移取,无须在实验室移取;专业精密螺纹设计使垫片和瓶口的气密性更好,作为顶空样品瓶使用,操作更方便和安全,并可保证分析结果的良好重复性。特别适用于 CTC Combi PAL、TriPlus和岛津AOC5000或者其他类似仪器,中心开孔的设计可用于SPME,同时也适用于顶空分析,且仍提供了足够的磁性面积来转移充满样品的瓶子。隔垫的厚度更薄,采用优质原料及无胶粘合工艺,具有良好的的弹性和密封性能,并使穿刺更容易、更安全,特别适合于自动SPME应用。呵呵,其实凡是长成下面这样子的仪器都是CTC的,贴了不同牌子而已~http://ng1.17img.cn/bbsfiles/images/2012/02/201202271719_351316_2067003_3.jpg
DIN 84-1970 有槽平頂錐頭螺釘(中文版).pdf
钳口进样瓶,螺纹进样瓶,你喜欢哪种作为日常进样瓶?为什么?
某日,氮气用完,要换氮气。用手推车推着空的氮气瓶去气站,推着推着在中途轮子就滚出来了!氮气瓶顿时砸在了地上!当时人就愣住了,轮子怎么就滚出来了呢?!结果从同事处得知,这个车子原来就已经坏了,只是在将就着用,而我太久没换过氮气,不知道它已经坏了……无奈,把轮子装回去,小心翼翼地继续把空氮气瓶推到气站,换了一瓶满的,然后继续更加小心翼翼地推回来。假如在推装满氮气的氮气瓶时,手推车轮子滚落,氮气瓶会不会爆炸?想来后怕。
近期在看网络讲堂的一些科研视频,发现视频都无法全屏观看。请问如何设置呢?谢谢
出口食品平板菌落计数 中华人民共和国进出口商品检验行业标准 SN 0168-92代替 ZB X09 001-86 Plate count for bacterial colonies in food for export 1 主题内容与适用范围 本标准规定了出口食品平板菌落计数的方法。 本标准适用于各种出口食品及其原料,有专门规定检验方法的除外。2 设备和材料2.1 工作台:超净工作台或放于清洁、光线充足的实验室里的水平工作台。琼脂平板在工作台上暴露15 min,每平板不得超过15个菌落。2.2 恒温培养箱:36±1℃。2.3 恒温水浴箱:45±1℃。2.4 均质器。 2.5 振荡器。2.6 吸管:1、10和25mL,具0.1mL刻度。2.7 平皿:直径为90 mm。2.8 稀释瓶:广口瓶或三角烧瓶,容量为200 mL和500 mL。2.9 玻璃珠:直径为5mm左右。 2.10 天平:感量0.1g。3 培养基和试剂 3.1 平板计数琼脂。3.2 75%乙醇。3.3 稀释剂:磷酸盐缓冲稀释液。4 操作程序 4.1 样品制备 4.1.1 以无菌操作取有代表性的样品盛于灭菌容器内,如有包装,则用75%乙醇在包装开口处擦拭后取样。4.1.2 制备样品匀液4.1.2.1 固体或半固体食品:以无菌操作取25 g样品,放入装有225mL稀释剂的灭菌均质杯内,于8000r/min均质1~2min,制成1:10的样品匀液。如样品均质时间超过2min,应在均质杯外加冰水冷却。4.1.2.2 干燥或干粉食品:以无菌操作取25 g样品,放入装有225mL稀释剂和适量玻璃珠的500 mL稀释瓶中。迅速振摇,将样品混匀,制成1 : 10的样品匀液。振摇时,幅度为30cm,7s内振摇25次,也可用机械振荡器振荡15s代替手摇。4.1.2.3 液体食品: 用灭菌吸管吸取25mL样品, 放入装有225mL稀释剂的500mL稀释瓶中,按4.1.2.2条中所述方法迅速振摇,制成1:10的样品匀液。吸取样品时,吸管插入液面下不要超过2.5cm。吸管内液体要在2~4s内完全排入稀释剂中。不要在稀释剂中吹洗吸管。4.2 稀释样品匀液 4.2.1 用10 mL灭菌吸管准确吸取1:10的样品匀液10 mL,放入装有90 mL稀释剂的200mL, 稀释瓶中。按4.1.2.2条中所述的方法,迅速振摇。制成1:100的样品液。从容器中吸取样品匀液和以后的稀释操作中,吸管尖不要碰着瓶口。吸入的液体应先高于所要求的刻度,然后提起吸管使其尖端离开液面并贴在容器内壁将液体调至所要求的刻度。4.2.2 分别用10mL灭菌吸管按4.2.1条所述方法将样品匀液制成10倍递增稀释的样品液,如10**-3、10**-4、10**-5……。4.3 平板接种4.3.1 对于每一个样品,选用合适的三个连续稀释度的样品液进行平板计数。 4.3.2 分别用灭菌吸管吸取1mL样品液放入作了适宜标志的平皿内。每个稀释度的样品液用两个平皿。如果某一样品液在取出供试部分前的放置时间超过3 min,应按4.1.2.2条所述方法再振摇该样品液。4.3.3 分别加12~15mL平板计数琼脂(已放45+1℃的水浴中恒温)到各平皿内。立即将平皿内的样品液和琼脂培养基充分混合。混合方法是将平皿倾斜和旋转。要防止把混合物溅到平皿壁和盖上。同时将平板计数琼脂倾入加有1 mL稀释剂的另一灭菌平皿作空白对照。将样品液加入平皿后应立即倾注琼脂培养基,每个样品从开始稀释到倾注最后一个平皿所用的时间不得超过20min。4.4 培养 待琼脂凝固后将平皿翻转,立即放进36±1℃的恒温培养箱内培养48±2h。培养箱应 保持一定的湿度,经48h培养的琼脂培养基的失重不得超过15%。4.5 菌落计数和记录4.5.1 培养后,立即计数每个平板上的菌落数。25~250个菌落为合适范围。如果不能立即计数,应将平板存放于0~4℃,但不得超过24 h。 4.5.2 如只有一个稀释度的两个平板上的菌落在合适范围内, 先计算两个平板的平均值,再将平均值乘以相应稀释倍数,作为每克(毫升)样品中平板菌落数(下表,样品1)。4.5.3 如有两个稀释度在合适范围内,先计算每个稀释度两个平板的平均值,再计算两个稀释度的平均值,然后计算每克(毫升)样品中平板菌落数(下表,样品2)。4.5.4 当最低稀释度的两个平板上都少于25个菌落时,计数这一稀释度两个平板上的实际菌落数,计算两个平板上的平均菌落数,将平均菌落数乘以稀释倍数,得到估计的平板菌落数。给这个数注上星号(*), 表明该数系从菌落数在25~250这一范围之外的平板估计所得(下表,样品3)。4.5.5 当所有平板上的菌落都超过250时,则应将最高稀释度的两个平板的平均菌落数乘以稀释倍数,得到估计的平板菌落数。给这个数注上星号(*) (意义同4.5.4)(下表,样 品4)。4.5.6 如果所有稀释度的平板都没有菌落,则以小于1乘以最低稀释倍数报告平板菌落数。给这个数注上星号(*) (意义同4.5.4条) (下表,样品5)。4.5.7 同一稀释度的两个平板中,一个有25~250个菌落,另一个的菌落多于250个,两个平板都要计数。计算方法同4.5.2条(下表,样品6)。4.5.8 两个连续稀释度中的每个稀释度都有一个平板的菌落数在25~250个范围内,而另一个的菌落数高于250或低于25,四个平板都要计数。计算方法参照4.5.2条和4.5.3条(下表,样品7)。 4.5.9 某稀释度的两个平板都有25~250个菌落,而另一稀释度的两个平板中只有一个平板的菌落数在 25~250范围内。四个平板都要计数,计算方法参照4.5.2条和4.5.3条 (下表,样品8、9)。4.5.10 蔓延生长菌落 通常有三种不同类型的蔓延生长菌落。第一种类型是链状菌落,菌落之间没有明显界线,这些菌落是当琼脂和试验物混合时,一个细菌块被分散所致;第二种类型是在琼脂和 平皿底之间形成的水膜样菌落;第三种是在平皿边缘或琼脂表面形成的水膜样菌落。如果所选择的平板出现过量的蔓延菌落生长,以致a.被蔓延菌落盖住的地方,包括由于蔓延菌落造成的抑制生长区面积超过平板面积的50%,或b.由于蔓延菌落造成的抑制生长区面积超过平板面积的25%,这样的平板报告为“蔓延菌落”,不予计数。计数其他平板上的菌落数,将这些数值的算术平均值报告为平板菌落数(下表,样品10)。 当有必要计数除以上a.和b.外的蔓延生长菌落时,将三种不同类型的蔓延菌落分别计数。对于第一种类型,如果仅有一条链,将它作为一个菌落计。如果有来源不同的几条链, 将每条链作为一个菌落计,不要把链上生长的各个菌落分开来数。第二种和第三种类型的蔓延生长形成易于鉴别的菌落,即按一般菌落计数,把计数的蔓延生长菌落数同一般菌落数加在一起,计算平板菌落数。4.5.11 操作者对同一平板复核自己的计数结果,其差异应在5%之内,而其他人对这一平板重复计数,其差异应在10%之内。否则,应找出原因,加以校正。 4.6 计算和记录数字 适宜稀释度的两个平板的菌落数平均值或两个稀释度的平板菌落数平均值乘以相应稀释倍数计算出每克(毫升)样品中平板菌落数。 记录时,只有在换算到每克(毫升)样品中平板菌落数时,才能定下两位有效数字,第三位数字采用四舍五入的方法记录。也可将样品的平板菌落数记录为10的指数形式(见下表中的例子)。5 结果报告 报告每克(毫升)样品中平板菌落数或估计的平板菌落数。 平板菌落数计算 样品号 菌 落 数 平板菌落数/g(mL) 1:100 1:1000 1:10000 1 多不可计 175 16 多不可计 208 17 190000(1.9×10**5) 2 多不可计 224 25 多不可计 245 30 250000(2.5×10**5)* 3 18 2 014 0 0 1600(1.6×10**3)* 4 多不可计 多不可计 523多不可计 多不可计 487 5100000(5.1×10**6)* 5 0 0 00 0 0 <100 (<1.0×10**2)* 6 多不可计 245 23 多不可计 278 20 260000(2.6×10**5) 7 多不可计 225 21多不可计 255 40 270000(2.7×10**5) 8 多不可计 210 18多不可计 240 28 230000(2.3×10**5) 9 多不可计 260 30 多不可计 230 28 270000(2.7×10**5) 10 多不可计 245 35多不可计 230 蔓延菌落 290000(2.9×10**5) 注:带星号*者为估计数。附 录 A 培养基制备 (补充件) A1 平板计数琼脂 胰蛋白胨 5.0g 酵母浸膏 2.5g 葡萄糖 1.0g 琼 脂 15.0g 蒸馏水 1000mL 将各成分加于蒸馏水中,煮沸溶解。分装试管或烧瓶,121℃高压灭菌15min。最终pH7.0±0.1。A2 磷酸盐缓冲稀释液 贮存液: 磷酸二氢钾(KH2PO4) 34.0g 蒸馏水 500mL 用大约175 mL的1mol/L氢氧化钠溶液调节pH至7.2,用蒸馏水稀释至1000 mL后贮存于冰箱。 稀释液:用蒸馏水稀释1.25mL贮存液至1000mL,分装于合适容器,121℃高压灭菌15min。附加说明: 本标准由中华人民共和国国家进出口商品检验局提出。 本标准由中华人民共和国河南进出口商品检验局、湖南进出口商品检验局负责起草 本标准主要起草人李志培、邓明义。 本标准主要参考美国食品和药物管理局(FDA)《细菌学分析手册》第6版第4章(1984年)。 中华人民共和国国家进出口商品检验局1992-12-28批准 1993-05-01实施
出口食品平板菌落计数 中华人民共和国进出口商品检验行业标准 SN 0168-92代替 ZB X09 001-86 Plate count for bacterial colonies in food for export 1 主题内容与适用范围 本标准规定了出口食品平板菌落计数的方法。 本标准适用于各种出口食品及其原料,有专门规定检验方法的除外。2 设备和材料2.1 工作台:超净工作台或放于清洁、光线充足的实验室里的水平工作台。琼脂平板在工作台上暴露15 min,每平板不得超过15个菌落。2.2 恒温培养箱:36±1℃。2.3 恒温水浴箱:45±1℃。2.4 均质器。 2.5 振荡器。2.6 吸管:1、10和25mL,具0.1mL刻度。2.7 平皿:直径为90 mm。2.8 稀释瓶:广口瓶或三角烧瓶,容量为200 mL和500 mL。2.9 玻璃珠:直径为5mm左右。 2.10 天平:感量0.1g。3 培养基和试剂 3.1 平板计数琼脂。3.2 75%乙醇。3.3 稀释剂:磷酸盐缓冲稀释液。4 操作程序 4.1 样品制备 4.1.1 以无菌操作取有代表性的样品盛于灭菌容器内,如有包装,则用75%乙醇在包装开口处擦拭后取样。4.1.2 制备样品匀液4.1.2.1 固体或半固体食品:以无菌操作取25 g样品,放入装有225mL稀释剂的灭菌均质杯内,于8000r/min均质1~2min,制成1:10的样品匀液。如样品均质时间超过2min,应在均质杯外加冰水冷却。4.1.2.2 干燥或干粉食品:以无菌操作取25 g样品,放入装有225mL稀释剂和适量玻璃珠的500 mL稀释瓶中。迅速振摇,将样品混匀,制成1 : 10的样品匀液。振摇时,幅度为30cm,7s内振摇25次,也可用机械振荡器振荡15s代替手摇。4.1.2.3 液体食品: 用灭菌吸管吸取25mL样品, 放入装有225mL稀释剂的500mL稀释瓶中,按4.1.2.2条中所述方法迅速振摇,制成1:10的样品匀液。吸取样品时,吸管插入液面下不要超过2.5cm。吸管内液体要在2~4s内完全排入稀释剂中。不要在稀释剂中吹洗吸管。4.2 稀释样品匀液 4.2.1 用10 mL灭菌吸管准确吸取1:10的样品匀液10 mL,放入装有90 mL稀释剂的200mL, 稀释瓶中。按4.1.2.2条中所述的方法,迅速振摇。制成1:100的样品液。从容器中吸取样品匀液和以后的稀释操作中,吸管尖不要碰着瓶口。吸入的液体应先高于所要求的刻度,然后提起吸管使其尖端离开液面并贴在容器内壁将液体调至所要求的刻度。4.2.2 分别用10mL灭菌吸管按4.2.1条所述方法将样品匀液制成10倍递增稀释的样品液,如10**-3、10**-4、10**-5……。4.3 平板接种4.3.1 对于每一个样品,选用合适的三个连续稀释度的样品液进行平板计数。 4.3.2 分别用灭菌吸管吸取1mL样品液放入作了适宜标志的平皿内。每个稀释度的样品液用两个平皿。如果某一样品液在取出供试部分前的放置时间超过3 min,应按4.1.2.2条所述方法再振摇该样品液。4.3.3 分别加12~15mL平板计数琼脂(已放45+1℃的水浴中恒温)到各平皿内。立即将平皿内的样品液和琼脂培养基充分混合。混合方法是将平皿倾斜和旋转。要防止把混合物溅到平皿壁和盖上。同时将平板计数琼脂倾入加有1 mL稀释剂的另一灭菌平皿作空白对照。将样品液加入平皿后应立即倾注琼脂培养基,每个样品从开始稀释到倾注最后一个平皿所用的时间不得超过20min。4.4 培养 待琼脂凝固后将平皿翻转,立即放进36±1℃的恒温培养箱内培养48±2h。培养箱应 保持一定的湿度,经48h培养的琼脂培养基的失重不得超过15%。4.5 菌落计数和记录4.5.1 培养后,立即计数每个平板上的菌落数。25~250个菌落为合适范围。如果不能立即计数,应将平板存放于0~4℃,但不得超过24 h。 4.5.2 如只有一个稀释度的两个平板上的菌落在合适范围内, 先计算两个平板的平均值,再将平均值乘以相应稀释倍数,作为每克(毫升)样品中平板菌落数(下表,样品1)。4.5.3 如有两个稀释度在合适范围内,先计算每个稀释度两个平板的平均值,再计算两个稀释度的平均值,然后计算每克(毫升)样品中平板菌落数(下表,样品2)。4.5.4 当最低稀释度的两个平板上都少于25个菌落时,计数这一稀释度两个平板上的实际菌落数,计算两个平板上的平均菌落数,将平均菌落数乘以稀释倍数,得到估计的平板菌落数。给这个数注上星号(*), 表明该数系从菌落数在25~250这一范围之外的平板估计所得(下表,样品3)。4.5.5 当所有平板上的菌落都超过250时,则应将最高稀释度的两个平板的平均菌落数乘以稀释倍数,得到估计的平板菌落数。给这个数注上星号(*) (意义同4.5.4)(下表,样 品4)。4.5.6 如果所有稀释度的平板都没有菌落,则以小于1乘以最低稀释倍数报告平板菌落数。给这个数注上星号(*) (意义同4.5.4条) (下表,样品5)。4.5.7 同一稀释度的两个平板中,一个有25~250个菌落,另一个的菌落多于250个,两个平板都要计数。计算方法同4.5.2条(下表,样品6)。4.5.8 两个连续稀释度中的每个稀释度都有一个平板的菌落数在25~250个范围内,而另一个的菌落数高于250或低于25,四个平板都要计数。计算方法参照4.5.2条和4.5.3条(下表,样品7)。 4.5.9 某稀释度的两个平板都有25~250个菌落,而另一稀释度的两个平板中只有一个平板的菌落数在 25~250范围内。四个平板都要计数,计算方法参照4.5.2条和4.5.3条 (下表,样品8、9)。4.5.10 蔓延生长菌落 通常有三种不同类型的蔓延生长菌落。第一种类型是链状菌落,菌落之间没有明显界线,这些菌落是当琼脂和试验物混合时,一个细菌块被分散所致;第二种类型是在琼脂和 平皿底之间形成的水膜样菌落;第三种是在平皿边缘或琼脂表面形成的水膜样菌落。如果所选择的平板出现过量的蔓延菌落生长,以致a.被蔓延菌落盖住的地方,包括由于蔓延菌落造成的抑制生长区面积超过平板面积的50%,或b.由于蔓延菌落造成的抑制生长区面积超过平板面积的25%,这样的平板报告为“蔓延菌落”,不予计数。计数其他平板上的菌落数,将这些数值的算术平均值报告为平板菌落数(下表,样品10)。 当有必要计数除以上a.和b.外的蔓延生长菌落时,将三种不同类型的蔓延菌落分别计数。对于第一种类型,如果仅有一条链,将它作为一个菌落计。如果有来源不同的几条链, 将每条链作为一个菌落计,不要把链上生长的各个菌落分开来数。第二种和第三种类型的蔓延生长形成易于鉴别的菌落,即按一般菌落计数,把计数的蔓延生长菌落数同一般菌落数加在一起,计算平板菌落数。4.5.11 操作者对同一平板复核自己的计数结果,其差异应在5%之内,而其他人对这一平板重复计数,其差异应在10%之内。否则,应找出原因,加以校正。 4.6 计算和记录数字 适宜稀释度的两个平板的菌落数平均值或两个稀释度的平板菌落数平均值乘以相应稀释倍数计算出每克(毫升)样品中平板菌落数。 记录时,只有在换算到每克(毫升)样品中平板菌落数时,才能定下两位有效数字,第三位数字采用四舍五入的方法记录。也可将样品的平板菌落数记录为10的指数形式(见下表中的例子)。5 结果报告 报告每克(毫升)样品中平板菌落数或估计的平板菌落数。 平板菌落数计算 样品号 菌 落 数 平板菌落数/g(mL) 1:100 1:1000 1:10000 1 多不可计 175 16 多不可计 208 17 190000(1.9×10**5) 2 多不可计 224 25 多不可计 245 30 250000(2.5×10**5)* 3 18 2 014 0 0 1600(1.6×10**3)* 4 多不可计 多不可计 523多不可计 多不可计 487 5100000(5.1×10**6)* 5 0 0 00 0 0 <100 (<1.0×10**2)* 6 多不可计 245 23 多不可计 278 20 260000(2.6×10**5) 7 多不可计 225 21多不可计 255 40 270000(2.7×10**5) 8 多不可计 210 18多不可计 240 28 230000(2.3×10**5) 9 多不可计 260 30 多不可计 230 28 270000(2.7×10**5) 10 多不可计 245 35多不可计 230 蔓延菌落 290000(2.9×10**5) 注:带星号*者为估计数。附 录 A 培养基制备 (补充件) A1 平板计数琼脂 胰蛋白胨 5.0g 酵母浸膏 2.5g 葡萄糖 1.0g 琼 脂 15.0g 蒸馏水 1000mL 将各成分加于蒸馏水中,煮沸溶解。分装试管或烧瓶,121℃高压灭菌15min。最终pH7.0±0.1。A2 磷酸盐缓冲稀释液 贮存液: 磷酸二氢钾(KH2PO4) 34.0g 蒸馏水 500mL 用大约175 mL的1mol/L氢氧化钠溶液调节pH至7.2,用蒸馏水稀释至1000 mL后贮存于冰箱。 稀释液:用蒸馏水稀释1.25mL贮存液至1000mL,分装于合适容器,121℃高压灭菌15min。附加说明: 本标准由中华人民共和国国家进出口商品检验局提出。 本标准由中华人民共和国河南进出口商品检验局、湖南进出口商品检验局负责起草 本标准主要起草人李志培、邓明义。 本标准主要参考美国食品和药物管理局(FDA)《细菌学分析手册》第6版第4章(1984年)。 中华人民共和国国家进出口商品检验局1992-12-28批准 1993-05-01实施
之前论坛组织网络讲堂起名字的活动怎么不声不响的没了消息?都参与了付出了却突然凭空消失了?有个说法么?
[align=center]我对裸辞的看法之-为什么会出现裸辞?[/align][color=#333333]照例科普:[/color][color=#333333]裸辞,指的是还没找好下家就辞职。[/color][color=#333333]本人裸辞过,也见过周围的人裸辞过,也见过来面试的人谈过裸辞的经历,也见过“被裸辞”的人。[/color][color=#333333]本身,我是对裸辞持反对意见的,这个下一篇再说。[/color][color=#333333]先讲一下我的裸辞经历,可能不是有代表性,我是未毕业前去参加工作(不是实习,拿着高中文凭去的,有正式合同),[/color][color=#333333]然后做了大半年,学校通知我两个月后参加毕业论文答辩,我还没做,于是提出离职,交接完工作后当月工资都没拿就走了。[/color][color=#333333]然后说一下有代表性的,为什么会出现裸辞这一现象,而且越来越普遍?[/color][color=#333333]大致分两种吧,大城市、小城市。[/color][color=#333333]大城市的裸辞原因是什么呢?最主要的原因是工作压力大,工作缺乏幸福感。[/color][color=#333333]像我在[/color][color=#333333]*[/color][color=#333333]京一个月因为下面的人犯错而被连带罚款每个月都超过[/color][color=#333333]2000,有些实习生进入公司不到一个月就被罚了两个月工资,[/color][color=#333333]做检测每天小心翼翼,谨慎又谨慎,因为有些仪器要小心伺候,有些样品比较贵重送来少之又少,必须一次测成功。[/color][color=#333333]有些样品着急出结果,仪器又恰巧坏掉,在规定时间出不了结果被投诉。[/color][color=#333333]还有就是大城市因为工作、生活节奏非常快(除了成都),我在上海待了两年,公司年会一张桌子都是闷头大吃,一个聊天的都没有。[/color][color=#333333]节奏快,老员工都不想理新进的员工,因为他们还有自己的事情要做,带过新人的都知道,除非自己能力比较强,工作游刃有余,[/color][color=#333333]要不然自己手上这么多活要做,还带一个拖油瓶,烦不烦。[/color][color=#333333]再加上有些新人都是刚进入职场,可以说是什么都不懂.(我在这有点歧视职场新人,但这基本是事实。)[/color][color=#333333]老员工想我都说了这么多遍,怎么他就不懂呢?新员工很委屈,你说的都是啥啊?[/color][color=#333333]一天挨三次批,当着很多人的面,别说一个女生,就一个男人都受不了。[/color][color=#333333]我和一个当天挨批当天提出离职的员工谈过话,不是正式场合,两个人几瓶啤酒,麻辣烫摊前聊了很久,[/color][color=#333333]他把他受过的怨气一条一条的跟我掰扯,都不是什么大事,都是职场小委屈。委屈多了,幸福感就缺失了。[/color][color=#333333]小城市大多数是什么原因呢?[/color][color=#333333]小城市机会小,可能你得到的工作机会并不是自己想要的,天天都做自己厌烦的工作,当一天和尚撞一天钟。[/color][color=#333333]我认识的一个酒厂的检测员,之前应聘的是白酒检测员,后来休产假的检测员回来了,[/color][color=#333333]给他调到品酒检测员,喝到胃痛又要被调到生产线做质检员。[/color][color=#333333]调他的第一天他就提出离职,他说[/color][color=#333333]实在是太烦了,与其待在这里受罪,不如潇洒告别。[/color][color=#333333]还有就是小城市的晋升大多并不是靠能力的,有可能部门领导走了,你带领团队干的正出色,老板的小侄子毕业了。[/color][color=#333333]这种不公正不公平的环境下,可能检测员不会去注重自己能力的提升,而是转战酒桌,巴结上司。有些成功了,晋升高层。[/color][color=#333333]成功者你可以鄙视他的成功道路,但你不能鄙视他的成功。[/color][color=#333333]有些看不惯,但周围又都是这种声音。总有一天会忍不住,[/color][color=#333333]冰冻三尺非一日之寒,裸辞并不是突然而来,它是叠加的负面情绪。[/color][color=#333333]因为薪资也好,因为压力也罢,因为厌倦、疲惫也无所谓,就像不断淤积的乙炔气碰见不起眼的小火星,一下就爆炸了。[/color][color=#333333][/color]
防有机流动相挥散的螺丝扣瓶和瓶塞目前的技术那种的比较好?王望老师不吝赐教
最近在淘宝上看到有这款螺口蓝盖的三角瓶,想在做菌落总数的实验中,能不能用它替代掉我们经常用的普通三角瓶加硅胶塞加牛皮纸的装营养琼脂的,如果可以,应该省事很多,各位觉得可以吗?就是下面这个图片的东西[img]http://ng1.17img.cn/bbsfiles/images/2017/08/201708241106_01_2795804_3.jpeg[/img]
9mm螺纹口样品瓶和11mm钳口瓶能通用吗?能通用于GC或者GC-MS吗?
Vip用户 liangpingmei039 在 网络讲堂版 被 禁止发帖 7 天,被封原因:广告。系统将会在 2012-8-4 自动解封,如有什么意见,请在投诉建议版投诉,特此通告!! --------仪器论坛管理员
从网络讲坛上下载的视屏,不能播放,方件类型是flv,需要下载什么样的播放器?
请问GC顶空进样瓶中有钳口和螺纹的,这两个规格有区别吗?如果没有区别,为什么会有两种不同规格的接口呢?
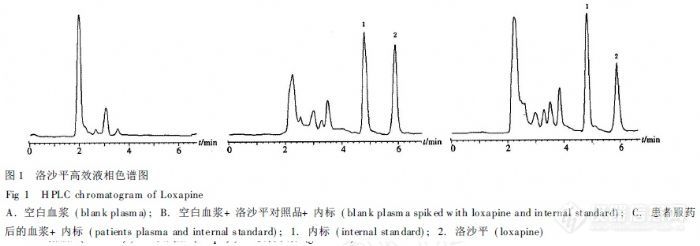
作者:赵敖; 黄伟侨; 陈清霞; 刘伟忠;(广东顺德伍仲佩医院检验科; 中山大学附属第一医院药学部; 中山大学附属第二医院药学部; 广州市脑科医院国家药品临床研究基地;)摘要:目的建立测定人血浆中洛沙平浓度的反相高效液相色谱法。方法以Diamonsil C18反相柱(150 mm×4.6 mm,5μm)为色谱柱,流动相为0.03 mol.L-1磷酸二氢钾(调pH6.4)-乙腈=83∶17;流速:1.0 mL.min-1;柱温:40℃;检测波长:256 nm。以乙酸乙酯为提取剂。结果洛沙平的高、中、低(1 000.0、400.0、10.0 ng.mL-1)3个浓度平均回收率分别为99.75%、98.94%、101.93%,日内、日间RSD均7%(n=5);分析方法的最低检测限为3.0 ng.mL-1;线性范围为10.0~1 000.0 ng.mL-1。曲线方程:Y=83.52X-3.65,r=0.999 5(n=10)。结论该方法灵敏、准确、简单、快速,可用于临床血药浓度监测和药动学研究。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208061110_381766_1606903_3.jpg
1. 使用瓶阀的材料不与瓶内盛有的气体发生化学放应,也不影响气体的质量。要根据气体的性质选用合适材质的瓶阀。(对强腐蚀性或有毒气体如H2S、HCl、NO2,需要使用国外进口不锈钢瓶阀以保证使用及储存的安全)。2. 瓶阀出气口的结构,能有效地防止气体错装,错用。可燃性气体的出口螺纹为左旋反牙,非可燃性气体的出口螺纹为右旋正牙。3. 氧气或强氧化性气体的瓶阀材料,必须选用无油脂的阻燃材料;与其接触的工具和相连的设备严禁带有油脂。4. 与瓶阀相连接的设备螺纹结构,必须与瓶阀出气口的结构相吻合。5. 瓶阀严禁使用硬质工具敲打、撞击。6. 贮存和运输工程中,必须配戴好瓶帽,以防倾倒、撞击损伤瓶阀。7. 开启瓶阀使用前,必须先确定与其相连的设备各接口的紧固情况,设备的良好状态。8. 注意缓慢开启瓶阀,往逆时针方向打开瓶阀,顺时针方向关闭瓶阀;通常先旋尽瓶阀,然后返回2/3打开状态。9. 关闭瓶阀停气时,不得过于用力拧紧瓶阀,轻轻关至瓶阀不出气即可,否则会损坏瓶阀的内部结构。10. 强腐蚀性气体气瓶用完后,必须要关紧瓶阀,以防外界空气倒入,腐蚀瓶阀。11. 开启瓶阀时,瓶阀的出气口不准对着人;同时操作者必须站在瓶阀的侧面,不能站在正面和后面。12. 瓶阀出现异常,应立即停止用气;并退回供应厂商处理。
芬兰研究人员最近开发出一款多点触控大型显示屏显微镜,该技术将显微镜和大型多点触控屏幕整合在一起,便于科研和教学等。这一新型显微镜由多点触控显示屏生产商MultiTouch公司和芬兰赫尔辛基大学等机构研究人员共同开发。赫尔辛基大学发布的新闻公报说,这项新技术将显微镜和一个46英寸多点触控显示屏通过网络连接在一起。这个大型显示屏能把用显微镜扫描的样本放大1000倍,“细胞甚至亚细胞都能看得一清二楚”。
如题:Dikma 2 mL螺纹广口瓶特点?正确答案:* 大开口,为自动进样器提供更多方便* 组装好的瓶盖和垫,方便直接使用* 带书写处, 方便铅笔等标记(可选)* 适用Agilent,Waters,Varian 和岛津等各种型号自动进样器* 瓶颈尺寸精确,保证自动进样器抓取无误* 严格的品质保证,每批产品尺寸完全一致* 平底保证与内衬管相配获得3钻石币的是:dahua1981(注册ID:dahua1981)获得2钻石币的是:rosmarinic(注册ID:v2770543)获得1钻石币的是:20071940xu(注册ID:20071940xu)
现急需20个进口棕色15mL螺口样品瓶,配备聚四氟乙烯盖子和垫子。有刻度。最好在西安,有现货。
我都不知道该怎么说好,我们局长不知道从哪弄了个什么项目,是关于上游水库的,让我们给分析,昨天晚上送来三个,是临时用车里的矿泉水瓶子采的样,本来说没带无菌瓶就不分析总大肠菌群和菌落总数了,可是今天早上又变卦了,又要分析这两荐,我和科长跟他争辩,不用无菌瓶采数值做出来也不准,局长告诉我们,不管那些,只要做出数就行。我当时感叹了一句:[color=#827e7f][size=5]这是上帝派来整我的啊[/size][/color]。[img]http://simg.instrument.com.cn/bbs/images/brow/em09501.gif[/img]没办法,我又现烘的管子,现配的试剂,终于在下午14:30分析完毕。这水样是前一天采的,放在保鲜柜里了,然后第二天下午分析总大肠菌群和菌落总数,你们说这数能准吗?
一、菌落总数介绍: 菌落是指细菌在固体培养基上生长繁殖而形成的能被肉眼识别的生长物,它是由数以万计相同的细菌集合而成。当样品被稀释到一定程度,与培养基混合,在一定培养条件下,每个能够生长繁殖的细菌细胞都可以在平板上形成一个可见的菌落。 菌落总数就是指在一定条件下(如需氧情况、营养条件、pH、培养温度和时间等)每克(每毫升)检样所生长出来的细菌菌落总数。按国家标准方法规定,即在需氧情况下,37℃培养48h,能在普通营养琼脂平板上生长的细菌菌落总数,所以厌氧或微需氧菌、有特殊营养要求的以及非嗜中温的细菌,由于现有条件不能满足其生理需求,故难以繁殖生长。因此菌落总数并不表示实际中的所有细菌总数,菌落总数并不能区分其中细菌的种类,所以有时被称为杂菌数,需氧菌数等。 菌落总数测定是用来判定食品被细菌污染的程度及卫生质量,它反映食品在生产过程中是否符合卫生要求,以便对被检样品做出适当的卫生学评价。菌落总数的多少在一定程度上标志着食品卫生质量的优劣。二、检验方法 菌落总数的测定,一般将被检样品制成几个不同的10倍递增稀释液,然后从每个稀释液中分别取出1mL置于灭菌平皿中与营养琼脂培养基混合,在一定温度下,培养一定时间后(一般为48小时),记录每个平皿中形成的菌落数量,依据稀释倍数,计算出每克(或每ml)原始样品中所含细菌菌落总数。 基本操作一般包括:样品的稀释--倾注平皿--培养48小时--计数报告。 国内外菌落总数测定方法基本一致,从检样处理、稀释、倾注平皿到计数报告无何明显不同,只是在某些具体要求方面稍有差别,如有的国家在样品稀释和倾注培养进,对吸管内液体的流速,稀释液的振荡幅度、时间和次数以及放置时间等均作了比较具体的规定。 检验方法参见: GB4789.2-94 《中华人民共和国国家标准 食品卫生微生物学检验 菌落总数测定》 SN0168-92 《中华人民共和国进出口商品检验行业标准 出口食品菌落计数》三、说明(一)样品的处理和稀释: 1.操作方法:以无菌操作取检样25g(或25ml),放于225mL灭菌生理盐水或其他稀释液的灭菌玻璃瓶内(瓶内预置适当数量的玻璃珠)或灭菌乳钵内,经充分振要或研磨制成1:10的均匀稀释液。 固体检样在加入稀释液后,最好置灭菌均质器中以8000~10000r/min的速度处理1min,制成1:10的均匀稀释液。 用1ml灭菌吸管吸取1:10稀释液1ml,沿管壁徐徐注入含有9ml灭菌生理盐水或其他稀释液的试管内,振摇试管混合均匀,制成1:100的稀释液。 另取1ml灭菌吸管,按上项操作顺序,制10倍递增稀释液,如此每递增稀释一次即换用1支1ml灭菌吸管。 2.无菌操作:操作中必须有“无菌操作”的概念,所用玻璃器皿必须是完全灭菌的,不得残留有细菌或抑菌物质。所用剪刀、镊子等器具也必须进行消毒处理。样品如果有包装,应用75%乙醇在包装开口处擦拭后取样。 操作应当在超净工作台或经过消毒处理的无菌室进行。琼脂平板在工作台暴露15分钟,每个平板不得超过15个菌落。 3.采样的代表性:如系固体样品,取样时不应集中一点,宜多采几个部位。固体样品必须经过均质或研磨,液体样品须经过振摇,以获得均匀稀释液。 4.样品稀释误差:为减少样品稀释误差,在连续递次稀释时,每一稀释液应充分振摇,使其均匀,同时每一稀释度应更换一支吸管。 在进行连续稀释时,应将吸管内液体沿管壁流入,勿使吸管尖端伸入稀释液内,以免吸管外部粘附的检液溶于其内。 为减少稀释误差,SN标准采用取10mL稀释液,注入90mL缓冲液中。 5.稀释液:样品稀释液主要是灭菌生理盐水,有的采用磷酸盐缓冲液(或0.1%蛋白胨水),后者对食品已受损伤的细菌细胞有一定的保护作用。如对含盐量较高的食品(如酱油)进行稀释,可以采用灭菌蒸馏水。(二)倾注培养 1.操作方法:根据标准要求或对污染情况的估计,选择2~3个适宜稀释度,分别在制10倍递增稀释的同时,以吸取该稀释度的吸管移取1ml稀释液于灭菌平皿中,每个稀释度做两个平皿。 将凉至46℃营养琼脂培养基注入平皿约15ml,并转动平皿,混合均匀。同时将营养琼脂培养基倾入加有1ml稀释液(不含样品)的灭菌平皿内作空白对照。 待琼脂凝固后,翻转平板,置36±1℃温箱内培养48±2h,取出计算平板内菌落数目,乘以稀释倍数,即得每克(每毫升)样品所含菌落总数。 2.倾注用培养基应在46℃水浴内保温,温度过高会影响细菌生长,过低琼脂易于凝因而不能与菌液充分混匀。如无水浴,应以皮肤感受较热而不烫为宜。 倾注培养基的量规定不一,从12~20ml不等,一般以15ml较为适宜,平板过厚可影响观察,太薄又易于干裂。倾注时,培基底部如有沉淀物,应将底部弃去,以免与菌落混淆而影响计数观察。 3.为使菌落能在平板上均匀分布,检液加入平皿后,应尽快倾注培养基并旋转混匀,可正反两个方向旋转,检样从开始稀释到倾注最后一个平皿所用时间不宜超过[