浅谈麦氏重排在质谱解析中的应用1. 前言 麦氏重排是Mclatterty对质谱分析中离子的重排反应提出的经验规则。麦氏重排(Mclatterty Rearrangement)是有机质谱裂解反应过程中十分重要的一种反应类型。是指具有不饱和官能团C=X(X为O、S、N、C等)及其γ-H原子结构的化合物,γ-H原子可以通过六元环空间排列的过渡态,向缺电子(C=X+)的部位转移,发生γ-H的断裂,同时伴随C=X的β键断裂(属于均裂),这种断裂称为McLafferty重排,简称麦氏重排。反应通式:http://ng1.17img.cn/bbsfiles/images/2012/11/201211211624_406040_2359621_3.bmp其中 X=O,NR2,CR2 Y=R,OR,NR2 Z=CR2,O 由于偶电子离子不存在游离基中心,所以只有奇电子离子才发生游离基诱导的重排反应。由麦氏重排产生的奇电子离子,对质谱的解析及化合物的研究有很重要的意义。1. 麦氏重排在质谱解析中的应用(1)麦氏重排对同分异构体的判别 同分异构体的识别可根据麦氏重排进行确认。如,3 -甲基- 2-丁酮2-戊酮,见图1。这两种化合物的质谱图十分相似,由于3-甲基- 2-丁酮没有γH存在,不符合麦氏重排发生的条件,故其不能发生麦氏重排;而 2-戊酮含有γ-H,符合麦氏重排发生的条件,因此它可以通过麦氏重排产生M/Z=58的奇电子离子。所以它们能根据有无较弱的M/Z=58碎片离子被区分开。http://ng1.17img.cn/bbsfiles/images/2012/11/201211211627_406041_2359621_3.bmp图12-戊酮通过麦氏重排形成的M/Z=58碎片离子的途径http://ng1.17img.cn/bbsfiles/images/2012/11/201211211628_406042_2359621_3.bmp(2)麦氏重排所形成的基峰离子 麦氏重排解释异戊巴比妥质谱图(图2)基峰,异戊巴比妥通过以下反应式可产生高丰度的碎片离子,先通过γ-H重排及随后的α断裂产生的http://ng1.17img.cn/bbsfiles/images/2012/11/201211211629_406043_2359621_3.bmp离子(M/Z=156),丰度为100%。http://ng1.17img.cn/bbsfiles/images/2012/11/201211211631_406045_2359621_3.bmp图2http://ng1.17img.cn/bbsfiles/images/2012/11/201211211634_406048_2359621_3.bmp
公司计划了很久要添置GCMS,不想呆等,在没回来之前我想先学习下相关知识。今天看到重排反应这块,于是产生了疑问,这个rH重排一点是r位上C的H马?我打个比方,像二丙基硫醚,H重排发生在与S相连的第二个C上的H!这个位置是r位?r位不是与官能团相连的第三个C位吗?我哪里理解错了,望各位老师不吝赐教,谢谢!
求助关于四甲基频哪醇重排副反应的文献!
求助关于四甲基频哪醇重排副反应的文献!
求助关于四甲基频哪醇重排副反应的文献!
求助关于四甲基频哪醇重排副反应的文献!
求助关于四甲基频哪醇重排副反应的文献!
求助关于四甲基频哪醇重排副反应的文献!
求助关于四甲基频哪醇重排副反应的文献!
求助关于四甲基频哪醇重排副反应的文献!
求助关于四甲基频哪醇重排副反应的文献!
求助关于四甲基频哪醇重排副反应的文献!
分析多组分时,只改变流动相的体积分数而不改变其组成,一般只会改变组分的保留时间,而不会发生峰位重排。而下列情况有可能发生峰位重排:1、流动相换了强溶剂;2、pH值改变;3、柱填料的改变;4、柱温改变;5、流动相组成改变(如加了离子对试剂,等)
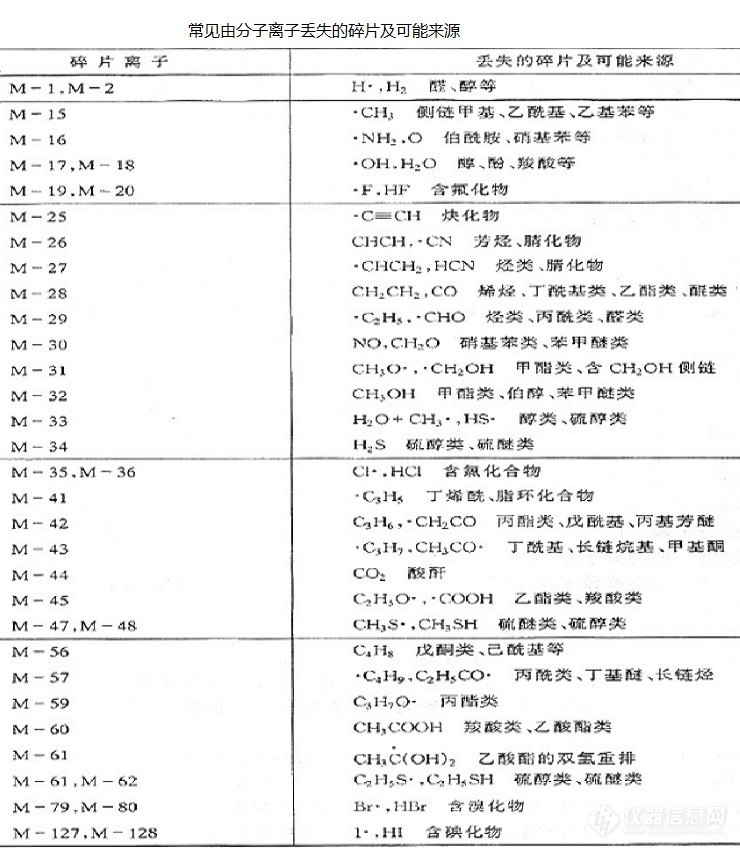
质谱, 即质量的谱图, 物质的分子在高真空下, 经物理作用或化学反应等途径形成带电粒子, 某些带电粒了可进一步断裂。 每一离子的质量与所带电荷的比称为质荷比(m/z,曾用 m/e). 不同质荷比的离子经质量分离器一一分离后, 由检测器测定每一离子的质荷比及相 对强度, 由此得出的谱图称为质谱。[b]一、质谱中的离子种类及碎片离子[/b][align=left][b]1、分子离子[/b][/align][align=left]分子被电子束轰击失去一个电子形成的离子称为分子离子。 分子离子用 M[sup]+[/sup]表示。 分子离子是一个游离基离子。在质谱图中与分子离子相对应的峰为分子离子峰。分子离子峰的质荷比就是化合物的相对分子质量, 所以,用质谱法可测分子量。[/align][align=left][b]2、同位素离子[/b][/align][align=left]含有同位素的离子称为同位素离子。 在质谱图上, 与同位素离子相对应的峰称为同位素离子峰。[/align][align=left][b]3、碎片离子[/b][/align][align=left]分子离子在电离室中进一步发生键断裂生 成的离子称为碎片离子。[/align][align=left][b]4、重排离子[/b][/align][align=left]经重排裂解产生的离子称为重排离子。 其结构并非原来分子的结构单元。 在重排反应中, 化学键的断裂和生成同时发生, 并丢失中性分子或碎片。[/align][align=left][b]5、奇电子离子与偶电子离子[/b][/align][align=left]具有未配对电子的离子为奇电子离子。这样的离子同时也是自由基,具有较高的反应活性。 无未配对电子的离子为偶电子离子。[/align][align=left][b]6、多电荷离子[/b][/align][align=left]分子中带有不止一个电荷的离子称为多电荷离子。 当离子带有多电荷离子时, 其质核比下降, 因此可以利用常规的四极质量分析器来检测大分子量化合物。[/align][align=left][b]7、亚稳离子[/b][/align][align=left]从离子源出口到检测器之间产生的离子。 即在飞行过程中发生裂解的母离子。 由于母离子中途已经裂解生成某种离子和中性碎片, 记录器中只能记录这种离子, 也称这种离子为亚稳离子, 由它形成的质谱峰为亚稳峰。[/align][align=left][b]8、准分子离子[/b][/align][align=left]比分子量多或少 1 质量单位的离子称为准分子离子,如:(M+H)+, (M-H)+。其不含未配对电子, 结构上比较稳定。[/align][b]二、分子离子峰[/b][align=left][b]1、分子离子峰强度[/b][/align][align=left]分子离子是质谱图中最有价值的信息,它不但是测定化合物分子量的依据,而且可以推测化合物的分子式, 用高分辨质谱可以直接测定化合物的分子式。 一般来讲, 从分子中失去的电子应该是分子中束缚最弱的电子, 如双键或叁键的π电子, 杂原子上的非 键电子。分子离子的丰度主要取决于其稳定性和分子电离所需要的能量。 易失去电子的化合物,如环状化合物,双键化合物等,其分子离子稳定,分子离子峰较强 而长碳链烷烃,支链烷烃等正与此相反。 各类化合物分子离子稳定性次序大致为:芳香环 (包括芳香杂环) 共轭烯 烯 脂环 硫醚,硫酮 酰胺 酮 醛 直链烷烃 醚 酯 胺 羧酸腈伯醇仲醇叔醇高度支链烃。芳环 (包括芳杂环) 、 脂环化合物、 硫醚、 硫酮、 共轭烯分子离子峰比较明显,直链酮、 酯、 酸、 醛、 酰胺、 卤化物等通常显示分子离子峰,脂肪族醇、 胺、 亚硝酸酯、 硝酸酯、 硝基化合物、 腈类及多支链化合物容易裂解, 分子离子峰通常很弱或不出现。分子离子峰不出现或丰度极低难以确认, 可根据不同情况改变实验条件予以验证。[/align][align=left](1)降低轰击电子的能量[/align][align=left]将常用的70eV 改变15eV 以减少形成的分 子离子继续断裂的几率, 降低了碎片离子的丰度, 使分子离子峰的相对丰度增加, 从而可能辨认出分子离子。[/align][align=left](2)用CI, FI, FD等软电离方法[/align][align=left] 降低轰击电子能量的结果会使仪器的灵敏度 下降, 虽然分子离 子峰的丰度有所提高, 但离子的绝对强度降低,一些由于热不稳定和低挥发性等原因而不出现分子离子峰的化合物, 用这种办法不会得到预期的效果, 这时可采取各种软电离的办法, 虽然碎片离子大量减少, 但可以突出分子离子峰。[/align][align=left](3)降低样品的气化温度[/align][align=left]气化温度的降低可以减少分子离子进一步断裂的可能性, 分子离子峰的相对丰度增加。 如三十烷烃在340℃时气化, 不出现分子离子峰,改变70℃气化时分子离子峰的丰度接近基峰。(4)制备衍生物某些化合物不易挥发或热稳定性差, 可以衍生化处理。 例如, 可将某有机酸制备成相应的酯, 酯容易气化, 而且易得到分子离子峰, 由此来推断有机酸的分子量。[b]2、分子离子峰的识别[/b] 解析时一般把谱图中最高质荷比的离子假设为分子离子,后用分子离子的判别标准一一对比, 若被检查离子不符其中任何一条标准,则它一定不是分子离子 若被检查离子符合所有条件, 则它有可能是分子离子。分子离子的判别可以参考如下标准:(1)分子离子必须是奇电子离子。 由于有机分子都是偶电子,所有失去一个电子生成的分子离子必是奇电子离子。(2)是否符合氮规则 (Nitrogen Rule) 。 有机化合物的分子量是偶数或奇数与所含有的氮原子的数目有关。凡不含氮原子或含偶数个氮原子的化合物, 其分子量必为偶数 含奇数个氮原子的化合物, 其分子量必为奇数, 这就是所谓的氮规则。(3)合理的中性碎片的丢失。这些中性碎片可能是小分子或者自由基基团。 这些中性碎片有着特殊的质量数, m/z最高值与邻近的碎片离子之间应有一个合理的质量差。例如: M+丢失一个质子H, CH[sub]3[/sub], H[sub]2[/sub]O,C[sub]2[/sub]H[sub]4[/sub]等是合理的。如果这个质量差落在4~14和21~25之间就是不合理的, 也即如果在M-4到M-13的范围内存在峰, 则说明原所假定的分子离子峰不是分子离子峰。 [/align][align=center][img=,690,792]https://ng1.17img.cn/bbsfiles/images/2018/12/201812121528306963_3736_3299836_3.jpg!w690x792.jpg[/img][/align][align=left] [/align][b]三、碎片离子[/b]碎片离子的质荷比及其丰度在质谱数据中占很大比例。碎片离子的相对丰度与分子结构有密切关系,高丰度的碎片峰代表分子中易于裂解的部分,如果有几个主要碎片峰,并且代表着分子的不同部分, 则由这些碎片峰就可以粗略地把分子骨架拼凑起来。 质谱解析的大量工作就是分析碎片离子的形成过程。[b]1、α断裂[/b]分子失去电子,形成游离基离子,它的电子有强烈的成对倾向,电子转移与邻近原子形成一个新键,同时邻近原子的α键断裂。因此,这种断裂通常称为“α”断裂反应。(1)饱和杂原子:杂原子的孤对电子电离能较低,很容易去失,形成游离基离子,进而发生α断裂,如[align=center][img=,381,55]https://ng1.17img.cn/bbsfiles/images/2018/12/201812121529194563_5528_3299836_3.png!w381x55.jpg[/img] [/align][align=left](2)不饱和杂原子:例如羰基化合物的α断裂过程如下[/align][align=center][img=,293,85]https://ng1.17img.cn/bbsfiles/images/2018/12/201812121529358013_9201_3299836_3.png!w293x85.jpg[/img] [/align][align=left](3)烯烃类的烯丙位裂解:[/align][align=center][img=,451,108]https://ng1.17img.cn/bbsfiles/images/2018/12/201812121549404453_861_3299836_3.png!w451x108.jpg[/img][/align][align=left]上述反应的进行与游离基中心给电子倾向有密切的关系。氮原子给电子能力很强,α断裂在脂肪族胺中占主导地位,其次是氧族元素,由给电子能力的差别造成的α断裂反应的难易程度按下列顺序排列:NS、O、π,R﹒Cl、BrH。当一个化合物有几个α键时,最容易去失的是最大的烷基游离基。[/align][align=center][img=,550,161]https://ng1.17img.cn/bbsfiles/images/2018/12/201812121549558533_5813_3299836_3.png!w550x161.jpg[/img] [/align][b]2、i断裂(诱导断裂)[/b]诱导断裂是由正电荷诱导、 吸引一对电子而发生的断裂, 其结果是正电荷的转移。 诱导断裂常用i来表示。一般情况下, 电负性强的元素诱导力也强。 在有些情况下, 诱导断裂和α断裂同时存在,。由于i断裂需要电荷转移, 因此,i断裂不如α断裂容易进行。 表现在质谱中, 相应α断裂的离子峰强,i断裂产生的离子峰较弱。例如乙醚,i断裂和α断裂同时存在, α断裂的几率大于i断裂。但由于α断裂生成的m/z 59还有进一步的断裂, 因此在乙醚的质谱中, m/z59并不比m/z 29强。[align=center][img=,525,129]https://ng1.17img.cn/bbsfiles/images/2018/12/201812121550245863_7057_3299836_3.png!w525x129.jpg[/img] [/align][b]3、σ断裂[/b]如果化合物分子中具有σ键, 如烃类化合物, 则会发生σ键断裂。σ键断裂需要的能量大, 当化合物中没有π电子和n电子时, σ键的断裂才可能成为主要的断裂方式。 断裂后形成的产物越稳定, 这样的断裂就越容易进行,阳碳离子的稳定性顺序为叔仲伯。因此, 碳氢化合物最容易在分支处发生键的断裂。 并且, 失去最大烷基的断裂最容易进行。[align=center][img=,632,122]https://ng1.17img.cn/bbsfiles/images/2018/12/201812121550559113_5880_3299836_3.png!w632x122.jpg[/img] [/align][b]4、重排开裂[/b]重排开裂时涉及到两个键的断裂,脱去一个中性分子,同时发生H重排。 重排的结果产生了在原化合物中不存在的结构单元的离子。(1)麦氏重排(Mclafferty rearrangement)分子离子或碎片离子结构中有 双键, 且在γ位上有H原子的正离子都能发生麦氏重排。 在开裂中, γ位上的H通过六元环过渡态的迁移到电离的双键碳或杂原子上, 同时烯丙键断裂, 生成中性分子和碎片离子。[align=center][img=,685,132]https://ng1.17img.cn/bbsfiles/images/2018/12/201812121551313893_5279_3299836_3.png!w685x132.jpg[/img][/align][align=center] [/align][align=left]醛、 酮、 羧酸、 酯、 酰胺、 碳酸酯、 磷酸酯、 肟、腙、 烯、 炔以及烷基苯等的含有γ-H的有机化合物很容易发生麦氏重排。[/align][align=left](2)逆迪尔斯一阿尔德重排(retro Diels-Alder fragmentation,RDA)[/align][align=left]对具有环内双键结构的化合物能发生RDA开裂, 一般生成一个带正电荷的共轭二烯自由基和一个中性分子。[/align][align=left](3)脱去小分子化合物的重排[/align][align=left]在一些醇类、 硫醇类、 卤代烃等有机化合物分子的质谱中经常出现脱去水、 硫化氢、 卤化氢等小分子化合物而生成的碎片离子。醇非常容易脱去水分子, 所以醇类化合物的分子离子峰相对丰度很小, 甚至不出现分子离子峰。[/align][align=left](4)复杂开裂复杂开裂是指在有机化合物的质谱中, 经常出现离子中两个或两个以上化学键连续发生断裂生成碎片的过程。除了重排反应以外, 环状化合物的质谱碎裂也是如此。复杂断裂一般是指环状化合物发生的多个键断裂, 有时涉及一个氢原子的转移。[/align][align=left] [/align][align=center][img=,592,175]https://ng1.17img.cn/bbsfiles/images/2018/12/201812121552179653_6977_3299836_3.png!w592x175.jpg[/img][/align][align=center] [/align][align=left](5)骨架重排[/align][align=left]骨架重排是指在有机化合物裂解过程中, 部分基团如甲基、 芳香基以及含O、N、S等的基团发生迁移,生成一些小的中性碎片、自由基离子等的过程。常见的中性碎片如CO、SO、SO[sub]2[/sub], S[sub]2[/sub], CH=CH等。如蒽醌发生芳基迁移, 存在下列裂解:[/align][align=center] [/align][align=center][img=,542,172]https://ng1.17img.cn/bbsfiles/images/2018/12/201812121552361343_3434_3299836_3.png!w542x172.jpg[/img][/align][align=center] [/align]
1 原子质量单位 Atomic Mass Unit 定义C原子质量的1/12为一个质量单位,简写为amu或u 。 2 毫原子质量单位 Milli Mass Unit 千分之一的原子质量单位,简写为 mmu,lmmu=1/1000u。 3 质荷比 Mass to Charge Ratio 离子的质量和所带电荷的比值,简写为m/z 。 4 质谱图 Mass Spectrum 质谱分析中以质荷比为横坐标,离子的相对强度为纵坐标所作的谱图。 5 分子离子 Molecular Ion 试样分子失去或得到一个电子而形成的离子。它在正离子场合下表示为M ·+。它的质荷 比即表明试样分子所对应的分子量数值。在分子中含不同同位素时,以天然丰度最大者作分子离子。 6 亚稳离子 Metastable Ion 是指离子在质谱仪的离子源中产生,在达到检测器前分解的离子。其表观质量记为m※。 7 母离子 Parent Ion 是指产生某一碎片的前体离子,母离子不一定是分子离子。 8 子离子 Daughter Ion 是指由母子离子裂解后形成的离子。 9 碎片离子 Fragment Ion 分子离子经过裂解后形成的离子。 10 重排离子 Rearrangement Ion 是指质谱过程中产生的与前体离子中原子排列不同的离子。
[size=6][b]苯酚[/b][/size] 苯酚[table=100%][tr][td][img=right]http://baike.baidu.com/pic/2/11849861571338684_small.jpg[/img] 【中文名称】苯酚;石炭酸【英文名称】phenol【结构或分子式】 所有C原子均以sp2杂化轨道形成σ键,O原子均以sp3杂化轨道形成σ键。 【相对分子量或原子量】94.11【密度】1.071【熔点(℃)】42~43【沸点(℃)】182【折射率】1.5425(41°C)【毒性LD50(mg/kg)】 大鼠经口530。【性状】 无色或白色晶体,有特殊气味。【溶解情况】 溶于乙醇、乙醚、氯仿、甘油、二硫化碳等。【用途】 用于制染料合成树脂、塑料、合成纤维和农药、水杨酸等。作外科消毒剂消毒能力大小的标准(石炭酸系数)。【制备或来源】 由煤焦油经分馏,由苯磺酸经碱熔。由氯苯经水解,由异丙苯经氧化重排,或由甲苯经侧链氯化和水解而制得。【其他】 加热能溶于水,有毒,具有腐蚀性,在空气中变粉红色。 [/td][/tr][/table]
质谱,即质量的谱图,物质的分子在高真空下,经物理作用或化学反应等途径形成带电粒子, 某些带电粒子可进一步断裂。 每一离子的质量与所带电荷的比称为质荷比(m/z,曾用 m/e)。不同质荷比的离子经质量分离器一一分离后,由检测器测定每一离子的质荷比及相对强度,由此得出的谱图称为质谱。 [font=&][size=14px]1、分子离子[/size][/font][font=&][size=14px]分子被电子束轰击失去一个电子形成的离子称为分子离子。分子离子用 M+表示。分子离子是一个游离基离子。在质谱图中与分子离子相对应的峰为分子离子峰。分子离子峰的质荷比就是化合物的相对分子质量, 所以,用质谱法可测分子量。[/size][/font][font=&][size=14px]2、同位素离子[/size][/font][font=&][size=14px]含有同位素的离子称为同位素离子。在质谱图上, 与同位素离子相对应的峰称为同位素离子峰。[/size][/font][font=&][size=14px]3、碎片离子[/size][/font][font=&][size=14px]分子离子在电离室中进一步发生键断裂生 成的离子称为碎片离子。[/size][/font][font=&][size=14px]4、重排离子[/size][/font][font=&][size=14px]经重排裂解产生的离子称为重排离子。其结构并非原来分子的结构单元。在重排反应中, 化学键的断裂和生成同时发生, 并丢失中性分子或碎片。[/size][/font][font=&][size=14px]5、奇电子离子与偶电子离子[/size][/font][font=&][size=14px]具有未配对电子的离子为奇电子离子。这样的离子同时也是自由基,具有较高的反应活性。无未配对电子的离子为偶电子离子。[/size][/font][font=&][size=14px]6、多电荷离子[/size][/font][font=&][size=14px]分子中带有不止一个电荷的离子称为多电荷离子。当离子带有多电荷离子时, 其质核比下降, 因此可以利用常规的四极质量分析器来检测大分子量化合物。[/size][/font][font=&][size=14px]7、亚稳离子[/size][/font][font=&][size=14px]从离子源出口到检测器之间产生的离子。即在飞行过程中发生裂解的母离子。由于母离子中途已经裂解生成某种离子和中性碎片, 记录器中只能记录这种离子, 也称这种离子为亚稳离子, 由它形成的质谱峰为亚稳峰。[/size][/font][font=&][size=14px]8、准分子离子[/size][/font][font=&][size=14px]比分子量多或少 1 质量单位的离子称为准分子离子,如:(M+H)+, (M-H)+。其不含未配对电子, 结构上比较稳定。[/size][/font] [font=&][size=14px]二、分子离子峰[/size][/font][font=&][size=14px]1、分子离子峰强度[/size][/font][font=&][size=14px]分子离子是质谱图中最有价值的信息,它不但是测定化合物分子量的依据,而且可以推测化合物的分子式, 用高分辨质谱可以直接测定化合物的分子式。 [/size][/font][font=&][size=14px]一般来讲, 从分子中失去的电子应该是分子中束缚最弱的电子, 如双键或叁键的π电子, 杂原子上的非 键电子。[/size][/font][font=&][size=14px]分子离子的丰度主要取决于其稳定性和分子电离所需要的能量。易失去电子的化合物,如环状化合物,双键化合物等,其分子离子稳定,分子离子峰较强 而长碳链烷烃,支链烷烃等正与此相反。[/size][/font][font=&][size=14px]各类化合物分子离子稳定性次序大致为:芳香环 (包括芳香杂环) 共轭烯 烯 脂环 硫醚,硫酮 酰胺 酮 醛 直链烷烃 醚 酯 胺 羧酸腈伯醇仲醇叔醇高度支链烃。[/size][/font][font=&][size=14px]芳环 (包括芳杂环) 、 脂环化合物、 硫醚、 硫酮、 共轭烯分子离子峰比较明显,直链酮、 酯、 酸、 醛、 酰胺、 卤化物等通常显示分子离子峰,脂肪族醇、胺、 亚硝酸酯、 硝酸酯、 硝基化合物、 腈类及多支链化合物容易裂解, 分子离子峰通常很弱或不出现。[/size][/font][font=&][size=14px]分子离子峰不出现或丰度极低难以确认, 可根据不同情况改变实验条件予以验证。[/size][/font][font=&][size=14px](1)降低轰击电子的能量[/size][/font][font=&][size=14px]将常用的70eV 改变15eV 以减少形成的分 子离子继续断裂的几率, 降低了碎片离子的丰度, 使分子离子峰的相对丰度增加, 从而可能辨认出分子离子。[/size][/font][font=&][size=14px](2)用CI, FI, FD等软电离方法[/size][/font][font=&][size=14px]降低轰击电子能量的结果会使仪器的灵敏度 下降, 虽然分子离 子峰的丰度有所提高, 但离子的绝对强度降低,一些由于热不稳定和低挥发性等原因而不出现分子离子峰的化合物, 用这种办法不会得到预期的效果, 这时可采取各种软电离的办法, 虽然碎片离子大量减少, 但可以突出分子离子峰。 [/size][/font][font=&][size=14px](3)降低样品的气化温度[/size][/font][font=&][size=14px]气化温度的降低可以减少分子离子进一步断裂的可能性, 分子离子峰的相对丰度增加。如三十烷烃在340℃时气化, 不出现分子离子峰,改变70℃气化时分子离子峰的丰度接近基峰。[/size][/font][font=&][size=14px](4)制备衍生物[/size][/font][font=&][size=14px]某些化合物不易挥发或热稳定性差,可以衍生化处理。例如, 可将某有机酸制备成相应的酯, 酯容易气化, 而且易得到分子离子峰, 由此来推断有机酸的分子量。[/size][/font][font=&][size=14px]2、分子离子峰的识别[/size][/font][font=&][size=14px]解析时一般把谱图中最高质荷比的离子假设为分子离子,后用分子离子的判别标准一一[/size][/font][font=&][size=14px]对比,若被检查离子不符其中任何一条标准,则它一定不是分子离子;若被检查离子符合所有条件, 则它有可能是分子离子。分子离子的判别可以参考如下标准:[/size][/font][font=&][size=14px](1)分子离子必须是奇电子离子。由于有机分子都是偶电子,所有失去一个电子生成的分子离子必是奇电子离子。[/size][/font][font=&][size=14px](2)是否符合氮规则 (Nitrogen Rule) 。有机化合物的分子量是偶数或奇数与所含有的氮原子的数目有关。凡不含氮原子或含偶数个氮原子的化合物, 其分子量必为偶数 含奇数个氮原子的化合物, 其分子量必为奇数, 这就是所谓的氮规则。[/size][/font][font=&][size=14px](3)合理的中性碎片的丢失。这些中性碎片可能是小分子或者自由基基团。这些中性碎片有着特殊的质量数, m/z最高值与邻近的碎片离子之间应有一个合理的质量差。[/size][/font][font=&][size=14px]例如: M+丢失一个质子H, CH3, H2O,C2H4等是合理的。如果这个质量差落在4~14和21~25之间就是不合理的, 也即如果在M-4到M-13的范围内存在峰, 则说明原所假定的分子离子峰不是分子离子峰。 [/size][/font][align=center] [/align][font=&][size=14px][/size][/font] [font=&][size=14px]三、碎片离子[/size][/font][font=&][size=14px]碎片离子的质荷比及其丰度在质谱数据中占很大比例。碎片离子的相对丰度与分子结构有密切关系,高丰度的碎片峰代表分子中易于裂解的部分,如果有几个主要碎片峰,并且代表着分子的不同部分, 则由这些碎片峰就可以粗略地把分子骨架拼凑起来。质谱解析的大量工作就是分析碎片离子的形成过程。[/size][/font][font=&][size=14px]1、α断裂[/size][/font][font=&][size=14px]分子失去电子,形成游离基离子,它的电子有强烈的成对倾向,电子转移与邻近原子形成一个新键,同时邻近原子的α键断裂。因此,这种断裂通常称为“α”断裂反应。[/size][/font][font=&][size=14px](1)饱和杂原子:杂原子的孤对电子电离能较低,很容易去失,形成游离基离子,进而发生α断裂,如 [img=,381,55]https://file.jgvogel.cn/134/upload/resources/image/210176.png?x-oss-process=image/resize,w_700,h_700[/img][/size][/font] [font=&][size=14px](2)不饱和杂原子:例如羰基化合物的α断裂过程如下[/size][/font][align=center][img]https://file.jgvogel.cn/134/upload/resources/image/210177.png?x-oss-process=image/resize,w_700,h_700[/img][/align][font=&][size=14px](3)烯烃类的烯丙位裂解:[/size][/font] [align=center][img]https://file.jgvogel.cn/134/upload/resources/image/210178.png?x-oss-process=image/resize,w_700,h_700[/img][/align][font=&][size=14px]上述反应的进行与游离基中心给电子倾向有密切的关系。氮原子给电子能力很强,α断裂在脂肪族胺中占主导地位,其次是氧族元素,由给电子能力的差别造成的α断裂反应的难易程度按下列顺序排列:NS、O、π,R﹒Cl、BrH。当一个化合物有几个α键时,最容易去失的是最大的烷基游离基。[/size][/font] [align=center][img]https://file.jgvogel.cn/134/upload/resources/image/210179.png?x-oss-process=image/resize,w_700,h_700[/img][/align][font=&][size=14px]2、i断裂(诱导断裂)诱导断裂是由正电荷诱导、 吸引一对电子而发生的断裂, 其结果是正电荷的转移。诱导断裂常用i来表示。一般情况下, 电负性强的元素诱导力也强。在有些情况下, 诱导断裂和α断裂同时存在,。由于i断裂需要电荷转移, 因此,i断裂不如α断裂容易进行。表现在质谱中, 相应α断裂的离子峰强,i断裂产生的离子峰较弱。例如乙醚,i断裂和α断裂同时存在, α断裂的几率大于i断裂。但由于α断裂生成的m/z 59还有进一步的断裂,因此在乙醚的质谱中, m/z59并不比m/z 29强。[/size][/font] [align=center][img]https://file.jgvogel.cn/134/upload/resources/image/210180.png?x-oss-process=image/resize,w_700,h_700[/img][/align][font=&][size=14px] 3、σ断裂如果化合物分子中具有σ键, 如烃类化合物, 则会发生σ键断裂。σ键断裂需要的能量大, 当化合物中没有π电子和n电子时, σ键的断裂才可能成为主要的断裂方式。断裂后形成的产物越稳定, 这样的断裂就越容易进行,阳碳离子的稳定性顺序为叔仲伯。因此, 碳氢化合物最容易在分支处发生键的断裂。并且, 失去最大烷基的断裂最容易进行。 [/size][/font][align=center][img]https://file.jgvogel.cn/134/upload/resources/image/210181.png?x-oss-process=image/resize,w_700,h_700[/img][/align] [font=&][size=14px]4、重排开裂[/size][/font][font=&][size=14px] [/size][/font][font=&][size=14px]重排开裂时涉及到两个键的断裂,脱去一个中性分子,同时发生H重排。重排的结果产生了在原化合物中不存在的结构单元的离子。[/size][/font][font=&][size=14px] [/size][/font][font=&][size=14px](1)麦氏重排(Mclafferty rearrangement)[/size][/font][font=&][size=14px]分子离子或碎片离子结构中有 双键, 且在γ位上有H原子的正离子都能发生麦氏重排。在开裂中, γ位上的H通过六元环过渡态的迁移到电离的双键碳或杂原子上, 同时烯丙键断裂,生成中性分子和碎片离子。[/size][/font][align=center][img]https://file.jgvogel.cn/134/upload/resources/image/210182.png?x-oss-process=image/resize,w_700,h_700[/img][/align][font=&][size=14px] [/size][/font] [font=&][size=14px]醛、 酮、 羧酸、 酯、 酰胺、 碳酸酯、 磷酸酯、 肟、腙、 烯、炔以及烷基苯等的含有γ-H的有机化合物很容易发生麦氏重排。[/size][/font][font=&][size=14px] [/size][/font][font=&][size=14px](2)逆迪尔斯一阿尔德重排(retro Diels-Alder fragmentation,RDA)[/size][/font][font=&][size=14px]对具有环内双键结构的化合物能发生RDA开裂, 一般生成一个带正电荷的共轭二烯自由基和一个中性分子。[/size][/font][font=&][size=14px] [/size][/font][font=&][size=14px](3)脱去小分子化合物的重排[/size][/font][font=&][size=14px]在一些醇类、 硫醇类、 卤代烃等有机化合物分子的质谱中经常出现脱去水、硫化氢、 卤化氢等小分子化合物而生成的碎片离子。醇非常容易脱去水分子, 所以醇类化合物的分子离子峰相对丰度很小, 甚至不出现分子离子峰。[/size][/font][font=&][size=14px](4)复杂开裂[/size][/font][font=&][size=14px]复杂开裂是指在有机化合物的质谱中,经常出现离子中两个或两个以上化学键连续发生断裂生成碎片的过程。除了重排反应以外, 环状化合物的质谱碎裂也是如此。复杂断裂一般是指环状化合物发生的多个键断裂, 有时涉及一个氢原子的转移。[/size][/font][align=center][img]https://file.jgvogel.cn/134/upload/resources/image/210183.png?x-oss-process=image/resize,w_700,h_700[/img][/align][font=&][size=14px][/size][/font] [font=&][size=14px](5)骨架重排[/size][/font][font=&][size=14px]骨架重排是指在有机化合物裂解过程中, 部分基团如甲基、 芳香基以及含O、N、S等的基团发生迁移,生成一些小的中性碎片、自由基离子等的过程。常见的中性碎片如CO、SO、SO2, S2, CH=CH等。如蒽醌发生芳基迁移, 存在下列裂解:[/size][/font][align=center][img]https://file.jgvogel.cn/134/upload/resources/image/210184.png?x-oss-process=image/resize,w_700,h_700[/img][/align]
[url=http://www.instrument.com.cn/training/training_info.asp?TRI_No=100391][b][color=#013add]在线报名[/color][/b][/url][color=#013add] [/color] [b][color=#d40a00]时间[/color][/b]2010年5月17日-21日 北京[b][color=#d40a00]主讲[/color][/b]王光辉、苏焕华等[b][color=#d40a00]大纲[/color]一、谱图解析基础知识[/b] 1、原子中电子的排布 2、奇电子离子与偶电子离子 3、氮规则 4、环加双键值 5、同位素峰 6、分子离子的识别 7、单分子反应 [b]二、离子的丰度[/b] 1、质荷比与离子丰度包含的结构信息 2、影响碎片离子丰度的基本因素 (a) 产物的稳定性 (b) 空间因素 (c) 键的不稳定性 [b]三、离子碎裂的基本类型[/b] 1 、电荷及游离基定域的概念 2 、σ 断裂,简单的键断裂 3 、α 断裂,游离基诱导键断裂 4、 i 断裂,电荷中心诱导键断裂 5、 α 断裂与 i 断裂的竞争 6、 环的开裂 7、 重排反应 (a) 游离基诱导的重排 (b) 电荷诱导的重排 8 、置换反应 (rd) 9 、消除反应 (re) [b]四、常见有机化合物的质谱特征[/b] 1、碳氢化合物 2、醇、酮、醛、酸、酯、醚3、胺类 4、酰胺类 5、腈 [b]五、由质谱图推测分子结构[/b] 1、基本方法及思路 2、实例练习 [b]六、NIST谱图库简介[/b] 注:学员可自带原始数据采集文件[url=http://www.instrument.com.cn/training/training_info.asp?TRI_No=100391][b][color=#f10b00]详细内容请查看[/color][/b][/url]
质谱技术由于具有质量分辨、信息量大、样品用量少、灵敏、快速等优点,多年来在测定有机物精确分子量、解析有机分子结构、研究有机反应机理等方面发挥着十分重要的作用。近年来,由于快原子轰击电离(FAB)、电喷雾电离(ESI)、基质辅助激光解吸/电离(MALDI)等软电离技术以及飞行时间质谱(TOF-MS)、傅里叶变换质谱(FT-MS)等新的质量分析方法的发展,以及各种色/质联用技术,如GC/MS、HPLC/MS、CE/MS,对于复杂体系的分离和分析十分有效,在医药领域如药代动力学研究和药物质量控制中发挥非常重要的作用;反应质谱RMS、串联质谱MS/MS等质谱新技术为研究药物-受体相互作用、药物光学纯度测定、生物超分子体系的弱相互作用和分子识别机理以及实现高通量药物筛选等提供了有力的工具。有机质谱的研究对象是有机[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]离子,如分子离子、碎片离子等,排除了溶剂对离子的影响,真正反应离子的化学性质。而像Gauss等计算软件正适于物质在[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]条件下的计算,而且其[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]条件下的模拟计算相当成熟。因此,使用计算软件模拟[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]化学性质具有可行性。同时,[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]离子的存在环境非常苛刻,如高真空、电磁场等。这使得现代分析仪器难以直接进行分析[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]离子结构。质谱技术主要通过离子的裂解和中性碎片的丢失来进行结构推测。分子离子的碎裂反应是有机质谱解析的基础。虽然用于有机质谱解析方法已经建立起来, 但这些方法并没有十分准确地描述分子离子的碎裂反应机理。到目前为止,质谱研究还只能属于实验科学,还需要计算化学来提高其理论水平。下面列举一些计算化学在质谱研究中的应用:1、离子碎裂反应的活化中性在电子轰击(EI)电离下,分子失去一个电子形成奇电子离子M +.。奇电子离子有两个活泼的反应中心,即电荷中心和自由基中心;偶电子离子只有电荷中心。分子离子的碎裂和产物离子的进一步碎裂主要是由这些中心引发的。对于由活性中心引发的碎裂反应,活性中性在离子中位置的确定是非常重要的。分子丢失一个电子之后,电荷和孤单电子一般在同一个原子上。而Radom等在对自由基的异构化进行理论计算研究时发现,反应可以被1,2-迁移基团X的质子化所促进。后来他们对甲醇的分子离子CH4O+.进行计算时发现CH4O+.不稳定[,最稳定的是.CH2OH2+.这样的结构,并随即被实验所证实。这种电荷于自由基中心分离的离子被称为荷基异位(diatonic)离子,其发现是近年来有机质谱的重要成就之一。在其它软电离源技术电离下,如化学电离(CI)、快原子轰击电离(FAB)、电喷雾电离(ESI)、基质辅助激光解吸/电离(MALDI)等,分子失去或者蒂合一个离子,形成准分子离子,如[M+H]+, [M+Na]+, [M-H]-, [M+Cl]-等。这些离子一般只有一个反应活泼中心,即电荷中心。Wesdemiotis等报道了使用快原子轰击产生一种新型的自由基离子,即低聚乙烯醚(R.)H(OCH2CH2)nO. (n=1,2), H(OCH2CH2)nOCH2. (n=1,2)与碱金属离子的络合物。理论计算表明,该离子也是一种荷基异位的离子,自由基中心在低聚乙烯醚的端基,电荷中心在碱金属上。该离子容易发生裂解产生含CH2=O的中型碎片-离子的复合物,以及氢迁移重排。2、分子离子以及碎片离子的空间结构化合物在电离后,其结构可能会发生变化。通过计算软件对离子空间结构的的模拟,可解析其裂解途径。在许多离子的碎裂反应过程中,键断裂后初生的中性碎片荷离子碎片在分离前,通过静电作用结合在一起而形成,被称为离子-中性复合物(ion-neutral complex)。Mcadoo等的理论计算表明,在丙烷分子离子的碎裂反应中,甲基自由基与乙基自由基形成一个离子-中性复合物[C2H5+...CH3.]。这两个成员简单分离则生成C2H5+和CH3.;若它们之间先发生氢原子(H.)转移再分离则生成C2H4+。和CH4。复合物的能量比分子离子失去CH4的阈值低5.3 kcal/mol,即其生成热比产物的生成热之和要低。在软电离源中形成的离子,经常有金属络合物或分子间氢键的形式存在分子簇离子。Cundari等[17]以FT-MS作为反应质谱来研究吡啶取代trans- Rh(PPh3)2CO(4-picoline) 配合物上的甲基吡啶时发生丢失CO。使用泛密函数计算表明,Rh-4-picoline, Rh-pyridine和Rh-CO的配位键能非常类似,而Rh的五配位的结构处在能量高位,因此丢失甲基吡啶和丢失CO是两条竞争反应。Marynick等使用泛密函数方法考察了MALDI基质与三肽VPL的簇状相互作用模型,研究其电离过程中质子从基质到分析物迁移的机理,发现质子有时在中性簇中迁移,而在阳离子簇中的迁移是自发的。3、质子迁移和重排反应:离子的自由基中心很容易引发附近质子的迁移反应,形成更稳定的重排结构。对于含有γ-氢的羰基化合物,如醛、酮、羧酸及其衍生物,McLafferty重排是其分离离子裂解过程中一个非常重要的反应。然而,自McLafferty首次报道这个反应以来,有关其机理是协同过程还是分步进行的问题长期争论不休。分子轨道理论计算结果表明,3-庚酮的McLafferty重排反应先经过1,5-氢迁移使分子离子异构化成荷基异位离子,后者的能量比前者约低8kcal/mol。苯丁酮红外多光子活化解离实验也证实上述机理。电荷中心也能引发附近质子的迁移反应,茶儿酮类化合物的加氢离子质谱裂解时,发现分子结构中的羰基最容易接受质子,而质子在各个质子化点上可以“流动”,其迁移的能垒直接影响离子的裂解,苯基上取代基的电子效应通过影响质子迁移的能垒来改变碎片离子的强度。除质子迁移重排之外,离子还可以发生其它形式的骨架重排,如2-(4, 6-Dimethoxypyrimidin-2-Ylsulfanyl)-N-Phenylbenzamide 及其衍生物,其负离子存在Smiles重排。总之,由于离子不稳定性,我们难以像常规化合物那样比较直接地对其进行结构分析。因此,使用计算化学模拟离子的结构以及其裂解途径,结合质谱技术探索[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]离子化学具有非常广阔的前景。
[align=center] [/align] [font=Tahoma, Helvetica, SimSun, sans-serif][size=18px][color=#444444]质谱分析中涉及多种离子类型,每种离子在解析化合物结构时扮演着特定的角色。以下是几种关键的离子类型及其定义: 1. 分子离子(母离子):当一个分子失去一个电子时形成,其质荷比(m/z)直接对应于分子的相对分子质量。是分析物进入质谱后,经过电离、加速、分离后,最接近正离子检测器的离子。分子离子峰能提供分子量的信息,但在硬电离条件下可能不明显或不存在。 2. 准分子离子:与分子存在简单关系的离子,如通过失去或获得一个氢原子形成的(M+H)+或(M-H)-,这些离子对于确定分子量同样重要。 3. 碎片离子(子离子):电离后有过剩内能的分子离子能以多种方式裂解,生成碎片离子。裂解方式包括简单开裂、重排开裂、复杂开裂和双重排开裂,这些碎片提供了化合物内部结构的线索。 4. 亚稳离子:在离子源到检测器的路径中不稳定的离子,它们在检测前分解,但其存在可以通过质谱图上的特定峰来推断,这些峰通常较弱且横跨几个质量单位。 5. 同位素离子:由元素的同位素构成的离子,出现在分子离子或碎片离子的质量数右侧,用于确认分子的组成。各种元素的同位素基本上是按照该同位素在自然界中的丰度比出现在质谱中,这对于利用质谱确定化合物及碎片的元素组成有很大作用。如自然界中氯元素的同位素35Cl和37Cl的丰度比约为3:1,当某一质谱峰的M+和M++2峰的强度比近似为3:1 时,其相应的化合物或碎片中就可能含有1个氯原子。 6. 重排离子:在裂解过程中发生结构重组的离子,保持电荷但改变了分子片段的连接方式,有助于理解化合物的内部结构。 7. 多电荷离子:带有两个或更多电荷的离子,常见于软电离质谱中,其质荷比小于单电荷离子,对于蛋白质等大分子的质谱分析尤为重要。当分子量为一万的大分子物质带有十个电荷时,其质荷比为1000。这就使得质量范围为1000左右的质量分析器,在使用软电离接口时,可以分析分子量达数万或数十万的大分子化合物。 8. 加合离子:当分子离子与溶剂分子、添加剂或其他小分子结合时形成,这种结合可以是有意的也可以是无意的,有助于识别和解析软电离质谱中的分子离子峰。 这些离子类型在质谱分析中至关重要,它们的识别和解析对于理解化合物的化学结构和组成至关重要。[/color][/size][/font]
1,分子离子分子经过电子轰击,失去一个价电子形成带正电荷的离子称为分子离子或母离子,质谱图中相应的峰称之为分子离子峰或母离子峰M+。分子离子峰一般位于质荷比最高的位置。约有75%的有机化合物产生的分子离子峰,判断分子离子峰有如下原则:(1)稳定性规律 可预见分子离子峰的强弱,需预先了解化合物结构。芳香(杂)环〉酯环〉硫醚、酮〉共轭烯烃〉直链烷烃〉酰胺〉酮〉醛〉胺〉酯〉醚〉羧酸〉腈〉伯醇〉叔醇〉缩醛(2)氮规律 含奇数个氮原子的分子量必为单数,否则为偶数。(3)质量差规律 判断依据:最高质量峰与其他碎片离子质量差。如出现以下质量差,4到13,19到25(含氟化合物例外),37,38,50到53,65,66,则最高质量峰不是分子离子峰。另外如差为14的情况出现,应考虑是否有同系物出现。(4)断裂方式规律 稳定性差的分子有易丢失的特定的离子团,如醇类的CH3,H2O等。(5)单质子增减规律 即M+1,M-1,醚、酯、胺、酰胺、腈、氨基酸酯、胺醇等的M+1峰较为显著,醛、醇和含氮化合物M-1峰较为显著。适当情况下也可采用降低EI的EM电压,采用CI或衍生化等方法获得较好的分子离子峰。2,同位素离子自然界的同位素分布大都已经被明确测定,根据同位素分布特点计算分子式常被用在质谱解析中,典型的分子组成式如C?H?N?O?,拜隆(Beynon)表的有助于迅速确定分子式。如166.062994,其分子式仅有一种可能即C9H10O3。3,碎片离子质谱电离过程中,过剩的能量导致碎片离子的产生。由于键能大小、碎片稳定性(诱导效应、π电子系统、杂原子共轭)、空间等因素导致不同的碎片离子产生。离子开裂类型有单纯开裂、重排、复杂开裂、双重重排。碎片离子的形成受化学结构的支配,所以可以将碎片“拼凑”成分子。4,亚稳离子亚稳态离子的产生是有离子本身的寿命决定的,我们研究亚稳态离子的规律是有效的确定开裂途径的方法。5,多电荷离子当丢失两个或两个以上电子就形成多电荷离子,芳香族化合物、有机金属化合物或共轭体系化合物易产生多电荷离子。6,离子-分子作用离子分子离子与中性分子碰撞,并从分子离子获得一个原子或基团,但丰度较低,常可以忽略。 有个人见解,仅供参考
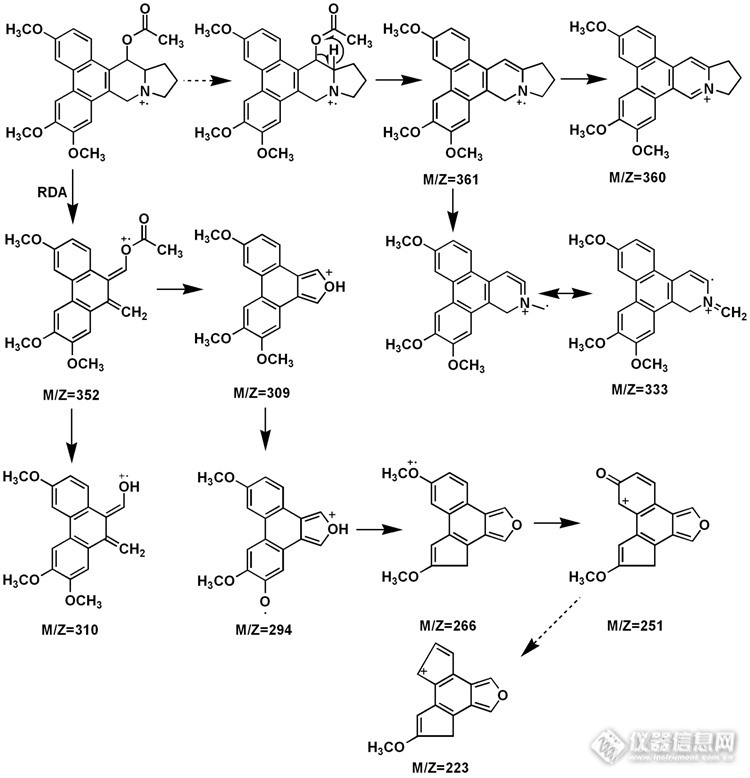
今天分享下娃儿藤碱(Tylophorine)中的一种化合物的质谱裂解途径,发现用CAS模板画出来的结构还是看起来比较舒服的,这类化合物具有菲并吲哚结构,所以其比较重要的裂解方式的RDA裂解方式,也表现出了很高的丰度。质谱图及结构式:http://ng1.17img.cn/bbsfiles/images/2014/04/201404281859_497669_2359621_3.jpg分子离子峰M/Z-421很弱,可以看到Base Peak为M/Z=361,相差60,这是由McL重排后得到的,该离子再经过α断裂失去氢自由基可以得到M/Z=360的碎片离子,丰度较高,而通过分子离子的RDA反应失去中性分子后将得到M/Z=352的碎片离子,该离子失去乙烯酮可以得到M/Z=310的碎片离子,同时由于邻位效应 氢重排会失去乙酰基得到M/Z=309的碎片离子,接着失去菲环上的甲基自由基得到M/Z=294的碎片离子,该离子失去CO得到M/Z=266的碎片离子(未看到),该离子失去甲基自由基得到M/Z=251的碎片离子。该碎片离子会再失去一份子CO而得到M/Z=223的碎片。质谱图上可以看到具有较强丰度的M/Z=333碎片离子,该离子的生成是电荷中心定域到氮原子上由其诱导的电子成对会使吲哚环失去乙烯自由基而生成。可能的质谱裂解途径:http://ng1.17img.cn/bbsfiles/images/2014/04/201404281859_497670_2359621_3.pngfile:///c:/DOCUME~1/ADMINI~1/APPLIC~1/360se6/USERDA~1/Temp/DDEMQ~1.M1B
1,分子离子分子经过电子轰击,失去一个价电子形成带正电荷的离子称为分子离子或母离子,质谱图中相应的峰称之为分子离子峰或母离子峰M+。分子离子峰一般位于质荷比最高的位置。约有75%的有机化合物产生的分子离子峰,判断分子离子峰有如下原则:(1)稳定性规律 可预见分子离子峰的强弱,需预先了解化合物结构。芳香(杂)环〉酯环〉硫醚、酮〉共轭烯烃〉直链烷烃〉酰胺〉酮〉醛〉胺〉酯〉醚〉羧酸〉腈〉伯醇〉叔醇〉缩醛(2)氮规律 含奇数个氮原子的分子量必为单数,否则为偶数。(3)质量差规律 判断依据:最高质量峰与其他碎片离子质量差。如出现以下质量差,4到13,19到25(含氟化合物例外),37,38,50到53,65,66,则最高质量峰不是分子离子峰。另外如差为14的情况出现,应考虑是否有同系物出现。(4)断裂方式规律 稳定性差的分子有易丢失的特定的离子团,如醇类的CH3,H2O等。(5)单质子增减规律 即M+1,M-1,醚、酯、胺、酰胺、腈、氨基酸酯、胺醇等的M+1峰较为显著,醛、醇和含氮化合物M-1峰较为显著。适当情况下也可采用降低EI的EM电压,采用CI或衍生化等方法获得较好的分子离子峰。2,同位素离子自然界的同位素分布大都已经被明确测定,根据同位素分布特点计算分子式常被用在质谱解析中,典型的分子组成式如C?H?N?O?,拜隆(Beynon)表的有助于迅速确定分子式。如166.062994,其分子式仅有一种可能即C9H10O3。3,碎片离子质谱电离过程中,过剩的能量导致碎片离子的产生。由于键能大小、碎片稳定性(诱导效应、π电子系统、杂原子共轭)、空间等因素导致不同的碎片离子产生。离子开裂类型有单纯开裂、重排、复杂开裂、双重重排。碎片离子的形成受化学结构的支配,所以可以将碎片“拼凑”成分子。4,亚稳离子亚稳态离子的产生是有离子本身的寿命决定的,我们研究亚稳态离子的规律是有效的确定开裂途径的方法。5,多电荷离子当丢失两个或两个以上电子就形成多电荷离子,芳香族化合物、有机金属化合物或共轭体系化合物易产生多电荷离子。6,离子-分子作用离子分子离子与中性分子碰撞,并从分子离子获得一个原子或基团,但丰度较低,常可以忽略。有个人见解,仅供参考[em0815] [em0815]
http://www.hbcnc.edu.cn/~hxx/jpkc/yjhx/hukun/mulu.htm 一、Arbuzov 反应 二、Arndt-Eister 反应 三、Baeyer-villiger 反应 四、Beckmann 重排五、Birch 还原六、Bouveault-Blanc 还原七、Bucherer 反应八、Bamberger,E. 重排九、Berthsen,A.Y 吖啶合成法十、Cannizzaro 反应十 一、Chichibabin 反应 十 二、Claisen 酯缩合反应十 三、Claisen-Schmidt 反应十 四、Claisen 重排十 五、Clemmensen 还原十 六、Combes 喹啉合成法十 七、Cope 消除反应十 八、Cope 重排十 九、Curtius 反应二 十、Crigee,R 反应二十一、Dakin 反应 二十二、Elbs 反应二十三、Edvhweiler-Clarke 反应二十四、Elbs,K 过硫酸钾氧化法二十五、Favorskii 反应二十六、Favorskii 重排二十七、Friedel-Crafts 烷基化反应二十八、Friedel-Crafts 酰基化反应二十九、Fries 重排 三 十、Fischer,O-Hepp,E 重排三十一、Gabriel 合成法 三十二、Gattermann 反应三十三、Gattermann-Koch 反应三十四、Gomberg-Bachmann 反应三十五、Hantzsch 合成法 三十六、Haworth 反应三十七、Hell-Volhard-Zelinski反应 三十八、Hinsberg 反应三十九、Hofmann 烷基化四十、Hofmann 消除反应四十一、Hofmann 重排(降解)四十二、Houben-Hoesch 反应四十三、Hunsdiecker 反应四十四、Kiliani 氯化增碳法四十五、Knoevenagel 反应四十六、Koble 反应四十七、Koble-Schmitt 反应四十八、Kolbe,H.Syntbexis of Nitroparsffini 合成四十九、Leuckart 反应五 十、Lossen 反应五十一、Mannich 反应五十二、Meerwein-Ponndorf 反应五十三、Michael 加成反应五十四、Martius,C.A. 重排五十五、Norrish Ⅰ和Ⅱ 型裂 五十六、Oppenauer 氧化五十七、Orton,K.J.P 重排 五十八、Paal-Knorr 反应五十九、Pschorr 反应六 十、Prileschajew,N 反应六十一、Prins,H.J 反应六十二、Pinacol 重排六十三、Perkin,W.H 反应六十四、Pictet-Spengler异喹啉合成法六十五、Reformatsky 反应六十六、Reimer-Tiemann 反应六十七、Reppe 合成法六十八、Robinson 缩环反应六十九、Rosenmund 还原七 十、 Ruff 递降反应七十一、Riley,H.L 氧化法七十二、Sandmeyer 反应七十三、Schiemann 反应七十四、Schmidt 反应七十五、Skraup 合成法七十六、Sommelet-Hauser 反应七十七、Stepen 还原-氰还原为醛七十八、Stevens 重排七十九、Strecker 氨基酸合成法八 十、异喹啉合成法八十一、Schiemann,G. 反应八十二、Schmidin,J. 乙烯酮合成八十三、Tiffeneau-Demjanov 重排八十四、Tischenko,V.反应八十五、Thorpe,J.F. 缩合八十六、Tollens,B. 缩合八十七、Ullmann 反应 八十八、Urech,F.羟腈合成法八十九、Vilsmeier 反应九 十、Van Ekenstein,W,A 重排九十一、Williamson 合成法九十二、Wacker 反应九十三、Wagner-Meerwein 重排 九十四、Wittig 反应 九十五、Wittig-Horner 反应九十六、Wohl 递降反应
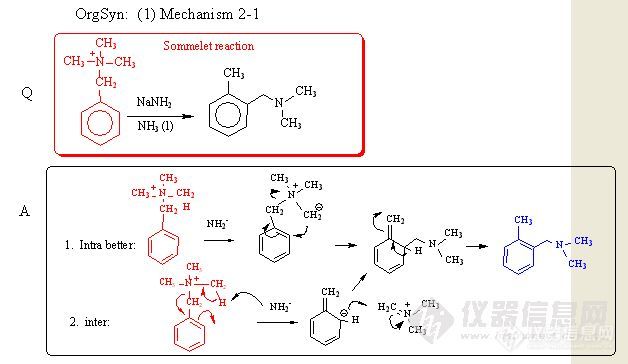
OrgSyn: (1) Mechanism 2-1http://ng1.17img.cn/bbsfiles/images/2011/05/201105130125_293844_1631320_3.jpg基本:1. 涉及: 季铵盐的理化性质2. Driving Force: 中间遇 N ylid, 终成中性分子3. 思索: inter 与 intra 是否并存? 比例?4. 实验探讨: inter? 是否捕获到 toluene?5. 体会: 苯环罕见的被电子 (Nu) 攻击!6. 其他: 本反应为 Sommelet Reaction进一步说明:本反应或许不容易发生, 但使用了强碱 (NaNH2) 并且涉及有氮叶立德的生成 (可以稳定过渡态), 导致 C-H 被脱除. 私下比较偏向分子内重排, 因为分子间涉及电荷分离. 若有分子间重排, 则可能中间淬灭时能捕获到甲苯, 或含氘的甲苯 (用重水或 DCl 淬灭). 即使有分子间重排, 也不能排除也存在分子内重排.
1,分子离子分子经过电子轰击,失去一个价电子形成带正电荷的离子称为分子离子或母离子,质谱图中相应的峰称之为分子离子峰或母离子峰M+。分子离子峰一般位于质荷比最高的位置。约有75%的有机化合物产生的分子离子峰,判断分子离子峰有如下原则:(1)稳定性规律 可预见分子离子峰的强弱,需预先了解化合物结构。芳香(杂)环〉酯环〉硫醚、酮〉共轭烯烃〉直链烷烃〉酰胺〉酮〉醛〉胺〉酯〉醚〉羧酸〉腈〉伯醇〉叔醇〉缩醛(2)氮规律 含奇数个氮原子的分子量必为单数,否则为偶数。(3)质量差规律 判断依据:最高质量峰与其他碎片离子质量差。如出现以下质量差,4到13,19到25(含氟化合物例外),37,38,50到53,65,66,则最高质量峰不是分子离子峰。另外如差为14的情况出现,应考虑是否有同系物出现。(4)断裂方式规律 稳定性差的分子有易丢失的特定的离子团,如醇类的CH3,H2O等。(5)单质子增减规律 即M+1,M-1,醚、酯、胺、酰胺、腈、氨基酸酯、胺醇等的M+1峰较为显著,醛、醇和含氮化合物M-1峰较为显著。适当情况下也可采用降低EI的EM电压,采用CI或衍生化等方法获得较好的分子离子峰。2,同位素离子自然界的同位素分布大都已经被明确测定,根据同位素分布特点计算分子式常被用在质谱解析中,典型的分子组成式如C?H?N?O?,拜隆(Beynon)表的有助于迅速确定分子式。如166.062994,其分子式仅有一种可能即C9H10O3。3,碎片离子质谱电离过程中,过剩的能量导致碎片离子的产生。由于键能大小、碎片稳定性(诱导效应、π电子系统、杂原子共轭)、空间等因素导致不同的碎片离子产生。离子开裂类型有单纯开裂、重排、复杂开裂、双重重排。碎片离子的形成受化学结构的支配,所以可以将碎片“拼凑”成分子。4,亚稳离子亚稳态离子的产生是有离子本身的寿命决定的,我们研究亚稳态离子的规律是有效的确定开裂途径的方法。5,多电荷离子当丢失两个或两个以上电子就形成多电荷离子,芳香族化合物、有机金属化合物或共轭体系化合物易产生多电荷离子。6,离子-分子作用离子分子离子与中性分子碰撞,并从分子离子获得一个原子或基团,但丰度较低,常可以忽略。
中国科技网讯 近日,德国马克斯—玻恩非线性光学与短脉冲光谱学研究所(MBI)的研究人员与国际伙伴一起研发了一个试验装置,首次可以准确确定电子从隧道效应障碍物中出来的时间点。该研究为原子和分子中的“多电子重排”在空间和时间上的直接分辨提供了一个普遍方法。相关研究发表在《自然》杂志上。 在神奇的量子世界里原子和分子不再适用经典的物理规律。在这里,电子可以克服能垒,尽管他们没有必要的能量,这就是所谓的“隧穿效应”。直接测量量子世界里的进程是非常困难的,尤其当他们时间尺度特别短的时候。因此,MBI的研究人员与来自以色列、加拿大和英国的同事一起研发了一个试验装置,让各种物理量的大小可以在比飞秒还短的时间尺度内变化。通过测量和计算的比较,科学家获得了一个量子时钟,从而能够以阿秒的精度确定发生电子隧穿的时刻。 研究人员先用一个强激光场诱导来自氦原子的电子隧道效应,再用一个较弱的探测激光场将发生隧道效应的电子引到侧向进行研究。这其中带正电的原子核的吸引力就表现为需要克服的能垒,而缓慢振荡并垂直照射隧穿电子的弱激光场则可以让电子像被橡皮筋牵引一样向原子核运动。当电子与原子核接近时会出现光闪烁的特性,这就是所谓的高次谐波。通过测量这些高次谐波的频率、偏转电子飞行路径的长度和偏转激光场的属性,研究人员就可以最终计算出电子跨越能垒的准确时间点。 MBI的奥尔加·斯米尔诺娃博士用一个简单的比喻来解释她们是如何得到电子隧穿时间点的。她说:“当你从一家咖啡店出来走向对面的公共汽车站,弱激光场就像左右交替吹的风,把你往路旁推。当我们知道了风的特点,即有多大、如何改变方向,我们就能说出你走出门口的时间。” 现在,研究人员继续用二氧化碳分子来进行类似的实验。相对于只有两个电子的氦,二氧化碳分子有20个电子。它们可能会停在不同的轨道,隧穿的电子根据所处轨道的不同会有一个很小的时间延迟。这个实验首次给了物理学家确认隧穿电子源头的机会。(驻德国记者 李山) 《科技日报》(2012-08-13 二版)
[align=center][b][font=宋体][color=#333333]实验人必知的质谱基础知识[/color][/font][/b][/align][font=宋体][color=#333333][back=white]质谱,物质的分子在高真空下,经物理作用或化学反应等途径形成带电粒子[/back][/color][/font][font='Times New Roman','serif'][color=#333333][back=white],[/back][/color][/font][font=宋体][color=#333333][back=white]某些带电粒子可进一步断裂,形成离子,每一离子的质量与所带电荷的比称为质荷比[/back][/color][/font][font='Times New Roman','serif'][color=#333333][back=white](m/z,[/back][/color][/font][font=宋体][color=#333333][back=white]曾用[/back][/color][/font][font='Times New Roman','serif'][color=#333333][back=white]m/e)[/back][/color][/font][font=宋体][color=#333333][back=white],不同质荷比的离子经质量分离器一一分离后,由检测器测定每一离子的质荷比及相对强度,由此得出的谱图称为质谱。[/back][/color][/font][align=center][font=宋体][color=#333333][back=white]不同离子的概念[/back][/color][/font][/align][b][color=#021EAA]1[/color][font=宋体][color=#021EAA]、分子离子[/color][/font][/b][font=宋体]分子被电子束轰击失去一个电子形成的离子称为分子离子。分子离子用[/font][font='Times New Roman','serif'] M[sup]+[/sup][/font][font=宋体]表示。分子离子是一个游离基离子。在质谱图中与分子离子相对应的峰为分子离子峰。分子离子峰的质荷比就是化合物的相对分子质量[/font][font='Times New Roman','serif'], [/font][font=宋体]所以[/font][font='Times New Roman','serif'],[/font][font=宋体]用质谱法可测分子量。[/font][font='Times New Roman','serif'][b][color=#021EAA]2[/color][/b][/font][b][font=宋体][color=#021EAA]、同位素离子[/color][/font][/b][font=宋体]含有同位素的离子称为同位素离子。在质谱图上[/font][font='Times New Roman','serif'], [/font][font=宋体]与同位素离子相对应的峰称为同位素离子峰。[/font][font='Times New Roman','serif'][b][color=#021EAA]3[/color][/b][/font][b][font=宋体][color=#021EAA]、碎片离子[/color][/font][/b][font=宋体]分子离子在电离室中进一步发生键断裂生[/font][font=宋体]成的离子称为碎片离子。[/font][font='Times New Roman','serif'][b][color=#021EAA]4[/color][/b][/font][b][font=宋体][color=#021EAA]、重排离子[/color][/font][/b][font=宋体]经重排裂解产生的离子称为重排离子。其结构并非原来分子的结构单元。在重排反应中,化学键的断裂和生成同时发生[/font][font='Times New Roman','serif'], [/font][font=宋体]并丢失中性分子或碎片。[/font][font='Times New Roman','serif'][b][color=#021EAA]5[/color][/b][/font][b][font=宋体][color=#021EAA]、奇电子离子与偶电子离子[/color][/font][/b][font=宋体]具有未配对电子的离子为奇电子离子。这样的离子同时也是自由基,具有较高的反应活性。无未配对电子的离子为偶电子离子。[/font][font='Times New Roman','serif'][b][color=#021EAA]6[/color][/b][/font][b][font=宋体][color=#021EAA]、多电荷离子[/color][/font][/b][font=宋体]分子中带有不止一个电荷的离子称为多电荷离子。当离子带有多电荷离子时,其质核比下降,因此可以利用常规的四极质量分析器来检测大分子量化合物。[/font][font='Times New Roman','serif'][b][color=#021EAA]7[/color][/b][/font][b][font=宋体][color=#021EAA]、亚稳离子[/color][/font][/b][font=宋体]从离子源出口到检测器之间产生的离子。即在飞行过程中发生裂解的母离子。由于母离子中途已经裂解生成某种离子和中性碎片,记录器中只能记录这种离子,也称这种离子为亚稳离子,由它形成的质谱峰为亚稳峰。[/font][font='Times New Roman','serif'][b][color=#021EAA]8[/color][/b][/font][b][font=宋体][color=#021EAA]、准分子离子[/color][/font][/b][font=宋体]比分子量多或少[/font][font='Times New Roman','serif'] 1 [/font][font=宋体]质量单位的离子称为准分子离子,如:[/font][font='Times New Roman','serif'](M+H)+[/font][font=宋体],[/font][font='Times New Roman','serif'] (M-H)+[/font][font=宋体]。其不含未配对电子,结构上比较稳定。[/font][align=center][font=宋体]分子离子峰[/font][/align][b][font='Times New Roman','serif'][color=#021EAA]1[/color][/font][font=宋体][color=#021EAA]、分子离子峰强度[/color][/font][/b][font=宋体]分子离子是质谱图中最有价值的信息,它不但是测定化合物分子量的依据,而且可以推测化合物的分子式,用高分辨质谱可以直接测定化合物的分子式。[/font][font='Times New Roman','serif'] [/font][font=宋体]一般来讲,从分子中失去的电子应该是分子中束缚最弱的电子,如双键或叁键的[/font][font='Times New Roman','serif']π[/font][font=宋体]电子,杂原子上的非[/font][font=宋体]键电子。[/font][font='Times New Roman','serif'][/font][font=宋体]分子离子的丰度主要取决于其稳定性和分子电离所需要的能量。易失去电子的化合物,如环状化合物、双键化合物等,其分子离子稳定、分子离子峰较强;而长碳链烷烃、支链烷烃等正与此相反。[/font][font='Times New Roman','serif'][/font][font=宋体]各类化合物分子离子稳定性次序大致为:芳香环[/font][font='Times New Roman','serif'] ([/font][font=宋体]包括芳香杂环[/font][font='Times New Roman','serif']) [/font][font=宋体]共轭烯[/font][font='Times New Roman','serif'] [/font][font=宋体]烯[/font][font='Times New Roman','serif'] [/font][font=宋体]脂环[/font][font='Times New Roman','serif'] [/font][font=宋体]硫醚、硫酮[/font][font='Times New Roman','serif'] [/font][font=宋体]酰胺[/font][font='Times New Roman','serif'] [/font][font=宋体]酮[/font][font='Times New Roman','serif'] [/font][font=宋体]醛[/font][font='Times New Roman','serif'] [/font][font=宋体]直链烷烃[/font][font='Times New Roman','serif'] [/font][font=宋体]醚[/font][font='Times New Roman','serif'] [/font][font=宋体]酯[/font][font='Times New Roman','serif'] [/font][font=宋体]胺[/font][font='Times New Roman','serif'] [/font][font=宋体]羧酸[/font][font='Times New Roman','serif'][/font][font=宋体]腈[/font][font='Times New Roman','serif'][/font][font=宋体]伯醇[/font][font='Times New Roman','serif'][/font][font=宋体]仲醇[/font][font='Times New Roman','serif'][/font][font=宋体]叔醇[/font][font='Times New Roman','serif'][/font][font=宋体]高度支链烃。[/font][font='Times New Roman','serif'][/font][font=宋体]芳环[/font][font='Times New Roman','serif'] ([/font][font=宋体]包括芳杂环[/font][font='Times New Roman','serif']) [/font][font=宋体]、[/font][font=宋体]脂环化合物、[/font][font=宋体]硫醚、[/font][font=宋体]硫酮、[/font][font=宋体]共轭烯分子离子峰比较明显,直链酮、[/font][font=宋体]酯、[/font][font=宋体]酸、[/font][font=宋体]醛、[/font][font=宋体]酰胺、[/font][font=宋体]卤化物等通常显示分子离子峰,脂肪族醇、胺、[/font][font=宋体]亚硝酸酯、[/font][font=宋体]硝酸酯、[/font][font=宋体]硝基化合物、[/font][font=宋体]腈类及多支链化合物容易裂解[/font][font='Times New Roman','serif'], [/font][font=宋体]分子离子峰通常很弱或不出现。[/font][font='Times New Roman','serif'][/font][font=宋体]分子离子峰不出现或丰度极低难以确认,可根据不同情况改变实验条件予以验证。[b]([/b][/font][b][font='Times New Roman','serif']1[/font][font=宋体])降低轰击电子的能量[/font][/b][font=宋体]将常用的[/font][font='Times New Roman','serif']70eV [/font][font=宋体]改变[/font][font='Times New Roman','serif']15eV [/font][font=宋体]以减少形成的分子离子继续断裂的几率,降低了碎片离子的丰度,使分子离子峰的相对丰度增加,从而可能辨认出分子离子。[/font][font='Times New Roman','serif'][/font][b][font=宋体]([/font][font='Times New Roman','serif']2[/font][font=宋体])用[/font][font='Times New Roman','serif']CI, FI,FD[/font][font=宋体]等软电离方法[/font][/b][font=宋体]降低轰击电子能量的结果会使仪器的灵敏度下降,虽然分子离子峰的丰度有所提高,但离子的绝对强度降低,一些由于热不稳定和低挥发性等原因而不出现分子离子峰的化合物,用这种办法不会得到预期的效果,这时可采取各种软电离的办法,虽然碎片离子大量减少,但可以突出分子离子峰。[/font][font='Times New Roman','serif'][/font][b][font=宋体]([/font][font='Times New Roman','serif']3[/font][font=宋体])降低样品的气化温度[/font][/b][font=宋体]气化温度的降低可以减少分子离子进一步断裂的可能性,分子离子峰的相对丰度增加。如三十烷烃在[/font][font='Times New Roman','serif']340[/font][font=宋体]℃[/font][font=宋体]时气化,不出现分子离子峰,改变[/font][font='Times New Roman','serif']70[/font][font=宋体]℃[/font][font=宋体]气化时分子离子峰的丰度接近基峰。[/font][font='Times New Roman','serif'][/font][b][font=宋体]([/font][font='Times New Roman','serif']4[/font][font=宋体])制备衍生物[/font][/b][font=宋体]某些化合物不易挥发或热稳定性差,可以衍生化处理。例如,可将某有机酸制备成相应的酯,酯容易气化,而且易得到分子离子峰,由此来推断有机酸的分子量。[/font][font='Times New Roman','serif'][b][color=#021EAA]2[/color][/b][/font][b][font=宋体][color=#021EAA]、分子离子峰的识别[/color][/font][/b][font=宋体]解析时一般把谱图中最高质荷比的离子假设为分子离子,后用分子离子的判别标准一一对比,若被检查离子不符其中任何一条标准,则它一定不是分子离子;若被检查离子符合所有条件,则它有可能是分子离子。分子离子的判别可以参考如下标准:([/font][font='Times New Roman','serif']1[/font][font=宋体])分子离子必须是奇电子离子。由于有机分子都是偶电子,所有失去一个电子生成的分子离子必是奇电子离子。[/font][font='Times New Roman','serif'][/font][font=宋体]([/font][font='Times New Roman','serif']2[/font][font=宋体])是否符合氮规则[/font][font='Times New Roman','serif'] (NitrogenRule) [/font][font=宋体]。有机化合物的分子量是偶数或奇数与所含有的氮原子的数目有关。凡不含氮原子或含偶数个氮原子的化合物,其分子量必为偶数;含奇数个氮原子的化合物,其分子量必为奇数,这就是所谓的氮规则。[/font][font='Times New Roman','serif'][/font][font=宋体]([/font][font='Times New Roman','serif']3[/font][font=宋体])合理的中性碎片的丢失。这些中性碎片可能是小分子或者自由基基团。这些中性碎片有着特殊的质量数,[/font][font='Times New Roman','serif']m/z[/font][font=宋体]最高值与邻近的碎片离子之间应有一个合理的质量差。[/font][font='Times New Roman','serif'][/font][font=宋体]例如:[/font][font='Times New Roman','serif']M+[/font][font=宋体]丢失一个质子[/font][font='Times New Roman','serif']H[/font][font=宋体]、[/font][font='Times New Roman','serif']CH[sub]3[/sub][/font][font=宋体]、[/font][font='Times New Roman','serif']H[sub]2[/sub]O,C[sub]2[/sub]H[sub]4[/sub][/font][font=宋体]等是合理的。如果这个质量差落在[/font][font='Times New Roman','serif']4~14[/font][font=宋体]和[/font][font='Times New Roman','serif']21~25[/font][font=宋体]之间就是不合理的,也即如果在[/font][font='Times New Roman','serif']M-4[/font][font=宋体]到[/font][font='Times New Roman','serif']M-13[/font][font=宋体]的范围内存在峰,则说明原所假定的分子离子峰不是分子离子峰。[/font][align=center][font=宋体]碎片离子[/font][/align][font=宋体]碎片离子的质荷比及其丰度在质谱数据中占很大比例。碎片离子的相对丰度与分子结构有密切关系,高丰度的碎片峰代表分子中易于裂解的部分,如果有几个主要碎片峰,并且代表着分子的不同部分,则由这些碎片峰就可以粗略地把分子骨架拼凑起来。质谱解析的大量工作就是分析碎片离子的形成过程。[/font][font='Times New Roman','serif'][b][color=#021EAA]1[/color][/b][/font][b][font=宋体][color=#021EAA]、[/color][/font][color=#021EAA]α[/color][font=宋体][color=#021EAA]断裂[/color][/font][/b][font=宋体]分子失去电子,形成游离基离子,它的电子有强烈的成对倾向,电子转移与邻近原子形成一个新键,同时邻近原子的[/font][font='Times New Roman','serif']α[/font][font=宋体]键断裂。因此,这种断裂通常称为[/font][font='Times New Roman','serif']“α”[/font][font=宋体]断裂反应。[/font][b][color=#021EAA]2[/color][font=宋体][color=#021EAA]、[/color][/font][color=#021EAA]i[/color][font=宋体][color=#021EAA]断裂(诱导断裂)[/color][/font][/b][font=宋体]诱导断裂是由正电荷诱导、[/font][font=宋体]吸引一对电子而发生的断裂[/font][font='Times New Roman','serif'], [/font][font=宋体]其结果是正电荷的转移。诱导断裂常用[/font][font='Times New Roman','serif']i[/font][font=宋体]来表示。一般情况下,电负性强的元素诱导力也强。在有些情况下,诱导断裂和[/font][font='Times New Roman','serif']α[/font][font=宋体]断裂同时存在。由于[/font][font='Times New Roman','serif']i[/font][font=宋体]断裂需要电荷转移,因此,[/font][font='Times New Roman','serif']i[/font][font=宋体]断裂不如[/font][font='Times New Roman','serif']α[/font][font=宋体]断裂容易进行。[/font][b][color=#021EAA]3[/color][font=宋体][color=#021EAA]、[/color][/font][color=#021EAA]σ[/color][font=宋体][color=#021EAA]断裂[/color][/font][/b][font=宋体]如果化合物分子中具有[/font][font='Times New Roman','serif']σ[/font][font=宋体]键,如烃类化合物,则会发生[/font][font='Times New Roman','serif']σ[/font][font=宋体]键断裂。[/font][font='Times New Roman','serif']σ[/font][font=宋体]键断裂需要的能量大,当化合物中没有[/font][font='Times New Roman','serif']π[/font][font=宋体]电子和[/font][font='Times New Roman','serif']n[/font][font=宋体]电子时,[/font][font='Times New Roman','serif']σ[/font][font=宋体]键的断裂才可能成为主要的断裂方式。断裂后形成的产物越稳定,这样的断裂就越容易进行,阳碳离子的稳定性顺序为[b][font=宋体][color=#FF4C00]叔[/color][/font][color=#FF4C00][/color][font=宋体][color=#FF4C00]仲[/color][/font][color=#FF4C00][/color][font=宋体][color=#FF4C00]伯[/color][/font][/b]。因此,碳氢化合物最容易在分支处发生键的断裂。并且,失去最大烷基的断裂最容易进行。[/font][b][color=#021EAA]4[/color][font=宋体][color=#021EAA]、重排开裂[/color][/font][/b][font='Times New Roman','serif'][color=#021EAA] [/color][/font][font=宋体]重排开裂时涉及到两个键的断裂,脱去一个中性分子,同时发生[/font][font='Times New Roman','serif']H[/font][font=宋体]重排。重排的结果产生了在原化合物中不存在的结构单元的离子。[/font][b][font=宋体]([/font]1[font=宋体])麦氏重排[/font](Mclafferty rearrangement)[/b][font=宋体]分子离子或碎片离子结构中有双键,且在[/font][font='Times New Roman','serif']γ[/font][font=宋体]位上有[/font][font='Times New Roman','serif']H[/font][font=宋体]原子的正离子都能发生麦氏重排。在开裂中,[/font][font='Times New Roman','serif'] γ[/font][font=宋体]位上的[/font][font='Times New Roman','serif']H[/font][font=宋体]通过六元环过渡态的迁移到电离的双键碳或杂原子上,同时烯丙键断裂,生成中性分子和碎片离子。[/font][b][font=宋体]([/font]2[font=宋体])逆迪尔斯一阿尔德重排[/font](retro Diels-Alder fragmentation,RDA)[/b][font=宋体]对具有环内双键结构的化合物能发生[/font][font='Times New Roman','serif']RDA[/font][font=宋体]开裂,一般生成一个带正电荷的共轭二烯自由基和一个中性分子。[/font][font='Times New Roman','serif'] [/font][b][font=宋体]([/font]3[font=宋体])脱去小分子化合物的重排[/font][/b][font=宋体]在一些醇类、[/font][font=宋体]硫醇类、[/font][font=宋体]卤代烃等有机化合物分子的质谱中经常出现脱去水、硫化氢、[/font][font=宋体]卤化氢等小分子化合物而生成的碎片离子。醇非常容易脱去水分子,所以醇类化合物的分子离子峰相对丰度很小,甚至不出现分子离子峰。[/font][font='Times New Roman','serif'][/font][font=宋体]([/font][b]4[font=宋体])复杂开裂[/font][/b][font=宋体]复杂开裂是指在有机化合物的质谱中,经常出现离子中两个或两个以上化学键连续发生断裂生成碎片的过程。除了重排反应以外,环状化合物的质谱碎裂也是如此。复杂断裂一般是指环状化合物发生的多个键断裂,有时涉及一个氢原子的转移。[/font][b][font=宋体]([/font]5[font=宋体])骨架重排[/font][/b][font=宋体]骨架重排是指在有机化合物裂解过程中,部分基团如甲基、[/font][font=宋体]芳香基以及含[/font][font='Times New Roman','serif']O[/font][font=宋体]、[/font][font='Times New Roman','serif']N[/font][font=宋体]、[/font][font='Times New Roman','serif']S[/font][font=宋体]等的基团发生迁移,生成一些小的中性碎片、自由基离子等的过程。常见的中性碎片如[/font][font='Times New Roman','serif']CO[/font][font=宋体]、[/font][font='Times New Roman','serif']SO[/font][font=宋体]、[/font][font='Times New Roman','serif']SO2, S2, CH=CH[/font][font=宋体]等。[/font][font='Helvetica','sans-serif'][color=#333333][back=white] [/back][/color][/font]
[color=#DC143C]苯酚[/color][img]http://ng1.17img.cn/bbsfiles/images/2009/11/200911232210_186191_1610969_3.jpg[/img]苯酚(C6H6O,PhOH),又名石炭酸、羟基苯,是最简单的酚类有机物,一种弱酸。常温下为一种无色晶体。有毒。有腐蚀性,常温下微溶于水 易溶于有机溶液;当温度高于65℃时,能跟水以任意比例互溶,其溶液沾到皮肤上用酒精洗涤。暴露在空气中呈粉红色。 苯酚是一种常见的化学品,是生产某些树脂、杀菌剂、防腐剂以及药物(如阿司匹林)的重要原料。 【中文名称】苯酚;石炭酸 【英文名称】phenol 【结构或分子式】 所有C原子均以sp2杂化轨道形成σ键,O原子均以sp3杂化轨道形成σ键。 【相对分子量或原子量】94.11 【密度】1.071 【熔点(℃)】42~43 【沸点(℃)】182 【折射率】1.5425(41) 【毒性LD50(mg/kg)】 大鼠经口530。 【性状】 无色或白色晶体,有特殊气味。 【溶解情况】 溶于乙醇、乙醚、氯仿、甘油、二硫化碳等。 【用途】 用于制染料合成树脂、塑料、合成纤维和农药、水杨酸等。作外科消毒剂消毒能力大小的标准(石炭酸系数)。 【制备或来源】 由煤焦油经分馏,由苯磺酸经碱熔。由氯苯经水解,由异丙苯经氧化重排。 【其他】 加热至65℃时能溶于水(在室温下,在水中的溶解度是9.3g,当温度高于65℃时能与水混溶),有毒,具有腐蚀性如不慎滴落到皮肤上应马上用酒精(乙醇)清洗,在空气中易被氧化而变粉红色。在民间有土方用石炭酸来治皮肤顽疾,以毒攻毒,如用来治脚底起泡。
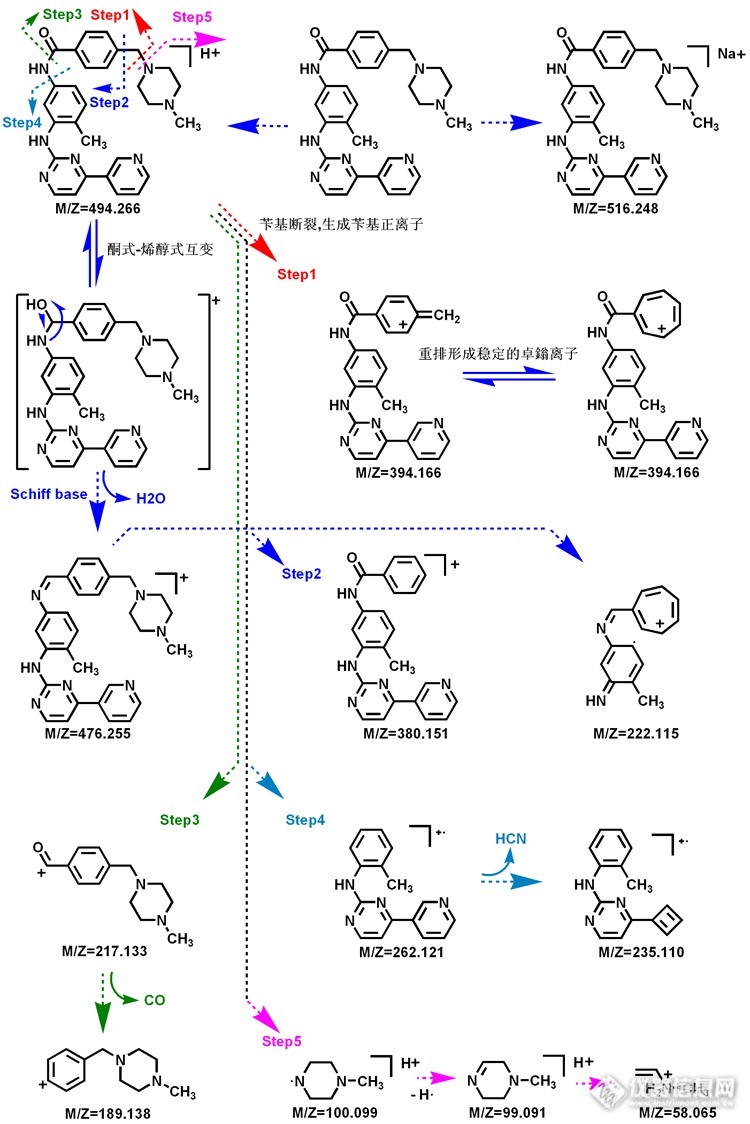
氟马替尼和伊马替尼皆为靶向治疗药物,伊马替尼(原称STI571)是一种治疗普通种类癌症的药物。其甲磺酸盐目前由诺华公司在市面上销售,在中国商品名称“格列卫”。它被用于治疗慢性粒细胞性白血病(CML),胃肠道间质瘤(胃肠道间质瘤)和其他一些疾病。到2011年,该药已被FDA批准用于治疗10个不同的癌症。对于慢性粒细胞白血病,酪氨酸激酶ABL被锁定在其活化形式。它导致慢性粒细胞白血病的异常表型为:过度增殖和白细胞计数高。伊马替尼可与酪氨酸激酶活性位置结合,并阻止其活动。甲磺酸氟马替尼是江苏豪森药业股份有限公司组织多家单位研究开发的氨基嘧啶类化合物甲磺酸氟马替尼是针对Bcr-abl设计的格列卫的结构修饰药物。药理实验显示疗效明显优于imatinib(格列卫),目前的数据支持甲磺酸氟马替尼进入临床进一步试验。本临床研究已得到中国食品药品监督管理局的批准并已被伦理委员会审阅通过。伦理委员会将保证所有参与者的权利得到保护。质谱图是某质谱解析爱好朋友提供的,觉得这个稍微难一点,所以很提人胃口,所以解析起来可能更有点意思!!!氟马替尼质谱图(ESI+):http://ng1.17img.cn/bbsfiles/images/2014/09/201409261650_515869_2359621_3.jpg氟马替尼可能的质谱裂解途径:http://ng1.17img.cn/bbsfiles/images/2014/09/201409261649_515868_2359621_3.png 氟马替尼分子量为562,质子化产物为563,585为其加钠峰,545碎片离子为脱水峰,结构中的酮式会与烯醇式互变,经过氢重排脱水,523与准分子离子相差40为脱去两分子的HF而生成,503为在523的基础上再失去一分子HF生成,基峰为463是与脂肪胺相连的苯环上苄基断裂,同时电荷转移,七元环的卓鎓离子更具有稳定性个人认为脂肪环上的N原子的碱性强一点所以其具有较强的质子亲和力,所以质子化发生位置可能就是在脂肪环的N原子上,除了苄基的断裂还有一种断裂方式就是与苯环相连的C-C键的断裂,从而得到449的碎片离子,423碎片离子是463碎片离子失去两分子的HF而生成的,285为酰胺键断裂电荷转移,由此推断可能质子化位置在酰胺N原子上,277亦为酰胺键断裂只不过正电荷定域在左侧,C-N键断裂会得到263的离子,由于游离基中心的诱导 该离子再失去氢自由基得到262的碎片离子,嘧啶与吡啶相连的氨基经过H重排发生1.3-键断裂,后得到173的碎片离子,58,99,100的离子均来自N脂肪环,C-N键断裂,失去氢自由基,以及开环所生成。依马替尼质谱图(ESI+):http://ng1.17img.cn/bbsfiles/images/2014/09/201409261651_515870_2359621_3.jpg依马替尼可能的质谱裂解途径:http://ng1.17img.cn/bbsfiles/images/2014/09/201409261659_515871_2359621_3.png伊马替尼在结构上与氟马替尼的差异不大,毕竟氟马替尼是伊马替尼的结构修饰药,所以结构上比伊马替尼在苯环上多了三氟甲基取代基,另外则是甲基吡啶环变成甲基苯环,伊马替尼分子量为493,准分子离子加氢峰为494,准分子离子加钠峰为516,离子都具有很高的丰度,476为烯醇互变引起脱水得到的,这个过程与氟马替尼一致,394为苄基断裂,380为与苯环相连的C-C键的断裂得到的 ,262为与苯环相连酰胺键的CN键断裂生成的离子,217为酰胺键断裂电荷转移得到的,后失去CO中性分子得到189碎片离子,222为酰胺键断裂,以及苄基断裂生成卓鎓的离子,235为262失去HCN得到,低质量端为含氮脂肪环产生的离子。注:参加原创不是目的,目的是和各位质谱解析爱好者,更深入、广泛的交流学习,分享自己的心得,同时认识到自己的不足!