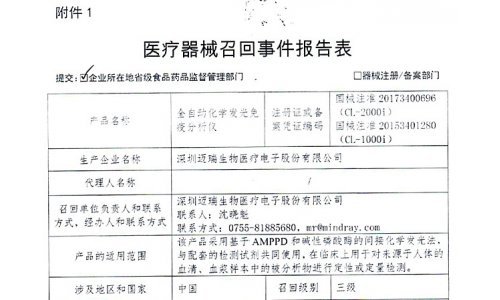
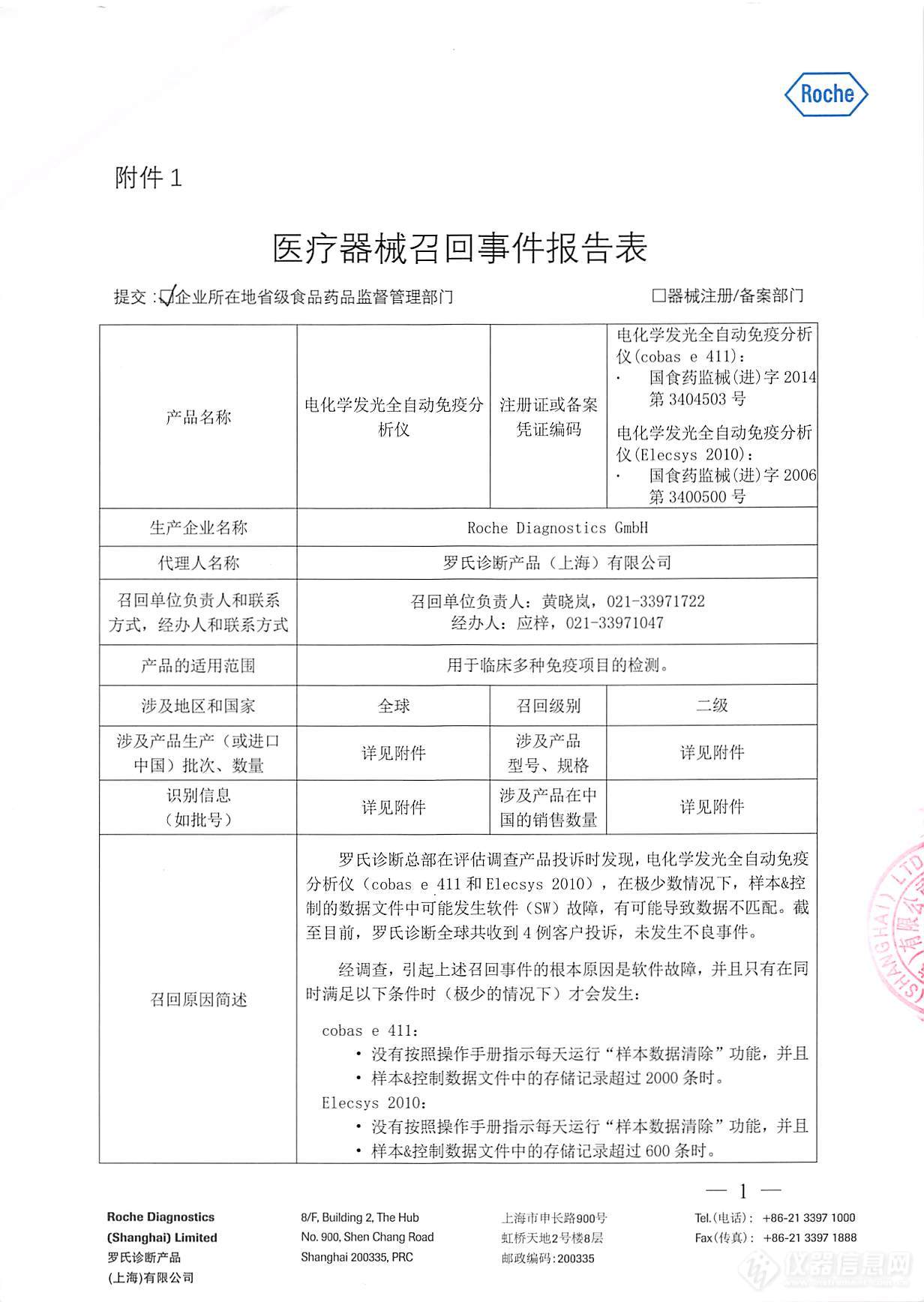
格力美国大召回:质量堪忧
1、格力遭美国合作伙伴诉讼,进行历史上规模最大的产品召回 2、产品质量频出及空调出口乏力致国际化战略生变 3、而除湿器召回的背后,亦显示出格力电器多元化的困境,小家电短板显现。 如果搜索“董明珠+国际化”,可以得到几十万条董明珠关于企业国际化的各种阐释。如今,这个一直把格力质量挂在嘴边的女强人,不得不一边召回那些在美国质量不过硬的除湿器,一边应对美国合作方的诉讼。 今年6月发生的格力电器北美除湿机安全隐患事件再度发酵,格力电器13日晚间发布公告,称将从美国和加拿大市场召回约225万台除湿机产品。 这是中国公司迄今为止在北美市场最大的召回事件。 而除湿器美国召回的背后,亦显示出格力电器多元化的困境,小家电短板显现。 “打脸”的召回 一向自诩技术领先的格力在美国却大规模暴露出产品质量问题。 日前,美国消费品安全委员会要求格力电器召回除湿机的消息让格力电器紧急停牌。 据美国消费品安全委员会发布召回公告,要求召回格力电器生产的225万台除湿机召回,因为这些机器可能过热并冒烟起火,从而对消费者构成火灾和烧伤威胁。 上述公告称,截止目前美国消费品安全委员会已收到与此问题相关的165起事故报告,包括46起火灾,造成了215万美元的财产损失,不过并未造成人员伤亡。 当天,格力紧急停牌并发布召回公告,预计召回将对公司造成一定损失,但对今年经营业绩不会有实质性影响。 格力看似主动的召回,事实上是迫于压力。 今年6月20日,格力美国分公司的另一股东Soleus公司将格力电器告上加州联邦法院,并提出1.5亿美元的高额索赔。Soleus公司的诉讼词称:“在得知其生产的一款除湿器存在品质缺陷容易着火问题后,格力电器不但没有立即召回处理,反而要求Soleus公司进行隐瞒。” Soleus公司还称,将此事报告给美国政府后,遭到格力电器的报复。 Soleus称,格力公司企图与大客户Sears百货公司解约。格力美国与Sears公司在2011年12月签署了一项销售金额达1.5亿美元的合约,根据合约,Sears公司将在2012-2015年期间向格力美国公司购买空调和除湿器产品。 “格里电器从未威胁、打压任何合作伙伴。”对此,格力方面仅有这样简单的一句回应。 中金公司研报认为,此次除湿机质量问题,一方面导致可能面临巨大的损失,另一方面令格力品牌在北美市场受损害。2011年,格力设立美国销售公司,希望在发达国家能够拓展自有品牌,而本次事件是格力全球化过程中的一次小挫折。 瑞银证券研报则认为,格力电器此次召回的产品售价从100美元至400美元不等,若假设均价为150美元,则总召回金额约3.3亿美元。但由于很多产品已经使用较久,且产品单价不高,预计实际召回比例不到一半,召回金额将不到10亿元人民币。 不过,不容忽视的是,今年7月初,格力电器总工程师黄辉以及工程师出身的副总裁庄培先后减持格力股票16万股和25万股,分别套现433万元和652万元。而前董事长朱江洪在2012年5月卸任后减持912万股。有业内人士认为,格力技术高管减持套现说明了技术人员在公司的核心地位受到了动摇。 有业内人士甚至认为,目前出口占格力的份额越来越重,随着被CPSC强令召回产品,这将直接影响格力的品牌信誉,也直接影响产品在海外市场的销售。 格力2013年中报显示,截至今年6月30日,格力海外销售收入为103.97亿元(折合约17亿美元),同比增长11.9% 毛利率为13.48%,同比增长了2.46%。 国际化生变 1998年,格力品牌在巴西各大超市登场,由此迈开格力海外发展的第一步。2001年,格力的海外生产之路也正式启航,在巴西玛瑙斯自由区投资3000万美元格力巴西生产基地正式竣工投产。此后,格力电器的海外触角进一步扩张,相继在南亚巴基斯坦、越南设立生产基地。 2012年3月16日,格力形象广告片在被称为“世界胡十字路口”的纽约时代广场的大屏幕上亮相。今年,格力电器首次对外发布了一份英文年报,希望全世界能够“读懂”自己。 格力公司的官网显示,格力的自主品牌已经进入了美国、法国、意大利、西班牙、菲律宾、澳大利亚、巴西、俄罗斯等100多个国家和地区,全球用户超过2亿。 作为中国家电企业之一,格力电器一系列的举动意味着其在国际化道路上煞费苦心。 尽管格力在自己官网上骄傲地宣称,世界上每3台空调中就有一台是格力造,但频繁被曝出产品质量出现问题,加之近年以来,空调出口市场乏力,没有增长表现,让以空调为主打的格力在国际化进程逐渐生变。 格力在今年早前就选择退出越南合资公司。 格力越南生产基地于2008年竣工并投产,是其在东盟的第一家、海外第三家空调生产基地。格力空调1999年以出口方式进入越南市场后,迅速获得了当地的市场份额,地处热带的越南市场对空调的硬性需求丰富,而新兴市场国家的人工成本大大低于发达国家水平,这正是催生格力将空调生产本地化的主要驱动力。 越南格力电器股份有限公司于2008年初在越南平阳成立,注册资本为越南盾500亿元(据2008年年报当期约合31.25万美元),以现金出资和技术作价出资计占总股本的20%。同年增资后比例增至31.25%,由于拥有原始股表决权比例为33.75%。在当年的年报中对该公司使用了 “运营良好”这样的积极描述。 但在2009年年报中该公司应收帐款数额则大幅上升。2010年公司资不抵债计提坏账准备47.15万,此时格力已不参与越南公司的生产经营和管理。 “以前格力电器国际化倾向选择人工成本较低的地区,未来主要考虑选择有硬性市场需求并且法制健全的国家”,董明珠在股东大会上曾承认格力电器己经从越南合资公司撤股,“当初的投资己经收回,没有造成重大损失”。 格力确认由于越南资方的不诚信,公司已经完全退出越南合资公司,但越南市场的出货量未受到影响。 格力电器称在未来二到三年中坚持出口自主品牌的道路,美国销售公司主要销售自主品牌,2012年销售额上亿美元。 但格力电器的全球化之路在美国却走的并不顺利。至少在靓丽广告屏的背后,格力电器不得不面对的无奈现实却是:格力美国公司自2010年合资成立至今,在美国市场还没有一款产品是冠以“格力”的品牌。 格力的短板 而这次被指隐瞒质量的产品正是格力的小家电。据悉,格力小家电原是格力集团下属企业,不属于格力电器。由于其品牌形象对格力空调造成影响,后注入格力电器,由格力电器管理。 据媒体报道,格力电器董事长兼总裁董明珠曾在去年股东大会现场表示,接下来格力旗下的小家电产品将全部统一使用“大松”品牌,但目前净水机、空气净化器、抽湿机均使用格力品牌。而收购回来的晶弘冰箱使用“晶弘”品牌。 业内人士指出,格力在小家电领域刚起步,在技术方面缺乏核心竞争力,同时,格力涉足小家电领域主要通过并购,后续整合直接关系到小家电业务的成败。目前,格力的成功建立在对空调的专业化经营基础上,欠缺多元化经营的经验。 格力电器半年报显示,今年上半年,公司总营收528.9亿元,其中空调的营收占了绝对的份额,收入468.2亿元,占比97.54%,毛利率达到了29.15%,同比增长5.40%。而小家电业务营业收入为7.16亿元,同比下降了8.88%,毛利率为15.00%,同比下滑7.93%。 而其竞争对手美的集团董事长方洪波曾向媒体表示,美的很多小家电毛利率超30%~40%,但有20多个种类亏损,目前正推进战略转型关停部分,效果将在2013年体现。不久前,美的集团将利润率高的小家电业务注入上市公司,目前已完成重组。 中金公司研报认为,格力的小家电品牌形象一直同格力空调不匹配。 从专业化到多元化,目前来看,格力小家电的短板尚需补齐,于国际化而言亦需如此。