原子和分子性质[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=15190]原子和分子性质[/url][color=#dc143c]电子书,书名信息都不全,而且只有第一章……如果有可能,希望能补全,谢谢。--handsomeland[/color]
分子光谱与分子结构 第一卷 双原子分子光谱[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=14616]分子光谱与分子结构 第一卷 双原子分子光谱[/url]
原子光谱和分子光谱的区别
[多选]吸光原子与其他气体分子或原子碰撞会引起?A温度升高B谱线变宽C谱线强度下降D吸收峰的频率增大E吸收峰的波长发生位移
分子光谱与分子结构 第二卷 多原子分子的红外光谱与喇曼光谱[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=14617]分子光谱与分子结构 第二卷 多原子分子的红外光谱与喇曼光谱[/url]
我最近正在做关于分子构象的实验。文献中采用了NOESY或者ROESY得到的谱图数据,再将分子中一直的两个氢原子距离当作标准来进行计算。得到所有空间相近的氢原子的距离。不知道有没有高手知道从谱图数据到得到距离的数据需要通过什么方法? 如何实现?
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=51341]原子和分子光谱学.pdf[/url]
[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]与分子吸收光谱有何区别
某化合物分子中含有一个氯原子和二个溴原子,其质谱图上的M;M+2 M+4 M+6?
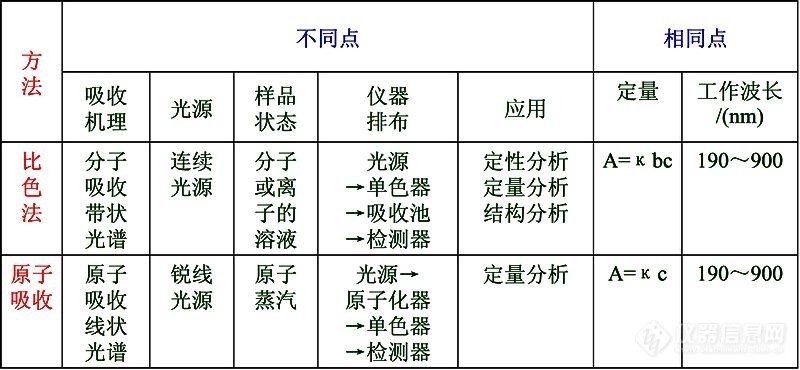
[b][color=#cc0000]来点专业的,分子光谱分析法与原子光谱分析法的区别!呵呵![/color][/b][img=,690,319]https://ng1.17img.cn/bbsfiles/images/2021/11/202111262027594060_7729_1841897_3.jpg!w690x319.jpg[/img]
分子间形成氢键后氢原子的化学位移有何变化,如何进行快速正确的归属
哪位高手有根据高分辨质谱的准确值模拟分子原子组成的软件?
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=19666]《原子与分子光谱导论》-北大王国文教授的经典之作[/url][img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=19667]《原子与分子光谱导论》-北大王国文教授的经典之作[/url]请下载的同志注意,两部分一定要下完整,不然不能解压。
[color=#333333]可以解释一下为什么原子光谱为线光谱,分子光谱为带光谱[/color]
[b][color=#cc0000]科普一下,分子光谱分析法与原子光谱分析法的区别![/color][/b][img=,690,319]https://ng1.17img.cn/bbsfiles/images/2021/11/202111262027594060_7729_1841897_3.jpg!w690x319.jpg[/img]
请问各位:为什么[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]用锐线光源,而分子光度分析要用连续光谱,不能用锐线光源?谢谢!! [em55]
分子的极性简介 如果分子中所有的化学键都是非极性的,那么价电子就被键合原子相等地共用。因而,在分子中电子是呈对称均匀分布的。这种均匀分布的发生与化学键的数目和它们在空间的伸展方向无关。具有这种特性的分子叫做非极性分子。如H2,Cl2,N2,O2等。像HCl和HBr这类双原子分子只有一对电子形成化学键,并且是极性键。其电子云分布是不对称、不均衡的,被叫做极性分子。如果分子含有多个极性键,从分子的整体来看,它可能是极性的,也可能是非极性的,这取决于分子中化学键的空间排布。如果分子中的极性键都相同,从分子的极性的总体来说,它只取决于化学键的空间排布。以上的看法可以从用带静电荷的棒来靠近细水流及四氯化碳流所发生的现象来证实,细的水流受到吸引而四氯化碳流不受影响。可以说明水分子是极性分子,而四氯化碳分子尽管是由4个极性键构成但因为其排布均匀,就其总体来说是非极性分子,具有类似结构的还有CH4、C2H6等。水分子的极性应归因于其弯曲的结构,而四氯化碳分子是正四面体结构,如下页图:二氧化碳分子的非极性则是由于它的直线型结构,锥形的氨分子是极性的。下面我们就极性键和极性分子的性质进一步做一些探讨。氯化氢分子是极性分子,而且是电偶极子(即把氯化氢分子看成是由数值相等而符号相反的彼此间有一定距离的一对电荷所组成的体系)。分子的极性是用它们的偶极矩μ来定量地表征的。对双原子分子来说(这是比较简单而易于理解的例子),μ是电子电荷的数值e与正负电荷“重心”间距离l的乘积。l值称为偶极长度:μ=el因为l是和分子大小(10-10m)为同一量度单位,而电子的电荷是1.602×10-19C(库仑),所以偶极矩μ的数量级将为10-29Cm。偶极矩越大,分子的极性越强。分子偶极矩的数值,在实验中是根据分子在电场中行为的研究来测定的。这样所得到的数值可以用于计算化合物中原子的有效电荷。例如,从实验测得HCl分子的偶极矩值等于0.35×10-29Cm,而用物理方法可以测得该分子中H—Cl的核间距为1.27×10-10m[或0.127nm(纳米)]。如果假设该分子中的键是离子型的,那么每一个离子(H+和Cl-)电荷的绝对值应等于1.602×10-19C,在这种情况下该分子的偶极矩应等于:1.602×10-19×1.27×10-10=2.02×10-29(Cm)但实际上,实验测得的偶极矩是0.35×10-29Cm,即为100%离这正与HCl分子中原子的有效电荷等于+0.17和-0.17(以电子电荷与单位)相符。知道了偶极矩的数值,也可以算出偶极长度,即正负电荷重心之间的距离(l),即通过上述计算,我们对离子键、共价键、极性(共价)键的理解就更加深刻了。应该说在离子键形成的化合物和共价键形成的化合物之间,并不存在截然明显的分界线。处于中间过渡的键的情况,大多是既具有典型共价键的性质也具有典型离子键的性质,或者也可以说具有部分离子性的共价键。关于极性分子所组成物质的性质和非极性分子所组成物质的性质也是不一样的。相邻的极性分子趋向于以偶极子的不同极相互确定指向,这时它们之间产生了静电吸引力。其结果之一就是使极性分子趋向于缔合。由极性分子组成的液体的另一特性是具有很强的使其它物质电离的作用,也就是当该液体与溶质相互作用时,具有生成溶剂化离子的能力。例如当氯化氢溶于水时,形成水合离子。但是,氯化氢在非极性的苯中所形成的溶液就不能导电,这就证明溶液中没有离子存在。
与原子的质量计量一样,分子的质量计量也先后存在3个量名称:相对分子质量、分子质量和分子量。众所周知,分子的质量为组成分子的各原子的质量之合。在日常专业工作中,不论是单质还是化合物,它们的分子质量都是根据各元素原子的个数和各元素的“相对原子质量”(由元素周期表上查到)计算得到。既然元素的相对原子质量是一个单位为“1”的相对质量,那么由此计算得到的分子质量必然也是一个单位为“1”的相对质量。对于某些结构复杂的生物大分子,往往都是通过电泳、离心或色谱分析等方法测得其近似分子质量,因而更是一个相对概念的量值。所以,我们过去长期习惯使用着的“分子量”实际上都是相对的分子质量。因此,国标指出“以前称为分子量”的即是“相对分子质量”(relative molecular mass),并将后者定义为“物质的分子或特定单元的平均质量与核素12C原子质量的1/12之比”。相对分子质量是两个质量之比,也在计算表达形式上进一步明确了“相对”的含义。对于定义中的“特定单元”,主要是指空气等组成成分基本不变的特殊混合物,它们的相对质量可根据其组成成分(N2,O2,CO2,Ar等)的相对分子质量和其在空气中的体积分数计算其平均质量,然后与 12C原子质量的1/12相比即可获得。相对分子质量的量符号为Mr,单位为“1”。 对于过去长期使用的“分子量”,其英文为molecular weight,确切原意为“分子重量”。它既不是质量概念,又没有相对的含意,因而也是一个不够准确和不够科学的量名称。根据国标规定,“分子量”应停止使用,凡过去使用“分子量”的场合都应换以使用“相对分子质量”。另外,过去一直以“Dalton”、“D”和“kD”作为分子量的单位,后来也曾有人提出以“u”作为分子量的单位,这些都是不恰当的用法。相对分子质量的单位只能是“1”,而不是“Dalton”,“D”,“kD”或“u”。 至于分子质量,国标中仅给出了一个量符号m,其单位为“kg”和“u”。从理论上说,分子质量应是一个与“原子质量”对应的绝对意义的质量。但在现实中,这样的“分子质量”几乎是不可能得到的,而且在实际工作中也不可能接触和使用它。
[center]如何区分分子量、分子质量和相对分子质量 与原子的质量计量一样,分子的质量计量也先后存在3个量名称:相对分子质量、分子质量和分子量。众所周知,分子的质量为组成分子的各原子的质量之和。在日常专业工作中,不论是单质还是化合物,它们的分子质量都是根据各元素原子的个数和各元素的“相对原子质量”(由元素周期表上查到)计算得到。既然元素的相对原子质量是一个单位为“1”的相对质量,那么由此计算得到的分子质量必然也是一个单位为“1”的相对质量。对于某些结构复杂的生物大分子,往往都是通过电泳、离心或色谱分析等方法测得其近似分子质量,因而更是一个相对概念的量值。所以,我们过去长期习惯使用着的“分子量”实际上都是相对的分子质量。因此,国标指出“以前称为分子量”的即是“相对分子质量”(relative molecular mass),并将后者定义为“物质的分子或特定单元的平均质量与核素12C原子质量的1/12之比”。相对分子质量是两个质量之比,也在计算表达形式上进一步明确了“相对”的含义。对于定义中的“特定单元”,主要是指空气等组成成分基本不变的特殊混合物,它们的相对质量可根据其组成成分(N2,O2,CO2,Ar等)的相对分子质量和其在空气中的体积分数计算其平均质量,然后与12C原子质量的1/12相比即可获得。相对分子质量的量符号为Mr.,单位为“1”。 对于过去长期使用的“分子量”,其英文为molecular weight,确切原意为“分子重量”。它既不是质量概念,又没有相对的含意,因而也是一个不够准确和不够科学的量名称。根据国标规定,“分子量”应停止使用,凡过去使用“分子量”的场合都应换以使用“相对分子质量”。另外,过去一直以“Dalton”、“D”和“kD”作为分子量的单位,后来也曾有人提出以“u”作为分子量的单位,这些都是不恰当的用法。相对分子质量的单位只能是“1”,而不是“Dalton”,“D”,“kD”或“u”。 至于分子质量,国标中仅给出了一个量符号m,其单位为“kg”和“u”。从理论上说,分子质量应是一个与“原子质量”对应的绝对意义的质量。但在现实中,这样的“分子质量”几乎是不可能得到的,而且在实际工作中也不可能接触和使用它。因此,我们可以不必花费精力去研究它。[/center]
氢原子光谱的分析 误差氢原子光谱的分析实验的误差分子
[color=#444444]一个分子结构式是R2C=CR2,R中的杂原子有两个个N和一个O.高度对称的分子,理论分子量在916,可是质谱(ESI 和 Maldi-TOF)都没有做出分子离子峰,请问各位大虾有什么高见?是不是高度对称的分子不容易出峰?有相关文献吗?[/color]
为什么原子光谱是线状光谱,而分子光谱是带状光谱?如题。
元素形成单质或化合物时,在邻近两个或多个原子之间的,主要的、强烈的相互作用叫化学键。一般来说,活泼金属和活泼非金属以离子键相结合。离子键没有方向性和饱和性。由离子键形成的化合物称离子化合物。在离子化合物中还可能存在共价键。当非金属形成化合物或单质时,通常以共价键结合(除惰性气体单原子分子外)。共价键是靠共用电子对形成的化学键,具有方向性和饱和性。分子中只含有共价键的化合物称共价化合物。
吴学周,物理化学家,中国分子光谱研究的奠基人之一和化学科学研究的卓越组织者。他为中国分子光谱研究和化学科学研究的发展贡献了毕生的 精力;他服从建设需要,投身工业基地,组织研究队伍,培养了几代科学研究人才;他在学术上的成就是对多原子分子的电子光谱和分子结构进行了开拓性研究,在振动光谱的应用研究、反应动力学研究和电化学研究中也有建树。
本公司近期准备购进原子吸收光谱仪一台主要是为了测药品,食品中的重金属请高人指点下哪个牌子的好,优势在哪里?价格以及到货周期怎么样?万分感谢
[size=4][font=黑体]简介:量子调控研究是国家中长期科技发展战略规划的重要内容。近日,中科院物理所纳米物理与器件实验室高鸿钧研究组与谢心澄研究员及英国利物浦大学Werner A. Hofer教授合作在单分子自旋态的量子调控研究中取得新进展[/font][/size]量子调控研究是国家中长期科技发展战略规划的重要内容。近日,中科院物理所纳米物理与器件实验室高鸿钧研究组与谢心澄研究员及英国利物浦大学Werner A. Hofer教授合作在单分子自旋态的量子调控研究中取得新进展。他们发现在酞菁铁分子Kondo效应中由于分子中心铁原子在金属表面的吸附位置不同对Kondo效应产生很大影响。相关研究结果发表在9月7日出版的《物理评论快报》(Phys. Rev. Lett. 99, 106402 (2007))上。这是首次报道吸附位置对单分子Kondo效应的调控作用,为单分子自旋态的量子调控及其在量子信息中应用研究提供了新思路。 Kondo效应是指磁性杂质中的局域自旋与自由电子强关联相互作用所引起的一系列低温反常现象。近年来,扫描隧道显微镜技术的迅速发展使人们能够精确地测量单个磁性原子或分子在金属表面上的Kondo效应,而在原子尺度上探索影响Kondo效应的因素是实现单分子自旋态量子调控的关键。 物理所高鸿钧研究组利用低温扫描隧道显微镜及扫描隧道谱,在对吸附在金表面的磁性分子酞菁铁的测量中,发现了Kondo温度高于室温的Kondo效应,并发现分子中心铁原子在金表面的吸附位置对Kondo效应影响很大。他们发现酞菁铁分子在金表面存在两种吸附取向,虽然在分子中心测量的扫描隧道谱显示两种分子取向都存在Kondo效应,但是彼此却存在很大差别。这种差别主要表现在两个方面:根据Fano理论拟合的Kondo温度,以及扫描隧道谱在费米面附近的线型。第一性原理计算及实验测量表明,两种取向的分子的中心铁原子吸附在金表面的不同位置:第一种分子取向,铁原子吸附在金表面两金原子之间的桥位置;第二种分子取向,铁原子吸附在金表面金原子的正上方。他们的理论分析表明,分子中心铁原子在金表面的吸附位置不仅影响到局域自旋与自由电子耦合相互作用的强弱,而且还会影响扫描隧道谱测量中隧穿电子的通道。 近年来,高鸿钧领导的研究组对纳米功能结构材料的调控生长、机制与物性等进行了系列研究(如:Phys. Rev. Lett. 97, 246101 (2006);97, 156105 (2006);96, 226101 (2006);96, 156102 (2006);Adv. Func. Mater. 17, 770 (2007))。根据该工作观察到的吸附位置对单分子Kondo效应,他们提出了调控单分子自旋量子态的可能途径:1)通过基底上不同位置或不同基底的物理化学性质(如:Phys. Rev. Lett. 97, 156105 (2006));2)通过调节纳米分子体系中非功能性侧链(如:Phys. Rev. Lett. 96, 226101 (2006))。这对量子调控和量子信息研究具有重要意义。 以上工作得到了国家自然科学基金委、国家科技部和中国科学院的资助。
[em0705] 现在正在学习拉曼理论的知识,看到GF矩阵方法来计算分子的振动频率时可能需要用编程来计算,不知哪位老师有好的程序?(我想用理论数值与观察值比较下) 如果文献上查不到某种物质的拉曼频移,大家是如何分析这种物质是不是你所要的东西呢? 希望各位老师给我点意见 谢谢!
[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]观察的是构成物质的元素(或曰原子)中的电子在原子轨道中的跃迁;而紫外可见光吸收观察的是构成物质的分子中的电子在分子轨道中的跃迁。两者有所同,有所不同。定量分析的原则同,而测量所需的光能量不同:[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]为X光,能量大,可激发电子从低的原子轨道向高的原子轨道跃迁;而紫外可见吸收为紫外光及可见光,能量小,只能激发电子从分子轨道向最低(或次低)的空的分子轨道跃迁。
[align=center][size=18px][color=#000000]原子发射光谱(ICP/AES)理论知识——自吸自蚀[/color][/size][/align][align=center][size=18px][color=#000000][/color][/size][/align][b][size=18px]谱线的自吸和自蚀[/size][size=18px]等离子体[/size][/b][size=18px]:以气态形式存在的包含分子、离子、电子等粒子的整体电中性集合体。等离子体内温度和原子浓度的分布不均匀,中间的温度、激发态原子浓度高,边缘反之。宏观上是中性的电离的气体,称为等离子体。[/size][b][size=18px]自吸[/size][/b][size=18px]:由弧焰中心发射出来的辐射光,被外围的基态原子所吸收,从而降低了谱线的强度。此现象叫自吸。[/size][size=18px] I = I[sub]0[/sub]e[sup]-ad[/sup][/size][size=18px][font=Calibri][size=14px] I[/size][/font][/size][sub][font=Calibri][size=14px]0[/size][/font][/sub][font=Calibri][size=14px][font=宋体]为弧焰中心发射的谱线强度,[/font][/size]a[font=宋体][size=18px]为吸收系数,[/size][/font]d[font=宋体][size=18px]为弧层厚度。[/size][/font][/font][b][size=18px]自蚀[/size][/b][size=18px]:元素浓度低时,不出现自吸。随浓度增加,自吸严重时,中心部分的谱线 将被吸收很多,从而使原来的一条谱线分裂成两条谱线,这个现象叫自蚀 。[/size][size=18px]在谱线上,常用r表示自吸,R表示自蚀。在共振线上,自吸严重时谱线变宽, 称为共振变宽[/size]
粒子和原子的区别