Cytek推出1管 16色 NK 细胞免疫分型方案,助您全面分析NK细胞表型!
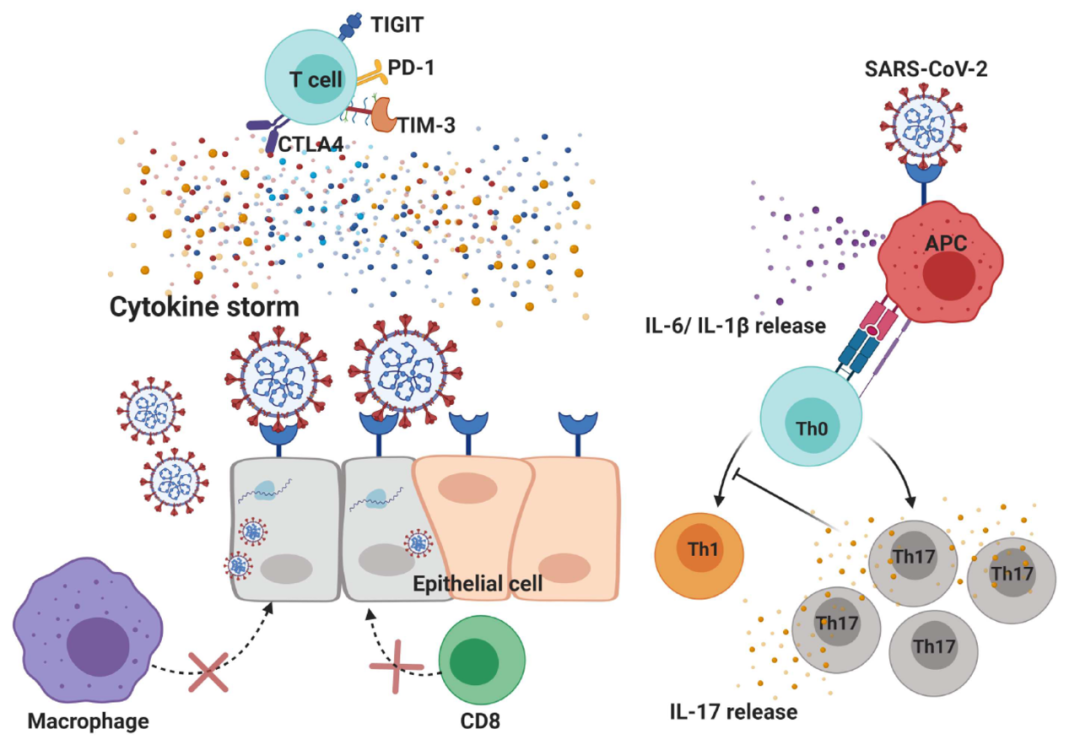
自然杀伤细胞(Natural Killer, NK)是先天淋巴细胞的亚群之一,但缺少抗原特异性。NK细胞的效应功能和靶细胞的识别是由对NK细胞表面受体的激活和抑制来平衡调节的,这些表面受体可以区分“自身”抗原、“改变的自身”抗原和“缺失的或非自身”抗原,因此,在消灭异常细胞的同时,可以避免攻击正常的细胞。1-3(图1)图1 – NK细胞识别自身/缺失的/非自身抗原细胞示意图NK细胞在抗肿瘤和抗病毒反应中起关键作用4-6。目前,各种转化研究和临床试验正在利用NK细胞独特的信号通路及其强大的抗肿瘤活性,通过多种手段比如CAR-NK细胞,来治疗血液和实体肿瘤。6研究显示,NK细胞表达的NK细胞受体和其他标记物种类繁多,因此,高参数流式细胞术对于全面的NK细胞表型分析是很有必要的。考虑到越来越多的NK细胞研究需求,Cytek推出了一款 16色 (18标记)NK 细胞免疫分型试剂,该试剂可在3激光以上配置的Cytek® 全光谱流式细胞分析系统上使用,仅需一管样本,研究者即可方便快捷的对人NK细胞免疫表型进行全面深入的分析。(图2)图2- Cytek® 16色人NK细胞免疫分型试剂Cytek® 16色人NK细胞免疫分型方案可识别和表征三种主要的人类NK细胞亚群:早期NK细胞(CD16- CD56bright),成熟NK细胞(CD16+CD56dim)和晚期NK细胞(CD16+CD56-),并支持对这三种NK细胞亚群的成熟和激活状态、迁移潜力、以及NK细胞表面的激活和抑制受体的表达进行分析。此外,该方案还可分析更多NK亚群,如CD226-CD56dim NK细胞,及CD57+CD56dimCD16+ NK细胞7-11。(图3)图3- 不同状态下的NK细胞示意图Cytek® 16色 NK 细胞免疫分型方案是一款预优化的试剂组合产品,避免了耗时的、耗费劳动力的、且昂贵的方案设计与优化。该方案详细的试剂组成请参考下表1。同时,方案经过系列测试,证实可以很好兼容人外周血单个核细胞(Peripheral Blood Mononuclear Cells, PBMCs)样本和EDTA采集管收集的血液样本。表1:Cytek® 16色NK细胞免疫分型方案(P/N R7-40011)的组成。方案可添加ViaDye&trade Red Fixable Viability Dye Kit (P/N R7-60008)作为死活染料。Cytek® 16色 NK 细胞免疫分型方案识别NK细胞及其激活状态的数据分析设门策略如下图4所示,依次进行单细胞门和非红细胞(non-RBC)设门后,通过进行谱系(CD14、CD19、CD123)阴性、CD3-、淋巴细胞、及HLA-DR-CD127- 系列设门,识别出NK细胞。利用CD56和CD16绘制二维点图,以确定三种主要的NK细胞亚群:早期NK细胞(CD16- CD56bright),成熟NK细胞(CD16+CD56dim)和晚期NK细胞(CD16+CD56-)。在代表总NK细胞群的密度图中,显示了各个NK细胞标记 vs. CD56,以及CD159a vs. CD159c 的表达情况。(图4)图4- 使用Cytek® 16色NK细胞免疫分型方案数据分析设门策略。数据来自于EDTA管收集的健康供者的全血样本。Cytek 还提供以下工具来进一步优化您的实验室工作流程,提高工作效率: &bull 完整的样品制备、染色和获取操作流程 &bull 实验及分析模板参考文献:Arachchige, A.S.P.M. (2021) Human NK cells: From development to effector functions. Innate Immunity 27(3): 212-229.Sivori, S., et al. (2019) Human NK cells: surface receptors, inhibitory checkpoints, and translational applications. Cellular & Molecular Immunology 16: 430-441.Kumar, V., McNerney, M. A new self: MHC-class-I-independent Natural-killer-cell self-tolerance. Nat Rev Immunol 5, 363–374 (2005). https://doi.org/10.1038/nri1603Bjö rkströ m, N.K., et al. (2022) Natural killer cells in antiviral immunity. Nature Reviews Immunology 22: 112-123. Cooper, M.A., et al. (2001) The biology of human natural killer-cell subsets. Trends Immunol. 22(11): 633-640.Ghaedrahmati, F., et al. (2023) Targeting immune checkpoints: how to use natural killer cells for fighting against solid tumors. Cancer Commun. 43(2): 177-213Stannard, K.A., et al. (2019) Human peripheral blood DNAM-1neg NK cells are a terminally differentiated subset with limited effector functions. Blood Adv. 3(11): 1681-1694.Lopez-Vergès, S., et al. (2010) CD57 defines a functionally distinct population of mature NK cells in the human CD56dimCD16+ NK cell subset. Blood 116(19): 3865-3874.Martinet, L.A., et al. (2015) DNAM-1 expression marks an alternative program of NK cell maturation. Cell Rep. 11: 85-97.Kurioka, A., et al. (2018) CD161 Defines a functionally distinct subset of pro-inflammatory natural killer cells. Front. Immunol. 9: 486Bjö rkströ m, Niklas K., Hans-Gustaf Ljunggren, and Johan K. Sandberg. "CD56 negative NK cells: origin, function, and role in chronic viral disease." Trends in immunology 31.11 (2010): 401-406.