对于一些被测的试验电压,被测的试验过程中,被测电压高近100kV,试验过程较长,不包括逐渐升压过程,无击穿后就得5min,往往升压过程中也有被击穿的试品,即整个试验过程中又频频伴有击穿和放电现象,此时普通的数字电压表易损坏。此时能否用模拟式(电工仪表型)电压表能接于RC分压器后测量高电压,避免数字电压表易损坏。
[align=center][b][size=14pt]WITec共聚焦拉曼快检技术在单细胞表型及生物医学领域的前沿应用[/size][/b][/align][align=center][size=11pt]会议时间[/size][size=11pt]:[/size][size=11pt]2020年[/size][size=11pt]4[/size][size=11pt]月[/size][size=11pt]2[/size][size=11pt][font=等线]日[/font]1[/size][size=11pt]0[/size][size=11pt]:00[/size][/align][b][size=12pt]内容[/size][size=12pt]介绍:[/size][/b][size=10.5pt]德国[/size][size=10.5pt]WITec的高分辨率、高灵敏度、共聚焦快速拉曼成像系统能够实现多种成像技术联用以满足客户的多样化、个性化需求,广泛应用于材料、地质及生命科学等领域。[/size][size=10.5pt]本次会议将带来上海氘峰医疗科技有限公司针对单细胞表型的拉曼数据分享以及德国[/size][size=10.5pt]WITec公司共聚焦拉曼快速成像在生物医学领域的前沿应用,欢迎关注![/size][b][size=12pt]讲师[/size][size=12pt]介绍:[/size][size=11pt]罗艳君[/size][size=11pt]:[/size][/b][size=11pt][font=等线]上海氘峰医疗科技有限公司总经理,负责公司曰常运营及市场销售。硕士期间师从于单细胞拉曼技术的前沿研究者黄巍教授(现为牛津大学工程系教授,主要研究方向:合成生物学、单细胞拉[/font][font=等线]曼)。氘峰致力于单细胞拉曼技术在生物医学领域的推广和应用,提供专业的第三方单细胞拉曼表型数据解决方案,服务于生医领域科学家。[/font][/size][b][size=11pt]胡海龙[/size][size=11pt]:博士[/size][/b][size=11pt]:[/size][size=11pt][font=等线]毕业于新加坡南洋理工大学物理系。[/font]2005起年在吉林大学超分子结构与材料国家重点实验室攻读硕士学位,主要研究半导体纳米材料的表面增强拉曼效应。2008起在南洋理工大学攻读博士学位,研究方向涉及近场拉曼光谱,针尖增强拉曼光谱及金属表面等离子体光学等多领域,工作先后在Nano Letter, ACS Nano与Nanoscale等杂志发表。同时与高校及科研机构展开广泛合作,共同发表文章超过15篇。2013年度荣获中国自费留学生优秀奖(新加坡区) ,同年加入德国WITec公司,现负责中国区应用技术支持[/size][size=11pt]。[/size][size=10.5pt]报名地址[/size][size=10.5pt]:[/size][url=https://www.instrument.com.cn/webinar/meeting_12843.html][u][color=#0000ff]https://www.instrument.com.cn/webinar/meeting_12843.html[/color][/u][/url]
[size=4](一)药物代谢的遗传多态性[/size][size=4]由于肝脏药酶系特别是P450的遗传多态性,以致造成药物代谢的个体差异,这影响了药物的药理作用、不良反应和致癌的易感性等。对某些药代谢的缺陷者称为:弱代谢者(poor metabolizer)或PM-表型1,而强代谢者(extensive metabolizer)称为EM-表型。在第一相中的药物代谢多态性以异喹胍和乙妥英为例,分别为P450UD6和P4502C的变异。对异喹胍的羟化作用有遗传性缺陷的个体,在应用β-受体拮抗剂、三环类抗郁剂、某些膜抑制抗心律紊乱药、抗高血压药和钙离子拮抗剂等,由于药物代谢的异常,使药效增强、时间延长,容易发生不良反应。在第二相反应的药物代谢多态性,以异烟肼和磺胺二甲嘧啶为例,可区分为乙酰化快型和慢型两种,慢型乙酰化个体长期服用肼苯达嗪和普鲁卡因酰胺后可产生红斑狼疮综合征,服异烟肼后易发生周围神经病变(表2-4)。P4501A1,P4501A2是芳香碳氢化合物羟化酶,激活某些致癌原,其遗传变异与某些癌的易患性有关。[/size][align=center][size=4]表2-4 遗传多态性与药物代谢[/size][/align][table][tr][td=1,1,126][size=4]代谢途径[/size][/td][td=1,1,158][size=4]药物举例[/size][/td][td=1,1,142][size=4]人群中的频率(%)[/size][/td][td=1,1,142][size=4]酶[/size][/td][/tr][tr][td=1,1,126][size=4]C-氧化[/size][/td][td=1,1,158][size=4]异喹胍,金雀花碱,右旋甲吗喃,阿片类[/size][/td][td=1,1,142][size=4]白种人5-10[/size][/td][td=1,1,142][size=4]CYP4502D6[/size][/td][/tr][tr][td=1,1,126][size=4]C-氧化[/size][/td][td=1,1,158][size=4]β-肾上腺受体拮抗剂,乙妥英,甲苯巴比士[/size][/td][td=1,1,142][size=4]白种人4[/size][/td][td=1,1,142][size=4]CYP4502C[/size][/td][/tr][tr][td=1,1,126][size=4]乙酰化[/size][/td][td=1,1,158][size=4]环已巴比土,异烟肼,磺胺二甲嘧啶,咖啡因[/size][/td][td=1,1,142][size=4]日本人10[/size][/td][td=1,1,142][size=4]N-乙酰基转移酶白种人30-70[/size][/td][/tr][/table]
该文该文汇总了单细胞代谢的研究方法,包括质谱 (MS),质谱成像( MS imaging), 毛细管电泳(CE)(其中主要是chip ce), 光谱学(optical spectroscopy),和荧光生物传感器等多种技术手段分析了几百个单细胞,对单细胞进行大分子层面上的表征,以此阐述细胞代谢的表型异质性(phenotypic heteroge-neity)。大概就这个意思吧,大牛的东西,读起来反正就是半懂不懂。
[align=left][color=#333333]9月30日,全国电磁计量技术委员会发布了《JJF1245电能表型式评价大纲》征求意见稿,并面向社会各计量机构及相关人员征求意见。[/color][/align][align=left][color=#333333] 《安装式交流电能表型式评价大纲 有功电能表》[/color][/align][align=left][color=#333333] 《安装式交流电能表型式评价大纲》参照国际建议OIML R46和国家标准GB/T 17215系列编制而成。[/color][/align][align=left][color=#333333] 本系列大纲替代原系列大纲JJF1245-2010,与原大纲相比,主要变化如下:采用新的框架结构:不再采用通用要求-特殊要求的结构。以国际建议OIML R46为主,增加国家标准GB/T 17215系列的相关内容。JJF 1245.1和JJF 1245.2基本对应了OIML R46的内容 JJF 1245.3参照了国家标准中无功电能表计量和技术要求的内容,按照JJF 1245.1的架构编写 JJF 1245.4按照JJF 1245.1和JJF 1245.3未涉及但国家标准包含的计量和技术要求以及安全相关要求的内容编写 JJF 1245.5基本上在原大纲JJF 1245.6-2010的基础上修订。[/color][/align][align=left][color=#333333] 增加了软件要求:JJF 1245.2参照国际建议OIML R46计量性能保护章节的内容,结合我国电能表的管理要求和技术特点对电能表提出软件要求,并给出验证方法 增加和修改了大量计量和技术要求:增加了耐久性、高次谐波、差模电流干扰、电流快速变化、振铃波等项目,修改了电压和电流谐波、恒定磁场、射频电磁场辐射、电压暂降和短时中断、振动、阳光辐射、防水等试验项目。[/color][/align][align=left][color=#333333] 本大纲引用了JJF 1001 通用计量术语及定义 JJF 1015 计量器具型式评价通用规范 JJF 1245.2-2018 安装式交流电能表型式评价大纲 软件要求 JJF 1245.4-2018 安装式交流电能表型式评价大纲 特殊要求和安全要求 JJF 1245.5-2018 安装式交流电能表型式评价大纲 功能要求 GB/T 2423.1-2008 电工电子产品环境试验第2部分:试验方法试验A:低温 GB/T 2423.2-2008 电工电子产品环境试验第2部分:试验方法试验B:高温 GB/T 2423.3-2016 电工电子产品环境试验第2部分:试验方法 试验CaB:恒定湿热试验 GB/T 2423.4-2008 电工电子产品环境试验第2部分:试验方法试验Db:交变湿热(12h+12h循环)等文件。[/color][/align][align=left][color=#333333] 《安装式交流电能表型式评价大纲 有功电能表》适用于频率为50Hz或60Hz单、三相安装式有功电能表(以下简称仪表)的型式评价。[/color][/align][align=left][color=#333333] 本大纲不适用于标称电压超过600V(多相仪表为线对中线电压)的仪表、用于连接电子式互感器的仪表、用于连接低压电流传感器的仪表、携带式仪表、仪表寄存器的数据接口及标准表。(更多详情请见附件)。[/color][/align][align=left][color=#333333] 《安装式交流电能表型式评价大纲 无功电能表》[/color][/align][align=left][color=#333333] 本部分是关于无功电能表型式评价的方法标准,其内容参照GB/T 17215.323-2008《交流电测量设备 特殊要求 第23部分:静止式无功电能表(2级和3级)》、GB/T 17215.324-2017《交流电测量设备 特殊要求 第24部分:静止式基波频率无功电能表 (0.5S级、1S级和1级)》、GB/T 15282-94《无功电度表》的标准要求,按照国际建议OIML R46框架编制而成。[/color][/align][align=left][color=#333333] 本大纲引用了JJF 1001 通用计量术语及定义 JJF 1015 计量器具型式评价通用规范 JJF 1245.1-2018 安装式交流电能表型式评价大纲 有功电能表 JJF 1245.2-2018 安装式交流电能表型式评价大纲 软件要求 JJF 1245.4-2018 安装式交流电能表型式评价大纲 特殊要求和安全要求 JJF 1245.5-2018 安装式交流电能表型式评价大纲 功能要求 GB/T 2423.1-2008 电工电子产品环境试验第2部分:试验方法试验A:低温 GB/T 2423.2-2008 电工电子产品环境试验第2部分:试验方法试验B:高温 GB/T 2423.3-2016 电工电子产品环境试验第2部分:试验方法 试验CaB:恒定湿热试验 GB/T 2423.4-2008 电工电子产品环境试验第2部分:试验方法试验Db:交变湿热(12h+12h循环)等。[/color][/align][align=left][color=#333333] 《安装式交流电能表型式评价大纲 无功电能表》适用于频率为50Hz或60Hz单、三相安装式无功电能表(以下简称仪表)的型式评价。[/color][/align][align=left][color=#333333] 本大纲不适用于标称电压超过600V(多相仪表为线对中线电压)的仪表、用于连接电子式互感器的仪表、用于连接低压电流传感器的仪表、携带式仪表、仪表寄存器的数据接口及标准表。(更多详情请见附件)。[/color][/align]附件下载:[color=#004499][url=http://www.jlck.cn/files/file/2018/10/8/810568.docx]JJF 1245.1 安装式交流电能表型式评价大纲 有功电能表[/url][/color][color=#004499][url=http://www.jlck.cn/files/file/2018/10/8/8105738.docx]JJF 1245.4 安装式交流电能表型式评价大纲 特殊要求与安全要求[/url][/color][color=#004499][url=http://www.jlck.cn/files/file/2018/10/8/8105757.doc]JJF+1245.2 安装式交流电能表型式评价大纲 软件要求[/url][/color][color=#004499][url=http://www.jlck.cn/files/file/2018/10/8/8105826.doc]JJF+1245.5 安装式交流电能表型式评价大纲 功能要求[/url][/color][color=#004499][url=http://www.jlck.cn/files/file/2018/10/8/8105844.docx]型评大纲修改意见表格(空)[/url][/color][color=#004499][url=http://www.jlck.cn/files/file/2018/10/8/8142827.docx]JJF 1245.3 安装式交流电能表型式评价大纲 无功电能表[/url][/color]
[color=#444444][b]全国流量计量技术委员会液体流量分委会[/b][/color][color=#444444] 关于对国家计量技术规范《热量表检定规程》和《热量表型式评价大纲》征求意见的通知[/color][color=#444444] 附件是《热量表检定规程》和《热量表型式评价大纲》和意见回执表,请提出宝贵意见(请填写在意见表中),于2019年1月12日将意见表发回联系人!(无意见按无意见反馈)。 [/color][color=#444444]意见请分别反馈至邮箱:[/color][color=#444444]qiup@nim.ac.cn (热量表检定规程)[/color][color=#444444]jinzhj@nim.ac.cn (热量表型式评价大纲)[/color][color=#444444]或者 秘书处 yangyt@bjjl.cn[/color][color=#444444]附件下载:[/color][color=#444444]《热量表检定规程征求意见稿》、编制说明及征求意见表[/color][color=#444444]《热量表型式评价大纲征求意见稿》、编制说明及征求意见表[/color][color=#444444]全国流量计量技术委员会液体流量分技术委员会秘书处[/color][color=#444444]2018年10月11日[/color]
按照国家质量监督检验检疫总局“关于授权建立国家电能表型式评价实验室(电力)的通知”(国质检量函496号),国家电网计量中心从2010年7月26日起正式获得“国家电能表型式评价实验室(电力)”的授权。 国家电网计量中心成为国家行政管理部门认可的电力行业首家电能表型式评价授权计量技术机构,有利于合理、合法、公平、公正地开展计量检测工作,更好地服务党和国家工作大局、服务电力客户、服务发电企业、服务社会发展。 国家电网计量中心作为国家电网公司系统最高计量技术机构,将秉承“行为公正、方法科学、数据准确、服务规范”的质量方针,认真贯彻落实国家计量法律法规,自觉接受政府监督管理,充分发挥行业引领作用,不断提高科研和试验能力,拓展服务领域,提升管理水平,推进计量技术创新和计量标准化建设,为我国电力计量事业的发展做出更大贡献。
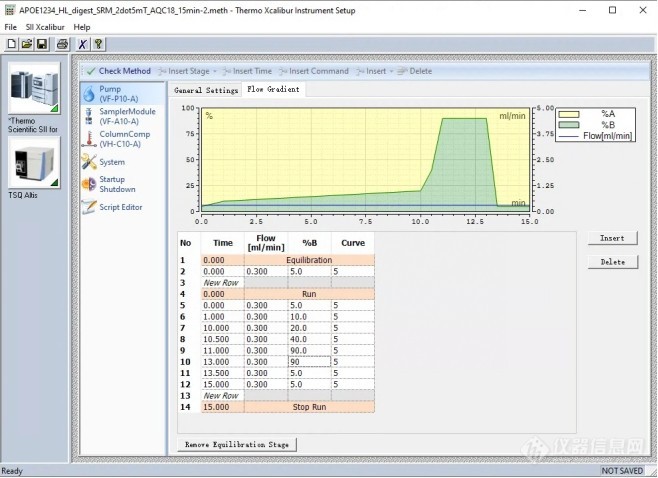
[align=center][b][font=宋体][font=Times New Roman]APOE[/font][font=宋体](载脂蛋白[/font][font=Times New Roman]E[/font][font=宋体])不同表型分型[/font][/font][/b][/align][b][font=宋体]背景[/font][/b][font=宋体][font=宋体]载脂蛋白E([/font][font=Times New Roman]apolipoprotein E, ApoE[/font][font=宋体])作为脂质转运蛋白和低密度脂蛋白受体的主要配体,在胆固醇代谢和心血管疾病中发挥重要作用。[/font][font=Times New Roman]ApoE[/font][font=宋体]有多种异构体,即 [/font][font=Times New Roman]ApoE2[/font][font=宋体]、 [/font][font=Times New Roman]ApoE3 [/font][font=宋体]和 [/font][font=Times New Roman]ApoE4[/font][font=宋体],分别由[/font][font=Times New Roman]APOE[/font][font=宋体]的等位基因 ε[/font][font=Times New Roman]2[/font][font=宋体],ε[/font][font=Times New Roman]3 [/font][font=宋体]和ε[/font][font=Times New Roman]4[/font][font=宋体]来编码;[/font][/font][font=宋体][font=Times New Roman]APOE4[/font][font=宋体]等位基因是阿尔茨海默病的主要危险因素,血清[/font][font=Times New Roman]ApoE[/font][font=宋体]增高与心血管疾病死亡率增加有关,而降低则与[/font][font=Times New Roman]AD[/font][font=宋体]相关死亡率增加有关;[/font][/font][font=宋体][font=宋体]这些研究发现是基于免疫法,如免疫透射比浊法。但基于免疫法的[/font][font=Times New Roman]apoE[/font][font=宋体]的研究数据差异较大;而基于[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱法([/font][font=Times New Roman][url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS[/font][font=宋体])的研究数据一致程度较高;[/font][/font][font=宋体][font=Times New Roman][url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS[/font][font=宋体]在定义被分析物和抗干扰方面具有优势,且在血清载脂蛋白的绝对定量上已有较为成熟的应用。[/font][/font][b][font=宋体]实验方法[/font][font=宋体][font=Arial]1[/font][/font][font=Arial].[font=宋体]样品制备[/font][/font][font=宋体][font=Times New Roman]1.1 APOE[/font][font=宋体]混合轻标[/font][font=Times New Roman]mix[/font][font=宋体]线性[/font][font=Times New Roman]1[/font][font=宋体]溶液配制:[/font][/font][/b][font=宋体][font=宋体]稀释剂:[/font][font=Times New Roman]0.1%SDC[/font][font=宋体]作为稀释剂[/font][/font][font=宋体][font=宋体]取浓度为[/font][font=Times New Roman]10 ng/[/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]的[/font][font=Times New Roman]APOE1234[/font][font=宋体]各轻标肽段溶液[/font][font=Times New Roman]10 [/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]至于离心管中(共[/font][font=Times New Roman]40 [/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]),再加入[/font][font=Times New Roman]10 [/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]稀释剂,混合成为[/font][font=Times New Roman]APOE[/font][font=宋体]混合轻标[/font][font=Times New Roman]mix[/font][font=宋体]线性溶液起始浓度最高点:[/font][font=Times New Roman]2 ng/[/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体],共[/font][font=Times New Roman]50 [/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体];[/font][/font][font=宋体][font=宋体]从[/font][font=Times New Roman]APOE[/font][font=宋体]混合轻标[/font][font=Times New Roman]mix[/font][font=宋体]线性溶液起始浓度[/font][font=Times New Roman]2 ng/[/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]继续往下梯度稀释,[/font][font=Times New Roman]2000 pg/[/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]、[/font][font=Times New Roman]1000 pg/[/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]、[/font][font=Times New Roman]500 pg/[/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]、[/font][font=Times New Roman]200 pg/[/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]、[/font][font=Times New Roman]100 pg/[/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]、[/font][font=Times New Roman]50 pg/[/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]、[/font][font=Times New Roman]20 pg/[/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体],以上[/font][font=Times New Roman]7[/font][font=宋体]各浓度点作为[/font][font=Times New Roman]APOE[/font][font=宋体]混合轻标[/font][font=Times New Roman]mix[/font][font=宋体]线性[/font][font=Times New Roman]1[/font][font=宋体];[/font][/font][b][font=宋体][font=Times New Roman]1.2 APOE[/font][font=宋体]混合重标[/font][font=Times New Roman]mix[/font][font=宋体]溶液配制:[/font][/font][/b][font=宋体][font=宋体]取浓度为[/font][font=Times New Roman]10 ng/[/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]的[/font][font=Times New Roman]APOE1234[/font][font=宋体]各重标肽段溶液[/font][font=Times New Roman]10 [/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]至于离心管中(共[/font][font=Times New Roman]50 [/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]),再加入[/font][font=Times New Roman]50 [/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]稀释剂,混合成为[/font][font=Times New Roman]APOE[/font][font=宋体]混合重标浓度最高点:[/font][font=Times New Roman]1 ng/[/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体],共[/font][font=Times New Roman]100 [/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体];[/font][/font][font=宋体][font=宋体]将[/font][font=Times New Roman]APOE[/font][font=宋体]混合重标浓度最高点稀释[/font][font=Times New Roman]10[/font][font=宋体]倍至终浓度为[/font][font=Times New Roman]200 pg/[/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]作为混合重标[/font][font=Times New Roman]mix[/font][font=宋体],共[/font][font=Times New Roman]500 [/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体];[/font][/font][b][font=宋体][font=Times New Roman]1.3 [/font][font=宋体]配制[/font][font=Times New Roman]APOE[/font][font=宋体]混合线性标曲梯度:[/font][/font][/b][font=宋体][font=宋体]稀释剂:[/font][font=Times New Roman]0.1%SDC[/font][font=宋体]作为稀释剂[/font][/font][font=宋体][font=宋体]取[/font][font=Times New Roman]APOE[/font][font=宋体]混合轻标[/font][font=Times New Roman]mix[/font][font=宋体]线性[/font][font=Times New Roman]1[/font][font=宋体]各浓度点[/font][font=Times New Roman]10 [/font][font=宋体]μ[/font][font=Times New Roman]L+[/font][font=宋体]混合重标[/font][font=Times New Roman]mix10 [/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体],加入[/font][font=Times New Roman]40 [/font][font=宋体]μ[/font][font=Times New Roman]L[/font][font=宋体]稀释剂,涡旋混匀,总体积为[/font][font=Times New Roman]60 μL[/font][font=宋体];[/font][/font][b][font=宋体][font=Times New Roman]2[/font][/font][font='Times New Roman'] [/font][font=宋体]仪器方法[/font][font='Times New Roman']2.1 [/font][font=宋体]质谱检测[/font][font=宋体]条件[/font][/b][font=宋体][font=Arial]Column:[/font][/font][font=宋体][font=Arial]ChromCore AQ C18 1.8 [/font][font=宋体]μ[/font][font=Arial]m[/font][font=宋体],[/font][font=Arial]2.1[/font][font=宋体]×[/font][font=Arial]100 mm[/font][/font][font=宋体][font=Arial]Mobile Phase:[/font][/font][font=宋体][font=Arial]A) 0.1%FA-H2O[/font][/font][font=宋体][font=Arial]B) 0.1%FA-ACN[/font][/font][font=宋体][font=Arial]Gradient:[/font][/font][font=宋体][font=Arial]t (min)[/font][/font][font=宋体][font=Arial]%A[/font][/font][font=宋体][font=Arial]%B[/font][/font][font=宋体][font=Arial]0[/font][/font][font=宋体][font=Arial]95[/font][/font][font=宋体][font=Arial]5[/font][/font][font=宋体][font=Arial]1[/font][/font][font=宋体][font=Arial]90[/font][/font][font=宋体][font=Arial]10[/font][/font][font=宋体][font=Arial]10[/font][/font][font=宋体][font=Arial]80[/font][/font][font=宋体][font=Arial]20[/font][/font][font=宋体][font=Arial]10.5[/font][/font][font=宋体][font=Arial]60[/font][/font][font=宋体][font=Arial]40[/font][/font][font=宋体][font=Arial]11[/font][/font][font=宋体][font=Arial]10[/font][/font][font=宋体][font=Arial]90[/font][/font][font=宋体][font=Arial]13[/font][/font][font=宋体][font=Arial]10[/font][/font][font=宋体][font=Arial]90[/font][/font][font=宋体][font=Arial]13.5[/font][/font][font=宋体][font=Arial]95[/font][/font][font=宋体][font=Arial]5[/font][/font][font=宋体][font=Arial]15[/font][/font][font=宋体][font=Arial]95[/font][/font][font=宋体][font=Arial]5[/font][/font][font=宋体][font=Arial]Flow Rate:[/font][/font][font=宋体][font=Arial]0.3 mL/min[/font][/font][font=宋体][font=Arial]Temperature:[/font][/font][font=宋体][font=Arial]40 [/font][font=宋体]℃[/font][/font][font=宋体][font=Arial]Injection:[/font][/font][font=宋体][font=Arial]10 [/font][font=宋体]μ[/font][font=Arial]L[/font][/font][font=宋体][font=Arial]MS:[/font][/font][font=宋体][font=Arial]TSQ Altis[/font][font=宋体]三重四级杆质谱采用[/font][font=Arial]SRM[/font][font=宋体]模式进行检测,检测周期[/font][font=Arial]15 min[/font][font=宋体];[/font][/font][font=宋体][font=Arial]Sample: [/font][/font][font=宋体][font=Arial]APOE[/font][font=宋体](载脂蛋白[/font][font=Arial]E[/font][font=宋体])[/font][/font][b][font=宋体][font=Times New Roman]2.2 APOE[/font][font=宋体]标样检测条件[/font][/font][/b][img=,526,]https://ng1.17img.cn/bbsfiles/images/2023/02/202302081625152027_6822_3237657_3.jpg!w658x478.jpg[/img][b][font=宋体][font=Times New Roman]3 [/font][/font][font=宋体]实验结果[/font][/b][font=宋体] [/font][b][font=宋体][font=Times New Roman]3.1 APOE[/font][font=宋体]标样检测结果[/font][/font][/b][img=,552,]https://ng1.17img.cn/bbsfiles/images/2023/02/202302081625266439_6227_3237657_3.jpg!w690x380.jpg[/img][b][font=宋体][font=Times New Roman]3.2 APOE[/font][font=宋体]标样检测结果[/font][font=Times New Roman]-[/font][font=宋体]线性范围及内标重现性[/font][/font][/b][font=Calibri] [/font][img=,553,]https://ng1.17img.cn/bbsfiles/images/2023/02/202302081625429789_7475_3237657_3.jpg!w690x312.jpg[/img][b][font=宋体][font=Times New Roman]3.3 [/font][font=宋体]实际样品检测结果[/font][/font][/b][img=,552,]https://ng1.17img.cn/bbsfiles/images/2023/02/202302081625543206_6217_3237657_3.jpg!w690x318.jpg[/img][img=,553,]https://ng1.17img.cn/bbsfiles/images/2023/02/202302081626061074_8109_3237657_3.jpg!w690x317.jpg[/img][img=,553,]https://ng1.17img.cn/bbsfiles/images/2023/02/202302081626164568_1650_3237657_3.jpg!w690x269.jpg[/img][b][font=宋体][font=Times New Roman]4 [/font][font=宋体]讨论与总结[/font][/font][/b][font=宋体][font=宋体]简单地说,本研究使用了[/font][font=Times New Roman]APOE1/2/3/4[/font][font=宋体]作为定量肽段,绝对定量方法使用合成的同位素标记肽作为内标物,检测样品中目标肽段的浓度;[/font][/font][font=宋体][font=宋体]结果表明,本实验室优化的前处理方法可尽可能实现该类肽段的释放,回收率达到[/font][font=Times New Roman]50-60%[/font][font=宋体];[/font][/font][font=宋体][font=宋体]更重要的是,在实际样本的检测中,根据[/font][font=Times New Roman]APOE1/2/3/4[/font][font=宋体]四条肽段的出现情况,可以得出实际血浆提供者的[/font][font=Times New Roman]APOE[/font][font=宋体]基因型,此结果已经与基因检测结果进行核对,且成功率达到[/font][font=Times New Roman]100%[/font][font=宋体];[/font][/font][font=宋体] [/font][font=宋体][font=宋体]公司名称:[/font][/font][font=宋体][font=宋体]南京品生医疗科技有限公司[/font][/font][font=宋体][font=宋体]色谱柱信息:[/font][/font][font=宋体][font=Arial]ChromCore AQ C18 1.8[/font][font=宋体]μ[/font][font=Arial]m, 2.1[/font][font=宋体]×[/font][font=Arial]100mm[/font][/font]

[font=微软雅黑][font=微软雅黑][img=,690,151]https://ng1.17img.cn/bbsfiles/images/2020/08/202008232050021425_1822_2507958_3.jpg!w690x151.jpg[/img][/font][/font][font=微软雅黑][font=微软雅黑]代谢组学是基于蛋白质组学、基因组学发展起来的一门新学科,研究对象一般为分子量在[/font]1500以内的小分子代谢物。代谢组学反映了生物体内已经发生的事,因此是最接近于表型的组学。目前广泛用于代谢组学研究的有色谱质谱联用,核磁技术,但是代谢物的种类多,浓度差异大,高灵敏度以及高分辨率的仪器是最迫切的需求。[/font][font=微软雅黑][font=微软雅黑]近年来代谢组学逐渐成为热门的研究领域,仪器信息网将于[/font]2020年9月8日举办“代谢组学技术及应用新进展”研讨会,从代谢组学、脂质组学到靶向代谢、修饰代谢,为业内专家与相关领域研究者提供交流的机会。[/font][font=微软雅黑][font=微软雅黑]会议时间:[/font]2020年9月8日13:30-19:00[/font][font=微软雅黑][font=微软雅黑]会议安排:[/font][/font][img=,690,338]https://ng1.17img.cn/bbsfiles/images/2020/08/202008232049481021_1224_2507958_3.jpg!w690x338.jpg[/img][font=微软雅黑] [/font][font=微软雅黑][font=微软雅黑]报名地址:[url=https://www.instrument.com.cn/webinar/meetings/webinar2020metabolomics]点击打开链接[/url][/font][/font][font=微软雅黑][font=微软雅黑]欢迎报名参加![/font][/font]
代谢组学是继基因组学、转录组学及蛋白质组学之后发展起来的一门新兴组学,是整合包括色谱联用质谱和核磁共振等现代分析技术、生物化学以及生物信息学等学科的一门交叉学科技术,用于研究生命活动链条下游的代谢物内稳态情况。相比于其他组学,代谢组学反映生命体已经发生的生物学事件,因此能够更准确直接地反映生命体终端和表型信息。目前,广泛应用于代谢组学数据采集的技术平台有氢/碳核磁共振技术、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱技术、液相色谱-质谱技术、毛细管电泳-质谱技术以及直接进样质谱技术等。鉴于代谢物种类多样且浓度差异大,代谢组学研究需要依托高灵敏度、高分辨率的分析技术。仪器信息网将于[color=#ff0000][b]2021年8月12日[/b][/color]举办[b][color=#ff0000]“2021年代谢组学技术及应用新进展”网络研讨会[/color][/b],聚焦代谢组学的多个细分领域,如代谢组学基础研究、微生物代谢组学、代谢组学与中医药、药物开发代谢组学、疾病诊断与代谢组学等,从技术难点、数据分析到应用进行剖析,为业内专家与相关研究学者提供更灵活的交流机会,促进合作。[url=https://insevent.instrument.com.cn/t/iQ][img=,690,503]https://ng1.17img.cn/bbsfiles/images/2021/08/202108031734138217_4950_2507958_3.png!w690x503.jpg[/img][/url][size=18px][color=#ff0000][b][url=https://insevent.instrument.com.cn/t/iQ]点击报名,免费参会:https://insevent.instrument.com.cn/t/iQ[/url][/b][/color][/size]
代谢组学是继基因组学、转录组学及蛋白质组学之后发展起来的一门新兴组学,是整合包括色谱联用质谱和核磁共振等现代分析技术、生物化学以及生物信息学等学科的一门交叉学科技术,用于研究生命活动链条下游的代谢物内稳态情况。相比于其他组学,代谢组学反映生命体已经发生的生物学事件,因此能够更准确直接地反映生命体终端和表型信息。目前,广泛应用于代谢组学数据采集的技术平台有氢/碳核磁共振技术、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱技术、液相色谱-质谱技术、毛细管电泳-质谱技术以及直接进样质谱技术等。鉴于代谢物种类多样且浓度差异大,代谢组学研究需要依托高灵敏度、高分辨率的分析技术。仪器信息网将于[color=#ff0000][b]2021年8月12日[/b][/color]举办[b][color=#ff0000]“2021年代谢组学技术及应用新进展”网络研讨会[/color][/b],聚焦代谢组学的多个细分领域,如代谢组学基础研究、微生物代谢组学、代谢组学与中医药、药物开发代谢组学、疾病诊断与代谢组学等,从技术难点、数据分析到应用进行剖析,为业内专家与相关研究学者提供更灵活的交流机会,促进合作。[url=https://insevent.instrument.com.cn/t/iQ][img=,690,503]https://ng1.17img.cn/bbsfiles/images/2021/08/202108031734138217_4950_2507958_3.png!w690x503.jpg[/img][/url][size=18px][color=#ff0000][b][url=https://insevent.instrument.com.cn/t/iQ]点击报名,免费参会:https://insevent.instrument.com.cn/t/iQ[/url][/b][/color][/size]
代谢组学是继基因组学、转录组学及蛋白质组学之后发展起来的一门新兴组学,是整合包括色谱联用质谱和核磁共振等现代分析技术、生物化学以及生物信息学等学科的一门交叉学科技术,用于研究生命活动链条下游的代谢物内稳态情况。 相比于其他组学,代谢组学反映生命体已经发生的生物学事件,因此能够更准确直接地反映生命体终端和表型信息。目前,广泛应用于代谢组学数据采集的技术平台有氢/碳核磁共振技术、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱技术、液相色谱-质谱技术、毛细管电泳-质谱技术以及直接进样质谱技术等。鉴于代谢物种类多样且浓度差异大,代谢组学研究需要依托高灵敏度、高分辨率的分析技术。 仪器信息网将于[color=#ff0000][b]2021年8月12日[/b][/color]举办[b][color=#ff0000]“2021年代谢组学技术及应用新进展”网络研讨会[/color][/b],聚焦代谢组学的多个细分领域,如代谢组学基础研究、微生物代谢组学、代谢组学与中医药、药物开发代谢组学、疾病诊断与代谢组学等,从技术难点、数据分析到应用进行剖析,为业内专家与相关研究学者提供更灵活的交流机会,促进合作。[url=https://insevent.instrument.com.cn/t/iQ][img=,690,503]https://ng1.17img.cn/bbsfiles/images/2021/08/202108031734138217_4950_2507958_3.png!w690x503.jpg[/img][/url][size=18px][color=#ff0000][b][url=https://insevent.instrument.com.cn/t/nk]点击报名,免费参会:https://insevent.instrument.com.cn/t/iQ[/url][/b][/color][/size]

[url=https://www.instrument.com.cn/webinar/meetings/FlowRACS/][img=,690,350]https://ng1.17img.cn/bbsfiles/images/2021/12/202112281152512795_9049_2507958_3.jpg!w690x350.jpg[/img][/url] 世间生灵,均由单个细胞组合而成或者发育而来,因此,单个细胞,是生命的功能单元和进化单位。显然,在单个细胞精度的分析与操作,能够在最“深”的水平来理解、设计和改造各种生命体系。但是,面对瀚如星海的细胞世界,如何快速探测细胞的功能呢? 拉曼光谱是一种散射光谱,是化合物中分子键被激发到虚能态却尚未恢复到原始态所引起的、入射光被散射后频率发生变化的现象。我们提出,“拉曼组”(Ramanome)作为一种信息极为丰富的分子光谱,能够在单细胞精度,定量检测细胞代谢各种底物的速率、各种拉曼敏感产物之多样性及其含量、细胞的环境应激性、细胞之间的代谢互作、细胞内代谢物相互转化网络等广阔的细胞代谢表型,还可区分不同的物种。 因此,拉曼组是一种直接刻画“代谢功能”的单细胞表型组。而且,拉曼组手段具有广谱适用、活体、无损、非标记、全景式表型、可分辨复杂功能、快速、高通量、低成本、能耦合下游测序、质谱或培养等重要优势,与现有的单细胞基因组、转录组、蛋白组和代谢物组等手段具有互补性,共同形成一个完整的单细胞多组学方法学体系。 在[b]基金委国家重大科学仪器研制项目、科技部合成生物学重点研发计划[/b]等的支持下,我们研制成功基于拉曼组概念和拉曼分选(RACS)技术的“单细胞分析仪器系列”,包括临床单细胞拉曼药敏快检仪(CAST-R)、高通量流式拉曼分选仪(FlowRACS)、单细胞拉曼分选-测序耦合系统(RACS-Seq)、单细胞微液滴分选系统(EasySort Lego / Compact)等。利用这些原创仪器,我们打通了从单细胞代谢表型组表征到相对应高质量单细胞基因组测定的全流程,为单细胞多组学体系提供了一个全新的维度。 青岛星赛生物科技有限公司(www.singlecellbiotech.com),专注于单细胞维度医疗器械与科学仪器的研发、生产、销售及相关技术服务,基于上述单细胞分析仪器系列,竭诚为客户提供原创、定制化、一体化、全方位的“单细胞代谢表型组表征-分选-测序-培养”解决方案。[b][size=18px][color=#ff0000] 2021年12月30日[/color][/size][/b][size=18px],星赛生物将携年度重磅创新单品——[b]全球首台高通量流式拉曼分选仪FlowRACS[/b]来袭![/size] 立足拉曼组/元拉曼组,依赖于微流控与AI技术,FlowRACS将为合成生物学、精准医学等领域带来重大突破。[b]产品真容、技术细节、精彩报告、有奖竞答[/b]……惊喜多多,不容错过。[size=24px][color=#ff0000][b][url=https://www.instrument.com.cn/webinar/meetings/FlowRACS/][img]https://simg.instrument.com.cn/bbs/images/brow/em17.gif[/img]点击参会![/url][/b][/color][/size]
1.前言 随着科学与技术的发展,新药研发的速度正在日益加快,使得新药安全性评价工作的压力也变得越来越大。在新药研究开发过程中,因为安全性问题而被淘汰的候选药物占相当大的比例。一旦潜在的药物分子通过了初步的生物学筛选过程,就应该尽量减少这些候选药物分子在产品研发过程中的流失,以免造成巨大的资金和时间的浪费。因此,人们努力寻找新的分析方法,以便从功效和安全性两方面使得先导化合物的筛选更有效,从而尽可能地减少这种浪费。目前的生物分析手段主要利用基因组和蛋白质组方法,分别从基因水平和细胞蛋白质表达水平上测量生物体系对药物的反应。这两种方法都较昂贵,且劳动强度较大,然而却可能是研究在不同水平上对生物异源物质的生物应答的有力工具。但是,基因组学和蛋白质组学都不能提供可以了解生物体中整体细胞功能的信息,因为两者都忽略了整体器官中动态的代谢状态。因此,Nicholson等人提出了一种基于核磁共振的新方法,叫做metabonomics,我们暂且称之为代谢组学,以便与由代谢物组(metabolome)衍生而来的metabolomics相区别。Metabolomics研究的是一个细胞或细胞类型中所有的小分子成分,而metabonomics则是通过分析生物体液和组织来对完整的生物体(而不是单个细胞)中随时间改变的代谢物进行检测、确定、定量和分类;然后将这些***代谢轨迹与病生理过程中的生物学事件关联起。从药物研究和毒理学评价的角度来看,基因组学方法是观察给药后基因表达的改变,主要采用基因芯片技术。然而,基因调节/表达与系统的整体功能之间的关系在目前还很不清楚,主要是因为决大部分DNA是非编码的,而编码蛋白质的基因不能孤立地发挥作用,而是需要与其邻近的基因和非编码DNA一起才能发挥其功能。正式由于这个原因,人们才发展了蛋白质组学。蛋白质组学方法可以对由给药或其它病生理过程引起的细胞蛋白质组成变化进行半定量的测量。蛋白质组方法所采用的技术主要包括双向凝胶电泳和质谱技术。与基因组方法相比,蛋白质组方法较慢,且劳动强度较大。需要强调的是,虽然这些方法能够在很大程度上揭示毒理学机理,并且给出与疾病相关的新的生物标记物,却很难将这些发现与经典的毒理学指标相关联。原因很简单,因为目前的技术和方法不能对给药后反应的整个进程进行测量,也不能对生物整体的应答进行测量。因此需要发展一种新的方法来实时给出多器官生物整体的在体信息。基于NMR的代谢组学(metabonomics)方法可以满足这样的要求。2.Metabonomics在药物毒理学研究中的应用 代谢组学的目的是要扩展和补充由基因组学和蛋白质组学方法得到的对生物异源物质应答的信息。其任务是定量测量生物体对病生理刺激或基因改变的动态多参数代谢反应,是研究药物毒性和基因功能的技术平台。这个概念是根据Nicholson小组近二十年来利用1H NMR技术研究生物体液、细胞和组织中多组分代谢组成的工作而提出的。在这些研究中,还利用了模式识别,专家系统和相关的生物信息学工具。在许多情况下,药物通过与遗传物质直接作用而产生毒性,或通过诱导系统合成与药物代谢有关的酶,从而产生有毒的产物。在这种情况下,用基因组和蛋白质组学方法来评价毒性是有用的。然而,在生物异源物质有可能只在药理学水平上产生作用,因而可能不会影响基因的调节和表达。再者,显著的毒理学效应可能与基因的改变和蛋白质的合成完全不相关。因此,在许多情况下,从基因组和蛋白质组角度考虑到的反应可能不能预测药物毒性。但是,所有的由药物引起的病生理紊乱都会由于直接的化学反应,或通过与控制代谢的酶或核酸相结合而引起内源生化物质在比例、浓度、代谢通量等方面的失调。如果这种变化足够大的话,就会影响整个生物体的功能。生物体液中的代谢物是与细胞和组织中的代谢物处于动态平衡,因此,生物体中由于中毒或代谢损害而引起的细胞功能异常一定会反映在生物体液成分的变化中。要检测血浆、尿液、胆汁等生物基质中的一些具有特殊意义的微量物质,选择合适的分析方法致关重要。高分辨1H NMR波谱就非常适合用来检测生物体液中的成分异常,因为该方法可以同时对所有的代谢物进行定量分析,而且不需要样品前期准备,对任何成分一样灵敏。虽然也可以采用如质谱等其它方法,但对不同成分离子化程度的差别会影响定量和检测的可靠性。NMR方法还可以有效地用来从组织萃取物或细胞悬液中找出异常的代谢物。还可以利用高分辨魔角旋转(HR-MAS)探头来检测完整组织中的代谢物组成。由1H NMR谱检测到的生物体液中的内源性代谢物模式完全依赖于动物体内的毒素的类型。每一种类型的毒物都会在生物体液中产生特征的内源代谢物浓度和模式变化,这种特征给我们提供了毒性作用的机理和毒性位置的信息。右图所示为一系列尿样的1H NMR谱图,是大鼠经不同的毒物处理后得到的。每一张谱图只需几分钟的时间,是非常有效的。可以看出,不同毒素引起的代谢物变化是有特征性的。因为几乎所有的代谢物都有其特征的NMR谱,因而可以作为毒物引起的代谢变化的指纹图谱。利用NMR方法,人们已经成功地发现了许多新的器官特异相关毒性的代谢标记物。作为分析生物化学技术,NMR正是在这种探索性的工作上具有优势。
[b][size=15px][color=#595959]健脾调肝饮(JPTGY)[/color][/size][/b][size=15px][color=#595959]具有[b]疏肝、理气、健脾、化痰[/b]的功效,长期临床实践发现其可[b]有效治疗肥胖[/b]。前期研究发现,JPTGY对肥胖患者的减肥效果令人满意,显著降低了患者的总胆固醇和甘油三酯水平,没有任何副作用。然而,由于中药制剂具有多途径和多靶点的特点,JPTGY治疗肥胖症的[b]机制尚不充分[/b]。[/color][/size] [size=15px][color=#595959]该研究旨在采用[b]高脂饮食(HFD)诱导的肥胖小鼠[/b]模型来评估[b]健脾调肝饮(JPTGY)的作用与肠道微生物群和粪便代谢变化之间的关系[/b]。[/color][/size] [align=center] [/align] [size=15px][color=#595959]通过HFD诱导C57BL/6小鼠建立肥胖动物模型。采用[b]脂质代谢的血清生化指标[/b]评价JPTGY在肥胖小鼠中的药效学。[/color][/size] [size=15px][color=#595959]通过16s rDNA基因序列结合基于[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-质谱([url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url])的[b]非靶向粪便代谢组学技术[/b],对对照组、HFD组和JPTGY暴露肥胖组的[b]粪便样本中的细菌群落和代谢产物[/b]进行了研究。[/color][/size] [align=center] [/align] [size=15px][color=#595959]JPTGY显著降低总胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白胆固醇(LDL-C)和高密度脂蛋白(HDL-C)。[/color][/size] [b][size=15px][color=#595959]JPTGY可以上调粪便微生物群的丰度和多样性[/color][/size][/b][size=15px][color=#595959],其特征是蛋白质细菌门较高。一致地,在属水平上,补充JPTGY诱导毛螺菌科NK4A136组、大肠杆菌、Turicibacter、梭状芽胞杆菌1和拟杆菌的富集,它们与14种关键的粪便代谢产物密切相关,对JPTGY治疗有反应。[/color][/size] [size=15px][color=#595959]代谢组学进一步分析表明,JPTGY对肥胖的治疗作用涉及亚油酸(LA)代谢途径、α-亚麻酸(ALA)代谢途径,甘油磷脂代谢途径、花生四烯酸(AA)代谢途径和嘧啶代谢途径,这暗示了JPTGY治疗肥胖的潜在机制。[/color][/size][font=mp-quote, -apple-system-font, BlinkMacSystemFont, &][size=15px][color=#595959][/color][/size][/font][size=15px][color=#595959][/color][/size][color=#3573b9]结论[/color][b][size=15px][color=#595959][/color][/size][/b][font=mp-quote, -apple-system-font, BlinkMacSystemFont, &][size=15px][color=#595959][/color][/size][/font] [b][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959]肥胖表型与肠道菌群和粪便代谢的联系揭示了JPTGY治疗高脂血症和肥胖的潜在因果关系[/color][/size][/b][size=15px][color=#595959]。[/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size]
[font=宋体][size=15px]类风湿性关节炎([font=&]Rheumatoid arthritis[/font],[font=&]RA[/font])是一种病因不明的自身免疫性疾病,其主要临床特征为关节的疼痛和肿胀,可导致持续性滑膜炎、全身性炎症反应及软骨和骨损伤,严重时甚至致残。目前临床上常用于治疗[font=&]RA[/font]的药物如甲氨蝶呤([font=&]MTX[/font])等,常导致高血压、胃溃疡等不良反应。近年来,中药方剂在世界范围内被广泛应用于[font=&]RA[/font]的治疗,为患者和临床医生提供了新的选择。[/size][/font] [font=宋体][size=15px][font=&]RA[/font]归属于中医的痹证,二妙散([font=&]TS[/font])、三妙丸([font=&]TW[/font])和四妙丸([font=&]FW[/font])是临床上治疗痹证的三种经典中药方剂[font=&](ESSF)[/font],这三种方剂目前已载入《中国药典》[font=&](2020[/font]年版[font=&])[/font],多用于治疗[font=&]RA[/font],具有广泛认可的治疗作用。然而,目前探讨其探讨其生物活性化合物或治疗机制的研究较少,且[font=&]ESSF[/font]由二妙散化裁而成,三种方剂的临床疗效未被单独考虑过,这极大地限制了[font=&]ESSF[/font]在临床实践中对不同严重程度[font=&]RA[/font]患者的灵活应用。因此,有必要系统地评价这三种单方治疗[font=&]RA[/font]的疗效,并探索其生物活性成分,其各自的治疗优势和具体的治疗机制,从而指导[font=&]ESSF[/font]的临床应用。[/size][/font] [font=宋体][size=15px]中医方证代谢组学([font=&]chinmedomics[/font])是一种基于方证关系精确评价中医疗效的新方法。它将代谢组学与中医血清药物化学相结合,在代谢表型水平上反映机体整体功能的变化,识别证型或疾病相关的生物标志物,据此来评估中药方剂的疗效,并探索证型的发生机制。中药血清药物化学的方法还可用来鉴别中药方剂在体内发挥一定作用的活性化合物,有助于阐明相关靶点和通路。[/size][/font] [font=宋体][size=15px]作者推测[font=&]ESSF[/font]可能通过影响花生四烯酸代谢途径和嘌呤代谢途径来达到对[font=&]RA[/font]的治疗效果。作者利用分子对接技术预测了[font=&]ESSF[/font]中生物活性化合物的潜在靶点,发现具有抗炎和抗组织损伤特性的生物活性化合物,如黄柏碱、棕榈碱、苍术内酯[font=&]III[/font]、苍术内酯和小檗碱等,可以与[font=&]COX-2[/font]、[font=&]mPGES-1[/font]、[font=&]ALOX5[/font]和[font=&]XDH[/font]这些参与花生四烯酸代谢和嘧啶代谢途径的关键蛋白相结合。为了验证分子对接的结果,作者进行了[font=&]western blot[/font]和[font=&]q[url=https://insevent.instrument.com.cn/t/jp]PCR[/url][/font]检测。结果显示,[font=&]3[/font]个方剂都能不同程度地抑制[font=&]COX-2[/font]、[font=&]ALOX5[/font]、[font=&]mPGES-1[/font]和[font=&]XDH[/font]的表达,其中[font=&]FW[/font]的抑制效果最好,其次是[font=&]TW[/font],最后是[font=&]TS[/font]。[/size][/font] [size=15px][font=宋体]花生四烯酸和[font=&]5-HETE[/font]是花生四烯酸代谢途径中的关键物质,其表达异常是免疫功能紊乱、发热、炎症、疼痛的主要原因。花生四烯酸最终通过环氧化酶[font=&]2(COX-2)[/font]的作用产生前列腺素[font=&]2(PGE2)[/font],前列腺素[font=&]E2[/font]合成酶[font=&](mPGES-1)[/font],在[font=&]RA[/font]发病过程中间接导致炎症反应、免疫损伤和骨损伤。同时,亚油酸代谢产生花生四烯酸,花生四烯酸在白三烯[font=&]A4[/font]水解酶[font=&](LTA4H)[/font]和花生四烯酸脂氧合酶[font=&]5(ALOX5)[/font]的催化下生成白三烯[font=&]B4(LTB4)[/font]。[font=&]LTB4[/font]可以刺激白细胞,诱导白细胞介素[font=&](IL)[/font]和[font=&]TNF-[/font][/font][font=&]α[/font][font=宋体]的产生,从而引发[font=&]RA[/font]。此外,尿酸和单磷酸腺苷是嘌呤代谢途径中的关键物质。黄嘌呤脱氢酶[font=&](XDH)[/font]可催化次黄嘌呤氧化为黄嘌呤,再氧化为尿酸,当其含量增加时,可引起骨损伤、痛风、炎症等一系列与尿酸相关的症状。因此,[font=&]COX-2[/font]、[font=&]mPGES-1[/font]、[font=&]ALOX5[/font]和[font=&]XDH[/font]是抗炎和抗组织损伤的关键靶点。[font=&]ESSF[/font]中的生物活性化合物可以抑制[font=&]COX-2[/font]和[font=&]mPGES-1[/font]的活性,从而减少[font=&]PGE2[/font]的产生,还可以降低[font=&]ALOX5[/font]活性,减少[font=&]LTB4[/font]的产生,从而减少一系列炎症因子的产生,减轻[font=&]RA[/font]大鼠的炎症、免疫损伤和骨损伤症状。此外,这些生物活性化合物可以降低[font=&]XDH[/font]的活性,使尿酸的生成减少,从而缓解了[font=&]RA[/font]大鼠的骨损伤和疼痛。[/font][/size] [size=15px][font=宋体]总之,本研究证明了ESSF[/font][font=&][font=宋体]具有良好的缓解和治疗[/font]RA[font=宋体]的疗效。[/font]TS[font=宋体]主要用于清热消炎,适用于[/font]RA[font=宋体]的早期治疗,能快速减轻关节肿胀程度。[/font]TW[font=宋体]适用于关节消肿后免疫器官功能恢复,且适用于[/font]TS[font=宋体]治疗一段时间后使用。[/font]FW[font=宋体]对关节和骨损伤的恢复效果最好,可在[/font]RA[font=宋体]治疗末期使用。[/font]ESSF[font=宋体]治疗[/font]RA[font=宋体]的关键作用机制是降低花生四烯酸和嘌呤代谢途径中[/font]COX-2[font=宋体]、[/font]mPGES-1[font=宋体]、[/font]ALOX5[font=宋体]和[/font]XDH[font=宋体]的活性,从而达到抗炎、恢复免疫和骨关节功能的目的。这些发现对[/font]ESSF[font=宋体]的临床应用具有重要的指导意义。此外,这些治疗靶点的发现[/font][/font][font=宋体]也[/font][font=&][font=宋体]为今后[/font]RA[font=宋体]的靶向治疗提供了方向。[/font][/font][/size]
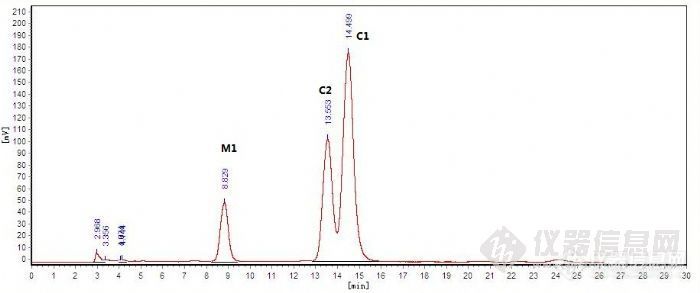
前言 代谢产物的鉴定在药物代谢研究过程中意义重大,如何准确地鉴定代谢产物的结构一直是广大药物代谢研究工作者致力攻克的难题。代谢产物的鉴定之所以难主要有以下几点原因:1.代谢产物在生物样品(血浆、尿液、胆汁、粪便等)中浓度极低。2.代谢产物容易受生物样品中内源性物质的干扰。3.代谢产物的不稳定性。4.仪器的灵敏度不够,等等。目前鉴定代谢产物的方式多为通过HPLC与质谱检测器进行联用推测代谢产物的结构,但该方法存在缺陷,如对同分异构体束手无策等。本实验前期通过专业的分离技术,得到某代谢产物M1,为重要的Ⅱ相代谢产物,该代谢产物因为量少(6mg)无法完全通过核磁鉴定,本文通过核磁给出的结构信息结合酶水解巧妙地鉴定了该代谢产物的结构,涉及保密,只给出有差别的部分结构信息。http://ng1.17img.cn/bbsfiles/images/2011/12/201112280311_341823_2160661_3.jpg1.试剂 色谱甲醇(Fisher),去离子水(Eyela Still Ace, SA-2100 E1, 日本),三氟乙酸(TFA,Dima),β葡萄糖苷酶(Sigma)。2.液相色谱条件 Shimadzu HPLC system, 由LC-10ATVP 泵, SPD-10AVP 紫外检测器, 以及CTO-10ASVP 柱温箱组成, 工作站为浙江大学N3000工作站。 色谱柱:Ultimate XB-C18柱(5μm, 4.6x250mm) 流动相:A通道:甲醇,B通道:水(0.05% TFA) 流 速:A通道0.500mL/min;B通道0.500mL/min 柱 温:30℃ 检测波长:275nm 进样量:20μL3.样品准备 对照品溶液的配置:取各纯品0.5mg,加入1mL50%甲醇水溶液,涡旋1mL,微孔滤膜过滤。水解过程:取代谢产物M1 0.5mg,溶于1mL水中,加入适量葡萄糖水解酶,37℃孵育2h,加入2mL的乙酸乙酯萃取,萃取2次,合并萃取液,45℃减压浓缩至干,用1mL50%甲醇水溶液溶解,进样分析。 4.结果与讨论http://ng1.17img.cn/bbsfiles/images/2011/12/201112280325_341830_2160661_3.jpg图1.代谢产物M1水解前的分析图谱(tR=8.951min)http://ng1.17img.cn/bbsfiles/images/2011/12/201112280315_341825_2160661_3.jpg图2.代谢产物M1水解后的分析图谱(tR=8.958min为剩余的未水解的M1,tR=14.720min为水解产物)http://ng1.17img.cn/bbsfiles/images/2011/12/201112280325_341831_2160661_3.jpg图3.已知化合物C1的分析图谱http://ng1.17img.cn/bbsfiles/images/2011/12/201112280325_341832_2160661_3.jpg图4.已知化合物C2的分析图谱http://ng1.17img.cn/bbsfiles/images/2011/12/201112280326_341833_2160661_3.jpg图5.水解产物与C1和C2合并进样分析图谱1.代谢产物M1只有6mg,理论上核磁是可以鉴定的,但基于一些原因,核磁谱图结果不理想,只能通过别的方法鉴定。但是从图1来看,代谢产物M1的纯度是很高的,如果用面积归一化法来计算的话,其含量至少在95%以上,但作者在此给大家透露点信息,代谢产物不同于植物中的化学成分,即使在色谱图上显示单一的色谱峰,但绝对纯度不一定很高,往往有未知的内源性成分如影子一样伴随着它,作者推测这可能是核磁图谱测试不理想的原因之一。2.机缘巧合的是,代谢产物M1两种水解产物均作为已知化合物被作者分离得到,并准确鉴定,因此剩余的实验就显得顺理成章。3.化合物C1和C2在结构上很相似,仅仅是葡萄糖醛酸基的位置不同,因此其表现在色谱行为上的差别也很小,如图5所示,二者没有达到基线分离。4.从各分析图谱可以看出,相同化合物的保留时间重现性非常高,且峰形之正太有目共睹,体现了Ultimate XB-C18柱的优越性能,保证了代谢产物结果鉴定的准确性。具体参数如:理论塔板数、分离度、对称因子等在此不一一列举。5.在整个分析过程中系统压力为19.4MPa左右,波动不超过0.2,换算为PSI也仅为2800左右,在流动相比例为50%的情况下,如此低的压力给测试者营造了“轻松的”实验氛围,避免了系统压力高产生的漏液报警的烦恼。6.一句话小结:本实验运用酶水解结合HPLC分析,成功鉴定了代谢产物M1的结构。

键和金刚烷基团的ADME色谱柱对于极性化合物能得到良好的保留与分离,对于代谢产物的分析具有优势。如LC Café espresso No.2016005所述,从疏水性及表面极性参数可以对其具有特长的溶出行为进行说明。本次实验以极性化合物别嘌呤醇与黄嘌呤氧化酶反应生成的代谢物别嘌呤二醇,嘌呤体代谢产生的次黄嘌呤、黄嘌呤以及尿酸作为样品(参照图1),分别使用CAPCELL PAK ADME、CAPCELL PAK C18 AQ、CAPCELL PAKC18 MGII以及3种他社杂化型ODS色谱柱(粒径均为5 μm)进行分析,对各色谱柱的溶出行为进行了比较。http://ng1.17img.cn/bbsfiles/images/2016/07/201607210842_601338_2222981_3.jpg分析所得色谱图见图2。分析所用HPLC条件如下:http://ng1.17img.cn/bbsfiles/images/2016/07/201607210842_601339_2222981_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/07/201607210842_601340_2222981_3.jpg如图2,各化合物的保留随着各色谱图右侧所示色谱柱表面极性的增加而增强。其中,只有键和金刚烷基团的CAPCELL PAK ADME色谱柱实现了尿酸(峰1)与次黄嘌呤(峰2)间的分离;键和C18基团的色谱柱均无法得到良好分离。进一步,在本次进行比较的色谱柱中,CAPCELL PAK ADME所得理论塔板数(别嘌呤醇:峰5)是最高的,彰显了其对极性化合物优异的分析能力。
[size=15px][color=#595959]正确使用有毒药物是中医的特点之一。最新公布的《古代经典名方中药复方制剂简化注册审批[/color][/size][b][size=15px][color=#595959]管理[/color][/size][/b][size=15px][color=#595959]规定》取消了对有毒中药的使用限制,表明有毒中药在临床实践中的使用是不可替代的。目前对这些药物的毒性评价通常遵循现代药物毒性评价体系,然而,[b]中药毒性反应[/b]的发生不仅与药物本身的性质有关,而且与人体的状态有关。中医的使用遵循辨证论治的原则,因此有必要将不同的“证”或“病”状态与中药的毒性结合起来,形成可靠的毒性评价体系。[/color][/size] [b][size=15px][color=#595959]附子[/color][/size][/b][size=15px][color=#595959]是乌头的子根,在临床应用中,附子对胸闷心痛、四肢冰冷、脉弱等疾病有奇效。因此,它被认为是治疗与[b]阳虚[/b]和寒凝疼痛相关的各种证候的关键草药。但在临床实践中,附子的用量经常超过药典规定的用量,其毒副作用极大地限制了其临床应用。该研究探讨附子对[b]肾阳虚证候模型[/b]的毒性作用,并试图揭示其潜在机制。[/color][/size][size=15px][color=#595959][/color][/size] [size=15px][color=#595959][/color][/size][size=15px][color=#595959]首先,通过肌肉注射氢化可的松25 mg/kg / d,连续10天建立肾阳虚证小鼠模型。然后探讨附子对正常小鼠和肾阳虚模型小鼠的[b]急性毒性[/b]。最后,通过血浆代谢物浓度和肝脏[b]CYP3A4[/b]酶活性分析,揭示附子在不同体质个体中产生不同药理学和毒理学效应的可能机制。[/color][/size][size=15px][color=#595959][/color][/size] [align=center] [/align] [size=15px][color=#595959][/color][/size][size=15px][color=#595959]附子(138 g/kg)对肾阳虚小鼠有严重的毒性作用,80%的小鼠死亡,而对[b]正常小鼠无致死毒性[/b]。说明附子对肾阳虚小鼠的毒性大于正常小鼠。肾阳虚小鼠肝脏CYP3A4酶活性较对照组降低20%,导致附子中毒性二酯二萜生物碱代谢减慢。[/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size] [b][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][/b][font=&][size=16px][color=#232323][/color][/size][/font][b][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][/b][font=&][size=16px][color=#232323][/color][/size][/font][size=15px][color=#595959][font=&][/font][font=&][/font][/color][/size][b][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][/b][size=15px][color=#595959]综上所述,该研究表明,[b]不同证候个体代谢酶活性的变化导致了中药的不同毒性作用[/b],强调了在中医临床应用中[b]考虑个体体质证候的重要性[/b],以及对中药特定证候动物模型进行[b]安全性评价和剂量预测的重要性[/b]。[/color][/size][size=15px][color=#595959][/color][/size]
欢迎大家一起交流讨论~代谢组学是继基因组学和蛋白质组学之后新近发展起来的一门学科,是系统生物学的重要组成部分。基因组学和蛋白质组学分别从和蛋白质层面探寻生命的活动,而实际上细胞内许多生命活动是与代谢物相关的,如细胞信号(cell signaling),能量传递等都是受代谢物调控的。代谢组学正是研究代谢组(metabolome)——在某一时刻细胞内所有代谢物的集合——的一门学科。基因与蛋白质的表达紧密相连,而代谢物则更多地反映了细胞所处的环境,这又与细胞的营养状态,药物和环境污染物的作用,以及其它外界因素的影响密切相关。因此有人认为,基因组学和蛋白质组学能够说明可能发生的事件,而代谢组学则反映确实已经发生了的事情。新陈代谢网络是十分复杂的网络,特别是人体的代谢网络,一直被认为是最复杂的代谢网络。现在多数信号通路的研究都是集中在代谢网络的一个很小的领域。基因组学、蛋白组学研究已经揭示了部分调节通路,但是和代谢网络直接相关的是代谢产物。但是从茫茫多的代谢产物中选取研究对象,无疑是大海捞针。代谢组学研究通过一定的手段能够帮助研究员从代谢产物海中跳出来,提供一个“航拍”的视角,一目了然地发现差异性代谢产物。然后通过已知的代谢通路逆推找出调节酶和基因,完成疾病发病机制、药物治疗机制等方面的研究。代谢组学主要研究的是作为各种代谢路径的底物和产物的小分子代谢物(MW1000)。其样品主要是尿液,血浆或血清,唾液,以及细胞和组织的提取液。主要技术手段是核磁共振(NMR ),液-质联用(LC-MS),气-质联用(GC-MS),色谱(HPLC,GC)等。通过检测一系列样品的谱图,再结合化学模式识别方法,可以判断出生物体的病理生理状态,基因的功能,药物的毒性和药效等,并有可能找出与之相关的生物标志物(biomarker)。代谢组学在新药的安全性评价,毒理学,生理学,重大疾病的早期诊断,个性化治疗,功能基因组学,中医药现代化,环境评价,营养学等科学领域中都有着极其广泛和重要的应用前景,是一门充满朝气的学科。 从近年来发表的相关SCI论文的数量可以看出代谢组学研究呈一个蓬勃发展的局面。从近年来国家拨付的相关研究基金也可以看出国家对代谢组学相关研究的重视。
SN/T 1768-2006 水产品中孔雀石绿和结晶紫及其代谢产物的快速测定方法 [img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=65371]孔雀石绿行标[/url]
请问大家,我要用动物组织做内源性代谢物的靶向代谢组学,用标曲去定量,配制标曲所用的空白基质该如何选择呢?我是打算用相应的空白组织匀浆液去做空白基质,但是我要如何将该基质中的本底干扰去掉呢?蹲蹲比较实用的经验
不能吃变质的肉,肉变质有以下几个表现:颜色变深。新鲜的肉表面有光泽,颜色均匀。新鲜猪肉呈红色或淡红色,脂肪洁白;牛羊肉颜色鲜红,脂肪大多颜色发黄;禽肉皮肤为淡黄色或白色,肉色白里泛红。随着贮藏时间的延长,由于肌红蛋白被氧化,肉色会逐渐变成红褐色。颜色越深,可食性越低。而当肉表面变成灰色或灰绿色,甚至出现白色或黑色斑点时,说明微生物已经产生大量的代谢产物,这样的肉就不能吃。表面发黏。新鲜的肉外表微干或湿润,切面稍潮湿,用手摸有油质感,但不发黏;而肉变质以后,由于微生物大量滋生,会产生黏性代谢产物,造成肉表面发黏,甚至出现拉丝。肉类表面发黏是腐败开始的标志。弹性变差。新鲜的肉质地紧密且富有弹性,用手指按压凹陷后会立即复原。贮藏越久,肉里面的蛋白质、脂肪会逐渐被酶分解,肌纤维被破坏,所以肉会失去原有的弹性,手指压后的凹陷不仅不能完全复原,甚至会留有痕迹。有异味。新鲜肉具有正常的肉味,而变质的肉由于蛋白质、脂肪、碳水化合物被微生物分解,会产生各种胺类、吲哚、酸类、酮类等物质,因而有明显的腐臭味。此外,新鲜的肉煮熟后肉汤透明,汤表面聚集大量油滴。而变质肉中的蛋白质被微生物分解,会产生很多低级代谢产物散落在汤里,造成肉汤浑浊,并且汤面几乎无油滴。
[size=15px][color=#595959][b]茱萸丸(ZYP)[/b]最早记录在宋代《太平圣惠方》中,由[b]黄连、吴茱萸按1:1[/b]的比例组成。在中医理论中,肝胆之气是肝胆功能的概括,肝胆之气功能障碍往往导致[b]消化系统[/b]疾病。ZYP是传统上[b]治疗肝胆胃肠疾病的药物[/b],具有明显的改善肝胆之气的作用。[/color][/size] [size=15px][color=#595959]先前的研究表明,ZYP通过调节粪便代谢稳态和粪便微生物丰度的双重作用,以及调节肝脏中miR-147等miRNA及其靶基因的表达,具有显著的抗胆汁淤积作用。然而,ZYP治疗胆汁淤积的机制尚未完全确定。 [size=15px]探讨ZYP对胆汁淤积大鼠模型mRNA-seq分析干预作用的机制。[/size] [size=15px]将所有大鼠随机分为5组:对照组(Control)、模型组(Model)、ZYP低剂量组(ZYP_L,0.6 g/kg)、ZYP高剂量组(ZYP_H,1.2 g/kg)、熊去氧胆酸组(UDCA,60 mg/kg),每组6只。适应饲养4天后,从第5天开始,ZYP_L、ZYP_H和UDCA组大鼠分别每天灌胃给药,直至第10天。同时,模型组和对照组给予等量的纯净水。第11天,试验组小鼠灌胃橄榄油溶异硫氰酸-A-萘酯(ANIT)溶液50 mg/kg,给予对照大鼠相应剂量的橄榄油。第12-14天,ZYP_L组、ZYP_H组和UDCA组大鼠分别灌胃0.6 g/kg、1.2 g/kg ZYP和60 mg/kg UDCA,模型组和对照组大鼠灌胃等量纯净水。第15天,用150 mg/kg戊巴比妥钠麻醉处死各组大鼠,取各组血液和肝组织进行检测。[/size][size=15px]采用血清生化和组织病理学结果评价ZYP的治疗效果,采用实时荧光定量[url=https://insevent.instrument.com.cn/t/jp]PCR[/url] (qRT-[url=https://insevent.instrument.com.cn/t/jp]PCR[/url])进行mRNA-Seq分析和验证。结合GO、KEGG和GSEA分析来确定ZYP影响胆汁淤积大鼠的机制。[/size][/color][/size][align=center] [/align][size=15px][color=#595959]ZYP能明显改善胆汁淤积大鼠血液生化指标及肝脏组织病理学的异常变化,调节脂肪酸代谢、视黄醇代谢、类固醇激素生物合成等胆汁、脂质代谢相关通路,减轻炎症、胆汁淤积及脂质代谢紊乱。必备基因Cyp2a1、Ephx2、Acox2、Cyp1a2、Cyp2c11、Sult2a1的相对表达量经qRT-[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]验证,与mRNA-seq分析趋势一致。[/color][/size][size=16px][color=#3573b9]结论[/color][/size] [size=15px][color=#595959]ZYP[b]通过调节胆汁代谢和脂质代谢相关通路,具有显著的抗胆汁淤积作用[/b]。这些结果表明,ZYP是一种治疗胆汁淤积症的新方法。[/color][/size]
HPLC-MS-QTOF测有害物质代谢用离子强度表示代谢物变化趋势可以吗? 还是要定量出每个代谢物? 如果可以用离子强度表示,依据是什么?定量的话,应该怎么定量
畜禽中农药代谢试验准则 1 范围本标准规定了畜禽中农药代谢试验的基本原则、方法和要求。本标准适用于农药登记动物代谢试验,用于确定农药在畜禽体内的吸附、转移、分布及可食用组织中残留物的主要成分,并为确定残留物定义和农药脂溶性提供依据。2 规范性引用文件下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB 11930 操作非密封源的辐射防护规定GB 12711 低、中水平放射性固体废物包装安全标准GB 14500 放射性废物管理规定GB 2763 食品中农药最大残留限量NY/T 3096 农作物中农药代谢试验准则国务院令第562号 放射性物品运输安全管理条例农业部公告第2308号 食品中农药残留风险评估指南农业部公告第2386号 农药残留检测方法国家标准编制指南环境保护部公告第65号(2017) 放射性废物分类3 术语和定义GB 2763、NY/T 3096、农业部公告第2308号、农业部公告第2386号界定的以及下列术语和定义适用于本文件。3.1 鉴定 identification 对化合物结构的精确确定,一般采用在不同色谱体系下代谢物与已知标样的对比方法,或使用如质谱(MS)、核磁共振(NMR)等结构鉴定技术。3.2 描述 characterization 对总放射性残留中未能鉴定的放射性残留物特征的阐述,一般包括有机溶剂溶解性、水溶性、中性、酸性、碱性、极性、非极性、不可提取等。3.3 放射性活度 radioactivity 一定量的放射性核素在一个很短的时间间隔内发生的核衰变速率,即核衰变数(dN)/时间间隔(dt),表示放射性核素的放射性强度,国际单位为贝克勒尔(Bq)。4 基本要求4.1 试验单位4.1.1 具有丙级以上非密封性放射性实验室资质。4.1.2 遵循同位素示踪实验操作规程进行代谢试验。4.1.3 具有满足代谢物分析技术要求的仪器、设备和环境设施。4.2 试验人员4.2.1 具有放射性工作人员许可证、个人剂量季度监测报告、职业病检测报告。4.2.2 具备进行农药代谢试验的专业知识和经验。4.2.3 掌握农药代谢试验的相关规定和技能。4.3 试验背景资料包括供试农药有效成分的名称、CAS号及理化性质、登记作物及防治对象,已有的植物代谢、畜禽代谢、农作物中农药残留,以及毒理和环境资料等。
代谢工程(Metabolic engineering)是生物工程的一个新的分支。代谢工程把量化代谢流及其控制的工程分析方法和用以精确制订遗传修饰方案并付之实施的分子生物学综合技术结合起来,以上述“分析——综合”反复交替操作、螺旋式逼近目标的方式,在较广范围内改善细胞性能,以满足人类对生物的特定需求的生物工程。 与所有传统的工程领域一样,代谢工程也包含“分析” 和“综合”两个基本步骤。因为代谢工程借助于DNA重组技术作为一种启用技术而出现,所以一开始人们的注意力仅仅放在这个领域的综合方面,譬如:新的基因在不同寄主中的表达,内酶的扩增,基因的删除,酶活力修饰,转录的解调或酶的解调等。这样前面定义的代谢工程,在相当程度上似乎是应用分子生物学技术表现形式,几乎没有工程的内容,因此从生物过程的角度来衡量,并不是够格的代谢工程。而更加重要的工程内容存在于代谢工程的分析方面。譬如,怎样确定定义生理状态的参数?怎样用这信息解释代谢网络控制的结构体系,进而提出达到某个目标的合乎道理的修饰位点?怎样进一步评估这些遗传修饰和酶的修饰的真实的生化效果,以便进行下一轮的途径修饰,直到达到目的?能不能提出一个可用来确定代谢修饰的最有希望的靶位的合理的步骤?在综合方面,代谢工程的另一个不同寻常的方面是它关注的是代谢途径集成的整体,而不是单个反应。这样,代谢工程研究的是整个生化反应网络,涉及到其自身的途径合成和热动力学可行性,还有途径流量及其控制。我们研究的出发点正在经历从单个酶反应向相互影响的生化反应体系转变。因此,通过对整个反应体系而不是一个个孤立的反应的考察就有可能获得关于代谢和细胞功能的更全面的认识,在这个的意义上“代谢网络”的观念是最为重要的。代谢工程让人们把注意力转向整个体系而不是其组成部分。因此,代谢工程使用来自还原论者的大量的研究的技术和信息来设法进行综合和设计;而关于整个体系的运转状态的观察,对于进一步的合理的分解和分析其自身来说,又是最好的指导。
[align=right][b]SGLC-GC/MS-004[/b][/align][b]摘要:[/b]建立了植物源性食品中208种农药及其代谢物残留量同时测定的方法。本应用按照新国标方法,采用岛津SHIMSEN QuEChERS 产品对梨、韭菜、大米、茶叶4类样品基质进行净化,同时采用岛津[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]串联质谱 [url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-TQ8050,岛津SH-1701 色谱柱进行分析,回收率及重现性良好。该方法前处理速度快,重现性好,灵敏度高,适用于梨、韭菜、茶叶和大米等植物源性食品基质中多种农药残留的同时检测。[b]关键词:[/b]QuEChERS 多农残 植物源性食品 [url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GC-MS[/color][/url]/MS[b]1. 实验部分1.1 实验仪器及耗材仪器配置:[/b]岛津[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-TQ8050 [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]-串联质谱联用仪;[b]耗材方法包:[/b][img=植物源性食品中208种农药及其代谢物残留量的测定]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGL-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-004_1.png[/img][font=arial, &][size=12px][/size][/font]本耗材方法包所含明细如下:[font=arial, &][size=12px][/size][/font][img=植物源性食品中208种农药及其代谢物残留量的测定]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGL-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-004_2.png[/img][img=植物源性食品中208种农药及其代谢物残留量的测定]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGL-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-004_3.png[/img]SHIMSEN Pipet[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url]:SHIMSEN Pipet PMII-10(P/N:380-00751-02);SHIMSEN Pipet PMII-100(P/N:380-00751-04);SHIMSEN Pipet PMII-1000(P/N:380-00751-06)。[b]1.2 分析条件1.2.1 色谱条件:[/b]毛细管柱: SH-1701 毛细管柱(30m* 0.25mm *0.25μm)程序升温:初始温度40℃保持1 min, 以40℃/min升温到120℃,再以5℃/min升温到240℃,以12℃/min升温到300℃, 保持10 min;载气:He流速:1.0 mL/min进样口温度:280 ℃进样量:1μL进样方式:不分流进样[b]1.2.2 质谱条件:[/b]电离模式:电子轰击电离(EI);电子轰击能量:70 eV离子源温度: 230 ℃接口温度:280 ℃溶剂延迟:3min数据采集模式:MRM;[b]1.3 样品前处理[/b]略[b]2. 结果及讨论2.1 标准品的总离子流色谱图[/b][img=植物源性食品中208种农药及其代谢物残留量的测定]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGL-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-004_4.png[/img][font=arial, &][size=12px][/size][/font][align=center]109种农药混合标准品的总离子流色谱图[/align][img=植物源性食品中208种农药及其代谢物残留量的测定]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGL-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-004_5.png[/img][font=arial, &][size=12px][/size][/font][align=center]113种农药混合标准品的总离子流色谱图[/align][font=arial, &][size=12px] [/size][/font][b]2.2 植物源性食品中208种农药及其代谢物的[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GC-MS[/color][/url]/MS检测添加回收结果[/b]将梨、韭菜空白样品进行40.0 μg/kg浓度加标;大米空白样品进行100.0 μg/kg浓度加标;茶叶空白样品进行250.0 μg/kg浓度加标后,按照上述前处理方法处理后上机,平行3份样品考察回收率和RSD,具体结果如下:梨样品加标回收率为73.75%-124.82%,RSD为0.11%-9.60%;韭菜样品加标回收率为76.47%-125.81%,RSD为0.05%-11.66%;茶叶样品加标回收率为60.24%-112.83%,RSD为0.39%-22.65%;大米样品加标回收率为66.61%-118.60%,RSD为0.38%-14.62%。[img=植物源性食品中208种农药及其代谢物残留量的测定]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGL-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-004_6.png[/img][img=植物源性食品中208种农药及其代谢物残留量的测定]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGL-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-004_7.png[/img][img=植物源性食品中208种农药及其代谢物残留量的测定]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGL-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-004_8.png[/img][img=植物源性食品中208种农药及其代谢物残留量的测定]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGL-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-004_9.png[/img][img=植物源性食品中208种农药及其代谢物残留量的测定]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGL-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-004_10.png[/img][img=植物源性食品中208种农药及其代谢物残留量的测定]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGL-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-004_11.png[/img][font=arial, &][size=12px][/size][/font][b]3. 结论[/b]综上,本方案按照新国标方法,采用岛津的SHIMSEN QuEChERS产品对梨、韭菜、茶叶、大米等植物源性食品样品进行净化,同时采用岛津[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]串联质谱 [url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-TQ8050,岛津SH-1701色谱柱进行分析,对普通水果、有色蔬菜、茶叶和谷物等4类植物源性食品中208种农药及其代谢物残留的检测方法进行了验证,结果表明,该方法操作简单、分析速度快、重现性好、准确度高,可以应对植物源性食品中多种农药残留同时测定的要求。
张星元:生物工程的一个新的分支:代谢工程代谢工程(Metabolic engineering)是生物工程的一个新的分支。代谢工程把量化代谢流及其控制的工程分析方法和用以精确制订遗传修饰方案并付之实施的分子生物学综合技术结合起来,以上述“分析——综合”反复交替操作、螺旋式逼近目标的方式,在较广范围内改善细胞性能,以满足人类对生物的特定需求的生物工程。为了满足人类对生物的特定需求而对微生物进行代谢途径操作,已有将近半个世纪的历史了。在氨基酸、抗生素、溶剂和维生素的发酵法生产中,都可以找到一些典型实例。操作的主要方法是,用化学诱变剂处理微生物,并用创造性的筛选技术来检出已获得优良性状的突变菌株。尽管这种方法已被广泛地接受并已取得好的效果,但对突变株的遗传和代谢性状的鉴定是很不够的,更何况诱变是随机的! DNA重组的分子生物学技术的开发把代谢操作引进了一个新的层面。遗传工程是我们有可能对代谢途径的指定酶反应进行精确的修饰,因此,有可能构建精心设计的遗传背景。DNA重组技术刚进入可行阶段不久,就出现了不少可用来说明这种技术在定向的途径修饰方面的潜在应用的术语。如分子育种(1981年),体外进化(1988年),微生物工程或代谢途径工程(1988~1991年),细胞工程(1991年)和代谢工程(1991年)。尽管不同的作者提出不完全相同的定义,这些定义均传达了与代谢工程的总目标和手段相似的含义。我们曾经把代谢工程定义为,代谢工程就是用DNA重组技术修饰特定的生化反应或引进新的生化反应,直接改善产物的形成和细胞的性能的学科。这样定义代谢工程强调了代谢工程工作目标的确切性。也就是说,先要找到要进行修饰或要引进的目标生化反应,一旦找准了目标,就用已建立的分子生物学技术去扩增、去抑制或删除、去传递相应的基因或酶,或者解除对相应的基因或酶调节,而广义的DNA重组只是常规地应用于不同步骤中,以便于达到这些目标。尽管在所有的菌种改良方案中都有某种定向的含义,但与随机诱变育种相比较,在代谢工程中工作计划的定向性更加集中更加有针对性。这定向性在酶的目标的选择,实验的设计,数据的分析上起着支配的作用。不能把细胞改良中的所谓“定向” 解释为合理的途径设计和修饰,因为“定向选择”与随机诱变之间没有直接关系。相反地我们可借助于“逆行的代谢工程”(reverse metabolic engineering), 从随机诱变而获得的突变株及其性状的实验结果,来提取途径及其控制的判断信息(critical information)。与所有传统的工程领域一样,代谢工程也包含“分析” 和“综合”两个基本步骤。因为代谢工程借助于DNA重组技术作为一种启用技术而出现,所以一开始人们的注意力仅仅放在这个领域的综合方面,譬如:新的基因在不同寄主中的表达,内酶的扩增,基因的删除,酶活力修饰,转录的解调或酶的解调等。这样前面定义的代谢工程,在相当程度上似乎是应用分子生物学技术表现形式,几乎没有工程的内容,因此从生物过程的角度来衡量,并不是够格的代谢工程。而更加重要的工程内容存在于代谢工程的分析方面。譬如,怎样确定定义生理状态的参数?怎样用这信息解释代谢网络控制的结构体系,进而提出达到某个目标的合乎道理的修饰位点?怎样进一步评估这些遗传修饰和酶的修饰的真实的生化效果,以便进行下一轮的途径修饰,直到达到目的?能不能提出一个可用来确定代谢修饰的最有希望的靶位的合理的步骤?在综合方面,代谢工程的另一个不同寻常的方面是它关注的是代谢途径集成的整体,而不是单个反应。这样,代谢工程研究的是整个生化反应网络,涉及到其自身的途径合成和热动力学可行性,还有途径流量及其控制。我们研究的出发点正在经历从单个酶反应向相互影响的生化反应体系转变。因此,通过对整个反应体系而不是一个个孤立的反应的考察就有可能获得关于代谢和细胞功能的更全面的认识,在这个的意义上“代谢网络”的观念是最为重要的。代谢工程让人们把注意力转向整个体系而不是其组成部分。因此,代谢工程使用来自还原论者的大量的研究的技术和信息来设法进行综合和设计;而关于整个体系的运转状态的观察,对于进一步的合理的分解和分析其自身来说,又是最好的指导。尽管代谢和细胞生理学可以为某组反应途径的分析提供主要的背景知识,应该指出流量及其控制的测定结果具有更广阔的应用范围。因而,代谢工程的概念除了可用来分析流经某组代谢途径的物质流和能量流,同样可以应用于在信号传感途径的信息流量的分析。对于信息流量尚未很好地定义,一旦信号途径的概念得到具体化,以上观念和方法将会在信号传感途径的相互作用的研究,以及胞外刺激控制基因表达的复杂机制的解释方面发挥作用。也许代谢工程最重要的贡献在于对活体条件下代谢流及其控制的强调。代谢流的概念本身实际上并不是新的。代谢流及其控制引起生化研究人员中的少数先知的注意,已有大约30多年历史了。作为他们工作的结果,代谢控制的观念成熟了,并且被严格的定义了,尽管这些观念曾经没有得到传统的生物学家广泛地接受。代谢工程最初被设想为特定的途径操作,很快又变成工程师们的分析技能的预期的输出端。发酵工程师们建立了量化代谢流及其控制的工程分析方法,从而看到了利用代谢控制分析这个有效的平台向这个过程导入严密性的机会,以及生化工程与发酵工程在生物学领域的交叉和互补。
胆固醇稳态对机体正常的细胞和系统功能至关重要,胆固醇平衡失调是心血管疾病、神经退行性疾病和癌症等其他疾病的基础[1]。胆固醇代谢包括内源性胆固醇合成、吸收和排泄等环节。研究表明,胆固醇在体内不能被降解,有效排泄是维持其稳态的重要环节[2]。体内积累的胆固醇最终通过肠道以粪便消除胆固醇和胆汁酸的形式达到平衡,目前已知的胆固醇排泄途径包括了胆固醇逆转运(reverse cholesterol transport,RCT)途径和经肠胆固醇排泄(transintestinal cholesterol excretion,TICE)途径;前者是肝脏将胆固醇转化为胆汁酸后经肠排出,后者是由血直接经肠道分泌和排出血浆脂蛋白来源的胆固醇,二者交汇于肠道,因此,肠道在胆固醇稳态中发挥了重要作用[3-4]。调血脂治疗是防治体内高胆固醇含量诱导的相关疾病的有效方法,目前临床常用调血脂药物他汀类的作用是通过降低低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)以限制内源性胆固醇合成,从而防治心血管等疾病的发生发展,但其相关发病率和死亡率仅降低了30%[5]。这意味着需要更多策略来解决这个严重的公共卫生事件。 雷公藤红素(celastrol,CeT)是一种从传统中药雷公藤Tripterygium wilfordii Hook. f.中提取分离出的活性成分,具有抗炎、抗癌和抗动脉粥样硬化等多种药理活性[6],且具有良好的成药性,被《Cell》杂志列为最可能转化为现代药物的5种有潜力传统药物之一[7]。Zhang等[8]前期研究发现,体外有效成分为CeT的南蛇藤能够通过在促进RCT减少脂质蓄积方面具有积极作用,其机制主要是通过激活清除剂受体B类成员1(scavenger receptor class B member 1,SRB1)、ABC转运体和细胞色素P450家族7亚家族A成员1(cytochrome P450 family 7 subfamily A member 1,CYP7A1)途径促进胆固醇代谢。然而,有关CeT调控胆固醇代谢的作用机制探索尚不完善。此外,迄今为止,并无有关CeT通过调控肠道TICE途径介导胆固醇代谢的相关研究。因此,本研究采用网络药理学和系统生物学理论,通过构建“CeT-靶点-肠道胆固醇代谢”多层次网络,初步预测CeT调控肠上皮细胞胆固醇代谢的作用机制[9-10],并结合实验深入探讨和验证CeT调控肠上皮细胞胆固醇代谢的作用及机制,旨在为维持体内胆固醇稳态提供新的方向和理论依据。 1 材料 1.1 细胞 大鼠小肠隐窝上皮IEC-6细胞(批号ZQ0783)由中国科学院上海细胞库提供。 1.2 药品与试剂 CeT(批号C0869)购自美国Sigma公司;肝X受体α(liver X receptor α,LXRα)抑制剂GSK2033(批号HY-108688)、Bodipy荧光染色(批号HY-W090090)购自美国MCE公司;0.25%胰蛋白酶(批号PB180229)购自美国Hyclone公司;DMEM高糖完全培养基(批号ZQ-121)、DMEM基础培养基(批号09122)购自上海中乔新舟生物科技有限公司;磷酸酶抑制剂(批号CW2383S)、蛋白酶抑制剂(批号CW2200S)、BCA试剂盒(批号CW0014S)、SDS-PAGE试剂盒(批号CW0022S)、Loading buffer(批号CW0028S)液购自康为世纪生物科技股份有限公司;CCK-8试剂盒(批号C0037)、RIPA裂解液(批号P0013B)、ECL化学发光试剂盒(批号P0018S)购自碧云天生物技术股份有限公司;油红O染色试剂盒(批号G1262-4)购自北京索莱宝科技有限公司;PVDF膜(批号ISEQ00010)购自美国Millipore公司;兔抗三磷酸腺苷结合盒转运蛋白G5(adenosine triphosphate-binding cassette transporters G5,ABCG5)抗体(批号27722-1-AP)、甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphate dehydrogenase,GAPDH)抗体(批号10494-1-AP)、山羊抗兔二抗(批号SA00001-2)购自美国Proteintech公司;兔抗ATP结合盒转运蛋白G8(ATP-binding cassette transporters G8,ABCG8)抗体(批号A01482-2)购自武汉博士德生物工程有限公司;兔抗NPC1样细胞内胆固醇转运蛋白1(NPC1 like intracellular cholesterol transporter 1,NPC1L1)抗体(批号PA5-116672)购自美国Thermo Fisher Scientific公司;兔抗LXRα抗体(批号ab41902)、DAPI染液(批号ab228549)购自英国Abcam公司。 1.3 仪器 ix 73型倒置荧光显微镜(日本Olympus公司);FC型酶标仪、Forma 3系列CO2培养箱、EVOS fl auto全自动荧光倒置荧光学显微镜(美国Thermo Fisher Scientific公司);ChemiDoc XRS+化学发光成像系统、Mini-PROTEAN Tetra蛋白电泳系统(美国Bio-Rad公司)。 2 方法 2.1 网络药理学研究 将PubChem(https://pubchem.ncbi.nlm.nih.gov/)得到的CeT 3D结构导入PharmMapper(http://www. lilab-ecust.cn/pharmmapper/)进行药物靶点预测。通过NCBI(https://www.ncbi.nlm.nih.gov/)得到肠道和胆固醇代谢靶点。并与CeT靶点取交集得到共有靶点;通过STRING(https://STRING-db.org)进行蛋白质-蛋白质相互作用(protein-protein interaction,PPI)网络构建,并导入Cytoscape 3.9.1软件构建网络模型并分析;通过DAVID(https://david. ncifcrf.gov/)进行基因本体(gene ontology,GO)功能及京都基因与基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)通路富集分析;利用PDB(https://www.rcsb.org/)筛选并下载分辨率小于0.25 nm的靶点的结晶复合式,结合上述得到的CeT 3D结构,采用Autodock进行分子对接,运用PyMol可视化处理。 2.2 实验验证 2.2.1 IEC-6细胞培养 IEC-6细胞用DMEM高糖完全培养基于37 ℃、5% CO2的恒温培养箱中常规培养。 2.2.2 CCK-8法检测细胞存活率 将对数生长期的IEC-6细胞接种于96孔板中,5×103个/孔。每孔加入100 μL含不同浓度(0.05、0.10、0.20、0.40、0.80 μmol/L)CeT的培养基,另设置加入无药物培养基的对照组,每组设置5个复孔,培养箱中培养24、48 h。每孔加入10 μL CCK-8试剂,于培养箱中孵育1~2 h后,采用酶标仪在450 nm处检测吸光度(A)值,计算细胞存活率。 细胞存活率=A给药/A对照 2.2.3 油红O染色评估CeT对肠上皮细胞胆固醇的影响 设置对照组、模型组和CeT(0.05、0.10、0.20 μmol/L)组,除对照组外,其余各组加入DMEM基本培养基配制的胆固醇胶束(cholesterol micelles, C-M,10 mmol/L)构建肠上皮细胞高胆固醇模型[11],给药组加入不同浓度的CeT溶液,对照组加入不含药物的培养基。干预24 h后,加入ORO Fixative固定液固定细胞;加入1 mL 60%异丙醇浸洗;加入油红O染液(ORO Stain A∶ORO Stain B=3∶2),洗涤至孔内无红色剩余;加入Mayer苏木素染色液,洗涤;加入油红O染液缓冲液;加入蒸馏水覆盖细胞并拍照,使用Image-Pro Plus软件以脂滴与整个图像的面积比进行定量。 2.2.4 Bodipy荧光标记法 按“2.2.3”项下方法进行分组和给药,干预24 h后,PBS洗涤,室温下多聚甲醛固定30 min;每孔加入2 μmol/L Bodipy染色液,于37 ℃细胞培养箱中孵育15 min;弃去染色液,PBS洗涤;DAPI复染核5 min,PBS洗涤;观察并拍照。使用Image-Pro Plus软件以荧光强度进行统计。 2.2.5 Western blotting检测TICE相关蛋白表达 按“2.2.3”项下方法进行分组和给药,干预24 h后,收集细胞;PBS洗涤后使用蛋白裂解液提取总蛋白质,BCA定量法测定蛋白质浓度。蛋白样品经十二烷基硫酸钠-聚丙烯酰胺凝胶电泳,转至PVDF膜,加入5%脱脂牛奶封闭3 h,用TBST洗涤后加入一抗,4 ℃孵育过夜;洗涤后加入二抗,室温孵育2 h;洗涤后进行显影,使用Image-Pro Plus软件分析条带灰度值。 2.2.6 免疫荧光检测LXRα/ABCG8和LXRα/ NPC1L1通路相关蛋白的影响 设置对照组、模型组、CeT(0.1 μmol/L)组、GSK2033(10 μmol/L)组和CeT+GSK2033组,除对照组外,其余各组加入DMEM基本培养基配制的胆固醇胶束(10 mmol/L)构建肠上皮细胞高胆固醇模型,各给药组加入相应药物,对照组加入不含药物的培养基。干预24 h后,PBS洗涤3次;4%多聚甲醛固定30 min,PBS洗涤3次后加入Trition X-100,室温下通透10 min;PBS洗涤3次后,加入免疫染色封闭液封闭60 min,吸去多余的牛血清白蛋白;分别滴加100 μL LXRα(1∶200)、ABCG8(1∶200)、NPC1L1(1∶200)一抗,4 ℃孵育过夜;回收一抗,PBS浸洗3次,滴加100 μL二抗(1∶300),室温避光孵育60 min;PBS洗涤3次,滴加DAPI复染核15 min,PBS洗涤3次;滴加抗淬灭剂10 μL,扣片,正面朝下盖在载玻片上,荧光显微镜下观察并拍照。使用Image-Pro Plus软件分析荧光强度。 2.2.7 统计学分析 采用GraphPad Prism 9.0和SPSS 26.0软件进行统计分析,数据以表示。两组间数据分布的正态性和方差齐性分别以Kolmogo? rov-Smirnov和Levene检验确定。组间均数比较采用t检验;多组间均数比较采用单因素方差分析,组间有差异进一步采用SNK-q检验进行两两比较。 3 结果 3.1 网络药理学研究 3.1.1 CeT-肠道胆固醇代谢靶点 通过TCMSP等数据库得到94个CeT相关靶点。通过NCBI Gene等数据库得到15 415个肠道相关靶点、14 177个胆固醇代谢相关靶点。并构建韦恩图预测CeT-肠道胆固醇代谢共有靶点,见图1。 图片 3.1.2 CeT-靶点-肠道胆固醇代谢网络构建 将PPI导入Cytoscape 3.8.1软件进行可视化,发现1个关键的子网络,见图2。 图片 3.1.3 CeT-肠道胆固醇代谢的GO功能富集分析 对CeT调控肠道胆固醇代谢的作用及机制进行GO富集分析,分别得到855个生物进程、17个细胞组成、53个分子功能,根据P<0.05,选出排名前10的条目,见图3。 图片 3.1.4 CeT-肠道胆固醇代谢的KEGG通路富集分析 CeT调控肠道胆固醇代谢的通路涉及34条,根据P<0.05,选出排名前10的通路,见图4。其中,主要涉及脂肪的消化和吸收、过氧化物酶体增殖物激活受体(peroxisome proliferators-activated receptor,PPAR)等信号通路。其中,肠道脂质代谢的关键通路(fat digestion and absorption)的靶点(ABCG5、ABCG8、NPC1L1)主要涉及CeT-靶点-肠道胆固醇代谢网络的关键网络之一(图5)。并且该网络主要涉及胆固醇排泄的关键途径——TICE途径。 图片 图片 3.2 分子对接分析 CeT与NR1H3(LXRα)结合能为?28.131 4 kJ/mol,可视化显示,匹配度良好,化合物与靶点结合的最优构象以氢键的方式呈现,结合活性良好,见图6。 图片 3.3 体外实验研究 3.3.1 CeT浓度筛选 不同浓度(0.05、0.1、0.2、0.4、0.8 μmol/L)的CeT分别干预IEC-6细胞24、48 h后,如图7所示,干预24 h时随着CeT浓度的增加细胞存活率降低,CeT的半数抑制浓度(half inhibitory concentration,IC50)为0.2 μmol/L。本研究在探索CeT安全浓度调控IEC-6细胞胆固醇代谢活性的同时,为了更进一步研究CeT在IC50时是否较安全浓度的效果更好,因此,选择0.05、0.10、0.20 μmol/L的CeT处理细胞24 h进行后续研究。 图片 3.3.2 CeT对IEC-6细胞内脂质的影响 如图8所示,油红O染色与Bodipy荧光标记结果均显示,与对照组比较,胆固醇胶束干预显著增加脂滴染色和荧光强度(P<0.001),表明造模成功;与模型组比较,各剂量CeT均显著抑制IEC-6细胞中脂质积累(P<0.05、0.01、0.001)。 图片 3.3.3 CeT对TICE途径关键蛋白的影响 NPC1L1是胆固醇吸收的重要蛋白,ABCG5/G8与胆固醇流出密切相关。如图9所示,与对照组比较,模型组NPC1L1蛋白表达水平显著升高(P<0.05),ABCG5和ABCG8蛋白表达水平显著降低(P<0.05、0.01);与模型组比较,CeT(0.2 μmol/L)组NPC1L1蛋白表达水平显著降低(P<0.05),CeT(0.1、0.2 μmol/L)组ABCG5和ABCG8蛋白表达水平显著升高(P<0.05、0.01)。因此,CeT可能通过抑制NPC1L1,促进ABCG5、ABCG8的表达,调控TICE途径介导的胆固醇摄取和流出。 图片 3.3.4 LXRα是CeT调控TICE途径的关键蛋白 如图10所示,与对照组比较,模型组LXRα、ABCG8表达显著降低(P<0.01),NPC1L1表达显著增加(P<0.001);与模型组比较,CeT组LXRα、ABCG8表达显著增加(P<0.001),NPC1L1表达显著降低(P<0.01),LXRα抑制剂GSK2033组ABCG8表达显著降低(P<0.01),NPC1L1表达显著增加(P<0.05);与CeT组比较,CeT+GSK2033组LXRα、ABCG8表达显著降低(P<0.01),NPC1L1表达显著增加(P<0.01)。因此,CeT可能通过促进LXRα的表达,调控TICE途径中的关键蛋白NPC1L1、ABCG8介导的胆固醇摄取和流出。 图片 4 讨论 胆固醇广泛存在于机体中,具有广泛的生理作用,是组织细胞中不可缺少的重要物质,它不仅参与细胞膜的形成,也是合成胆汁酸、维生素D及甾体激素的重要原料,但当其过量时便会导致高胆固醇血症,研究表明,心血管疾病、胆石症和肿瘤与高胆固醇血症密切相关[12-13]。胆固醇在体内不能被降解,机体有效排泄胆固醇是维持胆固醇稳态的重要环节[2]。因此,促进体内胆固醇排泄以维持体内胆固醇的动态平衡可能是治疗胆固醇失衡相关疾病的新策略。 基于此,本研究通过网络药理学方法,探讨CeT通过调控肠上皮细胞胆固醇代谢的潜在靶点及相关机制。PPI网络发现,CeT调控肠上皮细胞胆固醇代谢涉及1个核心子网络。其中,ABCG5/8与NPC1L1为胆固醇摄取与流出相关的核心靶点。本研究通过体外构建和模拟肠上皮细胞高胆固醇环境,探索CeT调控肠上皮细胞胆固醇代谢的机制,油红O和Bodipy结果均显示,CeT能够呈浓度相关性地降低胆固醇胶束干预的肠上皮细胞内的脂质积蓄。进一步通过结合KEGG通路分析发现,该子网络中的核心靶点与肠道脂质代谢的关键通路(fat digestion and absorption)相匹配,通过深度分析该通路发现,其主要涉及肠上皮细胞摄取与流出胆固醇中的TICE途径。已有研究表明,胆固醇从体内排出的唯一途径是通过粪便直接排出或转化为胆汁酸后排出,粪便排泄可通过2种独立途径进行,第1种途径是胆汁分泌,该途径已被广泛描述和研究。第2种途径是通过TICE途径[14]。在2009年Van团队初步研究估计,TICE对野生型小鼠体内排出的粪便中性固醇总量的贡献约为30%[15]。接下来,该团队在2010年通过实验得出在小鼠中TICE途径占粪便中性甾醇排泄的70%[16]。在人体生理情况下,TICE途径排泄的胆固醇占粪便胆固醇排泄总量的35%[2,17]。TICE指由血直接经肠道分泌和排出血浆脂蛋白来源的胆固醇。包括肝源性含载脂蛋白B的脂蛋白被基底膜侧低密度脂蛋白受体(low density lipoprotein receptor,LDLR)和其他可能受体吸收、内化,最终通过ABCG5/G8以及其他可能的转运体从顶端膜流出排泄到肠腔[18]。另有研究发现,利用Ezetimibe抑制NPC1L1介导的胆固醇摄取可显著增强TICE途径[2]。而本研究表明,CeT干预处于高胆固醇环境中的肠上皮细胞后,NPC1L1被抑制,而ABCG5、ABCG8被激活。提示,CeT主要通过抑制NPC1L1减少肠上皮细胞胆固醇摄取和促进ABCG5、ABCG8增加胆固醇流出。 LXRα由于其抗动脉粥样硬化、去除胆固醇和抗炎活性,在胆固醇稳态的转录调控中发挥极其关键作用[19]。研究发现,LXRα可调控NPC1L1在肠上皮细胞中的表达,降低肠道胆固醇的吸收[20]。此外,ABCG5和ABCG8是LXRα的直接靶基因,常形成异二聚体ABCG5/G8发挥作用,负责将细胞内胆固醇泵入肠腔并最终通过粪便排出体外[21]。PPI子网络表明,NPC1L1、ABCG5以及ABCG8主要由LXRα交联。因此,在上述研究的基础上,通过分子对接模拟了CeT与LXRα的对接模式,结合活性良好。采用LXRα抑制剂GSK2033处理,结果显示,NPC1L1和ABCG5/G8主要受LXRα调控。提示,CeT可能通过LXRα/ABCG5/ABCG8和LXRα/ NPC1L1途径分别介导IEC-6细胞胆固醇摄取和流出,进而促进TICE途径介导的胆固醇排泄。 本研究通过网络药理学和相关实验发现,CeT可能通过抑制肠上皮细胞胆固醇摄取和促进胆固醇流出维持机体胆固醇稳态,这一效应与核心靶点LXRα密切相关,本研究拓展了CeT调控体内胆固醇代谢的机制,为维持体内胆固醇稳态和胆固醇失衡相关疾病的新药研发提供了新思路。