原标题:英开发出质谱成像技术运用新方法 推动癌组织分析进入数字时代 在癌症研究领域,质谱成像(MSI)是一种非常有前途的技术,但目前该技术的运用还受原始数据预处理、图像精确度及图像识别能力等问题限制。英国帝国理工学院近日发布新闻公报称,该校研究人员开发出一种新方法,可有效解决上述问题。新方法将改变病体组织的检测方式,从而推动癌症组织分析进入数字时代。相关研究成果刊发在最新一期《美国国家科学院院刊》上。 质谱成像技术主要是利用质谱直接扫描生物样品,分析化学成分在细胞或组织中的结构、空间与时间分布信息。这种成像方法不局限于特异的一种或几种蛋白质分子,可在生物组织样本中找到每一种蛋白质分子,并提供它们在组织中空间分布的精确信息。早在几年前,就有科学家提出利用该技术来确定生物组织类型的构想,但却一直没有设计出实用有效的方法。 新方法利用解吸电喷雾电离技术来优化数据预处理,提高图像精确度,并通过提取生物组织特定的分子印记来强化不同生物组织类型的生化特性,以增强图像识别能力。研究人员称,利用新开发的集成生物学信息平台,可将质谱成像技术获得的大量人体组织的具体信息数据,用于构建各种类型的组织数据库。通过多样本分析,并与传统的组织学分析结果进行比较,计算机就可以学习识别不同类型的组织,从而使癌变组织的解析变得相对简单高效。他们将自己设计的工作流程用于直肠结肠癌组织的检测,效果良好。 与标准组织学动辄几周才会得出完整结果的检测手段相比,利用质谱成像技术进行单一检测,仅需几小时即可获得更详尽的信息,不仅会显示组织是否发生癌变,还会显示癌症是哪一种类型和亚型。这些信息对于医生选择最有效的治疗方法十分重要。 研究人员指出,自19世纪后期染色技术用于显示组织结构以来,对组织病理学样本的分析方法鲜有变化。直到今天,染色法依然是医院组织学分析的主流手段,并且变得越来越复杂,耗费也越来越高。而质谱成像技术可能改变组织学的基本范式,科学家将不再根据组织的结构,而是根据它们的化学成分来定义组织类型。将来的检测不再依靠专家的眼睛,而是以海量数据为基础,仅一个检测所得到的信息就远比多个传统组织学检测所得到的更多。他们表示,新研究克服了一些质谱成像技术实际应用所遇到的障碍,将成为创建下一代完全自动化的组织学分析手段的第一步。 总编辑圈点 这是用互联网思维改造传统检测方法的一种尝试,它首先选取了质谱成像方法中最容易快速成像的解吸电喷雾电离技术,实现了数据快速采集;其次,通过将质谱成像得到的结果数字化,建立样本库,提高了数据规模,保证了分析精度;最后,与大数据、云计算等结合,可不断提高检测的准确性,为可靠应用提供保证。新思维已经提高了单个样本的检测精度,我们对它在群体和地区性疾病的检测预防方面也应有所期待。

今天到这里来发布一个消息,对坛里各位师生都有用,版主不要认为是广告帖,高抬贵手啊。《核磁共振原理与实验方法》原书由武汉大学出版社出版,ISBN:9787307059894。出版时间:2008-04-01。大32开本,32个印张,精装版,每本定价95元,该书是核磁共振专著。前5章为核磁共振基础知识;第6章是介绍核磁共振谱仪和操作程序;第7和第8章是理论计算方法和表象理论,很有看点;第9章是该书所特有,如想设计新的实验就有必要一读;第10章一维谱,包括谱仪各种指标测试和13C谱编辑;第11章自旋回波和驰豫时间测量;第12 章双共振,重点讨论各种自旋去偶;第13章二维谱,是读者感兴趣的部分; 第14章多量子跃迁,比较专业;第15章供关心固体高分辨的读者一阅;第16章是书中的重点,分析了84个实用脉冲序列,体现了理论与实验相结合的价值。《核磁共振原理与实验方法》适用于从事核磁共振研究的专业人员,应用核磁共振技术做结构分析的相关工作人员,以及大学教师、研究生、科研人。该书2008年出版,很快售罄,一直未再版。http://ng1.17img.cn/bbsfiles/images/2015/04/201504011326_540416_2995925_3.jpg网上对该书需求度很高。现在,两位老师(高汉宾、张振芳)不顾年事已高,重新整理,与时俱进,以数字出版方式,在武汉大学出版社的天线出版网上正式网络出版,出版号: UDPN 978-7-307-01368-1。http://ng1.17img.cn/bbsfiles/images/2015/04/201504011333_540417_2995925_3.jpg http://ng1.17img.cn/bbsfiles/images/2015/04/201504011334_540418_2995925_3.jpg扫一扫同时,两位老师的另一新作《磁共振成像原理》也以数字出版形式出版,出版号: UDPN 978-7-307-01369-8。该书没有纸质出版,数字出版是唯一形式。http://ng1.17img.cn/bbsfiles/images/2015/04/201504011338_540419_2995925_3.jpg http://ng1.17img.cn/bbsfiles/images/2015/04/201504011339_540420_2995925_3.jpg扫一扫该书简介:随着磁共振成像在临床诊断中普遍应用,磁共振影像已为大众所熟悉,希望了解磁共振成像的人与日俱增,为此,需要一本具有一定深度的普及读物供大家阅读和参考。本书从物理角度论述磁共成像原理,全书共分14章。 第一章 磁共振成像概述 第二章 连续与离散傅里叶变换 第三章 离散采样与傅里叶重建像 第四章 稳态κ空间采样 第五章 稳态快速κ空间采样 第六章 κ空间分区采样和回波平面成像(EPI) 第七章 Bloch方程的解与旋密度、T1、T2 的测量 第八章 分辨率、信噪比、对比度 第九章 化学位移谱成像和抑制脂肪信号 第十章 磁场不均匀对图像的影响 第十一章 随机运动、弛豫与扩散 第十二章 运动伪影和速率补偿 第十三章 磁共振血管成像(MRA) 第十四章 磁化率成像与脑功能成像(FMIR)参考文献
日咳黏附素等电点全柱成像毛细管等电聚焦电泳检测方法的建立及验证
本节微课的目标主要是使大家了解什么是拉曼成像以及拉曼成像可以做什么。具体的课程内容是通过通俗易懂,生动形象的方式向大家介绍拉曼成像的原理,成像方法以及应用示例。观看了本节微课后,希望大家能明白什么情况
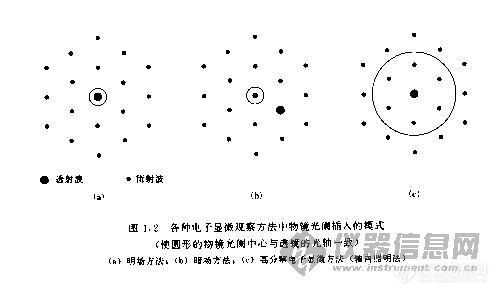
[img]http://ng1.17img.cn/bbsfiles/images/2007/07/200707291922_59373_1615209_3.jpg[/img]我从教科书上看到了TEM成像的几种类型,比如明场像、暗场像、高分辨像等三种。对于明场像和暗场像的成像方式和操作方法我大概了解,就是分别让透射电子和衍射电子成像,而对于高分辨像如何同时让透射电子和衍射电子成像的操作方法感到疑惑,就像上面这个图中所示的那样。在电镜上是如何操作来获得样品的高分辨像呢?我看到一份国外的网上教程,他们的示意图上标明当入射电子与样品成一定夹角时才能获得高分辨像,是否真的如此?还是有其他什么方法?请各位大侠根据自己的理解介绍一下,最好能有相关的图片就更好了。
http://www.bioon.com/biology/UploadFiles/201203/2012030911450761.jpg细胞S-腺苷甲硫氨酸成像图,随着每个时间点蛋氨酸(右下)的增加,荧光强度也增高通过基因工程技术使得细胞表达一种经修饰(改造)过的RNA,又称Spinach,研究人员能对活细胞中的小分子代谢物进行成像,并观察它们随时间变化是如何改变的。每个细胞新陈代谢都会产生代谢产物。假如能得知产物生成效率的话,就能辨识如癌症状态下细胞代谢的异常或确定药物能否将细胞的代谢状况恢复到正常状态。康奈尔大学威尔医学院的研究人员说发表在3月9日的《科学》杂志上的相关论文详细描述了这种先进的技术方法,这一技术将有可能彻底颠覆以往对代谢组学的认识,提供数千种细胞内代谢产物的动态变化的化学指纹图谱。威尔康乃尔医学院药理学副教授Samie R. Jaffrey博士说:“动态观察到代谢产物的变化将为我们提供新的和强大的武器,方便我们了解代谢在疾病状态下是如何改变的,并帮助我们找到可以将它们恢复到正常水平的方法”。Jaffrey博士领导威尔康乃尔的其他三名研究人员共同完成了这项研究。他说:“细胞的代谢水平调控着细胞诸多功能,也正因为如此,代谢水平的变化可以是细胞内在特定的时间内发生什么变化的写照”。例如生物学家都知道,肿瘤细胞存在代谢异常,这些细胞对葡萄糖能源的利用存在异常并产生独特的代谢产物如乳酸,从而有不一样的新陈代谢过程。Jaffrey博士说:“能够看到这些代谢异常的话,就可以了解癌症的发生发展。但是到现在为止,测量活细胞中代谢产物一直非常困难。Jaffrey博士和他的团队展开的科学研究表明:可以用特定的RNA序列来检测细胞中代谢产物的水平。这些RNAs是基于能在细胞发出绿色光的Spinach RNA设计的。Jaffrey博士研究小组修改Spinach的RNAs,使得它们一旦遇到它们专属绑定的代谢物时就关闭,造成Spinach荧光开启。他们设计出了RNA序列以追踪细胞中五个不同代谢产物包括二磷酸腺苷、细胞能量分子ATP和参与调节基因活性的甲基化过程的SAM(S-腺苷蛋氨酸)水平的变化。他说:“在此之前,一直没有人能够实时观察到细胞中代谢产物水平是如何变化的”。Jaffrey博士说:“在活细胞中运用RNA传感器,研究人员能够测量单个细胞中的目标代谢产物水平随着时间的变化而发生的改变,你可以看到这些代谢物如何响应信号刺激或遗传变化进而发生动态变化的。你可以筛选出能使得这些基因异常发生正常化的药物,我们的一个主要目标是确定药物是否能使细胞的新陈代谢正常化。新技术克服了现行的用绿色荧光蛋白(GFP)标记活细胞以充当传感器的缺点。如果将绿色荧光蛋白和其他发光蛋白质融合到能结合某种代谢物产物的自然存在的蛋白质中的话,绿色荧光蛋白和其他发光蛋白质就可以用来充当代谢感应器。但在某些情况下,代谢产物与自然存在的蛋白质结合方式会扭转蛋白质结构,进而影响已经融入到这些蛋白质中的荧光蛋白。另外,对于大多数的代谢产物,并没有可用来融合绿色荧光蛋白以制造传感器的蛋白质。通过使用RNA作为代谢物传感器,这个问题引刃而解了。Jaffrey博士说:“关于RNA令人惊奇的是,你可以得到基本上你想要结合任何一种小分子代谢物的RNA序列。他们可以在几个星期就能生产出来”。然后,这些人造序列融合到Spinach中,并在细胞中以单链RNA的形式表达。Jaffrey博士说:“这种做法能让你得到任何你想研究的小分子代谢物,以及这些小分子代谢物在细胞内的情况”,他和他的同事们将这一技术的运用范围扩大到能检测活细胞内的蛋白质和其他分子。他补充说道:该技术可应用于多种疾病研究中。Jaffrey博士说:“我们非常有兴趣研究导致发育障碍如自闭症的大脑神经细胞内的代谢如何是变化的,有很多的机会能让这一新的工具发挥用处”。这篇研究论文的合著者包括威尔康乃尔医学院药理系Jeremy S. Paige博士、Thinh Nguyen Duc博士、Wenjiao Song博士。这项研究由美国国立卫生研究院的生物医学成像和生物研究所以及McKnight基金会资助。康奈尔科技企业和商业中心(CCTEC)已经代表康奈尔大学提出了这项技术的专利保护申请。Samie Jaffrey博士是Lucerna技术的创始人和科学顾问,并持有该公司股权。此外,Lucerna技术拥有上述描述技术的相关许可证。
凝胶成像定义 凝胶成像即:对DNA或RNA胶 进行切胶、拍照、观察、分析 ,的实验室类仪器, 凝胶成像系统可以应用于分子 量计算,密度扫描,密度定量, PCR定量等生物工程常规研究。凝胶成像应用范围 总体上来说凝胶成像可应用于:凝胶成像系统可以用于:蛋白质、核酸、多肽、氨基酸、多聚氨基酸等其他生物分子的分离纯化结果作定性分析 (1)分子量定量 对于一般常用的DNA胶片,利用分子量定量功能,通过对胶上DNA Marker条带的已知分子量注释,自动生成拟合曲线,并以它衡量得到未知条带的分子量。通过这种方法所得到的结果较肉眼观察估计要准确很多。 (2)密度定量 一般常用的测定DNA(脱氧核糖核酸)和RNA(核糖核酸)浓度的方法是紫外吸收法,但它只能测定样品中的总核苷酸浓度,而不能区分各个长度片段的浓度。利用凝胶成像系统和软件,先将DNA胶片上某一已知其DNA含量的标准条带进行密度标定以后,可以方便的单击其他未知条带,根据与已知条带的密度做比较,可以得到未知DNA的含量。此方法也适用于对PA GE蛋白胶条带的浓度测定。 (3)密度扫描 在分子生物学和生物工程研究中,最常用到的是对蛋白表达产物占整个菌体蛋白的百分含量的计算。传统的方法是利用专用的密度扫描,但利用生物分析软件结合现在实验室常规配备的扫描仪或者直接用白光照射的凝胶成像就能完成此项工作。 (4)PCR定量 PCR定量主要是指,如果PCR实验扩增出来的条带不是一条,那么可以利用软件计算出各个条带占总体条带的相对百分数。就此功能而言,与密度扫描类似,但实际在原理上并不相同。PCR定量是对选定的几条带进行相对密度定量并计算其占总和的百分数,密度扫描时并对选择区域生成纵向扫描曲线图并积分。
作为实验室里最为常用的仪器之一,成像设备直接为您的论文提供影像。而这些影像质量的好坏,有时候甚至决定着您的论文能否发表。当然,拥有一台好的、运行稳定的设备也是老板和技术主管的心愿。那么,如何从纷繁的市场上选择到一款好的成像设备呢?很多号称“王牌”的设备是否真的能够打满分呢?下面的文章就向您介绍选择成像系统的“四项基本原则”。有了这些原则,您在选择成像仪时自然成竹在胸,无往不胜。原则一:“只选对的,不选贵的”市场上各品牌、各型号的成像仪林林种种,但是从成像原理上可以分成两大类,分别是拍照成像和扫描成像。拍照成像简单说就是样品和相机的相对位置不动,可以进行单次成像或多次成像;而扫描成像则是相机对样品进行局部成像,然后通过样品或相机的移动对整个样品进行成像。拍照成像目前主要采用CCD相机成像,由于可以设置不同的曝光时间,常被用来进行微弱的化学发光及生物发光的成像。而扫描成像则由于精度高、重复性好被广泛用于大型样品以及多通道成像中。可以说,对于大型样品或多通道应用,能选择扫描成像的,尽量不要选择拍照成像。原理搞清楚了,选择起来就简单了。不同的原理导致了不同应用的最佳选择,所以千万不要相信什么“全能王”之类的鬼话,没有任何一款机器可以通吃所有应用领域。下面就实验室最常见的一些应用简单的说明选择的依据:核酸电泳凝胶:一般此类凝胶都采用EB染色、紫外激发,而且凝胶较小。推荐采用一般的凝胶成像设备即可完成。蛋白电泳凝胶:一般此类凝胶采用考染或银染,白光透射成像。对于小型凝胶您可以选择一般的凝胶成像设备,但是对于大型凝胶,特别是双向电泳凝胶,由于CCD拍照成像会有几何扭曲,而且透镜效应也会导致不同区域的信号强度差异,另外CCD拍照也无法保证不同凝胶的成像参数保持一致,因此扫描成像是最好选择。转印膜:这个稍微有些复杂。一般转印膜有比色法显色、同位素、化学发光和荧光等不同检测手段。比色法显色就是产生有颜色的条带或斑点,一般采用普通的凝胶成像设备即可;同位素可以采用压胶片曝光的方法,但是费时、费力而且容易过饱和,比较通用的方法是由FujiFilm在1981年发明的磷屏成像技术,获得信号潜影的磷屏通过激光扫描就可以获取同位素的信号。而化学发光是目前最常用的蛋白印迹的检测手段,无疑,冷CCD拍照成像对这种微弱的光信号是最合适的。荧光是所有这些检测手段中最令人赞叹的和最有前景的。这不仅仅是因为荧光染料具有最宽的动态范围,而且还在于它能够为我们提供多通路的检测途径(同样适用于凝胶,通用电气公司的2D DIGE技术就是采用三种荧光染料标记蛋白而形成多通路检测的)。当然,您可以使用单一荧光检测,这时您对凝胶成像设备的要求就包括了新的激光光源和相应的滤光片。如果您是一个完美主义者,或者您需要对邻近或重叠的目标分子进行成像,那么多通道荧光检测是您的不二之选。这时扫描成像绝对是最佳选择,这样选择不仅仅是因为扫描成像能够带来更高的灵敏度和分辨率,更重要的是,不同通道之间没有几何扭曲,拟合性好。微孔板及其他特殊需求:对于拍照成像而言,由于几何扭曲的问题,对微孔板成像就变得比较复杂了,一般必须一个专用的校正装置才可完成。当然,如果采用扫描成像一般不需要任何额外附件。很多实验室现在都对小动物成像非常感兴趣,然而对小动物进行真的不是一件简单的事,一方面小动物需要进行麻醉和固定;另一方面还需要对信号位置进行三维定位。因此,能同时提供功能、代谢和解剖图像的PET/CT是进行这类成像的最有力的工具。限于篇幅,这部分将不做更多介绍。原则二:实践是检验真理的唯一标准这可不是在上政治课,每个厂家都对自己的产品是“王婆卖瓜,自卖自夸”,经常给您上两个小时课中间还不用休息,什么“专利技术”、“人性化设计”、“生命科学产业大奖”。只有您想不到的,没有他做不到的。可是,这些东西对用户到底有什么意义?就没有几个人说得清了。好用才是硬道理。任凭你说得天花乱坠,拿来我试试,不就什么都清楚了。现在多数厂商都提供Demo机服务,还有技术人员现场答疑解惑,那就请各位上场,真刀真枪的拼一下,谁的性能好,价格优,那我就要谁的。当然,我们的实际测试结果仅仅是针对我们自己的样品和现场demo的机器而已。我们不能据此对相关品牌和相关型号做太多评判。由于具体应用的限制、操作技巧的差异以及可能的仪器状态的区别,我们有可能没有给出公允的评价。但无论如何,这些讯息对我们采购者和使用者来说都是非常重要的。
[font=&][size=14px]质谱成像(Imaging Mass Spectrometry, IMS)这种最新原位分析技术主要是利用质谱直接扫描生物样品,分析分子在细胞或组织中的“结构、空间与时间分布”信息。其基本流程(以质谱分析生物组织标记物为例)见下: [color=#333333] [/color][/size][/font][img]https://file.jgvogel.cn/134/upload/resources/image/406626.jpeg?x-oss-process=image/resize,w_700,h_700[/img][font=&][size=14px]简单而言,质谱成像技术就是借助于质谱的方法,再配套上专门的质谱成像软件控制下,使用一台通过测定质荷比来分析生物分子的标准分子量的质谱仪来完成的。但是随着这项技术的不断发展,也陆续出现了许多针对各种问题的新技术。[/size][/font][font=&][size=14px]最早的质谱成像技术是基质辅助激光解吸电离(MALDI,matrix assisted laser desorption ionization)质谱分子成像技术,由范德堡大学(Vanderbilt University)的Richard Caprioli等在1997年提出,他们通过将MALDI质谱离子扫描技术与专业图像处理软件结合,直接分析生物组织切片,产生任意指定质荷比(m/z)化合物的二维离子密度图,对组织中化合物的组成、相对丰度及分布情况进行高通量、全面、快速的分析,可通过所获得的潜在的生物标志物的空间分布以及目标组织中候选药物的分布信息,来进行生物标志物的发现和化合物的监控。[/size][/font][font=&][size=14px]正如数字图像包括三个通道:红,绿,蓝一样(单个亮度定义了每个像素的颜色),质谱成像也包含了数以千计的通道,每一个对应于一个特殊的光谱峰值,“你可以通过质谱方法从这些像素中获得任何信号,然后调整图像中所需分子像素的相对亮度,最后,得到一张分子特异性的成像图。”[/size][/font][font=&][size=14px]这种方法可用于小分子代谢物,药物化合物,脂质和蛋白,而且,质谱成像能相对快速的利用许多分子通道,完全无需特殊抗体,下面列出五种先进的质谱成像方法。[/size][/font][font=&][size=14px]1、MALDI质谱分子成像技术[/size][/font][font=&][size=14px]在对组织或生物体进行成像,分析小分子构成的时候,有一个“拦路虎”总是阻碍实验的进程,那就是多肽,这些多肽体积十分大,要想对它们进行分子成像几乎是不可能的,比如,想要研究肿瘤边缘的分子微环境,如果直接成像是不可能获得清晰图像的。[/size][/font][font=&][size=14px]来自范德堡大学的质谱方法专家Richard Caprioli博士因此发明了基质辅助激光解吸电离(MALDI)质谱分子成像技术,这项技术不局限于特异的一种或者几种蛋白质分子,它可在组织切片中找到每一种蛋白质分子,并提供这些蛋白质分子在组织中的空间分布的精确信息,而事先无需知道所检测蛋白的信息。同时,可对这些蛋白质分子含量进行相对定量。[/size][/font][font=&][size=14px]MALDI质谱分子成像是在专门的质谱成像软件控制下,使用一台通过测定质荷比来分析生物分子的标准分子量的质谱仪来完成的。被用来研究的组织首先经过冰冻切片来获得极薄的组织片,接着用基质封闭组织切片并将切片置入质谱仪的靶上。通过计算机屏幕观察样品,利用MALDI系统的质谱成像软件,选择拟成像部分,首先定义图像的尺寸,根据尺寸大小将图像均分为若干点组成的二维点阵,来确定激光点轰击的间距。激光束通过这个光栅图案照射到靶盘上的组织切片,软件控制开始采集质谱数据,在质谱仪中,激光束对组织切片进行连续的扫描,组织样品在激光束的激发下释放出的分子被质谱仪所鉴定从而获得样品上每个点的质荷比(m/z)信息,然后将各个点的分子量信息转化为照片上的像素点。在每个点上,所有质谱数据经平均化处理获得一幅代表该区域内化合物分布情况的完整质谱图。仪器逐步采集组织切片的质谱数据,最后得到具有空间信息的整套组织切片的质谱数据。这样就可以完成对组织样品的“分子成像”。设定m/z的范围,即可确定该组织区域所含生物分子的种类,并选定峰高或者峰面积来代表生物分子的相对丰度。图像中的彩色斑点代表化合物的定位,每个斑点颜色的深浅与激光在每一个点或像素上检测到的信号大小相关。[/size][/font][font=&][size=14px]通过增加单位面积上轰击的激光点数量和像素,研究人员可以获得更多的样品信息,例如,采用4000像素比200像素能够得到更好的样品图像。质谱分子成像技术是一种半定量或相对定量技术,图像上颜色深的部分表明有更多的生物分子聚集在组织的这个部分,然而,不可能据此确定生物分子在组织的不同部位的实际绝对含量。选择组织图像上的任意一个斑点,图像都能够给出一个质谱谱图或者离子谱图,代表在组织的该部位存在这种生物分子,然后,与做指纹图谱类似,像做指纹图谱那样,将样品的离子谱图与已知标准品进行对照,分析差异,从而进行生物标志物的发现和药物作用的监控。[/size][/font][font=&][size=14px]2、电喷雾电离技术[/size][/font][font=&][size=14px]一般质谱成像方法由于体积庞大,重量重,需要冗长的样品准备阶段,因此,并不适用于即时成像(bed side applications),比如,要帮助外科医生进行实时的肿瘤边界成像监控,那么就要寻找新的方法了。[/size][/font][font=&][size=14px]一种称为电喷雾电离技术(desorption electrospray ionization,DESI)的MS成像技术解决了这个问题。DESI技术于2004年首次提出,由于这一方法具有样品无需前处理就可以在常压条件下,从各种载物表面直接分析固相或凝固相样品等优势而得到了迅速的发展。[/size][/font][font=&][size=14px]这种方法的原理是带电液滴蒸发,液滴变小,液滴表面相斥的静电荷密度增大。当液滴蒸发到某一程度,液滴表面的库仑斥力使液滴爆炸。产生的小带电液滴继续此过程。随着液滴的水分子逐渐蒸发,就可获得自由徘徊的质子化和去质子化的蛋白分子DESI与另外一种离子源:SIMS(二次离子质谱)有些相似,只是前者能在大气压下游离化,发明这项技术的普渡大学Cooks博士认为DESI方法其实就是一种抽取方法,即利用快速带电可溶微粒(比如,水或者乙腈acetonitrile)进行离子化,然后冲击样品,获得分析物的方法。[/size][/font][font=&][size=14px]DESI系列产品最大的优势就在于无需样品处理,一般质谱和高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]分析,样品必须经过特殊的分离流程才能够进行分析检测,使得一次样品检测常常需要约一个小时,而DESI系列产品可将固体样品直接送入质谱,溶液被喷射到检测表面,促使样品离子均匀分布。采用这一手段的质谱分离过程,只需3分钟左右即可完成。[/size][/font][font=&][size=14px]3、APIR MALDI/LAESI技术[/size][/font][font=&][size=14px]了解细胞的内部成分是理解健康细胞不同于病变细胞的关键,但是,直到目前为止,唯一的方法是观察单个细胞的内部,然后将其从动物或植物中移除,或者改变细胞的生存环境。但是这么做的话,会使细胞发生变化。科学家还不是很清楚一个细胞在病变时与健康细胞的差别,或者当它们从一个环境移到另一个环境中产生的变化。[/size][/font][font=&][size=14px]来自华盛顿大学Akos Vertes教授希望能从另外一个方面来进行活细胞分析,在他的一项关于活叶样品中初级和次级代谢产物分布的研究中,研究人员发现叶片中积累基质很厚,常导致光谱末端低分子量部分模糊,而且基质辅助激光解析电离(MALDI)质谱分析需要在真空中进行,但是,活体样本在真空中无法存活。[/size][/font][font=&][size=14px]实际上,MALDI质谱分析的原理是将分析物分散在基质分子中并形成晶体,当用激光照射晶体时,由于,基质分子经辐射所吸收的能量,导致能量蓄积并迅速产热,从而使基质晶体升华,致使基质和分析物膨胀并进入[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相[/color][/url]。而生物样品也可以直接吸收能量的,比如,2.94mm波长的光能激活水中氢氧键。[/size][/font][font=&][size=14px]因此,Vertes等人想到复合两种技术来解决这一问题。首先他们利用大气压红外线(an atmosphericpressure infrared,APIR)MALDI激光直接激活组织中的水分,使样品气化,就像是组织表面发生了细胞大小的核爆炸,从而获得了离子化微粒,进入质谱中进行分析。但是并不是所有的气化微粒都带电,大部分其实是不带电的,会被APIR MALDI遗漏。[/size][/font][font=&][size=14px]为了捕捉这些中性粒子,Vertes等人采用了第二种方法:[/size][/font][font=&][size=14px]LAESI(laser ablation electrospray ionization,激光烧蚀电喷雾电离),这种方法能捕捉大量带电微滴的微粒,然后重新电离化。通过对整个样品进行处理,复合这两种方法,就能覆盖更多的分子,分析质量更高。[/size][/font][font=&][size=14px]与一般质谱成像过程不同,Verte的方法还在成像中增加了高度,从而实现了3D代谢物成像。这项技术的分辨率是直径10mm,高度30mm,这与生物天然的立体像素相吻合,这样科学家们就可以获得天然构像。[/size][/font][font=&][size=14px]4、二次离子质谱技术[/size][/font][font=&][size=14px]质谱成像技术能将基质辅助激光解吸电离质谱的离子扫描与图像重建技术结合,直接分析生物组织切片,产生任意质荷比(m/z)化合物的二维或三维分布图。其中三维成像图是由获得的质谱数据,通过质谱数据分析处理软件自动标峰,并生成该切片的全部峰值列表文件,然后成像软件读取峰值列表文件,给出每个质荷比在全部质谱图中的命中次数,再根据峰值列表文件对应的点阵坐标绘出该峰的分布图。[/size][/font][font=&][size=14px]但是,一般的质谱成像技术不能对一些携带大分子碎片的化学成分进行成像,来自宾夕法尼亚州州立大学的NicholasWinograd教授改进了一种称为二次离子质谱(SIMS,secondary ion mass spectrometry)的方法,可以对样品进行完整扫描,三维成像。[/size][/font][font=&][size=14px]SIMS早在用于生物学研究之前就已经应用广泛了,比如,分析集成电路(integratedcircuits)中的化学成分,这种质谱技术是表面分析的有利工具,能检测出微小区域内的微量成分,具有能进行杂质深度剖析和各种元素在微区范围内同位素丰度比的测量能力。[/size][/font][font=&][size=14px]这种技术具有几个优点:[/size][/font][font=&][size=14px]速度快(-10,000 spectra per second),亚细胞构造分辨率(-100nm),以及不需要基质。但是另外一方面,不同于MALDI方法,SIMS方面不是一种“软”技术,这种方法只能对小分子成像,因此常常需要进行粉碎。[/size][/font][font=&][size=14px]Winograd教授改进了这一方法,他利用了一种新型SIMS光束(carbon-60磁性球),这种新光束比传统的SIMS光束对物体的化学损伤更小。C60同时撞击样品表面,类似于“一阵爆炸”,这样重复的轰击使得研究人员能深入样品,进行三维分子成像,Winograd教授称这个过程是“分子深度成像”(molecular depth profiling)。[/size][/font][font=&][size=14px]C60的能量与其它的离子束相当,却不到达样品表面以下,这样样品可以连续地被逐层剥离,研究人员就可以得到纵面图形,最终获得三维的分子影像。Winograd教授等人用含有肽的糖溶液将硅的薄片包裹起来并进行SIMS实验,随着薄膜逐渐被C60剥蚀,可以获得糖和肽的稳态信号。最终,薄膜完全剥离后就可以获得硅的信号。如果用其它的射线或原子离子代替C60,粒子束会快速穿过肽膜而无法提供有关生物分子的信息。因此,这种方法具有良好的空间分辨率,能够获得巨噬细胞和星型细胞的细胞特征和分析物的分布情况。[/size][/font][font=&][size=14px]这里还要说到一点,SIMS和上一技术(APIR MALDI/LAESI技术)都可以对三维成像,但两者也有差别,SIMS方法中,采用高能离子轰击样品,逐出分析物离子(二级离子),离子再进入质量分析器。MALDI方法则用激光辐射样品使之离子化,另外SIMS探针可以探测到100nm的深度,能提供纳米级的分辨率,而MALDI可以探测更深,但空间分辨率较低。[/size][/font][font=&][size=14px]5、纳米结构启动质谱技术[/size][/font][font=&][size=14px]质谱在检测生物分子方面有很大潜力,但现有方法仍存在一些缺陷,灵敏度不够高和需要基质分子促使分析对象发生离子化就是其中之二。比如说,需要溶解或者固定在基质上的方法检测代谢物,较易错判,因为这些代谢物与那些基质常常看上去都一样。另外基于固定物基质的系统也不允许研究人员精确的判断出样品中某一分子到底来自于哪儿。[/size][/font][font=&][size=14px]来自斯克利普斯研究院的Gary Siuzdak博士发明了一种称为纳米结构启动质谱(nanostructure-initiator mass spectrometry,NIMS)的新技术,这种技术能以极高的灵敏度分析非常小的区域,从而允许对肽阵列、血液、尿和单个细胞进行分析,而且还能用于组织成像。 [/size][/font][font=&][size=14px]NIMS利用了一种特制的表面,这种多孔硅表面上聚集了一种含氟聚合物,这些分子在受到激光或离子束照射时会猛烈爆发,这种爆发释放出离子化的分析物分子,它们被吸收到表面上,使其能够被检测到。这种方法利用激光或离子束来从纳米尺度的小囊中气化材料,从而克服了一般质谱方法缺少所需的灵敏度和需要基质分子促使分析对象发生离子化的缺陷。 [/size][/font][font=&][size=14px]通过这种方法可以分析很多类型的小分子,比如,脂质,糖类,以及类固醇,虽然每一种分析材料需要的含氟聚合物有少许差别,但是这是一种一步法的方法,比MALDI简单多了——后者需要固定组织,并添加基质。 [/size][/font][font=&][size=14px]由于,含氟聚合物不能很好的离子化,因此,会发生轻微的光谱干扰,而且由于离子化过程是“软性”的——就像MALDI,所以NIMS产生的生物分子是整块离子化,而不是片段离子化。不过这种技术对于完整蛋白的检测灵敏度没有MALDI高[/size][/font]
[color=#000000]2024年3月15日,国家标准GB/T 43688-2024《磁共振成像/波谱仪质量控制方法》正式发布,于2024年10月1日正式实施。该标准由TC487(全国光电测量标准化技术委员会)归口 ,主管部门为中国科学院。[/color][color=#000000]该标准主要起草单位:中国计量科学研究院 、北京大学第三医院 、上海联影医疗科技股份有限公司 、中国科学院空天信息创新研究院 、广东省中量检测有限公司 、北京大学 、北京航空航天大学 、北京万东医疗科技股份有限公司 、重庆大学 、中国计量大学 、美的集团(上海)有限公司 、北京印刷学院 、广东省建筑设计研究院有限公司 、广州计量检测技术研究院 、山东第一医科大学 。[/color][color=#000000]本标准从国内外磁共振影像和放疗设备的生产、临床使用情况出发,研究可溯源至国际单位制(SI)的设备性能评价方法并将其标准化。[/color][color=#000000]2013 年底我国MRI 的市场保有量已达到6400台,以目前速度,我国MRI市场容量将在2017 年应可突破万台大关。[/color][color=#000000]国内磁共振企业在规模和技术水平上也逐步得到发展,无论低场,还是高场1.5TMRI 系统都已有自主研发机型生产,并上市销售;生产企业也由原来的少数几家发展到近20家,但国内市场,尤其是中高端市场,仍以通用电器、西门子、飞利浦等公司的磁共振成像产品占据绝对优势。[/color][color=#000000]本标准构筑提升了我国磁共振设备质控的基础,并为其它重大数字诊疗装备质控提供了共性技术支撑。[/color][来源:仪器信息网] 未经授权不得转载[align=right][/align]
光学技术作为一种无损的检验方法,在物证的发现、记录、提取、检验、鉴定和保全等各个方面都发挥着重要的作用。刑事影像技术方向的主要任务是利用先进的光学技术获取与物证相关的影像资料,通过区分物质的方法得到物证的清晰影像以及深入挖掘能够揭示案件事实真相的物证信息。http://www.zolix.com.cn/filespath/images/20150812153905.jpg 光谱成像技术能够根据不同物质光谱特征准确记录其空间分布状态,为物证鉴定光学检验提供了将形态检验和成分检验相结合的机会。 目前公安部物证鉴定中心有关光谱成像技术的研究已获得5项国家级科研项目资助,1项部级科研项目资助。已经在“十一五"和“十二五"国家科技支撑计划实施阶段,成功实现了科研衔接和可持续性研究态势。基于以上成果及未来的发展趋势,公安部物证鉴定中心与中国工程物理研究院以及卓立汉光旗下的四川双利合谱科技有限公司联合成立多光谱成像侦查技术联合实验室,将进一步促进和推广多光谱成像技术在刑侦领域的应用。基于联合实验室的平台,将逐步的建立光谱成像测试标准以及物证光谱数据库及数据分析网络服务器。http://www.zolix.com.cn/filespath/images/20150812153808.jpg 适用范围: 通过研究证明,光谱成像技术能够应用于痕迹检验、文件检验、微量物证检验、生物物证发现等物证鉴定领域多个专业的工作中。正是由于光谱成像技术适用性强的特点,体现出这项技术深入研究的价值和推广普及的潜力。http://www.zolix.com.cn/filespath/images/20150812153829.jpg 目前,国内技术人员,应用不同波段范围、不同工作原理的光谱成像技术,针对不同检验对象,进行了大量实验研究,均已取得一定的研究进展,具体研究情况整理如下http://www.zolix.com.cn/filespath/images/20150812153847.jpg
成像和成像有什么区别
[i][font='Times New Roman'][font=宋体]引言[/font][/font][/i][font='Times New Roman'][font=宋体]在上一期的专栏里[/font][/font][font=宋体],我们对荧光成像和生物发光的基本原理进行了对比。同时也留下了几个问题:[/font][font='Times New Roman'][font=宋体]针对我的课题[/font][/font][font=宋体],生物发光和荧光成像哪个好?什么情况下选择生物发光,什么情况下选择荧光成像。别急,今天将为大家解答关键问题:[/font][b][font=宋体][color=#ff0000]荧光成像和生物发光成像的优缺点是什么?[/color][/font][/b][align=center][font='Times New Roman']一、 [/font][b][font=宋体]荧光成像技术的优点[/font][/b][/align][font='Times New Roman'][font=宋体]相比生物发光成像[/font][/font][font=宋体],[/font][font='Times New Roman'][font=宋体]荧光成像技术的优势主要表现在[/font][/font][font=宋体]:[/font][font='Times New Roman']1. [/font][b][font='Times New Roman'][font=宋体]荧光蛋白及荧光染料的标记能力更强[/font][/font][font=宋体]。[/font][/b][font=宋体]荧光标记分子种类繁多,包括荧光蛋白、荧光染料、量子点标记等,可以对基因、蛋白、抗体、化合药物等进行标记。[/font][font=宋体][color=#ff0000]应用范围极广[/color][/font][font=宋体],可以对样本进行[/font][font=宋体][color=#ff0000]多色标记[/color][/font][font=宋体],一个样本同时获得多种细胞或药物的分布[/font][font=宋体]。[/font][font='Times New Roman']2. [/font][b][font='Times New Roman'][font=宋体]信号强度[/font][/font][font=宋体]高[/font][/b][font=宋体]由于荧光成像的[/font][font=宋体][color=#ff0000]光子强度较生物发光更强[/color][/font][font=宋体][font=宋体],持续时间长,对[/font]C[/font][font='Times New Roman']CD[/font][font=宋体]的灵敏度要求相对较低,不需要必须配备低温冷[/font][font='Times New Roman']CCD[font=宋体]即可获得清晰的成像结果,节省实验成本和购置成本。[/font][/font][font='Times New Roman']3. [/font][b][font='Times New Roman'][font=宋体]实验成本低[/font][/font][font=宋体],[/font][font='Times New Roman'][font=宋体]成像过程简单[/font][/font][/b][font='Times New Roman'][font=宋体]相比生物发光成像,成像前无需注射荧光素酶底物。有合适的激发光源照射就可以发出特定波长的发射光[/font][/font][font=宋体]。[/font][font='Times New Roman'][font=宋体]只要荧光基团稳定,就可实现[/font][/font][font='Times New Roman'][color=#ff0000][font=宋体]随时激发随时发光随时检测[/font][/color][/font][font='Times New Roman'][font=宋体]。[/font][/font][font='Times New Roman']4. [/font][b][font=宋体]从活体到离体均可成像[/font][/b][font=宋体][font=宋体]相比生物发光只能在活细胞内才会产生发光。荧光蛋白或荧光染料只需要保持荧光基团稳定即可稳定发光。可以在活体或离体组织器官进行观察,在实验前期荧光材料制备阶段,可以直接在[/font]E[/font][font='Times New Roman']P[font=宋体]管中进行成像观察[/font][/font][font=宋体]。[/font][font='Times New Roman']5. [/font][b][font=宋体]应用范围广[/font][/b][font=宋体]相比生物发光成像,荧光成像技术应用范围极广。在肿瘤生长与转移、药物的分布与代谢、纳米颗粒的靶向性与代谢、植物基因的表达、生物相容性材料开发、新型标记技术的开发等多个研究中均可用到荧光成像技术。([/font][font=宋体][color=#ff0000][font=宋体]点击了解[/font]FOBI[font=宋体]整体荧光成像在上述领域的应用[/font][/color][/font][font=宋体])[/font][align=center][font='Times New Roman']二、 [b][font=宋体]生物发光技术的优点[/font][/b][/font][/align][font='Times New Roman'][font=宋体]相比荧光成像[/font][/font][font=宋体],生物发光成像的主要优势表现在:[/font][b][font=宋体]1[font=宋体]、特异性强,无自发荧光[/font][/font][/b][font=宋体]以荧光素酶作为体内报告源的生物发光方法,特异性极强。由于动物本身没有任何自发光,使得生物发光具有极低的背景和极高的信噪比。[/font][b][font=宋体]2[font=宋体]、[/font][/font][font='Times New Roman'][font=宋体]高灵敏度[/font][/font][/b][font='Times New Roman'][font=宋体]由于生物体内很多物质在激发光的照射[/font][/font][font=宋体]下[/font][font='Times New Roman'][font=宋体]也会发出荧光[/font][/font][font=宋体],[/font][font='Times New Roman'][font=宋体]这些非特异性荧光背景会影响检测灵敏度[/font][/font][font=宋体],[/font][font='Times New Roman'][font=宋体]荧光成像的灵敏度最高可在动物体内检测到约[/font]10[/font][sup][font='Times New Roman']4[/font][/sup][font='Times New Roman'][font=宋体]细胞,而生物发光具有在动物体内监测[/font]10[/font][sup][font='Times New Roman']2[/font][/sup][font='Times New Roman'][font=宋体]数量级细胞的灵敏度。[/font][/font][b][font=宋体]3[font=宋体]、检测深度更高[/font][/font][/b][font='Times New Roman'][font=宋体]对于需要在深部[/font][/font][font=宋体]组织[/font][font='Times New Roman'][font=宋体]下进行的研究(检测的深度在[/font]3~4cm[font=宋体])[/font][/font][font=宋体],[/font][font='Times New Roman'][font=宋体]应用生物发光是最佳的选择[/font][/font][font=宋体]。[/font][b][font=宋体]4[font=宋体]、[/font][/font][font='Times New Roman'][font=宋体]精确定量[/font][/font][/b][font=宋体]由于荧光素酶基因是插入细胞染色体中稳定表达的,单位细胞的发光数量、发光条件相对稳定。即使标记细胞在动物体内有复杂的定位,亦可从动物体表的信号水平测量出发光细胞的相对数量。[/font][font='Times New Roman'][color=#ff0000][font=宋体]荧光成像和生物发光技术[/font][/color][/font][font=宋体][color=#ff0000],[/color][/font][font='Times New Roman'][color=#ff0000][font=宋体]是互为补充[/font][/color][/font][font=宋体][color=#ff0000],[/color][/font][font='Times New Roman'][color=#ff0000][font=宋体]分别满足不同的研究领域[/font][/color][/font][font=宋体][color=#ff0000]。对于不同的研究,可根据两者的特定及实验要求,选择合适的方法。[/color][/font][table][tr][td][font='Times New Roman'] [/font][/td][td][align=center][font='Times New Roman']优点[/font][/align][/td][td][align=center][font=宋体]缺点[/font][/align][/td][/tr][tr][td][align=center][font=宋体]荧光成像技术[/font][/align][/td][td][font=Wingdings][color=#333333]2 [/color][/font][font=Verdana][color=#333333]荧光染料、蛋白标记能力强,可用于多重标记[/color][/font][font=宋体][color=#333333],[/color][/font][font=Verdana][color=#333333]信号强度大,成像速度快[/color][/font][font=宋体][color=#333333]。[/color][/font][font=Wingdings][color=#333333]2 [/color][/font][font=Verdana][color=#333333]实验成本低[/color][/font][font=宋体][color=#333333]。[/color][/font][font=Wingdings][color=#333333]2 [/color][/font][font=宋体][color=#333333]体内、体外,器官、活体均可成像。[/color][/font][font=Verdana][color=#333333] [/color][/font][font=Wingdings][color=#333333]2 [/color][/font][font=Verdana][color=#333333]应用范围极广[/color][/font][/td][td][font=Wingdings][color=#333333]n [/color][/font][font=Verdana][color=#333333]非特异性荧光限制了灵敏度,体内检测最低约[font=Verdana]104[/font][font=宋体]细胞[/font][/color][/font][font=宋体][color=#333333]。[/color][/font][font=Wingdings][color=#333333]n [/color][/font][font=Verdana][color=#333333]检测深度受限制[/color][/font][font=宋体][color=#333333],[/color][/font][font=Verdana][color=#333333]较难精确体内定量[font=Verdana] [/font][/color][/font][font=宋体][color=#333333]。[/color][/font][/td][/tr][tr][td][align=center][font=宋体]生物发光技术[/font][/align][/td][td][font=Wingdings][color=#333333]2 [/color][/font][font=Verdana][color=#333333]特异性强,无自发荧光[/color][/font][font=宋体][color=#333333],[/color][/font][font=Verdana][color=#333333]背景低[/color][/font][font=宋体][color=#333333]。[/color][/font][font=Wingdings][color=#333333]2 [/color][/font][font=Verdana][color=#333333]高灵敏度,在体内可检测到几百个细胞[/color][/font][font=Wingdings][color=#333333]2 [/color][/font][font=Verdana][color=#333333]可精确定量[/color][/font][font=宋体][color=#333333]。[/color][/font][/td][td][font=Wingdings][color=#333333]n [/color][/font][font=Verdana][color=#333333]信号较弱,检测时间较长,需要灵敏的[font=Verdana]CCD[/font][font=宋体]镜头,仪器价格贵[/font][/color][/font][font=宋体][color=#333333]。[/color][/font][font=Wingdings][color=#333333]n [/color][/font][font=Verdana][color=#333333]要求高[/color][/font][font=宋体][color=#333333],[/color][/font][font=Verdana][color=#333333]需要注入荧光素,实验成本高[/color][/font][font=宋体][color=#333333]。[/color][/font][font=Wingdings][color=#333333]n [/color][/font][font=宋体][color=#333333]只能用于细胞标记,应用范围窄。[/color][/font][/td][/tr][/table][i][font=宋体]结束语[/font][/i][font=宋体]随着活体成像技术的发展特别是荧光标记技术的发展,越来越多的生物学研究需要用到活体光学成像的方法。无论大家是选择生物发光或者荧光成像技术,苦恼总是随之而来,例如:[/font][font=宋体][color=#ff0000]生物素在体内可以维持多长时间?荧光蛋白和染料种类繁多,我该怎样选择呀?[/color][/font][font=宋体][font=宋体]别急,下期我们继续为大家介绍关于活体成像技术应用与选择的问题与难点。[/font][/font][font=宋体][font=宋体][url=http://dwz.date/cwes]点击了解更多活体成像技术的应用与仪器信息![/url][/font][/font][align=center][font='Times New Roman'][font=宋体]参考文献[/font][/font][/align][font='Segoe UI'][color=#222222]1. [/color][/font][font='Segoe UI'][color=#222222]Su, Y., Walker, J.R., Park, Y. [/color][/font][i][font='Segoe UI'][color=#222222]et al.[/color][/font][/i][font='Segoe UI'][color=#222222] Novel NanoLuc substrates enable bright two-population bioluminescence imaging in animals. [/color][/font][i][font='Segoe UI'][color=#222222]Nat Methods[/color][/font][/i][font='Segoe UI'][color=#222222] [/color][/font][b][font='Segoe UI'][color=#222222]17, [/color][/font][/b][font='Segoe UI'][color=#222222]852–860 (2020). [/color][/font][font='Segoe UI'][color=#222222]2. [/color][/font][url=#!][font='Segoe UI'][color=#222222]M.Keyaerts[/color][/font][/url][url=#!][font='Segoe UI'][color=#222222]V.Caveliers[/color][/font][/url][url=#!][font='Segoe UI'][color=#222222]T.Lahoutte[/color][/font][/url][font='Segoe UI'][color=#222222] [/color][/font][url=https://www.sciencedirect.com/science/referenceworks/9780444536334][font='Segoe UI'][color=#222222]Comprehensive Biomedical Physics[/color][/font][/url][font=等线][color=#222222] [/color][/font][url=https://www.sciencedirect.com/science/referenceworks/9780128012383][font='Segoe UI'][color=#222222]Volume 4[/color][/font][/url][font='Segoe UI'][color=#222222], 2014, Pages 245-256.[/color][/font]
[b]摘要[/b]在神经科学和神经外科中对活体大脑组织中神经元的成像能力是一项基本要求。尤其是需求一种具有测微计尺分辨率的大脑形态学的非侵入探针的开发,因为它可以在临床诊断上提供一种非侵入式光学活体组织检查的手段。在这一领域,双光子激光扫描显微镜(2PLSM)是一个强大工具,并已成为活体生物样品最小侵入性损害的高分辨率成像的标准方法。但是,(2PLSM)基于光学方法提供足够分辨率的同时,对荧光染料的需求妨碍了图像对比度的提高。本文中,我们提供了一种活体大脑组织以细胞分辨率的高对比度成像方法,无需荧光探针,使用光学三次谐波发生进行成像。我们利用细胞水平的特殊几何学和大脑组织的液体内容物来获取THG的部分相匹配,提供了一种荧光对比度机制的替代方法。我们发现THG大脑图像允许快速、无侵入性标记的神经元、白质结构、血管同时成像。而且,我们利用THG成像来引导微吸管指向活体组织中指定的神经元。这个工作是一个无标记活体大脑成像的主要步骤,并开启了活体大脑中激光引导的微注射技术发展的可能性。[b]材料与方法[/b]THG成像对于THG成像实验,我们使用了一台商业化双光子激光扫描显微镜([color=#ff0000]TrimScope, Lavision BioTec[/color])。光源是一个光学参量震荡器(Mira-OPO,APE),810nm泵浦光来自一个Ti:Sa锁模激光器(Coherent Chameleon Ultra II)。使用一个20X,0.95N.A水浸物镜(Olympus XLUMPFL-IR)将光聚焦到样品上。使用epidetection几何学描述THG实验。使用分光镜(Chroma T800lpxrxt)将背景散射THG光子从入射激光束中分离出来,用一个THG波段的带通滤波器(Chroma HQ390-70X)过滤。检测器是GaAsP高灵敏度光电倍增管(Hamamatsu H7422-40),400nm处量子效率为25%。最高分辨率成像(1024×1024像素)的典型获取时间为1.6s,我们用于目标定向实验的512 X 512像素成像时间为0.6s。 为与前向端口比较,使用了一个定制的投射端口。这个端口使用了一个1.4N.A油浸物镜,一个长波分光镜(UQG optics)和一个400nm的相干窄带滤波器。对于THG与SR-101联合实验我们用1200nm的OPO来同时产生两种信号。使用一个594nm带通和561nm隔断的分光镜将SR-101荧光从THG信号中分离。SR-101信号使用一个PMT检测(Hamamatsu H6780-20)。Nile Red和THG成像也是由1200nm的OPO同步激发。在这个案例中THG信号由投射端口测量,Nile Red荧光通过一个593∕40 nm的带宽滤波器检测。对于THG和GFP联合成像,用来泵浦OPO的Ti:Sa激光被调谐到970nm并耦合到显微镜中。组织块的GFP和THG信号使用同一个检测器连续测量。但使用一个不同的(561∕40 nm)带通滤波器检测GFP。使用显微镜软件(Imspector Pro)获取图像并以16bit 的tiff格式存储,图像分析使用Image J(MacBioPhotonics)进行。[b]主要结果[/b] [img=,575,768]http://qd-china.com/uploads/bio-product/21.jpg[/img]Fig. 1.无标记活体大脑的三次谐波显微成像(A)脑组织THG成像的epidetection几何学图示。插图:THG原理。注意基质中没有光学激发发生。(B) 树突处的聚焦激光束。通过将激光聚焦体积设定到树突直径的几倍大小,可以获得部分相匹配,显著的THG信号将会产生。(C)细胞体内的聚焦激光束。由于不好的结构相匹配状态,没有THG信号产生。(D) 小鼠大脑组织的活神经元成像。体细胞以暗影存在。 [img=,466,500]http://qd-china.com/uploads/bio-product/22.jpg[/img]Fig. 2.活体大脑组织的THG成像(A)小鼠皮质的THG图像 (B) 与A同位置的Nile Red染色的双光子荧光图像 (C) 大鼠凹陷的脑回THG图像(水平切面) (D)小鼠脑胼胝体THG图像,轴突纤维束被清晰得分辨。Movie S1是这个结构的一个3D投影 (E)小鼠大脑纹状体的THG图像(冠状面)。白质和神经元细胞清晰可见。明亮的粒状结构是垂直穿行图像平面的轴突纤维。Movie S2是这个区域的3D投影。(F)麻醉活小鼠的脑皮质上层的血管THG图像(z栈平均投影密度是50um) [img=,510,767]http://qd-china.com/uploads/bio-product/23.jpg[/img]Fig. 3. THG与双光子成像的叠加 (A)小鼠额前叶脑皮质的THG图像 (B)SR-101标记的星细胞双光子图像 (C) A、B的叠加提供了神经网络中星细胞的分布信息 (D) 小鼠额前叶皮质的THG图像 (E) GFP标记的生长抑素神经元的双光子荧光图像 (F)D、E的叠加显示了生长抑素神经元在脑前叶皮质结构中的分布 [img=,461,768]http://qd-china.com/uploads/bio-product/24.jpg[/img]Fig. 4.THG成像深度与自动化细胞检测 (A-C) 小鼠额前叶皮质的THG图像,成像深度分别为100, 200, and 300 μm 。每幅图像都是3个以2微米深度间隔独立图像的最大密度投影(D) 110 μm深度处神经元细胞的自动检测THG图像。细胞检测的运算法则定义为以红色显示的神经元 (E)红色标记:来自A-C的图像栈的细胞可见性对比。黑色标记:作为一个深度功能的平均检测到的THG密度。 [img=,531,768]http://qd-china.com/uploads/bio-product/25.jpg[/img]Fig. 5. 无标记目标定向和细胞活性(A)小鼠新大脑皮层的THG图像 (B) 在对一个神经元进行THG引导膜片钳之后同一位置的THG图像 (C)一个200um深处钳住神经元的大视野THG图像(5幅深度间隔2um的图像平均) (D)记录以100pA电流脉冲刺激B中被钳住的神经元的动力势训练 (E) 测量在THG扫描期间静止膜电位的改变。即使以最高的能量,也只观察到4%的电压变化,保持了完全的可逆性。0.8秒的周期相应于图像扫描时间。(F)最大观察到的静止膜电位Vs扫描时的激光能量。没有非线性效应出现。
12月20日,美国匹兹堡大学的研究人员基于量子测量和纳米技术的界面工作,实现了由钻石晶体包裹的单个电子组成的纳米级磁成像的重要进展。研究人员表示,被认为是计算任务“动力室”的量子计算或许也可应用于高精度测量等纯电子工业以外的其他领域。 该校物理学和天文学系的助理教授古鲁德弗·达特表示,该纳米磁共振成像技术可针对单个分子或细胞内的一群分子进行扫描。传统的磁共振成像技术在这种分子层面不能很好工作,因此需要创建一种新设备来适应这种高精密度观测的需求。 在构建这种装置中,科研团队面临的一个重大挑战是:需要在钻石晶体内利用单个电子的共振准确测量出磁场。共振是指一个物体在特定频率下,以最大振幅做出摆动的倾向,自然中存在着很多共振的现象,例如乐器的音响共振、摆钟共振和电路的共振等。共振十分强大,物理学家可用其对力、质量和电磁场等进行灵敏测量,但共振也限制了人们可以准确测量的最大磁场范围,在磁成像中,物理学家只能从接近传感器共振频率的分子处探测到狭长的磁场,使成像过程变得更加困难。 科研人员利用量子计算的方法避开了硬件上的不足,以便能观测到整个磁场。与此前使用的标准技术相比,通过扩展磁场,科学家能将最大可探测场强和精度之间的比例提升10%。这使科研团队离研发出纳米级的磁共振设备又近了一步,届时科学家能够以非侵入的方式,研究分子、材料和细胞等的属性,在不伤害原子的情况下,显示它们所处的位置。而目前类似研究所采用的方法都不可避免地会破坏样本。 研究人员表示,以上只是初步结果,他们期望在日后更多的研究中获得更多成果。达特表示:“这对于我们理解分子或活体细胞等具有直接影响。我们的工作显示量子计算也可以超越纯电子设备领域,为高精度测量取得进展扫清基本的路障。”
什么叫"成像无光谱,光谱不成像"简单说就是,,成像光谱仪比以前有么关键性的技术。。 [b]问题补充:[/b]成像光谱仪之前是什么仪??
[b][size=4]利用双(2, 4, 6)三氯苯基过氧化草酸酯( TCPO) 2过氧化氢(H2O2 ) 2咪唑2荧光探针的化学发光体系,研究了荧光探针化学发光成像,对几种常用的荧光探针(丁基罗丹明、罗丹明B、罗丹明6G、荧光素及异硫氰酸荧光素等)进行了定量分析。本方法具有高灵敏度、成像分析高通量等优点,线性范围宽,检出限达10 - 11mol/L。对四甲基异硫氰酸罗丹明(TR ITC)标记的单克隆羊抗人IgG的化学发光成像分析,比相同条件下荧光成像的检出限低一个数量级。[/size][/b]
一、前沿2009年10月6日,瑞典皇家科学院宣布,将2009年诺贝尔物理学奖的一半授予美国科学家威拉德• 博伊尔和乔治• 史密斯,因为他们于1969年发明了半导体集成电路成像技术,CCD感应器。经过四十年的发展,CCD技术由实验室逐步走向了市场,具有越来越广阔的应用。CCD数码成像对摄影产生了革命性的影响。在感光胶片之外,人们可以通过电子电路捕捉图像,这些以数字形式存在的图像更加易于处理和分发。数字图像已经成为许多研究领域中不可替代的重要工具。数码成像技术应用到显微镜上,以替代以往的胶卷拍摄,现在已经广泛应用了。以前我们用胶卷来进行显微拍摄,要等一卷拍完,冲洗出来才能确定拍摄的图像是否清晰,如果拍摄的图像不理想,而显微观察的样品又失效了,就需要重新制作样品,给研究工作带来很大的不便,而现在使用显微数码相机来拍摄显微图像,所见即所得,当时就是保存处理,甚至统计分析,极大的提高了工作效率。二、显微数码成像系统的组成显微数码成像系统包括CCD/CMOS专业相机,图像采集处理软件,显微镜接口,数据传输线等,其中最核心的设备是CCD和CMOS图像传感器,前者由光电耦合器件构成,后者由金属氧化物器件构成。两者都是光电二极管结构感受入射光并转换为电信号,主要区别在于读出信号所用的方法。CCD(Charge Coupled Device ,感光耦合组件)上感光组件的表面具有储存电荷的能力,并以矩阵的方式排列。当其表面感受到光线时,会将电荷反应在组件上,整个CCD上的所有感光组件所产生的信号,就构成了一个完整的画面。CCD的结构分三层 ,第一层“微型镜头”“ON-CHIP MICRO LENS”,这是为了有效提升CCD的总像素,又要确保单一像素持续缩小以维持CCD的标准面积,在每一感光二极管上(单一像素)装置微小镜片。CCD的第二层是“分色滤色片”,目前有两种分色方式,一是RGB原色分色法,另一个则是CMYG补色分色法。原色CCD的优势在于画质锐利,色彩真实,但缺点则是噪声问题。第三层:感光层,这层主要是负责将穿过滤色层的光源转换成电子信号,并将信号传送到影像处理芯片,将影像还原。数码成像的核心器件除CCD,现在越来越多的使用CMOS(Complementary Metal-Oxide Semiconductor,互补性氧化金属半导体,CMOS和CCD一样同在数码相机中可记录光线变化的半导体。CMOS传感器中每一个感光元件都直接整合了放大器和模数转换逻辑,当感光二极管接受光照、产生模拟的电信号之后,电信号首先被该感光元件中的放大器放大,然后直接转换成对应的数字信号。CMOS的优势在于成本低,耗电需求少,便于制造, 可以与影像处理电路同处于一个芯片上,缺点是较容易出现杂点。三 显微镜成像系统相关参数对CCD/CMOS数码成像系统的结构和原理有了一个基本了解后,我们再对成像系统的一些基本参数作一个说明。在实际应用中,很多用户对像素多少很敏感,一上来就提到我要多少万像素的成像系统,其实在专业成像应用中,像素多少只是影响成像的一个因素,还有其他很多指标,包括分辨率,感光器件大小,动态范围,灵敏度,量子效率,信噪比等。感光器件的面积大小是衡量显微成像系统质量的一个重要指标,感光器件的面积越大,捕获的光子越多,感光性能越好,信噪比越低。当前数码成像系统中较常应用的感光器件规格如下:1英寸(靶面尺寸为宽12.7mm*高9.6mm,对角线16mm),2/3英寸, 1/2英寸,1/3英寸,另外有时也用到1/1.8英寸,1/2.5英寸的CCD/CMOS感光器件。 像素是CCD/CMOS能分辨的最小的感光元件,显微数码成像系统的像素由低到高有:45万左右,140万左右,200万左右,300万左右,500万左右,900万像素,甚至还有更高的达到2000万像素以上。一般来说,像素越高,图像分辨率越高,成像也就越清晰,但有时候图像分辨率达到一定程度后,就不是影响成像质量的主要指标了。比如图像分辨率高,噪声也很高时,成像质量也不会很好。暗电流是导致CCD噪音的很重要的因素。暗电流指在没有曝光的情况下,在一定的时间内,CCD传感器中像素产生的电荷。我们在做荧光拍摄的时候,需要的曝光的时候比较长,这样导致CCD产生较多的暗电流,对图像的质量影响非常大。通常情况下通过降低CCD的温度来最大限度的减少暗电流对成像的影响。Peltier制冷技术一般可将CCD温度降低5-30°C,在长时间拍摄或一次曝光超过5-10秒,CCD芯片会发热,没有致冷设备的芯片,“热”或者白的像素点就会遮盖图像,图像会出向明显的雪花点。CCD结构设计、数字化的方法等都会影响噪音的产生。当然通过改善结构、优化方法,同样能减少噪音的产生。显微荧光或其他弱光的拍摄对CCD噪音的降低要求很高,应选用高分辨率数字冷却CCD成像系统,使其能够捕获到信号极其微弱的荧光样品图像,并且能够最大程度的降低噪音,减少背景,提供出色的图像清晰度。所以一般在荧光及弱光观察时需要选择制冷CCD。在显微数码成像过程中,对于荧光及弱光的拍摄,除了制冷降低热噪声外,还可使用 BINNING技术提高图像的灵敏度,BINNING像素合并是一种非常有用的功能,它可被用来提高像素的大小和灵敏度,比如摄像头像素大小为5u,当经过2x2合并后,像素大小为10u,3X3合并后,像素大小为15u, 这是图像的整体像素变少了,但成像的灵敏度可提高9倍。动态范围表示在一个图像中最亮与最暗的比值。12bit表示从最暗到最亮等分为212=4096个级别,16bit即分为216个级别,可见bit值越高能分出的细微差别越大,一般CMOS成像系统动态范围具有8-10bit, CCD以10-12bit为主,少部分可达16bit。对动态范围进行量化需要一个运算公式,即动态范围值 = 20 log (well depth/read noise),动态范围的值越高成像系统的性能就越好。量子效率也称像素灵敏度,指在一定的曝光量下,像素势阱中所积累的电荷数与入射到像素表面上的光子数之比。不同结构的CCD其量子效率差异很大。比如100光子中积累到像素势阱中的电荷数是50个,则量子效率为50%(100 photons = 50 electrons means 50% efficiency)。值得注意的是CCD 的量子效率与入射光的波长有关。对显微数码成像系统的参数有了整体认识后,在实际应用中选择合适型号的产品就比较容易了。高分辨率显微数码成像技术在国外已有二十来年的发展历史,产品目前已比较成熟。国外的专业数码产品有多个品牌,比较著名的有德国的ProgRes,美国Roper Scientific的系列产品,另外OLYMPUS、NIKON、LEICA、ZEISS等显微镜厂家也有一些配套的专业数码成像系统 。其中CCD成像系统主要采用SONY及KODRA公司的芯片,因此相关产品性能差别不是很大。国内专业数码成像产品的设计制造时间还不长,但随着配套技术的成熟,100万像素以上的CCD/CMOS专业数码成像产品开始陆续推出,主要的专业厂家有北京的大恒、微视、杭州欧普林,广州明美等企业。北京大恒早期主要研发生产图像采集卡,目前可以量产140万像素的CCD摄像头,130万/200万/320万/500万像素CMOS摄像头,主要用到工业领域。
[align=left][font=宋体][color=#374151]摘要:光学显微成像技术在神经科学研究中发挥着不可或缺的作用。文章将深入探讨两种主要的光学显微成像技术,即荧光显微镜和多光子显微镜,在神经科学领域的应用案例。我们首先介绍了这些技术的基本原理和发展历程,然后详细描述了它们在神经细胞成像、突触可塑性研究和脑功能成像中的应用。通过这些案例,我们展示了光学显微成像技术在神经科学研究中的重要性,以及它们对我们深入理解神经系统的贡献。[/color][/font][/align][font=宋体][color=#374151]关键词:神经科学、荧光显微镜、多光子显微镜、神经细胞成像[/color][/font][font=宋体][color=#374151]光学显微成像技术自17世纪以来一直在科学研究中扮演着重要的角色。随着技术的不断发展,光学显微镜已经成为许多科学领域的核心工具之一,尤其在生命科学和神经科学领域。文章将深入探讨光学显微成像技术在神经科学研究中的应用案例,重点介绍荧光显微镜和多光子显微镜这两种主要技术的原理和应用。[/color][/font][font=宋体][color=#374151]一、光学显微成像技术应用[/color][/font][font=宋体][color=#374151]1.荧光显微镜的应用[/color][/font][font=宋体][color=#374151]荧光显微镜是一种广泛应用于神经科学研究的工具,它使用荧光染料或标记物来可视化和研究神经系统的结构和功能。以下是荧光显微镜在神经科学研究中的应用案例,包括神经细胞成像、突触可塑性研究、脑疾病研究等方面。[/color][/font][font=宋体][color=#374151](1)神经细胞成像[/color][/font][font=宋体][color=#374151]荧光显微镜在观察和研究神经细胞的结构和功能方面发挥了关键作用。通过使用荧光标记的抗体或分子探针,研究人员可以可视化神经元的不同结构,包括轴突、树突、细胞核等。这有助于研究神经细胞的形态特征以及它们在不同生理条件下的变化。[/color][/font][font=宋体][color=#374151](2)突触可塑性研究[/color][/font][font=宋体][color=#374151]荧光显微镜在突触可塑性研究中也具有重要应用。突触可塑性是指突触的结构和功能如何受到刺激和学习的影响。通过标记突触相关的蛋白质或分子,研究人员可以实时观察突触的变化,如突触增强或突触抑制,以深入理解学习和记忆的神经机制。[/color][/font][font=宋体][color=#374151](3)脑功能成像[/color][/font][font=宋体][color=#374151]荧光显微镜在脑功能成像方面也具有潜力。通过将钙指示剂或光遗传学标记物引入神经元,研究人员可以实时监测神经元的活动。这种技术使我们能够理解大脑不同区域的活动模式,以及不同刺激下神经元的响应。这对于研究认知过程、行为和神经疾病有着重要意义。[/color][/font][font=宋体][color=#374151](4)神经干细胞研究[/color][/font][font=宋体][color=#374151]荧光显微镜也被广泛用于研究神经干细胞。通过标记和追踪神经干细胞的命运和分化过程,研究人员可以理解神经系统的发育和再生机制。这对于神经系统修复和治疗神经系统疾病具有潜在应用。[/color][/font][font=宋体][color=#374151](5)荧光标记的蛋白表达[/color][/font][font=宋体][color=#374151]荧光显微镜也可用于研究不同蛋白质在神经系统中的表达和定位。通过使用荧光标记的蛋白表达技术,研究人员可以观察不同蛋白质的分布和相互作用,从而深入理解神经系统中的信号传导和调控。[/color][/font][font=宋体][color=#374151](6)脑疾病研究[/color][/font][font=宋体][color=#374151]荧光显微镜在研究脑疾病方面也发挥着关键作用。研究人员可以使用荧光显微镜来研究神经系统疾病的病理机制,如帕金森病、阿尔茨海默病和精神分裂症。这有助于发现潜在的治疗方法和药物筛选。[/color][/font][font=宋体][color=#374151]荧光显微镜在神经科学研究中的应用是多方面的,涵盖了神经细胞成像、突触可塑性研究、脑功能成像、神经干细胞研究、蛋白质表达和脑疾病研究等多个领域。这一技术为神经科学家提供了非常强大的工具,帮助他们深入理解神经系统的结构和功能,以及与神经相关的疾病的机制。未来,随着技术的不断发展,荧光显微镜将继续在神经科学领域中发挥关键作用,为我们揭示神经系统的奥秘提供更多的洞察力。[/color][/font][font=宋体][color=#374151]2.多光子显微镜的应用[/color][/font][font=宋体][color=#374151]多光子显微镜(Multi-Photon Microscopy)是一种先进的成像技术,它利用非线性光学效应,如多光子吸收,为神经科学家提供了强大的工具,用于研究神经系统的结构和功能。相比传统的荧光显微镜,多光子显微镜具有许多显著的优势,包括更深的成像深度、较少的光损伤、更少的荧光标记物和更高的空间分辨率。以下是多光子显微镜在神经科学研究中的应用领域:[/color][/font][font=宋体][color=#374151](1)脑功能成像[/color][/font][font=宋体][color=#374151]脑功能成像是多光子显微镜的一个主要应用领域。这种技术允许研究人员实时观察活体动物的脑活动,包括神经元的兴奋与抑制、突触传递和脑区之间的相互作用。多光子显微镜能够提供高分辨率的三维图像,而无需使用荧光标记物。这对于研究大脑的基本功能、学习和记忆等过程至关重要。[/color][/font][font=宋体][color=#374151](2)钙离子成像[/color][/font][font=宋体][color=#374151]钙离子在神经元内起着关键的信号传导作用。多光子显微镜可以用于监测神经元内的钙离子浓度变化,这对于理解神经元的兴奋性和突触传递至关重要。通过使用荧光钙染料,研究人员可以实时观察神经元内钙离子浓度的动态变化,以及不同神经元之间的协同作用。[/color][/font][font=宋体][color=#374151](3)神经元形态学研究[/color][/font][font=宋体][color=#374151]多光子显微镜在研究神经元的形态学和结构上也具有独特的优势。它可以提供高分辨率的三维成像,允许研究人员详细观察神经元的分支结构、突触连接和细胞器的分布。这对于理解神经元的连接方式、发展和退行性疾病的机制至关重要。[/color][/font][font=宋体][color=#374151](4)活体动物模型研究[/color][/font][font=宋体][color=#374151]多光子显微镜也在活体动物模型研究中发挥着关键作用。研究人员可以使用这种技术观察小鼠、果蝇等模型动物的脑活动,从而研究不同物种的神经系统功能和行为。这对于神经药理学、疾病建模和药物筛选具有重要意义。[/color][/font][font=宋体][color=#374151](5)细胞内成像[/color][/font][font=宋体][color=#374151]多光子显微镜也可用于单个神经元或突触的细胞内成像。这允许研究人员观察细胞内的亚细胞结构、蛋白质运输和突触形成等过程。这对于研究神经元的分子机制和突触可塑性非常有帮助。[/color][/font][font=宋体][color=#374151]多光子显微镜的应用领域不仅局限于神经科学,还扩展到其他生命科学领域,如细胞生物学、免疫学和生物医学研究。其高分辨率和深层成像能力使其成为许多领域中不可或缺的工具。[/color][/font][font=宋体][color=#374151]尽管多光子显微镜在神经科学研究中具有巨大的潜力,但它也面临着一些挑战。其中之一是成像速度,尤其在观察大脑活动时,需要高速成像以捕捉快速的神经事件。另一个挑战是数据处理和分析,因为高分辨率、三维和四维成像产生了大量的数据,需要强大的计算资源和分析工具。[/color][/font][font=宋体][color=#374151]未来,我们可以期待多光子显微镜技术的不断改进和发展,以应对这些挑战。新的激光技术、荧光标记物和成像算法将继续推动这一领域的进展,为我们深入理解神经系统的复杂性提供更多的洞察力。多光子显微镜将继续在神经科学领域中发挥关键作用,有望帮助我们解决一些最具挑战性的神经科学问题。[/color][/font][font=宋体][color=#374151]二、光学显微成像技术在神经科学研究中的应用存在问题[/color][/font][font=宋体][color=#374151]光学显微成像技术在神经科学研究中的应用虽然具有众多优势,但也存在一些问题和挑战,这些问题需要科研人员不断努力来解决。以下是一些存在问题:[/color][/font][font=宋体][color=#374151]1.有限的成像深度[/color][/font][font=宋体][color=#374151]传统的光学显微成像技术受到光的折射和吸收的限制,导致成像深度受到限制。这在研究深层脑区时成为问题,因为光无法有效透过多层组织,导致深层神经元无法清晰成像。多光子显微镜已经在这一方面取得了进展,但仍然存在深度限制。[/color][/font][font=宋体][color=#374151]2.光损伤和毒性[/color][/font][font=宋体][color=#374151]荧光标记物和强光源在成像过程中可能对生物样本产生光损伤和毒性作用。这对于活体成像和长时间观察是一个挑战,因为它可能导致样本的退化和死亡。科研人员需要努力寻找更温和的成像方法和标记物,以减轻这些问题。[/color][/font][font=宋体][color=#374151]3.数据量庞大[/color][/font][font=宋体][color=#374151]高分辨率和多维成像技术产生大量的数据,需要强大的计算资源和复杂的数据分析工具。处理和管理这些数据可能是一个挑战,尤其是在长期实验和大规模成像项目中。[/color][/font][font=宋体][color=#374151]4.标记物的选择[/color][/font][font=宋体][color=#374151]合适的荧光标记物对于获得高质量的成像数据至关重要。然而,选择适当的标记物可能会受到限制,因为一些标记物可能会干扰样本的正常生理活动,或者不适合特定的实验条件。因此,需要不断开发新的标记物和成像方法。[/color][/font][font=宋体][color=#374151]5.解析度限制[/color][/font][font=宋体][color=#374151]光学显微成像的分辨率受到光的波长限制,通常受到绕射极限的限制。虽然一些超分辨率成像技术已经出现,但它们仍然无法突破光学分辨率极限。这可能会限制对神经系统微观结构的精确观察。[/color][/font][font=宋体][color=#374151]6.活体成像的挑战[/color][/font][font=宋体][color=#374151]对于活体成像,尤其是在大脑中,样本的运动和呼吸等因素可能导致成像失真。稳定和精确定位样本是一个技术挑战。[/color][/font][font=宋体][color=#374151]尽管存在这些问题,光学显微成像技术仍然是神经科学研究的不可或缺的工具,因为它们提供了独特的实时、高分辨率和非侵入性的成像能力。科研人员不断努力解决这些问题,通过技术创新和改进,光学显微成像技术有望继续为神经科学领域的研究提供更多洞察力。[/color][/font][font=宋体][color=#374151]三、下一步研究方向[/color][/font][font=宋体][color=#374151]基于上述问题,光学显微成像技术在神经科学研究中的应用仍然需要不断改进和发展。下面是可能的下一步研究方向,以解决这些问题:[/color][/font][font=宋体][color=#374151]1.改进成像深度[/color][/font][font=宋体][color=#374151]研究人员可以探索新的成像方法,如双光子显微镜和光学波前调制成像,以增加成像深度。此外,开发新的光学透明样本制备技术,如透明大脑样本技术,可以帮助克服深度限制问题。[/color][/font][font=宋体][color=#374151]2.减少光损伤和毒性[/color][/font][font=宋体][color=#374151]研究人员可以寻找更温和的成像条件,减少光损伤和荧光标记物的毒性。此外,使用先进的成像系统,如自适应光学成像,可以减小激光功率,同时保持高分辨率。[/color][/font][font=宋体][color=#374151]3.数据管理和分析工具[/color][/font][font=宋体][color=#374151]开发更强大的数据管理和分析工具,以处理庞大的成像数据。机器学习和深度学习方法可以帮助提高数据分析的效率,并自动检测和量化细胞和结构。[/color][/font][font=宋体][color=#374151]4.标记物的改进:寻找更多、更具选择性的标记物,以减少对样本的干扰。这可以包括荧光标记物的改进、发展新的基因表达标记和探测技术。[/color][/font][font=宋体][color=#374151]5.突破分辨率极限[/color][/font][font=宋体][color=#374151]进一步发展超分辨率成像技术,以突破传统光学分辨率极限,获得更高的细节分辨率。例如,结构光显微镜和单分子成像技术可以帮助提高分辨率。[/color][/font][font=宋体][color=#374151]6.活体成像技术改进:研究人员可以探索新的样本固定和稳定技术,以减小样本运动对成像的影响。另外,开发新的活体成像方法,如头部悬置成像和小型显微成像技术,可以帮助在动态活体条件下进行成像。[/color][/font][font=宋体][color=#374151]7.多模态成像[/color][/font][font=宋体][color=#374151]结合不同的成像技术,如光学显微镜与电生理记录、光学显微镜与功能磁共振成像(fMRI)等,以获得更全面的神经科学数据。[/color][/font][font=宋体][color=#374151]8.多尺度成像[/color][/font][font=宋体][color=#374151]开发多尺度成像方法,能够在微观和宏观水平上同时观察神经系统的活动,从神经元到整个脑区。[/color][/font][font=宋体][color=#374151]这些研究方向代表了改进和扩展光学显微成像技术在神经科学研究中的应用的可能途径。通过不断的技术创新和跨学科合作,神经科学家和工程师有望克服这些问题,提高光学显微成像技术的效能和应用广度,以更深入地理解神经系统的复杂性。[/color][/font][font=宋体][color=#374151]四、结论[/color][/font][font=宋体][color=#374151]光学显微成像技术在神经科学研究中的应用案例清楚地表明,这些技术在揭示神经系统的复杂性和功能中起到了关键作用。然而,这仅仅是一个开始,未来仍有许多挑战和机遇等待我们探索。例如,新的成像技术和荧光标记方法的不断发展将进一步扩展我们的研究领域。此外,将光学显微成像技术与其他分子生物学和生物化学技术相结合,可以更全面地理解神经系统的功能。[/color][/font][font=宋体][color=#374151]在未来,我们可以期待更高分辨率、更深层次的成像以及更多三维和四维成像的发展。这将有助于解决神经科学中的一些最具挑战性的问题,如神经网络的复杂性和神经退行性疾病的机制。光学显微成像技术将继续为神经科学研究提供有力的工具,推动我们对大脑和神经系统的理解不断深入。[/color][/font][font=宋体][color=#374151]参考文献:[/color][/font][font=宋体][color=#374151][1]高宇婷,潘安,姚保利等.二维高通量光学显微成像技术研究进展[J].液晶与显示,2023,38(06):691-711.[/color][/font][font=宋体][color=#374151][2]王义强,林方睿,胡睿等.大视场光学显微成像技术[J].中国光学(中英文),2022,15(06):1194-1210.[/color][/font][font=宋体][color=#374151][3]章辰,高玉峰,叶世蔚等.自适应光学在双光子显微成像技术中的应用[J].中国激光,2023,50(03):37-54.[/color][/font][font=宋体][color=#374151][4]曹怡涛,王雪,路鑫超等.无标记光学显微成像技术及其在生物医学的应用[J].激光与光电子学进展,2022,59(06):197-212.[/color][/font][font=宋体][color=#374151][5]关苑君,马显才.光学显微成像技术在液-[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]分离研究中的应用[J].中山大学学报(医学科学版),2022,43(03):504-510.DOI:10.13471/j.cnki.j.sun.yat-sen.Univ (med.sci).2022.0319.[/color][/font][font=宋体][color=#374151][6]陈廷爱,陈龙超,李慧等.结构光照明超分辨光学显微成像技术与展望[J].中国光学,2018,11(03):307-328.[/color][/font][font=宋体][color=#374151][7]安莎. 轴平面光学显微成像技术及其应用研究[D].中国科学院大学(中国科学院西安光学精密机械研究所),2021.DOI:10.27605/d.cnki.gkxgs.2021.000055.[/color][/font][font=宋体][color=#374151][8]杜艳丽,马凤英,弓巧侠等.基于空间光调制器的光学显微成像技术[J].激光与光电子学进展,2014,51(02):13-22.[/color][/font][font=宋体][color=#374151][9]莫驰,陈诗源,翟慕岳等.脑神经活动光学显微成像技术[J].科学通报,2018,63(36):3945-3960.[/color][/font][font=宋体][color=#374151][10]张财华,赵志伟,陈良怡等.自适应光学在生物荧光显微成像技术中的应用[J].中国科学:物理学 力学 天文学,2017,47(08):26-39.[/color][/font]
[back=transparent]质谱成像是以质谱技术为基础的可视化方法,通过质谱离子源直接扫描生物样本,可以在一张组织切片上同时分析数百种分子的空间分布特征,已成为精确解析药物分子及其代谢产物组织空间分布的关键技术之一,[back=transparent]质谱成像[/back]应用于药物ADME的研究。[/back]一般在生活中肾脏是药物排泄的主要器官。但是药物排泄过程的正常与否关系到药效强度、药效维持时间以及毒副作用。所以,这是我们必须要借助一些科学例如高分辨质谱技术来助力药物。近年来,高分辨质谱成像技术的诞生为定位药物组织分布研究提供了全新的技术和思路。本文将主要介绍TransMIT AP-SMALDI 10高分辨率质谱成像系统如何一步步揭秘伊马替尼在小鼠肾脏组织中的空间分布特征。TransMIT AP-SMALDI 10质谱成像系统是目前少有的集高空间分辨率和高质量精度于一体的质谱成像系统。该系统采用常压基质辅助激光解吸电离技术,通过先进的准直光束聚焦实现了5μm的成像分辨率;质谱端搭载Thermo Scientific? Q Exactive?系列质谱仪,保证了离子分析的高质量分辨率和高质量精度。综上所述,研究成功的揭示了伊马替尼在重要排泄器官肾脏中的组织分布特征,同时也获取了组织中各种内源性化合物的空间分布信息,为研究药物分子的累积和排泄机制提供了可靠的科学依据。TransMIT AP-SMALDI 10质谱成像系统集高空间分辨率、高质量分辨率和高质量精度于一身,不仅成为了药代动力学研究的利器,也应用于肿瘤标志物研究、植物次生代谢物研究、药用植物药效成分研究、微生物和单细胞研究等。未来,期待TransMIT AP-SMALDI 10质谱成像系统为我国药物研发人员和各领域科研工作者带来更多的惊喜,加快研究进程,加速成果转化。
紧急求助静电力显微镜中电场梯度成像的工作原理, 组里最近买了一台omicron的真空AFM,除了向扫描表面之外,还想进行电场梯度成像。我的助教在导电的针尖上加了一个偏压(AC bias),想测量电场梯度。我是个新手,接触AFM 才2个月,所以想请教各位,在经过这个改变后,我们的AFM 是不是就可以测电场梯度了,另外,静电力显微镜中电场梯度成像的3个方法中,相检测 (phase detection)、频率调制 (frequency modulation)和振幅检测 (amplitude detection) 的工作原理是怎样的。哪个个方式更合适我们的AFM呢请多多指教咯^__^
这款[url=http://www.f-lab.cn/vivo-imaging/micam05.html][b]高速荧光成像系统[/b]micam05[/url]是专业为神经成像,钙成像应用而设计的[b]高速神经成像系统[/b],能够长时间高速成像和记录存储高速图像.高速荧光成像系统micam05具有超低噪音,非常适合[b]染料成像[/b]和[b]钙成像[/b]应用,也可用于[b]荧光蛋白质电压[/b]/钙指示剂,如FRET成像和[b]GCaMP成像,血红蛋白成像[/b]或[b]黄素蛋白成像[/b]。[b]高速荧光成像系统micam05特点[/b]采用USB3.0接口高速数据传输技术,外部设备的兼容性好,适合实时像素输出和额外的模拟输入。用于多种类型科研CCD相机具有多种CMOS相机提供不同的空间/时间分辨率,这些机头可以很容易地切换或更换。(不可能同时使用不同类型的摄像机头)。直接数据存储和USB3.0高速数据传输的长期数据采集新的USB3.0接口允许更快的数据传输处理器的PC可以直接硬盘或SSD数据采集并行,无论内存容量,几分钟到几小时的长期记录都可以。(注意采样率、像素数量、使用的相机数量和PC规格将影响总记录时间)。多达四个摄像头可以很容易地连接和使用在一个完全同步多摄像机的系统中。最多两相机接口板可以连接到micam05处理器。每个接口板配备两个摄像头端口,因此,多达四个的同类型的摄像头可以随时连接。这允许从不同的角度多个荧光波长及三维同时成像。实时光强度监视器/输出可用作标准功能。高速荧光成像系统:[url]http://www.f-lab.cn/vivo-imaging/micam05.html[/url]
在《自然·物理学》杂志网络版上,美国加州大学伯克利分校和西班牙马德里自治大学的科学家声称,他们已找到了一种新方法,能够克服超声成像图案解析度不高的局限,将超声成像的解析度提高50倍。 研究人员在论文中描述了如何捕获从一个目标反射回的倏逝波,并重建出仅为声波波长1/50的微小细节。与能传输很长距离的传播波相比,倏逝波是一种在物体附近很短距离内渐次减弱的振动。 论文第一作者、加州大学伯克利分校大规模集成纳米制造中心的博士后研究员朱捷(音译)表示,利用他们的设备,他们检获并传输了倏逝波,该波中包含有来自目标的超亚波长信息的重要部分,从而使他们得以实现超清晰的声学成像。 研究人员指出,可捕捉倏逝波的设备是一种三维多孔结构的超材料。它包含1600个空心铜管,并集束在一个横截面为6.3厘米见方、长为16厘米的 棒条中。将其靠近目标物,就能捕获到倏逝波,并把倏逝波传送到另一端。在实际应用中,这个超材料设备可装在超声探头的一端以大幅改善成像质量。该设备还能 改善水下超声探测(声纳)的效果,或提高工业应用领域的无损检测水平。对于超声检查来说,成像解析度通常都在毫米级别,有了该设备,解析度就只受限于这些 孔的大小。 实验中,铜管中的小孔直径约为1毫米。使用2KHz(千赫)的超声波,图像的解析度通常会受限于波长,即200毫米。利用这种多孔超材料,解析的 特征尺寸可小至4毫米,也就是波长的1/50。研究人员表示,如果没有这种超材料,要检测如此深的亚波长目标几乎是不可能的。
只知道它是束斑逐步扫描成像区域,百度搜了下资料大部分是HAADF-STEM成像原理,主要介绍的是Z衬度成像。那如果只是单纯的STEM,它的衬度和信号是什么?扫描式的相比TEM有什么好处吗?束斑在扫描时与试样表面成一定角度还是近乎垂直的?恳请大神不吝赐教或者推荐一些学习资料,谢谢!
随着红外技术的不断发展,红外成像仪在日常检测中时常使用到。同时使用红外热成像仪检测中存在的问题及对策 随着”三集五大”体系建设和变电设备“状态检修”的大力推进,传统的传统的变电设备检修和运行模式发生了根本性改变, 能够实时、有效、动态地评价设备健康状况成为确保设备安全、稳定 运行的前提, 红外成像仪是目前变电运行人员检测运行设备健康状况 的有力保证,可以有效的避免因设备发热而造成的非计划停电,为提 高供电可靠率做出了贡献策 针对当前变电设备红外成像检测技术的应用中存在问题及改进方法进行了思考以及对红外测温未来发展的展望。 由于这种 技术无需对所测设备停电,即可准确发现安全隐患,所以更要充分利 用好、发挥好红外成像检测这一高科技手段,夯实变电设备“状态检 修”基础,确保运行的可控、在控、预控。 一 目前在使用中所存在的问题: 目前在使用中所存在的问题: 重设备,轻人员,培训工作不到位。 ( 1)重设备,轻人员,培训工作不到位 目前,红外成像设备已基本覆盖到重要的生产班组,极大提高了 生产一线的技术装备水平,然而,好的检测设备必须得到正确和规范 的应用,才可能发挥其最好的性能,不能只重视检测设备的配置,而 忽略了对人员进行必要的培训, 目前对红外成像仪方面培训的主要方式还是以产品说明书为主,没有专业的培训教材和权威的培训师资, 虽然厂家的技术人员会不定期到各基层单位组织测温培训, 但由于运 行人员倒班的原因,造成了一线人员缺乏热像仪的操作技能培训,同 时,昂贵的机器也需要专业的使用和维护技巧,没有经过专业培训, 在使用红外线成像器材时就不可避免要出现:保养不当、充电电池报 废、昂贵的红外线镜头被划损等等现象,既造成了经济损失,也影响 了测温工作的正常开展。 对策:(1)建立完善的红外成像检测制度,对红外检测工作的准备、 对策 风险预控、规范、安全注意事项等进行详细的规定。同时根据各站所 管辖的一、二次设备详细列表并建立测温表单,以表单的形式使测温 制度和规范落到实处;(2)加强红外热成像仪使用技术的培训,考 虑到运行人员工作的特殊性, 可以首先由相关厂家的技术人员对各个 部门的技术专责进行培训并考核, 然后由各个部门的专责负责对各个 集控站,变电站站长进行培训。 此文转自:深圳市杰创立仪器有限公司
要采购低温冰箱,荧光PCR仪,高压灭菌锅,凝胶成像仪,显微成像系统等,哪几家公司(国外)的性价比高且结实耐用啊,求高手指点。
红外线热成像检测是一项越来越被肯定的工业检测技术,就一般工厂检测应用而言,主要以提高设备运转的可靠性、工业安全及节能等为目的。工厂设备以电气及机械两大类为主,并以电气设备的检测应用为最多,另外还包括转动、传动机械装置的检测,炉壁、管线的防火与隔热层(保温/保冷)的状态检测。 工厂,工程设备的正常运作是确保施工质量,提高效率所必备的条件,对于提前检测设备的情况确保机械正常运作,是十分重要的。因为预知维护检测是预先检测并诊断设备的潜在故障因素,有目的按计划地进行维护工作。这种维护检测作业不仅提高设备运转的可靠性,并降低设备的检修费用与工时,减少设备过度维护出现的问题。红外线热像检测技术同时具备非破坏性检测、非接触式测量、直觉观测、不受电磁干扰、测温快速、灵敏度高等特性,是最有效的预知保养维护工作中对设备状态监测和故障诊断的方法之一。设备出现异常时,通常显示出一定的征兆,如振动、声响、电量、光、温度、压力、异物等各种物理量的测量,可供发现并诊断问题。许多的设备异常,在初期阶段会显示可觉察的温度差异,而红外线热成像是以测量温度为检测方法,将检测所得的热图像与温度值,根据设备的构造及特性进行分析,发现并诊断问题,提出建议改进方案。
随着MALDI-TOF等生物质谱仪器性能的提升和应用领域的扩大,基于MALDI的质谱成像技术已成为研究肿瘤标志物、药物代谢、脂类分布等方面的有力手段。最新样品前处理方法以及自动化基质喷涂等技术的发展,大大提高了质谱成像技术的灵敏度和分辨率。利用原位酶切技术直接鉴定组织切片上的蛋白质和多肽是IMS当前的热点和关键。体内药物代谢物分布、脂类物质分布以及植物组织的质谱成像等研究逐渐成为新的应用热点。本文较系统地介绍了生物组织质谱成像技术的研究进展。详见附件。http://simg.instrument.com.cn/bbs/images/brow/em09510.gif
刚学习化学发光,请专家指点化学发光检测仪采用液相(态)检测方法比化学发光固相(态)检测(成像系统)灵敏多少个数量级? 3~5个?对于化学发光检测,是不是PMT单光子检测做的工作,化学发光成像系统一定不可以做? 例如?
http://img3.17img.cn/bbs/upfile/images/20100518/201005181701392921.gifHORIBA拉曼-AFM技术最新进展讲座时间:2014年9月22日 10:00 主讲人:刘仕锋物理学硕士,2005年加入HORIBA Scientific,多年从事拉曼光谱仪应用支持工作,为用户提供应用实现、功能开拓、及仪器培训等应用支持。http://img3.17img.cn/bbs/upfile/images/20100518/201005181701392921.gif【简介】 随着扫描探针隧道显微镜(SPM)在上世纪80年代的出现,纳米尺度成像成为了可能。该技术使材料表面各种物理特性的表征方法得以快速持续发展,然而如何实现无标记的化学组分表征仍是一项挑战。 在过去的几十年里,光学光谱已经成为纳米材料分析的有力工具,它为分子结构和化学组分分析提供了独特的方法。不过,这种方法的空间分辨率在很大程度上受限于光学衍射极限。于是,将两种技术联用成为一种极富吸引力的独特方法。本报告将会为大家介绍为什么要用AFM-Raman、同区域成像和TERS以及HORIBA提供的解决方案等内容。-------------------------------------------------------------------------------1、报名条件:只要您是仪器网注册用户均可报名参加。2、报名并参会用户有机会获得100元京东卡一张哦~3、报名截止时间:2014年9月22 日 9:30 4、报名参会:http://simg.instrument.com.cn/meeting/images/20100414/baoming.jpg