国家药监总局(CFDA)南方医药经济所副所长陶剑虹在第四届生物类似物发展论坛上表示,目前,CFDA正式启动了生物类似物药物监管准则的编制,预计年内将向企业发布技术指南。“将按照欧盟和WHO的相关规定,分别针对创新型和非创新型品种建立不同的监管审批原则”。 在国内生物类似物法规一片空白的背景下,该指南对生物制品行业的意义巨大。一位接近国家药品审评中心(CDE)的与会专家也透漏,CFDA正在研究制定生物类似物的相关审评监管政策,CDE专门对生物类似物企业指南进行开会讨论。“会前第一版内部已经有了,会后第一版据说年底就会有。不过,与此前业内期望国家出台符合中国国情的生物类似物政策不同的是,该指南更趋向于是一个国际标准,可能在执行操作方面才会有中国特色”。 据陶剑虹介绍,从明年起到2018年,全球进入专利药物到期密集期,而面对生物类似物巨大的机遇,我国却在政策层面上面临阻碍,没有明确的生物类似物研发指导原则和相关法规。为此,国内38位院士联名上书,呼吁尽快出台适合国情的生物类似物审批政策,缩短审批流程,为生物类似物创造良好环境,建言报告也得到了积极回应。 据了解,我国《药品管理法》2001年颁布,最新的配套细则也有7年历史,且未对生物类似物发布明确的技术指南。国内涉足生物类似物的药企只能按照创新药的开发流程来报批,开发过程繁琐冗长,消耗了大量的时间和资金。2011年-2013年,我国企业每年申请审批的生物制品超过1000种,但能获批上市的只有70余种。 相较之下,世界各国针对生物类似物已出台了相应的监管政策。欧洲早在2006年就建立了初具规模的生物类似物审批途径;美国FDA的监管态度也日趋明朗,今年9月出台的生物类似药紫皮书为该类药物的研发和推进奠定了基石;日本、韩国、澳大利亚均发布了生物类似物审批的指导原则;巴西、墨西哥、委内瑞拉、哥伦比亚和印度也已经发布了生物类似物审批的草案。
国家食品药品监管总局(CFDA)积极研究并准备出台生物类似药(biosimilar,又译“生物类似物”)研究技术指导原则的消息在业内不胫而走。根据CFDA药化注册司的部署,药品审评中心承担了生物类似药研究技术指导原则的起草撰写工作,日前已启动了生物类似药研究技术指导原则制定专项工作。“中国药监审评部门着手生物类似药指导原则的调研和起草等相关工作,这是一个鼓舞人心的消息。指导原则的制定要从一开始就参考国际水准,考虑战略定位,具体实施则需要有循序渐进和全球合作的心态。”盛德国际律师事务所生物科学战略顾问、中国药科大学国家药物政策与医药产业经济研究中心研究员苏岭在接受本报采访时说。审批的挑战“在制定我国生物类似药的规范时,如何既可以让企业减少申报程序,节省研发、临床的时间和成本,同时又保证它与原研药的一致性,将是我国药监部门面临的一个挑战。”中国药学会理事长、中国工程院院士桑国卫在“生物类似药政策法规及技术指导原则高层研讨会”上指出。按照现行的审批机制,虽然生物类似药按照新药审批可以规避和原研制品在专利上的纠缠,但审批速度并未因此得到提升。目前,国内生物类似药没有明确的分类要求,没有公开的技术审评要求,申请人和审评机构对其技术要求没有统一的认识。信达生物制药质量部执行总监孙左宇博士说,生物类似药与创新药的审评在流程和时限上没有区别,没有时间优势、费用更贵的状态阻碍了我国生物类似药的发展。长春金赛药业药物研究院副院长王英武指出:“我国目前缺少专门针对生物类似药临床对比性试验的指导原则和申报途径,临床试验必须要与参比药品进行大规模的头对头比较,使得研发成本大幅提高,并延长了产品研发周期和申报速度。”标准如何制定美国药品研究和制造商协会主席罗伯特·J·胡金在接受本报记者采访时指出:“对于生物类似药,各个国家应该遵循一些普遍的理念和原则,这些理念是科学性,是没有任何偏见的。”“首先要通过科学标准来确定生物类似药和原研产品能够达到一致,如果能够达到一致,那就按照生物类似药的一套程序去上市。如果达不到科学和医学严格的标准,和要仿制的生物制品不具有等同性,那就应该当成新药去审批上市。”罗伯特·J·胡金这样建议。目前,全球已有22个国家或组织陆续制定颁布了其生物类似药相关指南,遵循的原则都是WHO的建议和EMEA的规范。苏岭认为,如何结合我国具体国情,又不失时机地与先进国家的要求和国际共识接轨,是鼓励开发高水平高质量的生物类似药和促进我国生物制药产业健康发展的契机。而从另一个角度讲,生物类似药更是涉及巨大利益的商业问题。一边是本土药企希望提升审批速度,使得生物类似药凭借价格优势迅速占领市场;另一边是原研厂家担忧生物类似药生产商绕开专利而实现“弯道超车”。“对于国内开发企业来说,急于求成、齐头并进是生物类似药开发的大忌。”苏岭说。
最近看了文献,发现有些检测样品,三聚氰胺很少,但是其类似物含量确很高,因此仅检测三聚氰胺是不够的(从专业技术上讲,管理部门仅三聚氰胺已经够头疼的),除了植物蛋白中--那个标准方法外,大家有好的方法同时检测三聚氰胺4种类似物.特别是样品前处理有好办法吗?
在化学药品分类中,对应于原研药品的是仿制药。而在生物制品注册分类中,和原研生物制品对应的类别是生物类似药(biosimilar drug)。为什么产生这个名称呢?因为生物药品多是大分子物质,在分子大小、制备工艺和产品性质方面,和都比化学药品复杂很多。因此即使采用完全相同的工艺,也不能确保生产的产品和原研产品是完全一致的。况且生物药品的仿制公司在研究自己产品时,是不能得到原研生物药品的工艺和秘密技术指标的。基于这些原因,生物类似药(biosimilar drug)就是在质量、安全和临床效果方面,和原研生物药品(innovator drug)类似的药品。 在过去的很长时间,美国FDA对于生物药品一直都实施最严格的管制措施,不承认生物类似药的合理存在。而欧盟则比较灵活,很早就承认生物类似药的地位并实施积极的注册管理,并逐步建立了比较完善的生物类似药的注册法规体系。在2012年,FDA开始建立和发布关于生物类似药的注册指南和法规体系。 我国对于非创新性的生物制品,已有注册申报制度和相关技术要求。但是,到目前还没有专门的针对生物类似药(biosimilar drug)的定义、配套指导原则和注册规定。例如按照《药品注册管理办法》(局令28号),所有生物制品都需要按照新药申请的程序申报和注册。而在我国目前的《药品注册管理办法》(局令28号)中,一些类别的生物药品就属于生物类似药(biosimilar drug): 7.已在国外上市销售但尚未在国内上市销售的生物制品。 10.与已上市销售制品制备方法不同的制品(例如采用不同表达体系、宿主细胞等)。 15.已有国家药品标准的生物制品。中国目前的非创新性生物制品的注册特点项目要求许可标准安全、有效、质量可控、在相似性方面无明确要求。注册资料要求比创新性生物制品低,但是比仿制药高。临床试验可以满足临床需要,但是允许差异。现有体系和生物类似药的区分需要调整技术要求,增加相似性要求,缩小和原研药品差距。 为了应对制药企业日益高涨的呼声,尽快适应生物类似药的注册需求,和国际注册监管态势接轨。国家局审评中心(CDE)在2013年底开始着手进行生物类似药注册审评体系的研究和建立。在2014年底,CDE召开了专题工作启动会,开始实施具体任务。任务实施分为四个阶段,分别是调研阶段、学术研讨阶段、框架制定阶段和完成初稿阶段。 为了完成此任务,审评中心(CDE)分别在2014年5月召开了有很多企业人员参加的内部研讨会,并在2014年7月兰州培训班上,进行了部门信息的介绍。 结合上述会议和培训的信息,和生物类似药相关的技术要点综合于下: 一.生物类似药的适用范围 目前,审评中心(CDE)认为生物类似药主要适用于重组蛋白产品,因为对这类产品的结构和功能了解比较透彻。目前认为如下产品不宜被列入生物类似药范畴:细胞产品、基因治疗产品以及组织提取的生物技术产品,不包括预防性疫苗。 对于结构复杂的重组蛋白、例如PEG修饰的蛋白产品,对其相似性分析难度很大。 二.生物参照药品的定义和相关要求 经过反复讨论,目前定义为:基于完整注册申报资料、已被我国药监局注册批准上市的药品。在生物药品的质量研究、非临床研究和临床研究中,通过对比研究来证明它们的相似性。 生物参照药品,具有如下特征: ---临床用参照药品必须在国内上市,药学研究和非临床研究参照药品来自其它国家批准的药品。 ---如果药学研究和非临床研究参照药品来自其它国家批准的药品,在进行临床前,还需要考虑桥接研究。 ---在药学对比研究中,允许分离制剂中的有效成分;但是要证明分离方法没有改变质量属性。 ---一般不接受生物类似药作为参照药品,除非有合理理由。 三.生物类似药的基本评价原则 生物类似药的评价原则如下: ---逐步递进式的对比研究 ---倒金字塔式研究 ---case by case原则 ---定义高度相似、相似和不相似 要做好这部分工作,需要做好如下两方面工作 工作思路 1. 充分调研参照药品,建立结构和功能的关系。 2. 确定影响产品质量的关键质量属性(CQA)。 3. 建立相似性的判定标准(例如高度相似、相似和不相似)。 4. 根据对比研究结果,优化改进工艺。 5. 根据工艺优化结果,进行后续非临床研究和临床研究。 相似性研究的设计考虑 1. 深入研究,建立关键质量属性(CQA)。 2. 采用灵敏、先进和经过验证的方法进行研究。 3. 对比研究中引入统计学概念。 4. 至少选择3批候选药品和参照药品3批进行研究;如果有10个批次的数据,是推荐选择的方案。 四.其他药学相关问题 关于生物类似药的研究,还有很多技术问题需要考虑和探讨。下面简要列入目前最让法规方和制药企业关心的问题如下: 4.1氨基酸序列应该和参照药品是一致的,这个一致指的是实际测试值一致,而不是文献值一致。 4.2在细胞基质方面,尽可能一致。如果不一致,需要提供验证证据。尤其是抗体药物,不同基质对于抗体表达修饰是不一样的,要慎重。表达质粒的要求,和细胞基质要求类似。 4.3药学质量研究方面,一个是标准如何建立,研究内容一般包括理化性质、生物活性、杂质、免疫项目、还需要包括影响因素试验、加速试验和长期稳定性试验。关键质量属性应该和参照药品保持一致。 4.4处方组成,规格和内包材。CDE建议最好和参照药品保持一致。如果不一致,需要证明这种差距对药品安全性的影响是可以接受的。关于处方,应该进行筛选和研究工作,应该和参照药品的处方进行对比。关于规格,我们建议用法和用料和参照药品尽量一致。内包材也可以不同,但是要有充分研究数据。 4.5申报临床阶段的药品质量要求。细胞库的建立,应该进行全面鉴定。除了2010版药典,还要参考2015版药典的要求。 4.6工艺验证,生产规模应该和大生产规模相当。如果临床试验期间,发生特殊情况,例如安全性问题,或者有效性问题,和参照药品对比不一致,如果调查发现是由于工艺问题导致的,可以调整工艺。 4.7质量标准和检验方法,应该是基本确定的,而且有充分的方法学研究工作。如果生物活性、或者免疫项目和参照药品不一致,要充分研究。 因为关于生物类似药的呼声日益迫切,因此审评中心(CDE)也在加快工作步骤,预计年底会推出指导原则的草案。作者:zhulikou431,高级工程师、PDA会员、ISPE会员、ECA会员、资深无菌GMP专家,在药品研发和注册、法规审计、国际认证、国际注册和质量体系建设与维护领域,具有较深造诣。
各省、自治区、直辖市和新疆生产建设兵团市场监管局(厅、委):近年来,宣称功能食品非法添加药品、药品衍生物或类似物的违法案件时有发生,危害人民群众身体健康。近期,总局组织内蒙古、江苏、安徽、福建、广东等(省、区)市场监管部门查办了宣称“减肥”功能食品非法添加药品、药品衍生物或类似物系列案件,认定了检验方法,并出具了专家有毒有害认定意见。现将《酚汀(酚丁)、酚酞及其酯类衍生物或类似物有毒有害专家认定意见》(附件)发给你们,可作为案件查办中甄别有毒有害物质成分、实施定罪量刑的参考。市场监管部门应当从速从严查处此类案件,依法吊销许可并处罚相关责任人;涉嫌犯罪的,要及时移送公安机关处理。附件:酚汀(酚丁)、酚酞及其酯类衍生物或类似物有毒有害专家认定意见[align=right]市场监管总局办公厅[/align][align=right]2023年10月8日[/align](此件公开发布)附件[align=center][font=方正小标宋简体][color=black]酚汀(酚丁)、酚酞及其酯类衍生物或类似物[/color][/font][/align][align=center][font=方正小标宋简体][color=black]有毒有害专家认定意见[/color][/font][/align]双丙酚汀是双醋酚汀的类似物,双醋酚汀曾为地方标准批准的药品,但后未获得国家药品监督管理部门批准作为药品或原料药品生产或进口;其类似物双丙酚汀也从未获得国家药品监督管理部门批准作为药品或原料药品生产或进口;双醋酚汀类似物酚酞虽曾为国家获批的药物,但由于其存在严重不良反应,国家药监局于2021年发布了《关于注销酚酞片和酚酞含片药品注册证书的公告(2021年第6号)》。根据《食品安全法》,食品不得添加药物,而该类原料也从未获得批准作为食品添加剂或新食品原料,以及保健食品原料,因此,在食品中检出酚汀(酚丁)、酚酞及其酯类衍生物或类似物(如4-氯双醋酚丁),均属于非法添加。由于酚汀(酚丁)、酚酞及其酯类衍生物或类似物与酚酞具有相同/相似的核心药效团和临床功效,具有类似属性和危害性,因此,添加有上述物质的食品有对人体产生毒副作用的风险,影响人体健康,甚至可危害生命。
二恶英及其类似物Ⅲ食品测定方法【http://www.china-pops.net】中国食品卫生杂志ZHONGGUO SHIPIN WEISHENG ZAZHI1999年第11卷第5期Vol.11No.5 1999二恶英及其类似物Ⅲ食品测定方法吴永宁 赵云峰关键词:二恶英 食品 检验方法 食品中PCDD/Fs分析属超痕量(pg-fg)、多组分(同系物、异构体的分离)和复杂前处理技术,对特异性、选择性和灵敏度的要求极高,成为当今食品和环境分析领域的难点。目前仅在发达国家的少数实验室能够开展。WHO指出仅有约100个实验室具备检测能力。〔1〕超痕量分析是因二恶英在环境样品中水平极低,WHO规定的TDI为1~4pg/kgBW;〔2〕相应要求食品中PCDD/Fs测定方法的检测限以脂肪计低于1pg/g(甚至为fg/g水平的测定),不到其它污染物含量的1/1000。所谓多组分是指PCDD/Fs中各同系物、异构体的毒性相差很大,具毒性的17种2,3,7,8-取代PCDD/Fs具有毒性,进行危险性评价时需选择性测定。而PCDD/Fs共有210个同系物、异构体,加上209个PCBs,共有419个二恶英及其类似物。另外,试样在进行仪器分析前要浓缩至1/1000、1/10000,提取液中的PCDD/Fs比其共提取物和基质中同系物及其它氯代化合物等干扰组分低得多,使得这一超痕量分析极为困难。只有良好的净化技术及特异性的分离手段才能满足要求。〔3~5〕为保证分析质量,国际组织及有关国家建立了官方分析方法与指南,如国际癌症研究中心(IARC)〔4〕、欧盟的公共标准局〔6〕、美国环境保护局(EPA)〔7,8〕和美国食品药品管理局(FDA)。〔9〕 FAO/WHO食品法典委员会正在着手建立食品二恶英限量标准和相应检验方法,起草人认为高分辨[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]与高分辨质谱联用技术(HRGC-HRMS)是目前唯一适用的的化学方法。而用DNA重组技术建立的生物学方法在二恶英总TEQ水平测定可达到特异性、选择性和灵敏度的要求,且所测结果与HRGC-HRMS方法相当,可作为大量样品筛选手段。〔10〕1[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]与质谱联用的化学分析方法 PCDD/Fs的化学分析有两种不同的方案,一为分析所有PCDD/Fs,目的在于了解各化合物的分布形式,鉴定其可能的来源;另一为仅测定2,3,7,8-取代的17种PCDD/Fs。后一方法较完善,以美国EPA1613方法为代表的HRGC-HRMS方法已成为各国公认的仲裁方法。本文主要以此为基础对这一领域的进展作简要综述。 环境及生物材料中PCDD/Fs的分析主要包括5个方面,即:样品采集、提取、净化、分离及定量测定。〔4,6〕1.1样品采集〔4,6〕 与有机氯农药残留检测方法相似,但PCDD/Fs应更注意安全操作和避免试验过程中的污染。PCDD/Fs具有光解作用,尤其在溶液中低氯代化合物光解作用更为迅速。故样品应避光、低温保存。样品的取样量依样品类型、污染水平、潜在干扰物质与方法的检测限而定。一般样品为1~50g,对于含脂低、污染轻的样品必要时可增加到100~1000g。1.2提取〔4~10〕 提取前,加入13C或37Cl标记的内标,用以测定提取净化效率与矫正分析丢失。PCDD/Fs的提取方法与有机氯农药残留检测方法相似,包括溶解、振摇、混匀、超声或索氏提取。提取步骤和溶剂选择取决于样品类型和净化方法。如脂肪和油可采用二氯甲烷+已烷(1+1)直接提取;其它食品可使用不同比例的提取溶剂,采用包括索氏提取在内的各种提取方法。许多实验室对比试验已经表明鱼、猪脂肪、牛奶、母乳、人血和脂肪组织所用各种提取方法回收率的可接受性。〔11~15〕作为新技术使用CO2为流体的超临界流体提取方法,也用于生物样品中PCDD/Fs的提取。〔16〕
[b]LIB-V2010-010_三聚氰胺及其类似物的检测(2010)-20100210[/b][url]http://ishare.iask.sina.com.cn/f/6767398.html[/url]LIB-V2010-010_三聚氰胺及其类似物的检测(2010)-20100210.rar说明:扉页 - 1 - 目录 - 1 - 1 三聚氰胺的资料 3 1.1 三聚氰胺事件 3 1.2 亲水色谱检测三聚氰胺的策略 3 1.3 有关科技论文 4 1.4 三聚氰胺及同系物的风险评估 4 1.5 FDA有关消息(FDA News) 5 1.6 更多信息(More information) 6 2 三聚氰胺及类似物的检测 6
【中文名称】蛋氨酸羟基类似物;液体羟基蛋氨酸;2-羟基-4-甲硫基-丁酸;MHB【英文名称】methionine hydroxy-analog; Alimet;MHB【结构或分子式】 【密度】1.23(20℃)【粘度 mPa·s(20℃)】0.105 ;0.035(38℃) ;0.5(0℃)【性状】 外观为深褐色粘液。有硫化物特殊气味。【用途】 用作饲料添加剂时可作为蛋氨酸营养补充剂,促进动物生长发育。【制备或来源】 以丙烯醛为原料,在催化剂作用下同甲硫醇反应,生成的甲硫基丙醛与氢氰酸给催化剂作用合成2-羟基-4甲硫基丁腈,在硫酸存在下水解,经精制得成品。【其他】 凝固点-40℃。是单体、二聚体和三聚体组成的平衡混合物,含量分别为65%、20%、3%。 在使用该产品后,需用水冲净皮肤,若眼睛粘上该产品,亦需用清水冲洗。【包装及贮运】 用250kg塑料桶运载。【生产单位】 美国孟山都公司
[align=left][/align]【作者】:崔靖 韩冬梅 徐隆昌 韦薇【题名】:曲妥珠单抗生物类似药质量"相似性评价标准"探讨【期刊】:药学学报【年、卷、期、起止页码】:2021-01-01【全文链接】:10.16438/j.0513-4870.2021-0998
新浪下载地址[url=http://ishare.iask.sina.com.cn/f/6767398.html][color=#0365bf]http://ishare.iask.sina.com.cn/f/6767398.html[/color][/url]LIB-V2010-010_三聚氰胺及其类似物的检测(2010)-20100210.rar说明:扉页 - 1 - 目录 - 1 - 1 三聚氰胺的资料 3 1.1 三聚氰胺事件 3 1.2 亲水色谱检测三聚氰胺的策略 3 1.3 有关科技论文 4 1.4 三聚氰胺及同系物的风险评估 4 1.5 FDA有关消息(FDA News) 5 1.6 更多信息(More information) 6 2 三聚氰胺及类似物的检测 6本论坛下载地址:[url=http://bbs.instrument.com.cn/shtml/20100210/2395991/]http://bbs.instrument.com.cn/shtml/20100210/2395991/[/url][url]http://bbs.instrument.com.cn/download.asp?ID=201073[/url]
[font=宋体]【作者】:[/font][font=&][size=16px][color=#5b616b][/color][/size][/font][font=&][font=BlinkMacSystemFont, -apple-system, &][size=16px][/size][/font][font=-apple-system, BlinkMacSystemFont, &][color=#3e3e3e]李思鹏,张仲理,许圣昌,张磊[/color][/font][font=BlinkMacSystemFont, -apple-system, &][size=16px][/size][/font][/font][font=&][size=16px][color=#333333][/color][/size][/font][font=&][size=16px][color=#5b616b][/color][/size][/font][font=宋体]【题名】:[/font][font=&] [/font][b][b]单抗生物类似药与原研药质量相似性研究解析[/b][/b][font=宋体]【期刊】:[/font][font=&][size=16px][color=#333333][/color][/size][/font][url=https://jpharmsci.org/article/S0022-3549(22)00208-8/abstract][font=-apple-system, BlinkMacSystemFont, &][size=12px][color=#3e3e3e]《中国新药杂志》 2022 年第31 卷第6 期[/color][/size][/font][/url][font=&][size=16px][color=#333333][/color][/size][/font][font=宋体]【年、卷、期、起止页码】:[/font][font=&][/font][list][color=#0071bc][/color]2022[/list][font=宋体]【全文链接】:[url=https://jpharmsci.org/article/S0022-3549(22)00208-8/abstract][font=BlinkMacSystemFont, -apple-system, &][size=16px][/size][/font]单抗生物类似药与原研药质量相似性研究解析--《中国新药杂志》2022年06期 (cnki.com.cn)[/url][font=BlinkMacSystemFont, -apple-system, &][size=16px][/size][/font][/font]
多巴胺,1,2,3,4-tetrahydro-1-methylisoquinoline-6,7-diol和异丙基肾上腺素极性较大,应用C18柱,苯基柱,氨基柱和腈基柱在反相条件下均无保留,采用五氟苯基柱有较好的保留行为,能有效的将多巴胺及其类似物分离。同时我们发现五氟苯基柱对单苯环的分类化合物有较好的分离效果。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=22315]多巴胺类药物的分离[/url]
食品中PCDD/Fs分析属超痕量(pg-fg)、多组分(同系物、异构体的分离)和复杂前处理技术,对特异性、选择性和灵敏度的要求极高,成为当今食品和环境分析领域的难点。目前仅在发达国家的少数实验室能够开展。WHO指出仅有约100个实验室具备检测能力。〔1〕超痕量分析是因二恶英在环境样品中水平极低,WHO规定的TDI为1~4pg/kgBW;〔2〕相应要求食品中PCDD/Fs测定方法的检测限以脂肪计低于1pg/g(甚至为fg/g水平的测定),不到其它污染物含量的1/1000。所谓多组分是指PCDD/Fs中各同系物、异构体的毒性相差很大,具毒性的17种2,3,7,8-取代PCDD/Fs具有毒性,进行危险性评价时需选择性测定。而PCDD/Fs共有210个同系物、异构体,加上209个PCBs,共有419个二恶英及其类似物。另外,试样在进行仪器分析前要浓缩至1/1000、1/10000,提取液中的PCDD/Fs比其共提取物和基质中同系物及其它氯代化合物等干扰组分低得多,使得这一超痕量分析极为困难。只有良好的净化技术及特异性的分离手段才能满足要求。〔3~5〕为保证分析质量,国际组织及有关国家建立了官方分析方法与指南,如国际癌症研究中心(IARC)〔4〕、欧盟的公共标准局〔6〕、美国环境保护局(EPA)〔7,8〕和美国食品药品管理局(FDA)。〔9〕 FAO/WHO食品法典委员会正在着手建立食品二恶英限量标准和相应检验方法,起草人认为高分辨[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]与高分辨质谱联用技术(HRGC-HRMS)是目前唯一适用的的化学方法。而用DNA重组技术建立的生物学方法在二恶英总TEQ水平测定可达到特异性、选择性和灵敏度的要求,且所测结果与HRGC-HRMS方法相当,可作为大量样品筛选手段。〔10〕
建立一种简单、快速、准确同时测定大米蛋白粉中三聚氰胺及其类似物三聚氰酸、三聚氰胺一酰胺、三聚氰胺二酰胺的方法。样品经二乙胺- 水- 乙腈(1:4:5,V/V)超声提取30min 后,提取液于70℃条件下氮气吹干,在吡啶介质中经甲基硅烷化衍生后采用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]- 质谱仪测定(内标法定量)。此方法检测限为0.5mg/kg、线性相关系数(20~1000μg/L 范围内)不小于0.9989;当加标量为1.0~5.0mg/kg 时,平均回收率为72.01%~96.45%、相对标准偏差不大于6.3%。此方法可用于大米蛋白粉中三聚氰酸及其类似物的检测。
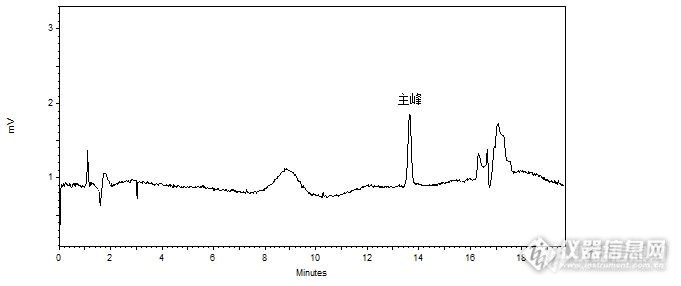
[align=center][b]纳克级激光计数检测器NQAD对胆酸类似物的分析[/b][/align][align=center][b][/b][/align][align=left]纳克级激光计数检测器NQAD是一种高灵敏度的通用型检测器,对于所有不挥发或半挥发样品均能够进行良好检测。[/align][align=left]本实验按照客户提供液相方法,使用NQAD检测器对客户提供的胆酸类似物样品进行了分析。色谱柱选择了柱流失更低的MGIII色谱柱,规格:5μm 4.6 mm i.d. × 150 mm。[/align][align=left][/align][align=left][b]1.精密度、定量限分析结果[/b][/align][align=left]首先对NQAD分析胆酸类似物的精密度进行验证。根据客户要求,将样品稀释至6.0μg/mL低浓度后,连续进样6针,计算精密度RSD%为1.9%,隔日继续进样,计算日间精密度结果为1.2%。进一步将样品稀释到3.0μg/mL后,以该浓度作为灵敏度溶液,得到S/N为19,根据S/N=10计算定量限约为1.6μg/mL,根据S/N=3计算检出限约为0.47μg/mL。图1结果为3.0μg/mL样品分析谱图。[/align][align=left][/align][align=center][img=,681,286]http://ng1.17img.cn/bbsfiles/images/2017/10/201710121028_01_2222981_3.jpg[/img][/align][align=center]图1 3.0μg/mL浓度NQAD分析结果[/align][align=left][img=,680,148]http://ng1.17img.cn/bbsfiles/images/2017/10/201710121030_02_2222981_3.jpg[/img][/align][align=center][/align][align=left][b]2.线性方程[/b][/align][align=left]在3.0-48μg/mL浓度范围内进行线性验证,以3.0、6.0、12、24、48五个浓度点每个点各进一针,得到线性结果如图2所示,相关系数R[sup]2[/sup]为0.9989,得到良好线性关系。[/align][align=center][img=,659,261]http://ng1.17img.cn/bbsfiles/images/2017/10/201710121030_01_2222981_3.jpg[/img][/align][align=center]图2 线性分析结果[/align][align=left][b]3.样品分析[/b][/align][align=left]以2.4 mg/mL高浓度进样10μL分析结果如图3所示,可明显看到多个杂质峰出现,对主峰前的2个杂质峰用标曲进行定量,结果如表1所示,含量分别为0.16%和0.23%。[/align][align=left][/align][align=left][/align][align=center][img=,690,274]http://ng1.17img.cn/bbsfiles/images/2017/10/201710121032_01_2222981_3.jpg[/img][/align][align=left]图3 2.4mg/mL浓度样品分析结果[/align][align=left][img=,673,154]http://ng1.17img.cn/bbsfiles/images/2017/10/201710121032_02_2222981_3.jpg[/img][/align][align=left][/align][align=center]表1 杂质分析结果[/align][align=center][img=,375,118]http://ng1.17img.cn/bbsfiles/images/2017/10/201710121033_01_2222981_3.jpg[/img][/align]
【序号】:1【作者】:金利群; 李晓庆; 李宗通; 柳志强; 郑裕国; 沈寅初; 【题名】:蛋氨酸羟基类似物的生产工艺及其在动物营养中的应用【期刊】:综述 【年、卷、期、起止页码】: 2013年07期【全文链接】:http://www.cnki.net/KCMS/detail/detail.aspx?QueryID=1&CurRec=1&recid=&filename=DWYX201307008&dbname=CJFD2013&dbcode=CJFQ&pr=&urlid=&yx=&uid=WEEvREcwSlJHSldTTEYzU3EyU1k0YS84eTUzU2ZlVGJya3ZQc2NsNXNBMD0=$9A4hF_YAuvQ5obgVAqNKPCYcEjKensW4IQMovwHtwkF4VYPoHbKxJw!!&v=MTYxMThNMUZyQ1VSTHlmYitabUZ5emhWTHJLSVRyU2RyRzRIOUxNcUk5RmJJUjhlWDFMdXhZUzdEaDFUM3FUclc=
生物类废物应根据其病源特性、物理特性选择合适的容器和地点,专人分类收集进行消毒、烧毁处理,日产日清。液体废物一般可加漂白粉进行氯化消毒处理。固体可燃性废物分类收集、处理、一律及时焚烧。固体非可燃性废物分类收集,可加漂白粉进行氯化消毒处理。满足消毒条件后作最终处置。1. 一次性使用的制品如手套、帽子、工作物、口罩等使用后放入污物袋内集中烧毁。2. 可重复利用的玻璃器材如玻片、吸管、玻瓶等可以用1000-3000mg/L有效氯溶液浸泡2-6h.然后清洗重新使用,或者废弃。3. 盛标本的玻璃、塑料、搪瓷容器可煮沸15min.或者用1000mg/L有效氯漂白粉澄清液浸泡2-6h,消毒后用洗涤剂及流水刷洗、沥干;用于微生物培养的,用压力蒸汽灭菌后使用。4. 微生物检验接种培养过的琼脂平板应压力灭菌30min,趁热将琼脂倒弃处理。5. 尿、唾液、血液等生物样品,加漂白粉搅拌后作用2-4h,倒入化粪池或厕所,或者进行焚烧处理。

http://ng1.17img.cn/bbsfiles/images/2012/07/201207131514_377437_2518341_3.jpg 近日,发表在《环境卫生展望期刊》上的一项研究得出了令人震惊的结论:现实中根本不存在“安全”的塑料制品。美国得克萨斯大学的研究者分别用455个各种类型的塑料容器(包括塑料袋和婴儿奶瓶)进行了测试。所有的塑料制品中都装上了模拟食品,经过微波炉加热、湿热(如蒸煮)和紫外线照射处理后,检测其中析出的化学成分。 结果显示,约95%的塑料制品都会析出类似雌激素的化学物质,其中100%的食品包装和食品保鲜盒以及98%的塑料袋都有雌激素类似物析出。并且即使这些塑料制品没有经过任何处理,只是用它们来盛放各种溶液,也会析出类似雌激素的化学物质。标明不含双酚A的奶瓶和水杯甚至比用聚碳酸酯制成的塑料杯所表现出来的雌激素活性还要高。如果将其暴露在紫外线环境中,比在盐水环境中释放出来的化学毒素更多。 好不容易生个孩子,奶粉钱都还没还清就被奶瓶伤害了,想必论坛里面有好多刚刚为夫为母的朋友吧,可知道我们所用的塑料产品到底有没有雌激素,该怎么样去维护孩子们健康的童年,我也很好奇,这个到底是怎么测出来的,有谁愿意测试一下吗,看看到底是不是真的,怎么样才算是含有雌激素呢?为了给孩子们一个健康的童年,大家行动起来吧!!!!!
理论上所有氮含量比蛋白质高的物质都可能被非法添加用以提高蛋白质的检测含量,不过按照违法者的思路,违法添加物应当氮含量高、无异味、颜色与乳制品类似、能溶于水,08年爆出的三聚氰胺即具有以上特点。按GB 5009.5-2010 《食品安全国家标准 食品中蛋白质的测定》检测乳制品中的蛋白质,其中的测定误差也会包括一些含氮的非蛋白质物质,(见GB/T 21704-2008 《乳与乳制品中非蛋白氮的测定》)。本文即针对乳制品中的某种含氮的非蛋白质物质进行方法学研究和测定。学习心得:本文建立了气质联用测定乳制品中三聚氰胺类似物的方法。在日常检验时发现部分数据异常,就对问题进行深入研究,发现其实是一种含氮的非蛋白质物质。再对这种物质进行检索,其实也是符合可能被用来非法添加的理想性能。因为目前尚无该物质的检测方法,因此我们认为很有必要对其检测方法进行研究。 由于性质与三聚氰胺类似,故前处理的思路类似,但毕竟结构不同,又对条件进行了分析优化:样品经萃取,固相萃取净化,提取液氮气吹干后衍生化试剂,于一定温度下衍生一段时间,采用气相色谱-质谱仪选择离子模式外标法测定。采用气质法定量先需找到特征离子:(1)通过对标准物质采用全扫描模式分析会产生哪些离子碎片;(2)在其中选择四个丰度较高且不是背景流失或干扰的离子最为定量离子(这里尤其要注意在全扫描模式下不要选择了柱流失离子,我是采用HP-5MS柱,差点选了背景流失的m/z=73)。另外,如果想了解物质在质谱中以何种基质裂解的,可以使用NIST的质谱分析功能:先在NIST中搜寻到要分析的物质质谱图,再右键单击选择“MS Interpreter”。试试看,效率很高的。 方法定量限为0.05mg/kg;线性相关系数(0.2~50mg/L)大于0.99;在实际样品中加标10、40mg/L,回收率为81.6~ 119.2%,相对标准偏差不大于9.1%。此方法能有效除去干扰、灵敏度高,回收率较好。P.S:不是三聚氰酸,实际上是检测过程中发现数据异常才对该物质进行研究的,具体是什么先卖个关子,感兴趣的朋友不妨回去翻翻自己过去的数据,或许也会有发现^_^
为何柠檬苦素和诺米林是同一波长出峰?是因为同属柠檬苦素类的原因么?柠檬苦素和诺米林是柠檬苦素类似物,出峰波长是一样,但出峰时间不一样。为何?
[b][color=#cc0000][font=微软雅黑]问:[/font][font=微软雅黑]货物类采购项目中,可以要求投标人在技术文件里提供类似业绩证明的材料吗?[/font][font=微软雅黑]答:[/font][font=微软雅黑][font=微软雅黑]可以,注意不要指定行业或区域。法律依据为《政府采购法实施条例》第二十条[/font] [font=微软雅黑]采购人或者采购代理机构有下列情形之一的,属于以不合理的条件对供应商实行差别待遇或者歧视待遇:(四)以特定行政区域或者特定行业的业绩、奖项作为加分条件或者中标、成交条件......[/font][/font][/color][/b]
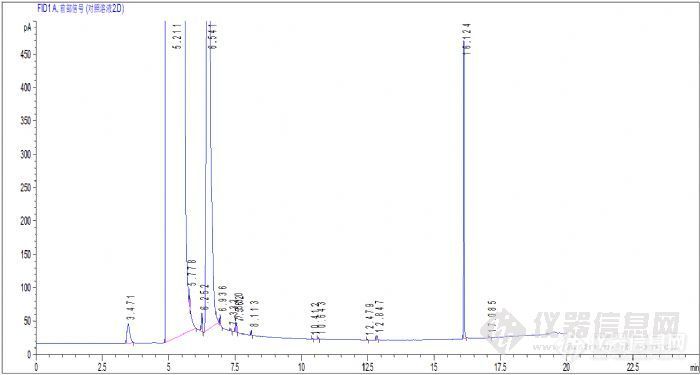
谁测过2-乙基丁醛或类似物质啊,我试了HP-innowax及FFAP。分离都不好。2-乙基丁醛不溶于水,溶于醇、醚。溶剂为甲醇HP-innowax 分离不好所以换了根柱子。FFAP分离度不是很理想,想调整一下也不知道从那下手。柱箱 程序 60 °C 用于 2 分钟 然后 10 °C/min 到 220 °C 用于 2 分钟进样口:200 °C 检测器 : 250 °C 流速: 2.5 mL/min上边的是对照峰,下边的是空白溶剂峰图。 大大看看需要怎么改才能分离的更好。http://ng1.17img.cn/bbsfiles/images/2012/05/201205172336_367576_2507089_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/05/201205172336_367575_2507089_3.jpg
MIBE药物是治疗乳腺癌的,最近缺文献了解该药物的,所以请求各位大神提供我几篇文献,外文的中文的都需要,因为知网找不到MIBE相关的东西,可能我也不了解,所以求助!!暂时知道该药物的中文名称是乙基3- 丁-2-烯酸乙酯。
不知道这篇原创是发在生命科学版面好呢,还是论文写作版面,想来一想,生命科学版面的人们目前有很多的学弟学妹在挣扎着忙SCI的发表,姑且暂时还是发在生命科学版面吧http://simg.instrument.com.cn/bbs/images/default/em09511.gif 现在想想还是 发表在 论文写作和投稿 版面吧 http://simg.instrument.com.cn/bbs/images/default/em09502.gif 本人在生物专业打杂了7年有余,如今毕业了,工作了,拿出当年的投稿经历与大家齐分享一下。 俗话说,外国的SCI不好发,那微生物类的SCI相当的不好发!不好发那也得发的,毕竟头上顶着毕业的压力(我们实验室的规定——硕士毕业必须要SCI一篇!!愁煞同门师兄师姐师弟师妹也,~~~~(_)~~~~ )http://simg.instrument.com.cn/bbs/images/default/em09509.gif 好了,闲话少说,说正题吧。—————————————————————————————— 当时的发表SCI历经4各月,第一次投稿:生物工程工艺 BP期刊(Biotechnology Progress,影响因子2.3左右吧),等了40多天,被无情地拒稿了,悲催了。想一想当时,俺可是抱着必胜的信心投的稿了,这结果太打击人了!!直接给拒绝了!!没有出现类似:大修、小修.....的结果 然后痛定思痛,想想可能是自己太那个啥了,于是放低心态转而改投:应用生物化学与生物技术 ABB(Applied Biochemistry and Biotechnology,影响因子1.7左右)投了后,等啊等,然而却一直没有更新状态,最后等不及了,干脆撤稿了!要知道撤稿不是儿戏,弄不好期刊是要把通讯作者“拉黑!!”的哦,当时感情好老板是该期刊的偶尔的审稿人,所以当时就发了一封电邮说明了一下,最好撤稿改投.... 这时候已经到了本人上研三的年底,时间不多了,经过与老板再三商量,及其不情愿的投了非洲微生物学报AMR(African Journal of Microbiology Research,影响因子0.6左右) http://ng1.17img.cn/bbsfiles/images/2012/12/201212271702_416285_2019107_3.gif 投了以后,就是等待消息。半个月以后,电邮说已经送到审稿人手中,再20天左右说审稿意见已经回来,过两天发给我(其实是老板的邮箱)。这两天我是没事就登陆邮箱,一上午登陆6、7次,一下午还是再登陆6、7次。心里面那个急( ⊙ o ⊙ )啊! 在焦急的等待第三天早上,邮件来了。结果:小修! 看着审稿人的意见,感觉还不算太尖锐,于是赶紧和老板说一下,一起商量着回复审稿人的意见。所幸这时审稿人没有要求追加实验数据啥的,只是对论文的某几个观点进行理论的补充(追加参考文献...) 和导师一起忙活了一上午,搞定。然后,老板说不要着急回复,等个一两个礼拜再回复,要不然显得不太尊重审稿人啥的。 于是 ,了无事事了10天左右,回复了。然后又是等待!!......... zheci这次一个礼拜后,电邮说Accept接受了,于是准备汇款的事宜。汇款完了,文章接受了,俺也顺利毕业了。http://simg.instrument.com.cn/bbs/images/default/em09503.gifhttp://ng1.17img.cn/bbsfiles/images/2012/12/201212271720_416295_2019107_3.gifhttp://ng1.17img.cn/bbsfiles/images/2012/12/201212271721_416296_2019107_3.gif.......................................................................................................未完待续..........敬请期待投稿的更详细的过程.............Cover Letter,等http://ng1.17img.cn/bbsfiles/images/2012/12/201212271722_416297_2019107_3.gif
[em0810] 请教各位!我要去一个做生物类器材的公司面试技术支持的职位。要准备什么啊?我对生物类的器材只是了解一点,不是很强的哦。拜托帮帮忙!
吴辰冰的创新观一是技术,国内生物制药特别是抗体大分子领域基本在仿制,少创新,基础科研匮乏。二是目前的监管和政策法规跟不上生物医药的发展,甚至起了抑制作用,需要在监管上要有新的导向,明确的政策法规。三,产业的资金缺乏,不是中国没有钱,没有投资者,而是缺少有长期眼光、专注行业的有专业背景投资人。9月16日,在中信国健药业股份有限公司(下称中信国健),记者专访了吴辰冰博士。一身得体的西服,鼻梁上架着一副无框眼镜,儒雅又不失威严,吴辰冰很年轻就在哈佛大学博得学术声誉,此后又长期做研发管理,是一个学者型的高管。正如他自己说的,他喜欢安静,在办公室的沙发上,不疾不徐地轻声和我聊了一个小时,期间很少有手势,只有谈及哈佛岁月时,才兴奋起来,声调明显高了几度,眼睛里闪着光,看来那真是段令他开心难忘的时光。吴辰冰,中信国健生物技术研究院院长兼首席科学官。中信国健,是中信集团公司和上海兰生国健药业有限公司共同投资的生物医药高新技术企业。对于一个制药人来说,吴辰冰的履历很完整,在佐治亚大学获得生物化学博士学位,在哈佛大学医学院研究免疫学,又进入雅培做治疗性抗体研究,然后进入药物研发外包企业睿智化学组建了生物药物研发平台,最后到中信国健负责生物药物的研发。从1997年博士毕业工作算起,吴辰冰在药物研发上已有了17年的经历。通过这些历练,对于上海生物药物的发展,乃至上海科技创新中心建设,吴辰冰有一线的观察和感悟。病人的痛苦,促使走上药物研发之路记者:毕业以后就从事研发?吴辰冰:我在读博士时,一直想留校做研究,因为我性格比较安静,喜欢做一些研究,博士毕业后就去哈佛医学院做博士后,我的导师是免疫领域非常有名的学者,如果想留在哈佛大学这样的一流机构里继续科研还是比较容易做到。那时我正在研究一种XLP基因病的机理,需要病人到医学院来采样,每次都能感受到病人的痛苦。有一天,一个病人没来,后来医生跟我说他已经去世了。这件事对我触动挺大,我觉得我还是应该去做药物研发,比做基础研究能更直接的帮助到病人。后来,我去了雅培制药公司,专门做治疗性抗体的研究,这在我职业道路上的一个转折。记者:博士和博士后读的专业不一样?吴辰冰:对,本科是在华东理工大学完成,学的是生物化学工程;博士在美国佐治亚大学读的,专业是生物化学和分子生物学,但是当时研究的领域是内分泌。在国外如果读完博士再去读博士后的话,他们都建议你选择较为不同的一个领域,所以读博士时我选择了内分泌信息通道,读博士后的时候又把这一套完全抛掉了,进入免疫学。记者:完全不相干的课程?吴辰冰:对的,是非常不同的两个研究领域,这对个人成长很有好处,就是要你的学术和视野不是局限于很窄的领域,要有目的性的到另外一个领域拓展视野,否则知识面比较窄。记者:学习压力很大吧?吴辰冰:对,特别在波士顿做博士后的那几年压力很大,所有工作全靠自己,没有人会帮你。那三年自己设计实验、做实验,在实验当中出现的问题自己解决。他们说大学是打基础,我觉得读博士也是打基础,真正学的东西是读博士后的那三年。记者:您读博士后时多少岁?吴辰冰:我1989年毕业,工作了2年后,1991年出国读博。1997年到波士顿开始做博士后,刚好30岁。三年后就进入雅培,在雅培工作10年。记者:在雅培您负责哪一块的?吴辰冰:我是负责免疫项目的开发和一些技术的开发,在雅培做了十多年,那里工作的规范性比较强,特别重要是时间观念,不能像在学术界想做什么就做什么,想做多久就做多久。我觉得在工业界做过的人,对项目的发展、项目的管理都有比较好的训练,所以现在我们招项目负责人,或者比较资深的管理者,一般都是聘用有产业化经营的人。因为运作模式不一样,这个人既要学术上过关,又要懂得在公司的运作环境和项目管理的模式。记者:你们引人才基本上还是从企业里找,科研院所不太多?吴辰冰:科研院所的人才比较合适做早期的基础科研,我们愿意招科研新人,一般就是博士后做个三四年。这样他的科研思维可塑性强,更容易融入企业。记者:项目靠企业,基础研究还是要靠科研院?吴辰冰:对,企业和科研院所有所分工,都很重要,各有风格,企业更讲究协作和分工,科研院所更讲究个人的创造力,所以两家的思维方式和工作方式都有差异。记者:怎么想到自己做新药开发?吴辰冰:我曾经做过一段技术外包服务工作,工艺做到了一定程度就交给别人了,有时候在旁边看着干着急,即便有不同看法,或者是开发的策略和我的想法有相左之处也没办法,毕竟是人家的东西,有他们的意图,你在旁边着急也没用,确实还是要自己做项目,才能真正把自己的想法变成现实。我来之前中信国健的研发能力相对薄弱,经过一年多的努力,现在中信国健的研发系统有200多人,团队的实力大大增强了,特别是引进了几个关键的技术领军人才,使中信国健的研发实力大大提升。记者:那你们新药研发的进展如何?吴辰冰:我们现在上市的两个药和完成临床三期的三个药,都是属于生物类似物,但我们在研的十几种产品大概有50%属于完全创新的。记者:研发团队从哪来?吴辰冰:我们整个研发系统加在一起大概250人。一是靠引进,包括引进海外的人才,这样能快速建立研发能力。还有就是我们内部培养,特别是在公司工作很多年,对公司整个业务也比较熟悉,他们可以在自己技术方面,或者在一些理念方面快速提升。记者:项目团队是怎么激励的?吴辰冰:当一个项目达到一个重要的里程碑的时候,我们对项目的管理以及项目参与人是有一定激励的。大部分是采取荣誉和物质奖励结合的方式。当达到一个节点性的成果都有对团队的奖励。新药研发环境充满挑战记者:现在的环境和以前有什么变化?吴辰冰:现在环境变了,竞争更激烈,而且现在市场比较乱,大家同时开发一类药的情况比较多,但在开发生物类似物方面我们有一定优势,毕竟我们早出发了将近10年,一些产品已经做完三期临床,马上就要推上市场的一些产品,而别人刚刚在报临床,完成这个过程需要5-7的年时间,所以我们有先发优势。以后的发展中,一定要有新药研发、有创新性、有知识产权,目前我们可以承受一点风险,可以做点新的东西。审批时间过长对创新的资本压力很大。记者:现在审批需要多久?吴辰冰:一个生物药物从研究到上市目前需要至少10年。这当中,接受监管部门的审批是非常关键、也是非常耗时的步骤。记者:你希望怎么简化?吴辰冰:现在欧洲的经验是在临床前开发注重质量,进入临床就做一个一期,或者直接做三期,二期可以跳过,整个开发过程大概就3年,也就是从申报到上市大概3年时间,再加上早期的临床前3年的研发,加起来就6年时间,我觉得这是一个比较合理的时间表,如果超过10年肯定不合理,因为在国外即便新药的开发也不会超过10年,在中国做仿制药都超过10年的话,中国这个行业就会被淘汰,自己限制了自己的发展,对行业起抑制作用。记者:医药研发代工(CRO)好像整个行业都不景气了?吴辰冰:这个行业经过一段时间的发展,可能需要整合了,就是强的更强,弱的更弱,有一些公司就会被淘汰了。记者:那上海的CRO企业整合后会怎么样?吴辰冰:药明康德应该还是老大,它的业务还处于比较健康的发展期。CRO从长远来说要走自己的路,就是要有新的商业模式,不能只是你给我钱,帮你做事情,这个阶段有可能再过一段时间就过去了。记者:张江有不少企业是CRO,他们转升级做新药可能吗?吴辰冰:比较困难,代工和创新的商业模式完全不一样,除非有一个公司把它买断,把所有的对外业务停掉,因为这里面有很多利益冲突,实验人员的分配就有问题,是做自己的项目,还是做别人项目。一旦开始做自己的药,别人就不大敢找你,客户担心信息流失,还有资源的分配不公平,你把好的资源全部放到自己项目上,做得最快、最好,别人的项目放一些比较次的资源,这样的利益冲突,没有办法平衡。一旦做了新药就没人再做找你做CRO,这对CRO是生死存亡的事,不能乱做。需要哪些创新记者:张江也有很多医药行业的外企,但这多药企好像对整个医药研发促进作用不明显。吴辰冰:我觉得氛围毕竟是有的,而且人才的聚集也有了,可能合作还是不够。记者:为什么?吴辰冰:可能各自的方向不一样,在中国做研发的外企有的对专利还有一定的顾虑,其实中国的专利保护已经有了很大的发展。跨国企业在中国搞研发,雇的员工大部分也是中国人,我觉得也应该视为中国创造的一部分,现在一些跨国企业你很难说他是哪个国家的公司,好多国家他都有分公司,他只要在中国能够有所贡献,有所发展都是好事情。至少在人才积累、知识交流等方面,各类企业都有所贡献。但是我也明显感觉到国内药企在研发创新方面的崛起以及与之伴随的人才流动。记者:相比较周边的江浙,上海
我们单位想要做一些矿物类的物相分析有做过的朋友么?我想请教几个问题1,做矿物的XRD分析对衍射仪有什么特殊要求么?2,样品需要进行什么处理么,有特殊要求么?3,在谱图分析时有什么特别注意的或特殊处理的么?(之前做过几个矿物类的样品,但分析的结果都不太好,离所需的分析结果差距甚大)谢谢了先
[size=16px][color=#ff0000][b][url=https://www.instrument.com.cn/job/position-79274.html]立即投递该职位[/url][/b][/color][/size][b]职位名称:[/b]生物类仪器管理工程师[b]职位描述/要求:[/b]Responsibilities:1.负责上海站点多个生物部门重点仪器的网格化管理,定期更新仪器主数据信息;2.推进仪器管理系统落地实施,与业务部门合作整理和归档仪器运维相关数据,沟通协调特殊技术问题,确保实验室仪器的正常运行;3.定期核查监控系统运行情况,确保使用率统计准确,并对低使用率仪器进行分析,与业务部门合作查找原因并制定改进方案,提高仪器使用率;4.负责公司生物类重点仪器的验收及报废技术审核工作;5.协调部门间生物类仪器资源调配及共享。Qualifications:1.大学本科以上学历,药学、动物学、免疫学、生物医学、细胞生物学、分子生物学、精密仪器等相关专业,具有1年以上相关工作经验;2.熟悉酶标仪,QPCR,流式细胞仪,组织细胞染色机,细胞分析仪等生物类仪器中的一种或几种,了解仪器的工作原理及日常维护;3.具有较强的沟通能力、组织协调能力和优秀的应变能力,做事严谨,有条理;4.有良好的团队合作精神和敬业精神;具有较强的创新意识、追求卓越的精神。[b]公司介绍:[/b] 药明康德新药开发有限公司于2000年12月成立,是全球领先的制药、生物技术以及医疗器械研发外包服务公司,在中美两国均有运营实体。作为一家以研究为首任,以客户为中心的公司,药明康德向全球制药公司、生物技术公司以及医疗器械公司提供一系列全方位的实验室研发、研究生产服务,服务范围贯穿从药物发现到推向市场的全过程。药明康德的服务旨在通过高性价比、高效率的外包服务帮助全球客户缩短药物及医疗器械研发周期、降低...[url=https://www.instrument.com.cn/job/position-79274.html]查看全部[/url][align=center][img=,178,176]https://ng1.17img.cn/bbsfiles/images/2021/08/202108160948175602_3528_5026484_3.png!w178x176.jpg[/img][/align][align=center]扫描二维码,关注[b][color=#ff0000]“仪职派”[/color][/b]公众号[/align][align=center][b]即可获取高薪职位[/b][/align]
二、 填空题(每小题2分,20分)1、 人体内最主要的含铁蛋白质是-----------------,正常人血液中含量最多的蛋白质是----------------。2、 磷酸戊糖代谢的主要生理意义是产生---------------和-------------------。3、 肽类激素作用的主要第二信使分子是------------------,它是由---------------酶催化而生成的。4、 DNA复制的方向是--------------------,蛋白质生物合成的方向是------------------。5、 各种tRNA分子的3末端均有一个共同的结构,是-------------------,这个臂的作用是----------------------。6、 人工合成的最主要的嘌呤类似物有------------------,嘧啶类似物-----------------,它们在临床上可用作抗癌药。7、 某一酶促反应的底物浓度相当于1/2Km,则此反应的初速度为-----------Vm。8、 写出下列英文缩写在生物化学中的中文含义,dNTP------------------------------,CAMP--------------。9、 在蛋白质生物合成过程中,携带转运氨基酸的核酸是 -----------------------,决定氨基酸排列顺序的是---------------------------------。10、脂肪酸β氧化的产物是-----------------------,细胞内进行此代谢反应的主要部位是---------------。四、名词解释(每题3分,15分) 1、限制性内切核酸酶 2、遗传信息传递中心法则 3、变构酶 4、蛋白质的亚基 5、密码子五、问答题(每题10分,20分)1、 简要解释糖尿病患者下述表现的生化机理。(1) 高血糖和糖尿(2) 酮症(3) 糖耐量曲线异常2、 简要说明缺乏叶酸和VitB12产生巨红细胞贫血的生化原因。
我想做蛋白质与小分子化合物(潜在抑制剂)相互作用的分析,确定他是底物类似物还是非底物类似物。2013年发表的两篇文章使用Electrospray ionization mass spectrometry (ESMS)方法,使用Qtof-micro MS instrument (Waters Corp.,Milford, MA).仪器来进行检测。文章名字:“New Classes of Alanine Racemase Inhibitors Identified byHigh-Throughput Screening Show Antimicrobial Activity against Mycobacterium tuberculosis”。我们学校现有的质谱仪:高效液相色谱-质谱联用仪,LTQXL。但是我去询问过了,做不了。请问各位知道哪里有这样的质谱可以做么?我在河北,不知道北京有没有。如果用其他的方法可以检测么?谢谢!!!!!!!!!