请问大家有测过蚯蚓生物标志物吗?如酶活性,中性红保留时间等,测这些生物标志物的时候,可以用冷冻条件下保存一段时间的蚯蚓吗?对酶活性测试会不会有影响呢?看了文献好久没有找到答案,谢谢大家
生物质谱具备高的分辨率和快速扫描速度,这些能力让生物质谱具备了高通量处理生物样品的能力。现在生物质谱在找寻生物标志物bio-marker发挥着重要作用,这些生物标志物可能是蛋白质(蛋白质组学),可能是代谢产物中某个代谢物(代谢组学)。发现并确定这些生物标志物对疾病的早期发现和治疗具有重要的意义(记得一句广告词:早发现早治疗),尤其对于癌症的早期诊断和治疗。很多仪器公司致力于质谱在生物标志物的发现和应用,如赛默飞世尔,具体新闻见:http://bbs.instrument.com.cn/post.asp?forumid=628&FTTID=1生物质谱在寻找这些生物标志物具有无可比拟的优势,你认为生物质谱未来的发展会成为医疗机构的诊断工具吗?我们检查身体的时候血样和尿样以后会用质谱做常规检查吗?大家可以讨论一下1质谱在寻找生物标志物的应用;2质谱和生命诊断的应用发展;3生物质谱如果成为诊断工具还需要哪些进步;4.自己寻找生物标志物的具体例子(涉及自己没发表的文章点到即止);5.。。。言之有理即加分

[color=#DC143C][size=4][center]生物标志物与危险度评定[/center][/size][/color][img]http://bbs.instrument.com.cn/images/affix.gif[/img][url=http://bbs.instrument.com.cn/download.asp?ID=196929]生物标志物与危险度评定.rar[/url][img]http://ng1.17img.cn/bbsfiles/images/2010/01/201001151022_196930_1626679_3.jpg[/img]
求购GB/T 18606-2001[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱法测定沉淀物和原油中生物标志物求购GB/T 18606-2001[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱法测定沉淀物和原油中生物标志物
中药质量是中药临床疗效的保障,中药科技工作者为中药质量控制做了大量的工作,但仍未能满足日益提高的对中药质量控制的要求。为提升我国中药产品质量和质量控制水平,中国工程院院士刘昌孝研究员针对中药生物属性、制造过程及配伍理论等医药体系自身的特点,提出了中药质量标志物(Q-marker)的新概念。中药质量标志物是存在于中药材和中药产品(如中药饮片、中药煎剂、中药提取物、中成药制剂)中固有的或加工制备过程中形成的、与中药的功能属性密切相关的化学物质,是反映中药安全性和有效性的标志性物质。质量标志物确定的基本方法和技术?中药质量标志物可基于基原性鉴别、物质分析和生物学评价3类方法和技术的集成和整合来确定质量标志物。基原性鉴别方法和技术主要有经验识别、形态观察、生物基原、DNA条码等。物质分析方法和技术主要有紫外光谱、红外光谱、指纹图谱、化学标志物等。生物学评价方法和技术主要有生物色谱、生物效价、药效指标、毒理学指标、药代指标和代谢产物、根据中医理论建立的药物性味和功效测定方法、网络药理学与网络毒理学方法等。
http://www.bioon.com/biology/UploadFiles/201112/2011121209251602.jpg肺腺癌是常见于非吸烟者的一种非小细胞肺癌形式,间皮瘤是能被石棉触发的一种罕见癌症。纽约大学癌症研究所研究人员正在从事于一种血液测试,这种血液测试的目的是测定与这些癌症形式相关的抗体,早期诊断疾病,甚至点出高风险的人。肺腺癌和间皮瘤癌细胞在它们的表面有聚糖生物标志物,病人甚至是早期的也有这些聚糖的抗体,研究人员已创造了用286个不同聚糖点提前制备的印刷聚糖芯片。作为高能量平台的一部分,这能被用于筛查血清样本来鉴定生物标志物。课题组正在比较来自患恶性间皮瘤病人的与接触石棉但无疾病症状的高疾病风险人的血清。虽然这个测试是在非常早的阶段,但它能帮助医生提醒有发生这些癌症风险的人。这可能尤其对可能没有被正式地筛查的非吸烟者有用,对那些可能对治疗反应不好需要更侵略性治疗方法牟疾病晚期病人也一样有用。这将允许为病人特定治疗和更好结果的治疗(与在医疗系统上更低负担一样),也能帮助鉴定药物发展的新路线。
有没有人用毛细管电泳做过生物标志物检测方面的啊?
帕金森病理发展的轨迹探索的研究仍在进行中。近期,一项在美国麻省理工学院和马萨诸塞州总医院帕金森病研究中心进行的一项病例对照研究表明,帕金森病患者黑质致密部(SNc)神经变性早于基底前脑(BF),并且建立了一种新型多光谱磁共振成像技术用于追踪PD变性的生物学标志物。 该研究入选了29例PD患者(Hoehn-Yahr分期1-3期)和27例相匹配的健康对照者,使用新型多光谱结构磁共振(MR)成像工具来衡量的黑质致密部(SNc)和基底前脑(BF)以验证帕金森病(PD)患者黑质致密部(SNc)发生神经变性早于胆碱能基底前脑(BF)。 研究者对每一例受试者进行多回波T1加权,多回波质子密度,T2加权,T2加权液体衰减反转恢复(FLAIR)序列等磁共振检查。对于SNc,创建了一个多重回波的平均加权值,提供高比率对比噪声的单个体积。使用T2加权FLAIR图像可视化观察BF。对于每一例受试者,手动标记这两个结构,并计算出它们的体积。 研究结果表明,与对照组相比,13例H-Y1期的PD患者SNc体积明显减小,16例H-Y2-3期患者则表现少量额外的体积减小。与此相反,BF体积的丢失则发生在疾病的后期,H-Y2-3期患者比对照者和H-Y1期患者体积丢失更明显。H-Y1期患者与对照组没有显著性差异。 因此,作者在结论中写到,我们的研究结果支持PD的神经病理学发展轨迹,并建立了新的多光谱磁共振成像方法作为追踪SNc和BF变性的生物学标志物。
农残检测版块我看大部分作品都是仪器检测方面的内容,可是农药残留现在不单单是残留本身的问题了,还有对作物本身的影响及这些受影响的作物人体摄入后又有哪些变化呢?很少提及!另外,农药残留如果单从仪器检出方面来评估的话,可能对整个地区的横断面的描述缺乏论据,如果我们能找出一个预警的信号,根据这个信号有针对性的检测,相比工作效率事半功倍,而且对这个地区农残的危害可以有一个预见作用。 因此,出于以上考虑,我把自己近期的一个课题摘要,跟大家分享一下,欢迎批评指正,也希望对大家有所启发。探讨细胞色素P450酶系作为农药残留生物标志物的可行性目的和意义农药使用范围不断地扩大,新型农药不断涌现,这必然造成对农作物和环境的污染。因此及时、准确地对污染情况进行分析、监测,减少和防止对农作物和环境的污染以及对污染情况进行评估显得刻不容缓。传统的监测和评估是利用现代化仪器和手段进行准确定量的理化分析,但有些农药代谢分解迅速不易检出,而且仅凭含量无法反映这些农药对生物的效应,要检测和评估其对生物和环境质量的影响,就要研究在农药作用下生物体内各种指标的变化。生物标志物(biological marker)就适应了这种需要。生物标志物是指生物体由于接触外源毒物后而产生可在生物介质中测定到的细胞、生物化学和生物分子的改变,主要包括机体酶系统、细胞内的DNA、蛋白质、、谷胱甘肽、抗坏血酸以及结构生理生化功能等。细胞色素P450酶系是生物体中最重要的一组代谢酶,可由许多内源性和外源性的化学物质诱导。利用P450酶系的诱导作用,可以将其作为毒物污染机体在分子水平上敏感的生物标记物。农药作为外源性毒物,生物体在遭受其污染后会诱导P450酶系进行解毒。因此,本研究项目探索细胞色素P450酶系作为农药污染生物标志物的可行性。拟用常用农药胁迫生物体,检测生物体内细胞色素P450酶系总量的变化,搞清常用农药不同浓度胁迫生物体后与生物体内细胞色素P450酶系剂量-效应关系以及细胞色素P450酶系各个家族、亚家族的诱导效应,找出农药污染后体内细胞色素P450酶系中变化较特异的家族或亚家族,作为农药污染后特异的诊断评估工具,可为我国环境质量评价、化学物毒性评价、生态风险评价与预警系统提供理论依据国内外研究进展细胞色素P450酶系是生物体中最重要的一组代谢酶,根据酶的氨基酸序列相似性,细胞色素P-450酶系被分类并命名为家族(CYP1,2,3)、亚家族(A,B,C…)、单个基因(A1,2,3…),当前发现的P450基因超家族包括36个基因家族,其可由许多内源性和外源性的化学物质诱导。利用P450酶系的诱导作用,可以将其作为毒物污染机体在分子水平上敏感的生物标记物。目前国内外非常重视污染物监测的生物标志物研究,肝细胞色素P450酶系的诱导已被提出作为评价环境污染状况的最灵敏的生物学反应之一。国内外很多学者研究了野生动物、鱼类、蚯蚓、小麦等生物细胞色素P450酶系对多环芳烃(PAHs)、多氯联苯(PCBs)污染的指示作用,对哺乳动物和鱼类研究主要集中肝细胞色素P4501A1,因为与该细胞色素结合的EROD(乙氧基异酚唑酮)便于检测,而对于植物细胞色素P450酶研究则集中考察其总量的变化上。有关生物体细胞色素P450酶系作为常用农药污染的生物标志物的研究少见报道,有些只研究特定农药污染水体后葱属植物的EROD的指示作用。对所涉及的细胞色素P450酶系各个家族对农药污染后指示作用的系统研究未见报道。对于农药污染后体内细胞色素P450 酶系总量及各个家族亚家族含量变化较特异的指示生物的研究亦未见报道,对生物体细胞色素P450酶系作为农药污染空气、土壤、水体的生物标志物的系统研究尚属空白。技术发展趋势:1. 细胞色素P450将作为农药残留的长期生物效应的诊断工具,考察农药残留的危害性。[/
请问有哪些小分子疾病标志物啊?
20世纪基因组学研究取得的巨大成就为蛋白质组学的发展奠定了基础。蛋白质组学是从整体水平上分析生命体、组织或细胞的蛋白质组成及其活动规律的科学,以基因表达产物为研究对象,延伸了基因组学研究深度,更深层次地揭示了生命活动规律。蛋白质组学的研究内容主要包括蛋白质表达存在方式(修饰形式)的鉴定、结构与功能分析、蛋白质定位、蛋白质差异表达以及蛋白质间相互作用分析等[1]。目前蛋白质组学研究技术主要包括:二维电泳技术、蛋白质芯片技术、质谱技术等[2]。其中,二维电泳技术是早期蛋白质组学的重要技术之一,但是由于实验步骤多,耗时长,重复性差等特点,已经逐步被新型技术所取代。蛋白质芯片技术是将多种蛋白质纯品点于芯片表面,形成蛋白质矩阵进行免疫等标记反应,主要受限于很多蛋白质无法获得纯品而不能用于芯片制备。质谱技术由于灵敏度高、特异性强、分析范围宽等优点逐渐成为蛋白质组学的主要研究手段,可以对特定生命过程中的功能性蛋白质分子进行定性和定量检测,因此在基础科研和临床研究中得到了广泛的应用[3,4]。一、基于质谱的蛋白质组学技术1.基于质谱的蛋白质组学定性技术:蛋白质定性鉴定的基本原理在于:蛋白质组的基本序列已经通过基因组学信息获得,可以用来鉴定多肽的氨基酸序列,并且获得多肽与蛋白质的对应关系[1],即质谱提供的多肽碎片数据可以与蛋白质数据库自动匹配来确定多肽序列与蛋白质归属。基本技术策略分为:(1)自上而下(Top–down)策略[5],即完整蛋白质在质谱中进行分析,可以提供完整蛋白质的质量数,但是由于质谱仪受到质量分析范围的限制,此方法在常规实验室不易实现。(2)自下而上(Bottom–up)策略[6],即蛋白质被蛋白酶水解成多肽,然后对多肽进行质谱分析和碎裂。基于这条策略的大致步骤为:蛋白质样品首先经过酶解降解为多肽,然后对多肽进行色谱–质谱分离与鉴定,最后通过搜索引擎(MASCOT:http://www.matrixscience.com/server.html, SEQUEST:http://fields.scripps.edu/sequest等)在公共蛋白质组学数据库(SWISS–PORT: http://web.expasy.org/groups/swissprot, NCBI:http://www.ncbi.nlm.nih.gov/pubmed等)中自动完成质谱数据的解析,确定多肽序列与蛋白质种类。该技术灵敏度高,特异性好,仪器自动化程度高,可以鉴定出生物样品中成千上万种蛋白质,被认为是大规模、高通量蛋白质定性检测的首选方法。2.基于质谱的蛋白质组学相对定量技术:对于大多数生命科学和医学研究来说,仅完成样品中蛋白质组的定性研究是远远不够的,还需要对蛋白质组进行定量分析。由于组学的研究对象是多个蛋白质,单次检测很难实现所有蛋白质的绝对定量,因此蛋白质组学定量多为相对定量检测。蛋白质组学定量的质谱技术包括谱图计数、质谱峰强度定量、同位素定量技术等。其中使用同位素作为内标定量的方法是目前质谱定量的最佳手段,即对整体蛋白质组进行同位素标记,并使用每一种天然蛋白质与同位素蛋白质的比值进行相对定量分析。主要分为细胞层面标记和蛋白质层面标记两种技术路线:(1)细胞层面标记的细胞培养氨基酸稳定同位素标记(stable isotope labeling with amino acids in cell culture,SILAC)方法[7]:即在两种细胞样品中分别加入轻重同位素标记的培养基,经过传代培养后,两种细胞样品中的全部蛋白质中分别嵌合了轻重同位素,可以在质谱上根据同位素的不同质荷比直接判断样品来源并进行定量比对。(2)蛋白质层面标记:使用含有同位素的小分子与样品全部蛋白质直接标记,如同位素标记相对和绝对定量技术(isobaric tags for relative and absolute quantification,iTRAQ)[8]、同位素编码亲和标记(isotope–coded affinity tag,iCAT) [9]、18O标记[10]等方法,此类方法使用带有稳定同位素的小分子与特定氨基酸侧链反应,使得多个样品可以分别连接含有不同同位素个数(多至8个)的小分子,从而产生一级数据相同但是二级数据不同的质谱谱图,通过二级谱图强度比对进行多个样品的定量分析。3.基于质谱的目标蛋白质绝对定量技术:质谱技术对目标蛋白质的绝对定量检测主要通过质谱多反应监控技术与同位素多肽内标技术联用来实现[11]。该方法首先选定目标蛋白质的一个或多个多肽,合成序列相同但含有稳定同位素的多肽作为内标,定量加入样品中,通过监测特定多肽及其同位素多肽的质谱峰强度进行比对和计算获得目标蛋白质的定量值。质谱多反应监控技术通过进行母离子筛选与子离子筛选等二次选择过程,筛选出目标蛋白质,而非目标蛋白质由于无法通过筛选达到检测器,极大降低了噪音干扰。因此,此方法针对性强,本底噪音低,是目前质谱技术中定量能力最好的一种,可以控制变异系数小于15%,检测限低至纳克每毫升,适合血液、组织等临床样品的定量检测[11]。二、质谱技术发现肿瘤蛋白质标志物质谱技术作为一项强有力的研究工具在科学研究中发挥着巨大的作用,特别在肿瘤相关研究中,目前已经获得美国食品药品监督管理局(Food and Drug Administration,FDA)批准的肿瘤标志物包括多种蛋白质前列腺特异性抗原(prostate–specific antigen, PSA), 癌胚抗原(carcinoembryonic antigen CEA), 人类表皮生长因子受体2(human epidermal growth factor receptor 2,Her–2), 人绒毛膜促性腺激素(human chorionic gonadotropin, HCG), 糖类抗原CA125等,均揭示了蛋白质与肿瘤发生发展密切相关。这些已有成果极大促进了质谱技术在肿瘤蛋白质标志物研究中的应用,并取得了标志性进展。例如:美国约翰霍普金斯大学的Chan课题组发现了新型卵巢癌蛋白质标志物,他们使用表面增强激光解析电离质谱技术(surface enhanced laser desorption and ionization time–of–flight mass spectrometry, SELDI–TOF MS)技术对503个妇女的血清进行了蛋白质组学的分析[12],在随后的大量临床验证中最终确定CA125、β2微球蛋白,转铁蛋白,甲状腺运载蛋白和载脂蛋白A1的联合检测可以作为卵巢癌的新型临床诊断指标。2009年9月该试剂盒OVA1(商品名称:http://ova–1.com)获得了美国FDA的认证,进入临床使用,被认为是国际肿瘤蛋白质标志物研究的重要标志性成果。同时,肿瘤仍然是国际上致死率最高的疾病之一,缺乏早期检测技术和有效治疗方案,临床中还存在着大量问题需要解决,新型标志物的研发迫在眉睫。由于肿瘤蛋白质标志物研究的难度大,风险高,因此近十年来仅有几例试剂盒获得了美国FDA批准,进入临床使用。大量标志物研究还停留在论文研究水平,其中临床问题、研究思路和技术方案的选择直接关系到研究的成功与否。1.临床问题选择:在肿瘤蛋白质标志物研究中,临床问题的选择是研究核心。在肿瘤研究中,需要解决的临床问题往往包括肿瘤早期检测、肿瘤分期检测、治疗方案与药物选择、疗效评估等多个方面。研究者需要根据不同肿瘤的临床情况,具体分析并凝练不同肿瘤的主要临床问题。例如,对于病程发展快、五年存活率低、没有有效手术或化疗手段的肿瘤,早期诊断是研究重点,如胰腺癌、卵巢癌、肺癌等;对于病程发展慢、手术效果明显的肿瘤,肿瘤的愈后与复发是需要关注的问题,如前列腺癌、肠癌等;还有一些肿瘤有特殊的检测需求,如乳腺癌虽然有临床有效的雌激素受体(estrogen receptor,ER),孕激素受体(progesterone receptor,PR),HER2等基因标志物,可以进行药物靶点治疗,但是三阴性乳腺癌的检测还缺乏有效的标志物与治疗方案。因此,在肿瘤蛋白质标志物研究实验开展之前,明确临床问题,并以此确定临床样品入组标准,是研究成功的核心基础。2.研究思路设计:不同于基础科学实验,临床实验需要在大量样本中进行实验结果的验证,因此肿瘤蛋白质标志物研究往往包括新型标志物发现和验证两部分。标志物发现实验是在疾病组和对照组之间进行蛋白质组学分析,鉴定样本中的未知蛋白质组并进行相对定量比较,分析数据选择出在两组样本中差异最大的一个或几个蛋白质作为新型标志物的候选物。随后,标志物验证实验在大量未知样本中进行蛋白质候选物的定量检测,使用发现实验中建立的区分标准进行判读,计算检测灵敏性(sensitivity)和特异性(specificity)。有效的蛋白质标志物研究往往需要发现与验证的两步设计思路来相互保证。3.技术方案选择:根据蛋白质标志物研究的两步设计思路,发现实验中使用基于质谱的蛋白质组学定性技术与相对定量技术对样本中的大量未知蛋白质进行分析,获得标志物候选物名单。验证实验中根据已有名单,进行目标蛋白质(非蛋白质组学)的精确定量检测。这几种质谱技术的配合使用,可以满足不同实验情况和目的,最终实现新型蛋白质标志物的成功研发。三、展望质谱技术是现阶段蛋白质组学研究的核心技术,具有灵敏度高、特异性强、分析通量大等优势,特别是其与同位素内标的联合使用,大大提高了质谱定量能力,因此在多种肿瘤标志物研究中取得了突破性进展并被广泛应用。目前,大量肿瘤蛋白质标志物候选物已经通过使用质谱技术被从血液、组织、体液中筛选出来,预计在完成大规模临床验证后可以作为新型标志物在临床使用,促进肿瘤检测水平的发展。同时值得注意的是,质谱技术还不具备进行蛋白质组的绝对定量能力。相对于免疫等传统蛋白质检测技术,仪器昂贵,操作复杂,自动化程度低,这些因素决定了质谱目前适用于蛋白质的临床研究,但不适用于蛋白质的临床检验,这是质谱技术面临的重要挑战之一。参考文献[1]何华勤. 简明蛋白质组学[M]. 北京:中国林业出版社, 2011:1,76,85-95,119,125-138.[2]RuediA, MatthiasM. Mass spectrometry-based proteomics[J]. Nature, 2003, 422(13):198-207.[3]甄艳, 施季森. 质谱技术在蛋白质组学研究中的应用[J]. 南京林业大学学报:自然科学版, 2011, 35(1):103-108.[4]孙瑞祥, 付岩, 李德泉,等. 基于质谱技术的计算蛋白质组学研究[J]. 中国科学E辑信息科学, 2006, 36(2):222-234.[5]WhiteleggeJ,HalgandF,SoudaP, et al. Top-down mass spectrometry of integral membrane proteins [J]. Expert Review Proteomics, 2006, 3(6):585-596.[6]ChaitBT. Mass spectrometry:bottom-up or top-down? [J]. Science, 2006, 314(5796):65-66.[7]TranDT, AdhikariJ, FitzgeraldMC. StableIsotope Labeling with Amino Acids in Cell Culture (SILAC)-based strategy for proteome-wide thermodynamic analysis of protein-ligand binding interactions [J]. Mol Cell Proteomics, 2014,13(7):1800-1813.[8]DytfeldD, KandarpaM, StrahlerJR, et al. Proteomic Profiling of Multiple Myeloma (MM) Cells Using iTRAQ and Label-Free Quantitative Proteomics for the Prediction of Complete or near Complete Response (CR/nCR) In Frontline Treatment with Lenalidomide, Bortezomib, and Dexamethasone [J]. Blood, 2010, 116(21):271-272.[9]García-SantamarinaS, BoronatS, DomènechA, et al. Monitoring in vivo reversible cysteine oxidation in proteins using ICAT and mass spectrometry [J]. Nat Protoc,2014,9(5):1131-1145.[10]MirzaSP, GreeneAS, OlivierM. 18O labeling over a coffee break:a rapid strategy for quantitative proteomics [J]. J Proteome Res, 2008,7(7):3042-3048.[11]曹冬, 张养军, 钱小红. 基于生物质谱的蛋白质组学绝对定量方法研究进展[J]. 质谱学报, 2008, 29(3):185-190.[12]ZhangZ, BastRC, YuY,et al. Three biomarkers identified from serum proteomic analysis for the detection of early stage ovarian cancer[J]. Cancer Res,2004,64(16), 5882-5890.
由我会组织生态环境部华南环境科学研究所等单位编制的团体标准《有机污染物人体暴露生物标志物筛选技术规范》已完成征求意见稿,根据《中国环境科学学会标准管理办法(试行)》的有关规定,现公开征求意见。请填写意见反馈表,并于2024年7月26日前将有关意见反馈我会(电子文档请同时发送至联系人邮箱)标准征求意见稿及其编制说明、意见反馈表可登录中国环境科学学会官网(http://www.chinacses.org)下载。联系人:生态环境部华南环境科学研究所 邝洪轩电 话:13570478575邮 箱:kuanghongxuan@scies.org地 址:广州市黄埔区瑞和路16-18号邮 编:510530联系人:中国环境科学学会 高强电 话:18515189927邮 箱:gaoqiang3411@163.com地 址:北京市海淀区红联南村54号邮 编:100082[url=http://file2.foodmate.net/wenku2024/wfx202407011513.zip]附件:[/url]1.有机污染物人体暴露生物标志物筛选技术规范(征求意见稿)2.有机污染物人体暴露生物标志物筛选技术规范(征求意见稿)编制说明3.意见反馈表
[align=left][font='calibri'][size=16px]外泌体[/size][/font][font='calibri'][size=16px]作为标志物用于肿瘤的早期诊断[/size][/font][/align][font='times new roman'][size=16px]外泌体是一种磷脂双层膜包裹的生物纳米颗粒,直径为[/size][/font][font='times new roman'][size=16px]30-200 nm[/size][/font][font='times new roman'][size=16px]。近年来,由于外泌体携带大量遗传物质,在介导细胞[/size][/font][font='times new roman'][size=16px]-[/size][/font][font='times new roman'][size=16px]细胞间通信中发挥重要作用,已成为液体活检最理想的分析目标。[/size][/font][font='times new roman'][size=16px]肿瘤生物标志物的检测可以协助肿瘤的早期诊断和治疗。近年来,外泌体在肿瘤的发生发展过程中显示出重要的作用,逐渐成为重要的诊断生物标志物和治疗靶标。肿瘤来源的外泌体携带分子和基因载体,反映了肿瘤细胞的部分组成,广泛分布于血液和包括尿液在内的其他体液。这些外泌体可以作为一种微创的液体活组织检查,对肿瘤进行实时的非侵入性分析,帮助疾病的临床诊断。外泌体作为疾病诊断和预后的标志物,相比于传统的[/size][/font][font='times new roman'][size=16px]miRNA[/size][/font][font='times new roman'][size=16px]分子具有明显的优势。肿瘤细胞衍生的外泌体携带的[/size][/font][font='times new roman'][size=16px]mRNA[/size][/font][font='times new roman'][size=16px]、[/size][/font][font='times new roman'][size=16px]miRNAs[/size][/font][font='times new roman'][size=16px]和蛋白质等生物活性分子通常构成了肿瘤细胞的总蛋白质组或转录组的一部分,反映了亲本细胞的遗传信息。而且这些生物活性分子由于受到外泌体双层膜结构的保护使其在运输过程中不被降解。此外,这些外泌体在不同的储存情况下,包括在[/size][/font][font='times new roman'][size=16px]4[/size][/font][font='times new roman'][size=16px]℃下短期储存[/size][/font][font='times new roman'][size=16px]96 h[/size][/font][font='times new roman'][size=16px]或在[/size][/font][font='times new roman'][size=16px]-80[/size][/font][font='times new roman'][size=16px]℃下长期储存,都具有很强的活力。外泌体的这些特性使其成为癌症诊断、预后和治疗反应的重要监测指标。[/size][/font][font='times new roman'][size=16px]多项体外研究表明,通过应用蛋白质组学和转录组学的方法,使用外泌体及其内容物和表面蛋白可以更早地发现癌症,从而提高预后和生存率[/size][/font][font='times new roman'][size=16px][43][/size][/font][font='times new roman'][size=16px]。结肠癌患者血浆标本中外泌体水平的提高与肿瘤细胞的整体存活率的下降有相当大的联系[/size][/font][font='times new roman'][size=16px][32][/size][/font][font='times new roman'][size=16px]。另一项研究表明,外泌体上的[/size][/font][font='times new roman'][size=16px]CD24[/size][/font][font='times new roman'][size=16px]、[/size][/font][font='times new roman'][size=16px]EDIL3[/size][/font][font='times new roman'][size=16px]和纤维连接蛋白被认为是早期乳腺癌的标志物。此外,在非小细胞肺癌的外泌体中,研究人员发现表皮生长因子受体([/size][/font][font='times new roman'][size=16px]EGFR[/size][/font][font='times new roman'][size=16px])、胎盘碱性磷酸酶([/size][/font][font='times new roman'][size=16px]PLAP[/size][/font][font='times new roman'][size=16px])和富亮氨酸的α[/size][/font][font='times new roman'][size=16px]-2-[/size][/font][font='times new roman'][size=16px]糖蛋白[/size][/font][font='times new roman'][size=16px]1[/size][/font][font='times new roman'][size=16px]([/size][/font][font='times new roman'][size=16px]LRG1[/size][/font][font='times new roman'][size=16px])的过表达。最近的报告显示,使用无标记的液相色谱[/size][/font][font='times new roman'][size=16px]-[/size][/font][font='times new roman'][size=16px]串联质谱([/size][/font][font='times new roman'][size=16px][url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS[/size][/font][font='times new roman'][size=16px])检测前列腺癌患者的尿液,研究人员发现存在于尿外泌体中的[/size][/font][font='times new roman'][size=16px]PCA3[/size][/font][font='times new roman'][size=16px]和[/size][/font][font='times new roman'][size=16px]TMPRSS2:ERG[/size][/font][font='times new roman'][size=16px]蛋白是潜在的生物标志物。这些发现表明从体液中分离得到的外泌体可能是肿瘤早期检测的重要非侵入性标记物。[/size][/font]
3美分、5分钟:“事情就是这么酷”美15岁少年研发的简易检测手段可在致命癌症初期发现标志物2013年03月14日 来源: 中国科技网 作者: 张梦然 本报记者 张梦然 综合外电http://www.stdaily.com/stdaily/pic/attachement/jpg/site2/20130314/021363195437453_change_chd3338_b.jpg杰克·安德雷卡在演讲 今日视点 许多人因史蒂夫·乔布斯的离世而认识了胰腺癌这个杀手。目前,在被发现罹患胰腺癌的病人中,每20人会有19人在5年后死亡,造成这种局面很大程度上是此类癌症十分难以觉察,直到患者已临近其生命的最后阶段,而此时的患者已不大可能对治疗有反应。 不过,一项最新的研究成果很可能改变这一切。据英国《每日邮报》在线版3月份消息称,来自美国马里兰州克朗斯维尔市的杰克·安德雷卡(Jack Andraka),以一种简单的浸沾测试来测试间皮素水平,由于间皮素是血液和尿液中发现早期胰腺癌的生物标志物,这个全新的测试以此有望彻底改变胰腺癌的治疗。 更令人震惊的是,杰克·安德雷卡,年仅15岁。 寻求帮助曾遭197名科学家拒绝 杰克·安德雷卡一直以全副身心热爱着科学和工程,据他自己说他非常迷恋“提出假设、检验假设、分析结果,然后再重来一遍”,还在自己家车库里鼓捣了一个实验作坊。但在他家的一个朋友因患胰腺癌去世后,他意识到对癌症进行提前检测的重要性。在一次上生物课时,安德雷卡偷偷阅读着《华尔街日报》,上面一篇关于碳纳米管的文章突然让他顿有所悟。 正是这次“顿悟”,让安德雷卡后来凭借着对胰腺癌诊断的独特便捷方式获得了“2012年英特尔国际科学与工程学大赛”中7.5万美元的奖金,这次比赛的选手多达1500名,每一名也都曾在自己国家披荆斩棘,而安德雷卡最后脱颖而出。 不过,在灵感浮现最初,安德雷卡很明白,科研仅靠灵光乍现的一刻显然是不够的。这位执着的少年开始为他的研究征求帮助,却先后遭到197名科学家的拒绝——有些相当直率地告诉安德雷卡,他的想法显而易见的不会有任何作为。 幸而,最后约翰霍普金斯大学的肿瘤病理学教授阿尼邦·梅特尔(Anirban Maitra)博士乐意提供他空间做实验室,并在其开发这种新方式时给予指导。 得到帮助的安德雷卡终于开始创建他的新型测试。 矛头对准癌症早期阶段 杰克·安德雷卡的测试法看起来简捷明了:主要利用了一张不起眼的普通滤纸,但他将人体的间皮素特异性抗体与单壁碳纳米管混合物质涂敷于其上。碳纳米管就像一种筒壁只有单个原子薄厚的空心圆筒,其会使纸具有导电性。而当抗体与目标蛋白质相遇时,会粘附于这种生物标物上并扩大,将碳纳米管分隔开一点点,进而也显著改变了滤纸条的导电性。 碳纳米管之间的这种距离变化,通过电表能够检测到——实验中安德雷卡用的普通卖场里买到的标价50美元的电表。当目标蛋白质越多,抗体粘附的量也就越多从而变的更大,测量到的电信号就越弱——这使人们通过简单手段就能相当精确地测量到生物标志物水平。 这是简单有效且成本低廉的胰腺癌“测试纸”。安德雷卡表示,他的测试方法可以推广到糖尿病试纸上,医生们可以十分轻松将这种试纸插入糖尿病患者所使用的设备中——在这种新滤纸上滴一滴血,就可以确定患者是否携带间皮素生物标志物,结果几乎瞬间出来,成本仅3美分。这种小小的动态传感器已被证明,比现有检查手法速度快28倍,便宜28倍,且灵敏度至少超100倍。更重要的是,据《每日邮报》文章称,这种方式被认为准确率超过90%。 该检测手法的问世,意味着患者在胰腺癌扩散之前,就能被检测出来,患者能在可治疗阶段就得到医治。而安德雷卡称,有可能提高生存率“接近100%”。 你就是自己的医生 除了针对胰腺癌外,安德雷卡的简单测试手法也可以被用于检测卵巢癌和肺癌,甚至轻易的改变生物标志物,用来检测一系列其他病症,或是检测对抗生素的抵抗力、对正接受化疗或放疗患者的进展予以跟踪。 “事情就是这么酷,它可适用于测试其他疾病,例如其他形式的癌症、肺结核、艾滋病,以及像大肠杆菌、沙门氏菌等环境污染物。”安德雷卡表示,“以上种种,一次3美分,只用5分钟。” 在先前的科学大赛中,安德雷卡被认为拥有直截了当描述一种复杂实验的能力,且很善于让外行人了解他的工作和想法。现在,这位天才少年正计划将其研究推向大众,以让人们更广泛的受惠于全新测试方式——这项突破性的技术将有公司来制造传感器,预计3年到5年就可以提供给公众。安德雷卡相信,这可能会让医学界的平衡出现一点改变。 按照安德雷卡的基本构想,这种可以称之为“测试纸”、传感器或是手持式疾病扫描仪的小东西,人们在家附近能很方便的购买到。“沃尔格林(美国著名连锁药店)和凯马特(美国国内最大的打折零售)的货架上就能找到。”安德雷卡描述道,“打个比方,如果你对自己身体有所怀疑的话,那就买个这种测试。若是真有问题,马上就会看到结果。” “而你自己就是自己的医生。”安德雷卡说。 《科技日报》(2013-03-14 二版)
根据《中国环境科学学会标准管理办法(试行)》的有关规定,经自愿申报、形式审查、专家论证等程序,《绿色替代品评估技术指南》《有机污染物人体暴露生物标志物筛选技术规范》2项团体标准项目通过了论证,拟正式立项。现将拟立项团体标准名称、牵头单位予以公示。公示期为2023年7月10日至7月24日。如对公示项目存在异议,请在公示期内与我会联系。
[size=16px]Q-[/size][size=16px]Marker[font=微软雅黑]是存在于中药材、中药饮片、中药提取物、中成药中固有的或在加工过程中形成的与其功能属性密切相关的化学物质[/font],[font=微软雅黑]可用于建立中药产业链的全过程控制体系[/font],[font=微软雅黑]有利于汇总质量控制与溯源[/font],[font=微软雅黑]是反映中药安全性和有效性的标志物。可基于基源鉴别、物质分析和生物学评价等方法和技术来确定。肖伟等基于基源鉴别、物质分析和生物学评价等方法和技术[/font],[font=微软雅黑]解析中药多成分[/font]-[font=微软雅黑]多靶点[/font]-[font=微软雅黑]多途径作用特征[/font],[font=微软雅黑]形成中药成分群与靶点群多维关联网络化的效应物质总和[/font],[font=微软雅黑]即功效成分群[/font],[font=微软雅黑]将[/font]Q-Marker[font=微软雅黑]转化为中药复方制剂生产过程质量控制的标志物[/font],[font=微软雅黑]使中药复方制剂可控地转化至实际生产[/font],[font=微软雅黑]从多维度的体内外药效试验和临床研究中得到印证[/font],[font=微软雅黑]保障中药复方制剂质量均一性[/font],[font=微软雅黑]提升其有效性[/font],[font=微软雅黑]全面反应中药关键质量属性。此外[/font],BioMarker[font=微软雅黑]与[/font]Q-Marker[font=微软雅黑]关联研究更能体现中药有效性与安全性[/font],[font=微软雅黑]整合相关研究结果[/font],[font=微软雅黑]选取关键质量属性参数[/font],[font=微软雅黑]设计合成小分子探针[/font],[font=微软雅黑]深入药效成分与靶点互作研究[/font],[font=微软雅黑]从[/font]“[font=微软雅黑]药材[/font]-[font=微软雅黑]加工[/font]-[font=微软雅黑]制剂[/font]-[font=微软雅黑]体内[/font]”[font=微软雅黑]全过程进行溯源及产品稳定性研究[/font],[font=微软雅黑]可为复杂的质量研究提供科学有效的新方法。[/font][/size]
美国药典USP标志物质目录[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=70978]美国药典USP目录[/url],希望对大家有所帮助。
GS标志物质列表中将新增两种多环芳烃 来源:技术壁垒资源网 时间:2011-11-09近期,德国在对消费品安全要求进行审查后,建议在GS安全性认证(安全测试)控制列表中增加两种多环芳烃(PAHs)致癌物质。这将使 GS 标志列表管控的多环芳烃总数达到 18个。 自愿性的德国GS标志认证基于美国环境保护署提出的技术指标列表对适用产品中的多环芳烃加以管控。目前,这份列表包含的 16种多环芳烃被分类为致癌物质。不过,最近由欧洲食品安全局(EFSA)和德意志研究联合会(DFG)参议院委员会认定的两种剧毒多环芳烃却未被列入表内。这两种物质——苯并荧蒽,苯并苝,都被列为第二类致癌物质,并被列入REACH法规附录XVII(第50项)。因此,德国倡议进一步控制消费品中的多环芳烃。这两种物质的加入将确保欧盟列出的所有八个第二类高致癌多环芳烃可通过GS标志进行管控。 德国技术设备及消费品委员会(AtAV 委员会)建议,申请GS标志应基于以下更新物质列表。在测试范围更新之后,ZEK 01.2-08规定的分析过程将是应用于GS标志认证的测试方法。 经验交流中心(ZEK)第67次会议在德国德国技术设备及消费品委员会(ZEK-04-11 号文件)的建议下同意了此次列表的扩大。从现在起,经过六个月的过渡期后,新的物质列表将应用于 GS 标志认证。如有疑问,请致电PONY谱尼测试零七五五二六零五零九零九
GB 29690-2013 食品安全国家标准 动物性食品中尼卡巴嗪残留标志物残留量的测定 液相色谱-串联质谱法
GB 29707-2013 食品安全国家标准 牛奶中双甲脒残留标志物残留量的测定 气相色谱法
[align=center][font='宋体'][size=16px][b][/b][/size][/font][/align][align=center][b][font=宋体]现代分析技术在中药质量标志物中的应用研究进展[/font][/b][/align][b][font=宋体]摘要:[/font][/b][font=宋体]中药质量标志物(Q-marker)已广泛应用于中成药的质量评价与控制。近年来越来越多的研究使用不同种类的分析仪器,密切联系中药有效性-物质基础- Q-marker研究,建立了丰富的中成药系统质量控制方法,为探讨建立中药全过程质量控制及质量溯源体系奠定了基础。然而,近十几年来,中成药的质量控制缺乏统一标准,虽逐渐被行业内重视,但仍不能体现其本身特性,许多现有质量标准及规范缺乏科学性、有效性、溯源性,对中药产业的健康发展产生了很大的影响。Q-marker研究关键步骤最初由刘昌孝院士于2016年首次提出,其中提到中药质量标准研究需要结合多种现代分析技术的理念在行业内引起了强烈反响。对目前中药产品Q-marker的研究现状进行综述及分析,将中药Q-marker的研究思路与不同分析仪器的特点相结合,形成具有分析仪器特色的中药Q-marker质量控制新思路,旨在引发专家同行的思考与共鸣,推动中成药质量控制方法的发展与完善,保障中药产品行业的快速稳步发展。[/font][b][font=宋体]关键词:[/font][/b][font=宋体]质量标志物;含量测定;分析仪器;色谱法;光谱法;质谱法;核磁共振波谱[/font][b][font=宋体]中图分类号:[/font][/b][font=宋体]R288 [/font][b][font=宋体]文献标志码:[/font][/b][font=宋体]A[/font][align=center][b][font=宋体]Advances in Application of Modern AnalyticalTechniques in Quality Marker (Q-marker) of Traditional Chinese Medicine[/font][/b][/align][b][font=宋体]Abstract:[/font][/b][font=宋体] The quality marker (Q-marker) of Traditional Chinese Medicine(TCM) was the core concept of quality evaluation and control of TCM in recentyears. Different kinds of analytical instruments were used to closely link theresearch on the Q-marker of TCM in Effectiveness-Material Basis- Q-marker. Toestablish a systematic quality control method for TCM, and lay a foundation forexploring the whole process quality control and quality traceability system ofTCM. However, in recent decades, the quality control of TCM lacks unifiedstandards. Although it has gradually been paid attention to by the industry, itstill can not reflect its own characteristics, lacks of scientific, effectiveand rational, seriously affecting the healthy development of the industry of TCM.In 2016, academician Changxiao Liu first proposed the key steps for the studyof Q-marker of TCM, which mentioned that the concept of combining variousmodern analytical techniques to control the quality of TCM has aroused strongrepercussions in the industry. This paper summarized and analysed the currentsituation of quality standards of TCM, combined the research ideas of Q-markerof TCM with different characteristics of analytical instruments, and formed anew idea of quality control of Q-marker of TCM with the characteristics ofanalytical instruments, aiming at arousing the thinking and resonance ofexperts and colleagues, and promoting the quality control of TCM. Thedevelopment and perfection of the method can ensure the rapid and steadydevelopment of the TCM product industry.[/font][b][font=宋体]Key words:[/font][/b][font=宋体] Q-marker the determination of content analyticalinstruments Chromatography Spectrometry Mass Spectrometry Nuclear Magnetic ResonanceSpectroscopy[/font][font=宋体]中药质量标志物(Q-marker)是存在于中药材和中药产品中固有的或加工制备过程中形成的、与中药的功能属性密切相关的化学物质,作为反映中药安全性和有效性的标示性物质进行质量控制[sup][1][/sup]。在中药生产及检测过程中建立有效的Q-marker控制方法和评价体系,对实现中药标准化、现代化和国际化具有推动作用[sup][2][/sup]。近年来,伴随着多种现代分析仪器的检测手段的更新、灵敏度的提高和精密度的提升,以及计算机软件与化学计量学方法的相互结合,更多的先进技术和方法应用到Q-marker的制定标准中,以进一步改善中药生产及检测的质量标准,建立中药全程质量控制及质量溯源体系[sup][3-7][/sup]。例如,将液相色谱法-串联质谱法、分子生物学检测技术、高效液相色谱-[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]电感耦合等离子体质谱[/color][/url]法等用于Q-marker的质量控制研究[sup][8-12][/sup]。中药Q-marker已广泛应用与质量控制研究中,研究者建立了中药材DNA条形码分子鉴定法、色素测定法、中药中真菌毒素测定法、近红外分光光度法、基于基因芯片的药物评价技术等指导方法,为今后药品标准项目的增订、限度标准的确定以及引导和规范新药和已上市药物的质量研究和评价奠定基础[sup][13-18][/sup]。现就近年来现代分析技术在Q-marker中的应用做一综述。[/font][b][font=宋体]1[/font][font=宋体]色谱法[/font][/b][font=宋体][color=#2e3033]色谱法在现代分析研究中主要是将不同极性的物质分离后消除彼此的检测影响,它主要包括[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]、液相色谱、薄层色谱、超临界流体色谱等。色谱法凭借其对不同极性样品的分离能力,在中药Q-marker研究中主要是辨识不同化学物质,从其生源途径或特异性分析初步筛选出更具专属性的化学成分作为Q-marker。[/color][/font][font=宋体][color=#2e3033]1.1 [/color][/font][b][font=宋体][color=#2e3033]薄层色谱法(TLC)[/color][/font][/b][font=宋体][color=#2e3033]TLC[/color][/font][font=宋体][color=#2e3033]是将适宜的固定相(如硅胶)均匀涂布于玻璃板、塑料或铝基片上,经过点样操作将样品置于薄层板,利用展开剂的扩散,与分析物的对照物按相同的方法在同一块薄层板上所得的色谱图作对比,还可用薄层扫描仪进行扫描。TLC操作相对简便,同时具有分离和鉴定的功能,它既可以对已知成分进行定性、定量分析,也可对未知成分或复杂成分进行特征性鉴别分析,配合扫描技术、数码成像和数据处理,可形成综合分析能力较强的TLC轮廓谱[sup][19][/sup]。影响其测定结果的因素较多,如薄层板的质量,展开湿度、温度、点样与显色技术及显色灵敏度等。TLC已应用于中药Q-marker中黄酮、皂苷、生物碱和糖类等成分的分离鉴定。马柏林[sup][20][/sup]等采用微乳薄层色谱鉴别法检测中药材杜仲花、叶、皮和种子中的Q-marker槲皮素、杜仲黄酮A、杜仲黄酮 B。孙悦[sup][21][/sup]等采用微乳薄层色谱鉴别法检测中药制剂复方石韦胶囊中的Q-marker苦参碱和氧化苦参碱、黄芪甲苷。在TLC实际应用中,十二烷基硫酸钠-正丁醇-正庚烷(27[/color][/font][font=宋体][color=#2e3033]∶[/color][/font][font=宋体][color=#2e3033]63[/color][/font][font=宋体][color=#2e3033]∶[/color][/font][font=宋体][color=#2e3033]10[/color][/font][font=宋体][color=#2e3033]或 39[/color][/font][font=宋体][color=#2e3033]∶[/color][/font][font=宋体][color=#2e3033]52[/color][/font][font=宋体][color=#2e3033]∶[/color][/font][font=宋体][color=#2e3033]9[/color][/font][font=宋体][color=#2e3033])在微乳展开剂中所占的比例较高,可用于分离鉴定黄酮类、生物碱和蒽醌类成分等[sup][22][/sup]。[/color][/font][font=宋体][color=#2e3033]1.2 [/color][/font][b][font=宋体][color=#2e3033][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法(GC)[/color][/font][/b][font=宋体][color=#2e3033]GC[/color][/font][font=宋体][color=#2e3033]是以气体为流动相,具有分离效率高、样品用量少、分析速度快等特点。适用于分离、鉴别和定量测定样品中的挥发性成分。GC在中药Q-marker研究中多用于中药材挥发性成分(如芳香醇、柠檬烯、蒎烯、龙脑)的测定,也可以经过衍生化反应后生成生物碱、脂肪类、内酯类、酚类、糖类等用于分析中药的其他成分。GC已经成为分离分析中药中Q-marker的重要分析方法之一,它在中药Q-marker的定性鉴别、挥发油类分析及含量测定等分析中都有广泛的应用研究。GC指纹图谱可建立全面反映中药所含Q-marker的种类与数量,为辨识中药Q-marker起到了关键的作用。李红梅[sup][23][/sup]等采用GC结合火焰离子化检测器,以水蒸气和正己烷萃取藿香正气水,以正十七烷为参照物,标识了16个共有指纹峰,为辨识藿香正气水Q-marker 提供了可靠的定性依据。何小稳[sup][24][/sup]等采用顶空单滴微萃取技术结合GC分析测定了百草油中挥发性成分薄荷醇和水杨酸甲酯的含量,避免了复杂的样品前处理过程,为辨识百草油Q-marker提供含量测定的方法。吴和珍[sup][25][/sup]等利用GC分析测定片姜黄挥发油中44种成分并对其中的10种Q-marker进行GC定量分析,定量结果准确可靠,为片姜黄挥发油Q-marker的辨识研究提供参考。阎正[sup][26][/sup]等利用毛细管GC对中成药东乐膏进行了分析,其中东乐膏由大黄、乳香、没药、冰片等药材制成,研究建立了8个Q-marker特征指纹峰的东乐膏GC指纹图谱,并对东乐膏中的主要挥发性Q-marker冰片的含量进行了快速分离测定。张铁军[sup][27][/sup]等确定了延胡索的Q-marker为延胡索乙素、延胡索甲素、黄连碱、巴马汀、去氢延胡索甲素、D-四氢药根碱及原阿片碱,为延胡素质量控制研究提供科学依据。[/color][/font][font=宋体][color=#2e3033]1.3 [/color][/font][b][font=宋体][color=#2e3033]高效液相色谱法(HPLC)[/color][/font][/b][font=宋体][color=#2e3033]高效液相色谱法是基于经典液相色谱而发展起来的,其传质阻力较小,分离效率较高、分离速度较快,且具强检测灵敏度,现已成为中药Q-marker研究中的重要手段之一,对于保证药物质量控制效果具有非常重要的作用。其基本操作方法是用具有一定极性的单一溶液或是不同比例的混合溶剂作为流动相,利用高压色谱泵将其注入填充有特定填料的色谱柱中,依靠流动相将所注入的试样带入柱内后进行分离,由色谱柱分离后的成分随流动相依次进入检测器,得到检测结果[sup][28][/sup]。张琦[sup][29][/sup]等利用超高效液相色谱系统建立了白芍药材的特征指纹图谱,在短短9 min快速标定了15个共有峰,并对其中5个Q-marker进行定性定量研究,完善了白芍药材的质量控制方法。巩丹丹[sup][30][/sup]等建立大黄、黄芩和黄连的HPLC组方指纹图谱,确定其融合模型,观察组方融合指纹图谱与一清片复方样品指纹图谱的一致性,从而以组方融合指纹图谱代替复方整体来智能预测复方制剂质量。卢建秋[sup][31][/sup]等采用HPLC法同时测定藿香正气水中甘草和陈皮的Q-marker甘草苷、橙皮苷的含量,采用HPLC法在段时间内同时测定了藿香正气水中厚朴的Q-marker厚朴酚与和厚朴酚、白芷的Q-marker欧前胡素和异欧前胡素、甘草的Q-marker甘草酸的含量。刘昌孝[sup][32][/sup]等将丹参素、丹酚酸B、丹参酮[/color][/font][font=宋体][color=#2e3033]Ⅱ[/color][/font][font=宋体][color=#2e3033]A[/color][/font][font=宋体][color=#2e3033]等9个化学成分确定为复方丹参片用于定性鉴别的Q-marker。并对复方丹参片提出建议,如果要对复方丹参片的有效成分进行质量控制,可以采用HPLC或[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]方法测定丹参素、丹酚酸B和丹参酮[/color][/font][font=宋体][color=#2e3033]Ⅱ[/color][/font][font=宋体][color=#2e3033]A[/color][/font][font=宋体][color=#2e3033]和三七皂苷R[sub]1[/sub]的量,为复方丹参片的质量控制提供科学依据。[/color][/font][font=宋体][color=#2e3033]1.4 [/color][/font][b][font=宋体][color=#2e3033]超临界流体色谱(SFC)[/color][/font][/b][font=宋体][color=#2e3033]SFC[/color][/font][font=宋体][color=#2e3033]是一种分离原理近似于正相色谱的分析技术,以超临界流体二氧化碳作为流动相对分析物产生分离作用。它是一种先进的分析技术,具有分析时间短、灵敏度高、绿色环保等优点。SFC为手性药物拆分提供了一种简便、快速、环保的新方法,可作为液相色谱或[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]的一种补充。SFC采用无毒、低成本的二氧化碳作为主要的流动相,可节省大量有机试剂,具有分析速度快、分离效果好等特点。对于成分比较复杂的中药而言,利用SFC能够快速分离中药中的多种成分,产生的废液少,相对环保,节约成本,并且能获得准确的结果。肖梦琦[sup][33][/sup]等利用SFC对人参与三七中的多种皂苷成分进行了分离测定,包括人参皂苷Rg[sub]1[/sub]、人参皂苷Re、人参皂苷Rb[sub]1[/sub]与三七皂苷R[sub]1[/sub]等Q-marker,为人参和三七的质量控制提供方法。杨杰[sup][34, 35][/sup]等利用SFC从中药淫羊藿中分离制备了12个结构相近(苷元相同,糖链不同;糖链相同,苷元不同;苷元相同,仅糖链中糖的连接位置不同的同分异构体)的黄酮单体化合物,鉴定其为淫羊藿的Q-marker,并对其进行了定性和定量分析。[/color][/font][b][font=宋体]2 [/font][font=宋体]光谱法[/font][/b][font=宋体]光谱法是根据物质的光谱强度来确定其相对含量的方法,它主要包括紫外光谱法、红外光谱法、拉曼光谱法、[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]法等。近年来光谱技术迅速发展,在多组分混合物分析中可以达到更高的分辨率,越来越多地被应用于农产品、食品和药品等领域的质量控制分析。大多数光谱法都能实现对中药样本的直接分析,无需额外分离提取,不仅对环境友好,而且降低了有机溶剂对中药有效成分产生不良影响的可能性。另外,因为效率高且仪器操作难度较低,还可实现在线监测。光谱法可根据确定的 Q-marker 来定性和定量,定性鉴别推荐采用传统方法与 DNA 条形码,定量可以采用一测多评的方法以及指纹图谱,从整体上对产品质量进行把控。[/font][font=宋体]2.1 [/font][b][font=宋体]紫外光谱法(ultraviolet[/font][font=宋体]spectrometry[/font][font=宋体],UV)[/font][/b][font=宋体]UV[/font][font=宋体]是分子最外层的价电子在不同能级轨道上跃迁而产生的,是一种常见的光谱分析方法。UV具有原理简单、操作方便、使用面广、灵敏度高、准确度高等特点。目前,UV较多的应用于中药Q-marker定性分析方面,对于外形相近的中药材,其可迅速进行真伪鉴别;对于不同产地的中药材,亦可迅速进行产地鉴别。另外,UV也广泛应用于中药Q-marker的质量控制方面,其可迅速测定中药有效成分的含量近年来,随着复方中药的研究为人们所关注,国内外对中药复方Q-marker的研究越来越多,UV也因其快速分析鉴定的优势得到广泛地应用。谭梅英[sup][36][/sup]等利用UV结合聚类分析方法,采集了5种叶类中药的UV图谱,并对图谱做一阶导数光谱处理,得到的指纹图谱进行聚类分析,准确地将布渣叶和其他四种叶类中药鉴别出来,并且反映了各样品之间的亲疏远近关系。邢丽红[sup][37][/sup]等以HPLC法为一级数据,测定金银花提取物中绿原酸、咖啡酸等5种Q-marker的含量,并采集UV光谱,分别建立了样品紫外吸收光谱与上述5种有机酸含量之间的校正模型,考察了各模型的预测能力。结果表明预测结果准确,紫外光谱法可快速测定金银花中有机酸的含量。Huang[sup][38][/sup]等建立了一种测定丹参和冠心宁注射液中单宁含量的方法,采用化学计量学方法对采集到的样品UV图谱构建偏最小二乘回归数学模型,相关系数r为0.952,模型表现良好,为中药注射剂中Q-marker的质量控制提供了技术支持。张铁军[sup][39][/sup]等通过性-效-物三元关系和作用机制研究结合UV法确定元胡止痛滴丸的Q-Marker为胡索甲素、延胡索乙素、欧前胡素、原阿片碱和异欧前胡素。[/font][font=宋体]2.2 [/font][b][font=宋体][url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]法(near infraredspectroscopy,NIRS)[/font][/b][font=宋体]NIRS[/font][font=宋体]是介于可见光和中红外光之间的电磁波,将物质的[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]通过适当的化学计量学多元校正将其浓度或性质关联建立模型,对未知样品进行预测,在有机化合物的鉴定中应用广泛。NIRS 法具有简单快速、不损伤样品,可直接测定液、固和胶状样品,适合于生产过程中的在线监测分析。理论上,每种物质结构不同,都应该有其独特的[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url],然而中药化学成分复杂,采集到的[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]由多种复杂成分的吸收叠加构成。[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]结合化学计量学方法分析后,可将背景光谱扣除,经过光谱波段的选择和光谱预处理后,Q-marker的特征吸收就可以用来定性及定量分析。Zang[sup][40][/sup]等利用NIRS对地龙提取物中的Q-marker鸟苷和肌苷两种核苷酸建立定量分析模型,采用偏最小二乘法将地龙水提过程实现质量的快速分析。雷晓晴[sup][41][/sup]等利用NIRS采集丹参样品的光谱,结合偏最小二乘法,对Q-marker丹参素、原儿茶醛、咖啡酸等11种化合物进行定性、定量分析,实现了丹参中多种成分的快速无损检测,更好地控制了丹参药材和饮片的质量。[/font][font=宋体]2.3[/font][b][font=宋体][url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]法(atomicabsorption spectrum,AAS)[/font][/b][font=宋体]AAS[/font][font=宋体]是由待测元素灯发出的特征谱线通过供试品蒸气时,被蒸气中待测元素的基态原子所吸收,吸收遵循一般分光光度法的吸收定律,通过测定辐射光强度减弱的程度可求出待测元素的含量[sup][42][/sup]。其主要用于中药材中微量元素的测定、杂质的测定以及制剂分析。崔朋雷[sup][42][/sup]等利用AAS对黄芪、甘草、合欢花3种治疗心血管疾病的中药测定其微量元素的含量,采用优化后的硝酸:高氯酸=4:1混酸体系作为消化液,为中药中铁、锰、锌、铜等元素的含量测定提供方法。王庆富[sup][43][/sup]等利用AAS测定凤尾草、贯众、海金沙和蜈蚣草中钙、镁、铜、锌、铁等8种元素的含量,矿物质元素含量与生长环境及药材对元素的富集作用存在一定关系,部分元素含量与药材种类及区域不同具有显著性差异。[/font][b][font=宋体]3 [/font][font=宋体]质谱法(mass spectrum,MS)[/font][/b][font=宋体]MS[/font][font=宋体]分析原理主要包括飞行时间质谱法、三重四级杆质谱法等,通过测定样品得离子质量和强度,来分析化合物的化学成分和结构。在中药Q-marker研究中主要用于鉴定和测定中草药及植物的化学成分的化学结构和含量。色谱联用技术的出现加快中药研发的步伐,该技术具有所需样品量少、速度快等特点,且可得到更多信息,目前,在药物分析领域正处于快速发展阶段并广泛应用于中药微量Q-marker研究的色谱联用技术包括[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]/质谱联用(GC-MS)、液相色谱/质谱联用(LC/MS)、液相色谱/质谱/质谱联用(LC/MS/MS)、毛细管电泳/质谱联用(CE/MS)和电感耦合等离子体/质谱联用([url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]ICP-MS[/color][/url])等。现代质谱技术凭借其灵敏度高、检测高效快速、离子对特征性强等优点在中药Q-marker代谢及Q-marker药代动力学研究领域发挥着不可替代的作用。MS技术可以实现对初步筛选出的 Q-marker 进行深入的传统中医理论的药效、药性学物质基础研究以及药动学变化的研究,进一步验证其生物活性。[/font][font=宋体]3.1 [/font][b][font=宋体][url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]技术([url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url])[/font][/b][font=宋体][url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url][/font][font=宋体]为中药Q-marker及其代谢物的复杂体系的分离分析提供了有效手段。[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]能给出分析物的质谱图,提供分析物的结构信息,对鉴别非常有用;[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]能将一级质谱中飞出的离子,选择碰撞打碎成碎片离子,由二级质谱选择测定,增加了分析物的特征性,并提供了更多的化合物结构信息,检测灵敏度大大提高。Han[sup][44][/sup]等利用超高效液相色谱结合飞行时间质谱研究了龙胆Q-marker龙胆苦苷在人体尿液的15种代谢产物,其中包括Q-marker经过氧化、环化、葡醛酸结合和去糖基化反应等代谢转化,该研究为新药研发提供了科学依据。Li[sup][45][/sup]等利用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS建立了穿心莲在血浆中Q-marker穿心莲内酯琥珀酸盐的定量检测方法,并成功应用于人体药代动力学研究,大大提高了检测的灵敏度,提高了检测效率。Li[sup][46][/sup]等利用UHP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS对散结镇痛胶囊在血浆中10种Q-marker建立同时定量检测方法,成功应用于大鼠体内的药动学研究,该方法检测限低,灵敏度高,为散结镇痛胶囊的临床开发提供了科学依据。[/font][font=宋体]3.2 [/font][b][font=宋体][url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用[/color][/url]技术(GC-MS)[/font][/b][font=宋体]采用GC-MC法,利用不同组分的挥发性差异,经过[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱的分离,依据Q-marker的色谱保留时间,以及质谱的分子离子与特征碎片离子组成的断裂模式,结合标准样品裂解图,对Q-marker逐个作出定性鉴定与定量分析。郭丰[sup][47][/sup]等利用基于毛细管[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]质谱联用分析技术,对中药木瓜的挥发油成分进行分析,从69种挥发油中选取16种含量最高的挥发油为Q-marker,更加准确的确定木瓜挥发油的主要Q-marker,为阐明木瓜的中药功效起到了推进作用。李升[sup][48][/sup]等利用GC-MS法检测出丁香挥发油中4种成分,辨识出丁香挥发油的Q-marker是3-烯丙基-2-甲氧基苯酚,占总成分的69.77%。该研究为丁香挥发油质量控制提供参考。郑莹[sup][49][/sup]等利用GC-MS枳壳挥发油主要为萜类成分,是其发挥促胃肠动力作用的主要Q-marker,其中Q-marker柠檬烯的含量与枳壳的促胃肠动力作用呈一定的正相关性。该研究为揭示枳壳药材促胃肠动力物质基础和作用机制提供了可靠的科学依据。孙蓉[sup][50][/sup]等提出一种基于“效-毒”相互评价的Q-marker的辨析技术,研究认为对于有毒中药的Q-marker,应分别同时建立功效和毒性研究,还应考虑含量限度和“效-毒”平衡问题。[/font][b][font=宋体][color=#222222]4 [/color][/font][font=宋体][color=#222222]核磁共振法(NMR)[/color][/font][/b][font=宋体][color=#222222]NMR[/color][/font][font=宋体][color=#222222]是一种物理方法,它检测的是组成有机化合物分子的原子核的性质及其周围化学环境的相互作用。在适当的磁场条件下,样品能够吸收射频区的电磁辐射,所吸收的辐射频率取决于样品的特性,吸收与分子中的某一给定的原子核有关,吸收峰频率对吸收峰强度作图构成 NMR谱图[sup][51][/sup]。刘晓婷[sup][51][/sup]等将NMR与固相萃取前处理设备结合,成功测定中药板蓝根饮片中的Q-marker表告依春的含量,实际测得板蓝根饮片中Q-marker表告依春含量为0.19-1.26 mg/g,显示出固相萃取强大的富集作用,可以克服NMR在低含量复杂样品的定量分析难题。禹珊[sup][52][/sup]等选择中药虎杖和板蓝根为研究对象,用NMR同时测定虎杖中Q-marker白藜芦醇和虎杖苷两种药效成分的含量以及板蓝根中Q-marker表告依春的含量。样品预处理方法简便,可为中药虎杖和板蓝根的Q-marker研究提供科学依据。熊亮,彭成[sup][53][/sup]采用多种波谱学技术和化学方法,鉴定了赶黄草所有成分的结构,认定赶黄草酮B可作为赶黄草代表性的Q-Marker,益母草碱可作为益母草代表性的Q-Marker。杨静[sup][54][/sup]等利用NMR、MS和LC-UV综合分析得出,丹参素、原儿茶醛、丹酚酸B、丹酚酸A、原儿茶酸、迷迭香酸等成分是丹红注射液的质量标志物。[/color][/font][b][font=宋体]小节[/font][/b][font=宋体]综上所述,随着现代分析技术的发展,检测手段的科学性、准确性与灵敏度不断提高,中药Q-marker质量控制标准会越来越完善。研究中药Q-marker必须立足于中药特色,密切联系中药有效性-物质基础-质量控制标志性成分研究,建立中药全程质量控制及质量溯源体系,只有这样,所建立的质量控制体系才能真正达到控制中药质量,保证中药用药安全、有效的目的。[/font][b][font=宋体] [/font][font=宋体] [/font][font=宋体] [/font][font=宋体] [/font][font=宋体] [/font][font=宋体] [/font][font=宋体]参考文献[/font][/b][font=宋体][1][/font][font=宋体]刘昌孝,陈士林,肖小河,等. 中药质量标志物(Q-Marker):中药产品质量控制的新概念[J]. 中草药, 2016, 47(09): 1443.[/font][font=宋体][2][/font][font=宋体]南洋,徐鹏,丁宏,等. 现代分析技术在中药质量评价中的应用[J]. 环球中医药, 2015, 8(11): 1421.[/font][font=宋体][3][/font][font=宋体]郝敏,陆兔林,毛春琴,等. 基于中药质量标志物的饮片质量控制研究[J]. 中草药, 2017, 48(09): 1699.[/font][font=宋体][4][/font][font=宋体]李振皓. 质谱及微流控芯片分析技术在中药质量评价中的应用研究[D]. 浙江大学, 2017.[/font][font=宋体][5][/font][font=宋体]马艳芹,张蓉蓉,房吉祥,等. 现代分析技术在中药质量控制中的应用进展[J]. 首都医药, 2013, 20(16): 14.[/font][font=宋体][6][/font][font=宋体]安卓玲. 中药质量标准与现代分析技术在中药指纹图谱中的应用[J]. 黑龙江医药, 2007(01): 45.[/font][font=宋体][7][/font][font=宋体]刘嘉. 基于离散小波变换的FTIR分析在中药材槐花等真伪鉴别中的应用研究[D]. 浙江师范大学, 2011.[/font][font=宋体][8][/font][font=宋体]王少敏,黄晓静,毛丹,等. QuEChERS-超高效液相色谱串联质谱法同时测定中药瓜蒌皮中22种真菌毒素[J]. 食品安全质量检测学报, 2018, 9(22): 5843.[/font][font=宋体][9][/font][font=宋体]秦艳,尹建兵,杜冬生,等. 中药紫花地丁黄酮碳苷类化学成分的超高效液相色谱-电喷雾离子源-四极杆飞行时间串联质谱研究[J]. 分析测试学报, 2017, 36(01): 9.[/font][font=宋体][10][/font][font=宋体]陈燕银. 现代分子生物学技术在食品和药品微生物检测中的应用[J]. 食品安全导刊, 2016(15): 87.[/font][font=宋体][11][/font][font=宋体]谷善勇,骆骄阳,刘好,等. 高效液相色谱-[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]电感耦合等离子体质谱[/color][/url]法检测17种大宗常用中草药中砷元素形态[J]. 中国中药杂志, 2019, 44(14): 3078.[/font][font=宋体][12][/font][font=宋体]李邦进. 高效液相色谱-[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]电感耦合等离子体质谱[/color][/url]检测中药中的五种砷形态[J].福建分析测试, 2018, 27(03): 20.[/font][font=宋体][13][/font][font=宋体]陈士林,姚辉,韩建萍,等. 中药材DNA条形码分子鉴定指导原则[J]. 中国中药杂志, 2013, 38(02): 141.[/font][font=宋体][14][/font][font=宋体]胡青,孙健,于泓,等. 快速液相-四级杆串联高分辨飞行时间质谱定性测定中药中50种染色色素[J]. 中国药学杂志, 2016, 51(15): 1316.[/font][font=宋体][15][/font][font=宋体]刘晨昕,冯俭. 红外分光光度法在中药药材真伪鉴定中的应用及前景概述[J].内蒙古中医药, 2012, 31(08): 89.[/font][font=宋体][16][/font][font=宋体]吴铮. 基因芯片技术临床应用于脊柱结核耐药检测的可行性研究[D]. 第三军医大学, 2010.[/font][font=宋体][17][/font][font=宋体]郝敏,陆兔林,毛春琴,等. 基于中药质量标志物的饮片质量控制研究[J]. 中草药, 2017, 48(09): 1699.[/font][font=宋体][18][/font][font=宋体]张宁. 基于中药质量标志物的杏贝止咳颗粒质量标准提升研究[D]. 南京中医药大学, 2019.[/font][font=宋体][19]Peiliang Zhang,Lei Zhang,Jiyao Shi,Na Zhang,Yue Li,TaoWu,Zhihong Cheng. TLC-electrostatic field induced spray ionization-MS analysisof diverse structural skeletons and its coupling with TLC bioautography forcharacterization of lipase inhibitory components in American ginseng[J].Journal of Pharmaceutical and Biomedical Analysis,2019,174.[/font][font=宋体][20][/font][font=宋体]马柏林,梁淑芳,董娟娥,等. 杜仲黄酮的微乳薄层色谱分离鉴定研究[J]. 西北林学院学报, 2001(02): 72.[/font][font=宋体][21][/font][font=宋体]孙悦,叶建成,梁生旺,等. 微乳液在苦参及其中成药薄层色谱分析中的应用研究[J]. 时珍国医国药, 2008(08): 2018.[/font][font=宋体][22][/font][font=宋体]房德敏,高颖,严震,等. 微乳薄层色谱在中药成分分析中的应用[J]. 中草药, 2011, 42(09): 1852.[/font][font=宋体][23][/font][font=宋体]李红梅,茹鑫,梁悦,等. 藿香正气水[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]指纹图谱特性研究[J]. 中成药, 2010, 32(01): 6.[/font][font=宋体][24][/font][font=宋体]何小稳,蒋晔,雷利利. 顶空单滴微萃取-[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法快速分析百草油中挥发性成分[J]. 中国中药杂志, 2010, 35(20): 2718.[/font][font=宋体][25][/font][font=宋体]洪宗超,吴和珍,杨艳芳,等. 基于GC-MS及GC技术对片姜黄挥发油成分的定性定量分析[J]. 中南药学, 2019, 17(03): 426.[/font][font=宋体][26][/font][font=宋体]阎正,韩媛媛,张亚莉,等. 东乐膏GC指纹图谱研究[J]. 中成药,2004(12): 3.[/font][font=宋体][27][/font][font=宋体]张铁军,许浚,韩彦琪,等. 中药质量标志物(Q-marker)研究:延胡索质量评价及质量标准研究[J]. 中草药, 2016, 47(09): 1458.[/font][font=宋体][28][/font][font=宋体]曾凡明. 高效液相色谱法在药品检验中的应用思考[J]. 山东化工, 2015, 44(02): 78.[/font][font=宋体][29][/font][font=宋体]张琦,王振中,萧伟,等. 白芍药材UPLC特征指纹图谱研究[J]. 中国中药杂志, 2011, 36(06): 712.[/font][font=宋体][30][/font][font=宋体]巩丹丹,董嘉俊,孙国祥,等. 用高效液相色谱组方指纹图谱智能预测中药质量的新模式[J]. 色谱, 2017, 35(06): 643.[/font][font=宋体][color=#2e3033][31][/color][/font][font=宋体][color=#2e3033]卢建秋. 中药藿香正气水质量评价与药动学研究[D]. 北京中医药大学, 2007.[/color][/font][font=宋体][color=#2e3033][32][/color][/font][font=宋体][color=#2e3033]刘昌孝,陈士林,肖小河,等. 中药质量标志物(Q-Marker):中药产品质量控制的新概念[J]. 中草药, 2016, 09: 1443.[/color][/font][font=宋体][color=#2e3033][33][/color][/font][font=宋体][color=#2e3033]肖梦琦. 超临界流体色谱技术在药物分析中的应用[D]. 湖北中医药大学, 2019.[/color][/font][font=宋体][color=#2e3033][34][/color][/font][font=宋体][color=#2e3033]金灯萍,彭国平,陆晓峰. 填充柱超临界流体色谱在中药中的分析与制备应用[J]. 中医药学刊, 2006(03): 541.[/color][/font][font=宋体][color=#2e3033][35][/color][/font][font=宋体][color=#2e3033]杨杰. 超临界流体色谱在中药分析及分离中的应用[A].中国化学会.第21届全国色谱学术报告会及仪器展览会会议论文集[C].中国化学会:中国化学会, 2017:2.[/color][/font][font=宋体][color=#2e3033][36][/color][/font][font=宋体][color=#2e3033]容丽英,谭梅英,文小燕,等. 清热凉血标准汤剂质量标准研究[J]. 海峡药学, 2019, 31(04): 63.[/color][/font][font=宋体][color=#2e3033][37][/color][/font][font=宋体][color=#2e3033]邢丽红,李文龙,瞿海斌. 金银花提取物中5种有机酸含量测定的紫外光谱法[J]. 药物分析杂志, 2011, 31(03): 547.[/color][/font][font=宋体][color=#2e3033][38][/color][/font][font=宋体][color=#2e3033]Huang H, Lv Y, Sun X, et al.Rapid determination of tannin in Danshen and Guanxinning injections using UVspectrophotometry for quality control[J]. Journal of Innovative Optical HealthSciences, 2018, 11(06): 1850034.[/color][/font][font=宋体][color=#2e3033][39][/color][/font][font=宋体][color=#2e3033]张铁军,许浚,申秀萍,等. 基于中药质量标志物(Q-Marker)的元胡止痛滴丸的“性-效-物”三元关系和作用机制研究[J]. 中草药, 2016, 47(13): 2199.[/color][/font][font=宋体][40]L.L.Gao,et al. Rapid determination of lumbrokinase potency in the earthwormextract intermediate by near-infrared spectroscopy, Chemom. Intell. Lab. Syst.185 (2019) 59-64.[/font][font=宋体][41][/font][font=宋体]雷晓晴,李耿,王秀丽,等. 基于[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]法快速测定丹参中5种成分模型的建立[J]. 中草药, 2018, 49(11): 2653.[/font][font=宋体][42][/font][font=宋体]崔朋雷,刘海燕,张冬暖,等. [url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]法测定一些中药中的重要微量元素[J]. 广州化工, 2013, 41(08): 123.[/font][font=宋体][43][/font][font=宋体]王清富,余娇,秦然,阮尚全.[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]法测定几种蕨类中矿质元素含量[J].内江师范学院学报, 2010, 25(12): 65.[/font][font=宋体][44][/font][font=宋体]Han H,Xiong A Z, He C Y, et al. Combination of UHPLC/Q-TOF-MS, NMR spectroscopy, andECD calculation for screening and identification of reactive metabolites ofgentiopicroside in humans[J]. Analytical and bioanalytical chemistry, 2014,406(6): 1781-1793.[/font][font=宋体][45][/font][font=宋体]Li S,Yang D, Zhang M, et al. Determination of dehydroandrographolide succinate inhuman plasma by liquid chromatography tandem mass spectrometry (LC–MS/MS):Method development, validation and clinical pharmacokinetic study[J]. Journalof Chromatography B, 2010, 878(24): 2274-2279.[/font][font=宋体][46][/font][font=宋体]Li J, LiD, Pan Y, et al. Simultaneous determination of ten bioactive constituents ofSanjie Zhentong Capsule in rat plasma by ultra-high-performance liquidchromatography tandem mass spectrometry and its application to apharmacokinetic study[J]. Journal of Chromatography B, 2017, 1054: 20-26.[/font][font=宋体][47][/font][font=宋体]郭丰. 毛细管[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱分析中药木瓜挥发油成分[J]. 中国药物经济学, 2015, 10(04): 19.[/font][font=宋体][48][/font][font=宋体]李升,郭楚君,张燕,等. [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱技术分析中药丁香挥发油成分[J]. 黑龙江医药科学, 2016, 39(04): 8.[/font][font=宋体][49][/font][font=宋体]郑莹,王帅,孟宪生,等. 中药枳壳挥发油成分[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱联用分析和促进胃肠动力药效研究[J]. 时珍国医国药, 2015, 26(03): 516.[/font][font=宋体][50][/font][font=宋体]孙蓉,李晓宇,王亮,等. 基于“效-毒”相关的Q-marker合理辨识与科学控制[J].世界科学技术-中医药现代化, 2016, 18(08): 1224.[/font][font=宋体][51][/font][font=宋体]刘晓婷. 固相萃取—定量核磁共振波谱法测定中药板蓝根饮片中表告依春、乳增宁胶囊中淫羊蕾苷和双黄连胶囊中绿原酸的含量[D]. 上海应用技术大学, 2017.[/font][font=宋体][52][/font][font=宋体]禹珊. 定量核磁共振波谱法分析中药虎杖和板蓝根中的有效成分[D]. 上海应用技术学院, 2015.[/font][font=宋体][53][/font][font=宋体]熊亮,彭成. 基于中药质量标志物(Q-Marker)的基本条件研究益母草和赶黄草的Q-Marker[J]. 中草药, 2016, 47(13): 2212.[/font][font=宋体][54][/font][font=宋体]杨静,江振作,柴欣,等. 中药注射液“Q-Markers”的辨析研究——丹红注射液研究实例[J]. 世界科学技术-中医药现代化, 2016, 18(12): 2056.[/font][font='宋体'][size=16px][/size][/font]
GB 29707-2013 食品安全国家标准 牛奶中双甲脒残留标志物残留量的测定 气相色谱法
寻求:生物标志化合物分析测试方面的资料
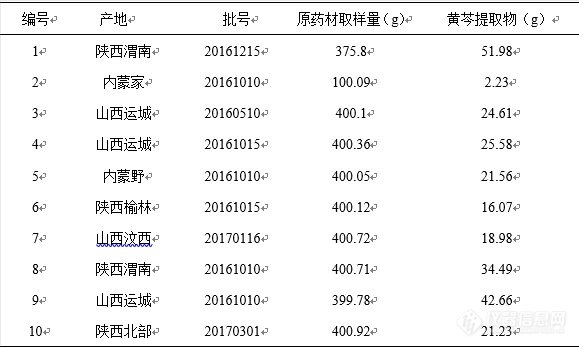
[b][/b][align=center][b]银黄颗粒质量标志物评价研究[/b][/align][b] 摘要[/b]目的:以黄芩药材、金银花药材、黄芩提取物、金银花提取物、银黄制剂为研究对象,考察并优化了样本在前处理环节的回流提取溶剂的体积、回流提取时间和提取溶剂的温度等。方法:采用高效液相色谱法,色谱柱为Venusil MP C[sub]18[/sub](4.6mm × 250 mm,5μm), Venusil MP C[sub]18[/sub](4.6mm × 250 mm,3μm)和 Agela MP S/N。以乙腈一0.3% 磷酸溶液为流动相进行梯度洗脱,流速为0.7 mLmin[sup]-1[/sup],检测波长为235 nm。结果和结论:通过各方面的考察,确定了银黄颗粒、黄芩药材和金银花药材在样品前处理环节的工艺优化参数,为银黄颗粒质量标志物研究提供借鉴指导。结论: 建立的提取方法稳定、可靠,有效成分达到最大提取效率,可用于银黄颗粒溯源检测的质量控制和综合评价。[b] 关键词:[/b]银黄颗粒;质量标志物;高效液相;黄芩;金银花[b] [/b][align=center][b][color=#333333]Evaluation of Quality Markers of Yinhuang Granules[/color][/b][/align]Objective: To investigate and optimize the volume ofreflux solvent, reflux extraction time and temperature of extraction solvent inthe pretreatment of samples, taking Scutellaria baicalensis, honeysuckle,Scutellaria baicalensis extract, honeysuckle extract and Yinhuang preparationas research objects. METHODS: High performance liquid chromatography was usedwith Venusil MP C18 (4.6 mm *250 mm, 5 micron), Venusil MP C18 (4.6 mm *250 mm,3 micron) and Agela MP S/N as chromatographic columns. The gradient elution was carried out with acetonitrile-0.3% phosphoric acid solution as mobile phase.The flow rate was 0.7 mL/min and the detection wavelength was 235nm. RESULTS AND CONCLUSION: The process optimization parameters of Yinhuanggranules, Radix Scutellariae baicalensis and Flos Lonicerae in samplepretreatment were determined through various aspects of investigation, whichcould provide reference and guidance for the study of quality markers ofYinhuang granules. CONCLUSION: The established extraction method is stable andreliable, and the effective ingredients can reach the maximum extractionefficiency. It can be used for quality control and comprehensive evaluation oftraceability detection of Yinhuang granules.Keywords: Yinhuang granules quality markers high performance liquidchromatography Scutellaria baicalensis honeysuckle[b]一、前言[/b] 银黄颗粒组方由金银花和黄芩构成,具有清热疏风、利咽解毒的功效,用于外感风热、肺胃热盛所致的咽干、咽痛、喉核肿大、口渴、发热急慢性扁桃体炎、急慢性咽炎、上呼吸道感染等症。该复方原料金银花为忍冬科植物忍冬的干燥花蕾或带初开的花,主产于山东、河南和河北等地。该复方原料黄芩为唇形科[url=https://baike.baidu.com/item/%E9%BB%84%E8%8A%A9%E5%B1%9E][color=windowtext]黄芩属[/color][/url]多年生草本植物,产于河北,河南,陕西,山西,山东等地。黄芩提取物的主要活性成分为黄芩苷、汉黄芩苷、黄芩素及汉黄芩素,金银花提取物是从金银花中提取的有机酸类活性成分。该制剂及其原料药成分复杂,生产厂家及产地众多,样品存在差异。中药质量标志物(Q-marker)已广泛应用于中成药的质量评价与控制。近年来越来越多的研究使用不同种类的分析仪器,密切联系中药有效性-物质基础- Q-marker研究,建立了丰富的中成药系统质量控制方法,为探讨建立中药全过程质量控制及质量溯源体系奠定了基础。[b]二、材料与方法1仪器与试剂、试药1.1仪器[/b] Waters e2695高效液相色谱仪(美国Waters公司),Waters 2998紫外检测器(美国Waters公司),Waters Empower色谱工作站(美国Waters公司);AGBP210S电子天平(Sartorius公司);MILLIPORE纯水机(MILLIPORE公司);高速万能粉碎机(北京市永光明医疗仪器有限公司,FW-80型);SB4200DTS超声波双频清洗机(宁波新芝生物科技股份有限公司);KDM-A控温电热套(金坛市医疗仪器厂);Venusil MP C[sub]18[/sub](4.6 mm × 250 mm,5 μm)和Venusil MP C[sub]18[/sub](4.6 mm × 250 mm,3 μm)。[b]1.2 试剂与试药[/b] 乙腈(上海星可高纯溶剂有限公司,色谱纯);甲醇(天津市科密欧化学试剂有限公司,色谱纯);其余试剂均为分析纯,水为超纯水。对照品来源:葛根素(批号:110752-200912)购自中国食品药品检定研究院。2样品的收集与前处理[b]2.1样品的收集[/b] 本研究从全国范围内收集黄芩、金银花药材各50批,分别制备相应的黄芩提取物和金银花提取物各50批,并制备银黄颗粒样品至少50批。(共计不少于250批样品)。[b]2.2黄芩、金银花药材的处理[/b] 对收集到的各批样品,均按照《中国药典》2015年版(第四部)药材取样法,四分法取样,1/4留样,剩余药材粉碎,使粉末分别过60目和20目筛,并按比例称重。所有黄芩、金银花药材样品均装袋密封,保存于冰柜(-20℃)中,备用。[b]2.3黄芩提取物的制备[/b] 取黄芩约100 g,置于1000 ml容量瓶中,加热回流两次,每次2 h,将滤液置于烧杯中浓缩至200 ml,用2 mol/L的盐酸调PH至1.0-2.0,80 ℃保温1 h,静置24 h.减压抽滤,沉淀加一倍量水混匀,用40 %氢氧化钠调节PH至7.0,加等量乙醇,搅拌溶解,滤过,滤液用2 mol/L的盐酸调PH 1.0-2.0, 60 ℃保温1 h,静置24 h,滤过,沉淀物加水洗至PH 5.0,95%乙醇洗至中性,挥尽乙醇,干燥,即得。[align=center]表1 黄芩提取物的提取[/align][align=center][img=,579,348]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091021374879_6392_3255306_3.png!w579x348.jpg[/img][/align][b]2.4金银花提取物的制备[/b] 称取金银花50.05 g置于圆底烧瓶中,加纯水回流提取三次,第一次8倍量水400 ml回流提取1 h,滤过,残渣加8 倍量水400 ml二次回流提取1 h,滤过,合并煎液,残渣加6倍量水300 ml,合并煎液,浓缩成浸膏,加浸膏量50%的淀粉混匀,置于烘箱中,60 ℃干燥,粉碎成粉,即得。[align=center]表2 金银花提取物的提取[/align][align=center] [img=,552,347]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091021550706_5584_3255306_3.png!w552x347.jpg[/img][/align][b]3供试品溶液方法考察的制备3.1供试品溶液制备方法考察3.1.1提取溶剂的选择[/b] 根据银黄颗粒的服用说明,该样品采用水为溶媒制备供试品溶液,由于临床应用中黄芩,金银花多采用水煎内服的用法,因此研究中以水作为提取溶媒,制备样品溶液。[b]3.1.2内标物溶液的制备[/b] 经查阅大量文献,本实验适用的内标物为葛根素。取葛根素对照品适量精密称定,以水超声溶解并定容制成浓度为30 μg*mL[sup]-1[/sup]的内标溶液[b]3.2银黄颗粒供试液制备方法考察3.2.1银黄颗粒不同料液比的考察[/b] 银黄颗粒研细后精密称取细粉1.0 g,称四份,置于100 ml或250 ml的圆底烧瓶中,分别精密加入煮沸的蒸馏水25 ml、50 ml、100 ml、150 ml于圆底烧瓶中,称重,加热回流30 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后0.5 ml等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表3、图1。[align=center]表3 银黄颗粒不同料液比单位质量色谱峰面积比较[/align][align=center] [img=,289,425]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091023281381_1955_3255306_3.png!w289x425.jpg[/img][/align][align=center]图1 银黄颗粒不同料液比单位质量色谱峰面积比较[/align][align=center][img=,289,123]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091023402582_6283_3255306_3.png!w289x123.jpg[/img][/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取体积为100 ml时值最大,最终选择回流提取体积为100 ml。[b]3.2.2银黄颗粒不同提取时间的考察[/b] 银黄颗粒研细后精密称取细粉1.0 g,称四份分别置于100 ml 的圆底烧瓶中,精密加入煮沸的蒸馏水25 ml于圆底烧瓶中,称重,分别加热回流20 min、30 min、40 min、60 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后0.5 ml等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表4、图2。[align=center]表4 银黄颗粒不同提取时间单位质量色谱峰面积比较[/align][align=center] [img=,292,421]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091024007921_8570_3255306_3.png!w292x421.jpg[/img][/align][align=center][img=,577,251]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091024513811_6890_3255306_3.png!w577x251.jpg[/img][/align][align=center]图2 银黄颗粒不同提取时间单位质量色谱峰面积比较[/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取时间为30 min时值最大,最终选择回流提取时间为30 min。[b]3.2.3银黄颗粒冷热水的考察[/b] 银黄颗粒研细后精密称取细粉1.0 g,称两份分别置于250 ml的圆底烧瓶中,第一份精密加入煮沸的蒸馏水100 ml于圆底烧瓶中,第二份精密加入100 ml常温蒸馏水,称重,加热回流30 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表5、图3。[align=center]表5 银黄颗粒冷热水单位质量色谱峰面积比较[/align][align=center][img=,287,427]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091025490101_4911_3255306_3.png!w287x427.jpg[/img][/align][align=center][img=,574,270]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091026003331_9248_3255306_3.png!w574x270.jpg[/img][/align][align=center]图3 银黄颗粒冷热水单位质量色谱峰面积比较[/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取溶剂为热水时值最大,最终选择提取溶剂为热水。[b]3.3黄芩药材供试液制备方法考察 3.3.1黄芩药材不同料液比的考察[/b] 按比例称取2 0~60目和过60目筛的黄芩药材粉末,共0.57 g,称取三份,置于100 ml或250 ml的圆底烧瓶中,分别精密加入煮沸的蒸馏水25 ml、50 ml、100 ml于圆底烧瓶中,称重,加热回流30 min ,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表6、图4。[align=center]表6 黄芩药材不同料液比单位质量色谱峰面积比较[/align][align=center][img=,291,425]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091026251557_1424_3255306_3.png!w291x425.jpg[/img][/align][align=center][img=,567,260]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091026352391_8450_3255306_3.png!w567x260.jpg[/img][/align][align=center]图4 黄芩药材不同料液比单位质量色谱峰面积比较[/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取体积为50ml时值最大,最终选择50ml为最佳提取容积。[b]3.3.2黄芩药材不同提取时间的考察[/b] 按比例称取2 0~60目和过60目筛的黄芩药材粉末,共0.57 g,称取四份,分别置于100 ml 的圆底烧瓶中,精密加入煮沸的蒸馏水25 ml于圆底烧瓶中,称重,分别加热回流20 min、30 min、40 min、60 min ,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表7、图5。[align=center]表7 黄芩药材不同提取时间单位质量色谱峰面积比较[/align][align=center][img=,289,424]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091027053867_9448_3255306_3.png!w289x424.jpg[/img][/align][align=center][img=,605,240]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091027125561_9333_3255306_3.png!w605x240.jpg[/img][/align][align=center]图5 黄芩药材不同提取时间单位质量色谱峰面积比较[/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取时间为40 min时值最大,最终选择40 min为最佳提取时间。[b]3.3.3黄芩药材冷热水提取的考察[/b] 按比例称取2 0~60目和过60目筛的黄芩药材粉末,共0.57 g,称取二份,置于100 ml的圆底烧瓶中,第一份精密加入煮沸的蒸馏水50 ml于圆底烧瓶中,第二份精密加入50 ml常温蒸馏水,分别称重,加热回流40 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表8、图6.[align=center]表8 黄芩药材冷热水单位质量色谱峰面积比较[/align][align=center][img=,287,424]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091027401011_8981_3255306_3.png!w287x424.jpg[/img][/align][align=center][img=,619,293]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091027478961_1794_3255306_3.png!w619x293.jpg[/img][/align][align=center][/align][align=center]图6 黄芩药材冷热水单位质量色谱峰面积比较[/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取溶剂为热水时值最大,最终选择热水提取是最佳的。[b]3.4金银花药材供试液制备方法考察3.4.1金银花药材不同料液比的考察[/b] 按比例称取2 0~60目和过60目筛的金银花药材粉末,共0.5 g,称取三份,置于100 ml或250 ml的圆底烧瓶中,分别精密加入煮沸的蒸馏水50 ml、100 ml、200 ml于圆底烧瓶中,称重,加热回流30 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表9、图7。[align=center]表9 金银花药材不同料液比单位质量色谱峰面积比较[/align][align=center][img=,358,511]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091031346401_7706_3255306_3.png!w358x511.jpg[/img][/align][align=center][img=,636,256]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091031349941_1562_3255306_3.png!w636x256.jpg[/img][/align][align=center]图7 金银花药材不同料液比单位质量色谱峰面积比较[/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取容积为100 ml,200 ml时值较大,100 ml与200 ml比较,两者的成分含量差别不大,所以选择100 ml提取较好。[b]3.4.2金银花药材不同提取时间的考察[/b] 按比例称取2 0~60目和过60目筛的黄芩药材粉末,共0.5 g,称取四份,分别置于250 ml 的圆底烧瓶中,精密加入煮沸的蒸馏水100 ml于圆底烧瓶中,称重,分别加热回流20 min、30 min、40 min、60 min ,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表10、图8。[align=center]表10 金银花药材不同提取时间单位质量色谱峰面积比较[/align][align=center][img=,290,424]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091030005792_6136_3255306_3.png!w290x424.jpg[/img][/align][align=center][img=,555,215]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091030053727_8053_3255306_3.png!w555x215.jpg[/img][/align][align=center][/align][align=center]图 9 金银花药材冷热水提取单位质量色谱峰面积比较[/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取溶剂为热水时值最大,最终选择热水提取最佳。[b]3.5 黄芩提取物,金银花提取物供试液制备方法考察[/b] 通过实验得知黄芩提取物,金银花提取物供试液制备方法考察同银黄颗粒供试液制备方法考察一致。[b]3.6 含葛根素内标的银黄颗粒、黄芩药材、金银花药材、黄芩提取物、金银花提取物供试液配制方法的确定3.6.1含葛根素内标银黄颗粒供试品溶液的配制[/b] 银黄颗粒研细后精密称取细粉1.0 g,置于250 ml圆底烧瓶内,精密加入煮沸的蒸馏水100 ml,称重,加热回流30 min(提前打开电热套预热),放冷,补重,过滤,取续滤液。另取葛根素对照品适量精密称定,以水超声溶解并定容制成浓度为30μg• mL-1的内标溶液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液。[b]3.6.2含葛根素内标黄芩药材供试品溶液的配制[/b] 从冰柜中取出黄芩药材粉末,放置室温。采用四分法取样,按比例称取2 0~60目和过60目筛的黄芩药材粉末,共0.57 g,置于100 ml圆底烧瓶中,精密加入煮沸的蒸馏水50 ml,称重,加热回流40 min(提前打开电热套预热),放冷,补重,过滤,取续滤液。另取葛根素对照品适量精密称定,以水超声溶解并定容制成浓度为30 μg• mL-1的内标溶液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液。[b]3.6.3含葛根素内标金银花药材供试品溶液的配制[/b] 从冰柜中取出金银花药材粉末,放置室温。采用四分法取样,按比例称取2 0~60目和过60目筛的黄芩药材粉末,共0.25 g,置于100 ml圆底烧瓶中,精密加入煮沸的蒸馏水50 ml,称重,加热回流30 min(提前打开电热套预热),放冷,补重,过滤,取续滤液。另取葛根素对照品适量精密称定,以水超声溶解并定容制成浓度为30 μg• mL-1的内标溶液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液。[b]3.6.4含葛根素内标金银花提取物供试品溶液的配制[/b] 从冰柜中取出金银花提取物粉末,按比例精密称取0.2 g,置于250 ml圆底烧瓶中,精密加入煮沸的蒸馏水100 ml,称重,加热回流30min(提前打开电热套预热),放冷,补重,过滤,取续滤液。另取葛根素对照品适量精密称定,以水超声溶解并定容制成浓度为30 μg• mL-1的内标溶液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液。[b]3.6.5含葛根素内标黄芩提取物供试品溶液的配制[/b] 从冰柜中取出黄芩提取物粉末,按精密称取0.04 g,置于250 ml圆底烧瓶中,精密加入煮沸的蒸馏水100 ml,称重,加热回流30 min(提前打开电热套预热),放冷,补重,过滤,取续滤液。另取葛根素对照品适量精密称定,以水超声溶解并定容制成浓度为30 μg• mL-1的内标溶液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液。[b]三、结论[/b] 实验考察了银黄颗粒在样本处理环节的回流提取溶剂的体积、回流提取时间和提取溶剂的温度等。最终选择回流提取体积为100 ml,选择回流提取时间为30 min,选择提取溶剂为热水。考察了黄芩药材在样本处理环节的回流提取溶剂的体积、回流提取时间和提取溶剂的温度等。最终选择50ml为最佳提取容积,选择40 min为最佳提取时间,选择热水提取是最佳的。考察了金银花药材在样本处理环节的回流提取溶剂的体积、回流提取时间和提取溶剂的温度等。最终选择100 ml体积提取溶剂,选择30 min提取是最佳的,选择热水提取最佳。本实验还确定了含葛根素内标的银黄颗粒、黄芩药材、金银花药材、黄芩提取物、金银花提取物供试液配制方法。[align=left][b]参考文献[/b][/align] 王亚丹,杨建波,戴忠,等.中药金银花的研究进展.药物分析杂志,2014,34(11):1928-1935 中国药典.一部.2015:1498 王彩芳,张楠,黄龙,等. HPLC法测定不同厂家银黄颗粒中黄芩苷的含量.医药论坛杂志,2006,27(24):27-28 王彩芳,黄龙,程茜,等.高效液相色谱法测定不同厂家银黄颗粒中绿原酸的含量.时珍国医国药,2007,18(5):1143-1144黄雄,黄嬛,王峻,等.银黄颗粒的HPLC特征图谱分析.药物分析杂志,2009,29(8):1320-1323 肖小河,王永炎.从热力学角度审视和研究中医药.国际生物信息与中医药论丛.新加坡:新加坡医药卫生出版社,2004:74 贺福元,罗杰英,刘文龙,等.中药谱效学研究方向方法初探.世界科学技术-中医药现代化,2004,6(6):44-50 赵渤年,于宗渊,丁晓彦,等.黄芩质量评价谱-效相关模式的研究.中草药,2011.42(2):380-383 高燕,赵渤年,于宗渊等.金银花抗流感病毒毒谱-效相关质量评价模式的研究.中华中医药杂志,2013.28(12):3508-3511 Ke Li, Wei Cheng, Xiao-Jian Liu, hu-Bin Li, En-Guang Hou, Yan Gao, Liang Wang, Qing Liu, Bo-Nian Zhao, Zong-Yuan Yu, Mathematical Modelling for the Quality Evaluation of BaikalSkullcap Root, Applied Mechanics and Materials, 2011 王荣梅,徐丽华,林永强.HPLC法同时测定银黄含片中6个咖啡酰奎宁酸类成分的含量.药物分析杂志,2012,32(1):57-60 高苏亚,范涛,王黎等.红外光谱技术结合化学计量学方法在中药研究中的应用.应用化工,2012,41(2):324-328 王鹏,王振国,薛付忠等.基于支持向量机法的中药性状与药性相关性研究. 江西中医药,2012,43(355):65-68 Cifford MN, Johnston KL, Knight S et al. Hierarchical scheme for [url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url] identification ofchlorogenic acids.J Agric Food Chem,2003 51(10):2900-2910张倩,张加余,隋丞琳,等. HPLC-DAD-ESI-MS/MS研究金银花水提工艺中绿原酸类成分的变化规律.中国中药杂志,2012 37(23):3564-3567 沈红,段金廒,钱大玮,等.黄芩及复方野马追胶囊中黄酮类成分的[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS分析.药物分析杂志,2009 29(9):1425-1429 赵胜男,李守拙.黄芩药材中黄酮类成分的HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]研究.承德医学院学报2012 29(4):345-347 Chkoshi E, Nagashima T, Sato H, et al. Simple preparation ofbaicalin from Scutellariae Rdixi. JChromatogr A,2009 1216(11): 2192 -2194高燕,吕凌,王亮,等.银黄颗粒HPLC指纹图谱与模式识别分析.中华中医药杂志,2017,32(09):4238-4242 丁晓彦,刘青,李岩,等.丹参脂溶性成分的HPLC指纹图谱及模式识别研究.中华中医药杂志,2016,3(6):2254-2256
近期,德国在对消费品安全要求进行审查后,建议在GS(安全性认证(安全测试))控制列表中增加两种多环芳烃(PAH)致癌物。这将使GS 标志列表管控的多环芳烃总数达到18个。自愿性的德国GS标志认证基于美国环境保护署提出的技术指标列表对适用产品中的多环芳烃加以管控。目前,这份列表包含的 16种多环芳烃被分类为致癌物质。不过,最近由欧洲食品安全局(EFSA)和德意志研究联合会(DFG)参议院委员会认定的两种剧毒多环芳烃却未被列入表内。这两种物质——苯并荧蒽,苯并苝,都被列为第二类致癌物质,并被列入REACH法规附录XVII(第50项)。因此,德国倡议进一步控制消费品中的多环芳烃。这两种物质的加入将确保欧盟列出的所有八个第二类高致癌多环芳烃可通过GS标志进行管控。德国技术设备及消费品委员会(AtAV委员会)建议,申请GS标志应基于以下更新物质列表。在测试范围更新之后,ZEK 01.2-08规定的分析过程将是应用于GS标志认证的测试方法。经验交流中心(ZEK)第67次会议在德国德国技术设备及消费品委员会(ZEK-04-11号文件)的建议下同意了此次列表的扩大。从现在起,经过六个月的过渡期后,新的物质列表将应用于GS标志认证。
三物黄芩汤(Sanwu Huangqin Decoction,SHD)作为我国传统的经典方剂之一,首载于汉代张仲景所著《金匮要略》[1],由黄芩、苦参、地黄组成。方中黄芩清热,苦参燥湿祛风,地黄滋阴养血,3药配伍,祛风而不燥,滋阴而不腻。SHD主治产后血亏阴虚,风邪入里化热之证,从汉代发展至清朝,处方组成、用法和功能主治等关键信息大多沿用《金匮要略》,现代临床应用较为广泛,可用于妇科疾病、红斑性肢痛症、慢性肝病、大肠癌等疾病的治疗[2],具有广泛的开发前景,但目前尚未有成方制剂上市。SHD中所含化学成分众多,但对其药效物质基础和复方质量标准控制的研究仍存在不足。《中国药典》2020年版[3]只收录了SHD中单味药材的含量测定指标,并未收载其复方的质量标准,目前现有SHD的质量研究方法指标单一,未能全面控制其质量,因此对SHD的质量控制方法应进一步完善。 中药质量标志物(quality marker,Q-Marker)与其有效性密切相关,是反映中药质量的标示性物质[4]。本文拟对SHD的处方考证与历史沿革及其现代化学成分和药理作用研究进行整理与归纳,同时,依据Q-Marker“五原则”对其进行预测,为SHD的临床应用、制剂全过程中的质量溯源及其质量评价与控制体系的完善提供一定的参考。 1 SHD的处方考证与历史沿革 1.1 数据来源和结果 基于中医智库古籍库、中医古籍全文数据库《国医典藏》等网络数据平台,以“SHD”“四肢烦热”为关键词或内容含“黄芩、苦参、地黄”及其方剂和中药的异名、别名进行文献检索。同时查阅原版古籍进行补充和校对。共获取108条含SHD的有效数据,涉及中医古籍共42部(其中包含日本古籍10部)。按成书朝代来分,汉代1部、唐代1部、宋代4部、明代7部、清代29部。 1.2 处方来源及衍变 SHD首载于东汉《金匮要略》,文中记载到:“治妇人在草蓐自发露得风。四肢苦烦热,头痛者,与小柴胡汤;头不痛,但烦者,此汤主之”。原方组成及制法记载:黄芩一两、苦参二两、干地黄四两,上三味,以水八升,煮取二升,温服一升,多吐下虫。东晋《肘后备急方》[5]:“又方,苦参二两,黄芩二两,生地黄半斤,水八升,煮取一升,分再服,或吐下毒,则愈”,其方剂药味组成与SHD相同,但主治伤寒时气温病5~6日以上者。唐代《备急千金要方》[6]卷第三载道:“SHD,黄芩苦参各二两,干地黄四两,上?咀,以水八升煮取二升,去滓,适寒温服一升,日二,多吐下虫”,方中黄芩用量较《金匮要略》有所增加,并补充了药材的制法及服用方法,将3味药材切碎煎煮后去渣服用,每日2次。宋代《类证活人书》[7]卷十九产后药方载:“SHD,治妇人草蓐中伤风,上锉如麻豆大,每服四钱,水一盏半,煎八分,服之”。明清医家多依从仲景SHD的记载,沿用过程中出现了千金SHD、黄芩汤等异名。千金SHD首载于明代《普济方》[8],其处方组成、用法和主治较仲景方均未改变。黄芩汤首载于清代《孕育玄机》[9],所载方剂组成在《金匮要略》基础上增加当归、川芎和人参,原文载“黄芩汤治产后伤风,四肢苦烦热,头疼。黄芩半两苦参一两生地二两,加当归、川芎,虚加人参。”按照时间顺序对部分典型古籍整理如下,见表1。 整理分析不同朝代记载SHD的医籍,发现从汉代至清朝,SHD的药味组成、药物剂量与配伍比例、功能主治稍有变化。药味组成方面,其中28条(96.55%)同《金匮要略》SHD组成相同,即由黄芩、苦参、地黄3味药材组成,三者皆为生品。主要变化集中在地黄的记载上,21条(72.41%)记载依从《金匮要略》为干地黄,5条(17.24%)将干地黄记为生地黄,如《校注妇人良方》[11]、《孕育玄机》等,1条(3.45%)将干地黄记为生干地黄,如《妇人大全良方》[12],2条(6.90%)未载地黄的炮制种类,如《不居集》[13]、《兰台轨范》[14]。 药物剂量方面,分析3味药材剂量记载完全的29部医籍中SHD的剂量变化,从汉代至明清时期,SHD全方药量随朝代演变逐渐增加,3味药材配伍比例虽有所变化,但总体仍依从《金匮要略》所载配伍比例,即黄芩-苦参-地黄1∶2∶4,处方组成为黄芩13.8 g、苦参27.6 g、地黄55.2 g。唐《备急千金要方》由于黄芩用量增加1倍,导致全方药量增加,药材配伍比例变为1∶1∶2。至宋代,古籍记载方剂组成为黄芩20.0 g、苦参40.0 g、地黄80.0 g,3味药材用量都有所增加,但配伍比例仍遵从1∶2∶4。明清大部分古籍所载SHD剂量组成为黄芩37.3 g、苦参74.6 g、地黄149.2 g,少部分由于黄芩、苦参用量变化导致药材配伍比例改变,如明代《校注妇人良方》苦参用量减少一倍导致配伍比例变为1∶1∶4。进一步利用Cytoscape 3.9.1软件对SHD药材配伍比例进行可视化分析,以古籍-朝代-配伍比例为节点,以各节点度值进行排列,图标大小和颜色深浅表示该节点出现的频数大小,见图1。SHD的古籍主要集中于清代,3味药材配伍比例出现频数顺序依次为:25次(1∶2∶4)、3次(1∶1∶2)、1次(1∶1∶4)。 功能主治方面,29部医籍均遵从仲景方“治妇人在草蓐,自发露得风,四肢苦烦热,头不痛,但烦者”。从汉代至明朝,SHD功能主治未发生明显改变,仅在清朝其适用范围有所扩展,可用于手足心热、心胸烦闷及妇人血证头痛等。 剂型与制法方面,汉代《金匮要略》所载SHD为汤剂,原制法为“上三味,以水八升,煮取二升,温服一升”。唐宋时期,SHD的剂型类似为煮散剂,如唐代《备急千金要方》中“上?咀,以水八升煮取二升,去滓,适寒温服一升”,宋代《类证活人书》《增注伤寒类证活人书》[15]、《妇人良方大全》等要求将药材锉成麻豆大小,取4钱,用一盏半或一盏的水煎煮后温服。后世古籍多遵从《金匮要略》的制法,皆为汤剂,只是煮取水量有所差异。按《中国科学技术史度量衡卷》[16]换算SHD的推荐制法,以水1 600 mL煎煮黄芩13.8 g、苦参27.6 g、地黄55.2 g,煮取400 mL,温服200 mL。 通过对SHD的处方来源及其历史衍变进行考证,可知SHD首载于汉代《金匮要略》,由黄芩-苦参-地黄以1∶2∶4配伍组成,主要用于治疗妇人产后血虚风入而成热之证。后世医籍大多沿用仲景方中SHD的药味组成、配伍比例及剂型制法,但在处方用量和功能主治等稍有变化。其中,SHD中3味药材的用量和全方总剂量随着朝代更迭呈现由小到大的趋势,汉代全方总剂量为96.6 g(黄芩13.8 g、苦参27.6 g、地黄55.2 g),宋代全方总剂量为120.0 g(黄芩20.0 g、苦参40.0 g、地黄80.0 g),明清时期全方总剂量为261.1 g(黄芩37.3 g、苦参74.6 g、地黄149.2 g);功能主治方面,后世医籍基本依从仲景方的记载,清朝时期扩展治疗手足心热、血证头痛、疳劳等,推测可能与方剂剂量增加有关。 2 SHD的现代研究 2.1 主要化学成分 2.1.1 单味药材化学成分 现有研究表明,黄芩中化学成分包括黄酮及其苷类、挥发油类及多糖类等,其中,现已鉴定出的黄酮及其苷类成分共有150余种、挥发油类成分有60余种、多糖类成分有6种[17]。陈馨等[18]采用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]技术从黄芩水煎液中鉴定出黄芩苷、二氢黄芩苷、汉黄芩苷、5,7,2-三羟基黄酮、黄芩素、去甲汉黄芩素、汉黄芩素、千层纸素A等125种化合物。陈欣等[19]采用水蒸气蒸馏法结合[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用[/color][/url]技术从海南黄芩中鉴定出54种挥发油成分,包括石竹烯、邻苯二甲酸单乙基己基酯和4-乙烯基-2-甲氧基苯酚等。刘鹏等[20]等通过水提醇沉法提取黄芩多糖,发现其中第3组分的多糖峰值高,峰型好,由果糖、甘露糖、鼠李糖、葡萄糖醛酸、半乳糖、阿拉伯糖、岩藻糖组成。 苦参中的化学成分包括生物碱类、黄酮类、脂肪酸类等。目前,研究者已经从苦参根中共鉴定出约60种生物碱和超过130种黄酮类化合物[21-22]。张晓雪等[23]采用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]技术从5年生苦参根的甲醇提取物中鉴定出苦参碱、氧化苦参碱、槐定碱、槐果碱、金雀花碱、臭豆碱、羽扇豆碱等47种生物碱类成分,其骨架类型主要为苦参碱型和金雀花碱型生物碱。李国仙[24]通过多种分离材料和色谱技术纯化苦参根95%乙醇提取物,并运用质谱和核磁共振等多种波谱技术鉴定出苦参酮、降苦参酮、高丽槐素、三叶豆紫檀苷、槐黄醇、苦参啶、苦参醇S、苦参醇W等54种化合物。牛克彦等[25]采用[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用[/color][/url]技术分析苦参脂肪酸的组成,发现其亚麻酸、亚油酸、棕榈酸和油酸含量较高。 地黄的主要化学成分有环烯醚萜苷类、苯乙醇苷类、糖类等200余种,其中,环烯醚萜类86种、紫罗兰酮类32种、苯乙醇类31种和三萜类9种[26]。朱徐东等[27]采用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]技术从5种地黄炮制品中共鉴定出梓醇、地黄苷A、地黄苷C、地黄苷D、密力特苷、栀子苷、京尼平苷酸等34种化学成分。卢兴美等[28]发现地黄炮制前后差异性成分为地黄苦苷元、地黄苷、地黄新萜E、地黄新萜F、野菰酸、橙皮苷、柚皮苷等32种成分。薛淑娟等[29]采用高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-蒸发光检测器法对4种地黄炮制品中果糖、甘露糖、葡萄糖等8种单糖的含量进行测定。 综上,SHD中单味药材化学成分的研究主要侧重于含量较高、易分离鉴定的化合物,如黄酮及其苷类、生物碱类、环烯醚萜苷类及苯乙醇苷类等成分,对微量组分、维生素等其他类成分及金属元素的研究则较少。 2.1.2 复方化学成分 中药复方化学成分复杂,其药效物质基础是质量控制研究的关键。与单味药相比,对SHD复方分离、鉴定的研究较少。SHD主要含有黄酮类、生物碱类、环烯醚萜苷类及苯乙醇苷类化合物。Zhou等[30]采用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]技术从SHD水煎液中鉴定出黄芩苷、二氢黄芩苷、汉黄芩苷、黄芩素、氧化苦参碱、苦参碱、槐定碱、槐果碱、氧化槐果碱、地黄苷D、毛蕊花糖苷、异毛蕊花糖苷等30种化合物,其中15种源于黄芩,6种源于苦参,9种源于地黄。Zhang等[31]采用高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]同时测定了SHD中黄芩苷、黄芩素、汉黄芩素、氧化槐果碱、氧化苦参碱和苦参碱的含量。然而现有关于SHD复方化学成分的研究大多集中于其单味药材的有效成分,多数为黄酮类及生物碱类等小分子化合物,而对方中所含多糖类等大分子化合物的研究则较少。此外,SHD中3味药合煎后化学成分间的相互作用及是否会产生新的化合物类型等报道较为缺乏,其可能也是影响SHD质量的潜在因素之一。 2.2 药理作用 2.2.1 抗肿瘤 现代药理研究表明,SHD的抗肿瘤作用可能与恢复肠道菌群失调、抑制炎症因子表达等有关。张璐等[32]研究发现,与对照组相比,SHD给药治疗12周后,条件性基因敲除APCMin/+小鼠肠道腺瘤数量、大便形态和隐血等一般症状有显著改善,粪便样本微生物测序OTU数量增加,表明SHD可通过减少APCMin/+小鼠肠道肿瘤数量、改善肠道菌群结构及多样性发挥其抗肿瘤作用。Zhou等[30]通过研究SHD对氧化偶氮甲烷/葡聚糖硫酸钠诱导的结直肠癌小鼠模型的影响,发现其可通过恢复回肠上皮细胞闭锁小带蛋白-1、紧密连接蛋白-1表达,显著抑制脂多糖激活的Toll样受体4/核因子-κB(nuclear facto-κB,NF-κB)信号传导,降低模型小鼠结肠肿瘤数量和疾病活动指数,从而发挥其治疗结肠癌的作用。 2.2.2 抑菌 SHD及其部分活性成分如生物碱、黄酮对多种细菌和真菌都有较好的抑制作用。张蕾[33]研究发现黄芩、苦参中提取分离得到的大部分化合物对白色念珠菌具有显著的抑制作用,最小抑菌浓度(minimum inhibitory concentration,MIC)均<25.0 μg/mL,而对金黄色葡萄球菌、肺炎克雷伯菌、大肠杆菌作用则较弱。唐海燕[34]采用琼脂二倍稀释法探究SHD制备成的三物黄芩颗粒对80株临床分离的细菌和真菌的体外抑菌效果,发现三物黄芩颗粒对白念珠菌的抑制效果最好(MIC≤0.125 mg/mL),其次是溶血性链球菌(MIC≤7.8 mg/mL)、肺炎链球菌(MIC为7.8 mg/mL)。 2.2.3 抗病毒 SHD可通过抑制病毒复制、减轻炎症反应发生和增强免疫功能达到抗病毒的作用。药理学实验研究表明,SHD在体外能抑制甲型流感病毒H1N1型(H1N1)复制的不同阶段,在体内,SHD可通过下调流感病毒4种靶蛋白血凝素、神经氨酸酶、核蛋白和离子通道蛋白的表达,从而改善H1N1病毒感染小鼠的临床症状[35]。另有研究表明,SHD可通过调控NF-κB通路中p65、磷酸化-p65、NF-κB激酶α/β、NF-κB抑制蛋白α(NF-κB inhibitor α,IκBα)和磷酸化-IκBα等蛋白的表达水平,降低血清、肺组织中白细胞介素-6(interleukin-6,IL-6)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、IL-1β和γ干扰素等炎症因子的含量,促进T、B淋巴细胞增殖和巨噬细胞吞噬、增强自然杀伤细胞的活性,从而减轻H1N1病毒小鼠的炎症反应和免疫功能紊乱[36]。 2.2.4 抗过敏 SHD可有效对抗I、IV型变态反应,具有一定的抗过敏作用。SHD能降低湿热证I型变态反应大鼠模型中血清总免疫球蛋白E(immunoglobulin E,IgE)水平,减轻胃肠道细胞充血、炎性细胞浸润和肝脏细胞病变[37]。朱晓燕[38]运用3种动物模型对三物黄芩颗粒治疗急性湿疹的抗过敏机制进行研究,采用大鼠被动皮肤过敏法建立I型变态反应动物模型,通过蓝斑直径的大小判断过敏反应的程度,结果显示三物黄芩颗粒3.35、6.70、13.40 g/kg可显著抑制卵白蛋白诱发的I型变态反应大鼠颅骨肥大细胞脱颗粒;三物黄芩颗粒6.70、13.40 g/kg可显著减少I型变态反应大鼠背部皮肤蓝色反应斑直径及小鼠耳肿胀;三物黄芩颗粒13.40 g/kg可显著降低致敏大鼠血清中总IgE含量并显著提高豚鼠致痒阈。 2.2.5 抗白塞病 白塞病是一种全身性免疫系统疾病,主要表现为反复口腔和会阴部溃疡、下肢结节红斑、眼部虹膜炎等[39]。现代药理研究表明,SHD可通过降低炎症因子水平、调节通路蛋白表达,从而改善白塞病的症状。朴勇洙等[40]采用虾原肌球蛋白构建白塞病小鼠模型,发现SHD可通过靶向脾脏组织中T盒转录因子21 mRNA的表达,抑制γ干扰素、IL-17炎症因子水平,达到治疗白塞病的作用。朱彬[41]研究发现SHD可显著降低白塞病小鼠疾病症状积分和血清中IL-17及TNF-α水平。此外,SHD还可显著降低白塞病小鼠外周血中炎症因子γ干扰素水平及磷酸化信号转导和转录激活因子3蛋白的表达[42]。网络药理学和实验验证表明SHD可下调模型小鼠脾脏组织中IL-4、IL-1β、IL-6等mRNA的表达、上调半胱氨酸天冬氨酸蛋白酶-3(cystein-asparate protease-3,Caspase-3)和Caspase-8等mRNA的表达,进而抑制IL-17信号通路的活化,治疗白塞病的效果[43]。 目前针对SHD复方配伍发挥药效的物质基础及其作用靶点、分子机制等相关研究仍较匮乏。此外,苦参中有效成分苦参碱、氧化苦参碱、槐果碱、槐定碱等喹诺里西啶类生物碱已被证实可造成神经、脏器等多种损伤[44-45],但对SHD不良反应的研究还不够深入,仅有急性毒性实验结果[34]。故建议未来可深入挖掘SHD复方配伍的药效物质基础及其药理作用机制。 2.3 临床应用 2.3.1 发热性疾病 SHD具有清热除烦、活血化瘀的功效,临床上多用于手足心热、烦热症、灼热足综合征等的治疗。洪海都等[46]阐述手足心热的病因为血瘀化热,治疗应以清泻实热、化瘀散结为主。SHD中黄芩清热解毒、泻火燥湿,辅以苦参退热祛湿,干地黄消散瘀滞,3药合用可减轻烦躁不安、阴血亏损等症状。另有研究表明SHD合四物汤加减治疗后,患者发热减轻、手足心热及失眠痊愈[47]。吕奎[48]在临床实践中运用SHD治疗34例春夏季节烦热症患者,1~4周后,患者周身烦热、口渴、盗汗等症状消失,总有效率为100%。柴浩然[49]擅用SHD治疗多种虚热疑难杂症如产后虚热、五心烦热、外阴及二耳灼热等。也有研究表明SHD能治愈灼热足综合征[50]。花海兵[51]将60例癌性发热患者随机分为中药组、对照组,前者予以SHD加减治疗,后者予以消炎痛栓治疗,连续用药10 d后中药组总有效率86.7%,显著优于对照组50%。徐银银等[52]结合经典和临床应用,以部位区分汗证,全身汗出不止的自汗用桂枝附子汤治疗、色正黄如柏汁的黄汗或腋汗用黄芪芍药桂枝苦酒汤治疗、颈部以上至头部盗汗用柴胡桂枝干姜汤治疗、手足心汗用SHD治疗。 2.3.2 红斑性肢痛症 红斑性肢痛症是一种原因不明的肢体远端皮肤温度升高、红肿,并产生剧烈灼热的神经系统疾病[53]。马海涛[54]采用SHD和人工冬眠合计结合治疗24例红斑性肢痛症患者,12 d内95.8%的患者疼痛及皮肤发红症状减轻。马成亮[55]依据临床观察,将肢痛症分为阴虚燥热、气阴两虚、阴阳俱虚、湿热蕴结4个证型。采用SHD加味治疗阴虚燥热型肢痛症取得较好疗效。 2.3.3 自身免疫性肝病 自身免疫性肝病是体内免疫异常引起的一组肝胆损伤性疾病,包括自身免疫性肝炎、原发性胆汁性胆管炎、原发性硬化性胆管炎及其中2种同时存在的重叠综合征[56]。王治宇等[57]将86例原发性胆汁性胆管炎随机分为2组,对照组采用熊去氧胆酸胶囊治疗,观察组在此基础之上给予加味SHD。2组肝功能和血脂变化指标及治疗前后临床症状变化有显著差异,且观察组总有效率为83.72%,远高于对照组65.12%。此外,SHD还可用于治疗自身免疫性肝炎、原发性胆汁性肝硬化、原发性硬化性胆管炎等[58]。2.3.4 皮肤性疾病 SHD可有效抑制花生四烯酸环氧合酶代谢产物的生成、清除自由基、抑制肥大细胞释放组胺等促炎介质,在皮肤性疾病的应用上也取得良好的临床效果。周浩[59]根据临床观察发现运用SHD治疗进行期银屑病时,患者的瘙痒、口渴、皮损等症状可得到控制,且疾病复发率低。缪泽群等[60]将60例阴伤湿热型掌跖脓疱病患者分为对照组和治疗组,对照组口服阿维A胶囊治疗,治疗组在此基础上联合SHD内服,6周后,治疗组总有效率显著高于对照组,且治疗组不良反应发生率显著低于对照组,说明SHD在联合治疗中可提高疗效、降低不良反应。姜红红[61]采用防己地黄汤联合SHD加减治疗嗜酸性粒细胞增多性皮炎患者,服药后患者皮疹、瘙痒及水肿等症状明显减轻。研究表明,温经汤联用SHD可用于治疗手心发热、耳后湿疹的灼口综合征[62]。史文丽等[63]运用SHD加味治疗乙肝相关性皮疹,服药9 d后患者面部?瘰明显减少,丙氨酸氨基转移酶指标恢复正常。 2.3.5 其他 除上述病证外,SHD在临床上还可用于直肠癌、复发性阿弗他溃疡等疾病的治疗。湿热下注是直肠癌的主要病因,SHD清热泻火之功效对直肠癌有较好的治疗效果[64-65]。许玉波等[66]在SHD治疗的30例白塞病患者临床观察中发现,治疗后症状评分显著低于治疗前,且临床痊愈率为66.67%。王晗峄等[67]在临床上应用加味SHD治疗儿童复发性阿弗他溃疡,二诊时患儿口腔溃疡疮面缩小、舌热等症状好转,继续服用药物三诊时患儿痊愈。另有研究表明,SHD还可用于治疗慢性咳嗽、便秘、慢性前列腺炎、乙肝相关性肾炎、肝源性糖尿病[63,68-69]。 综上,虽然SHD在发热性疾病、神经系统疾病、免疫系统疾病、皮肤性疾病等都有一定的应用,但其文献数量较少且陈旧,主要以病例报道、临床观察为主,作用机制研究较为滞后,其质量控制和评价指标不明确可能是制约其临床应用与发展的关键因素之一。 3 SHD的Q-Marker预测 Q-Marker是中药质量控制和评价的重要指标[70-72]。本文从质量传递与溯源、成分特有性、成分有效性、复方配伍环境和成分可测性出发,对SHD的Q-Marker进行预测分析。 3.1 质量传递与溯源 中药化学成分是中药复方发挥药效的物质基础,笔者使用中药系统药理学数据库平台分别检索SHD中3味药材的成分,结果为黄芩(143个)、苦参(113个)、地黄(76个),共332个化学成分。根据药物筛选原则,设定口服生物利用度≥30%、药物相似度≥0.18[73],同时,通过查阅已发表的相关文献对其进行补充[74-80],共得到126个活性成分,其中,39个来自黄芩(如黄芩素、黄芩苷、汉黄芩素、汉黄芩苷和千层纸素A等),52个来自苦参(如苦参碱、氧化苦参碱、槐定碱、槐果碱、苦参酮等),38个来自地黄(梓醇、地黄苷A、京尼平苷酸和桃叶珊瑚苷等)。 中药复方中的活性成分需要吸收入血才能发挥作用,入血成分分析是质量传递体系的重要环节之一。张蕾[33]对SHD的化学成分及其体内过程的研究结果表明,SHD中有7个主要活性成分能以原型成分入血,分别为苦参中的苦参碱、氧化苦参碱和氧化槐果碱,黄芩中的5,7,2',6'-四羟基黄酮、粘毛黄芩素III、汉黄芩素和千层纸素A。李淑娇等[81]运用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]技术分析得到13种黄芩入血成分,分别为黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、千层纸素A、千层纸素苷等。宿美凤等[82]分析发现苦参碱、槐定碱、氧化槐果碱、氧化苦参碱、金雀花碱等18种生物碱以原型入血。张雅阁等[83]对地黄的入血成分进行分析,确定其入血活性成分为梓醇和地黄苷D。Tao等[84]采用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]技术对ig地黄提取物后大鼠的入血成分进行分析,结果显示,地黄中的梓醇和毛蕊花糖苷为原型入血成分。SHD的入血成分见表2,为研究SHD的药效物质基础提供了一定的依据。 综上,基于质量传递与溯源的原则,从SHD中各药材所含成分入手,追踪到SHD中326个化学成分、126个活性成分,再结合36个入血成分综合考量,从而分析SHD的Q-Marker。 3.2 成分特有性 3.2.1 黄芩成分的特有性分析 黄芩为唇形科植物黄芩Scutellaria baicalensis Georgi的干燥根,主要含有黄酮类、挥发油类、多糖类、苯乙醇苷类等成分。一般认为黄酮及其苷类化合物是黄芩的有效物质基础,其中黄芩素、汉黄芩素、黄
中药Q-Marker是存在于中药材和中药产品中固有的或加工制备过程中形成的、与中药功能属性密切相关的化学物质,作为反映中药安全性和有效性的标志性物质进行质量控制。 《中华人民共和国卫生部药品标准》(维吾尔药分册)收载了洋甘菊药材基源、性状、鉴别,尚未收载含量测定项。《美国药典》《英国药典》《欧洲药典》均以芹菜素-7-O-葡萄糖苷含量作为质量评价标准,专属性较低-。为更好地评价洋甘菊药材质量,从植物亲缘学及化学成分特有性、临床药效和传统药性、成分可测性及成分有效性方面对洋甘菊的Q-marker进行预测分析,为建立药材科学合理的质量控制方法提供参考。 基于植物亲缘学及化学成分特有性证据的Q-marker预测分析 我国境内的菊科植物约有240个属,2300个种,化学成分30余类,主要有萜类、黄酮类、香豆素类等-。其中母菊属植物全球约40种,分布于欧洲、亚洲(西部、北部和东部)、非洲南部以及西北美,我国有洋甘菊和同花母菊两种-。在同花母菊中鉴定出28个挥发油成分,丙酸香叶酯和金合欢烯为主要成分-。金合欢烯也是洋甘菊挥发油的主要成分,此外还有α-红没药醇、母菊[b][url=http://www.baidu.com/link?url=Z33pCyjtNFQlX705WBym24rw3uCNQif693UJoHrVXQSWb-em36U9LuvHl14yEBScF41s7-3BDXa8owEzDclTvmW86l2ZrAyIn6DQomiPoEq]薁[/url][/b]等倍半萜。母菊[b][url=http://www.baidu.com/link?url=Z33pCyjtNFQlX705WBym24rw3uCNQif693UJoHrVXQSWb-em36U9LuvHl14yEBScF41s7-3BDXa8owEzDclTvmW86l2ZrAyIn6DQomiPoEq]薁[/url][/b]等倍半萜是挥发油中最有价值的成分之一,由于其性状为蓝色黏稠液体,也被称作“蓝油”,常作为评定药材质量的标准。通过分析母菊属植物和洋甘菊的特征性成分,可将黄酮、倍半萜类化学成分作为洋甘菊的Q-marker。 基于化学成分有效性的Q-marker预测分析 现代药理研究表明,洋甘菊提取物具有多种药理活性。其中以倍半萜为主导的挥发油成分和黄酮类成分含量较高,也是主要的药效物质基础。洋甘菊总黄酮通过下调ACC/FAS/DGAT2信号通路蛋白表达改善血脂水平;芹菜素及其糖苷、槲皮素、木犀草素与6,7-二羟基香豆素通过抑制α-淀粉酶和α-葡萄糖苷酶的吸收发挥降血糖作用;α-红没药醇、芹菜素、槲皮素与母菊[b][url=http://www.baidu.com/link?url=Z33pCyjtNFQlX705WBym24rw3uCNQif693UJoHrVXQSWb-em36U9LuvHl14yEBScF41s7-3BDXa8owEzDclTvmW86l2ZrAyIn6DQomiPoEq]薁[/url][/b]体内体外实验中均能够抑制炎性因子表达,母菊[b][url=http://www.baidu.com/link?url=Z33pCyjtNFQlX705WBym24rw3uCNQif693UJoHrVXQSWb-em36U9LuvHl14yEBScF41s7-3BDXa8owEzDclTvmW86l2ZrAyIn6DQomiPoEq]薁[/url][/b]可通过调节NF-κB信号通路发挥抗炎作用。因此,黄酮类及挥发油成分为洋甘菊的主要药效物质基础,可作为其Q-marker的选择参考。 基于成分与传统功效的相关性 在维吾尔药志中记载洋甘菊花解痉、消炎、解热、促进溃疡愈合和杀菌等作用。现代药理学研究表明,洋甘菊中倍半萜成分α-红没药醇与母菊[b][url=http://www.baidu.com/link?url=Z33pCyjtNFQlX705WBym24rw3uCNQif693UJoHrVXQSWb-em36U9LuvHl14yEBScF41s7-3BDXa8owEzDclTvmW86l2ZrAyIn6DQomiPoEq]薁[/url][/b]具有抗炎镇痛、抑菌、抗肿瘤,黄酮成分芹菜素、槲皮素具有抗氧化、解热镇痛抗炎等活性,作用与洋甘菊传统功效相对应,因此可选择α-红没药醇、母菊[b][url=http://www.baidu.com/link?url=Z33pCyjtNFQlX705WBym24rw3uCNQif693UJoHrVXQSWb-em36U9LuvHl14yEBScF41s7-3BDXa8owEzDclTvmW86l2ZrAyIn6DQomiPoEq]薁[/url][/b]、芹菜素、槲皮素作为洋甘菊的Q-marker。 基于化学成分可测性的Q-marker预测分析 采用HPLC法同时测定3批洋甘菊中槲皮素、木犀草素和芹菜素含量。研究发现洋甘菊中咖啡酰奎宁酸成分(绿原酸和异绿原酸A、B、C)含量高,可作为指标成分。测定欧洲不同国家洋甘菊精油的成分与含量,8个样品中红没药醇氧化物A含量最高,3个样品中α-红没药醇含量最高,母菊[b][url=http://www.baidu.com/link?url=Z33pCyjtNFQlX705WBym24rw3uCNQif693UJoHrVXQSWb-em36U9LuvHl14yEBScF41s7-3BDXa8owEzDclTvmW86l2ZrAyIn6DQomiPoEq]薁[/url][/b]含量范围为0.7%--15.3%。建立HPLC指纹图谱,显示12个特征峰,从中指认了咖啡酸、丁香酸、阿魏酸和槲皮素,4种成分分离度高,具有可测性,结合定量分析测定4种黄酮与5种酚酸成分的浓度,结果显示槲皮素>杨梅素>丁香酸>咖啡酸>山柰酚>阿魏酸>芦丁>没食子酸>对香豆酸。咖啡酸、丁香酸和杨梅素含量浓度范围较大,不考虑作为Q-maker的参考,因此可选择咖啡酰奎宁酸类成分(绿原酸、异绿原酸A、B、C)总含量、红没药醇氧化物A、α-红没药醇、槲皮素作为洋甘菊药材质量标志物的指标。
宇测生物完成数千万元Pre-B轮融资,本轮融资由正轩投资领投,老股东博远资本、创首投资和知名国际产业投资机构持续加注跟投。[color=#000000][b]本轮融资后宇测生物将重点推进医疗诊断、健康体检、医药检测等系统的市场化布局,打造国产高端诊断品牌;以神经标志物为核心,进一步完善神经血液标志物筛查和诊断方案,提高宇测单分子免疫检测技术核心品牌价值和能力。同时,公司将正式开启海外市场布局,实现国产高端品牌出海目标。[/b][/color][size=18px][color=#548dd4][b]一、神经科学血检市场蓄势待发[/b][/color][/size]全球人口老龄化带来的神经退行性疾病已经不容忽视。以阿尔茨海默病为首的神经退行性疾病已经给许多家庭带来巨大的身心、经济负担。有效的早筛、早诊和早治疗变得至关重要。近年来,随着超敏检测技术的快速发展,基于单分子免疫检测技术的血液生物标志物检测已被证明可以有效预测和诊断阿尔茨海默病,并已纳入国内外阿尔茨海默病诊疗专家共识。与此同时,针对AD病因的突破性靶向药物乐意保(仑卡奈单抗)通过国家药品监督管理局批准,正式进入中国,用于治疗由阿尔茨海默病引起的轻度认知障碍和阿尔茨海默病轻度痴呆,AD领域真正意义上完成了“有方法可测,有药物可医”的完整闭环。以阿尔茨海默病为首的神经科学诊疗市场展现出蓄势待发的蓬勃生机。[size=18px][color=#548dd4][b]二、单分子免疫检测技术的蓝海市场机会[/b][/color][/size]神经生物标志物在血液中的浓度极低,通常在pg/mL甚至fg/mL级别,传统免疫方法学受限于灵敏度水平,难以实现准确定量,无法推广临床应用。单分子免疫检测技术基于超高检测灵敏度,真正实现了神经标志物在血液中的精准检测和临床应用。随着单分子免疫检测技术日益成熟和市场化推广,新技术的发展将为IVD市场开拓百亿规模全新的蓝海机会。[size=18px][color=#548dd4][b]三、宇测生物的先发市场布局[/b][/color][/size]宇测生物凭借独立自主的单分子免疫检测平台,率先布局国内神经血液标志物市场,通过构建“产学研”高效转化平台,打造高端技术品牌,树立学术影响旗帜,推进以神经科学为核心的新型生物标志物的临床转化与市场推广,并已与国内多家头部医院形成深度合作,发表多篇高影响力学术论文。公司多年的技术沉淀和产品线整合,已完成在AD筛查、体检和诊断深度布局,全面覆盖上市AD核心指标的商业化试剂盒,推动单分子技术在神经血液标志物中的规范和标准,树立单分子免疫AD血检行业壁垒。宇测生物单分子免疫检测产品应用于高端科研和头部临床单位,预示着公司在神经系统疾病应用领域的领先地位。作为先行者,公司始终保持对单分子免疫领域的持续创新,不断推出新产品和新技术,保持先发优势,提高领先单分子免疫检测技术核心品牌价值和能力。[size=18px][color=#548dd4][b]四、国产化国际品牌建设规划[/b][/color][/size]宇测生物申请核心专利40+项,已授权20+项,拥有中国首张单分子技术发明专利,PCT专利获得中国、日本、加拿大、澳大利亚授权,美国、欧盟等国家区域正同步申请中。已就基于单分子免疫技术的神经血液标志物检测产品同多家国际企业达成合作。除了积极推进全球商业化战略外,扩大产品全球注册的力度,建立全球化运营体系,优化全球供应链管理,加强与国际科研机构的合作,共同开展针对神经血液标志物的前沿技术研究和应用开发,推动宇测生物成为具有国际影响力的全球化品牌。[来源:仪器信息网] 未经授权不得转载[align=right][/align]
[font=宋体][font=宋体]盘龙七片是著名老中医、骨伤科专家王家成老先生所献祖传秘方,由盘龙七、壮筋丹、五加皮等[/font]29[font=宋体]味中药组成,其具有活血化瘀、祛风除湿、消肿止痛的功效[/font][sup][1][/sup][font=宋体]。临床常用于治疗风湿性关节炎、腰肌劳损、软组织损伤、外伤性骨折等疾病。[/font][font=宋体]近年的研究显示,[/font][font=宋体]类风湿性关节炎[/font][font=宋体]([/font]rheumatoidarthritis[font=宋体],[/font]RA[font=宋体])[/font][font=宋体]是盘龙七片目前治疗的主要疾病。盘龙七片[/font][font=宋体]曾被《卫生部药品标准中药成方制剂》收载([/font]1998[font=宋体]年版第二十册),其中列出了盘龙七片复方组成配比和制法以及性状、鉴别检查,且被[/font][font=宋体]中成药治疗类风湿关节炎临床应用指南推荐为治疗[/font]RA[font=宋体]的临床用药[/font][font=宋体]。[/font][font=宋体]盘龙七片作为功效相对单一且临床疗效突出的中药复方代表,当前仍然存在一定质量控制方面的问题,《中国药典》[/font]2020[font=宋体]年版也未收载对盘龙七片的质量控制方法。可见,当前盘龙七片质量控制方法需要进一步提升。因此,本研究根据质量标志物([/font]quality markers[font=宋体],[/font]Q-Marker[font=宋体])的研究内涵[/font][sup][2-6][/sup][font=宋体],从中药成分与功效相关性角度,针对盘龙七片“祛风除湿”抗炎的主要功效,进行盘龙七片[/font]Q-Marker[font=宋体]筛选。首先采用超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url][/font]-[font=宋体]四极杆[/font]-[font=宋体]飞行时间质谱联用([/font]UPLC-QTOF-MS/MS[font=宋体])技术对盘龙七片化学成分进行表征,采用[/font]UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS[font=宋体]的[/font]MRM[font=宋体]扫描模式建立化学成分同时定量方法;进一步结合前期网络药理学预测结果,分析候选“功效成分群”从“药材[/font]-[font=宋体]成药”到“成药[/font]-[font=宋体]入血”的动态转移情况,从中筛选转移率较高成分。然后采用分子对接技术,评价“功效成分群”与盘龙七片“祛风除湿”抗炎关键靶点的结合活性,最后通过偏最小二乘回归对“功效成分[/font]-[font=宋体]体外活性”结果进行关联分析,将关联系数较高成分作为[/font]Q-Marker[font=宋体],以期为盘龙七片质量控制提供具有特有性、有效性、传递性的质控指标,保障其质量的有效追踪、溯源。[/font] 本研究从盘龙七片[/font]44[font=宋体]种化学成分中筛选出在“饮片[/font]-[font=宋体]成药[/font]-[font=宋体]入血”间转移能力较好,和“祛风除湿”关键靶点结合活性较高的[/font]6[font=宋体]个化合物作为盘龙七片主要功效相关的[/font]Q-Marker[font=宋体]:去氢木香内酯、龙胆苦苷、木香烃内酯、[/font]β-[font=宋体]蜕皮甾酮、迷迭香酸和染料木素。其中,去氢木香内酯是木香的主要成分,具有显著的抗炎活性,可以通过调控抑制核因子[/font]-κB[font=宋体]([/font]nuclear factor-κB[font=宋体],[/font]NF-κB[font=宋体])[/font]/MAPK[font=宋体]和[/font]Nrf2-Hmox-1[font=宋体]通路,抑制白细胞介素([/font]interleukin[font=宋体],[/font]IL[font=宋体])[/font]-1β[font=宋体]、[/font]IL-6[font=宋体]和肿瘤坏死因子([/font]tumor necrosis factor[font=宋体],[/font]TNF[font=宋体])[/font]-α[font=宋体]水平[/font][sup][16][/sup][font=宋体]。龙胆苦苷是秦艽的主要成分,可以通过调控[/font]CD147/p38/NF-κB[font=宋体]通路抑制金属蛋白酶([/font]metalloproteinases[font=宋体],[/font]MMP[font=宋体])分泌,从而减轻胶原诱导关节炎小鼠的滑膜炎症和软骨破坏程度[/font][sup][30][/sup][font=宋体]。[/font]β-[font=宋体]蜕皮甾酮是牛膝、重楼、壮筋丹的主要成分,有研究表明,以[/font]β-[font=宋体]蜕皮甾酮为主的组合物可显著恢复骨关节炎([/font]osteoarthritis[font=宋体],[/font]OA[font=宋体])大鼠模型中的关节粘连、软骨损伤、滑膜组织病变,其机制与其对花生四烯酸通路中的炎症因子[/font]PGE2[font=宋体],[/font]COX-2[font=宋体]水平的调控作用有关,同时,该组合物对关节液中的炎症因子[/font]CHI3L1[font=宋体]和[/font]IL-1β[font=宋体]也有较明显的抑制作用[/font][sup][31][/sup][font=宋体]。迷迭香酸是丹参的主要成分,具有广泛的药理作用,包括抗氧化、抗凋亡、抗肿瘤和抗炎等。迷迭香酸可通过抑制炎性因子[/font]IL-1b[font=宋体]、[/font]IL-6[font=宋体]、[/font]IL-17[font=宋体]分泌;调控[/font]ADAMTS-4[font=宋体]、[/font]ADAMTS-5[font=宋体]、[/font]ACAN[font=宋体]、[/font]COL2[font=宋体]基因的表达来达到治疗[/font]RA[font=宋体]和[/font]OA[font=宋体]的作用[/font][sup][32][/sup][font=宋体]。[/font][font=宋体]另外,迷迭香酸还可以通过独立于[/font]Fas/Fas-[font=宋体]配体([/font]FasL[font=宋体])相互作用的线粒体途径诱导活化[/font]T[font=宋体]细胞(靶向[/font]T[font=宋体]细胞亚群[/font]CD3[sup]+[/sup][font=宋体]、[/font]CD25[sup]+[/sup][font=宋体]和[/font]CD4[sup]+[/sup][font=宋体]、[/font]CD25[sup]+[/sup] T[font=宋体]细胞)和[/font]NK[font=宋体]细胞凋亡,进一步抑制炎性因子[/font]IL-17[font=宋体]释放,达到[/font]RA[font=宋体]治疗作用[/font][sup][33][/sup][font=宋体]。染料木素是杜仲[/font][i]Eucommia ulmoides[/i] Oliv.[font=宋体]的主要成分,可以通过抑制[/font]NF-κB[font=宋体]、前列腺素([/font]prostaglandin[font=宋体],[/font]PGs[font=宋体])、诱导型一氧化氮合酶([/font]inducible nitric oxide synthase[font=宋体],[/font]iNOS[font=宋体])、促炎细胞因子和活性氧([/font]reactive oxygen species[font=宋体],[/font]ROS[font=宋体])等多种信号通路具有较强的抗炎活性[/font][sup][34][/sup][font=宋体]。另有研究表明染料木素能通过[/font]Janus kinase 2[font=宋体]([/font]JAK2[font=宋体])[/font]/[font=宋体]转录激活因子[/font]3[font=宋体]([/font]transcription activator 3[font=宋体],[/font]STAT3[font=宋体])通路呈剂量依赖性地抑制[/font]IL-6[font=宋体]和[/font]VEGF[font=宋体]的表达和分泌,从而抑制信号转导因子和[/font]STAT3[font=宋体]的核易位。此外,染料木素还能抑制[/font]IL-6[font=宋体]诱导的血管内皮细胞的迁移和血管形成,起到抗关节炎的作用[/font][sup][35][/sup][font=宋体]。[/font][font=宋体]本研究通过探索盘龙七片“功效成分群”在“饮片[/font]-[font=宋体]成药[/font]-[font=宋体]入血成分”间的动态循行规律,采用“[/font]Q-Marker-[font=宋体]体外生物活性”关联算法,建立从“功效成分群”到[/font]Q-Marker[font=宋体]的筛选策略。所选定的[/font]Q-Marker[font=宋体]可从“成分[/font]-[font=宋体]功效”角度为其整体质量提升及临床安全用药提供参考。[/font]
我是临床医学专业的研究生,硕士期间研究的[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]检测某种临床标志物。现在写了一篇关于这个标志物的质谱方法应用进展,不知道是投偏我专业临床方便的杂志还是分析化学方面类的文章?如果投[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LCMS[/color][/url]技术类文章那些会比较好呢?谢谢