非对映异构体仅仅是构型上的差别,为何理化性质会差别很大呢?而且液相分析时很多非对映异构体用普通的反相就能分开,为什么仅仅一个构型上的差别会导致这么大的理化性质差异呢?求指教
请问外消旋体在碳谱和氢谱上有什么特点,如何利用核磁来区分对映异构体和非对映异构体
用普通的反相柱跑对映异构体,为什么会出现双峰?用的是普通反相柱而不是手性柱,对映异构体是纯品,无杂质,双峰峰高基本一致,请教其中的原理。
一个药物有多个手性碳,已知一个异构体的结构,能否通过NMR来判断另外几个非对映异构体的结构?希望各位多多帮助,谢谢!
[size=3][b]请问在对手性化合物(RS)原料药进行光学纯度控制中,用手性柱对其杂质对映异构体(SR)进行控制,而用普通的C18柱对非对应异构体(RR+SS)进行控制,但此RR与SS在C18上是重合的,这样可以吗?前提是该四个异构体无法在手性柱的一个流动相体系中出现,所以才出此下策。[/b][/size]
各位版友,小弟我最近在开发一个拥有4个手性中心的化合物的HPLC,目前已经购买了这个化合物的5个杂质对照品了,其中一个杂质是对映异构体,准备买大赛璐的手性柱进行分离,其他4个杂质均为非对映异构体,目前分别采用了0.1%的三氟乙酸作为流动相与乙腈梯度洗脱,5mM磷酸二氢钾(PH7.0)/(PH2.5)与乙腈梯度洗脱,采用前一个流动相峰宽有点宽,后一个流动相峰形很好,但是无法分开,想请教有分离非对映异构体的版友们支招啊!兄弟我不甚感激!
我用一个光学纯的化合物合成了双手性碳的产物,过柱后得到的是液态物质,重结晶后获得了一个光泽度较好的片状晶体.我将这种物质拿去过手性柱,试了几个流动相,都只出来一个单峰,郁闷死了,我该怎么办?怎样才知道它是是单一物还是非对映异构体的混合物?
大家好,我最近在分析一个含有对应异构体的一个样品,但是怎么分离结果都不是很理想。我采用的分析方法见下:waters2690,流动相:甲醇:60——80,乙酸:40——20,20min,最后改变了几次流动相梯度和时间,但是均存在肩峰。敢问各位大侠是怎么分离对应异构体的?

实验目的:分离API与其对映异构体试验方法:Column:Amylose-2(正相色谱柱) 流动相:正己烷:EtOH:TFA=940:60:1 样品溶剂 :正己烷:EtOH:MaOH=60:20:20出现问题:API的峰前沿处出现鼓包现象http://ng1.17img.cn/bbsfiles/images/2016/05/201605261937_594965_2828391_3.png解决方法:1.减小样品溶剂极性;2.调节流动相的酸碱性解决结果:1.减小样品溶剂极性后,鼓包仍然存在,所以认为溶剂与流动相的极性差别不是鼓包的原因,为什么不用流动相溶解样品,是因为固体样品在流动相中的溶解性不好;2.提高流动相中的TFA比例,即正己烷:EtOH:TFA=940:60:2,结果鼓包更严重,由此提示TFA对实验结果有影响;3.直接减去流动相中的TFA,即正己烷:EtOH=940:60,结果鼓包消失,但是API峰变宽,拖尾结论:这个可能是由于样品本身的特殊性引起的,即样品对酸有特异敏感性。这个也从平常的滤膜吸附试验中可以看出,在酸性溶液中,滤膜吸附特别严重致谢:感谢仪器论坛各位大神的帮助,谢谢!
问题是:我要做一个物质非对应异构体(AB两个对映异构体)的液相色谱谱方法学的验证,但是我得不到纯的A或B的对照品。所以在做验证的时候,里面很多项目没办法进行。比如说:检测线、回收率等等。等待大家的支持!
各位老师: 实验中碰到下面难题:一个含有2个手性中心的化合物,有4个对映异构体;顺利将该化合物四个对映体拆分后,利用在线旋光测出了这四个对映体的旋光性,依次为 (+)/(-)(+)/(-);问题是:这四个对映体的绝对构型(R)/(S)目前条件没有办法得到;在如何描述这个对映体上碰到了麻烦! 对于一个仅含有一个手性中心的化合物A,即便不知道其绝对构型,如果测定出了其对映体的旋光性,可以用 (+)-A 或 (-)-A 来表示该手性化合物的两个对映异构体;但对与含2个手性中心,有4个对映体的化合物,不知道其绝对构型,仅知道旋光性,按照上面的命名显然会造成歧义;目前也没有查到率属于上述情况的能供参考的文献,请各位老师支招,有没有比较好的办法来表示这四个对映体?麻烦了,非常感谢!
条件已经建立 这个需要做线性吗 怎么做线性 有必要做线性吗 欢迎讨论药品对映体只有一个
各位版友,大家好。 目前手上有1化合物及其对映体,纯度均大于95%,需开发检测方法,其本身无紫外吸收。为提高效率,准备委外与自行开发并行,现寻求各位版友帮助,帮忙提供一些第三方拆分机构信息。PS:已联系大赛璐,YMC,菲罗门(均无对应检测器),研创已送样。望各位版友提供更多的资源,万分感谢。[img]http://simg.instrument.com.cn/bbs/images/default/em09505.gif[/img]
如何用NMR区分对应异构体
我现在分析一个含多个手性中心的物质,非对映异构体有好几个,其中有几个用反相分不开,用正相分开了,现在要写分析方法,对于这几个杂质的纯度测定应该归属到"相关物质"还是"非对映体纯度"一项不太确定,请大家给点建议!
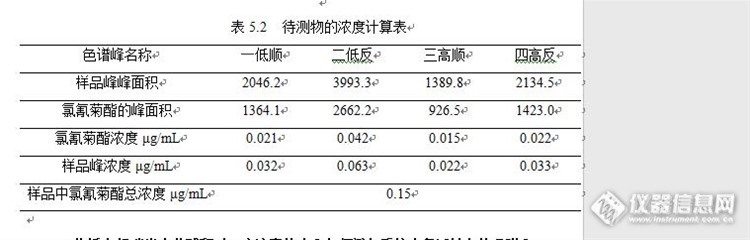
节选自《气相色谱百问精编》第239页 第五节异构体峰定量常规 GC色谱柱分析氯氰菊酯时,一般会出现一组四个异构体峰,如何对其进行定性定量分析?(1).问题在GC分析中,常常会碰见存在顺反异构体的化合物,如很多菊酯类农药、烯酰吗啉等。像氯氰菊酯在气相色谱中会出四个峰,四个峰的峰面积各不相同,那么如何准确计算样品中氯氰菊酯的含量?(2).原因氯氰菊酯共有四个顺反异构体8个手性对映异构体:一对低效顺式,一对低效反式,一对高效顺式和一对高效反式。常规GC柱分析时,出峰顺序为一低顺、二低反、三高顺、四高反,色谱条件控制的好,出四个峰,分析条件不恰当,有时只能出三个峰。(3).解决方案气相色谱分析中,样品中各组分在色谱柱中被分离,经检测器后,记录仪上得到一张色谱图。利用谱图中每个组分峰的位置(保留时间,tR)可进行定性分析,峰高或峰面积可进行定量分析。定性分析就是确定色谱图中每个色谱峰究竟代表什么组分。对组成不太复杂的样品,若欲确定色谱图中某一未知色谱峰所代表的组分,可选择一系列与未知物组分相接近的标准纯物质溶液,依次进样,当某一纯物质tR与未知色谱峰tR相同时,即可初步确定为该未知色谱峰所代表的组分。定量分析就是根据色谱峰峰高或峰面积来计算样品中各组分的含量,常用定量方法有峰面积百分比法、归一化法、内标法、外标法和标准加入法。首先,定性。选择氯氰菊酯标准溶液进样,记录四个异构体色谱峰的tR。在各种操作条件不变的情况下,进未知物组分,当未知色谱峰tR与氯氰菊酯标准品的四个异构体色谱峰tR相同时,可初步确定未知色谱峰是氯氰菊酯异构体之一。其次,定量。第一,配制已知浓度的氯氰菊酯标准溶液,进样,计算四个异构体峰的峰面积,将四个峰的峰面积相加得出总峰面积,用各个峰面积除总峰面积,算得相对百分数,乘以氯氰菊酯标准溶液的浓度,为各个异构体峰的浓度。计算公式如下:http://ng1.17img.cn/bbsfiles/images/2016/06/201606031653_595941_1645480_3.jpg(4).案例分析①氯氰菊酯标准溶液四个峰浓度分配计算配制氯氰菊酯标准溶液0.1μg/mL,进样后出四个峰,分别是一低顺二低反三高顺四高反,例如计算一低顺的实际浓度,一低顺的峰面积为1364.1,四个峰总面积为6375.8,f为http://ng1.17img.cn/bbsfiles/images/2016/06/201606031655_595942_1645480_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/06/201606031655_595943_1645480_3.jpg
氯氰菊酯Cypermethrin,化学名称为(R S)–α–氰基–(3–苯氧苄基)(1RS,3R S 1R S,3S R)–3–(2,2–二氯乙烯基)–2,2–二甲基环丙烷羧酸酯,分子式为C22H19Cl2NO3;共有8种光学异构体。杀虫活性的强弱与分子构型的手征性有关;其中,顺式氯氰菊酯含有(S)–(1R,3R)和(R)-(1S,3S)两个对映体;反式氯氰菊酯含有(S)-(1R,3S)和(R)–(1S,3R)两个对映体;均为高效体。顺式、反式氯氰菊酯的分子结构见下图。奇怪的是所有的异构体只有一个cas号052315-07-8?是否CAS不区分光学和空间异构体?但是右旋葡萄糖(D-glucos)的CAS号是50-99-7,左旋葡萄糖(L-glucose)是921-60-8,α右旋葡萄糖(α-D-glucose)是26655-34-5?[IMG]file:///C:/Documents%20and%20Settings/owner/桌面/Doc1.htm[/IMG]
HPLC法在药物对映体的分离和测定中的应用 (转) 摘 要:由于药物对映体之间在药理、毒理及吸收等方面存在较大差异,因此,建立分离和测定对映体化合物的方法十分重要。本文综述HPLC法在分离和测定药物对映体的常用方法,包括手性衍生化试剂、手性流动相和手性固定相在药物对映体分离测定中的应用。对对映体化合物的分析鉴定有指导意义。 手性化合物的拆分是当前分析化学中最为活跃的领域之一,自然界中的许多化合物都是有旋光性的,而合成手性药物中大多(88%)是外消旋体,许多手性药物的对映体在生理过程中显示了不同生理活性。据研究反应停的致畸作用主要是由于其(S)-(-)异构体所致。因此,建立高专属性、高灵敏度、高分离度的对映体拆分和测定方法,对提高药物的活性、减小副作用,深入研究药物的作用机理等具有重要的理论和实际意义。对映体化合物之间除对偏振光的偏转方向不同外,具有完全相同的理化性质,因而其分离比较困难。传统的拆分方法有分步结晶、微生物和酶消化法等,或者用手性衍生化试剂将其转化成非对映体,然后根据其物理性质不同进行分离,但这些方法难于进行微量的分离和测定。80年代以来,随着快速、准确、微量的光学异构体的HPLC拆分及测定方法的建立和发展,使HPLC迅速成为药物对映体分离和测定最为广泛应用的方法。手性HPLC拆分法是以现代HPLC技术为基础,引入手性环境使对映异构体间呈现物理特征的差异而进行分离。通常分间接法和直接法,前者是对映体混合物以手性试剂作柱前衍生,形成一非对映体,然后以常规(偶也见手性)固定相分离。后者是直接以手性流动相(CMP)或手性固定相(CSP)直接进行分离。1 手性衍生化试剂法 手性衍生化试剂(CDR)法是在分子间引入手性中心,其产物为非对映异构体(diastereomer,DSTM),从而进行分离。下列情况通常选用CDR法进行拆分:(1)不宜直接拆分。添加某些基团,以增加色谱系统的选择性。如游离胺类在CSP上往往是颇弱的色谱性质,生成中性化合物后则获显著改善。(2)提高紫外或荧光检测的效果。刘雁鸣等[1]用 NBD-(L)-APY荧光试剂柱前衍生化测定布洛芬对映体,提高了检测灵敏度。对CDR的要求通常为:溶质分子至少有一个(多个时其性质各不相同)功能团供衍生(多为-NH2,-OH或-COOH)。光学活性试剂必需是手性高纯度;反应条件必须温和、简便;宜附有发色或荧光基团。目前,已有许多商品化的CDR可供选用,常见的CDR可分为以下几类:(1)异硫氰酸酯和异氰酸酯类 此类试剂易与大多数醇类及胺类化合物反应进而被分离,如麻黄素类,肾上腺素类,肾上腺素拮抗剂,儿茶酚胺类等。王亚芹等[2]采用S(+)-1-(1-苯基)乙基异氰酸酯为衍生化试剂分析了血浆中普罗帕酮的对应体,并研究了其在健康人体内的药代动力学。邱宗荫等[3]用乙酰葡萄糖异硫氰酸酯(GITC)为柱前CDR,以反相HPLC法测定血浆中地佐西平对映体的血药浓度,线性范围为5~200μg.L-1。陈冰等[4]用GITC为柱前CDR,用反相HPLC法测定血浆中普罗帕酮对映体的血药浓度,适合用于临床药动药效学研究。(2)萘衍生物类 由于此类化合物有利于提高立体选择性和检测灵敏度,因此萘的各种衍生物用作手性试剂十分普遍。Wainer等[5]选用萘甲醛(NDH)为手性试剂,与其缩合成恶唑烷衍生物,成功地分离了麻黄碱、4-甲氧基麻黄碱、伪麻黄碱。Bhatti[6]等用S-(+)-1-(1-萘基)-乙基异氰酸酯为CDR,用HPLC法测定了人血浆中美托洛尔对映体浓度。(3)酰氯与磺酰氯类 此类试剂可与化合物直接缩合,或与样品反应后,再引入其它基团,合成更有利于拆分与检测的衍生物。Sallustio等[7]以SOCl2与芳丙酸类消炎镇痛药如2-苯丙酸、酮洛芬及非诺洛芬的血浆样品提取物反应,然后再与R-2-苯乙胺成酰胺衍生物,产物以NP(Sil,乙腈∶二氯甲烷,5∶95)分离,异构体均可完全拆分。(4)光学活性氨基酸类 为最早采用的色谱手性试剂,为提高反应活性和定量回收率,常将羧基转化成酰氯、酸酐等。此类试剂广泛用于胺、羧酸及醇类药物,尤其是氨基酸类,其衍生化法多基于肽合成原理。本类方法要求手性药物具有活泼反应基团,同时两个对映体的衍生化速度应相同,否则会引起非对映体与原对映体的组成产生差异,另外要求手性衍生化试剂光学纯度高,反应要迅速、彻底,因此应用受到一定限制。

[align=center][color=#333333][img=,600,374]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201454548064_5639_932_3.jpg!w690x431.jpg[/img][/color][/align][color=#333333]小月和小旭是一对双胞胎兄弟,模样十分相似,经常被别人认错,而他们的妈妈却能轻松识别开来,虽然长相非常相似,但是他们的习性也会有差异,所以妈妈根据他们的特点进行辨别。[/color][color=#333333][b]同分异构体[/b][/color][color=#333333][color=#333333]同样地,在变幻万千的化学世界里,也存在很多结构和性质相似的物质,例如同分异构和对映异构体,这给我们的色谱分离带来了较大的困难,例如熊墩果酸和熊果酸。[/color][/color][color=#333333][/color][align=center][img=,300,227]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201458333982_238_932_3.jpg!w640x486.jpg[/img] [img=,300,227]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201458378677_8106_932_3.jpg!w640x486.jpg[/img][/align][align=center][color=#a0a0a0]齐墩果酸 [/color][color=#a0a0a0]熊果酸[/color][/align][color=#333333]面对这些物质,不仅需要一副“火眼金睛”,还需要一颗“耐心”,需要针对其独有的特性来进行分离。月旭色谱柱键合相独特的选择性,赋予您一副火眼金睛,接下来只需要一颗耐心静待分离结果哦。对映异构体一般通过手性色谱柱进行拆分,月旭不同选择性的手性键合相也能满足您不同的分离需求,而今天所要介绍的是同分异构体的分离。月旭色谱柱分离同分异构体,常见的有Ultimate XS-C18、Ultimate PFP、Ultimate PAH以及Ultimate XB-C30等色谱柱。[b]🔺 Ultimate XS-C18 和Ultimate XB-C30色谱柱分离齐墩果酸和熊果酸:色谱条件[/b]流动相:乙腈:水=93:7检测波长:210nm柱温:20℃流速:1ml/min进样量:10μl[/color][align=center][b]Ultimate XS-C18对照溶液色谱图[/b][/align][align=center][img=,600,238]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201455076447_8021_932_3.jpg!w521x207.jpg[/img][/align][align=center][color=#333333][img=,600,62]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201455151124_9322_932_3.png!w690x72.jpg[/img][/color][/align][align=center][b][/b][/align][align=center][b]Ultimate XB-C30对照溶液色谱图[/b][/align][align=center][img=,600,361]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201455203099_7222_932_3.jpg!w687x414.jpg[/img][/align][align=center][img=,600,53]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201455234503_2074_932_3.png!w690x62.jpg[/img][/align]用Ultimate XS-C18和Ultimate XB-C30色谱柱来分离齐墩果酸和熊果酸,分离度能达到检测要求。[b]🔺 Ultimate PFP来分离α、β、ϒ 、δ生育酚:[/b]生育酚为维生素E的水解产物,天然的生育酚都是d-生育酚(右旋型),它有α、β、ϒ 、δ等多种同分异构体。[b]色谱条件[/b]流动相:甲醇/水梯度方法检测波长:294nm/325nm柱温:20℃流速:0.8ml/min进样量:10μl [table=276][tr][td=1,1,63]时间[/td][td=1,1,72]流动相A[/td][td=1,1,71]流动相B[/td][td=1,1,70]流速[/td][/tr][tr][td=1,1,63]0[/td][td=1,1,72]4[/td][td=1,1,71]96[/td][td=1,1,70]0.8[/td][/tr][tr][td=1,1,63]13[/td][td=1,1,72]4[/td][td=1,1,71]96[/td][td=1,1,70]0.8[/td][/tr][tr][td=1,1,63]20[/td][td=1,1,72]0[/td][td=1,1,71]100[/td][td=1,1,70]0.8[/td][/tr][tr][td=1,1,63]24[/td][td=1,1,72]0[/td][td=1,1,71]100[/td][td=1,1,70]0.8[/td][/tr][tr][td=1,1,63]24.5[/td][td=1,1,72]4[/td][td=1,1,71]96[/td][td=1,1,70]0.8[/td][/tr][tr][td=1,1,63]30[/td][td=1,1,72]4[/td][td=1,1,71]96[/td][td=1,1,70]0.8[/td][/tr][/table][align=center][/align][align=center][b]混合对照色谱图[/b][/align][align=center][img=,600,171]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201455395319_5064_932_3.jpg!w690x197.jpg[/img][/align][align=center][img=,600,107]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201455422441_9663_932_3.png!w690x124.jpg[/img][/align][color=#333333][/color]Ultimate PFP色谱柱,含氟固定相有很强的几何尺寸和立体形状选择性,能分离一些用烷基固定相很难分离的结构相似的物质。此项目中,采用月旭Ultimate PFP色谱柱进行分离,能获得符合标准要求的分离度。[align=center][b]🔺 Ultimate PAH分离主成分及异构体杂质[/b][/align][align=center][img=,300,258]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201455454425_4582_932_3.png!w252x217.jpg[/img] [img=,300,268]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201455487098_9010_932_3.png!w238x213.jpg[/img][/align][align=center]主成分 杂质[/align][b]色谱条件[/b]流动相:乙腈/水=57/43检测波长:266nm柱温:35℃流速:1.0ml/min进样量:10μl[align=center][b]混合对照色谱图[/b][/align][align=center][img=,600,211]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201455517791_9417_932_3.png!w690x243.jpg[/img][/align][align=center][img=,600,72]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201455553754_9107_932_3.png!w690x83.jpg[/img][/align][color=#333333][/color][color=#333333]月旭Ultimate PAH(4.6*250mm,5μm),在此色谱条件下检测样品,分离度可以达到要求。看到这里,如果您想拥有辨别同分异构体的“火眼金睛”,即使他们是齐天大圣和六耳猕猴,只要您想,最后都会守得云开见月明,一览其真面目。[/color]
我正在分析一个含有手性异构体的物质(非对映),常规的流动相最好的在35分钟前后分离度是1.1。因为我想用一个方法同时检测异构体和有关物质,所以不打算用手性柱,想考虑一下用手性流动相的方法。粗略思路大概清楚,就是加入手性氨基酸和二价金属离子。但是具体的操作就不明了,比如这种方法对产品性质有什么要求,不知道我的产品能否适应此种方法,流动相要选择何种氨基酸,怎么调节pH之类的,谁能指点一下或者给个参考资料的。我做的产品是两性物质。pka1=2.8,pka2=7.9。
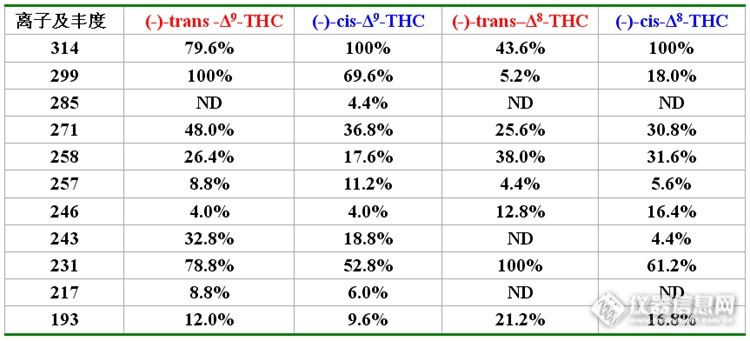
四氢大麻酚质谱裂解机理研究及其异构体的鉴别摘 要:通过GC/MS对两类THC的质谱裂解方式进行研究,对比了顺反异构体的差异,以及烯键位置不同对裂解所产生的影响,并通过所存在的差异性对其异构体鉴定提供依据。关键词:Δ9-THC;Δ8-THC;EI(电子轰击);质谱裂解机理;异构体一、概述 在有机化学与药物化学的研究中,如何区分具有不同药理活性的立体异构体,一直是个困扰人们的难题。质谱虽然是有机比合物分离鉴定的一种有效分析手段,但在立体异构体的区分方面尚存在许多困难,仅在离子的丰度上有所差异,顺反异构体的物理性质差别不大,双键带氢的顺反异构体也不例外,这类顺反异构体我们通过核磁共振谱可以快速、准确地加以测定和区别,而对于顺反异构体的混合物通过核磁很难做以鉴别,或者采用X光单晶衍射法,而对于不能培养成单晶的样品,此手法不能使用。所以其鉴定存在着一定的困难,色谱具有良好的分离能力,而质谱具有很好的定性功能,通过色谱质谱仪器的联用对有机化合物的鉴定已经成为一种有力的手段。大麻有镇静和兴奋功能,在医学上可用来做止痛剂,亦有研究用作医疗癌症和精神科疾病。吸食大麻有迷幻效果,一直有说可影响人的精神和生理。四氢大麻酚(Tetrahydrocannabinol),简称THC,又称Δ9-四氢大麻酚(Δ9-THC),最早由以色列雷霍沃特魏茨曼科学研究所的三名研究人员在1964年分离出来。从大麻中可以分离得到其异构体Δ8- THC。2013年,美国科学家研究发现,四氢大麻酚或可抗艾滋感染,表明其具有较强的生理活性,而立体化学构型往往会影响其生理活性,Δ9-THC仅双键异构和立体异构就有30个,而对于其来讲有两个手性中心,4种对应异构体,分别是左旋体和右旋体以及其所对应的顺反异构体,在常规质谱中不能区分旋光对映体,然而在手性条件下对映体将会显示出差异,利用产生的不同特征离子可以区分旋光对映体。所以其立体构型的研究就显得重要尤为重要了,而运用质谱手段对其鉴定还尚未见报道。http://ng1.17img.cn/bbsfiles/images/2014/10/201410211559_519327_2359621_3.pngTabel1. Δ9-THC及其异构体的结构式以及空间立体构型二、结果分析2.1Δ9-THC的质谱图http://ng1.17img.cn/bbsfiles/images/2014/10/201410211602_519329_2359621_3.png2. 2Δ9-THC的质谱裂解途径 分子被电离时,按照化学基本原理,分子优先失去电离能最低的电子而形成分子离子,所以我们往往直观的认为处于最高占据轨道(HOMO轨道)最容易失去电子而生成分子离子,而一般根据电离能的大小遵循σ[font=
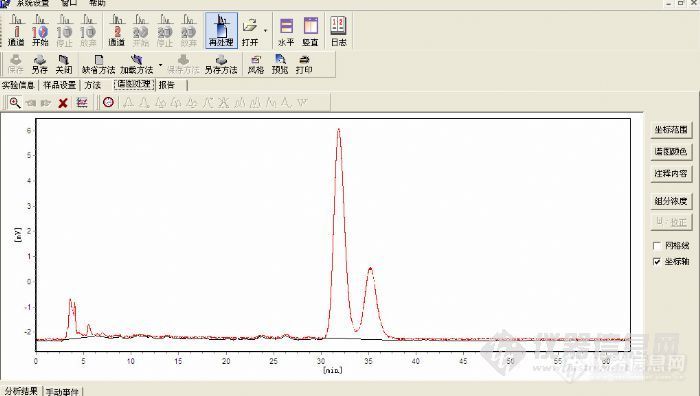
手性色谱柱在手性异构体拆分中的应用实例 手性是自然界的一种普遍现象,构成生物体的基本物质如氨基酸、糖类等都是手性分子。手性分子的重要性不仅表现在与生物相关的领域,在功能材料领域,如液晶、非线性光学材料、导电高分子方面也显示出诱人前景。随着对手性分子认识的不断深入,人们对单一手性物质的需求量越来越大,对其纯度的要求也越来越高。单一手性物质的获得方法大致有以下三种:①手性源合成法。②不对称合成法。③外消旋体拆分法。那么外消旋体的拆分方法主要有1 机械拆分法 2 化学拆分法3 生物化学拆分法4 色谱拆分法5 萃取拆分法6 膜拆分法,等。这里介绍的是色谱拆分法,各种色谱技术均可用于手性拆分。可以将外消旋体与手性试剂作用生成非对映异构体,用普通的色谱技术拆分;也可以使用手性流动相或手性固定相进行拆分,而以后者最为简便、廉价,下面介绍的实例也是后者。 仪器 高效液相色谱仪(安捷伦1200型),Waters600. 试剂 甲醇(色谱级),重蒸水,乙腈(色谱级) 手性柱为CHIRALPAKR AD-RH Column Size 150×4.6mmhttp://ng1.17img.cn/bbsfiles/images/2010/11/201011282059_262536_2165260_3.jpg C18柱为依利特分析柱, Column Size 250×4.6mm 下图为样品1的分析图谱, 分析条件:C18柱为依利特分析柱,Column Size 250×4.6mm,甲醇:水 50:50,柱温25度。 http://ng1.17img.cn/bbsfiles/images/2010/11/201011282101_262537_2165260_3.jpg 显而易见,为一单一化合物,即而测试核磁共振谱,经解析为一含手性中心的化合物,其为R型还是S型,亦或是R型和S型共同存在,无从得知。 于是我们决定用手性色谱柱进行分析,旨在判断是否为混合物。 分析条件 手性柱为CHIRALPAKR AD-RHColumn Size 150×4.6mm ,已腈:水 30:70,柱温 25度(波长280) 分析图谱如下http://ng1.17img.cn/bbsfiles/images/2010/11/201011282120_262538_2165260_3.jpg 结果显而易见,为两种异构体的混合物,其量比大约3:2。 经过对样品1进行分析的结果,我们对样品2也进行了同样分析。其分析图谱如下: 分析条件:C18柱为依利特分析柱,Column Size 250×4.6mm,甲醇:水 50:50,柱温25度。 http://ng1.17img.cn/bbsfiles/images/2010/11/201011282127_262539_2165260_3.jpg 经核磁图谱解析仍为一手性化合物,于是进行了手性柱色谱分析。 分析条件 手性柱为CHIRALPAKR AD-RHColumn Size 150×4.6mm ,已腈:水 40:60,柱温 25度(波长280) 图谱如下:http://ng1.17img.cn/bbsfiles/images/2010/11/201011282132_262540_2165260_3.jpg 分析结果显示样品2为一混合物,其量比约为3:1 结论:我们在得知样品为一手性化合物时,为确定其是否为一异构体混合物,对其进行了手性柱色谱分析,结果显示为混合物,我们进而对其进行了累计制备,分别得到了R型和S型单体,也是实验室对手性拆分的成功实例。 最后,补充一句,次此实验所用手性柱在保养方面与一般的色谱柱还是有些差别的,其最后保存在40%的已腈水中,避免以高浓度的有机溶剂冲洗洗柱子。
异构体和同分异构体的区别

这是一支进口的666.DDT混合标准溶液。我们公司买的。CMA评审考核时候来的是一支国产的666、DDT混合标准样品。对照的时候发现标液上写的666、DDT的命名写的分别是a、b、d、g四种异构体。但是考核的标样写的却是α、β、δ、γ四种异构体。我知道这只是个不同表述方法的名字而已。但是这abcd四个名字,分别对应哪几个α、β、δ、γ 呢?http://ng1.17img.cn/bbsfiles/images/2017/02/201702141458_01_2206495_3.png
好像常规的有机四大谱都分辨不了手性异构体啊,至于分离可以用手性色谱摸索一下。有没有其他可以判断手性异构体的绝对构型以及区分手性异构体的技术啊?望大侠们指教。
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=71348]应用自动内循环技术分离异构体[/url]应用自动内循环技术分离异构体旋光异构体药物在全世界50中主要药物中占了50%。对旋光异构体的分离一直是液相色谱分离中的一个难点。本文描述了应吉尔森制备色谱系统结合内循环分离技术对旋光异构体的分离。
各位大侠,用岛津GC2010,计算同分异构体的时候,该用浓度校准还是组校准。比如,氯菊酯有两个同分异构体,两个同分异构体都是50ppb,那该用组还是浓度校准的哪个去计算,做曲线时,组的浓度应该怎么设定,是50ppb,还是100ppb。六六六和DDT的计算也是这样的吗?
在做日化香精分析的时候总会出现某些物质的异构体,比如佳乐麝香异构体,那么请教下,这个异构体是否要加到佳乐麝香的含量去?我认为是要将异构体加入到原物质上!
超高效液相色谱-电喷雾质谱法结合同位素稀释技术检测动物源性食品中的六溴环十二烷异构体 施致雄 封锦芳 李敬光 赵云峰 吴永宁 建立了使用超高效液相色谱-电喷雾四极杆质谱(UPLC-ESI-MS)结合同位素稀释技术准确测定动物源性食品中六溴环十二烷(HBCD)的3种非对映异构体的方法。试样在加入同位素内标13C-HBCD后进行索氏提取,提取液去除脂肪后经硅胶固相萃取柱浓缩、净化后,通过Waters ACQUITY UPLCTMBEH C18色谱柱分离,以甲醇-乙腈混合液和水为流动相进行梯度洗脱。在UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]分析过程中以保留时间和母离子信息进行定性,选择离子记录(SIR)方式定量。该法对于所测试的鲜奶、鱼肉等样品,检出限为0.1~0.4ng/g,定量限为0.4~1.2ng/g。对于加标鱼肉样品,添加水平为0.6,2.0和6.0ng/g时,3种被测物的加标回收率为92.9%~99.3%,相对标准偏差为3.1%~8.0%。【作者单位】:中国疾病预防控制中心营养与食品安全所 首都医科大学公共卫生与家庭医学学院 中国疾病预防控制中心营养与食品安全所 中国疾病预防控制中心营养与食品安全所 中国疾病预防控制中心营养与食品安全所 北京100050 首都医科大学公共卫生与家庭医学学院 北京100069 北京100069 北京100050 北京100050 北京100050 首都医科大学公共卫生与家庭医学学院 北京100069【关键词】:超高效液相色谱 电喷雾质谱 同位素稀释 六溴环十二烷异构体 食品【基金】:国家高技术研究发展计划(“863”计划)专题课题(No.2006AA06Z043) “十一五”国家科技支撑计划重大项目(No.2006BAK02A10) 北京市教育委员会科技发展计划项目(No.KM200810025022).【分类号】:TS207【DOI】:CNKI:SUN:SPZZ.0.2008-01-000【正文快照】: 1,2,5,6,9,10-六溴环十二烷(hexabrom ocy-c lododecane,HBCD)是一种非芳香的溴代环烷烃,主要用作添加性的阻燃剂添加在热塑性塑料中,最终产品主要为苯乙烯树脂。另外在纺织品涂层、电缆线、橡胶粘合剂及不饱和聚酯的生产中也有应用。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=107349]超高效液相色谱-电喷雾质谱法结合同位素稀释技术检测动物源性食品中的六溴环十二烷异构体[/url]
欧盟限量基准中规定了氰戊菊酯:RR+SS 异构体 RS+SR异构体的限量。两个异构体在不同的物体中限量是不一样的,请问一下,我现在没有他们单独的标准品,怎么通过峰来判断,在保留时间上氰戊菊酯有两个峰,这四种同分异构体是怎么出峰的,出峰顺序是怎么样的。[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用仪[/color][/url],DB-5柱,非常感谢!