第一章 总则第一条 为加强药物Ⅰ期临床试验的管理,有效地保障受试者的权益与安全,提高药物Ⅰ期临床试验的质量,根据《中华人民共和国药品管理法》、《药品注册管理办法》、《药物临床试验质量管理规范》等相关规定,参照国际通则,制定本指导原则。第二条 本指导原则适用于药物Ⅰ期临床试验,旨在为药物Ⅰ期临床试验的组织管理和实施提供原则性指导。人体生物利用度或生物等效性试验可参考本指导原则。第二章 职责要求第三条 申办者应建立筛选国家药物临床试验机构和研究者的程序和标准,选择、委托获得相关专业资格认定的药物临床试验机构进行药物Ⅰ期临床试验。 第四条 申办者应建立质量保证体系,对临床试验的全过程进行监查和稽查,确保临床试验的质量,保障受试者的权益与安全。申办者可以委托合同研究组织执行临床试验中的某些工作和任务。申办者对临床试验的真实性及质量负最终责任。第五条 国家药物临床试验机构的药物Ⅰ期临床试验研究室负责药物Ⅰ期临床试验的实施。研究者应遵循《药物临床试验质量管理规范》,并严格执行临床试验方案,对临床试验的真实性和质量负责,保护受试者的权益与安全。第六条 临床试验生物样本分析应在符合国家有关管理规定的实验室进行。第七条 伦理委员会在审查试验方案和知情同意书等资料的基础上,应针对药物Ⅰ期临床试验的特点,重点关注试验风险的管理及控制、试验方案和知情同意书的修改等,对临床试验进行必要的监督检查,加强对受试者的权益与安全的保护。
关于印发药物临床试验伦理审查工作指导原则的通知 国食药监注436号 2010年11月02日 发布 各省、自治区、直辖市食品药品监督管理局(药品监督管理局),总后卫生部药品监督管理局: 为加强药物临床试验的质量管理和受试者的保护,规范和指导伦理委员会的药物临床试验伦理审查工作,提高药物临床试验伦理审查工作质量,根据《药品注册管理办法》和《药物临床试验质量管理规范》的有关规定,国家局组织制定了《药物临床试验伦理审查工作指导原则》,现予印发。请你局指导本辖区内药物临床试验机构学习,参照执行。 附件:药物临床试验伦理审查工作指导原则起草说明 国家食品药品监督管理局 二○一○年十一月二日
一直以来,大型制药公司研发药物的临床试验数据都作为公司的高度机密,而保存在公司的数据库中。葛兰素史克(GSK)决定打破常规,公开公司的“高度机密”。讨论公布在研药物所有临床试验数据利弊.
国食药监注483号各省、自治区、直辖市食品药品监督管理局(药品监督管理局),总后卫生部药品监督管理局: 为加强药物Ⅰ期临床试验的管理,有效的保障受试者的权益与安全,提高药物Ⅰ期临床试验的研究质量与管理水平,根据《中华人民共和国药品管理法》、《药品注册管理办法》和《药物临床试验质量管理规范》等有关规定,国家局组织制定了《药物Ⅰ期临床试验管理指导原则(试行)》,现予印发。请你局组织本行政区域内药物临床试验机构学习,参照执行。 附件:《药物Ⅰ期临床试验管理指导原则(试行)》起草说明 国家食品药品监督管理局 二O一一年十二月二日药物Ⅰ期临床试验管理指导原则(试行)第一章 总则 第一条 为加强药物Ⅰ期临床试验(以下简称I期试验)的管理,有效地保障受试者的权益与安全,提高Ⅰ期试验的研究质量与管理水平,根据《中华人民共和国药品管理法》、《药品注册管理办法》、《药物临床试验质量管理规范》等相关规定,参照国际通行规范,制定本指导原则。 第二条 本指导原则适用于Ⅰ期试验,旨在为Ⅰ期试验的组织管理和实施提供指导。人体生物利用度或生物等效性试验应参照本指导原则。第二章 职责要求 第三条 申办者应建立评价药物临床试验机构的程序和标准,选择、委托获得资格认定的I期试验研究室进行Ⅰ期试验。 第四条 申办者应建立质量保证体系,对I期试验的全过程进行监查和稽查,确保临床试验的质量,保障受试者的权益与安全。 第五条 申办者可以委托合同研究组织(CRO)执行I期试验中的某些工作和任务。委托前对合同研究组织的研究条件、能力、经验以及相应的质量管理体系进行评价。当合同研究组织接受了委托,则本指导原则中规定的由申办者履行的责任,合同研究组织应同样履行。申办者对临床试验的真实性及质量负最终责任。 第六条 Ⅰ期试验研究室负责Ⅰ期试验的实施。研究者应遵循临床试验相关法律法规、规范性文件和技术指导原则,执行临床试验方案,保护受试者的权益与安全,保证临床试验结果的真实可靠。 第七条 药物临床试验生物样本分析应在符合《药物临床试验生物样本分析实验室管理指南》(以下简称《实验室管理指南》)的实验室进行。从事药物临床试验生物样本分析的实验室均应接受药品监督管理部门的监督检查。 第八条 伦理委员会应针对Ⅰ期试验的特点,加强对受试者权益与安全的保护,重点关注:试验风险的管理与控制,试验方案设计和知情同意书的内容,研究团队的人员组成、资质、经验,受试者的来源、招募方式,实施过程中发生的意外情况等。
各省、自治区、直辖市食品药品监督管理局(药品监督管理局),总后勤部卫生部药品监督管理局: 为加强药物I期临床试验的管理,提高临床试验生物样本分析实验室的分析质量,有效地保障受试者的权益与安全,确保所产生的数据和结果的可靠性、完整性和科学性,根据《药物临床试验质量管理规范》,我司组织起草了《药物Ⅰ期临床试验管理指导原则(征求意见稿)》、《药物临床试验生物样本分析实验室管理规定(征求意见稿)》。现公开征求意见,请于2011年4月30日前将修改意见反馈我司。(征求意见稿可在国家食品药品监督管理局网站下载) 联系人:蓝恭涛,唐慧鑫 电 话:010—88330742,0722 传 真:010—88363228 地 址:北京市西城区宣武门西大街26号院2号楼 邮 编:100053 E-mail:yjjdc@sda.gov.cn 附件:1.《药物Ⅰ期临床试验管理指导原则(征求意见稿)》 2.《药物临床试验生物样本分析实验室管理规定(征求意见稿)》 3.起草说明 国家食品药品监督管理局药品注册司 二○一一年三月十八日
国食药监注482号各省、自治区、直辖市食品药品监督管理局(药品监督管理局),总后卫生部药品监督管理局: 为加强药物临床试验生物样本分析实验室的管理,提高生物样本分析数据的质量和管理水平,根据《药品注册管理办法》、《药物临床试验质量管理规范》、《药物非临床研究质量管理规范》,参照国际规范,国家局组织制定了《药物临床试验生物样本分析实验室管理指南(试行)》,现予印发。请你局组织本行政区域内有关单位学习,参照执行。 附件:《药物临床试验生物样本分析实验室管理指南(试行)》起草说明 国家食品药品监督管理局 二O一一年十二月二日药物临床试验生物样本分析实验室管理指南(试行)第一章 总 则 第一条 为加强药物临床试验生物样本分析实验室的管理,提高生物样本分析数据的质量和管理水平。根据《药品注册管理办法》、《药物临床试验质量管理规范》、《药物非临床研究质量管理规范》,参照国际规范,制定本指南。 第二条 药物临床试验生物样本(以下简称生物样本)是指按照药物临床试验方案的要求、从临床试验受试者采集的需要进行分析的材料(如血浆、血清、尿液、粪便、组织和细胞等)。药物临床试验生物样本分析实验室(以下简称实验室)是指对生物样本中药物、药物代谢物及生物标志物等进行分析,为药品注册申请提供数据支持的机构。 第三条 凡为提交药品监督管理部门作为药品注册数据而进行生物样本分析的实验室,均须遵循本指南,并接受药品监督管理部门的监督检查。第二章 组织机构和人员 第四条 实验室应建立完善的组织管理体系,任命实验室负责人和项目负责人,并配备相应的实验人员。隶属于药物I期临床试验研究室(以下简称研究室)的实验室,应纳入研究室的质量保证体系;独立的实验室应建立质量保证部门,并任命质量保证部门负责人。 第五条 实验室负责人应具备相关专业本科以上学历,熟悉业务,能有效组织、指导和开展实验室业务工作。对分析工作的实施和结果负责。其职责包括: (一)全面负责实验室的建设,确保实验室具有满足工作要求的各项条件。 (二)组织制定和修改管理制度、技术规范和标准操作规程;定期审阅所有管理制度、技术规范和标准操作规程文件,确保所有文件适时更新。 (三)制定主计划表,掌握各项分析工作的进展。 (四)确保质量保证工作的开展。 (五)建立有效的沟通交流机制,以保证与申办者、药物临床试验机构及研究者之间可以及时、有效地沟通。 (六)建立完善的教育培训和考核制度。 (七)在每项实验开始前,指定项目负责人,试验过程中确需更换项目负责人时,应记录更换的原因和时间,并保留相关记录。 (八)审查、批准实验方案、标准操作规程、结果或报告。 (九)指定专人负责档案资料与生物样本的管理。 第六条 质量保证部门应配备与其开展的工作相适应的人员。质量保证部门负责人的职责为: (一)负责质量保证部门的工作安排和运行; (二)审核分析实验方案、实验记录、结果或报告; (三)根据每项工作的内容和持续时间制订稽查计划并实施稽查,详细记录稽查的内容、发现的问题、采取的措施等,并向实验室负责人和项目负责人报告; (四)检查实验室环境、设施、仪器设备和档案管理等; (五)参与标准操作规程的制订和审核,并保存标准操作规程的副本。 第七条 项目负责人具体负责某项临床试验生物样本的分析工作,具备相应专业本科或以上学历,两年以上生物样本分析工作经验,能够独立进行生物样本分析方法的建立和验证,并对所承担项目的分析方法、分析结果和分析报告负直接责任。项目负责人的职责包括: (一)制订该项目的实验方案; (二)全面负责该项目的运行管理、组织实施; (三)建立并验证分析方法,撰写验证分析报告; (四)确保所有参与该项目的实验人员明确各自所承担的工作,并掌握和执行相关的标准操作规程; (五)掌握工作进展,确保实验记录及时、完整、准确和清晰; (六)确保实验中偏离方案的情况及采取的措施均有详细记录; (七)整理、分析实验数据和结果,撰写分析报告; (八)及时处理质量保证部门的报告。 第八条 实验室工作人员应符合以下要求: (一)具备严谨的科学作风和良好的职业道德以及相应的学历,经过专业培训与考核,并保存个人的培训与考核记录,具备相应的经验和能力并取得上岗资格; (二)熟悉本指南要求,掌握并严格执行相关的标准操作规程; (三)及时、完整、准确和清晰地进行实验记录,对实验中发生的可能影响实验结果的任何情况应及时报告给项目负责人; (四)对涉及保密的技术资料、受试者信息等履行其保密责任; (五)根据工作岗位的需要着装,保持工作环境正常有序,遵守健康检查制度,确保实验样本不受污染。
药物临床试验生物样本分析实验室管理规定(征求意见稿)第一章 总 则第一条 为提高临床试验生物样本分析实验室的分析质量,确保所产生的数据和结果的可靠性、完整性和科学性,根据《药品注册管理办法》、《药物临床试验质量管理规范》、《药物非临床研究质量管理规范》,参照国际通则,制定本规定。第二条 临床试验生物样本是指按照临床试验方案的要求、从临床试验受试者采集的需要加以分析的材料(如血浆、血清、尿液、粪便、组织和细胞等)。临床试验生物样本分析实验室(以下简称“实验室”)是指对临床试验生物样本中药物及其代谢物分析,以及对临床试验生物样本进行血液学、生物化学、生物物理学等学科的检测或评估,为药品注册申请提供数据支持的机构。第三条 所有经过国家食品药品监督管理局批准进行临床试验生物样本分析的实验室,均须遵循本规定。第二章 组织机构和人员第四条 实验室应建立完善的组织管理体系,任命负责人、质量保证部门负责人、分析负责人,并配备相应的实验人员。第五条 所有人员应符合以下要求:(一)具备严谨的科学作风和良好的职业道德以及相应的学历,经过专业培训,具备所承担的工作需要的理论知识、工作经验和业务能力;(二)严格履行职责,熟练掌握并严格执行与所承担工作有关的标准操作规程;(三)及时、完整、准确和清晰地进行实验记录,对实验中发生的可能影响实验结果的任何情况应及时报告;(四)对涉及保密的技术资料、受试者信息等履行其保密责任;(五)根据工作岗位的需要着装,遵守健康检查制度。第六条 实验室负责人应具备相应专业的理论知识,具备有效组织、指导和开展实验室业务工作的能力。实验室负责人的职责为:(一)负责或协调所在机构法人与申办者签订书面合同;(二)建立有效的联系机制,以保证与申办者、药物临床试验机构之间可以及时、有效地沟通;(三)建立完善的教育培训和考核制度,确保实验人员具有相应专业的理论知识、技能和经验,保存实验人员的学历资质、工作经历、专业培训以及工作性质描述等材料; (四)全面负责实验室的建设,确保实验室具有满足工作要求的各项条件;(五)组织制定和修改管理制度、技术规范和标准操作规程;(六)制定主计划表,掌握各项分析工作的进展;(七)聘任质量保证部门负责人;(八)在每项实验开始前,指定分析负责人,试验过程中确需更换时,应记录更换的原因和时间,并保留相关记录;(九)审查、批准实施方案、分析结果或分析报告;(十)指定专人负责档案资料的管理。第七条 实验室应设立独立的质量保证部门,其人员的数量应与其开展的分析工作相适应。质量保证负责人的职责为:(一)负责质量保证部门的工作安排和运行;(二)审核实施方案、实验记录、分析结果或分析报告;(三)根据每项分析工作的内容和持续时间制定稽查计划并实施稽查,详细记录稽查的内容、发现的问题、采取的措施等,并向实验室负责人和/或分析负责人报告;(四)定期或不定期检查实验室环境、设施、仪器设备和档案管理等;(五)参与标准操作规程的制定、审核标准操作规程,并保存标准操作规程的副本;第八条 每项分析工作必须指定分析负责人。分析负责人的职责包括:(一)制定该项目的实施方案;(二)全面负责该项目的运行管理、组织实施;(三)建立并验证分析方法;(四)确保所有参与该项目的实验人员明确各自所承担的工作,并掌握和执行相关的标准操作规程;(五)掌握工作进展,确保实验记录及时、完整、准确和清晰; (六)确保实验中偏离试验方案的情况及采取的措施均有详细记录;(七)整理、分析实验数据和结果,撰写分析报告;(八)及时处理质量保证部门的报告。
[font=-apple-system, BlinkMacSystemFont, &][size=18px]目前,我国多种抗新冠病毒药物完成临床前研究,进入临床试验阶段。[/size][/font]
近日,在中国心脏大会“牛津—阜外心血管病研究热点论坛”上,有学者披露,我国将参与全球大规模多中心药物临床试验,增强他汀类药物控制心血管发病风险的作用。 通过抑制胆固醇酯转运蛋白(CETP)而升高高密度脂蛋白、降低低密度脂蛋白,是在使用他汀类药物基础上力求使心血管发病风险进一步下降的新希望。然而,首个CETP抑制剂Torcetrapib因导致心血管事件的增加而提前终止。之后的医学分析发现,该抑制剂自身产生醛固酮水平增高、电解质紊乱的副作用,是导致心血管事件增加的罪魁祸首。目前,降脂强度最强的CETP抑制剂是Anacetrapib,临床3期研究显示,该抑制剂可以降低40%低密度脂蛋白,升高140%高密度脂蛋白,而对醛固酮水平、电解质均无影响,也未发现有明显副作用。 中国医学科学院阜外心血管病医院中国牛津国际医学研究中心主任蒋立新教授说,CETP抑制剂Anacetrapib研究由牛津大学设计并组织实施,即将在全球范围内遴选医疗机构开展大规模多中心临床试验,该试验将入选3万名高危心血管疾病患者,而中国作为重要参与者,将入选9400名患者,整个计划预计持续4年。 蒋立新介绍,中国牛津国际医学研究中心负责中国区域实施,目前已基本确定协作单位80余家,登记病人近万名,预计今年年底正式启动该研究
中药临床试验申报资料中存在的问题SFDA药品审评中心审评一部许青峰一、对药品注册临床要求的理解: 总体要求、分类要求、受试例数二、试验常见问题试验设计、安全性数据总结分析三、对药品注册临床要求的理解(一)总体要求1、药物临床研究必须经国家药品监督管理局批准后实施,必须执行《药物临床试验质量管理规范》(GCP)2、药物的临床研究包括临床试验和生物等效性试验。3、申请新药注册、应当进行临床试验和生物等效性试验,申请已有国家标准的药品注册(仿制药),一般不进行临床研究,需用工艺和标准控制药品质量的中成药,应当进行临床试验。4、临床试验分为Ⅰ、Ⅱ、Ⅲ、Ⅳ期。申请新药注册应当进行Ⅰ、Ⅱ、Ⅲ期临床试验。有些情况下可仅进行Ⅱ期和Ⅲ期。或者Ⅲ期临床试验。5、药物临床研究的受试例数应当根据临床研究的目的,符合相关统计学的要求和本办法所规定的最低临床研究病例数要求。
2010年回顾之九,临床试验失败录 http://img2.jiansuo.net/blog/upload/74/75/t_51484.jpg http://www.dxyer.cn/images/zoomin.gif 2010年大药厂经历不少重大临床试验失败或挫折(健康博客)新药研发处处有风险,过临床试验一期,也许比例最高,但进入临床II和III时,风险就明显加大.尤其在FDA提高对新药审批的门槛,对安全和疗效优越性特别看重时,药厂的临床试验就需要精心设计,必须拿出过硬数据,否则FDA拒绝批准可能性很大,至少会要求补充更多临床试验数据,拖延额二年以上时间.在过去的一年中,我们既看到让人鼓舞的临床研究进展和21种NCE新药上市,同时也看到不少令人可惜和遗憾的临床后期失败或重大挫折,在以下的失败产品名录中,不乏有曾经抱很大希望,甚至很有可能成为重磅药. 有的项目真的很可惜,比如罗氏德糖尿病药,临床效果比默克的药还好,就是因为安全因素,需要重新考虑新剂量,估计未来凶多吉少. 阿斯利康与雅培合作开发复方药,并不是完全没戏,但因为最佳上市时机错过,从商业角度考虑,只能放弃.所有这些项目的失败对这些大药厂打击很大.裁人成了减少损失的必然选择.临床试验失败之后,礼来决定结束糖尿病新药, 10月阿斯里康终止骨质疏松药开发项目,核销4.4亿研发损失 12月礼来皮肤癌药物III期临床试验受挫 患者死亡后期试验停止12 月 因为临床IIb失败,西雅图遗传公司放弃AML新药开发 9月罗氏阿瓦斯丁治疗胃癌临床III期失败 2月,临床效果欠佳,辉瑞终止骨关节疼抗体药研发项目 6月礼来老年痴呆药物 semagacestat临床试验失败 8月 诺华在二度遭遇临床III失败后,被迫放弃肺癌ASA404药物开发项目 11月辉瑞因III期临床试验年老年痴呆药 Dimebon失败而放弃 3月罗氏糖尿病新药taspoglutide因为有高血压风险被迫延迟申报甚至放弃 6月葛兰素发现其收购的新药临床试验疗效很弱,肾毒风险大而彻底放弃 12月强生/阿斯利康由于安全因素终止双方合作项目 12月FDA拒绝批准强生与其合作伙伴合作开发的抗生素ceftobiprole 1月因被FDA拒绝,错失商机,阿斯利康决定放弃与雅培合作开发的降血脂复方药 12月评论: 做新药研发,临床试验风险很大, 国内很少有公开报道和承认新药临床试验失败的消息, 究竟是我们的临床试验百发百中, 还是为了保护民族工业, 让效果一般的新药过关? . 如果未来还是这样的局面,那说明国家的钱被大忽悠了. 老百姓就更被蒙了.
药物作为一种特殊物品,在上市之前要进行一系列的安全性和有效性的考察。你知道疫苗怎么做临床试验吗?
3月25日,由南开大学药学院团队自主研发的化药1类新药CP0119片取得国家药品监督管理局签发的《药物临床试验批准通知书》,获准用于治疗结肠慢传输的临床试验。该项目是南开大学作为申报单位的第二项获得临床批件的新药项目,团队曾在2017年获批了南开大学首个新药临床批件。流行病学调查结果显示,我国结肠慢传输发病率达7.3%~20.39%,且近年来发病率呈逐年上升趋势,严重影响患者生活质量,损害患者身心健康,而且可能引发多种严重并发症。现有治疗方法主要分为基础治疗和药物治疗,基础治疗包括调整生活方式和认知治疗,经过4-8周的基础治疗无效可选用药物治疗。但目前现有的治疗手段与治疗效果存在局限性,可选用的治疗方法常常不能令人满意,结肠慢传输的治疗仍然具有挑战性。因此,研发一种高效低毒的治疗药物具有重要意义。[align=center][img=,600,598]https://img1.17img.cn/17img/images/202404/uepic/f56ec165-88cb-40a1-854c-0c4d27555528.jpg[/img][/align][align=center]CP0119靶向Transgelin治疗结肠慢传输性便秘的作用机制[/align]基于此,南开大学药学院院长领衔成立了CP0119创新药物研发团队,项目负责人为周红刚、孙涛和杨光教授。据项目负责人介绍,CP0119是一种新型小分子胶转蛋白(Transgelin)激动剂,Transgelin是钙调蛋白家族中的一种肌动蛋白结合蛋白,相对分子量为22 kDa,主要分布于平滑肌细胞中。同时,CP0119能够激动肠道平滑肌细胞上的Transgelin,促进G激动蛋白(G-actin)向F激动蛋白(F-actin)的聚集,增加肠平滑肌细胞中应力纤维束的形成,进而增强细胞收缩能力,促进肠道蠕动,最终达到改善结肠慢传输的效果。目前没有以Transgelin为靶点治疗便秘的同类药物上市,CP0119的成功开发属于全新靶点的化药1类创新药物。项目骨干艾笑羽副教授和谷小婷老师主要负责推动项目的临床前研究工作。该项目历时4年完成了原料药的中试放大、制剂开发、系统化药理和药代研究以及标准化临床前GLP安全性评价,充分证明了CP0119质量可控、安全有效。因此,CP0119的开发有望成为结肠慢传输患者的新治疗选择,具有较高的经济效益和社会效益。该项目成果还得到了天津医科大学总医院消化科王邦茂主任等临床专家的高度评价。CP0119项目的研发由南开大学药学院和药物化学生物学全国重点实验室(全重)的创新药物研发团队承担,也是与华润医药中国医药研究开发中心和天津国际生物医药联合研究院合作的重要成果,是践行产学研和全重共建单位之间合作的实例。在国家大力发展新质生产力和鼓励高校科研成果转化的大背景下,CP0119片临床试验的成功获批,不仅进一步助力南开大学创新药物研发能力,同时也对培养我校创新药学人才和助力健康中国建设具有重要意义。[来源:南开大学][align=right][/align]
[color=#444444]因为临床试验样品分析这块经常出问题,所以年后领导决定本公司内部建立临床样品分析组,对本公司临床试验生物样品中的药物浓度进行检测,不再委托第三方。我想问下,这样可以吗,建立的实验室是否需要什么资质认证?法规有没有明确的规定?如果没有规定的话,是否存在潜规则啊?[/color]
1、注册分类5和6缓控释制剂如何进行临床研究问题?答:如属于注册分类5的产品,如果参比制剂(如:缓释片)与新开发制剂(如:缓释胶囊)具有相同释放特点(如:同属24小时缓释),则可仅进行单次给药的生物等效性研究。否则,需完成单次、多次给药的药代动力学比较研究和不少于100对的临床试验。属于注册分类6的产品,参比制剂必须选择相同释放特点的被仿产品,进行生物等效性研究。2、属于注册分类5的脂质体品种,已做药代动力学研究,100对临床是否足够?答:具体问题具体分析。在药代动力学特点变化比较大的情况下(如因粒度而致分布有很大变化可能导致安全有效性的变化),应完成的临床研究就不仅仅限于100对的验证性研究。可能需要完成Ⅰ-Ⅲ期的所有研究。 3、分散片是否属于速释制剂,是否需要按特殊制剂进行临床研究。答:多数分散片的开发依据为较普通片剂释放快,但实际的生物等效性研究结果显示与普通片剂生物等效,因此目前并未将分散片按速释剂型看待。 4、关于如何考虑开发提高生物利用度的产品?答:有些已上市产品其口服的生物利用度较低,申报单位以提高生物利用度为目的开发新的产品。对此,应首先考虑原产品是否为安全有效的药物,如果是,则应针对新开发产品的特点降低临床用药剂量,至于降到多少合适,则需要进行生物利用度比较研究、生物等效性研究乃至临床试验加以确认。 5、对Ⅱ期临床研究中探索剂量时病例数的要求,是否三个剂量组都需要做100例?答:Ⅱ期临床研究本身为探索性研究,需要进行多个试验,目前对某一个试验中各组的病例数并无统一要求,实验设计前需要进行深入的文献调研,综合考虑药品的适应证、剂量、用药周期、治疗窗的情况和是否得到统计学的差异综合考虑后确定。 6、注册分类6药物,哪些应进行生物等效性研究?答:就注册分类6药物哪些应进行生物等效性研究问题,请参照《药品注册管理办法》附件二化学药品注册分类及申报资料要求中“五、临床试验要求”的相关技术要求。 7、注册分类6药物,如儿童用药,是否可以基于伦理考虑免做生物等效性试验?答:注册分类6研究药物,如系儿童用药,可能基于伦理考虑不适于在儿童人群进行生物等效研究,但生物等效性研究的目的在于考察制剂的质量,该类研究可以在健康成人志愿者人群中进行。
11月11日晚,食药总局终于使出了杀手锏,第一次曝光了涉嫌临床试验数据造假的八家企业名单,并表示对其涉及的11个药品注册申请不予批准。 “其实对于上述处罚,医药企业并不害怕,他们现在都与临床试验机构互相推诿责任。”一位业内人士向记者透露,医药企业真正害怕的是食药总局的“三年禁令”。“不能申报新药,企业如何发展、业绩如何保证,尤其是上市公司。”他说。 药企最怕“三年禁令” 国家食药总局相关人士对记者表示,这11个药品注册申报资料的临床试验数据存在擅自修改数据、瞒报数据以及数据不可溯源等涉嫌弄虚作假问题。“食药总局下一步还将继续开展临床试验数据现场核查工作。”他说。 药物临床试验是指任何在人体(病人或健康志愿者)进行的药物的系统性研究,以证实或发现试验药物的安全性和有效性。药物临床试验一般分为Ⅰ、Ⅱ、Ⅲ、Ⅳ期临床试验。 食药总局相关人士表示,将在查清事实的基础上,明确注册申请人、药物临床试验机构和合同研究组织的相关人员的责任,涉及医疗机构的相关责任人由卫生计生部门处理,涉嫌犯罪的移交公安机关。 食药总局之前称,对核查中发现临床试验数据真实性存在问题的相关申请人,三年内不受理其药品申请。将弄虚作假的申请人、临床试验机构、合同研究组织以及相关责任人员等列入黑名单。弄虚作假的直接责任人参与研究或组织研究的临床试验资料十年内不予受理。 制剂出口巨头华海药业中枪 记者12日分别致电上述企业。华海药业相关人士表示,公司正在研究出问题的环节,可能是临床试验机构的问题,不是企业的问题。“至于出口制剂是否存在临床数据造假问题,我们没有收到任何信息”。 作为我国知名制剂出口企业华海药业在此次事件中也中枪。食药总局称,华海药业坎地沙坦酯片原始记录缺失、分析测试系统无稽查轨迹、试验用药品未留样、部分图谱真实性高度存疑,甚至隐瞒弃用试验数据、修改调换试验数据。 今年8月,华海美国和普洛康裕签署战略合作协议,双方将展开化学原料药及制剂产品在美国市场的业务合作。目前,该公司有30多个ANDA申请文号,预计未来每年有5至10个ANDA 文号获批,海外制剂业务将长期受益。 华海药业三季报显示,公司2015年前三季度实现营业收入24.21亿元,同比增长34.09%;实现归母净利润3.35亿元,同比增长65.73%。中国证券金融股份有限公司持股1646.28万股,占比2.08%;中央汇金投资有限责任公司持股1177.33万股,占比1.65%。 华海药业指出,上述增长归结于原料药和中间体业务营收稳定增长,前三季度实现营业收入约14.53亿元,同比增长约30%,主要是沙坦类产品和神经类产品销售大幅增长。而国际制剂业务营收大幅增长,制剂业务实现营业收入约9.68亿元,其中国际制剂业务同比增长43%,预计全年制剂业务有望增长40%左右。 八家企业宽限期内未主动撤回申请 记者了解到,食药总局清理临床数据造假行动是从7月22日开始,食药总局副局长吴浈明确表态“药物临床试验中的问题是比较严重的,不规范、不完整的问题非常普遍,不可靠、不真实、弄虚作假的问题确实存在,已经严重影响了药品审评审批的正常进行,严重干扰了上市药品有效安全的科学评价,严重破坏了审评审批的正常秩序。” 随后,食药总局出了一份企业核查清单,医药界哗然了。自查核查品种清单1622个受理号中,进口有171个受理号,新药948个受理号,已有国家标准503个受理号。受理号中有309个受理号分别属于国内103家医药类上市公司,包括华海药业、恒瑞医药(51.16, 0.00, 0.00%)等国内外制药龙头企业。其中,化药需要自查1283个受理号,占79.1%,中药大多是2005年至2006年的受理号,共237个,占14.6%。生物制品共102个受理号。 “我们非常重视这个事情,董事长、总经理全部开会研究。”国内一家知名研发企业副总告诉记者。另一家上市药企老总说,公司有6个品种在名单上,现在已经撤回了3个药品申请。 为了给予药企业充分的自查时间,食药总局给出了一个多月的宽限期,允许企业自动撤回有问题的申请。8月28日,食药总局公布,此次自查结果中,申请人提交自查资料的注册申请为1094个,占 67%;主动撤回的注册申请317个,占20%;申请减免临床试验等不需要提交的注册申请193个,占12%。但上述八家企业的11个品种并不在企业主动撤回之列。 土豆点评:这个发现数据涉及造假,是在审查资料的时候发现啊?还是去现场进行注册核查的时候发现的啊?现场注册核查是不是开始严格查电子数据的真实性了?
化学药临床试验申报资料中存在的问题卓宏目录:一、临床研究在新药开发过程中的地位二、临床研究的基础三、临床研究的必要条件四、临床研究的定义及内容五、各类新药临床研究的要求六、各期临床试验的目的七、临床研究应注意问题一、临床研究在新药开发过程中的地位临床前研究:化学合成,动物试验临床研究:Ⅰ期临床、Ⅱ期临床、Ⅲ期临床上市:Ⅳ期临床二、临床研究的基础1、药学基础2、药理毒理基础3、临床方案设计的基础考虑:有动物试验依据,可根据国外资料、文献,适应症不超出已上市的范围,安全性要注意动物试验结果及常规试验。
新华社悉尼12月11日电(记者赵小娜)澳大利亚研究者日前表示,他们对一种白血病新药的试验显示出较好的初步效果,有20%的患者血液中已检测不到癌细胞,这种新药有可能为白血病患者带来治愈希望。 据当地媒体报道,慢性淋巴细胞性白血病是澳大利亚最常见的白血病类型,对这种病一直缺乏有效的治疗方法。澳大利亚“沃尔特与伊丽莎?霍尔医学研究所”经数年研究开发出了这种代号为ABT-199的新药,目前正在墨尔本两家医院对数十名患者进行临床试验。 研究人员康宁·塔姆博士说,经过一年半的试验,有20%的患者血液中已检测不到癌细胞。他说,之前很多患者对化疗和其他治疗方法没有任何积极反应,只能任病情恶化,而“新药完全改变了这一现状”,患者有望恢复健康重回正常生活。 塔姆博士表示,这种药物上市销售还需几年时间,但对愿意参与试验的患者,研究者现在即可提供这种药物。(完)
[color=#c00000][i]同济大学附属东方医院再生医学研究所何志颖研究员表示:项目研究从2018年开始,2021年4月Pre-IND,2024年1月18日IND获批!历时6年艰辛。[b]这是东方医院首个干细胞成药临床试验项目,希望能造福于心衰患者![/b][/i][/color]据报道1月18日,天士力公告其一款创新干细胞药物获得国家药监局批准进入临床试验,主治慢性心力衰竭。公告称,公司收到国家药监局核准签发关于[b]人脐带间充质干细胞注射液(B2278注射液)[/b]项目的《药物临床试验批准通知书》,同意开展伴冠状动脉旁路移植术指征的慢性缺血性心肌病导致的慢性心力衰竭的临床试验。[b]人脐带间充质干细胞注射液[b](B2278注射液)[/b]由上海市东方医院(同济大学附属东方医院)研发,2022年8月天士力与东方医院签署《技术转让(合作)合同》受让相关技术及成果,并在全球范围内,优先在中国开展药品注册申报及后续临床试验开发。[/b]临床前研究证明,B2278注射液可通过旁分泌作用调控心肌组织微环境,对于缺血性心肌病中的心肌细胞组织损伤有明显抑制作用,增加动物心功能,促进血管再生,减少心肌凋亡。心力衰竭是由于心脏结构和/或功能异常导致心室充盈和/或射血能力受损的一组临床综合征,是大部分心血管疾病发展的最终阶段,随着年龄增长,心衰患病率和发病率均明显增加。目前对于心力衰竭的治疗主要包括药物治疗、血运重建、细胞和基因治疗,其中冠状动脉旁路移植术(CABG)是常用的血运重建治疗方式,《2022年中国心血管外科手术和体外循环数据白皮书》显示,2022年CABG占心外科手术总量21.1%。上述治疗手段可以在一定程度上延缓心力衰竭的进展,但不能使死亡心肌再生。伴随CABG手术的心肌局部注射干细胞有望通过刺激心脏细胞的增殖和分化、抑制心肌细胞损伤及免疫调节等作用,修复心肌细胞使心肌收缩增强从而对心力衰竭发挥治疗作用。目前国际上获批的干细胞品种已达十余种,但是尚无治疗心衰的干细胞产品上市。[来源:仪器信息网] 未经授权不得转载[align=right][/align]
中国科技网讯 加拿大一个临床医学研究小组证明,由克里姆比尔神经医学中心迈克尔·泰米安斯基博士研发的一种神经保护剂药物可有效保护大脑减轻中风损伤效应。试验成果在线发表于10月9日《柳叶刀·神经医学》网站上,同时预测该中风药物成效的实验研究成果亦同步发表在《科学·转化医学》杂志上。 该项具有里程碑意义的临床试验,由卡尔加里大学霍奇基斯脑研所迈克尔·希尔博士领导,是一次随机、双盲、由加拿大和美国多个研究中心参与的试验。该研究评估了NA-1药物对曾接受神经介入治疗脑动脉瘤而引发轻微中风的患者的疗效。动脉瘤患者在接受此种介入治疗后,90%以上的患者会出现缺血性中风,但通常并不会引起明显的神经性伤残。 在试验中,受试者被随机抽取接受Tat-NR2B9c或安慰剂治疗。结果表明,接受Tat-NR2B9c治疗的患者,因脑动脉瘤修复术后造成的大脑损伤程度有所下降。该药物在脑动脉瘤破裂患者身上也取得了良好的临床试验效果。而在安慰剂对照组中,只有68%的患者取得了较好的效果。 希尔博士表示,为研发此类药物,人们此前已做过成千次的尝试,但最终均未能成功地将实验室里的成果转化到人体上。该临床试验成果是中风研究的一次飞跃。泰米安斯基博士认为,此次试验首次证明了,以提高大脑对中风抵御能力而设计的这种药物,在人体中展现了降低中风损伤效应的功效。此次临床试验也为血管性痴呆症等其他脑损伤的治疗提供了借鉴。(冯卫东) 《科技日报》(2012-10-16 二版)
食品安全一直广受诟病!如果我们对其有临床实验的要求,严格监管控制,那我们还会如此担心食品安全吗?先前我们都佩服先吃螃蟹的人,从结果上来看,我们知道螃蟹很美味。但从科学的角度来讲并不是每个人都适合吃,螃蟹是凉性,女性朋友最不宜常吃,影响意义深远哦!而销售商没有必要的提示,只宣传其美味而不顾对女性之不良影响。田螺一样美味,但寄生虫不可忽视。还有非洲人吃大腥腥使人类得了艾滋。以上事例都给我们带来严重后果,确实是这样,不是能吃的食品就无毒。是药三分毒大家都知道,所以有临床志愿者为我们实验。作一种未知的尝试。以上实例等同于我们的实验志愿者,以临床发现为我们发现问题而提供依据。我们现在发现N多种通过转基因或是其他技术而生产我们未知食品,依人群喜好而变种,这样的风险有多大!是否应该建立临床实验数据而被广泛食用才对!
我们实验室主要进行的是中兽药的临床试验,包括靶动物安全性、药效评价试验(Ⅱ期临床)、药效评价田间试验(Ⅲ期临床试验、临床验证试验),现在想要申请CNAS,之前查看了一些相关的认可资料和已获CNAS认可的机构的认可资料,但有些问题仍不太明白,不知如何下手?请大家指点一下。1.CNAS对人员的社保有要求吗?我们实验室的研发人员属于同一个集团,但社保缴纳在不同的全资子公司,这次申请CNAS我们想以其中一个子公司(暂定为A)的名义申请。2.仪器设备采购也与人员一样的情况,有一部分仪器是由集团统一采购的,从固定资产角度来说不属于A.3.兽药的药效评价试验涉及到如下环节:动物给药处理、采样动物组织样本、检测、根据各自指标得出兽药的有效性的结论,CNAS涵盖的范围是“检测”这一个环节,还是从动物给药处理到得出结论整个流程呢?4.检测参数方面,目前我了解的检测参数是根据检测标准来确定的,我看到比较多的是以“动物血清”为对象,以“胆固醇”为参数,但是,这样的话就会需要太多的参数,我们想以“中兽药”为对象,以“治疗鸡大肠杆菌病的药物临床试验”为参数,是不是只要找到了对应的标准,这种也可以成立?
[center]美国CUPID首项基因治疗临床试验结果喜人[/center]近日,在美国新奥尔良召开的美国心脏协会(AHA)科学大会上,研究人员公布了CUPID试验的Ⅰ期临床试验结果。CUPID试验是由美国13家医疗单位共同参与的一项随机、双盲、安慰剂对照、平行分配设计的Ⅰ/Ⅱ期临床试验,预计将纳入46名晚期心力衰竭患者;此项研究同时也是应用基因替代技术治疗晚期心力衰竭的首项临床试验。 众所周知,钙离子是肌肉收缩的关键影响因素。肌浆网钙ATP酶(SERCA)亦被称为肌浆网钙泵,是参与钙离子调节的主要蛋白;而SERCA2a主要存在于心肌和骨骼肌慢肌纤维中,其功能是ATP依赖性地逆浓度梯度将钙离子由胞浆排入肌浆网内,促进心肌舒张。大量研究表明,在衰竭的心肌细胞中,SERCA2a活性及其mRNA表达量均明显下降,心衰部位心肌SERCA2a表达量较正常心肌降低30%左右;动物实验显示,将SERCA2a基因转导到衰竭的心肌后,SERCA2a活性及其表达量明显增加,心功能指标明显改善。由此可知,心肌SERCA2a的减少与心力衰竭的进程之间存在明显相关性。 因此,许多研究机构开展了应用SERCA2a基因转导技术治疗晚期心力衰竭的研究。MYDICAR是Celladon公司开发的一种用于治疗晚期心力衰竭的基因靶向酶替代治疗药物,是一种由1型腺相关病毒(AAV1)壳体与人SERCA2a cDNA共同组成的重组病毒载体系统。这种药物经导管在左心室前壁及侧壁注射后,可将SERCA2a基因转移至体内,增加心肌中SERCA2a的表达,改善和恢复心脏功能。 在这次Ⅰ期临床试验中,9名心力衰竭患者接受了MYDICAR治疗。其中7名在6个月内出现不同程度的病情好转,包括:有5名患者症状获得改善,有4名患者机体功能得到改善,有2名患者生物标记物指标得到改善,有6名患者左心室功能或左室重构获得改善。另外2名患者因体内已经存在病毒载体的抗体,因而病情未出现好转。更为重要的是,MYDICAR在试验中表现出较好的安全性,获得了负责评估该试验的安全委员会及研究者的肯定。 目前,CUPID试验中的Ⅱ期临床试验已经开始招募受试者,它将对MYDICAR治疗晚期心力衰竭病人的安全性和有效性作出进一步的评价。信息来源:医药经济报
多年来临床检验质量一直是检验工作者关注的核心问题,如何做好临床实验室的质量管理,特别是在与国际临床实验室质量管理模式接轨的同时,提出适合于我国经济发展现状、适合我国国情的实验室基本资格要求、适用于不同级别临床实验室的质量管理方案已成为我们面临的重要任务。 根据国际标准化组织ISO 15189:2003《医学实验室-质量和能力的专用要求》中的定义,以诊断、预防、治疗人体疾病或评估人体健康提供信息为目的,对取自人体的材料进行生物学、微生物学、免疫学、化学、血液免疫学、血液学、生理学、细胞学、病理学或其它检验的实验室统称为临床实验室(以下简称实验室),也称之为医学实验室。针对临床实验室质量管理,一些发达国家和国际组织已经出台了一些法律和标准供我们借鉴。美国国会于1967年就通过了专门针对临床实验室质量管理的法律,即临床实验室改进法案(Clinical Laboratory Improvement Act 1967,简称CLIA 67)。在实行此法案20年后,1988年又通过了对CLIA 67的修正案临床实验室改进法案修正案(Clinical Laboratory Improvement Amendment 88,简称CLIA 88),并于1992年正式实施。法国政府也于1999年11月26日发布了NOR:MESP9923609A《关于正确实施医学生物分析实验的决议》。1999年,国际标准化组织制订了医学实验室的管理标准,即ISO 15189《医学实验室-质量和能力的专用要求》。目前国际上对临床实验室的质量管理主要分为以CLIA 88为代表的法律文件和ISO发布的推荐标准两种形式。ISO 15189主要强调实验室内部质量体系的建立,在此基础上建立的实验室认可制度是一种自愿行为,是实验室质量保证的较高标准;CLIA 88着眼于政府对临床实验室质量的外部监控,是政府对实验室强制执行的资格要求,两者存在互补性。这些文件对我们制定临床检验质量保证方案提供了很好的参考作用。
【序号】:1【作者】: 彭朋元唯安胡薏慧【题名】:载药医疗器械临床试验质量控制要点【期刊】:药物评价研究. 【年、卷、期、起止页码】:2021,44(02)【全文链接】:https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CJFD&dbname=CJFDLAST2021&filename=YWPJ202102007&uniplatform=NZKPT&v=rN02X8_as4SvGbMhBnHoiLNembr77XHnzUEZj_uYmgzp0lXDalaFhOSxcGcSttlk
由细菌、病毒、支原体、衣原体等多种病原微生物所致的感染性疾病遍布临床各科,其中细菌性感染最为常见,因此抗菌药物也就成为临床最广泛应用的药物之一。在抗菌药物治愈并挽救了许多患者生命的同时,也出现了由于抗菌药物不合理应用导致的不良后果,如不良反应的增多,细菌耐药性的增长,以及治疗的失败等,给患者健康乃至生命造成重大影响。抗菌药物的不合理应用表现在诸多方面:无指征的预防用药,无指征的治疗用药,抗菌药物品种、剂量的选择错误,给药途径、给药次数及疗程不合理等。为提高细菌性感染的抗菌治疗水平,保障患者用药安全及减少细菌耐药性,特制订《抗菌药物临床应用指导原则》(以下简称《指导原则》)。《指导原则》对感染性疾病中最重要的细菌性感染的抗菌治疗原则、抗菌药物治疗及预防应用指征以及合理给药方案的制订原则进行阐述,并列出常用抗菌药物的适应证及注意事项,各种常见细菌性感染的病原治疗,以期达到提高我国感染性疾病的抗菌治疗水平,减缓细菌耐药性的发展,降低医药费用的目的。《指导原则》共分四部分,一是“抗菌药物临床应用的基本原则”,二是“抗菌药物临床应用的管理”,三是“各类抗菌药物的适应证和注意事项”,四是“各类细菌性感染的治疗原则及病原治疗”。对上述内容有以下几点说明。1、本《指导原则》为临床应用抗菌药物获取最佳疗效,并最大程度避免或减少不良反应而制定,不是教材或参考书,也不涉及具体的给药方案。2、本《指导原则》主要限于治疗细菌、支原体、衣原体、立克次体、螺旋体、真菌等病原微生物所致感染性疾病的抗菌药物,不包括各种病毒性疾病和寄生虫病的治疗药物。3、本《指导原则》中抗菌药物临床应用的基本原则在临床治疗中必须遵循,各类抗菌药物的适应证和注意事项以及各种感染的病原治疗则供临床医师参考。4、为加强对抗菌药物临床应用的管理,本《指导原则》对抗菌药物应用中的管理也提出了要求,应当遵循。5、本《指导原则》仅涉及国内临床常用抗菌药物的部分品种,重点介绍各类药物的抗菌作用、适应证和注意事项,有关抗菌药物临床应用的详细内容仍应参考有关专业书籍。6、本《指导原则》中涉及临床各科部分常见和重要的感染性疾病,其他未涉及的感染仍应参考有关专业书籍。7、在医疗工作中临床医师仍应结合患者具体情况,制订个体化给药方案。8、“病原治疗”中除本《指导原则》所列通常选用的药物品种外,临床医师可根据患者临床情况、细菌耐药性及当地药物供应情况选用最合适的抗菌药物。
[font=&][size=16px][color=#333333]中国生物微信公号4月24日消息,今日,由国药集团中国生物研究院研发的重组新冠病毒疫苗Ⅰ/Ⅱ期临床试验在河南商丘启动。4月9日,中国生物研究院基因重组新冠疫苗获得国家药品监督管理局临床试验批件,成为中国生物第三个获批临床的新冠疫苗,唱响了全球首家三重奏。[/color][/size][/font]
由细菌、病毒、支原体、衣原体等多种病原微生物所致的感染性疾病遍布临床各科,其中细菌性感染最为常见,因此抗菌药物也就成为临床最广泛应用的药物之一。在抗菌药物治愈并挽救了许多患者生命的同时,也出现了由于抗菌药物不合理应用导致的不良后果,如不良反应的增多,细菌耐药性的增长,以及治疗的失败等,给患者健康乃至生命造成重大影响。抗菌药物的不合理应用表现在诸多方面:无指征的预防用药,无指征的治疗用药,抗菌药物品种、剂量的选择错误,给药途径、给药次数及疗程不合理等。为提高细菌性感染的抗菌治疗水平,保障患者用药安全及减少细菌耐药性,特制订《抗菌药物临床应用指导原则》(以下简称《指导原则》)。《指导原则》对感染性疾病中最重要的细菌性感染的抗菌治疗原则、抗菌药物治疗及预防应用指征以及合理给药方案的制订原则进行阐述,并列出常用抗菌药物的适应证及注意事项,各种常见细菌性感染的病原治疗,以期达到提高我国感染性疾病的抗菌治疗水平,减缓细菌耐药性的发展,降低医药费用的目的。《指导原则》共分四部分,一是“抗菌药物临床应用的基本原则”,二是“抗菌药物临床应用的管理”,三是“各类抗菌药物的适应证和注意事项”,四是“各类细菌性感染的治疗原则及病原治疗”。对上述内容有以下几点说明。1、本《指导原则》为临床应用抗菌药物获取最佳疗效,并最大程度避免或减少不良反应而制定,不是教材或参考书,也不涉及具体的给药方案。2、本《指导原则》主要限于治疗细菌、支原体、衣原体、立克次体、螺旋体、真菌等病原微生物所致感染性疾病的抗菌药物,不包括各种病毒性疾病和寄生虫病的治疗药物。3、本《指导原则》中抗菌药物临床应用的基本原则在临床治疗中必须遵循,各类抗菌药物的适应证和注意事项以及各种感染的病原治疗则供临床医师参考。4、为加强对抗菌药物临床应用的管理,本《指导原则》对抗菌药物应用中的管理也提出了要求,应当遵循。5、本《指导原则》仅涉及国内临床常用抗菌药物的部分品种,重点介绍各类药物的抗菌作用、适应证和注意事项,有关抗菌药物临床应用的详细内容仍应参考有关专业书籍。6、本《指导原则》中涉及临床各科部分常见和重要的感染性疾病,其他未涉及的感染仍应参考有关专业书籍。7、在医疗工作中临床医师仍应结合患者具体情况,制订个体化给药方案。8、“病原治疗”中除本《指导原则》所列通常选用的药物品种外,临床医师可根据患者临床情况、细菌耐药性及当地药物供应情况选用最合适的抗菌药物。
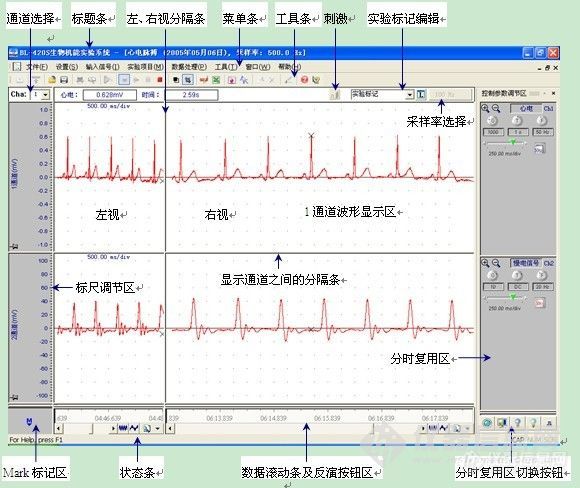
好像记得有这么句格言:“ In life, constantly having to leave or enter. So, see, unseen; remember, forgotten. Life, and constantly have to be lost. Then, invisible, see; forgotten, remember. However, unseen, is it right? Was equal to does not exist? Remember, is it right? It will never disappear? ”(“生命中,不断地有离开者或进入者。于是,看见的,看不见的;记住的,遗忘了。 生命中,不断地有得到和失落。于是,看不见的,看见了;遗忘的,记住了。 然而,看不见的,是不是就等于不存在?记住的,是不是永远不会消失?”) 也许,面对实验,论坛上的老师们经验都很丰富,也许,老师们都说做实验有什么恐惧,有什么悲伤呢?是的了,各位老师说的是对的,不应该有啥子恐惧和悲伤,毕竟就是做实验。也许这就是所谓的‘整个自然界就是一场强弱之间的壮烈较量,是强者战胜弱者的永恒胜利’。俺的第一次实验简直是太多太多,第一次做光谱,俺没有恐惧过,俺也和各位老师一样,顺顺利利做完了实验……;第一次做色谱,俺也没有恐惧过,还是顺顺利利做完了实验……;唯独第一次做动物活体解剖实验——离体心脏灌流实验让俺感到了恐惧和悲伤,也许各位老师不以为然,可是俺恐惧过,害怕过,看到一个个活奔乱跳的大白鼠的被实验师用那锋利的手术刀活体解剖,取下心脏做药物离体心脏灌流的实验。第一次看到导师和实验师做这个实验的时候,俺心里一阵恶心,一种揪心的疼痛,五味杂陈的感觉加上一阵眩晕,当时的心情真的不好受(其实,本科阶段看过实验老师做过大白兔的采血等实验,还好,因为,白兔实验完毕后还可以存活。但是这次活生生的取下内脏器官做实验,大白鼠就会在突然间活生生的心脏被从身体里摘除下来,立马老鼠就会失去生命,尽管离体的心脏可以在灌注机子上存活几个小时,但是毕竟这只心脏已经不属于它了,被从它身体里掏出来了),导师用坚毅的目光直视着俺,像是鼓励,又像是不解……每次实验阶段都要做好多大白鼠,那些可怜的大白鼠就在实验台上永远的消逝了。下面分享几张简单实验的照片(解剖后的图片有点血腥了的,就不上图了)http://ng1.17img.cn/bbsfiles/images/2012/08/201208051757_381650_2355529_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208051758_381651_2355529_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208051758_381652_2355529_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208051758_381653_2355529_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208051758_381654_2355529_3.jpg 机能仪器电脑屏幕显示 还记得有句英语格言说:“Five stages of grief. Denial, anger, bargaining, depression, and acceptance”.(悲痛有五个阶段:拒绝,愤怒,自欺欺人,消沉,接受。)格言说的多好呀,人的悲痛有五个阶段,这里的悲痛也许就是心理斗争,绝对的心理斗争,第一次看到活体生理机能机实验的时候,俺就是恐惧和悲痛,从内心深处产生了拒绝,愤怒,然后就是自欺欺人,回想实验和导师的目光,俺只能用阿Q精神鼓励自己,然后就是几天的消沉,最后就是默默接受,默默的看着导师和实验师们每天在那里做活挖心脏的实验,时间久了,也就接受了,这里的接受就是接受了导师和实验师们的实验过程,俺只是个助手,助手必须慢慢习惯,慢慢接受,慢慢学习会。 说真的,俺找过导师,和导师交流过,俺想做和动物试验无关的课题,可导师就是不同意,说没有新意,必须做动物试验,因为这个也是药物临床前重要试验阶段,对药物的各方面的研究较细,如药物的血药浓度、药物的相互作用、药物的药理毒理等方面的研究,这些临床前的研究工作都是来自于动物试验,没有试验动物数据的可靠性和稳定性,我们就不能进行一期临床试验,药物也就不能进行二期临床试验等。离体动物心脏灌流装置可用于Langendorff灌流,适用于大鼠、豚鼠、兔等哺乳类小动物心脏。它能够保证恒压、恒温环境,从而保持离体心脏的生理活性,使相关实验顺利进行。可用于观察药物对哺乳类动物离体心脏活动影响,并可测定动物心脏冠脉流量、左室内压、心率、心电等相关指标的变化。并且该仪器和实验现在国内做的不多,比较容易出成绩,除了服从,俺还是服从,尽管俺恐惧做那个实验,也为那些大白鼠感到悲伤,还是接受了现实…… 7月20日,那个值得俺纪念的日子,哪天俺做了第一次大鼠活体心脏摘除试验,面对活奔乱跳的大白鼠,俺还是有点懵。先是把大白鼠从笼子中取出,打上抗凝剂肝素钠,然后给大白鼠腹腔注射乌拉坦进行轻微麻醉,待大白鼠麻醉后,就把它绑在试验板上。拿起手术剪刀,俺还是不敢动手,虽然已经接受了这个现实,但是自己动手做的时候还是恐惧,害怕,导师这次没帮忙,实验师也在那里看着,用鼓励的目光鼓励俺,俺看到大白鼠躺在实验台上,俺充满了恐惧感,又那么无助,可是还是在无奈的心情下狠心拿起了止血钳和手术剪,每剪一次,就能感受到大白鼠撕心裂肺的疼痛,我也一样的感受与不忍,快速几剪刀后,就看到了跳动的心脏。立刻对大白鼠进行了心脏的摘除实验,心脏摘下来后,马上在K-H液中进行挤血处理,造成缺血心脏模型,再快速进行离体心脏主动脉挂机再灌注试验……然而,俺看到大白鼠从挣扎到死亡的整个过程,俺感受得到摘除心脏时大白鼠的撕裂的疼痛感应,它的生命从有到无的那种挣扎过程,虽然俺稳、准、狠地摘除了它正在跳动的心脏,面对它即将冰凉身体,俺的心情失落无比。之前的稳,准,狠也变得不起作用,因为血留干了。看着大白鼠绝望的眼神,我感觉那种“功留天地间”的感触......突然间,俺觉得自己也被掏空了一样,一个生命就这样在俺的手中......蓦然间俺的眼泪涌了出来,觉得自己很残忍,此刻再不会因为自己的摘除和做实验得到导师的赞许而洋洋得意…… 大白鼠的生命,活着做了人类的试验品,死了也许比活着好。但是,人类为了实验,不得不去杀害小生命时候,应该是有愧疚之心的;对于它们的贡献,俺们也应该感恩。没有这些可爱的小动物人类怎么办?只能拿人类自己做实验??同一个实验室的一个师姐说:“大白鼠,白又白,四只小腿拷起来,剪血管、分神经,两只管子插起来,麻醉打在耳静脉,心肝脾肺肾取出来,一动不动真可爱。”唉,悲催了的,俺还是相信:俺们人类应该爱护小动物,爱护小生命。或许,大白鼠没有人类的大脑那么发达,但它肯定会想:我为人类作了那么多贡献,为什么还是要死?它肯定心里怨恨,否则,大白鼠死前为什么拿那种眼神看我?所以,今天我把自己的话告诉你,大白鼠。我是很感谢你的,为我做了不少的贡献。由于要作为药物临床前动物实验,俺的这个实验需要用活跃的心脏造成缺血进行心脏灌流实验,摘除心脏而导致你的死亡,这并不是一个实验者的本意…… 发帖之时,俺已经克服了恐惧和悲痛,因为俺已经很熟练,很坦然,为了给做课题,为了自己的论文,俺已经能坦然面对大白鼠,因为,俺知道原因了,原因一、实验用大鼠的基因序列和人类的差不多,医学的科研和临床药理实验大多数都是由大小白鼠来完成的。当中以小白鼠做遗传学实验很好,因为它的全基因组和人类的相似度极高,很多人类难以治愈的疾病可以在
[align=center]抗癌药物应用中的临床药学[/align][align=center] [/align][align=center]摘 要[/align][align=center] [/align][align=left]恶性肿瘤严重威胁人类健康,死亡率占所有疾病死亡率的首位,引起人们的普遍关注。提高抗癌药物药效可以明显延长患者的生命并且提高患者的生活质量,减轻痛苦。因此,抗癌药物发挥最大药效的研究十分必要。临床药学是研究药物防治疾病的合理性和有效性的药学学科,近十几年来在我国得到了广泛重视并有了极大的发展。本文主要就抗癌药物如何发挥最大药效进行分析和探讨,阐述了各方面的研究进展和不足,并对抗癌药物的发展前景进行了展望。随着医药学的飞速发展,更先进合理的肿瘤治疗方案必将普遍运用于临床。[/align][align=left] [/align][align=left]关键词:抗癌药物;应用;临床药学;研究进展[/align][align=center] [b]Applicationof anticancer drugs in clinical pharmacy [/b][/align][align=center][b]ABSTRACT[/b][/align][align=center][b] [/b][/align]Malignant tumor is a serious threat to human health,its mortality accounts for the first place of all disease’s mortality, thus hascaused the widespread attention worldwide. Improving the efficacy of anticancerdrugs can prolong the lifetime of patients and improve their quality of life withthe alleviated pains. Therefore, study on the efficacy of anticancer drugs is maximumnecessary. Clinical pharmacy is a pharmaceutical subject includes validity of thestudied drugs for their prevention and treatment of the diseases in the pastdozen years, which has been widely concerned and has a great development in China. This papermainly analyzed and discussed how to maximize the efficacy of anticancer drugs,and the progress on various aspects and its shortcomings, and the development ofanticancer drugs was also prospected. With the rapid development of medicinetoday, more advanced tumor reasonable treatment program will be generally used inclinic.[b]Keywords[/b]: Anticancerdrugs Application Clinical pharmacy Research progress[align=center] [/align][b]1 引言[/b]近年来,由于对抗癌药物作用原理有了更深的了解,加之临床上可用于恶性肿瘤的治疗药物不断增加,化学治疗已由单药连续化疗过渡到多药联合、间段大剂量用药,使化疗效果有很大改善,成为抗恶性肿瘤的一种“根治性”手段[sup][/sup]。另外,增强抗肿瘤老药的药效也正在成为肿瘤治疗药物开发中的新关注对象[sup][/sup]。但由于人们对抗癌药物认识不足,药源性疾病不断增加,导致无数人命丧九泉的事实,促使临床药学迅速崛起。临床药学主要通过药师进入临床,运用药学专业知识,协助医师提出个体化给药方案,并监测患者的整个用药过程,从而提高药物治疗水平,发挥药物的最大药效。在抗癌药物的应用中,从临床药师的干预、最大限度克服耐药性等方面提高药物治疗水平,发挥药物的最大药效至关重要。[b]2 临床药师的干预[/b][align=left]化疗药物在杀伤肿瘤细胞的同时也会对人体正常细胞产生损伤,导致化疗相关毒副反应,并且化疗方案常常需多药联合、放化疗联合,使得化疗药的不良反应相对更多。临床药师可通过对化疗药及辅助用药的选择、剂量的调整、药物的相互作用及用药教育等几方面干预肿瘤患者的临床用药,提升合理用药水平,减少不良反应的发生率,从而提高患者的生存质量。[/align][align=left]2.1 药物的选择[/align]化疗方案制定前应全面评估患者的身体状态,充分了解肿瘤累及的范围,明确临床分期、既往接受药物治疗后的疗效等,权衡患者对抗肿瘤药物治疗的接受能力、对可能出现的毒副反应的耐受力和经济承受力等因素,协助医师进行药物筛选,制定个体化的药物治疗方案。治疗时要清楚方案中哪些药物需要做药学监护、监测指标及监测周期,并随患者病情变化及时调整,尽量规避风险,客观评估疗效[sup][/sup]。临床药师可以通过比较同类药物的药动学、药效学、不良反应等方面的差别,协助医师把药疗方案设计得更完善、实用、规范。临床医师选药一般是从药品的适应症和禁忌症等方面考虑,而临床药师可从“专治”“首选”“药物相互作用”“成本/效果值最合理”来考虑。例如,从药物相互作用方面考虑,联合用药是肿瘤科较为常见的一种治疗手段,其目的是为了达到药物间的协同作用以增加疗效,减少毒副反应。但肿瘤患者尤其是病情危重患者使用药品种类繁多,易发生药物相互作用[sup][/sup]。对可能存在的药物相互作用,药物与食物间的相互作用,临床药师要特别关注。实际工作中药物相互作用问题比较复杂,有药剂学,药代动力学及药效学方面的多种原因。当给医师提出药物相互作用的警示时,还要考虑是否有可替换的无相互作用的药物。如果有可供选择的药物,就调整为其他无相互作用的药物。如果没有可供选择的药物,可采用药物代谢动力学了解药物的清除情况,分析其血药浓度并调整剂量,将药物的相互作用降至最低[sup][/sup]。例如,使用培美曲塞时补充叶酸可降低培美曲塞的毒性[sup][/sup];甲氨蝶岭与其他骨髓毒性药物合用,可进一步抑制骨髓机能。大剂量使用该药后4-24h内静脉或口服给予亚叶酸钙,可防止发生严重而持续的骨髓抑制;白介素2能降低达卡巴嗪的血浆浓度,可能由于提高了达卡巴嗪的分布容积之故。白介素2与地塞米松合用可使患者耐受更大剂量的白介素2,并减轻其毒性[sup][/sup]。此外,化疗辅助药是化疗方案顺利实施的保证,也是减轻化疗毒副作用、减少患者痛苦的主要措施。因此正确选择辅助药也是临床药师的干预点之一,防治骨髓抑制药和止吐药是化疗时常用的辅用药[sup][/sup]。抗肿瘤药物之间的相互作用尚未充分阐明。但是随着抗癌药物应用数量的增多及新的联合用药方式的发展,应重视药物间的相互作用,充分了解药动学及药效学特征。若存在相互作用,就应改变用药方案或调整常用剂量,以求在一定程度上消除可能产生的毒性或亚临床效应。2.2 化疗药剂量的调整恰当的药物剂量应是使药物在最小的毒副反应下发挥最佳的疗效。药物剂量的恰当与否直接关系到用药的安全与疗效。肿瘤患者的药物剂量尤其重要。根据影响代谢的因素来确定剂量,影响药物在人体内的代谢过程是多因素的,抓住其中关键的因素来确定剂量,就可以达到较好的效果。如卡铂,主要根据肾功能来确定剂量[sup][/sup]。根据血药浓度监(TDM),测通过TDM了解患者的 PK 参数,从而实现个体化用药,确保患者在可耐受的情况下达到最优化的疗效。目前只有少数的抗肿瘤药物,其量效关系已经较为明确,TDM已较成熟,如甲氨蝶呤、氟尿嘧啶、依马替尼及卡铂等而大多数抗肿瘤药物,其PK参数和疗效的关系尚未完全明确,TDM的标准尚未建立,还需进一步研究[sup][/sup]。2.3 用药教育癌症治疗中,应严密观察病情变化,监测生命体征:观察心率、血压的变化,每日测体温4次,如有异常及时报告医生[sup][/sup]。同时,对于出院患者要进行出院带药的服药指导。告诉患者药品正确的储存与保管方法,特别是注射剂和生物制品等。使患者清楚药物的治疗疗程,提醒患者按要求复查血常规及肝肾功能,定期返院化疗。对重点病人应加强随访,跟踪用药教育的效果。[b]3 克服耐药性[/b]在恶性肿瘤的治疗中,药物治疗具有不可替代的作用。但在化疗过程中肿瘤细胞产生的耐药,以及多药耐药(MDR)是肿瘤化疗失败的主要原因和临床上亟待解决的难题[sup][/sup]。耐药性产生的机制很多,目前研究较多的是P-糖蛋白参与的耐药。肿瘤细胞的MDR是肿瘤化疗的一大障碍。因此,研制能逆转MDR的化疗增效剂是肿瘤研究的一大热点。但至今无一种有效的逆转MDR药物广泛应用于临床。以药物的特性及细胞增殖动力学为依据[sup][/sup]设计合理的联合化疗方案以及从中药中开发高效、低毒的逆转剂,具有重要的临床意义。中国医科院天津血液病研究所杨纯正教授等发现治疗慢性粒细胞性白血病的当归芦荟丸有效成分---靛玉红在临床试验中显示出逆转耐药和抗肿瘤的双重效应,此类药物值得期待,是寻找具有克服耐药的新抗癌药的重要方向。肿瘤多药耐药产生的机制极其复杂,迄今未有MDR 逆转剂成功地应用于临床,但近几十年来对 MDR 的研究和认识取得了许多重大进展。随着对MDR研究的不断深入,相信将有希望为克服肿瘤多药耐药提供更多的思路和途径。[align=center]4 其他方面[/align]4.1 有效防止静脉用药外渗在多种给药方法中,现在抗癌治疗的主要手段之一还是依靠静脉输液。静脉注射给药能快速地将药物送入体内,提高血清中药物的浓度,达到化疗效果。患者在接受化学药物治疗的过程中,因长期输液反复静脉穿刺及化学治疗药物对血管、黏膜、皮下组织、皮肤的刺激,药物从针眼外渗或从血管口外漏,均可致静脉无菌性炎症,局部组织疼痛灼热感,严重者可使组织坏死溃烂,长期不愈,成为临床护理工作中待解决的问题[sup][/sup]。因而为了达到减少静脉输注药物外渗以提高药效的目的,根据常见静脉抗癌药物损伤组织的机制,提出积极的预防、诊断、治疗和护理措施。护理工作者要对抗癌药物的毒性反应进行详细了解,并且要尽量保证静脉穿刺一次成功,加强静脉防治知识的宣教。为了防止抗癌药物外渗对患者所造成的痛苦,就要完善好预防工作,真正做到防患未然。在临床治疗当中,要避免抗癌药物外渗的发生,使患者的治疗能够得到正常进行[sup][/sup]。[align=left]4.2 加强护理[/align] 患者诊断为癌症后十分焦虑和恐惧,对各种治疗有疑虑,情绪紧张。应根据患者的不同年龄、知识层次、病情轻重及性格特点做好心理护理[sup][/sup],为让患者配合治疗,应采用多种沟通方式使其打消顾虑,消除紧张害怕心理,治疗前向患者讲解治疗法的安全性、可靠性、必要性[sup][/sup],主动关心病人,同时不隐瞒用药的不良反应,使患者在思想上有充分的准备,使其以良好的状态接受治疗。由于各种不良反应会给患者带来心理负担,首先应建立起和谐融洽的护患关系,工作中与病人多交流,用诚恳热情,乐观自信的情绪,严肃认真的工作态度去感染病人,使其在心理上获得安全和信任。协调好病友间的关系,相互理解关心鼓励,提高病人家庭和社会支持水平,从而树立病人战胜疾病的信心。[align=center]5 结语[/align][align=left]新抗癌药不断涌现,基础研究不断深入,合理用药和联合用药提高了化疗效果。多种途径、多种方法的研究和应用,连续静脉滴注、动脉给药、介入治疗、抗癌药与增效药合用、抗癌药与解毒药合用、大剂量化疗加造血干细胞移植等,使化疗疗效均有不同程度的提高。减轻抗癌药的不良反应,以增加病人对抗癌药的耐受性,提高药物的使用剂量,也可使化疗疗效提高。近年来在减少胃肠道反应和减轻骨髓抑制方面,取得了突破性进展,明显减轻病人用药期间的痛苦,提高用药剂量,减少并发症等方面均起到很大作用。减少多药耐药性的发生,也是当前的重要研究课题,以提高对难治性肿瘤的治疗效果。提高病人的免疫功能,改善病人的营养状况和一般状况,给予支持治疗、扶正培本的中医中药治疗和免疫治疗,这将有利于增强病人对治疗的耐受性,并提高病人的生活质量,增加治疗作用。[/align]个人认为结合免疫治疗的多种肿瘤治疗方案是一个重要发展方向。传统认为化疗主要通过细胞毒作用直接杀伤肿瘤细胞,而免疫治疗主要通过调动机体免疫系统达到抑制肿瘤生长和长期控制肿瘤的目的。由于化疗存在免疫抑制作用,因此化疗联合免疫治疗的模式曾经受到质疑。但是,随着研究的深入,越来越多的数据显示化疗和免疫治疗存在协同作用。[align=left] [/align][b]参考文献[/b] 卜风英.化疗患者预防感染的重要性.包头医学,2009,33(11):58~59 梁岩,何珩,孙翠萍.抗肿瘤用药的应用及进展.中国医疗前沿,2009,4(21):17~18 陈晓媛,张虹,高晨燕.小分子靶向抗肿瘤药物临床研究策略探讨及案例分析.新药申报与审评技术,2013,22(3):269~273 孙西洋,任常山,曹心珂.抗肿瘤药物的靶向给药系统研究进展.中国医药生物技术,2008,3(6):461~464 王爱军,金永新,要林青等.抗肿瘤药物治疗中临床药师的干预技巧.中国药事,2013,27(1):97~99 Paz-AresLG, Smith MR.Genitourinary malignancies .Cancer Chemoter Biol ResponseModi,2001,19(21):573~595 van Meerten E [i]et al[/i].Interaction with the clinical significance of antitumor drugs.Foreign Medical Scienceson Pharmacy,2006,23(1):31~35 王祎,刘燕,丁秀云.抗肿瘤药物的研究进展.包头医学,2012,36(3):129~132 李嘉,包春波.抗肿瘤化学药物研究进展.华西药学杂志,2009,4(21):1~5 徐贞,史美祺.抗肿瘤药物的剂量选择.读者园地,2012,28(5):379~380 张岩.肝癌介入治疗术前术后护理.中国社区医师医学专业半月刊,2009,11(21):127~128 卿晨.恶性肿瘤化疗耐药及克服耐药的研究.昆明医科大学学报,2013,34(1):1~3 梁岩,何珩,孙翠萍.抗肿瘤用药的应用及进展.中国医疗前沿,2009,4(21):17~18 侯清平,李青枝.肿瘤患者化学药物治疗过程中的静脉管理.实用医技杂志,2013,20(4):406~407 王秋平.抗癌药物外渗的预防和处理.大家健康,2013,7(3):121~127 张岩.肝癌介入治疗术前术后护理.中国社区医师医学专业半月刊,2009,21(11):168~169 孙燕.50年来我国抗肿瘤药物临床研究的进展.新药研发论坛,2009,18(18):1695~1700[align=left] [/align]