维纶基牛奶蛋白纤维和维纶基大豆蛋白纤维定性分析的研究维纶基大豆蛋白纤维是迄今为止我国获得的唯一完全知识产权的纤维发明,在纺织行业得到了快递的发展,广泛的应用,但与维纶基大豆蛋白纤维一样由我国企业自主研发的维纶基牛奶蛋白纤维也申请到专利好几年了,但迟迟没有相关标准的出台,使这一我国自主研发的新型纤维得不到有效利用新型纤维的不断推出,为我们提供了更多的纤维原料,但同时由于国家标准的相对滞后,给检测工作者带来了很大的难题,下面就目前市场上两种新型蛋白复合纤维给予试验,进行定性分析。主要原理是在观察了维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维显微结构和燃烧性状后,研究两者在常用化学试剂中的溶解性。试验结果表明,维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维在88%甲酸和浓硝酸中都能够部分溶解;在沸腾水浴中,维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维能够完全溶解于75%硫酸和98%硫酸牛奶蛋白纤维是再生蛋白质纤维,是以牛奶为原料经脱水、脱脂、分离、纯化、浓缩制成牛奶酪蛋白,与高分子化合物共混、共聚制成纺丝液,再经湿法纺丝而成;牛奶酪蛋白与聚乙烯醇制得的纤维称为维纶基牛奶蛋白纤维;牛奶酪蛋白与纤维素共聚制得粘胶基牛奶蛋白纤维。牛奶蛋白纤维含有多种氨基酸,具有良好的亲肤性和吸湿导湿性,抗菌防蛀,服用性强,受到消费者的青睐。维纶基牛奶蛋白纤维呈浅黄色,是由牛奶酪蛋白和聚乙烯醇大分子共混、共聚、醛化、揉和、脱泡,湿法纺成的纤维,克服了合成纤维吸湿性差和天然纤维强度低的不足,其比电阻介于天然纤维和合成纤维之间,吸湿性也优于聚乙烯醇纤维,在直接染料、弱酸性染料、活性染料和中性染料中都有良好的上染能力。本文在观察维纶基牛奶蛋白纤维和维纶基大豆蛋白纤维显微结构和燃烧性状后,研究两者在常用化学试剂中的溶解性,为纤维检测提供参数。大豆蛋白纤维属于再生植物蛋白纤维类,是以榨过油的大豆豆粕为原料,利用生物工程技术,提取出豆粕中的球蛋白,通过添加功能性助剂,与腈基、羟基等高聚物接枝、共聚、共混,制成一定浓度的蛋白质纺丝液,改变蛋白质空间结构,经湿法纺丝而成. 其有着羊绒般的柔软手感,蚕丝般的柔和光泽,棉的保暖性和良好的亲肤性等优良性能,还有明显的抑菌功能,被誉为“新世纪的健康舒适纤维”。大豆纤维是以脱去油脂的大豆豆粕作原料,提取植物球蛋白经合成后制成的新型再生植物蛋白纤维,是由我国纺织科技工作者自主开发,并在国际上率先实现了工业化生产的高新技术,也是迄今为止我国获得的唯一完全知识产权的纤维发明。1 试验1. 1试验材料、仪器和试剂纤维细度成分显微分析仪,万分之一电子天平;SHA-C水浴振荡器;鼓风恒温烘箱; 索氏萃取器;酒精灯;具塞三角瓶若干。甲酸(88%);硫酸(75%);浓硫酸(98%);浓硝酸;1MOL/L次氯酸钠溶液;石油醚(馏程为40℃~60℃)。1.2试验方法显微结构试验:用纤维细度成分显微分析仪观察纤维的显微结构。 以下试验维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维同一方法分别做一次燃烧性状试验:点燃酒精灯,用镊子夹取10mg左右纤维束,徐徐靠近火焰,观察试样对热的反应情况。将纤维移入火焰,观察纤维的燃烧情况;然后离开火焰,观察纤维的燃烧情况,并用鼻子闻试样燃烧刚熄灭的气味。最后,待试样熄灭冷却,观察残留物灰分的状态。预处理:取纤维5g左右,用定量滤纸包好,置于索氏萃取器中,用石油醚萃取1h,每小时至少循环6次,待试样中的石油醚挥发后,把试样浸入冷水中浸泡1h,再在(65±5)℃的水中浸泡1h,浸泡过程中时时搅拌。水(mL)与试样(g)之比为100:1。然后抽吸脱水,晾干。溶解性试验:准确称取试样1g置于具塞三角瓶中,加入100mL化学试剂,在搅拌条件下观察不同温度下纤维和试剂随时间的变化情况。待一定时间后,洗涤,抽吸排液,烘干。2 试验结果2.1显微结构在显微镜下观察维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维的横截面呈腰圆形或哑铃形,纵向有沟槽,两种纤维在显微镜下几乎无差别,无法区分这两种纤维。2.2燃烧性状维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维靠近火焰时现象都是熔融并卷曲;进入火焰,熔融、卷曲并燃烧;离开火焰,燃烧,有时会自然熄灭。燃烧过程中散发出蛋白质燃烧时所特有的臭味。纤维燃烧的一端形成黑褐色硬块。两种纤维在燃烧情况下,火焰颜色,气味几乎无差别,无法区分这两种纤维。2.3溶解性取维纶基牛奶蛋白纤维与和维纶基大豆蛋白纤维分别置于88%甲酸、75%硫酸、浓硫酸、浓硝酸和1MOL/L次氯酸钠溶液中进行溶解性试验, 品名/溶液88%甲酸[/ali
如题,肌原纤维蛋白形成凝胶的微观结构用什么观察?光学显微镜能观察吗?
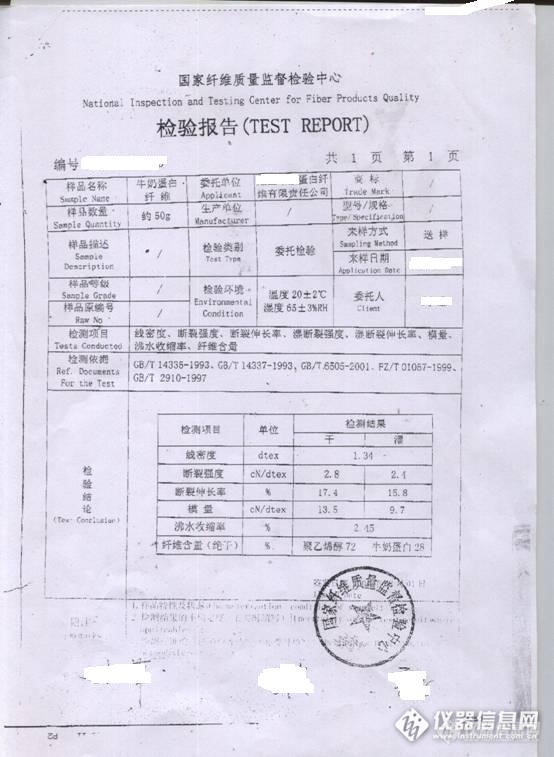
维纶基牛奶蛋白纤维和维纶基大豆蛋白纤维定性分析的方法研究 维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维都是由聚乙烯醇和蛋白共混制得,所以化学性质及其相似,一直以来由于维纶基牛奶蛋白纤维没有相关的检测方法,检测机构对维纶基牛奶蛋白纤维出具的检测报告都是维纶基大豆蛋白纤维 维纶基大豆蛋白纤维的成分定量分析方法是先用次氯酸钠溶液溶解掉蛋白质,然后用盐酸溶解聚乙烯醇,同样维纶基牛奶蛋白纤维也是可以用这种方法进行溶解,下面看看常规的检测方法能不能分析出这两种纤维1.维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维,其纤维成分定性的基本方法:①.显微镜法: 在显微镜下观察维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维的横截面呈腰圆形或哑铃形,纵向有沟槽;②.燃烧: 维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维靠近火焰时现象都是熔融并卷曲;进入火焰,熔融、卷曲并燃烧;离开火焰,燃烧,有时会自然熄灭。燃烧过程中散发出蛋白质燃烧时所特有的臭味;③.溶解法:共同的维纶基,加上都是蛋白质,化学性质非常接近,在75%硫酸、浓硫酸、浓硝酸和0.1MOL/L次氯酸钠溶液中,溶解现象和状态都是一样的,都无法将两者定性2.个人通过研究和分析认为,只有通过两者氨基酸的组分不同进行定性,从而确定纤维牛奶中氨基酸的组成表”取自《乳与乳制品的生理功能特征》一书。“大豆蛋白质的氨基酸组成表”取自《大豆制品工艺学》一书。大豆蛋白质的氨基酸组成可以参考“全酸沉淀蛋白”的氨基酸组成,做为比较的依据。因为大豆蛋白纤维使用的是大豆分离蛋白,即是酸沉蛋白。http://ng1.17img.cn/bbsfiles/images/2013/09/201309121130_463904_2154459_3.jpghttp://ng1.17img.cn/bbsfiles/images/2013/09/201309121130_463905_2154459_3.jpghttp://ng1.17img.cn/bbsfiles/images/2013/09/201309121130_463907_2154459_3.jpg3.维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维的通过测其氨基酸的组成不同,可以定性出大豆蛋白与牛奶蛋白,如果是大豆蛋白复合纤维,然后用GB/T2910.101-2009大豆蛋白复合纤维和其他纤维的混合物-定量化学分析进行测试。完全溶解,则为维纶基大豆蛋白纤维,如果是维纶基牛奶蛋白纤维,也可以用此方法进行定量法定性,相关详细步鄹如下:3.1 试验3.1.1试验材料、仪器和试剂万分之一电子天平;SHA-B水浴振荡器;鼓风恒温烘箱;索氏萃取器,离心机,具塞三角瓶,1MOL/L次氯酸钠溶液,氢氧化钠,20%盐酸溶液等3.1.2目前行业内认为定性牛奶蛋白纤维的最好方法:牛奶蛋白纤维在2.5%NaOH 溶液下,100℃恒温加热30分钟,即可出现牛奶蛋白特有的现象。状态:在整个溶解的过程下,纤维体积膨胀渐呈冻胶状,颜色会从本色逐渐变成深红色,然后再有深红色褪色至浅黄色。此方法经试验,并不是所有的牛奶蛋白复合纤维都出现此特有现象,有时不是很明显,只能作为判断的一种辅助方法,不能作为定性的标准方法。3.1.3在显微镜下观察牛奶蛋白复合纤维或大豆蛋白复合纤维,能确定是其中的一种,然后用1MOL/L次氯酸钠溶液,常温下振荡溶解30分钟,此时,蛋白全部溶解,剩余纤维抽滤,冲洗干净,取少量纤维在显微镜下查看,初步判定为聚乙烯醇,然后燃烧,根据味道和燃烧现象,确定其为维纶基蛋白纤维3.2需要确定蛋白质纤维为何种纤维,经初步试验分析,常规方法无法准确定性,下面是维纶基牛奶纤维的专利拥有者在相关国家检测机构取得的检测报告http://ng1.17img.cn/bbsfiles/images/2013/09/201309121131_463909_2154459_3.jpg以上报告可能确定是维纶和牛奶蛋白复合,但其报告检测依据个人不是特别认同,也咨询过相关人员,没有给予明确答复,检测的具体方法没有明确,国家并没有发布相关的检测标准,不能作为判断纤维的依据,所以目前情况下仍然不能使该纤维大面积推广使用。3.3个人认为,只有通过两者氨基酸的组分不同进
Nucl. Acids Res.:结构和生化方法研究质粒分配蛋白ParB和着丝粒DNA的相互作用近期北京生命科学研究所所叶克穷实验室在Nucleic Acids Research杂志在线发表论文,通过结构和生化的方法研究了质粒分配蛋白ParB和着丝粒DNA的相互作用。该研究由科技部、北京市政府和国家自然科学基金资助,在北京生命科学研究所完成。本文的第一作者为北京生命科学研究所和武汉大学联合培养的博士研究生黄林,研究员叶克穷博士是本文的通讯作者。此研究还得到研究生朱星,武汉大学的殷平和张翼教授的帮助。所有的细胞需要将遗传物质DNA的稳定分配到子代细胞,这个分配过程在真核生物中非常复杂。对于细菌的一些低拷贝质粒,由着丝粒DNA、马达蛋白ParA以及着丝粒结合蛋白ParB三个成分构成的简单系统就能完成质粒在子代细菌中的分配。ParB和着丝粒DNA结合形成分配复合物,分配复合物进一步和ParA结合。ParA能形成纤维结构,并通过纤维的生长把结合在纤维两端的质粒推向分裂细胞的两级。这个系统提供了一个简单并且易于操作的模型来研究遗传物质的分配。革兰氏阳性菌Leifsonia xyli subsp. Cynodontis的质粒pCXC100包含一个Ib型质粒分配系统。然而一直以来研究人员对于ParB包含的DNA结合结构域尚不清楚,叶克穷实验室通过结构和生化的方法研究了ParB的三维空间结构以及ParB和着丝粒DNA之间的作用方式。研究人员解析了ParB DNA结合结构域的晶体结构,发现它折叠成RHH二聚体结构域,这个结果进一步说明RHH结构域在结合着丝粒过程中的普遍性。研究人员还利用高分辨DNA印迹实验和定量DNA结合实验分析了ParB和着丝粒DNA的相互作用,发现着丝粒区域由九个无间隔的9碱基对正向重复序列组成,ParB和连续重复序列的结合时具有高度的协同性。有意思的是,单独一个ParB二聚体分子和DNA结合时,至少需要一个重复序列以及两边相邻序列共18个碱基对DNA。研究人员分析了ParB识别这18个碱基对中每个序列的特异性。研究结果说明pCXC100 在形成分配复合物时,每个着丝粒重复序列能被相邻的ParB分子同时识别的独特方式
大豆蛋白纤维是标准的纤维属名吗?
大豆蛋白纤维也是一种复合纤维,是大豆蛋白和聚乙烯醇复合纤维,牛奶蛋白也有一种牛奶蛋白和聚乙烯醇复合的纤维,其中大豆蛋白纤维在市场上比较普遍,但最近两年牛奶蛋白聚乙烯醇纤维在市场上也比较多见,其中显微镜和燃烧法,大豆蛋白纤维和牛奶蛋白聚乙烯醇纤维都比较相似,化学性质也相似,不知大家有没有遇到这两种纤维,怎么来定性,定量?

下面这个是大豆与羊毛动物纤维,蚕丝二组分混合物分析方法,溶解大豆蛋白,利用蛋白含量占大豆蛋白复合纤维的比例来确定大豆蛋白复合纤维含量,有点不可理解?大豆蛋白复合纤维,目前是大豆蛋白和聚乙烯醇复合,仅仅用蛋白溶解后,剩余的聚乙烯醇的含量来‘推算’出来大豆蛋白复合纤维的含量,是有点欠妥,虽然规定了大豆蛋白复合纤维的蛋白含量,但是实际的大豆蛋白复合纤维中,大豆蛋白和聚乙烯醇含量的比例不一定的,也就是说比例不是那么固定的,这样的检测方法对检测公司来说是没有任何问题的,也是标准的一个进步,但对生产企业来说,确实是致命的,没有规定大豆蛋白复合纤维的配比必须是多少,这个检测很可能每批次大豆与羊毛动物纤维,蚕丝产品的标示和实际检测结果是不合格的。而实际生产添加的各成分是标准的?比如填充,大豆与羊毛动物纤维,蚕丝混合,生产企业是烘干后,按照回潮率计算,按重量比添加混合的,这样企业就根据这样的比例进行标示,这个是最准确的,也是最合理的?大家认为呢?[img=,690,172]http://ng1.17img.cn/bbsfiles/images/2017/10/201710250916_01_2154459_3.png!w690x172.jpg[/img][img=,690,138]http://ng1.17img.cn/bbsfiles/images/2017/10/201710250913_01_2154459_3.png!w690x138.jpg[/img]
[font=宋体] 成分分析之蛋白类复合纤维发现与明命名的历程[/font] [font=宋体]纺织纤维中蛋白类纤维相对较早的是牛奶蛋白复合纤维和大豆蛋白复合纤维,这两种纤维在国内已经运用十年以上了,也有标准的检测方法,应用的范围也比较广,属于产业化发展了。[/font][font=宋体] 国内牛奶蛋白复合纤维国内首先是上海正家牛奶丝科技有限公司在国外的基础上研发出来的,当然不是国内研发的,只能算国产化,[/font][font=宋体][color=#333333][back=white]牛奶蛋白纤维是以牛乳作为基本原料,经过脱水、脱油、脱脂、分离、提纯,使之成为一种具有线型大分子结构的乳酪蛋白;再与[/back][/color][/font][font=宋体]腈纶[/font][font=宋体][color=#333333][back=white]采用高科技手段进行共混、交联、接枝,制备成纺丝原液;最后通过湿法纺丝成纤、固化、牵伸、干燥、卷曲、定形、短纤维切断(长丝卷绕)而成的。[/back][/color][/font][font=宋体][color=#333333][back=white][/back][/color][/font][font='Helvetica','sans-serif'][color=#333333][back=white] [/back][/color][/font][font=宋体][color=#333333][back=white]相比于牛奶蛋白复合纤维来说,大豆蛋白复合纤维绝对是比较牛掰了,因为它是我国也是迄今为止我国获得的唯一[/back][/color][/font][font=宋体]完全知识产权[/font][font=宋体][color=#333333][back=white]的纤维发明,由河南企业家李管奇董事长带领团队进行研发出来的;大豆纤维是以脱去油脂的大豆豆粕作原料,提取植物球蛋白经合成后制成的新型再生植物蛋白纤维,是由我国纺织科技工作者自主开发,并在国际上率先实现了工业化生产的高新技术,,[/back][/color][/font][font='Helvetica','sans-serif'][color=#333333][back=white] [/back][/color][/font][font=宋体][color=#333333][back=white]蛋白复合纤维运用和命名也是比较少见的,就是每当新的成分标准出台或者化学纤维属名标准出台,蛋白复合纤维的名称都会有变化,最早牛奶纤维就叫牛奶蛋白复合纤维,然后出来产品定量分析标准后,大家有都同意把牛奶蛋白复合纤维更名为[/back][/color][/font][font=宋体]牛奶蛋白改性聚丙烯腈纤维,其检测标准为[/font]FZ/T 01103-2009 [font=宋体]纺织品[/font] [font=宋体]牛奶蛋白改性聚丙烯腈纤维混纺产品定量化学分析方法。[/font][font=宋体] 但是[/font]GBT 29862-2013[font=宋体]纺织品[/font] [font=宋体]纤维含量的标识,这个标准出来后,又改成蛋白改性聚丙烯腈纤维,使用的捡测方法依然为[/font]FZ/T 01103-2009 [font=宋体]纺织品[/font] [font=宋体]牛奶蛋白改性聚丙烯腈纤维混纺产品定量化学分析方法。[/font] [font=宋体]这次改名其实也是更加的合理和准确,因为在纺织品成分分析中,常规的方法根本无法确定蛋白是不是牛奶蛋白,只是能确认蛋白而已,所以这个改名大家也是很容易接受。[/font] [font=宋体]到了今年,[/font]GB T 4146.1-2020[font=宋体]纺织品[/font] [font=宋体]化学纤维[/font] [font=宋体]第[/font]1[font=宋体]部分:属名的实施后,蛋白改性聚丙烯腈纤维有改名了,不能这么叫了,现在最新叫法为[/font][font=宋体]聚丙烯腈纤维[/font] [font=宋体](含有蛋白),这个还没有进行标准统一,很多检测单位也是[/font]2[font=宋体]种叫法都不算错的过程中运转。[/font] [font=宋体]大豆蛋白复合纤维,也是同样的道理,[/font]GB/T2910.101-2009 [font=宋体]纺织品定量化学分析[/font] [font=宋体]大豆蛋白复合纤维与某些其他纤维的混合物,虽然检测方法就叫大豆蛋白复合纤维,但是还是在[/font]GBT 29862-2013[font=宋体]纺织品[/font] [font=宋体]纤维含量的标识出台后,改为蛋白改性聚乙烯醇纤维,[/font]GB/T4146.1-2020[font=宋体]纺织品[/font] [font=宋体]化学纤维[/font][font=宋体]第[/font]1[font=宋体]部分:属名的实施后,目前统称为聚乙烯醇纤维(含有蛋白)。[/font][font=宋体] 蛋白复合纤维是所有的纤维中名称改变次数最多,改变最频繁的,也是标准的不断变化和严谨的一个过程,不管怎么改变,新的纤维能给我们生活带来更多的选择和更加的感受这就很好了。[/font][font=宋体] 篇幅有限,如需更多的了解,欢迎大家留言交流,尽力满足大家![/font]
最近见到维纶基牛奶蛋白纤维,不知怎么出报告,大家怎么进行测试的,又遇到过的吗?
请教下做过膳食纤维的老师,我按照国标提取总膳食纤维,提取完毕烘干后膳食纤维和硅藻土是混合的,我要测里面的蛋白要怎么测定????能将硅藻土和膳食纤维分开吗》????
各位老师,面料中有遇到大豆蛋白复合纤维的吗?以前遇到大豆蛋白复合纤维都是作为填充物的,现在做为面料出现,并且含量很低,这样的混纺面料有什么意义呢?
GBT2910.101-2009 大豆蛋白复合纤维与某些其他纤维的混合物FZT 01102-2009 纺织品 大豆蛋白复合纤维混纺产品定量化学分析方法?都是测试大豆蛋白复合纤维的成分,问:问什么在同一年内有两个标准,但是内容几乎没有什么变化?目的是什么?
大家好,不知道大家做牛奶蛋白纤维聚合物的多不多,行业标准制订了牛奶蛋白改性聚丙烯晴聚合物的检测方法,可是最近牛奶蛋白聚乙烯醇聚合物在市场上出现较多,大家对这样的产品有没有好的定性定量方法?
各位老师,大豆复合纤维名称改为聚乙烯醇纤维(含有蛋白)了吗?
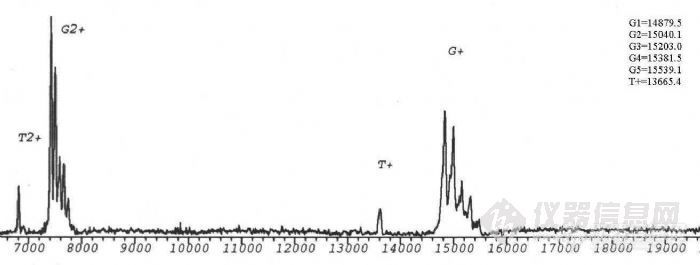
生物质谱在糖蛋白结构分析中的应用项目完成人:桑志红 蔡 耘项目完成单位:国家生物医学分析中心 随着人们对糖蛋白参与生命活动机理的日益深入了解,对天然糖蛋白及重组糖蛋白类药物的分析越来越受到重视。重组糖蛋白类药物的质量控制更是直接关系到药物的疗效及至人类的健康。九十年代以来,随着带有反射功能的基质辅助激光解吸附电离飞行时间质谱(MALDI-TOF-MS)和纳升电喷雾串联质谱(nano-ESI-Q-TOF)等具有软电离方式的现代质谱 技术的发展,质谱以其高灵敏度和强有力的分析混合物的能力,提供了生物大分子的分子量、序列、一级结构信息以及结构转换、修饰等方面的信息,使糖基化分析有了重要的进展。 通常研究糖蛋白的方法是把蛋白链上的寡糖切下来,分别研究蛋白部分和寡糖部分的结构,因此无法研究与两部分共同相关的结构问题,也不能区分不同糖基化位点上切下来的寡糖。自90年代初,国外有人开始用质谱法研究糖蛋白的结构,同时描述了各个位点的不均一性。我们用建立的现代生物质谱技术研究糖蛋白一级结构的方法,将其应用与基因重组糖蛋白的结构分析。为糖蛋白结构分析及基因重组糖蛋白类药物的质量控制提供新的手段。一、 生物质谱研究糖蛋白结构方法的建立实验所用仪器为:1.德国BRUKER 公司的REFLEXIII型基质辅助激光解吸附电离飞行时间质谱仪,N2激光器,波长337nm,线性飞行距离150cm,加速电压2kv。2.英国Micromass 公司Q-TOF型电喷雾串联质谱仪。源温80°C,气体流速40L/h,枪头电压650V,检测频率2.4S,氩气碰撞池压力6*10-5mbar。1. 基质的选择,在MALDI-TOF-MS分析中,基质起着相当重要的作用。不同的基质对不同类的物质响应不同,a-氰基-4-羟基肉桂酸用于测定糖蛋白核糖核酸酶B效果相对较好。2. 糖蛋白分子量的测定,糖蛋白核糖核酸酶B由124个氨基酸组成,在34位Asn处连有一个高甘露糖型N-糖链。由于糖链的微不均一性,与普通蛋白质及核酸不同,其分子离子峰在MALDI-TOF-MS 质谱图上表现为一簇峰,各峰之间约相差一个糖基。正是由于这种微不均一性,使得其分子离子峰变宽,灵敏度降低。糖链分子量越大,峰越宽,灵敏度越低,所以一般只有糖链较短,蛋白的质量不太大的糖蛋白才能测定其平均分子量。用MALDI-TOF可直接测定糖蛋白核糖核酸酶B的平均分子量为 15208.6Da。http://ng1.17img.cn/bbsfiles/images/2011/03/201103211511_284179_1604317_3.jpg3. 糖含量的测定,采用O聚糖酶及内糖苷键酶F分别作用于核糖核酸酶 B,只有内糖苷键酶F能够是其分子量发生变化,表明核糖核酸酶B分子中不存在O-连接糖链存在着N-连接糖链。内糖苷键酶F切断N-糖链五糖核心最内侧的GlcNAc-GlcNAc糖苷键,得到含一个GlcNAc的肽链,减去GlcNAc,可以计算出准确的肽链分子量T=13695.6,与糖蛋白平均分子量之差为糖链的平均分子量G=1513.4,平均糖含量为:(糖链大小/糖蛋白分子量)×100%=9.95%。4. 糖基化位点的确定,研究糖基化类型及糖基化位点的策略:采用蛋白酶酶解与糖苷内切酶酶解相结合的方法,通过酶切前后含糖肽片的位移,结合网上数据库检索,可以确定糖基化类型和糖基化位点。以不同类型的糖苷内切酶作用于糖蛋白(N-糖苷键酶或O-糖苷键酶),在MALDITOF-MS 上观察其质量的变化,可以直接确定糖蛋白中是否含有响应类型的糖链,这是我们确定糖蛋白中糖苷键类型的基础。我们采用先将核糖核酸酶B还原烷基化,加Glu-C酶切,产物再用内糖苷肩酶F酶切,可观察到含糖肽段出现位移,将核糖核酸酶B的肽质量指纹图进行数据库检索,证实发生位移的肽段中含有N-糖链特异连接位点,由此确定34位Asn为糖基化位点。另外我们采用内糖苷键酶F及肽-N-聚糖酶F两种酶进行差位酶切法对含糖肽段进行验证,两种酶酶切后分子离子峰的差值除以GlcNAc的质量,结果就是N-糖基化位点的个数5. 质谱测定氨基酸序列, 我们对核糖核酸酶B肽质量指纹谱中的含糖肽段进行了串联质谱测定,首先在一级质谱图中选择离子4972.23,在串联质谱的碰撞活化室以氩气与其碰撞产生碎片,从碎片的质荷比推算出此肽片中的一段氨基酸序列,检索结果为核糖核酸酶B,从而判断其理论序列是否一致。6. 糖链结构的研究,凝集素对糖肽的亲和提取,进一步分析糖肽序列及糖链结构的关键是含糖肽段的提取。核糖核酸酶B中糖链为高甘露糖型,我们选用对其有特异性吸附的伴刀豆球蛋白对其进行提取利用这种简捷的亲和质谱的方法,对糖肽段进行了分析。建立了亲和质谱分析糖肽类物质的方法,为今后糖肽序列分析及糖链结构分析奠定了基础。二、基因重组糖蛋白人促红细胞生成素(rhEPO)的结构分析。 利用以上建立的方法,我们对样品重组人促红细胞生成素进行了分析,断定此样品为非完全糖基化,样品中只存在N-连接的糖链,无O-糖链。应用酶切法用肽-N-聚糖酶处理后,得到两个含糖肽段,进行数据库检索,测得38位及83位为N-糖基化位点,与文献报道相符,结果可靠。因此,该项课
花生蛋白纤维,大家听说过吗??有应用于服装产品吗?
有奖问答’对错题:二组分纤维混纺含量分析时,大豆蛋白复合纤维与其他纤维混纺产品的含量分析,用碱性次氯酸钠法溶解蛋白质纤维?( )
大豆蛋白复合纤维,桑蚕丝,聚酯纤维三组分成分测试,怎么定量,用哪种方法定量较适合?

http://ng1.17img.cn/bbsfiles/images/2016/05/201605201157_594045_2154459_3.png看上面的标准,这个大豆蛋白复合纤维中大豆蛋白的含量怎么来计算的?
[font=宋体]抗体,作为一类特殊的蛋白质,在免疫系统中发挥着至关重要的作用,它们能够特异性地识别并中和外来病原体,如细菌和病毒。而蛋白质,作为生命活动的基础分子,具有多种多样的功能,从酶催化到结构支撑,无所不包。抗体与蛋白的区别在于,抗体是一类具有特定功能的蛋白质,而蛋白质则是更广泛的一类生物分子。本文将深入探讨抗体与蛋白的具体区别,并详细解析抗体蛋白的结构与功能,为读者提供一个全面而深入的理解。[/font][font=宋体] [/font][b][font=宋体]抗体与蛋白的区别?[/font][/b][font=宋体] [/font][font=宋体]定义:[/font][font=宋体][font=宋体]抗体([/font][font=Calibri]antibody[/font][font=宋体])是指机体由于抗原的刺激而产生的具有保护作用的蛋白质。它(免疫球蛋白不仅仅只是抗体)是一种由浆细胞(效应[/font][font=Calibri]B[/font][font=宋体]细胞)分泌,被免疫系统用来鉴别与中和外来物质如细菌、病毒等的大型[/font][font=Calibri]Y[/font][font=宋体]形蛋白质,仅被发现存在于脊椎动物的血液等体液中,及其[/font][font=Calibri]B[/font][font=宋体]细胞的细胞膜表面。抗体能识别特定外来物的一个独特特征,该外来目标被称为抗原。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]抗体是一类能与抗原特异性结合的免疫球蛋白。抗体按其反应形式分为凝集素、沉降素、抗毒素、溶解素、调理素、中和抗体、补体结合抗体等。按抗体产生的来源分为正常抗体(天然抗体),如血型[/font][font=Calibri]ABO[/font][font=宋体]型中的抗[/font][font=Calibri]A[/font][font=宋体]和抗[/font][font=Calibri]B[/font][font=宋体]的抗体,和免疫抗体如抗微生物的抗体。按反应抗原的来源分为异种抗体,异嗜性抗体,同种抗体和自身抗体。按抗原反应的凝集状态分为完全抗体[/font][font=Calibri]IgM[/font][font=宋体]和不完全抗体[/font][font=Calibri]IgG[/font][font=宋体]等。抗体在医疗实践中应用甚为广泛。如用于疾病的预防、诊断和治疗方面都有一定的作用。临床上用丙种球蛋白预防病毒性肝炎、麻疹、风疹等,国际上用抗[/font][font=Calibri]Rh[/font][font=宋体]免疫球蛋白预防因[/font][font=Calibri]Rh[/font][font=宋体]血型不合引起的溶血症。诊断上如类风湿因子用于类风湿性关节炎,抗核抗体([/font][font=Calibri]ANA[/font][font=宋体])、抗[/font][font=Calibri]DNA[/font][font=宋体]抗体用于系统性红斑狼疮,抗精子抗体用于原发性不孕症的诊断等;治疗上如毒素中毒用抗毒治疗以及免疫缺陷性疾病的治疗等。[url=https://cn.sinobiological.com/resource/antibody-technical][b]抗体相关资源[/b][/url][/font][/font][font=宋体] [/font][font=宋体]蛋白:[/font][font=宋体][font=宋体]蛋白质是生命的物质基础,是有机大分子,是构成细胞的基本有机物,是生命活动的主要承担者。没有蛋白质就没有生命。氨基酸是蛋白质的基本组成单位。它是与生命及与各种形式的生命活动紧密联系在一起的物质。机体中的每一个细胞和所有重要组成部分都有蛋白质参与。蛋白质占人体重量的[/font][font=Calibri]16%~20%[/font][font=宋体],即一个[/font][font=Calibri]60kg[/font][font=宋体]重的成年人其体内约有蛋白质[/font][font=Calibri]9.6~12kg[/font][font=宋体]。人体内蛋白质的种类很多,性质、功能各异,但都是由[/font][font=Calibri]20[/font][font=宋体]多种氨基酸([/font][font=Calibri]Amino acid[/font][font=宋体])按不同比例组合而成的,并在体内不断进行代谢与更新。点击查看:[url=https://cn.sinobiological.com/resource/protein-review][b]蛋白相关资源[/b][/url][/font][/font][font=宋体] [/font][b][font=宋体]区别与联系:[/font][/b][font=宋体][font=宋体]蛋白质还是有一定的区别以及关联性的,虽然说抗体是蛋白质,但是蛋白质不一定是抗体。[/font] [font=宋体]主要是因为抗体是通过人体内的浆细胞所产生的,而且还可以喝相应的抗原特异性相互结合,这样在一定程度上就能发挥出蛋白质。[/font][/font][font=宋体] [/font][b][font=宋体]抗体[/font][font=宋体]蛋白[/font][font=宋体]结构[/font][font=宋体]解析[/font][font=宋体]:[/font][/b][font=宋体][font=宋体]抗体是一种免疫球蛋白,由[/font][font=Calibri]B[/font][font=宋体]淋巴细胞产生。抗体的单体是一个[/font][font=Calibri]Y[/font][font=宋体]形的分子,有[/font][font=Calibri]4[/font][font=宋体]条多肽链组成。其中包括两条相同的重链,以及两条相同的轻链,之间由双硫键连接在一起。每条重链[/font][font=Calibri]50kDa[/font][font=宋体],每条轻链[/font][font=Calibri]25kDa[/font][font=宋体],轻重链间存在二硫键链接。[/font][/font][font=宋体] [/font][font=宋体]轻链[/font][font=宋体][font=宋体]轻链包括可变区和恒定区,可变区约占轻链的[/font][font=Calibri]1/2[/font][font=宋体]。[/font][/font][font=宋体] [/font][font=宋体]重链[/font][font=宋体][font=宋体]重链包括可变区和恒定区。根据重链的不同,可以将抗体分为不同的种类,例如哺乳动物[/font] [font=Calibri]Ig [/font][font=宋体]的重链有α、δ、ε、γ和 μ 五种[/font][font=Calibri],[/font][font=宋体]相对应可以将哺乳动物[/font][font=Calibri]Ig[/font][font=宋体]分为 [/font][font=Calibri]IgA[/font][font=宋体]、[/font][font=Calibri]IgD[/font][font=宋体]、[/font][font=Calibri]IgE[/font][font=宋体]、[/font][font=Calibri]IgG [/font][font=宋体]和 [/font][font=Calibri]IgM [/font][font=宋体]五类。[/font][/font][font=宋体] [/font][font=宋体]可变区[/font][font=宋体][font=宋体]抗体分子的[/font][font=Calibri]N[/font][font=宋体]端存在一段氨基酸序列变化较大的区域,该区域称为可变区。可变区中存在可以与抗原特结合的部位,即抗原结合位点。一个抗体有两个抗原结合位点,可以同时结合两个抗原分子。在可变区中有三个区域的序列高度变化,成为高变区([/font][font=Calibri]hypervariable region[/font][font=宋体],[/font][font=Calibri]HVR[/font][font=宋体])又称为抗原互补决定区([/font][font=Calibri]complementarity determining region[/font][font=宋体],[/font][font=Calibri]CDR[/font][font=宋体])。可变区主要通过其[/font][font=Calibri]3[/font][font=宋体]个[/font][font=Calibri]CHR[/font][font=宋体]区形成[/font][font=Calibri]3[/font][font=宋体]个环状结构与抗原特异性结合。可变区中非[/font][font=Calibri]CDR[/font][font=宋体]部分成为骨架区([/font][font=Calibri]framework region[/font][font=宋体],[/font][font=Calibri]FR[/font][font=宋体]),其氨基酸组成和排列变化相对[/font][font=Calibri]CDR[/font][font=宋体]较少。[/font][/font][font=宋体] [/font][font=宋体]恒定区[/font][font=宋体][font=宋体]抗体分子[/font][font=Calibri]C[/font][font=宋体]端氨基酸序列相对稳定,该区域称为恒定区。同一种抗体的恒定区是相同的。抗体轻链的恒定区由一个[/font][font=Calibri]Ig[/font][font=宋体]结构域构成;重链的恒定区由[/font][font=Calibri]3-4[/font][font=宋体]个串联的[/font][font=Calibri]Ig[/font][font=宋体]结构域及一个用于增加灵活性的铰链区构成。[/font][font=Calibri]IgA[/font][font=宋体]、[/font][font=Calibri]IgE[/font][font=宋体]、[/font][font=Calibri]IgG[/font][font=宋体]有三个结构域([/font][font=Calibri]CH1[/font][font=宋体]、[/font][font=Calibri]CH2[/font][font=宋体]、[/font][font=Calibri]CH3[/font][font=宋体]),[/font][font=Calibri]IgD[/font][font=宋体]、[/font][font=Calibri]IgM[/font][font=宋体]有四个结构域([/font][font=Calibri]CH1[/font][font=宋体]、[/font][font=Calibri]CH2[/font][font=宋体]、[/font][font=Calibri]CH3[/font][font=宋体]、[/font][font=Calibri]CH4[/font][font=宋体])。不同种类抗体的铰链区存在一定的差异,[/font][font=Calibri]IgA[/font][font=宋体]的铰链区较短,[/font][font=Calibri]IgD [/font][font=宋体]的铰链区较长,[/font][font=Calibri]IgM [/font][font=宋体]和[/font][font=Calibri]IgE [/font][font=宋体]无铰链区。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Fab[/font][font=宋体]片段[/font][/font][font=宋体][font=Calibri]IgG[/font][font=宋体]分子在木瓜蛋白酶的作用下可以被降解为两个[/font][font=Calibri]Fab[/font][font=宋体]段及一个[/font][font=Calibri]Fc[/font][font=宋体]段。[/font][font=Calibri]Fab[/font][font=宋体]段由抗体轻链的可变区、轻链的恒定区、重链的可变区及重链恒定区构成。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Fc[/font][font=宋体]段[/font][/font][font=宋体][font=Calibri]Fc[/font][font=宋体]段包含了所有抗体分子共有的蛋白质序列以及各个类别独有的决定簇。[/font][font=Calibri]Fc[/font][font=宋体]段有多种生物学活性,具有结合补体、结合[/font][font=Calibri]Fc[/font][font=宋体]受体、通过胎盘等作用。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多关于[url=https://cn.sinobiological.com/resource/antibody-technical/antibody-structure-function][b]抗体的结构和功能[/b][/url]详情:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/antibody-structure-function[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
来自清华大学生科院、医学院、普林斯顿大学Lewis Thomas实验室等单位的研究人员报道了一种重要的转运因子的蛋白结构,这一结构的6个跨膜区域以未报道过的新折叠形式出现,这一发现对于了解核黄素(维生素B2)的运输,以及进一步拓展其生物学结构具有重要意义。研究论文发表在最近一期《自然》(Nature)杂志上。 文章的通讯作者是清华大学生命科学院院长施一公教授,其研究组主要致力于运用结构生物学和生物化学的手段研究肿瘤发生和细胞调亡的分子机制:专注于肿瘤抑制因子和细胞凋亡调节蛋白的结构和功能研究、重大疾病相关膜蛋白的结构与功能研究、胞内生物大分子元件的结构与功能研究。另外两位作者分别是王佳伟(Jiawei Wang)和张鹏(Peng Zhang)。该研究组近期研究发现了一类重要的蛋白:能量耦合因子(energy-coupling factor,ECF)转运蛋白,这类蛋白是一些微量营养元素的运输因子,负责原核生物的维生素摄入。每个ECF转运因子都包含一种嵌入细胞膜的能结合底物的蛋白结构——S组件。这一结构是能量耦合的关键部件,由两个ATP结合蛋白和一个跨膜蛋白组成。然而目前这一结构的具体构架,以及运输机制并不清楚。
我是做蛋白结构解析的。蛋白与配体具有强亲和性结合,那么每个氨基酸化学位移的变化是否能用化学位移滴定法跟踪,为何?这个问题困扰我的实验,求解……谢谢帮助!
[font=宋体][font=宋体]跨膜蛋白按功能可以分为多种类型,其中包括[/font][font=Calibri]G[/font][font=宋体]蛋白偶联受体([/font][font=Calibri]G[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url][/font][font=宋体])、离子通道、转运蛋白以及其他类型受体等。这些蛋白在细胞内发挥着不同的作用,例如在信号传递、物质转运和细胞通讯等方面。[/font][font=Calibri]G[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url][/font][font=宋体]是一类广泛存在于生物体中的跨膜蛋白,它们可以识别并与外界分子相互作用,从而引发各种细胞内信号,因此它们被用作药物筛选的靶标。离子通道则可以调节细胞内外的离子浓度,如钠离子、钾离子、钙离子等,这对于细胞的正常运作至关重要。转运蛋白则可以协助物质的跨膜运输,对生物体代谢进行调控。这些跨膜蛋白虽然功能不同,但是在生物体中发挥着各自独特和不可或缺的作用。[/font][/font][font=宋体] [/font][font=宋体]一型跨膜蛋白和二型跨膜蛋白是两种常见的膜蛋白类型,它们在结构和功能上存在差异。下面是它们的简要对比图解:[/font][font=宋体]一型跨膜蛋白:[/font][font=宋体] [/font][font=宋体] [font=宋体]———————[/font][/font][font=宋体] [font=Calibri]| [/font][font=宋体]膜外 [/font][font=Calibri]|[/font][/font][font=宋体] [font=Calibri]| [/font][font=宋体]区域 [/font][font=Calibri]|[/font][/font][font=宋体] [font=宋体]———————[/font][/font][font=宋体] [font=Calibri]| [/font][font=宋体]跨膜 [/font][font=Calibri]|[/font][/font][font=宋体] [font=Calibri]| [/font][font=宋体]螺旋 [/font][font=Calibri]|[/font][/font][font=宋体] [font=宋体]———————[/font][/font][font=宋体] [font=Calibri]| [/font][font=宋体]膜内 [/font][font=Calibri]|[/font][/font][font=宋体] [font=Calibri]| [/font][font=宋体]区域 [/font][font=Calibri]|[/font][/font][font=宋体] [font=宋体]———————[/font][/font][font=宋体][font=宋体]一型跨膜蛋白具有一个跨越细胞膜的[/font] [font=宋体]α 螺旋结构。它包括一个在细胞外区域的 [/font][font=Calibri]N [/font][font=宋体]端、一个跨膜螺旋结构和一个在细胞内区域的 [/font][font=Calibri]C [/font][font=宋体]端。这种结构使得一型跨膜蛋白在跨越细胞膜时保持稳定,并具有信号传递和细胞识别等重要功能。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体]二型跨膜蛋白:[/font][font=宋体] [/font][font=宋体] [font=宋体]———————[/font][/font][font=宋体] [font=Calibri]| [/font][font=宋体]膜外 [/font][font=Calibri]|[/font][/font][font=宋体] [font=Calibri]| [/font][font=宋体]区域 [/font][font=Calibri]|[/font][/font][font=宋体] [font=宋体]———————[/font][/font][font=宋体] [font=Calibri]| [/font][font=宋体]跨膜 [/font][font=Calibri]|[/font][/font][font=宋体] [font=Calibri]| [/font][font=宋体]区域 [/font][font=Calibri]|[/font][/font][font=宋体] [font=宋体]———————[/font][/font][font=宋体] [font=Calibri]| [/font][font=宋体]膜内 [/font][font=Calibri]|[/font][/font][font=宋体] [font=Calibri]| [/font][font=宋体]区域 [/font][font=Calibri]|[/font][/font][font=宋体] [font=宋体]———————[/font][/font][font=宋体] [font=Calibri]| [/font][font=宋体]胞质 [/font][font=Calibri]|[/font][/font][font=宋体] [font=Calibri]| [/font][font=宋体]尾部 [/font][font=Calibri]|[/font][/font][font=宋体] [font=宋体]———————[/font][/font][font=宋体] [/font][font=宋体][font=宋体]二型跨膜蛋白同样具有跨越细胞膜的结构,但它包括一个在细胞内区域的[/font] [font=Calibri]C [/font][font=宋体]端和一个在胞质尾部的结构。二型跨膜蛋白通常通过细胞内区域与一些信号转导途径进行相互作用,并发挥重要的调节和调控功能。[/font][/font][font=宋体] [/font][font=宋体]一型跨膜蛋白通过单一的跨膜螺旋结构连接细胞内外区域,而二型跨膜蛋白则包含额外的胞质尾部。这些结构差异导致两种跨膜蛋白在细胞中的功能和相互作用方式上存在差异。[/font][font=宋体] [/font][font=宋体]目前义翘神州提供[url=https://cn.sinobiological.com/resource/protein-review/transmembrane-proteins][b]跨膜蛋白表达和制备平台[/b][/url],包含[/font][font=宋体][font=宋体]①[/font][font=Calibri]VLP[/font][font=宋体]技术平台:它可以将完整天然构象的膜蛋白展示在类病毒颗粒表面,这种方法不仅可以保留膜蛋白的完整结构,同时也能够真实地模拟其在细胞膜上的位置和构象;[/font][/font][font=宋体][font=宋体]②去垢剂技术平台:由于存在疏水结构域,跨膜蛋白与膜的结合非常紧密,需要用去垢剂([/font][font=Calibri]detergent[/font][font=宋体])才能从膜上洗涤下来,[/font][font=Calibri]Detergent[/font][font=宋体]作为一种两亲性分子,疏水尾部包裹目的蛋白的疏水区域,亲水头部位于与溶液接触的界面。微团的形成是膜蛋白增溶的基础,当去垢剂浓度高于[/font][font=Calibri]CMC[/font][font=宋体]([/font][font=Calibri]Critical micelle concentration[/font][font=宋体],临界胶束浓度)时会形成微团,增溶后,去垢剂将蛋白周围的磷脂置换,从而实现收集目标膜蛋白的目的,后续再进行蛋白纯化,最终蛋白呈现在含有[/font][font=Calibri]Detergent[/font][font=宋体]的溶液中。义翘神州成功搭建了去垢剂技术平台,利用该平台可有效提高跨膜蛋白的产量和纯度。[/font][/font][font=宋体][font=宋体]③[/font][font=Calibri]Nanodisc[/font][font=宋体]技术平台:义翘神州已成功搭建了[/font][font=Calibri]Nanodisc[/font][font=宋体]技术平台,利用跨膜蛋白与磷脂结合能够维持其良好活性的特性,制备出稳定的产品,满足动物免疫、抗体筛选、[/font][font=Calibri]cell-based assays[/font][font=宋体]等场景。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/transmembrane-proteins[/font][/font]
德国Gerhardt格哈特听闻此德国三粗(粗蛋白、粗脂肪、粗纤维)仪器厂家到2016年已有170年历史,哪位大神知道此厂家的历史可以分享一下吗?
改性腈纶和蛋白改性聚丙烯腈纤维显微镜下观察有什么不同?
[font=宋体][font=宋体]抗体融合蛋白([/font][font=Calibri]Ig[/font][font=宋体]融合蛋白)是指在基因水平上将目的基因同免疫球蛋白部分片段基因相连,并在真核或原核表达系统中表达的重组蛋白。抗体融合蛋白具有抗体的特性及融合功能蛋白的活性,可广泛应用于免疫诊断、免疫治疗、抗体纯化及抗体和抗原的定量分析等,特别可用于免疫导向药物的制备。根据结合的[/font][font=Calibri]Ig[/font][font=宋体]片段的不同,可以将抗体融合蛋白分为[/font][font=Calibri]Fab[/font][font=宋体]融合蛋白、[/font][font=Calibri]Fc[/font][font=宋体]融合蛋白与单链抗体([/font][font=Calibri]scFv[/font][font=宋体])融合蛋白。[/font][/font][font=宋体] [/font][font=宋体][b]抗体融合蛋白结构:[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]Fab[/font][font=宋体]融合蛋白、单链抗体融合蛋白研究表明,抗体可变区的[/font][font=Calibri]N[/font][font=宋体]端空间结构上与互补决定区([/font][font=Calibri]CDR[/font][font=宋体])形成的抗原结合部位十分接近,有的抗体可变区[/font][font=Calibri]N[/font][font=宋体]端残基甚至直接参与抗原结合部位的形成,如果将效应蛋白与抗体片段的[/font][font=Calibri]N[/font][font=宋体]端结合,可能对抗体可变区的空间构型造成较大影响,从而降低抗体与抗原的结合能力。因此,通常将蛋白与抗体片段的[/font][font=Calibri]C[/font][font=宋体]端进行结合,形成抗体融合蛋白。[/font][/font][font=宋体] [/font][b][font=宋体][font=Calibri]Fc[/font][font=宋体]融合蛋白[/font][/font][/b][font=宋体] [/font][font=宋体][font=Calibri]Fc[/font][font=宋体]融合蛋白在结构上是将抗体的[/font][font=Calibri]Fc[/font][font=宋体]区与功能蛋白进行融合,可将[/font][font=Calibri]Fc[/font][font=宋体]的[/font][font=Calibri]N[/font][font=宋体]端或[/font][font=Calibri]C[/font][font=宋体]端与目的基因进行融合。根据结合蛋白的不同,可以有多种构型。[/font][/font][font=宋体] [/font][font=宋体][b]抗体融合蛋白作用原理:[/b][/font][font=宋体] [/font][font=宋体]含有抗体可变区的抗体融合蛋白[/font][font=宋体] [/font][font=宋体][font=Calibri]Fab[/font][font=宋体]融合蛋白与[/font][font=Calibri]scFv[/font][font=宋体]融合蛋白含有抗体的可变区,可以进行抗原[/font][font=Calibri]-[/font][font=宋体]抗体反应,其作用原理为利用抗体[/font][font=Calibri]-[/font][font=宋体]抗原特异性结合的特性,通过这种特性的引导,将具有生物活性的蛋白靶向引导至细胞的特定部位,进而发挥一定的生物效应。[/font][/font][font=宋体] [/font][font=宋体]不含抗体可变区的抗体融合蛋白[/font][font=宋体] [/font][font=宋体][font=宋体]该类融合蛋白含有的抗体功能区为[/font][font=Calibri]Fc[/font][font=宋体]区,不能进行抗原[/font][font=Calibri]-[/font][font=宋体]抗体反应,[/font][font=Calibri]Fc[/font][font=宋体]段的作用为延长药物在血浆内的半衰期、增加融合蛋白的稳定性等。[/font][font=Calibri]Fc[/font][font=宋体]融合蛋白药理作用的发挥依赖于功能蛋白部分,利用受体[/font][font=Calibri]-[/font][font=宋体]配体之间的相互作用产生一系列的生物学效应。[/font][/font][font=宋体] [/font][font=宋体][b]抗体融合蛋白制备:[/b][/font][font=宋体] [/font][font=宋体]最初抗体融合蛋白制备的方法为化学交联法,但这种方法制备的抗体融合蛋白组成不均一、性能不稳定、免疫源性大,随着基因工程技术的发展,该技术已被淘汰。目前主要利用基因工程技术来进行抗体融合蛋白的制备。[/font][font=宋体] [/font][font=宋体][font=宋体]其制备原理为:将抗体基因与目的蛋白基因通过一段接头序列([/font][font=Calibri]linker[/font][font=宋体])进行链接,然后将链接产物亚克隆至载体中,并用原核或者真核表达系统进行表达。制备抗体融合蛋白过程中,一个关键的问题是两蛋白间的接头序列[/font][font=Calibri](Linker)[/font][font=宋体]的长度,[/font][font=Calibri]linker[/font][font=宋体]的长短对蛋白质的折叠和稳定性非常重要。如果接头序列太短,可能影响两蛋白高级[/font][font=Calibri]-[/font][font=宋体]结构的折叠,从而相互干扰;如果接头序列太长,又涉及免疫原性的问题。抗体融合蛋白与双特异性抗体抗体融合蛋白是将抗体的部分片段与目的蛋白进行融合表达得到的重组蛋白,若将两个具有不同抗原特异性的抗体片段连接至同一蛋白,即可得到双特异性抗体。[/font][/font][font=宋体] [/font][font=宋体][b]单克隆抗体与抗体融合蛋白区别:[/b][/font][font=宋体] [/font][font=宋体]单克隆抗体抗体[/font][font=宋体] [/font][font=宋体][font=宋体]结构:[/font][font=Calibri]Y[/font][font=宋体]型[/font][/font][font=宋体][font=宋体]制备方法:杂交瘤技术[/font][font=Calibri]/[/font][font=宋体]基因重组[/font][/font][font=宋体][font=宋体]表达系统:真核系统[/font][font=Calibri]/[/font][font=宋体]原核系统[/font][/font][font=宋体][font=宋体]真核系统[/font][font=Calibri]/[/font][font=宋体]原核系统[/font][/font][font=宋体][font=宋体]作用原理:特异性识别抗原,[/font][font=Calibri]Fc[/font][font=宋体]段引起[/font][font=Calibri]ADCC[/font][font=宋体]、[/font][font=Calibri]ADCP[/font][font=宋体]、[/font][font=Calibri]CDC[/font][font=宋体]等作用。[/font][/font][font=宋体] [/font][font=宋体]抗体融合蛋白[/font][font=宋体] [/font][font=宋体]结构:具有多种结构[/font][font=宋体]制备方法:基因重组[/font][font=宋体][font=宋体]表达系统:真核系统[/font][font=Calibri]/[/font][font=宋体]原核系统[/font][/font][font=宋体][font=宋体]作用原理:功能蛋白与靶分子间的受体[/font][font=Calibri]-[/font][font=宋体]配体的相互作用[/font][/font][font=宋体] [/font][font=宋体][font=宋体]详情可以参考:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/fusion-protein[/font][/font][font=Calibri] [/font]
[color=#333333]老师有下面这个标准吗?成分分析中见过这种纤维吗?[/color][color=#333333]FZ/T 50018-2013《蛋白粘胶纤维蛋白质含量[/color][color=#333333]试验方法》?[/color]
有没有做过黑木耳或类似产品的朋友,现在急需总糖、粗蛋白、粗脂肪粗纤维经验值。gb/t6192-2008中要求总糖(以转化糖计)大于等于22%粗蛋白大于等于7%粗脂肪大于等于0.4%粗纤维3.0-6.0%另外,产品标准上要求以转化糖计,而给的方法标准上则是用葡萄糖滴定。要求以转化糖计的,转化糖是不是要用蔗糖水解以后制得,不能用葡萄糖代替吧?急啊!!谁能帮帮忙,谢谢!!
求一张金属硫蛋白分子结构的三维图片,需要彩色高清!谢谢!
羊绒蛋白纤维,这个里面没有羊绒,这个名称合规吗?