[font=宋体][font=宋体]抗体融合蛋白([/font][font=Calibri]Ig[/font][font=宋体]融合蛋白)是指在基因水平上将目的基因同免疫球蛋白部分片段基因相连,并在真核或原核表达系统中表达的重组蛋白。抗体融合蛋白具有抗体的特性及融合功能蛋白的活性,可广泛应用于免疫诊断、免疫治疗、抗体纯化及抗体和抗原的定量分析等,特别可用于免疫导向药物的制备。根据结合的[/font][font=Calibri]Ig[/font][font=宋体]片段的不同,可以将抗体融合蛋白分为[/font][font=Calibri]Fab[/font][font=宋体]融合蛋白、[/font][font=Calibri]Fc[/font][font=宋体]融合蛋白与单链抗体([/font][font=Calibri]scFv[/font][font=宋体])融合蛋白。[/font][/font][font=宋体] [/font][font=宋体][b]抗体融合蛋白结构:[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]Fab[/font][font=宋体]融合蛋白、单链抗体融合蛋白研究表明,抗体可变区的[/font][font=Calibri]N[/font][font=宋体]端空间结构上与互补决定区([/font][font=Calibri]CDR[/font][font=宋体])形成的抗原结合部位十分接近,有的抗体可变区[/font][font=Calibri]N[/font][font=宋体]端残基甚至直接参与抗原结合部位的形成,如果将效应蛋白与抗体片段的[/font][font=Calibri]N[/font][font=宋体]端结合,可能对抗体可变区的空间构型造成较大影响,从而降低抗体与抗原的结合能力。因此,通常将蛋白与抗体片段的[/font][font=Calibri]C[/font][font=宋体]端进行结合,形成抗体融合蛋白。[/font][/font][font=宋体] [/font][b][font=宋体][font=Calibri]Fc[/font][font=宋体]融合蛋白[/font][/font][/b][font=宋体] [/font][font=宋体][font=Calibri]Fc[/font][font=宋体]融合蛋白在结构上是将抗体的[/font][font=Calibri]Fc[/font][font=宋体]区与功能蛋白进行融合,可将[/font][font=Calibri]Fc[/font][font=宋体]的[/font][font=Calibri]N[/font][font=宋体]端或[/font][font=Calibri]C[/font][font=宋体]端与目的基因进行融合。根据结合蛋白的不同,可以有多种构型。[/font][/font][font=宋体] [/font][font=宋体][b]抗体融合蛋白作用原理:[/b][/font][font=宋体] [/font][font=宋体]含有抗体可变区的抗体融合蛋白[/font][font=宋体] [/font][font=宋体][font=Calibri]Fab[/font][font=宋体]融合蛋白与[/font][font=Calibri]scFv[/font][font=宋体]融合蛋白含有抗体的可变区,可以进行抗原[/font][font=Calibri]-[/font][font=宋体]抗体反应,其作用原理为利用抗体[/font][font=Calibri]-[/font][font=宋体]抗原特异性结合的特性,通过这种特性的引导,将具有生物活性的蛋白靶向引导至细胞的特定部位,进而发挥一定的生物效应。[/font][/font][font=宋体] [/font][font=宋体]不含抗体可变区的抗体融合蛋白[/font][font=宋体] [/font][font=宋体][font=宋体]该类融合蛋白含有的抗体功能区为[/font][font=Calibri]Fc[/font][font=宋体]区,不能进行抗原[/font][font=Calibri]-[/font][font=宋体]抗体反应,[/font][font=Calibri]Fc[/font][font=宋体]段的作用为延长药物在血浆内的半衰期、增加融合蛋白的稳定性等。[/font][font=Calibri]Fc[/font][font=宋体]融合蛋白药理作用的发挥依赖于功能蛋白部分,利用受体[/font][font=Calibri]-[/font][font=宋体]配体之间的相互作用产生一系列的生物学效应。[/font][/font][font=宋体] [/font][font=宋体][b]抗体融合蛋白制备:[/b][/font][font=宋体] [/font][font=宋体]最初抗体融合蛋白制备的方法为化学交联法,但这种方法制备的抗体融合蛋白组成不均一、性能不稳定、免疫源性大,随着基因工程技术的发展,该技术已被淘汰。目前主要利用基因工程技术来进行抗体融合蛋白的制备。[/font][font=宋体] [/font][font=宋体][font=宋体]其制备原理为:将抗体基因与目的蛋白基因通过一段接头序列([/font][font=Calibri]linker[/font][font=宋体])进行链接,然后将链接产物亚克隆至载体中,并用原核或者真核表达系统进行表达。制备抗体融合蛋白过程中,一个关键的问题是两蛋白间的接头序列[/font][font=Calibri](Linker)[/font][font=宋体]的长度,[/font][font=Calibri]linker[/font][font=宋体]的长短对蛋白质的折叠和稳定性非常重要。如果接头序列太短,可能影响两蛋白高级[/font][font=Calibri]-[/font][font=宋体]结构的折叠,从而相互干扰;如果接头序列太长,又涉及免疫原性的问题。抗体融合蛋白与双特异性抗体抗体融合蛋白是将抗体的部分片段与目的蛋白进行融合表达得到的重组蛋白,若将两个具有不同抗原特异性的抗体片段连接至同一蛋白,即可得到双特异性抗体。[/font][/font][font=宋体] [/font][font=宋体][b]单克隆抗体与抗体融合蛋白区别:[/b][/font][font=宋体] [/font][font=宋体]单克隆抗体抗体[/font][font=宋体] [/font][font=宋体][font=宋体]结构:[/font][font=Calibri]Y[/font][font=宋体]型[/font][/font][font=宋体][font=宋体]制备方法:杂交瘤技术[/font][font=Calibri]/[/font][font=宋体]基因重组[/font][/font][font=宋体][font=宋体]表达系统:真核系统[/font][font=Calibri]/[/font][font=宋体]原核系统[/font][/font][font=宋体][font=宋体]真核系统[/font][font=Calibri]/[/font][font=宋体]原核系统[/font][/font][font=宋体][font=宋体]作用原理:特异性识别抗原,[/font][font=Calibri]Fc[/font][font=宋体]段引起[/font][font=Calibri]ADCC[/font][font=宋体]、[/font][font=Calibri]ADCP[/font][font=宋体]、[/font][font=Calibri]CDC[/font][font=宋体]等作用。[/font][/font][font=宋体] [/font][font=宋体]抗体融合蛋白[/font][font=宋体] [/font][font=宋体]结构:具有多种结构[/font][font=宋体]制备方法:基因重组[/font][font=宋体][font=宋体]表达系统:真核系统[/font][font=Calibri]/[/font][font=宋体]原核系统[/font][/font][font=宋体][font=宋体]作用原理:功能蛋白与靶分子间的受体[/font][font=Calibri]-[/font][font=宋体]配体的相互作用[/font][/font][font=宋体] [/font][font=宋体][font=宋体]详情可以参考:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/fusion-protein[/font][/font][font=Calibri] [/font]
[font=宋体][font=宋体]抗体融合蛋白是一种将抗体片段与功能蛋白融合表达的重组蛋白,具有抗体的特性和功能蛋白的活性。它可广泛应用于免疫诊断、免疫治疗、抗体纯化、抗体和抗原的定量分析以及免疫导向药物的制备等领域。根据结合的[/font][font=Calibri]Ig[/font][font=宋体]片段的不同,可以将抗体融合蛋白分为[/font][font=Calibri]Fab[/font][font=宋体]融合蛋白、[/font][font=Calibri][url=https://cn.sinobiological.com/resource/protein-review/fc-fusion-proteins][b]Fc[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/resource/protein-review/fc-fusion-proteins][b]融合蛋白[/b][/url]与[url=https://cn.sinobiological.com/resource/antibody-technical/scfv-antibody-production][b]单链抗体([/b][/url][/font][font=Calibri][url=https://cn.sinobiological.com/resource/antibody-technical/scfv-antibody-production][b]scFv[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/resource/antibody-technical/scfv-antibody-production][b])[/b][/url]融合蛋白。制备抗体融合蛋白的方法主要有化学交联法和基因工程技术,其中基因工程技术是目前主要的方法。在制备过程中,需要注意两蛋白间的接头序列的长度,以确保蛋白质的折叠和稳定性。抗体融合蛋白在免疫学、生物制药和医学等领域具有广泛的应用前景,为疾病的诊断、治疗和药物研发提供了新的工具和方法。[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]双特异性抗体如何与蛋白融合[/font][font=Calibri]?[/font][/font][/b][font=宋体] [/font][font=宋体]双特异性抗体是一种特殊的抗体,具有两个不同的抗原结合位点。通过技术手段,可以将双特异性抗体与另一种蛋白质融合。[/font][font=宋体] [/font][font=宋体]①使用基因工程技术,将双特异性抗体的基因与目标蛋白质的基因进行融合,然后通过表达载体在细胞内表达融合蛋白质。[/font][font=宋体] [/font][font=宋体]②使用化学手段,将双特异性抗体与目标蛋白质进行化学偶联。这需要使用特定的化学偶联剂,将双特异性抗体的特定基团与目标蛋白质的特定基团连接起来。[/font][font=宋体] [/font][font=宋体]需要注意的是,融合蛋白质的功能和性质取决于其组成成分的特性和比例,因此在融合过程中需要谨慎选择和设计组成成分,以确保融合蛋白质具有所需的功能和性质。[/font][font=宋体] [/font][b][font=宋体]抗体融合蛋白具有广泛的应用,包括但不限于以下方面:[/font][/b][font=宋体] [/font][font=宋体]①免疫诊断:抗体融合蛋白可以用于检测抗原,如病毒、细菌、肿瘤标志物等。通过将抗体片段与荧光蛋白、酶等标记物结合,可以实现对抗原的高灵敏度检测。[/font][font=宋体]②免疫治疗:抗体融合蛋白可以用于治疗肿瘤、感染性疾病等。通过将抗体片段与细胞毒素、免疫调节因子等效应分子结合,可以实现对肿瘤细胞的靶向杀伤或调节免疫反应。[/font][font=宋体]③抗体纯化:抗体融合蛋白可以用于分离和纯化抗体。通过将抗体片段与亲和标签结合,可以利用亲和层析等技术实现对抗体的纯化和富集。[/font][font=宋体]抗体和抗原的定量分析:抗体融合蛋白可以用于定量分析抗体和抗原的浓度。通过将抗体片段与荧光染料等标记物结合,可以利用流式细胞术等技术实现对抗体和抗原的定量分析。[/font][font=宋体]④免疫导向药物的制备:抗体融合蛋白可以用于制备免疫导向药物,即将药物与抗体片段结合,利用抗体的特异性结合能力,将药物定向引导至病变部位,提高药物的疗效并降低副作用。[/font][font=宋体] [/font][font=宋体][font=宋体]更多[url=https://cn.sinobiological.com/resource/antibody-technical/bispecific-antibody][b]双特异性抗体[/b][/url]详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/bispecific-antibody[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
[font=宋体][font=宋体]无细胞蛋白表达是一种体外重组蛋白质表达技术也称为无细胞蛋白质合成技术([/font][font=Calibri]CFPS[/font][font=宋体]:[/font][font=Calibri]Cell-free protein synthesis[/font][font=宋体]),是指用含有蛋白合成必需的组分(核糖体,转运[/font][font=Calibri]RNA[/font][font=宋体],氨酰合成酶,启动[/font][font=Calibri]/[/font][font=宋体]延伸[/font][font=Calibri]/[/font][font=宋体]终止因子,三磷酸鸟苷,[/font][font=Calibri]ATP[/font][font=宋体],[/font][font=Calibri]Mg2+[/font][font=宋体]和[/font][font=Calibri]K+[/font][font=宋体])的细胞裂解物在体外进行蛋白合成。无细胞蛋白表达技术适用于制备各种类型的蛋白质,包括难表达蛋白质、毒性蛋白质、复杂蛋白质等。在药物研究、生物制造和生命科学等领域中得到广泛关注和应用,无论是研究、开发还是商业化应用过程。目前无细胞蛋白表达主要应用于药物研发领域,例如抗体制备和生物药物生产等。随着人工智能技术的不断发展,无细胞蛋白表达技术可以与人工智能算法结合,构建计算机辅助的高通量生产系统,实现个性化、精准的生物医学治疗。除此之外,还能够应用于其他领域,例如基因工程、环境保护和农业生产等。随着无细胞蛋白表达技术的不断发展和人工智能技术的不断进步,我们可以看到更多的新领域和新应用出现,给生物科技行业带来更多的机遇和挑战。[/font][/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体]相较于传统的活细胞蛋白表达技术,无细胞蛋白表达技术具有以下几个显著的优势:[/font][/b][font=宋体] [/font][font=宋体][font=Calibri]1. [/font][font=宋体]更高的蛋白质表达量:传统的活细胞蛋白表达技术受限于细胞本身的多方面因素,其表达的蛋白质数量往往受到限制。而无细胞蛋白表达技术通过在体外底物浓度高的环境中进行合成反应,不但避免了传统活细胞表达所面临的方方面面的限制,还能够很好地控制反应体系,从而获得表达量更高的蛋白质。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2. [/font][font=宋体]更快的表达速度:传统活细胞蛋白表达需要细胞生长并达到最佳密度才能进行蛋白质表达,这个过程往往需要数天时间。而无细胞蛋白表达技术通常只需要数小时就能够完成蛋白质的表达,这个速度明显快于传统活细胞表达技术。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3. [/font][font=宋体]更精准的蛋白质合成:无细胞蛋白表达技术在体外进行蛋白质合成,能够精确控制底物浓度、反应温度、反应剂比例等参数,因此可以更加精准地合成定制的蛋白质,这对于研究和应用来讲具有重要意义。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4. [/font][font=宋体]更灵活控制:在无细胞蛋白表达技术中,可以使用分离的组分体系进行蛋白质的合成,可以控制底物和反应剂的比例,也可以在适当的反应条件下进行自定义的修饰,如蛋白质标记、药效分析等。这些优点使得无细胞蛋白表达技术更加灵活、可控,适用于更广泛的应用领域。[/font][/font][font=宋体] [/font][b][font=宋体] [/font][font=宋体]无细胞蛋白表达应用[/font][/b][font=宋体] [/font][font=宋体]无细胞蛋白表达技术是一种飞速发展的新型生物技术,具有广阔的应用前景和潜力。该技术可以快速、高效、经济地合成蛋白质,可广泛应用于医疗、制药、农业、生物材料等多个领域。[/font][font=宋体] [/font][font=宋体][font=Calibri]1. [/font][font=宋体]医疗领域:无细胞蛋白表达技术在医疗领域应用广泛,可以用于生产多种蛋白质药品,如单克隆抗体等。其中,单克隆抗体是一种重要的治疗药物,具有高度特异性和亲和力,可用于肿瘤、心血管疾病、自身免疫性疾病等疾病的治疗。传统单克隆抗体生产方法需要花费大量时间和成本,而无细胞蛋白表达技术则可以在短时间内大规模合成单克隆抗体,从而大大缩短生产周期,并且可以降低成本。此外,无细胞蛋白表达技术也可以用于疫苗研发。比如疟疾疫苗研究开发昂贵又耗时,目前利用[/font][font=Calibri]WGE[/font][font=宋体]系统可加速疫苗研发,并建立高通量疟原虫抗体筛查系统。[/font][font=Calibri]Stark[/font][font=宋体]等利用大肠杆菌的便携式冻干裂解物再水化,[/font][font=Calibri]1h[/font][font=宋体]内合成高致病性病原体土拉弗朗西斯菌亚种的生物偶联疫苗,与工程菌生产的疫苗相比,其可引发更高水平的病原体特异性抗体。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2. [/font][font=宋体]制药领域:是无细胞蛋白表达技术的一个重要应用领域。药物开发的成功率取决于药物分子对目标蛋白的亲和力,而目标蛋白对于专一的细胞表达系统和分类的组织或器官非常敏感。通过无细胞蛋白表达技术,研究人员可以在不依赖于细胞的情况下直接生产大量需要的蛋白质,为药物研发提供了更快更便捷的方法。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3. [/font][font=宋体]基础研究领域:利用无细胞蛋白质合成系统可以直接对表达产物进行核磁共振分析,目前已确定了数千个蛋白质的结构。可以通过合成蛋白质建立蛋白质阵列,解开基因产物的功能;应用核糖体展示和 [/font][font=Calibri]mRNA [/font][font=宋体]展示技术,更有利于实现高通量筛选,全面深入研究基因特征和功能。通过无细胞蛋白表达技术可以实现对大型蛋白质的生产和分析,同时也为基础研究打开了新的研究领域。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]目前义翘神州无细胞合成服务正在活动中,活动时间[/font][font=Calibri]2023[/font][font=宋体]年[/font][font=Calibri]10[/font][font=宋体]月[/font][font=Calibri]23[/font][font=宋体]日[/font][font=Calibri]-12[/font][font=宋体]月[/font][font=Calibri]31[/font][font=宋体]日。有需求的可以咨询或者进入义翘神州网进行查看。更多详情可以关注[/font][font=Calibri]https://cn.sinobiological.com/services/cell-free-protein-synthesis-service[/font][/font]
[font=宋体][font=宋体]重组蛋白是利用[/font][font=Calibri]DNA(RNA)[/font][font=宋体]重组技术表达的蛋白重组。蛋白表达是将目的基因通过电转化或者热激等手段转入合适的宿主中,利用宿主的特定生理、生化和遗传特点进行目标蛋白大量表达及纯化的生物技术。目前,较为主流的表达宿主有大肠杆菌([/font][font=Calibri]E.coli[/font][font=宋体])、毕赤酵母([/font][font=Calibri]P.pastoris[/font][font=宋体])、昆虫[/font][font=Calibri]-[/font][font=宋体]杆状病毒([/font][font=Calibri]Bac-to-Bac[/font][font=宋体]系统)以及哺乳动物细胞系([/font][font=Calibri]CHO[/font][font=宋体]、[/font][font=Calibri]HEK293[/font][font=宋体])等。鉴于目标蛋白的应用场景和自身理化性质的差异,选择合适的表达宿主尤为关键。[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]大肠杆菌([/font][font=Calibri]E.coli[/font][font=宋体]):[/font][/font][/b][font=宋体] [/font][font=宋体]表达系统:原核[/font][font=宋体]优势:经济、快速、高产量、应用广泛[/font][font=宋体]劣势:包涵体;无翻译后修饰;大分子蛋白表达困难[/font][font=宋体]推荐表达:细菌类蛋白;抗原类蛋白;细胞因子;酶类[/font][font=宋体] [/font][b][font=宋体]酵母细胞:[/font][/b][font=宋体]表达系统:真核[/font][font=宋体]优势:经济、快速、高产量;部分翻译修饰[/font][font=宋体]劣势:非人源糖基化;高甘露糖修饰[/font][font=宋体]推荐表达:细胞因子;少分子量蛋白;酶类[/font][font=宋体] [/font][b][font=宋体][font=宋体]杆状病毒[/font][font=Calibri]-[/font][font=宋体]昆虫细胞:[/font][/font][/b][font=宋体]表达系统:真核[/font][font=宋体]优势:基因容量大;可溶蛋白;适合毒性蛋白;类似哺乳动物系统;翻译后修饰[/font][font=宋体]劣势:周期长;成本高;缺少部分糖基化[/font][font=宋体]推荐表达:细胞质蛋白;毒性蛋白;跨膜蛋白;分泌蛋白;激酶;[/font][font=宋体] [/font][b][font=宋体]哺乳动物细胞[/font][font=宋体]表达[/font][font=宋体]:[/font][/b][font=宋体]表达系统:真核[/font][font=宋体]优势:可溶蛋白;更低内毒素;更好的活性;更好的翻译后修饰;可瞬时转染与稳定转染表达[/font][font=宋体]劣势:周期长;成本高;[/font][font=宋体]推荐表达:分泌蛋白;跨膜蛋白;重组抗体;抗体等[/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州拥有原核细胞表达平台、哺乳动物瞬时表达平台、杆状病毒[/font][font=Calibri]-[/font][font=宋体]昆虫蛋白表达平台,同时提供[url=https://cn.sinobiological.com/services/e-coli-protein-expression-service][b]原核([/b][/url][/font][font=Calibri][url=https://cn.sinobiological.com/services/e-coli-protein-expression-service][b]E. coli[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/services/e-coli-protein-expression-service][b])蛋白表达服务[/b][/url]……可实现重组蛋白和重组抗体的高通量和高产量表达,可为客户提供[url=https://cn.sinobiological.com/services/recombinant-antibody-production-service][b]重组表达服务[/b][/url]及一站式定制需求。详情可以关注 大肠杆菌蛋白表达平台:[/font][font=Calibri]https://cn.sinobiological.com/services/platform/e-coli-protein-expression[/font][/font][font=宋体] [/font][font=宋体] [/font]
[font=宋体][font=宋体]抗体融合蛋白,亦被称为[/font][font=Calibri]Ig[/font][font=宋体]融合蛋白,是通过在基因层面上巧妙地将目标基因与免疫球蛋白的部分基因片段相互连接,随后在真核或原核表达系统中实现表达而得到的一种重组蛋白。这种独特的蛋白不仅继承了抗体的卓越特性,更融合了功能蛋白的活性,使其在多个领域展现出广泛的应用前景。[/font][/font][font=宋体] [/font][font=宋体]在免疫诊断领域,抗体融合蛋白能够精准识别并绑定抗原,为疾病的早期发现和诊断提供了有力工具。在免疫治疗领域,它则能够引导药物直达病灶,提高治疗效果并减少副作用。此外,抗体融合蛋白在抗体纯化、抗体和抗原的定量分析等方面也发挥着重要作用,特别是在免疫导向药物的制备中,其重要性更是不言而喻。[/font][font=宋体] [/font][font=宋体][font=宋体]根据与[/font][font=Calibri]Ig[/font][font=宋体]片段结合方式的不同,抗体融合蛋白可分为多个类型,包括[/font][font=Calibri]Fab[/font][font=宋体]融合蛋白、[/font][font=Calibri][url=https://cn.sinobiological.com/resource/protein-review/fc-fusion-proteins][b]Fc[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/resource/protein-review/fc-fusion-proteins][b]融合蛋白[/b][/url]以及[url=https://cn.sinobiological.com/resource/antibody-technical/scfv-antibody-production][b]单链抗体([/b][/url][/font][font=Calibri][url=https://cn.sinobiological.com/resource/antibody-technical/scfv-antibody-production][b]scFv[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/resource/antibody-technical/scfv-antibody-production][b])[/b][/url]融合蛋白。这些不同类型的抗体融合蛋白各具特色,为科学研究和临床应用提供了丰富的选择。[/font][/font][font=宋体] [/font][b][font=宋体]结构[/font][font=宋体][font=Calibri]Fab[/font][font=宋体]融合蛋白、单链抗体融合蛋白[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]研究表明,抗体可变区的[/font][font=Calibri]N[/font][font=宋体]端空间结构上与互补决定区([/font][font=Calibri]CDR[/font][font=宋体])形成的抗原结合部位十分接近,有的抗体可变区[/font][font=Calibri]N[/font][font=宋体]端残基甚至直接参与抗原结合部位的形成,如果将效应蛋白与抗体片段的[/font][font=Calibri]N[/font][font=宋体]端结合,可能对抗体可变区的空间构型造成较大影响,从而降低抗体与抗原的结合能力。因此,通常将蛋白与抗体片段的[/font][font=Calibri]C[/font][font=宋体]端进行结合,形成抗体融合蛋白。[/font][/font][b][font=宋体] [/font][font=宋体][font=Calibri]Fc[/font][font=宋体]融合蛋白[/font][/font][/b][font=宋体][font=Calibri]Fc[/font][font=宋体]融合蛋白在结构上是将抗体的[/font][font=Calibri]Fc[/font][font=宋体]区与功能蛋白进行融合,可将[/font][font=Calibri]Fc[/font][font=宋体]的[/font][font=Calibri]N[/font][font=宋体]端或[/font][font=Calibri]C[/font][font=宋体]端与目的基因进行融合。根据结合蛋白的不同,可以有多种构型。[/font][/font][font=宋体] [/font][b][font=宋体]作用原理[/font][/b][font=宋体]含有抗体可变区的抗体融合蛋白[/font][font=宋体][font=Calibri]Fab[/font][font=宋体]融合蛋白与[/font][font=Calibri]scFv[/font][font=宋体]融合蛋白含有抗体的可变区,可以进行抗原[/font][font=Calibri]-[/font][font=宋体]抗体反应,其作用原理为利用抗体[/font][font=Calibri]-[/font][font=宋体]抗原特异性结合的特性,通过这种特性的引导,将具有生物活性的蛋白靶向引导至细胞的特定部位,进而发挥一定的生物效应,也就是所谓的“生物导弹”。[/font][/font][font=宋体] [/font][font=宋体]不含抗体可变区的抗体融合蛋白[/font][font=宋体][font=宋体]该类融合蛋白含有的抗体功能区为[/font][font=Calibri]Fc[/font][font=宋体]区,不能进行抗原[/font][font=Calibri]-[/font][font=宋体]抗体反应,[/font][font=Calibri]Fc[/font][font=宋体]段的作用为延长药物在血浆内的半衰期、增加融合蛋白的稳定性等。[/font][font=Calibri]Fc[/font][font=宋体]融合蛋白药理作用的发挥依赖于功能蛋白部分,利用受体[/font][font=Calibri]-[/font][font=宋体]配体之间的相互作用产生一系列的生物学效应。[/font][/font][font=宋体] [/font][b][font=宋体]抗体融合蛋白制备[/font][/b][font=宋体] [/font][font=宋体][font=宋体]最初抗体融合蛋白制备的方法为化学交联法,但这种方法制备的抗体融合蛋白组成不均一、性能不稳定、免疫源性大,随着基因工程技术的发展,该技术已被淘汰。目前主要利用基因工程技术来进行抗体融合蛋白的制备。其制备原理为:将抗体基因与目的蛋白基因通过一段接头序列([/font][font=Calibri]linker[/font][font=宋体])进行链接,然后将链接产物亚克隆至载体中,并用原核或者真核表达系统进行表达。[/font][/font][font=宋体][font=宋体]制备抗体[url=https://cn.sinobiological.com/resource/protein-review/fusion-protein][b]融合蛋白[/b][/url]过程中,一个关键的问题是两蛋白间的接头序列[/font][font=Calibri]( Linker )[/font][font=宋体]的长度,[/font][font=Calibri]linker[/font][font=宋体]的长短对蛋白质的折叠和稳定性非常重要。如果接头序列太短,可能影响两蛋白高级[/font][font=Calibri]-[/font][font=宋体]结构的折叠,从而相互干扰;如果接头序列太长,又涉及免疫原性的问题。[/font][/font][b][font=宋体] [/font][font=宋体]抗体融合蛋白与双特异性抗体[/font][/b][font=宋体] [/font][font=宋体]抗体融合蛋白是将抗体的部分片段与目的蛋白进行融合表达得到的重组蛋白,若将两个具有不同抗原特异性的抗体片段连接至同一蛋白,即可得到[url=https://cn.sinobiological.com/resource/antibody-technical/bispecific-antibody][b]双特异性抗体[/b][/url]。[/font][font=宋体] [/font][b][font=宋体]单克隆抗体与抗体融合蛋白区别[/font][/b][font=宋体] [/font][img=单克隆抗体与抗体融合蛋白区别,690,155]https://ng1.17img.cn/bbsfiles/images/2024/03/202403081113369902_7816_5907840_3.png!w690x155.jpg[/img][font=宋体] [/font][font=宋体][font=宋体]更多详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/fusion-protein[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
[font=宋体]在现代生命科学研究中,[url=https://cn.sinobiological.com/resource/protein-review/protein-production][b]重组蛋白表达技术[/b][/url]扮演着至关重要的角色。通过将外源基因导入宿主细胞,并使其表达特定蛋白,我们能够获取大量高纯度的重组蛋白,为疾病治疗、药物研发和生物工程等领域提供了强有力的支持。本文将介绍重组蛋白表达的原理、表达系统、生产步骤以及应用前景。[/font][font=宋体][b]一、重组蛋白表达的原理[/b][/font][font=宋体][font=宋体]重组蛋白表达是利用[/font][font=Calibri]DNA[/font][font=宋体]重组技术,将目标基因(外源基因)导入宿主细胞中,并通过宿主细胞的生物机制使其表达出特定蛋白。其主要步骤包括:[/font][/font][font=宋体][font=宋体]基因克隆:将目标基因经过[/font][font=Calibri][url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url][/font][font=宋体]扩增后,与表达载体连接,形成重组质粒。[/font][/font][font=宋体]转染或转化:将重组质粒导入宿主细胞中,可以使用化学方法、电穿孔或者嗜热菌等方式进行转染或转化。[/font][font=宋体]表达蛋白:重组质粒进入宿主细胞后,融合到宿主细胞的染色体中,随后遵循细胞的转录和翻译机制,表达出目标蛋白。[/font][font=宋体] [/font][b][font=宋体]二、常见的重组蛋白表达系统[/font][/b][font=宋体]大肠杆菌表达系统:大肠杆菌是常用的重组蛋白表达宿主细胞之一。其优点在于生长快速、易于培养,并且能够产生大量的蛋白。此外,大肠杆菌的遗传工具和代谢途径也被广泛研究,提供了便利。[/font][font=宋体]酵母表达系统:酵母表达系统包括酿酒酵母和毕赤酵母。这些酵母细胞具有真核细胞的特点,能够进行正确的蛋白折叠和修饰。同时,酵母细胞也可以进行大规模培养和高表达,适用于一些复杂蛋白的表达。[/font][font=宋体]昆虫细胞表达系统:昆虫细胞表达系统常用于大规模蛋白表达。昆虫细胞具有真核细胞的优势,能够对蛋白进行正确的折叠和修饰,适合于表达大量需求复杂结构的重组蛋白。[/font][font=宋体]哺乳动物细胞表达系统:哺乳动物细胞的表达系统可用于高效表达复杂蛋白和进行蛋白质研究。哺乳动物细胞具有真核细胞特点,能够进行正确的蛋白质修饰和折叠,并且在一些特殊情况下需要考虑到人类蛋白的免疫原性。[/font][font=宋体] [/font][font=宋体][b]三、重组蛋白生产步骤[/b][/font][font=宋体] [/font][font=宋体]细胞中有两个蛋白生产阶段:转录和翻译,被称为分子生物学的中心法则。换言之,转录和翻译步骤属于重组蛋白表达步骤。[/font][font=宋体] [/font][font=宋体]为了生产重组蛋白,基因被分离并克隆到表达载体中。重组蛋白的生产需要蛋白表达系统、蛋白纯化系统和蛋白识别系统。[/font][font=宋体] [/font][font=宋体][b]获取重组蛋白的基本步骤:[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1.[/font][font=宋体]目标基因的扩增。[/font][/font][font=宋体][font=Calibri]2.[/font][font=宋体]插入克隆载体。[/font][/font][font=宋体][font=Calibri]3.[/font][font=宋体]亚克隆到表达载体中。[/font][/font][font=宋体][font=Calibri]4.[/font][font=宋体]转化到蛋白表达宿主中[/font][font=Calibri]([/font][font=宋体]细菌[/font][font=Calibri]([/font][font=宋体]大肠杆菌[/font][font=Calibri])[/font][font=宋体]、酵母细胞、哺乳动物细胞或杆状病毒[/font][font=Calibri]-[/font][font=宋体]昆虫细胞系统[/font][font=Calibri])[/font][font=宋体]。[/font][/font][font=宋体][font=Calibri]5.[/font][font=宋体]重组蛋白鉴定试验[/font][font=Calibri](Western blot[/font][font=宋体]或荧光[/font][font=Calibri])[/font][/font][font=宋体][font=Calibri]6.[/font][font=宋体]大规模生产。[/font][font=Calibri]([/font][font=宋体]大规模发酵[/font][font=Calibri])[/font][/font][font=宋体][font=Calibri]7.[/font][font=宋体]分离和纯化。[/font][/font][font=宋体] [/font][font=宋体]需要考虑多种因素:[/font][font=宋体][font=Calibri]1.[/font][font=宋体]选择哪个宿主系统?[/font][/font][font=宋体][font=Calibri]2.[/font][font=宋体]如何分离和纯化重组蛋白?[/font][/font][font=宋体] [/font][font=宋体]选择适当的表达宿主或使用正确的纯化方法并不容易,应考虑目标重组蛋白的性质。下面列出了一些重要因素:[/font][font=宋体] [/font][font=宋体]? 膜结合[/font][font=宋体]? 溶解度[/font][font=宋体]? 单或多结构域[/font][font=宋体][font=宋体]? 大小[/font][font=Calibri]([/font][font=宋体]分子量[/font][font=Calibri])[/font][/font][font=宋体]? 表达位置[/font][font=宋体] [/font][font=宋体][font=宋体]对于大多数没有足够经验来表达和分离重组蛋白的人来说,重组蛋白的生产是非常耗时的。许多生物公司为各种不同规模的重组蛋白表达提供良好的服务:[/font][font=Calibri]https://cn.sinobiological.com/services/recombinant-protein-expression-service[/font][font=宋体],例如义翘神州[/font][/font][font=宋体] [/font][font=宋体][b]四、重组蛋白表达技术的应用前景[/b][/font][font=宋体]药物研发:重组蛋白表达技术被广泛应用于药物研发领域,用于生产重组蛋白药物。这些药物包括多肽类、蛋白类和抗体类药物,如生长因子、抗体药物和血液制剂等。通过重组蛋白表达技术,我们可以获得高效纯度的药物,满足临床上的需求。[/font][font=宋体]生物工程:重组蛋白表达技术被广泛应用于生物工程领域,用于生产特定的蛋白产品。这些产品可以应用于食品、化妆品、工业发酵等领域,如酶制剂、生物染料和生物材料等。[/font][font=宋体]疾病治疗:通过重组蛋白表达技术,我们能够合成特定的蛋白,用于疾病的治疗和诊断。例如,利用重组抗体技术,可以开发出用于癌症治疗和免疫治疗的抗体药物。[/font][font=宋体] [/font][font=宋体][font=宋体]详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/protein-production[/font][/font]
[font=宋体]抗体,作为一类特殊的蛋白质,在免疫系统中发挥着至关重要的作用,它们能够特异性地识别并中和外来病原体,如细菌和病毒。而蛋白质,作为生命活动的基础分子,具有多种多样的功能,从酶催化到结构支撑,无所不包。抗体与蛋白的区别在于,抗体是一类具有特定功能的蛋白质,而蛋白质则是更广泛的一类生物分子。本文将深入探讨抗体与蛋白的具体区别,并详细解析抗体蛋白的结构与功能,为读者提供一个全面而深入的理解。[/font][font=宋体] [/font][b][font=宋体]抗体与蛋白的区别?[/font][/b][font=宋体] [/font][font=宋体]定义:[/font][font=宋体][font=宋体]抗体([/font][font=Calibri]antibody[/font][font=宋体])是指机体由于抗原的刺激而产生的具有保护作用的蛋白质。它(免疫球蛋白不仅仅只是抗体)是一种由浆细胞(效应[/font][font=Calibri]B[/font][font=宋体]细胞)分泌,被免疫系统用来鉴别与中和外来物质如细菌、病毒等的大型[/font][font=Calibri]Y[/font][font=宋体]形蛋白质,仅被发现存在于脊椎动物的血液等体液中,及其[/font][font=Calibri]B[/font][font=宋体]细胞的细胞膜表面。抗体能识别特定外来物的一个独特特征,该外来目标被称为抗原。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]抗体是一类能与抗原特异性结合的免疫球蛋白。抗体按其反应形式分为凝集素、沉降素、抗毒素、溶解素、调理素、中和抗体、补体结合抗体等。按抗体产生的来源分为正常抗体(天然抗体),如血型[/font][font=Calibri]ABO[/font][font=宋体]型中的抗[/font][font=Calibri]A[/font][font=宋体]和抗[/font][font=Calibri]B[/font][font=宋体]的抗体,和免疫抗体如抗微生物的抗体。按反应抗原的来源分为异种抗体,异嗜性抗体,同种抗体和自身抗体。按抗原反应的凝集状态分为完全抗体[/font][font=Calibri]IgM[/font][font=宋体]和不完全抗体[/font][font=Calibri]IgG[/font][font=宋体]等。抗体在医疗实践中应用甚为广泛。如用于疾病的预防、诊断和治疗方面都有一定的作用。临床上用丙种球蛋白预防病毒性肝炎、麻疹、风疹等,国际上用抗[/font][font=Calibri]Rh[/font][font=宋体]免疫球蛋白预防因[/font][font=Calibri]Rh[/font][font=宋体]血型不合引起的溶血症。诊断上如类风湿因子用于类风湿性关节炎,抗核抗体([/font][font=Calibri]ANA[/font][font=宋体])、抗[/font][font=Calibri]DNA[/font][font=宋体]抗体用于系统性红斑狼疮,抗精子抗体用于原发性不孕症的诊断等;治疗上如毒素中毒用抗毒治疗以及免疫缺陷性疾病的治疗等。[url=https://cn.sinobiological.com/resource/antibody-technical][b]抗体相关资源[/b][/url][/font][/font][font=宋体] [/font][font=宋体]蛋白:[/font][font=宋体][font=宋体]蛋白质是生命的物质基础,是有机大分子,是构成细胞的基本有机物,是生命活动的主要承担者。没有蛋白质就没有生命。氨基酸是蛋白质的基本组成单位。它是与生命及与各种形式的生命活动紧密联系在一起的物质。机体中的每一个细胞和所有重要组成部分都有蛋白质参与。蛋白质占人体重量的[/font][font=Calibri]16%~20%[/font][font=宋体],即一个[/font][font=Calibri]60kg[/font][font=宋体]重的成年人其体内约有蛋白质[/font][font=Calibri]9.6~12kg[/font][font=宋体]。人体内蛋白质的种类很多,性质、功能各异,但都是由[/font][font=Calibri]20[/font][font=宋体]多种氨基酸([/font][font=Calibri]Amino acid[/font][font=宋体])按不同比例组合而成的,并在体内不断进行代谢与更新。点击查看:[url=https://cn.sinobiological.com/resource/protein-review][b]蛋白相关资源[/b][/url][/font][/font][font=宋体] [/font][b][font=宋体]区别与联系:[/font][/b][font=宋体][font=宋体]蛋白质还是有一定的区别以及关联性的,虽然说抗体是蛋白质,但是蛋白质不一定是抗体。[/font] [font=宋体]主要是因为抗体是通过人体内的浆细胞所产生的,而且还可以喝相应的抗原特异性相互结合,这样在一定程度上就能发挥出蛋白质。[/font][/font][font=宋体] [/font][b][font=宋体]抗体[/font][font=宋体]蛋白[/font][font=宋体]结构[/font][font=宋体]解析[/font][font=宋体]:[/font][/b][font=宋体][font=宋体]抗体是一种免疫球蛋白,由[/font][font=Calibri]B[/font][font=宋体]淋巴细胞产生。抗体的单体是一个[/font][font=Calibri]Y[/font][font=宋体]形的分子,有[/font][font=Calibri]4[/font][font=宋体]条多肽链组成。其中包括两条相同的重链,以及两条相同的轻链,之间由双硫键连接在一起。每条重链[/font][font=Calibri]50kDa[/font][font=宋体],每条轻链[/font][font=Calibri]25kDa[/font][font=宋体],轻重链间存在二硫键链接。[/font][/font][font=宋体] [/font][font=宋体]轻链[/font][font=宋体][font=宋体]轻链包括可变区和恒定区,可变区约占轻链的[/font][font=Calibri]1/2[/font][font=宋体]。[/font][/font][font=宋体] [/font][font=宋体]重链[/font][font=宋体][font=宋体]重链包括可变区和恒定区。根据重链的不同,可以将抗体分为不同的种类,例如哺乳动物[/font] [font=Calibri]Ig [/font][font=宋体]的重链有α、δ、ε、γ和 μ 五种[/font][font=Calibri],[/font][font=宋体]相对应可以将哺乳动物[/font][font=Calibri]Ig[/font][font=宋体]分为 [/font][font=Calibri]IgA[/font][font=宋体]、[/font][font=Calibri]IgD[/font][font=宋体]、[/font][font=Calibri]IgE[/font][font=宋体]、[/font][font=Calibri]IgG [/font][font=宋体]和 [/font][font=Calibri]IgM [/font][font=宋体]五类。[/font][/font][font=宋体] [/font][font=宋体]可变区[/font][font=宋体][font=宋体]抗体分子的[/font][font=Calibri]N[/font][font=宋体]端存在一段氨基酸序列变化较大的区域,该区域称为可变区。可变区中存在可以与抗原特结合的部位,即抗原结合位点。一个抗体有两个抗原结合位点,可以同时结合两个抗原分子。在可变区中有三个区域的序列高度变化,成为高变区([/font][font=Calibri]hypervariable region[/font][font=宋体],[/font][font=Calibri]HVR[/font][font=宋体])又称为抗原互补决定区([/font][font=Calibri]complementarity determining region[/font][font=宋体],[/font][font=Calibri]CDR[/font][font=宋体])。可变区主要通过其[/font][font=Calibri]3[/font][font=宋体]个[/font][font=Calibri]CHR[/font][font=宋体]区形成[/font][font=Calibri]3[/font][font=宋体]个环状结构与抗原特异性结合。可变区中非[/font][font=Calibri]CDR[/font][font=宋体]部分成为骨架区([/font][font=Calibri]framework region[/font][font=宋体],[/font][font=Calibri]FR[/font][font=宋体]),其氨基酸组成和排列变化相对[/font][font=Calibri]CDR[/font][font=宋体]较少。[/font][/font][font=宋体] [/font][font=宋体]恒定区[/font][font=宋体][font=宋体]抗体分子[/font][font=Calibri]C[/font][font=宋体]端氨基酸序列相对稳定,该区域称为恒定区。同一种抗体的恒定区是相同的。抗体轻链的恒定区由一个[/font][font=Calibri]Ig[/font][font=宋体]结构域构成;重链的恒定区由[/font][font=Calibri]3-4[/font][font=宋体]个串联的[/font][font=Calibri]Ig[/font][font=宋体]结构域及一个用于增加灵活性的铰链区构成。[/font][font=Calibri]IgA[/font][font=宋体]、[/font][font=Calibri]IgE[/font][font=宋体]、[/font][font=Calibri]IgG[/font][font=宋体]有三个结构域([/font][font=Calibri]CH1[/font][font=宋体]、[/font][font=Calibri]CH2[/font][font=宋体]、[/font][font=Calibri]CH3[/font][font=宋体]),[/font][font=Calibri]IgD[/font][font=宋体]、[/font][font=Calibri]IgM[/font][font=宋体]有四个结构域([/font][font=Calibri]CH1[/font][font=宋体]、[/font][font=Calibri]CH2[/font][font=宋体]、[/font][font=Calibri]CH3[/font][font=宋体]、[/font][font=Calibri]CH4[/font][font=宋体])。不同种类抗体的铰链区存在一定的差异,[/font][font=Calibri]IgA[/font][font=宋体]的铰链区较短,[/font][font=Calibri]IgD [/font][font=宋体]的铰链区较长,[/font][font=Calibri]IgM [/font][font=宋体]和[/font][font=Calibri]IgE [/font][font=宋体]无铰链区。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Fab[/font][font=宋体]片段[/font][/font][font=宋体][font=Calibri]IgG[/font][font=宋体]分子在木瓜蛋白酶的作用下可以被降解为两个[/font][font=Calibri]Fab[/font][font=宋体]段及一个[/font][font=Calibri]Fc[/font][font=宋体]段。[/font][font=Calibri]Fab[/font][font=宋体]段由抗体轻链的可变区、轻链的恒定区、重链的可变区及重链恒定区构成。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Fc[/font][font=宋体]段[/font][/font][font=宋体][font=Calibri]Fc[/font][font=宋体]段包含了所有抗体分子共有的蛋白质序列以及各个类别独有的决定簇。[/font][font=Calibri]Fc[/font][font=宋体]段有多种生物学活性,具有结合补体、结合[/font][font=Calibri]Fc[/font][font=宋体]受体、通过胎盘等作用。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多关于[url=https://cn.sinobiological.com/resource/antibody-technical/antibody-structure-function][b]抗体的结构和功能[/b][/url]详情:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/antibody-structure-function[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
本文引用自发酵《在发酵工艺角度看蛋白表达》引用发酵 的 在发酵工艺角度看蛋白表达在分子生物学角度讲,找到或合成外源蛋白基因,构建质粒,并导入细胞以表达具有生物活性的折叠正确的蛋白,是一种成熟的常规技术。目前,包括酶,抗原,抗体,激素,其他小分子调节蛋白在内的很多蛋白,都已经用这种技术实现了工业化生产。在具体的工艺选择上,历史沿袭习惯和表达体系的选择,对工艺稳定性,成本,有巨大的影响。 目前,常用的蛋白表达系,有3个类别:1,大肠杆菌表达系。大肠杆菌的遗传背景十分清楚,代谢相对简单,发酵副产物少,在不是很严格的情况下,是表达蛋白的首选。通过按经验选择合适的菌株及合适的质粒,既可以以包涵体的形式得到大量的目标蛋白,又可以在细胞外得到可溶性蛋白,是常见的一种表达系。2,酵母菌表达系。用酵母做表达系,理由之一,也是遗传背景清楚,而且,当蛋白分子量过小,不能形成包涵体时,或蛋白的二硫键过多,不易体外复性时,酵母菌就成了合适的选择。另外,酵母对蛋白也会有一个简单的修饰,近似于高等动物的蛋白糖基化过程。这样,在合成在体液中发挥作用的蛋白,而且,又不能(技术水平限制)用动物细胞时,就可以退而求其次的选用酵母菌表达。一般是用信号肽把蛋白导出细胞,在发酵液中以可溶性蛋白的形式存在。这也是一个常见的表达系。3,动物(或说,人的)细胞表达系。这种情况,在纯度或毒性方面有较高要求的产品应用。一般国外产品应用较多,国内还没有用动物细胞表达蛋白实现商业化生产的报道。由于技术限制,国内工业化生产用这个方法目前还有较大难度。这3种表达系,各自有自己的优缺点。首先,在潜在的毒性影像方面讲,由于和真核生物亲缘关系太远,大肠杆菌就最不合适。其次是酵母菌。而在表达量和代谢控制成本上来讲,酵母菌和动物细胞又是差强人意的。现在,很多蛋白习惯性的选用酵母菌做表达系,就是因为早期提取蛋白技术低下,而动物细胞培养技术又不过关的原因所致。目前,虽然提取工艺提高了,但作为蛋白这种高附加值产品,运作成本集中在销售而不是生产,所以,降低生产成本的诉求很低。站在降低开发难度的角度讲,一方面,质粒构建和质粒与菌株的匹配方面依赖大量经验,另一方面,发酵工艺策略选择与发酵工艺优化又需要很大的投入,所以,技术开发部门沿用自己熟悉的,已经积累了大量经验的表达系,是合理的。不过,随着分子技术进一步的发展,分子技术进入低附加值的产品领域又是必然的,降低生产成本就变的越来越必要了。 大肠杆菌表达系有两种得到外源蛋白的方法:1,缓慢的表达,得到可溶性蛋白,这种方法产量和酵母菌表达类似,与酵母菌比,不具有明显的优势,一般是有做大肠杆菌传统的研究机构生产小分子蛋白的一种沿袭性做法。2,使用T7启动子表达蛋白,这样,高速的蛋白表达速率使蛋白来不及折叠,在细胞内形成非水溶性的包涵体。最后目标蛋白可以达到总细胞质量的15%-25%,这样,就为降低成本提供了一种可能。不过,在使用T7启动子表达时,也存在两个难点:1,蛋白的复性技术,如果形成可溶性蛋白,那利用(使用分子技术加载在目标蛋白上)信号肽,只要过一遍柱子就能分离得到纯度非常高的,具有生物活性的产品,而形成包涵体,对提取,复性就有较高的要求,特别是二硫键的存在,会对复性产生很大的影响。在目前国内和国际流行技术看,并不是所有的蛋白都能在预定成本下复性的。2,任何情况下,高产都是代谢网络互相依赖与作用的结果。在如此高的表达量下,甚至细胞的形态都已经发生很大变化,正常代谢受到严重干扰,以至于放大时,摇瓶工艺对发酵工艺几乎没有任何参考价值。发酵工艺策略的选择将直接依赖于工程人员在生化,生理水平对菌株的理解,而匮乏可资参考的数据资料。发酵工艺的优化要离开摇瓶经验在发酵罐上逐步进行,这样,整个发酵工艺的确立就需要比想象中要大得多的人员与时间的投入。另外,再说一下糖基化的问题。在动物细胞内合成的折叠正确的蛋白,在分泌入体液前会有一个糖基化的过程,加上一个糖链就不会很快被蛋白酶当做折叠错误的蛋白水解掉。但是以微生物为表达系表达的蛋白,不具有动物细胞的修饰过程,用大肠杆菌表达的目标蛋白,很快会在血液中被降解。解决或回避这个问题,有两种方法:1,用动物细胞表达,一般,是用癌化的人类细胞。由于动物细胞培养技术要求过高,在国外比较昂贵的医药中有应用,国内不常见。2,由于酵母菌也有一个对蛋白的粗略的修饰过程,可以用酵母菌表达目标蛋白。这个技术,国内国外都在用,可以是一个权宜之计。主要难点集中在对合适菌株的分子水平的改造,以达到尽可能接近满意的修饰效果。这样,就可以在不同目标蛋白上表达系和发酵工艺上做出选择。如果是小分子,无糖基化修饰或不在体液中发挥作用的蛋白,可以选择大肠杆菌和酵母菌表达系,得到可溶性蛋白,然后提取。如果分子量合适,并对生产成本有诉求,而且可以比较方便的复性,则选用大肠杆菌表达系,得到包涵体,然后复性。如果是需要在体液中发挥活性并有糖基化要求的 蛋白,则选用经过分子生物学改造的酵母菌表达系。当然,并不是任何一个实验室都同时拥有或擅长所有的方向的。而难点,往往集中在以下3个方面:1,大肠杆菌蛋白包涵体复性。2,糖基化修饰。3,发酵工艺(工程菌株的工业水平)的确定。做工程一般是理科实验室的弱项,而工科实验室做基础又很少,在把工科和理科结合方面,我们实验室还是有经验和成功先例的。下面,以溶菌酶为例,阐述一下蛋白表达系的选择和工艺的确定。溶菌酶是一类具有种属差异的非特异性免疫物质,在动物界中普遍存在,种类繁多,其实,在植物和微生物中也有发现。但研究最多的还是动物。开发兽用溶菌酶,主要是想作为抗生素的替代物,作为添加剂使用。因此是一个低附加值的产品。下面一切的工作,都会围绕“兽用”和“低附加值”展开。首先,比较几种常见和认为有效的溶菌酶,杀菌效果最好的是人的溶菌酶,但考虑到潜在的危险(具有对人溶菌酶产生抗性,并使抗性基因扩散),舍尔求其次,用了鸟类蛋清溶菌酶,作为表达对象。然后,在得到溶菌酶蛋白的一级结构后,对此进行了分析。此蛋白不会用于体液内,故没有糖链修饰的问题。分子量不是很大,但也不太小,130左右的氨基酸构成,足以形成包涵体,这就为用大肠杆菌表达系高效表达提供了可能。讨厌的是有4个二硫键,其中有两个在结构复杂区域,折叠正确有一定的困难。但是,如果用酵母菌做,可能没法解决成本问题,即便优化工艺现在过去了,也不会是最终版本----肯定会有人用大肠杆菌做。所以,结论就是必须知难而进,拿下复性工艺。另外,由于是低附加值产品,发酵吨位就不能太小。以往分子生物学流行的50升,100升小罐发酵,肯定是不行的。发酵罐的放大,除了溶氧,剪切力发生变化,更重要的是搅拌线速度改变了胞外酶以及包括细胞本身的代谢方式和速度。在胞内体现就是氧化还原电势的改变,这在工艺上会带来很多麻烦。虽然说,一般是放大后产量往往提高,但放大过程中,小罐的经验就不能照搬了。同时,也因为是低附加值产品,发酵过程中诸如质粒丢失等稳定性要求,就很高了,应为只有稳定,才能控制成本。这样,工艺就成了第二个难点。明白这些之后,按照大肠杆菌的喜好,合成了溶菌酶的基因。然后构建质粒,导入细胞。在摇瓶水平表达溶菌酶。在筛选复性条件的同时,就同时在发酵罐水平对工艺稳定性进行了优化。首先,为了进一步提高质粒稳定性,对初始培养基进行了重新设计。并改动发酵工艺策略,由于是胞内产物,我们应用高细胞密度发酵控制法延长限制性生长时间(不能用经典发酵的延长对数期生长时间的办法,对工程菌不适合,会造成质粒丢失,代谢紊乱等一系列问题),提高细胞量,并改变了诱导时机,得到了稳定的高产,具体数据比较枯燥,就不在此展开了。提取方面,经过不懈的努力,我们也掌握了比较成功的复性条件(具体由另外人员负责,也不做详细介绍了)。这样,工艺才基本拼凑好。进一步优化,在试生产多次重复时在进行。以上,是外源蛋白表达的粗略的技术和工艺的过程。
[font=宋体][b][font=宋体]抗绿色荧光蛋白[/font][font=Calibri](GFP)[/font][font=宋体]抗体,小鼠单克隆[/font][/b][/font][font=宋体] [/font][font=宋体][font=Calibri]GFP[/font][font=宋体]([/font][font=Calibri]Green fluorescent protein[/font][font=宋体],绿色荧光蛋白)标签含有 [/font][font=Calibri]238 [/font][font=宋体]个氨基酸,分子量约为 [/font][font=Calibri]26.9 KDa[/font][font=宋体],最先是 [/font][font=Calibri]1962 [/font][font=宋体]年下村修等在维多利亚多管发光水母([/font][font=Calibri]Aequorea victoria[/font][font=宋体])中发现的。[/font][font=Calibri]GFP [/font][font=宋体]标签在紫外线的照射下会发出绿色的荧光,而且与靶蛋白融合后不会显著地影响天然蛋白质的组装和功能。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]凭借[/font] [font=Calibri]10 [/font][font=宋体]多年在蛋白表达和抗体制备领域的技术积淀,义翘神州自主研发了多款抗 [/font][font=Calibri]GFP [/font][font=宋体]标签抗体。高品质的抗 [/font][font=Calibri]GFP [/font][font=宋体]标签抗体可用于检测 [/font][font=Calibri]GFP[/font][font=宋体](绿色荧光蛋白),满足多种应用的需求,包括蛋白印迹([/font][font=Calibri]WB[/font][font=宋体])、[/font][font=Calibri]ELISA [/font][font=宋体]或免疫沉淀([/font][font=Calibri]IP[/font][font=宋体])。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]特异性:单克隆抗绿色荧光蛋白([/font][font=Calibri]GFP[/font][font=宋体])识别[/font][font=Calibri]N[/font][font=宋体]末端和[/font][font=Calibri]C[/font][font=宋体]末端[/font][font=Calibri]GFP[/font][font=宋体]([/font][font=Calibri]27 kDa[/font][font=宋体])标记的融合蛋白。抗体与原核表达载体表达的融合蛋白反应。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]免疫原:[/font][font=Calibri]GFP[/font][font=宋体]标记的融合蛋白[/font][/font][font=宋体] [/font][font=宋体][font=宋体]生化[/font][font=Calibri]/[/font][font=宋体]生理作用:[/font][font=Calibri]GFP ([/font][font=宋体]绿色荧光蛋白[/font][font=Calibri])[/font][font=宋体]是一种用于检查基因表达和蛋白定位的报告分子。[/font][font=Calibri]GFP [/font][font=宋体]用紫外线[/font][font=Calibri]/[/font][font=宋体]蓝光激发时会发出绿光。[/font][font=Calibri]GFP [/font][font=宋体]荧光保持稳定,可在活细胞中进行无创检测。[/font][font=Calibri]GFP [/font][font=宋体]被认为是监测几种活细胞或生物体动态过程的工具。当在真核细胞或原核细胞中表达并被蓝光或紫外光照射时,[/font][font=Calibri]GFP [/font][font=宋体]产生明亮的绿色荧光。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]外形:[/font][font=Calibri]0.01 M [/font][font=宋体]磷酸盐缓冲液 [/font][font=Calibri](pH 7.4)[/font][font=宋体],含 [/font][font=Calibri]15 mM [/font][font=宋体]叠氮化钠[/font][/font][font=宋体] [/font][font=宋体][font=宋体]储存及稳定性:如需连续使用,请在[/font][font=Calibri]2-8[/font][font=宋体]°[/font][font=Calibri]C[/font][font=宋体]下储存,最长一个月。若需延长储存时间,可将溶液分装并冷冻。不建议反复冻融。如果长期储存时出现轻微浑浊,请在使用前通过离心澄清溶液。若工作稀释样品在[/font][font=Calibri]12[/font][font=宋体]小时内未使用完,则应丢弃。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]该如何选择表达克隆的标签[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1[/font][font=宋体]、首先,需要确定融合标签的目的[/font][/font][font=宋体] [/font][font=宋体][font=宋体]蛋白纯化[/font] [font=宋体]:标签的普遍用途是蛋白纯化。小分子[/font][font=Calibri]6XHis Tag[/font][font=宋体]常被用于细胞内源蛋白的纯化。[/font][font=Calibri]6XHis Tag[/font][font=宋体]也广泛应用于大肠杆菌的蛋白纯化。可是哺乳动物细胞中因非分泌蛋白自身存在高组氨酸背景,因此极少使用[/font][font=Calibri]6XHis Tag[/font][font=宋体]。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Western Blot[/font][font=宋体]检测:若需要做[/font][font=Calibri]Western Blot[/font][font=宋体]实验来检测细胞裂解物中蛋白的表达,你可以选择有匹配的抗体的小分子标签。[/font][font=Calibri]FLAG Tag[/font][font=宋体]以其分子量小以及拥有许多与之匹配的商业化的抗体等优势,成为[/font][font=Calibri]Western Blot[/font][font=宋体]实验中常用的[/font][font=Calibri]Tag[/font][font=宋体]。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]免疫沉淀反应:[/font][font=Calibri]FLAG Tag[/font][font=宋体]其分子量小以及拥有大量相匹配的商业用抗体等优势成为免疫沉淀反应中最常用的[/font][font=Calibri]Tag. [/font][font=宋体]其他常用的标签有:[/font][font=Calibri]HA[/font][font=宋体]和[/font][font=Calibri]cMyc.[/font][/font][font=宋体] [/font][font=宋体][font=宋体]免疫共沉淀。首先,裂解您的样本,以释放蛋白。向试管中添加裂解液的同时,加入靶向融合标签的抗体,抗体会识别融合标签。然后抗体与蛋白[/font] [font=Calibri]A [/font][font=宋体]或 [/font][font=Calibri]G [/font][font=宋体]偶联微珠结合,后者拉出您的目标蛋白,以及与之复合的其他蛋白。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]活细胞成像:荧光蛋白([/font][font=Calibri]Fluorescent Proteins, FPs[/font][font=宋体])是活细胞成像常用的标记蛋白。其中最常用的是绿色荧光蛋白([/font][font=Calibri]GFP[/font][font=宋体])和它的衍生物([/font][font=Calibri]CFP, YFP, etc.[/font][font=宋体]),以及一些红色变体,如[/font][font=Calibri]dTomato[/font][font=宋体]和[/font][font=Calibri]mCherry.[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2[/font][font=宋体]、考虑融合标签的影响[/font][/font][font=宋体] [/font][font=宋体]任何一类标签处于氨基酸序列的任一位置,都具有影响目的蛋白表达或功能的可能性。最主要原因是标签可能会干扰蛋白的正确折叠,致使目的蛋白失活或形成包涵体。其次,标签可能会中断亚细胞定位信号,这种情况下,蛋白能够正确翻译和折叠,但在细胞内所处的位置是错误的。因此,您需要知道添加的标签对目的蛋白的表达是否有影响。[/font][font=宋体] [/font][font=宋体][font=Calibri]3[/font][font=宋体]、考虑是在[/font][font=Calibri]N-[/font][font=宋体]端还是[/font][font=Calibri]C-[/font][font=宋体]端标记[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]N-[/font][font=宋体]端或[/font][font=Calibri]C-[/font][font=宋体]端标记的选择还需要根据蛋白结构、定位等特性。然而,倘若你没有确切的蛋白结构,或蛋白功能域图谱,建议分别构建[/font][font=Calibri]N-[/font][font=宋体]端标记和[/font][font=Calibri]C-[/font][font=宋体]端标记的表达克隆,以检测哪个更有效。[/font][/font][font=宋体] [/font][font=宋体][url=https://cn.sinobiological.com/services/recombinant-protein-expression-service][b]重组蛋白表达技术[/b][/url]现已在生物学各个具体领域应用广泛,尤其是蛋白质的大规模生产和体内功能研究都需要应用重组蛋白表达载体。[/font][font=宋体] [/font][font=宋体][font=宋体]更多[url=https://cn.sinobiological.com/resource/protein-review/protein-tag][b]蛋白标签[/b][/url]详情可以关注义翘神州:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/protein-tag[/font][/font]
[font=宋体]蛋白表达系统指宿主、外源基因、载体和辅助成分组成的体系,通过这个体系可以实现外源基因顺利的实现在宿主中表达。[b]蛋白表达体系通常由以下几部分组成:[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1. [/font][font=宋体]宿主:用来表达的生物体,可以为细菌(大肠杆菌、枯草芽孢杆菌)、酵母、植物细胞、动物细胞等。由于各种宿主生物本身的特性多种多样,因此采用的表达体系也不相同[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2. [/font][font=宋体]载体:载体的选择需要根据宿主而定,根据宿主不同,分为原核(大肠杆菌、枯草芽孢杆菌)表达载体、酵母表达载体、植物表达载体、哺乳动物表达载体、昆虫表达载体等。载体中还有外源基因片段,外源基因通过载体介导,可以在宿主中表达。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3. [/font][font=宋体]辅助成分:有的表达系统中还包括了协助载体进入宿主的辅助成分,比如:昆虫[/font][font=Calibri]-[/font][font=宋体]杆状病毒表达系统中的杆状病毒。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]重组蛋白表达的三个主要系统是细菌表达系统(例如乳酸乳球菌和大肠杆菌)、酵母和杆状病毒以及哺乳动物细胞介导的蛋白表达。[/font] [/font][font=宋体] [/font][b][font=宋体]应用:[/font][/b][font=宋体] [/font][font=宋体]表达后的蛋白常应用于:[/font][font=宋体][font=Calibri]1[/font][font=宋体])作为抗原制备抗体;[/font][/font][font=宋体][font=Calibri]2[/font][font=宋体])参与细胞实验与动物实验;[/font][/font][font=宋体][font=Calibri]3[/font][font=宋体])测定蛋白酶活;[/font][/font][font=宋体][font=Calibri]4[/font][font=宋体])研究蛋白相互作用;[/font][/font][font=宋体][font=Calibri]5[/font][font=宋体])研究蛋白结晶结构;[/font][/font][font=宋体][font=Calibri]6[/font][font=宋体])免疫组化实验;[/font][/font][font=宋体][font=Calibri]7[/font][font=宋体])药物蛋白研究、生产等。[/font][/font][font=宋体] [/font][b][font=宋体]影响蛋白表达的因素有:[/font][/b][font=宋体] [/font][font=宋体][font=Calibri]1.[/font][font=宋体]蛋白本身的特性:蛋白分子量大小、蛋白来源[/font][font=Calibri]/[/font][font=宋体]物种、是否为毒性蛋白,蛋白翻译后修饰程度、蛋白自身结构的复杂程度[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2.[/font][font=宋体]宿主的选择:宿主本身的特性、蛋白表达需求等都影响着蛋白表达[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3.[/font][font=宋体]蛋白需求量:蛋白应用范围对应的需求量不同,所以要根据需求量确定表达系统[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4.[/font][font=宋体]质粒载体的选择:载体是携带外源基因的工具,要根据系统选择合适的载体才能使蛋白更好的表达[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]5.[/font][font=宋体]融合标签的选择:蛋白重组表达过程中采用亲和标签融合表达有两方面的作用:一方面是为了使蛋白纯化过程变得更加容易;另一方面是为了促进某些不溶性蛋白可溶[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]6.[/font][font=宋体]蛋白表达系统的优化:重组蛋白的表达往往不像理论那样一帆风顺,在实际的表达过程中有可能产生各种各样的问题,因此表达系统的优化很重要。[/font][/font][font=宋体] [/font][b][font=宋体]如何选择合适的表达系统[/font][/b][font=宋体]没有一个表达系统是完美的,要针对每个重组蛋白来评估哪种系统最有效。每个蛋白表达系统的生产速度、成本、糖基化和折叠等特性都各不相同,且跨度很大。如下图:[/font][font=宋体] [/font][font=宋体][font=宋体]更多详情可以关注:义翘神州[url=https://cn.sinobiological.com/resource/protein-review/protein-production-systems][b]蛋白表达系统[/b][/url][/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/protein-production-systems[/font][/font]
[font=宋体][font=宋体]无细胞蛋白表达系统([/font][font=Calibri]Cell-Free Protein Expression System[/font][font=宋体])是一种基于原核和真核细胞提取物构建的体外蛋白表达系统。它具有许多优点,例如可以在短时间内生产大量的蛋白质,同时避免了细胞内的复杂调控机制和翻译后修饰等繁琐过程。因此,无细胞蛋白表达系统在生物制药、生物材料、生物燃料等领域具有广泛的应用前景。本文将详细介绍无细胞蛋白表达系统的优缺点。[/font][/font][font=宋体][b]一、无细胞蛋白表达系统的优点[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1.[/font][font=宋体]高效性:无细胞蛋白表达系统具有高表达效率的优点,这是由于体外体系中不存在靶蛋白累积所需的细胞分裂和细胞复杂代谢反应。此外,由于无细胞蛋白表达系统不受到细胞毒性和免疫反应的限制,可以实现大规模的蛋白质表达。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2.[/font][font=宋体]灵活性:无细胞蛋白表达系统可以使用一系列不同的原核和真核细胞提取物作为反应体系,例如[/font][font=Calibri]E.coli[/font][font=宋体]、小麦胚芽和人类细胞等。这意味着可以根据不同的实验目的和需求进行合理的选择,以适应多样化的研究需要。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3.[/font][font=宋体]易操作性:无细胞蛋白表达系统非常容易操作。与传统的细胞表达系统相比,无细胞蛋白表达系统不需要细胞培养、生长和繁殖。此外,无细胞蛋白表达系统可以快速进行,通常只需要数小时至几天即可完成目标蛋白的表达。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4.[/font][font=宋体]简单纯化:由于无细胞蛋白表达系统可以避免有机溶剂和离子交换剂等复杂的步骤,从而使目标蛋白的纯化工作更加简便和迅速。例如,可以使用亲和柱、凝胶过滤和电泳分析等方法来快速分离和纯化蛋白质。[/font][/font][font=宋体] [/font][font=宋体][b]二、无细胞蛋白表达系统的缺点[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1.[/font][font=宋体]成本较高:尽管无细胞蛋白表达系统可以大规模进行蛋白质表达,但是所需的原核和真核细胞提取物通常需要较高的成本。此外,涉及到的一些试剂和设备也比较昂贵,使得无细胞蛋白表达系统在应用过程中存在一定的经济压力。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2.[/font][font=宋体]表达限制:由于无细胞蛋白表达系统缺乏复杂的代谢反应和细胞分化机制,因此它不适用于某些特定类型的蛋白。例如,它无法表达复杂的膜蛋白和困难的药物蛋白等。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3.[/font][font=宋体]不稳定性:无细胞蛋白表达系统通常具有一定的稳定性问题。由于缺乏细胞膜的保护,无细胞蛋白表达体系会更容易受到外部条件的影响,如温度、[/font][font=Calibri]pH[/font][font=宋体]、离子浓度等,从而导致蛋白质的不稳定性、聚集和降解等现象。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4.[/font][font=宋体]不适合复杂蛋白结构:无细胞蛋白表达系统对于复杂蛋白结构的模拟效果不佳。例如,膜蛋白、多肽和糖蛋白等复杂蛋白质可能会被无细胞蛋白表达系统无法很好地复制,从而限制了其应用范围。[/font][/font][font=宋体] [/font][font=宋体]无细胞蛋白表达系统具有高效、灵活、易操作、简单纯化等优点,但同时也存在着成本较高、表达限制、不稳定性和不适合复杂蛋白结构等缺点。在实际应用中,需要根据具体的研究目的和需求进行选择,并结合其他技术手段来弥补其不足之处。[/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/services/cell-free-protein-synthesis-service][b]无细胞蛋白表达服务[/b][/url],服务优势:[/font][font=宋体]①快速、高效 ②高成功率 ③一致性 ④高难度抗体表达[/font][/font][font=宋体] [/font][font=宋体][font=宋体]详情可以咨询,具体[/font][font=Calibri]https://cn.sinobiological.com/services/cell-free-protein-synthesis-service[/font][/font]
[font=宋体]膜蛋白表达是生物学和医学领域中一个重要的研究课题,但很多人对此并不十分了解。本文将为大家解答关于膜蛋白表达的常见问题,帮助大家更好地理解这一领域的基本概念、研究方法和应用前景。[/font][font=宋体] [/font][font=宋体][font=Calibri]Q1:[/font][font=宋体]义翘神州膜蛋白[/font][font=Calibri]VLP[/font][font=宋体]平台是利用什么系统表达的?[/font][/font][font=宋体][font=Calibri]A1:VLP[/font][font=宋体]平台我们采用的是[/font][font=Calibri]HEK293[/font][font=宋体]细胞表达的,获得的蛋白更接近天然构象,更有利于客户进行后续的研究和应用。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Q2:[/font][font=宋体]膜蛋白[/font][font=Calibri]VLP[/font][font=宋体]产品可以做体内生物素标记吗?[/font][/font][font=宋体][font=Calibri]A2:[/font][font=宋体]可以的,可以选择在蛋白上加[/font][font=Calibri]AVI[/font][font=宋体]标签或者选择对[/font][font=Calibri]VLP[/font][font=宋体]本身生物素化,体内定点生物素标记,具体根据您的需求选择。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Q3:[/font][font=宋体]抗体与抗原结合在胞外,全长的多次跨膜蛋白意义大吗?[/font][/font][font=宋体][font=Calibri]A3:[/font][font=宋体]多次跨膜蛋白在细胞膜上多次跨越,在胞外形成多个胞外区,比如[/font][font=Calibri]Claudin18.2[/font][font=宋体]、[/font][font=Calibri]CD20[/font][font=宋体]、[/font][font=Calibri]CD133[/font][font=宋体]都有两个[/font][font=Calibri]ECL[/font][font=宋体]([/font][font=Calibri]extracellular loops[/font][font=宋体]),每个[/font][font=Calibri]ECL[/font][font=宋体]都有特定功能甚至会相互影响。全长可以保证蛋白构象天然完整,而且[/font][font=Calibri]ECL[/font][font=宋体]展现完全,帮助筛选靶向多次跨膜蛋白抗原的理想抗体。给大家看下面两张图,全长的意义就显而易见了,结构完整,功能上也有保证。这么看,全长也不是我们[/font][font=Calibri]ACRO[/font][font=宋体]一直在强调全长,而是客户需要全长的多次跨膜蛋白,满足客户需要的产品是[/font][font=Calibri]ACRO[/font][font=宋体]的初衷。我们也比较过,单独的胞外[/font][font=Calibri]ECL[/font][font=宋体]区蛋白活性确实比全长蛋白差。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Q4:[/font][font=宋体]相比其他非[/font][font=Calibri]Nanodisc[/font][font=宋体]产品,[/font][font=Calibri]Nanodisc[/font][font=宋体]有什么好处吗?[/font][/font][font=宋体][font=Calibri]A4:Nanodisc-[/font][font=宋体]膜蛋白与去垢剂[/font][font=Calibri]-[/font][font=宋体]膜蛋白相比,的确有不同。首先,原理上,[/font][font=Calibri]Nanodisc[/font][font=宋体]膜蛋白是将膜蛋白除去去垢剂之后组装在类细胞膜的[/font][font=Calibri]Nanodisc[/font][font=宋体]上。其次,应用上,我们都知道,去垢剂会溶膜从而对细胞产生损伤,[/font][font=Calibri]Nanodisc[/font][font=宋体]版本的膜蛋白因不含去垢剂,可以进一步扩展到用于细胞试验、[/font][font=Calibri]CAR[/font][font=宋体]阳性率检测,应用范围是更广的。另外,我们[/font][font=Calibri]ACRO[/font][font=宋体]使用的[/font][font=Calibri]Nanodisc[/font][font=宋体]技术已经获得专利持有方的授权,在研发过程中是可以放心使用的。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Q5:VLP[/font][font=宋体]和[/font][font=Calibri]Nanodisc[/font][font=宋体]平台下的多次跨膜蛋白怎么去除非特异抗体?[/font][/font][font=宋体][font=Calibri]A5:[/font][font=宋体]非特异抗体的影响不容忽视,使用[/font][font=Calibri]VLP[/font][font=宋体]和[/font][font=Calibri]Nanodisc[/font][font=宋体]平台下的膜蛋白的确可能产生非特异抗体,我们这两个平台均有对应的用于反筛去除非特异抗体的空白对照:[/font][font=Calibri]VLP-[/font][font=宋体]膜蛋白有同型对照产品空白[/font][font=Calibri]VLP[/font][font=宋体];[/font][font=Calibri]Nanodisc[/font][font=宋体]有两款[/font][font=Calibri]MSP1D1[/font][font=宋体]空白产品,其中一款[/font][font=Calibri]MSP1D1[/font][font=宋体]作为[/font][font=Calibri]tag free [/font][font=宋体]膜蛋白的同型对照,如果使用生物素化的[/font][font=Calibri]Nanodisc-[/font][font=宋体]膜蛋白,另一款[/font][font=Calibri]MSP1D1[/font][font=宋体]可以作为同型对照。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Q6:VLP[/font][font=宋体]相关蛋白能适合冻干保存吗?[/font][font=Calibri]VLP[/font][font=宋体]的用于免疫有什么注意事项?比如能否乳化,对佐剂类型有没有要求?[/font][/font][font=宋体][font=Calibri]A6:[/font][font=宋体]包膜[/font][font=Calibri]VLP[/font][font=宋体]产品我们目前都是液体[/font][font=Calibri]-70[/font][font=宋体]°[/font][font=Calibri]C[/font][font=宋体]保存,干冰发货;非包膜[/font][font=Calibri]VLP[/font][font=宋体]我们是冻干保存的。[/font][font=Calibri]VLP[/font][font=宋体]免疫主要是需要注意佐剂量的选择,因为[/font][font=Calibri]VLP[/font][font=宋体]本身是可以增强免疫原性的,跟常规蛋白不同。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Q7:VLP[/font][font=宋体]和[/font][font=Calibri]Nanodisc[/font][font=宋体]产品稳定性如何。冷冻长时间保存可以吗?[/font][/font][font=宋体][font=Calibri]A7:VLP[/font][font=宋体]和[/font][font=Calibri]Nanodisc[/font][font=宋体]本身的稳定性是很好的,是可以在[/font][font=Calibri]-70[/font][font=宋体]°[/font][font=Calibri]C[/font][font=宋体]长期保存的。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Q8:[/font][font=宋体]如何确认[/font][font=Calibri]VLP-Claudin18.2[/font][font=宋体]表达的是该目标蛋白,纯度如何评估?产品上的电镜图片,怎么确认颗粒上有该蛋白[/font][font=Calibri]?[/font][/font][font=宋体][font=Calibri]A8:Claudin18.2-VLP [/font][font=宋体]我们会通过[/font][font=Calibri]anti-Claudin18.2[/font][font=宋体]特异性的抗体进行检测验证。纯度我们通过电泳[/font][font=Calibri]/HPLC/DLS[/font][font=宋体]电镜进行评估。常规负染电镜因分辨率低是没办法看到[/font][font=Calibri]VLP[/font][font=宋体]上是否有[/font][font=Calibri]Claudin18.2[/font][font=宋体]的。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州搭建了基于[/font][font=Calibri]HEK293[/font][font=宋体]表达系统的[/font][font=Calibri]VLP[/font][font=宋体]([/font][font=Calibri]virus-like particle[/font][font=宋体])技术平台,能够将目的膜蛋白完整展示在[/font][font=Calibri]VLP[/font][font=宋体]表面,使其能够像普通蛋白一样进行检测,已上线的[/font][font=Calibri]Claudin 18.2[/font][font=宋体]、[/font][font=Calibri]GPRC5D[/font][font=宋体]、[/font][font=Calibri]Claudin 6[/font][font=宋体]等产品均展示出良好活性。义翘神州目前可以为客户提供[url=https://cn.sinobiological.com/services/membrane-protein-expression-service][b]膜蛋白定制服务[/b][/url],助力药物研发进程。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]多次跨膜蛋白开发技术平台:[/font][font=Calibri]https://cn.sinobiological.com/services/platform/multi-pass-transmembrane-protein[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]VLP[/font][font=宋体]形式的膜蛋白表达服务:[/font][font=Calibri]https://cn.sinobiological.com/services/membrane-protein-expression-service[/font][/font]
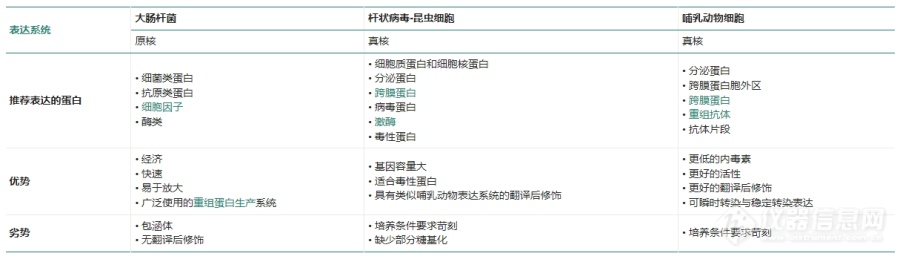
[font=宋体][font=宋体]义翘神州具有每年[/font][font=Calibri]1,000[/font][font=宋体]多种新蛋白的研发能力,依托先进的蛋白表达技术,在重组蛋白生产如跨膜蛋白、酶、激酶、病毒抗原等积累了丰富的经验。我们拥有多种重组蛋白表达系统,包括昆虫细胞、哺乳动物细胞和原核蛋白表达系统,为客户提供高品质、低成本的活性重组蛋白,满足您的不同需求。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供从基因合成、载体构建到蛋白质表达、纯化的一站式服务,可以根据客户需求,选用不同表达[/font][font=Calibri]/[/font][font=宋体]纯化标签、表达宿主等,真正为客户实现深度私人定制。多种纯化体系,为蛋白表达、纯化提供多种选择,帮助客户最大限度提高研究项目的成功率。‘’[/font][/font][font=宋体] [/font][font=宋体][b]重组蛋白表达服务的类型:[/b][/font][font=宋体] [/font][font=宋体][font=宋体]一、[/font][font=Calibri]VLP[/font][font=宋体]形式的膜蛋白表达服务[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州利用[/font][font=Calibri]HEK293[/font][font=宋体]表达系统构建了[/font][font=Calibri]VLP[/font][font=宋体]技术平台,为客户提供膜蛋白定制服务,助力药物研发。[/font][/font][font=宋体] [/font][font=宋体]优势:[/font][font=宋体]? 活性优,哺乳动物细胞表达,更接近真实构象[/font][font=宋体][font=宋体]? 多应用,免疫、[/font][font=Calibri]ELISA[/font][font=宋体]、[/font][font=Calibri]SPR/BLI[/font][font=宋体]、[/font][font=Calibri]PK/PD[/font][font=宋体]等[/font][/font][font=宋体] [/font][font=宋体]二、哺乳动物细胞瞬时表达服务[/font][font=宋体]义翘神州的哺乳动物瞬时表达系统提供灵活的定制服务,满足多样化需求。[/font][font=宋体] [/font][font=宋体]优势:[/font][font=宋体]? 高效表达载体[/font][font=宋体]? 高密度细胞培养[/font][font=宋体] [/font][font=宋体][font=宋体]三、杆状病毒[/font][font=Calibri]-[/font][font=宋体]昆虫细胞蛋白表达服务[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州在杆状病毒[/font][font=Calibri]-[/font][font=宋体]昆虫细胞蛋白表达方面具有丰富的经验,特别是病毒类蛋白、激酶等。[/font][/font][font=宋体] [/font][font=宋体]优势:[/font][font=宋体]? 高效表达胞内和胞外蛋白[/font][font=宋体]? 大规模蛋白表达生产能力[/font][font=宋体] [/font][font=宋体][font=宋体]四、原核([/font][font=Calibri]E.coil[/font][font=宋体])蛋白表达服务[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州[/font][font=宋体]“一站式”服务以及内毒素去除等附加服务,以满足不同的定制需求。[/font][/font][font=宋体] [/font][font=宋体]优势:[/font][font=宋体]? 多种表达载体和菌株[/font][font=宋体]? 丰富的包涵体纯化经验[/font][font=宋体] [/font][font=宋体]五、生产用稳定株构建服务[/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供优质稳定细胞株构建服务,满足客户蛋白[/font][font=Calibri]/[/font][font=宋体]抗体生产、免疫治疗药物开发等诸多需求。[/font][/font][font=宋体] [/font][font=宋体]优势:[/font][font=宋体][font=宋体]? 稳定细胞株抗体产量可达[/font][font=Calibri]2-4 g/L[/font][/font][font=宋体][font=宋体]? 团队重组表达经验[/font][font=Calibri]15[/font][font=宋体]年以上[/font][/font][font=宋体] [/font][font=宋体]六、检测用细胞系构建服务[/font][font=宋体] [/font][font=宋体]义翘神州提供稳定表达特定基因的细胞株构建服务,可应用于多种研究领域。[/font][font=宋体] [/font][font=宋体]优势:[/font][font=宋体]? 快速交付,经验丰富[/font][font=宋体]? 应用场景广泛,满足多样化实验需求[/font][font=宋体] [/font][font=宋体]选择哪种[url=https://cn.sinobiological.com/services/recombinant-protein-expression-service][b]蛋白表达服务[/b][/url]取决于目的蛋白的来源、蛋白功能、产率、成本和纯化蛋白的用途等诸多因素,每个系统都有其优缺点,根据不同应用选择合适的表达系统对重组蛋白非常重要。下面是重组蛋白表达服务选择指南:[img=重组蛋白表达服务选择指南,690,198]https://ng1.17img.cn/bbsfiles/images/2023/11/202311031655095289_8336_5907840_3.png!w690x198.jpg[/img][/font][font=宋体][font=宋体]更多关于重组蛋白表达服务详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/services/recombinant-protein-expression-service[/font][/font][font=Calibri] [/font]
很多朋友问这样一个问题:为什么毕赤酵母表达困难?他们自己也很纳闷,重组酵母pcr检测也证明目的基因重组了,但是诱导之后就是在表达上清中检测不到目的蛋白,仔细研究操作手册后仍然不知道原因。本人,根据自己的经验,采用倒推的方法,按实验过程从后向前分析,供大家参考:1、诱导之后表达上清中检测不到目的蛋白:分析1:检测的方法是否有问题,要考虑是不是蛋白表达量低而没有检测到? 如果是蛋白表达低,可以选择浓缩蛋白,具体的方法很多,有TCA、丙酮、浓缩柱等等方法,之前在本版已经发过帖,在此不赘述。 2、如果蛋白浓缩N倍之后仍然检测不到,那基本可以确证蛋白并不在上清中。那么蛋白到哪里去了,考虑是否没有分泌出来,而是在胞内,那就需要通过裂解酵母来检 测胞内蛋白,具体的方法很多,在此也不赘述,曾整理过相关破碎的帖子。 3、如果胞内也没有目的蛋白表达,那么基本可以确定蛋白并没有表达。 4、为什么没有表达呢?倒推回来就是诱导的过程了,诱导体系是什么?甲醇浓度是多少?培养问题是多少,转速是多少?这些都要注意。甲醇一般是0.5%-1.0%,本人用的 是0.5%,也有很多人也用1.0%,曾见过一个帖子,说超过1.5%反而会抑制表达,没有验证过,供大家参考。培养问题28-30度比较合适,转速250rpm比较合适,诱导 体系没有固定的体系,说明书上推荐的是BMGY到OD600 2~6,换到BMMY中OD600 为1左右。 5、如果诱导的过程也没有问题,那问题就复杂了,特别是重组酵母PCR检测证明目的基因确实已经发生了重组。这个时候是最郁闷的了,但是郁闷怎么办,还是要找原 因,在此我给的建议是先做RT-PCR证明mRNA水平的情况,也就是说有没有转录。如果转录了,后续的操作也没有问题(本帖的1、2、3、4项),那么只有重新设计实 验,比如换酵母株,有文章上说:用GS115表达不出蛋白,换KM71H后,大部分克隆能表达。 6、有个帖子说的很好,在此和大家分享一下。 1、 菌株:用GS115表达不出蛋白,换KM71H后,大部分克隆能表达。 2、温度: 在28度和室温下诱导表达,表达水平可能都不低。 3、pH:手册上用6.0,pH提高到6.8,不表达的蛋白可能就表达出来。BMMY的pH7.0-7.5比较合适。国内外做的最好的rHSA,最适pH大概5-6左右。pH3的时 候yeast和peptone好像会沉淀的,可以用磷酸和磷酸二氢钾调,具体比例自己去试试。 4、偏爱密码子: codon bias一般不是主要的问题,你要表达的蛋白特性才是主要问题,酵母对分子量大(30KD以上),结构复杂(如一些蛋白酶),二硫键含量多的 蛋白往往不能有效表达,尤其是分泌表达。密码子改造对一些较小的而且结构简单的蛋白表达量的提高可能有一些作用。比如一位战友用Pichia酵母表达一个单链 抗体,29KD,含有2对二硫键,表达量约几毫克每升,选用酵母偏好密码子全基因合成后,表达量没有什么提高。 5、表达时间与空质粒转化对照:诱导时间长了以后,是会有很多蛋白分泌出来的,时间越长杂蛋白就越多,且分子量都比较大。最好做一个空质粒转化的对照, 这样就会比较肯定到底是不是自身的蛋白分泌的结果。 6、污染:每个样品从G418板上挑10个左右单克隆于2ml BMGY摇菌(30ml玻璃管,比LB管大一点),纱布一般用8层,一天左右看着比较浑离心,留样1ml,余 1ml换2ml BMMY诱导表达,3,4层纱布足够了。 污染一般都是跟瓶口覆盖有关的原因造成的,只盖纱布肯定会污染。加盖报纸后,就再没遇到过污染。如果只用6层纱布,污染的可能当然很大,100ml三角瓶, 装量10ml培养液,用橡筋把8层纱布和2层报纸拴紧封口,空气浴摇床。 7、不表达:蛋白有没有表达就要看你的运气了,一般重复2-3次实验都没有表达菌株,这个蛋白就放弃表达了。 8、表达量: 30KD,10mg/L表达量已经很高,最直接的方法是发酵,一般提高5-10倍。大肠杆菌一样出现大团的超表达蛋白。 9、糖基化:酵母分泌表达的N糖基化是可以预测的,有如下序列:N X S/T就是潜在的糖基化位点,X为任意氨基酸,1个糖基化位点会加上1-3KD左右的糖基。另外可 能还有O糖基化话,但是无法预测其位点,不过很少听说表达蛋白有O糖基化的。如果胞内表达,不存在糖基化的问题。 10、表型与表达:重组SalI和BglII酶切产生单交换和双交换,结果就是产生Mut+和Muts表型的菌株;前者在甲醇诱导表达时生长快,消耗的甲醇多,后者生长慢,消耗 的甲醇少,所以诱导表达时Muts表型要求更高的菌体浓度。一般用Mut+表型的较多,但是对某些蛋白Muts菌株可能表达的更好,只有试试才知道你的蛋白用那种菌 株表达较好。 11、培养基 YPD:最基本的培养用;BMGY:诱导表达前培养用;BMMY:诱导表达用;MD:电转化后筛选his+用。 YEPD是不能代替BMGY的,因为有葡萄糖,这样残留的葡萄糖会影响下一步的诱导表达。不过有一种方法是可行的,就是用YPG培养基代替,只是把YEPD中的葡萄糖 用3%的甘油代替,也可以降低成本。摇瓶毕竟不能和发酵罐比,甘油残余会抑制甲醇利用。 BMGY、BMMY灭菌后才能加甲醇、磷酸钾、生物素。配制BMMY时也没必要用5%过滤除菌的甲醇,在灭菌后使用前加100%甲醇至你要的浓度。 YNB可以高压灭菌,没问题的,也可以0.22um过滤处理,天冬氨酸和苏氨酸要待培养基高压灭菌后加入;配YPD时可以加入YPD一起灭菌,但时间不能太长,温度不能 太高,一般121-125度12-15分钟足够了。若时间过长,温度过高,可能导致YPD焦化。glucose和含氮化合物在一起容易产生美拉德反应,这是配制培养基中的禁忌。 颜色很深的话,基本不能使用了。或者含有葡萄糖和/或YNB的培养基108度35min高压灭菌。 小量发酵其实可以把培养基成分中的YNB和生物素去除,培养基价格便宜,操作又方便,可以直接灭菌,效果也很好(效果不比含YNB的差)。 如果是用自己配置的培养基,如玉米浸提液、麦芽浸提液、麦麸浸提液等等,可以不用换液,采取添料来维持酵母对培养基的营养需要。 用无机盐进行大规模发酵,更省钱。更多有关蛋白表达纯化的相关资料,请点击:资料专区
[font=宋体][b]什么是抗体纯化?抗体纯化原理:[/b][/font][font=宋体][font=宋体]抗体纯化是指从抗血清([/font][font=Calibri]pAb[/font][font=宋体])、腹水或杂交瘤细胞系([/font][font=Calibri]mAb[/font][font=宋体])细胞培养上清液中提取抗体的过程。纯化后的抗体适用于多种应用。该过程可以在提供抗体纯化服务的实验室中进行,如果有必需的设备和工具,也可以自行纯化。如研究人员担心原始研究的完整性受到破坏,可在实验室中进行纯化,确保研究快速进行。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]抗体的主要来源之一是在动物体内生成的抗血清。在这种情况下,反复向动物体内注射抗原,直到抗体开发完成为止,其血液用于制备抗血清,经纯化后可获得多克隆抗体。抗体的另一个来源是克隆细胞,其作为相同细胞群的一部分生成抗体;这种方法用于大规模生产单克隆抗体。查看更多有关[/font][font=宋体]“单克隆抗体纯化”的信息。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]什么是蛋白纯化?[/b][/font][font=宋体] [/font][font=宋体]重组蛋白的纯化是生物学研究中的重要技术。为了研究蛋白的特定功能和结构,研究人员必须将重组蛋白从生物体中分离并纯化。蛋白纯化方法主要利用不同重组蛋白之间的相似性和差异性。可以根据蛋白之间的相似性去除非蛋白物质,然后根据蛋白之间的差异分离纯化目标重组蛋白。[/font][font=宋体] [/font][font=宋体][font=宋体]蛋白标签是一种可以提高重组蛋白的溶解度、简化蛋白纯化的简单有效的工具,并通过简单的方法跟踪蛋白表达和纯化过程。此外,蛋白标签是追踪活细胞中蛋白和进程的一种有效工具,可以通过显微镜直接跟踪或者通过[/font][font=Calibri]Western blot[/font][font=宋体]、免疫沉淀或免疫染色间接进行跟踪。[/font][/font][font=宋体] [/font][font=宋体][b]蛋白纯化原理:[/b][/font][font=宋体] [/font][font=宋体]不同的重组蛋白具有不同的氨基酸序列和空间结构,导致其物理、化学和生物学特性存在差异。我们也可以根据目标蛋白与其他蛋白和裂解液的性质差异设计合理的蛋白纯化方案。[/font][font=宋体] [/font][font=宋体][font=宋体]大多数的纯化方案需要不止一步才能达到理想的纯度水平。该过程中的每一步都会造成一定的产品损失,假设每一步的获得率为[/font][font=Calibri]80%[/font][font=宋体]。因此,建议尽可能减少纯化步骤。起始原料的选择是纯化过程设计的关键。[/font][/font][font=宋体] [/font][font=宋体]在背景信息、检测方法和样品规格都已到位的情况下,可以考虑采用三阶段纯化策略。纯化分为捕获、中度纯化和精细纯化三个阶段,每个阶段都有特定的目标。捕获阶段的目标是分离、浓缩和稳定目标产物。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供重组蛋白表达纯化服务和[url=https://cn.sinobiological.com/services/monoclonal-antibody-production-services][b]单克隆抗体定制服务[/b][/url],更多详情可以关注[/font][font=Calibri]https://cn.sinobiological.com/services/monoclonal-antibody-production-services[/font][/font][font=宋体][font=Calibri]https://cn.sinobiological.com/services/recombinant-protein-expression-service[/font][/font]
大肠杆菌表达蛋白以可溶和不溶两种形式存在,需要不同的纯化策略。现在,许多蛋白质正在被发现而事先并不知道它们的功能,这些自然需要将蛋白质纯化出来后,进行进一步的研究来获得。分析蛋白质的方法学现已极大的简化和改进。必须承认,表达蛋白纯化比起DNA克隆和操作来是更具有艺术性的,尽管DNA序列具有异乎寻常的多样性(因而它是唯一适合遗传物质的),但它却有标准的物理化学性质,而每一种蛋白质则有它自己的由氨基酸序列决定的物理化学性质(因而它具有执行众多生物学功能的用途)。正是蛋白质间的这些物理性质上的差异使它们得以能进行纯化但这也意味着需要对每一种待纯化的蛋白质研发一套新的方法。所幸的是,尽管存在这种固有的困难,但现已有多种方法可以利用,蛋白质纯化策略也已实际可行。目前,待研究蛋白或酶的基因的获得已是相当普遍的事。可诱导表达系统特别是Studier等发展的以噬菌体T7RNA聚合酶为基础的表达系统的出现使人们能近乎常规地获得过表达(overexpression),表达水平可达细胞蛋白的2%以上,有些甚至高达50%.(一)试剂准备采用T7· Tag Affinity Purification Kit1. T7·Tag抗体琼脂。2. B/W缓冲液:4.29mM Na2HPO4,1.47 mM KH2PO4,2.7 mM KCl,3. 0.137mM NaCl,1%吐温-20,pH7.3。4. 洗脱缓冲液: 0.1M柠檬酸,pH2.2。5. 中和缓冲液:2M Tris,pH10.4.6. PEG 20000.(二)操作步骤1.100ml 含重组表达质粒的菌体诱导后,离心5000g×5min,弃上清,收获菌体,用10ml预冷的B/W缓冲液重悬。2. 重悬液于冰上超声处理,直至样品不再粘稠,4℃离心 14000g×30min,取上清液,0.45μm膜抽滤后作为样品液。3. 将结合T7·Tag抗体的琼脂充分悬起,平衡至室温,装入层析柱中。4. B/W缓冲液平衡后样品液过柱。5. 10ml B/W缓冲液过柱,洗去未结合蛋白。6. 用5ml洗脱缓冲液过柱,每次1ml,洗脱液用含150μl中和缓冲液的离心管收集,混匀后置于冰上,直接SDS-PAGE分析。7. 将洗脱下来的蛋白放入透析袋中,双蒸水透析24hr,中间换液数次。8. 用PEG 20000浓缩蛋白。(三)注意事项蛋白在过层析柱前,要0.45μm膜抽滤,否则几次纯化后,柱子中会有不溶物。
[font=宋体][font=宋体]抗组蛋白抗体是抗核抗体家族的一个亚基,专门针对组蛋白亚基或组蛋白复合物。[/font][font=Calibri]1959[/font][font=宋体]–[/font][font=Calibri]60[/font][font=宋体]年,[/font][font=Calibri]Henry Kunkel[/font][font=宋体]、[/font][font=Calibri]H.R.Holman[/font][font=宋体]和[/font][font=Calibri]H.R.G.Dreicher[/font][font=宋体]在对红斑狼疮细胞病因的研究中首次报道了这些抗体。如今,抗组蛋白抗体仍被用作系统性红斑狼疮的标志物,但也与其他自身免疫性疾病有关,如[/font][font=Calibri]Sj?gren[/font][font=宋体]综合征、皮肌炎或类风湿性关节炎。抗组蛋白抗体可作为药物诱导性狼疮的标志物。[/font][/font][font=宋体] [/font][b][font=宋体]特异性[/font][/b][font=宋体] [/font][font=宋体][font=宋体]组蛋白是蛋白质的复合体,[/font][font=Calibri]DNA[/font][font=宋体]储存在其周围。抗组蛋白抗体可以靶向组蛋白复合物或显示的任何蛋白质亚基。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]抗组蛋白抗体靶向五大类组蛋白亚基:[/font][font=Calibri]H1[/font][font=宋体]、[/font][font=Calibri]H2A[/font][font=宋体]、[/font][font=Calibri]H2B[/font][font=宋体]、[/font][font=Calibri]H3[/font][font=宋体]和[/font][font=Calibri]H4[/font][font=宋体]。抗组蛋白的抗体多种多样,因此除了靶向蛋白亚基外,不同的抗体也可能对不同的复合物,包括[/font][font=Calibri]H2A-H2B[/font][font=宋体]二聚体或[/font][font=Calibri]H3-H4[/font][font=宋体]四聚体。有证据表明,不同药物暴露产生的[/font][font=Calibri]IgG[/font][font=宋体]和[/font][font=Calibri]IgM[/font][font=宋体]抗组蛋白抗体对不同组蛋白复合物的表位具有特异性。高度修饰的组蛋白已被证明能促进更大的免疫反应。[/font][/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体]检测抗体[/font][/b][font=宋体] [/font][font=宋体][font=宋体]抗组蛋白抗体可以使用[/font][font=Calibri]ELISA[/font][font=宋体]测定法进行临床检测。测试需要血样。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]间接免疫荧光也可用于检测抗组蛋白抗体。均匀、扩散染色表明存在抗组蛋白抗体、染色质和一些双链[/font][font=Calibri]DNA[/font][font=宋体]。义翘神州提供[url=https://cn.sinobiological.com/services/immunofluorescence-servicehttp://][b]免疫荧光检测服务[/b][/url]![/font][/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体]抗组蛋白抗体阳性说明什么?[/font][/b][font=宋体] [/font][font=宋体]抗组蛋白是含有五个亚单位的碱性蛋白,抗组蛋白阳性说明可产生了组蛋白抗体,多存在系统性红斑狼疮、类风湿关节炎、风湿病等疾病中,建议患者对症治疗。[/font][font=宋体] [/font][b][font=宋体]正常值:[/font][/b][font=宋体]正常人抗组蛋白抗体为阴性。[/font][font=宋体] [/font][font=宋体]在探索抗组蛋白抗体的道路上,科学家们从未停止脚步。他们致力于解开这一生物标志物的所有谜团,以期为人类健康带来更多福祉。作为普通公众,我们也可以通过学习和了解抗组蛋白抗体的相关知识,为自己的健康保驾护航。让我们共同期待未来科学研究在抗组蛋白抗体领域取得的更多突破,为人类的健康事业贡献智慧和力量。[/font][b][font=宋体] [/font][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
[font=宋体][font=宋体]传统意义上,抗核抗体([/font][font=Calibri]antinuclear antibodies[/font][font=宋体],[/font][font=Calibri]ANA[/font][font=宋体])是所有抗细胞核抗原成分的自身抗体的总称,包括一大类抗体。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]然而,随着[/font][font=Calibri]ANA[/font][font=宋体]检测技术的改进、尤其是培养细胞抗原基质(如[/font][font=Calibri]HEp-2[/font][font=宋体]细胞,即人喉癌上皮样细胞系)的广泛运用,[/font][font=Calibri]ANA[/font][font=宋体]针对的靶抗原成分已由细胞核扩展到整个细胞成分,包括细胞核、细胞浆、细胞骨架及细胞分裂周期蛋白等。目前对[/font][font=Calibri]ANA[/font][font=宋体]的定义为:以真核细胞的各种成分为靶抗原的自身抗体的总称。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]ANA[/font][font=宋体]的检测方法,目前国际及国内指南或共识推荐的均是间接免疫荧光法([/font][font=Calibri]indirect immunofluorescence[/font][font=宋体],[/font][font=Calibri]IIF[/font][font=宋体]),而且是以[/font][font=Calibri]HEp-2[/font][font=宋体]细胞为实验基质的[/font][font=Calibri]IIF[/font][font=宋体]。此外还有[/font][font=Calibri]ELISA[/font][font=宋体]、线性免疫印迹法、化学发光免疫分析法等,各有优缺点。瑞金医院检验科实验室、皮肤科实验室均采用[/font][font=Calibri]IIF[/font][font=宋体]法检测[/font][font=Calibri]ANA[/font][font=宋体]。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]IIF-ANA[/font][font=宋体]规范的结果报告内容应包括:检测方法、定性结果(阳性[/font][font=Calibri]/[/font][font=宋体]阴性)、荧光模型、滴度、临床建议。[/font][font=Calibri]IIF-ANA[/font][font=宋体]荧光模型分[/font][font=Calibri]3[/font][font=宋体]类:细胞核荧光模型([/font][font=Calibri]14[/font][font=宋体]种)、细胞浆荧光模型([/font][font=Calibri]9[/font][font=宋体]种)、细胞有丝分裂荧光模型([/font][font=Calibri]5[/font][font=宋体]种);国内共识建议必报的荧光模型有[/font][font=Calibri]13[/font][font=宋体]种,细胞核类的有均质型、斑点型(需区分致密斑点型)、着丝点型、核点型、核仁型、核膜型,细胞浆类的有胞浆纤维型、胞浆颗粒型、胞浆网状[/font][font=Calibri]/[/font][font=宋体]线粒体型、胞浆极型[/font][font=Calibri]/[/font][font=宋体]高尔基体型、胞浆棒状环状型、胞浆线性[/font][font=Calibri]/[/font][font=宋体]肌动蛋白型。[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]抗核抗体[/font][font=Calibri]P[/font][font=宋体]蛋白抗体阳性通常指的是抗核糖体[/font][font=Calibri]P[/font][font=宋体]蛋白抗体阳性,它可能意味着身体存在结缔组织疾病,尤其是系统性红斑狼疮([/font][font=Calibri]SLE[/font][font=宋体])。[/font][/font][/b][font=宋体][font=宋体]包括类风湿关节炎、干燥综合征的患者等,阳性率并不是很高,特异性也不是很好。系统性红斑狼疮是一种自身免疫性疾病,可能会对皮肤黏膜、肝功能、中枢神经系统等造成损伤。抗核糖体[/font][font=Calibri]P[/font][font=宋体]蛋白抗体对系统性红斑狼疮具有高度特异性,尤其是在伴有典型神经系统症状的中枢神经系统损害型红斑狼疮中,出现抗核糖体[/font][font=Calibri]P[/font][font=宋体]蛋白抗体阳性的几率比较高。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]所以出现抗体阳性后,一定要到医院请专科大夫来进行诊断,并来进行合理的解释,再进行其他实验室检查,包括血沉、[/font][font=Calibri]C[/font][font=宋体]反应蛋白 、血尿常规、肝肾功能、类风湿因子,以及相关其他,如[/font][font=Calibri]SM[/font][font=宋体]抗体、核小体抗体、[/font][font=Calibri]SSA[/font][font=宋体]抗体、[/font][font=Calibri]SSB[/font][font=宋体]抗体等自身抗体检查。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/services/platform/facs-b-cell-sorting][b]单[/b][/url][/font][font=Calibri][url=https://cn.sinobiological.com/services/platform/facs-b-cell-sorting][b]B[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/services/platform/facs-b-cell-sorting][b]细胞分选平台[/b][/url],可向全球客户提供[url=https://cn.sinobiological.com/services/single-b-cell-antibody-service][b]单[/b][/url][/font][font=Calibri][url=https://cn.sinobiological.com/services/single-b-cell-antibody-service][b]B[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/services/single-b-cell-antibody-service][b]细胞抗体制备服务[/b][/url],整个过程涉及单[/font][font=Calibri]B[/font][font=宋体]细胞分离、测序、克隆和单[/font][font=Calibri]B[/font][font=宋体]细胞抗体筛选等步骤。更多详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/single-b-cell-technology[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
[font=宋体][font=Calibri]E. coli[/font][font=宋体]具有遗传背景清楚、细胞增殖快、表达量高、稳定性好和抗污染能力强等特点,适用于多种属蛋白的表达,尤其对小分子蛋白的生产具有极大的优势,但也存在一些问题,如易形成包涵体和含有内毒素等。义翘神州提供从密码子优化到重组蛋白表达[/font][font=Calibri]/[/font][font=宋体]纯化的一站式服务以及内毒素去除等附加服务,以满足不同的定制需求。我们拥有丰富的[/font][font=Calibri]E. coli [/font][font=宋体]可溶性蛋白表达[/font][font=Calibri]/[/font][font=宋体]纯化及蛋白复性经验,拥有多种[/font][font=Calibri]E. coli[/font][font=宋体]细胞株和表达载体,可为客户提供优质的[url=https://cn.sinobiological.com/services/e-coli-protein-expression-service][b]原核蛋白表达服务[/b][/url]。下面是在原核蛋白表达实验中常遇见的几大问题,为大家一一讲解:详情关注:[/font][font=Calibri]https://cn.sinobiological.com/services/e-coli-protein-expression-service[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]1[/font][font=宋体]、我不知道我的蛋白它有什么特性及其结构?[/font][/font][font=宋体] [/font][font=宋体]首先,你要确定一件事,那就是这几个蛋白质有人研究过没有?还是最新发现的蛋白质?如果没有人研究过,那就得用先测部分氨基酸,然后设计引物克隆了。如果有人研究过,那就好了可以根据软件来预测。[/font][font=宋体] [/font][font=宋体][font=宋体]如有[/font][font=Calibri]swiss[/font][font=宋体]—[/font][font=Calibri]pdb[/font][font=宋体]软件,但这个是要有氨基酸序列,知道基因序列,可以在[/font][font=Calibri]ncbi[/font][font=宋体]上进行[/font][font=Calibri]blastx[/font][font=宋体],得到蛋白。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2[/font][font=宋体]、如何选择蛋白表达宿主菌?[/font][/font][font=宋体] [/font][font=宋体]原核系统和真核细胞偏爱的密码子有不同,因此,在用原核系统表达真核基因的时候,真核基因中的一些密码子对于原核细胞来说可能是稀有密码子,从而导致表达效率和表达水平很低。[/font][font=宋体] [/font][font=宋体]原核表达现象:[/font][font=宋体]一、蛋白不表达[/font][font=宋体]①蛋白为毒蛋白[/font][font=宋体]②序列含有稀有密码子[/font][font=宋体] [/font][font=宋体]二、蛋白表达不理想[/font][font=宋体]①蛋白明显降解[/font][font=宋体]②蛋白表达为包涵体[/font][font=宋体]③二硫键错误折叠[/font][font=宋体]④过高的本底表达[/font][font=宋体] [/font][font=宋体][font=Calibri]3[/font][font=宋体]、质粒测序正确,蛋白无法表达怎么办?[/font][/font][font=宋体] [/font][font=宋体][font=宋体]①分析一下稀有密码子,如果比较多,可以尝试[/font][font=Calibri]rosetta[/font][font=宋体]([/font][font=Calibri]DE3[/font][font=宋体]);[/font][/font][font=宋体][font=宋体]②可能是基因本身的问题。[/font][font=Calibri]RNA3[/font][font=宋体]’的特殊结构可能导致转录出现问题,这种情况可以尝试融合表达,譬如[/font][font=Calibri]pET-32a[/font][font=宋体]。[/font][/font][font=宋体][font=宋体]③也许是表达量太低,也可以试一下[/font][font=Calibri]westernblot[/font][font=宋体],定性的检测一下。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4[/font][font=宋体]、如果[/font][font=Calibri]IPTG[/font][font=宋体]诱导后细胞停止了生长,是不是表示细胞死了?[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]T7RNA[/font][font=宋体]聚合酶非常活跃,[/font][font=Calibri]T7[/font][font=宋体]转录和翻译信号极强,因此,一旦诱导,细胞的主要生理活动都向着目的蛋白表达的方面转化。在通常情况下,细胞将停止生长,形成克隆的能力大大降低,但并未死亡。菌落形成试验可以用来检测表达系统的性能。也有一些例外情况,例如特别的目的基因以及一些极为严紧的载体[/font][font=Calibri]/[/font][font=宋体]宿主菌组合(比如含有[/font][font=Calibri]pLysE[/font][font=宋体]的宿主菌)等,这时在诱导后菌落还是会继续生长。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]5[/font][font=宋体]、如何提高重组蛋白在原核细胞里的表达水平,特别是可溶性表达?[/font][/font][font=宋体] [/font][font=宋体]这个问题是最困扰做原核蛋白表达纯化的人的。比如大肠杆菌表达蛋白本身表达量就大,但是表达的大都是包涵体,想要获得可溶性蛋白,就需要做复性,或是再设计实验时就想办法让其在上清中表达。一般就要通过基因优化,载体宿主优化筛选,表达条件优化,诱导条件优化等等。[/font][font=宋体] [/font][font=宋体]①降低重组蛋白合成的速率[/font][font=宋体]可溶性蛋白的产率取决于蛋白的合成速率,蛋白的折叠速率,以及聚集的速率。高水平表达时,肽链聚集的速率一旦超过折叠速率,就会形成包涵体。因此,降低重组蛋白合成的速率有利于提高重组蛋白的可溶性表达。[/font][font=宋体] [/font][font=宋体]②密码子优化[/font][font=宋体][font=宋体]密码子优化就是根据表达系统对密码子的偏好性进行优化筛选。经过优化的基因序列往往能提高[/font][font=Calibri]mRNA[/font][font=宋体]二级结构的稳定性,有利于新生肽段的正确折叠,提高外源活性蛋白的表达。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]③表达温度的选择大肠杆菌的最适生长温度在[/font][font=Calibri]37[/font][font=宋体]~[/font][font=Calibri]39[/font][font=宋体]℃之间,但此温度下极易生成包涵体蛋白,降低可溶性蛋白的表达,而低温培养条件下表达外源蛋白能有效地增加可溶蛋白的比例。[/font][/font][font=宋体] [/font][font=宋体]④诱导条件优化[/font][font=宋体]摇瓶培养时,应选用低菌体浓度诱导,因为在低菌浓度下菌体处于对数生长期,生长活跃,有利于表达可溶性蛋白。然而,如果能保证合理的补料与充分的通气,在较高菌浓度下诱导也同样可能获得可溶蛋白的高效表达。在某些情况下,诱导剂的流加能显著提高可溶蛋白的表达水平。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=Calibri]6[/font][font=宋体]、义翘神州提供标签去除服务吗?[/font][/font][font=宋体] [/font][font=宋体]是的。我们构建载体时可以在标签蛋白和目的蛋白之间加上蛋白酶的酶切位点,这样纯化后就可以利用蛋白酶去除标签,得到完整的目的蛋白。蛋白酶的切割效率受目的蛋白的影响,具体由实验结果而定。[/font][font=Calibri] [/font]
[font=宋体]在分子生物学和生物工程领域,蛋白表达载体构建是至关重要的技术之一,它涉及到将目的基因插入到适当的表达载体中,以便在宿主细胞内进行蛋白表达。这一过程不仅有助于研究基因的功能和蛋白质的结构,还为药物开发、基因治疗等领域提供了有力支持。本文将详细介绍蛋白表达载体构建的整个流程,包括目的基因的选择、载体的选择与改造、基因插入、转化、筛选与鉴定等关键步骤。[/font][font=宋体] [/font][b][font=宋体]蛋白表达载体构建流程:[/font][/b][font=宋体] [/font][font=宋体][font=宋体]①[/font][font=Calibri]NCBI[/font][font=宋体]查找目的基因的[/font][font=Calibri]CDS[/font][font=宋体]序列[/font][/font][font=宋体][font=宋体]进入[/font][font=Calibri]NCBI[/font][font=宋体](美国国家生物技术信息中心)的网站。[/font][/font][font=宋体]在搜索框中输入目的基因的名称或关键词。[/font][font=宋体][font=宋体]在搜索结果中找到[/font][font=Calibri]CDS[/font][font=宋体]([/font][font=Calibri]Coding Sequence[/font][font=宋体])序列,通常会显示基因的[/font][font=Calibri]DNA[/font][font=宋体]序列。[/font][/font][font=宋体][font=宋体]记录或复制所需的[/font][font=Calibri]CDS[/font][font=宋体]序列信息。[/font][/font][font=宋体] [/font][font=宋体]②选择合适的表达载体[/font][font=宋体]根据目的基因的性质和所需的表达水平,选择适合的表达载体。[/font][font=宋体]考虑载体的克隆容量、复制子类型、筛选标记等。[/font][font=宋体] [/font][font=宋体]③确定双酶切位点[/font][font=宋体]根据目的基因和载体,选择合适的双酶切位点。[/font][font=宋体][font=宋体]确保酶切位点在[/font][font=Calibri]CDS[/font][font=宋体]序列和载体上都是独特的,避免切割其他部位。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]④[/font][font=Calibri]Primer 5[/font][font=宋体]预测目的序列酶切位点[/font][/font][font=宋体][font=宋体]使用[/font][font=Calibri]Primer 5[/font][font=宋体]或其他相关软件,根据已知的[/font][font=Calibri]CDS[/font][font=宋体]序列设计酶切位点的引物。[/font][/font][font=宋体]通过软件预测引物的特异性,确保它们仅与目的基因结合。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]⑤双酶切[/font][font=Calibri]buffer[/font][/font][font=宋体][font=宋体]根据选择的酶,准备相应的酶切[/font][font=Calibri]buffer[/font][font=宋体]。[/font][/font][font=宋体][font=宋体]注意[/font][font=Calibri]buffer[/font][font=宋体]的[/font][font=Calibri]pH[/font][font=宋体]值和离子浓度,确保酶的活性。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]⑥目的基因[/font][font=Calibri]CDS[/font][font=宋体]序列引物设计[/font][/font][font=宋体][font=宋体]根据[/font][font=Calibri]CDS[/font][font=宋体]序列,设计一对引物用于[/font][font=Calibri][url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url][/font][font=宋体]扩增目的基因。[/font][/font][font=宋体]确保引物的特异性,避免与其他基因序列发生非特异性结合。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体]⑦转化[/font][font=宋体][font=宋体]制备感受态细胞,使其处于易于接受外源[/font][font=Calibri]DNA[/font][font=宋体]的状态。[/font][/font][font=宋体][font=宋体]将[/font][font=Calibri][url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url][/font][font=宋体]扩增得到的目的基因与载体混合,进行转化反应。[/font][/font][font=宋体]将转化后的细菌在选择培养基上培养,筛选含有重组载体的阳性克隆。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体]⑧双酶切及鉴定[/font][font=宋体][font=宋体]提取阳性克隆的质粒[/font][font=Calibri]DNA[/font][font=宋体]。[/font][/font][font=宋体]使用设计的引物进行双酶切反应。[/font][font=宋体]对酶切产物进行电泳分析,观察是否获得预期的片段,并进行凝胶回收。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体]⑨测序[/font][font=宋体]将回收的酶切产物进行序列测定。[/font][font=宋体][font=宋体]对比测序结果与目的基因的[/font][font=Calibri]CDS[/font][font=宋体]序列,确保没有突变或错误。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体]⑩阳性菌落扩大培养,用于后期蛋白纯化研究[/font][font=宋体] [/font][font=宋体]选择测序正确的阳性菌落进行扩大培养。[/font][font=宋体]在摇瓶或发酵罐中进行高密度培养,为后续的蛋白表达提供充足的原料。[/font][font=宋体]在确定目的基因在载体上正确表达后,可以进行蛋白纯化研究。[/font][font=宋体]通过适当的纯化技术,如亲和层析、离子交换等,分离和纯化目的蛋白。[/font][font=宋体]对纯化的蛋白进行质量分析和功能研究。[/font][font=宋体] [/font][font=宋体][font=宋体]综上所述,蛋白表达载体构建是一个系统性的过程,涉及到多个关键步骤和复杂的技术操作。通过遵循这一流程,研究人员能够成功地在宿主细胞内表达所需蛋白,并进一步对其进行分析和功能研究。随着生物技术的不断发展,蛋白表达载体构建的应用领域将越来越广泛,为人类对生命现象的深入理解和疾病的防治提供更多可能性。因此,不断优化和完善这一技术对于生命科学领域的发展至关重要。更多[url=https://cn.sinobiological.com/resource/protein-review/protein-production][b]蛋白表达生产[/b][/url]详情可以关注[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/protein-production[/font][/font]
为获得某蛋白(A)的特异性抗体,你用该蛋白免疫家兔,你将如何监控针对蛋白(A)抗原产生抗体的动态过程?(简述所选择方法的原理及步骤)期待您的解答,非常感谢。
70kDa)中的七个得到了可溶性表达,而其它的融合标签(GST,MBP和hexahistidine)系统则只得到了四个可溶性表达的蛋白。表1. 用大量的目标蛋白评估NusA标签对提高融合蛋白可溶性的作用参考文献a目的蛋白数目目的插入序列种属目标蛋白大小范围NusA融合蛋白可溶性比例Shih等(2002)40酵母,哺乳动物,植物,昆虫9-10060Korf等(2005)75人6-12760bKohl等(2008)96人1-11844ca. Korf等和Kohl等的研究中包含了六组氨酸标签。b. 可溶性蛋白量大于等于10%即认为该融合蛋白可溶。c. 纯化后的融合蛋白如果在SDS-PAGE后考染在合适位置出现条带即认为可溶。Korf等的还发现对于定位于真核细胞细胞器,质膜或者骨架的蛋白,相对于其它标签系统来讲,NusA标签是最好的可溶性表达的选择。Kohl等(2008)也发现只要在20-25℃诱导表达,NusA标签能够大大提高难表达的蛋白比如膜蛋白的可溶性。与Korf等的研究结果一致,Kohl等也发现25℃诱导表达比30℃或37℃诱导表达可以纯化得到更多的NusA融合蛋白。切除NusA标签获得后保持活性且正确折叠的蛋白表2总结了16个采用NusA标签成功获得可溶性蛋白,在切除标签后这些蛋白仍有正确折叠结构和活性。大部分这种研究是是关于分子量小于或接近20kDa的目标蛋白。纯化后的目标蛋白产量范围在1.5-100mg/L。趋化因子和细胞因子可以得到高达30-100mg/L的产量。其它关于这些蛋白表达和纯化的有参考价值信息包括:■ 植物磷酸烯醇式丙酮酸—羧化酶激酶(Ermolova 2003)——目标蛋白切除标签后用BDA(蓝色葡聚糖)亲和层析树脂纯化。纯化后蛋白的催化活性比未切除标签的融合蛋白高50倍。■ Xklp3a,Tep3Ag和E8R(De Marco 2004)——用蛋白酶切割后,His-融合的TEV和NusA被Ni2+离子亲和色谱选择性去除。与Ni2+亲和结合的标签被紧密地结合在树脂上,在流出液中则可以得到纯化的目的蛋白。所有这三种蛋白在纯化后都正确折叠且均一分散在溶液中。纯化的膜结合蛋白E8R牛痘病毒蛋白在Tris缓冲液中除去NusA后出现了沉淀,然而加入0.02%的月桂酰基麦芽糖苷和150mM的氯化钠后,蛋白又重新变得可溶。■ 环麦芽糖糊精酶(Turner 2005)——这个蛋白属于α-淀粉酶家族。这个家族的蛋白通常在大肠杆菌中很难以活性形式表达出来。将其与肠激酶混合孵育24小时以上会使其活性逐渐增强,直到达到未经肠激酶处理过的融合蛋白的2倍以上,这也说明标签的存在降低了该酶的活性。可以用固化了Cu2+的亲和层析柱去除切除的融合标签。■ 八种人趋化因子(Magis-trelli 2005)——所有的蛋白都在OrigamiTM B菌株中表达提高它们在胞质中的二硫键形成率。在趋化因子编码序列的C端引入了AviTMTag(亲和素)生物素化序列。切割后的细胞趋化因子可以用单体的亲和素树脂亲和层析与切割下的NusA标签和蛋白酶混合物分离开。所有切割纯化后的蛋白在细胞趋化实验中都显示了活性,而没有一个融合蛋白有这样的活性。■ 蚯蚓血红蛋白(Karlsen 2005)——酶切后,用分子筛分离纯化蚯蚓血红蛋白,纯化后的蛋白通过圆二色谱检测得到的α-螺旋结构与模型预期结果一致,且纯化后的蛋白可以以单体的形式稳定保存。■ 人白介素-29(Li 2006)——用S-蛋白亲和层析比Ni2+亲和层析可以得到更纯的目的蛋白。将融合蛋白N端的NusA/His•Tag®/S•Tag™标签切掉后,用链亲和素琼脂去除生物素标记的凝血酶。用水疱性口膜炎病毒(VSV)处理固定的人羊膜上皮细胞(WISH 细胞)后,通过检测纯化的IL-29对细胞的保护效应来检测其抗病毒活性。■ 人干扰素-λ2(Li 2007)——酶切后,用Novagen提供的EKaptureTM琼脂除去重组的肠激酶。先用纯化后的干扰素-λ2处理WISH细胞,24小时后加入VSV病毒,可以观察到干扰素-λ2可以有效地保护细胞免于病毒介导的病变。表2. 切除NusA标签获得后保持活性且正确折叠的蛋白参考文献目的蛋白目的蛋白分子量(kDa)切割用蛋白酶融合蛋白亲和层析固定介质纯化后目的蛋白产量(mg/L)Ermolova等(2003)植物磷酸烯醇式丙酮酸羧化酶激酶32凝血酶Ni2+1.5De Marco等(2004)Xklp3ATep3AgE8R15NRa32bTEV酶TEV酶TEV酶Ni2+5.02.54.0Turner等(2005)环麦芽糖糊精酶69肠激酶Cu2+1.6Magistrelli等(2005)八种人趋化因子8-21Xa因子Ni2+30-100Karlsen等(2005)蚯蚓血红蛋白15TEV酶Ni2+NRaLi和He(2006)人白介素-2920凝血酶S-蛋白60Li和Huang(2007)人干扰素-λ220肠激酶Ni2+65a. 未报道b. 根据NCBI报道预测的全长蛋白分子量与NusA标签融合且具有活性的蛋白 与这些切除NusA标签后保持活性且正确折叠的蛋白不同,还有很多报道指出目的蛋白在“NusA-目的蛋白”的融合形式时具有很好的活性。比如单链(ScFv)催化活性抗体14D9(Zheng 2003),来自Aequorea victoria的绿色荧光蛋白(Nallamsetty 2006),人二氢叶酸还原酶(Nallamsetty 2006),来自Ensis directus蛏子的精氨酸酶激酶(Compaan 2003),来自B. thuringiensis的修饰δ-内毒素(Kumar 2005),人BCMA跨膜受体(Guan 2006),植物α-双加氧酶1(Liu 2006),以及来自Plasmodium falciparum的b-ketoacyl-acyl载体蛋白合成酶(Lack 2006)等,反映了各种不同背景的蛋白都显示出了与NusA标签融合后的活性。NusA标签提高蛋白可溶性的可能机制 Houry(1999)等揭示NusA蛋白是分子伴侣GroEL在体内的必须底物。而GroEL与其共作用因子GroES是大肠杆菌唯一的在所有生长条件下必需的分子伴侣系统。Douette等(2005)研究了融合蛋白NusA-UCP1(uncoupling protein 1)的可溶产量。UCP1是一种线粒体膜蛋白。这些作者发现16℃培养时,当GroEL共过表达的情况下,融合蛋白的可溶性有更大的提高。这个结果也表明NusA与分子伴侣途径相作用,从而阻止参与蛋白的聚集。总结 已有充分的证据证明NusA标签系统能显著提高多种不同来源蛋白的可溶性表达,而这些蛋白在单独表达时往往形成不可溶的包涵体。在一些研究报告中,用蛋白酶切除NusA标签能使目的蛋白仍保持正确折叠和生物学活性;相反,在另外许多报道中也指出当目的蛋白与NusA融合而非切除时,融合蛋白也同样具有活性。NusA标签系统的成功至少部分地是由于其与大肠杆菌分子伴侣系统相互作用的结果。
[font=宋体][font=宋体]真核蛋白表达系统是一种广泛应用的蛋白表达方式,通常利用酵母、昆虫或哺乳动物细胞作为宿主。这种表达系统所生成的蛋白与目标[/font][font=Calibri]DNA[/font][font=宋体]具有极高的相似性,能诱导高效蛋白表达。那么,在实施真核蛋白表达时,有哪些关键的纯化步骤呢?接下来,我们将详细解析这一过程。[/font][/font][font=宋体] [/font][font=宋体]首先,我们要明确真核蛋白表达的纯化步骤是至关重要的环节。这些步骤不仅关系到最终产品的纯度和产量,还直接影响其生物活性和应用价值。因此,选择合适的纯化方法对于整个实验的成功至关重要。[/font][font=宋体] [/font][b][font=宋体]真核蛋白表达及纯化步骤主要有以下几个方面:[/font][/b][font=宋体] [/font][font=宋体][font=Calibri]1[/font][font=宋体]、重组质粒构建:将目的基因克隆进表达载体,常见的方法包括限制性切酶切割,基因合成等,根据连接酶说明,进行线性载体和目的基因片段的酶联,最后对质粒测序做好验证;[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2[/font][font=宋体]、蛋白诱导表达:普适条件下查看蛋白是否表达,若不表达,更换载体,表达菌株等方法查看是否表达,如果表达,继续实验;[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3[/font][font=宋体]、蛋白表达部位分析:分析蛋白是可溶性还是不溶性的表达,即在超声后上清表达还是沉淀表达;是否与你的目标蛋白表达部位相同,相同进行后续蛋白表达条件优化;[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4[/font][font=宋体]、蛋白表达优化:优化诱导[/font][font=Calibri]IPTG[/font][font=宋体]浓度、诱导温度,进行放大培养;[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]5[/font][font=宋体]、蛋白纯化:根据目标蛋白的性质进行样本处理,然后进行亲和纯化,获取目的蛋白。[/font][/font][font=宋体] [/font][font=宋体][b]真核表达系统的选择与应用[/b][/font][font=宋体]酵母蛋白表达系统[/font][font=宋体]酵母真核蛋白表达系统有甲醇酵母表达系统,酿酒酵母表达系统,裂殖酵母表达系统以及克鲁维酸酵母表达系统等,其中最早应用于基因工程的酵母是酿酒酵母,但现在运用最广泛的酵母表达系统还是甲醇酵母表达系统中的毕赤酵母真核蛋白表达系统。[/font][font=宋体] [/font][font=宋体]哺乳动物细胞表达系统[/font][font=宋体][font=宋体]哺乳动物细胞表达系统是真核表达系统中唯一可以表达复杂蛋白的系统,它能够指导真核表达蛋白进行正确折叠,提供复杂的[/font][font=Calibri]N[/font][font=宋体]型糖基化和准确的[/font][font=Calibri]O[/font][font=宋体]型糖基化等多种翻译后加工功能,所以它和昆虫酵母系统比较更具有发展潜力,哺乳动物细胞真核表达的蛋白与天然真核表达蛋白的结构、糖基化类型和方式几乎相同且能正确组装成多亚基蛋白[/font][font=Calibri],[/font][font=宋体]但成本较高也一定程度上减缓了它的发展速度。哺乳动物细胞表达系统主要是通过改造宿主细胞来提高外源蛋白的表达效率,常用的宿主细胞有[/font][font=Calibri]CHO[/font][font=宋体]、[/font][font=Calibri]COS[/font][font=宋体]、[/font][font=Calibri]BHK[/font][font=宋体]、[/font][font=Calibri]SP2 /0N[/font][font=宋体]等,哺乳动物转染方法[/font][font=Calibri]*[/font][font=宋体]有脂质体转染法,电穿孔法以及病毒转染等。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州[url=https://cn.sinobiological.com/resource/protein-review/protein-purification-techniques][b]蛋白纯化技术[/b][/url]:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/protein-purification-techniques[/font][/font][font=Calibri] [/font]
我现在急需鼠的转铁蛋白受体的抗体~!有的请回复。。谢谢
[font=宋体]什么是双特异性抗体?[/font][font=宋体][font=宋体]双特异性抗体([/font] [font=Calibri]bispecific antibody[/font][font=宋体],[/font][font=Calibri]BsAb[/font][font=宋体],简称双抗)是指能同时特异性结合两个抗原或抗原表位的人工抗体。形象比喻,它就像一座连接[/font][font=Calibri]2[/font][font=宋体]个抗原(表位)的桥梁。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]双特异性抗体在自然条件下并不存在,而是通过细胞融合或重组[/font][font=Calibri]DNA[/font][font=宋体]技术制备实现的。由于其特异性和双功能性,现已成为抗体工程领域的研究热点,在肿瘤治疗及自身免疫病等领域中具有广阔的应用前景。除此之外,双特异性抗体还被应用于治疗骨质疏松、血友病等其他领域。[/font][/font][font=宋体] [/font][font=宋体]双特异性抗体的作用机制:[/font][font=宋体]双特异性抗体在抗肿瘤治疗中的主要作用机制是:[/font][font=宋体][font=宋体]([/font][font=Calibri]1[/font][font=宋体])招募[/font][font=Calibri]T[/font][font=宋体]细胞或自然杀伤细胞,并将它们重定向至肿瘤细胞,增强其对肿瘤细胞的杀伤力;[/font][/font][font=宋体][font=宋体]([/font][font=Calibri]2[/font][font=宋体])同时阻断发病进程中两个不同的信号传导通路而发挥独特或重叠的功能,影响肿瘤细胞的生长增殖及存活;[/font][/font][font=宋体][font=宋体]([/font][font=Calibri]3[/font][font=宋体])同时靶向细胞表面不同的抗原或表位,增强其与肿瘤细胞的特异性结合并直接杀伤肿瘤细胞。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]双抗[/font][font=Calibri]VS[/font][font=宋体]单抗,有何优势?[/font][/font][font=宋体]与普通单克隆抗体相比,双特异性抗体具有同时结合两种特异性表位或目的蛋白的功能,因此可以发挥特殊的功能起到单抗药物难以达到的生物学功能。[/font][font=宋体] [/font][font=宋体]例如,将效应细胞直接靶向肿瘤细胞以增强其细胞毒性、提高抗体选择性和功能性、共刺激或抑制受体。相对单抗,双抗具备更强特异性、靶向性,可以降低脱靶毒性;相较单抗的组合疗法,也可有效降低治疗成本等。[/font][font=宋体] [/font][font=宋体]但双抗药物开发复杂性和技术壁垒更高,对于技术平台和靶点选择的适配性要求也有所提高。[/font][font=宋体] [/font][font=宋体]双特异性抗体的制备方法[/font][font=宋体][font=宋体]([/font][font=Calibri]1[/font][font=宋体])化学偶联法:该方法于[/font][font=Calibri]1985[/font][font=宋体]年首次被使用,其原理是通过化学偶联剂将两个完全的单抗或[/font][font=Calibri]Fab2[/font][font=宋体]片段偶联成一种双特异性抗体。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]2[/font][font=宋体])双杂交瘤融合法:将两种杂交瘤细胞通过细胞融合的方法,合成双杂交瘤细胞株,筛选出具有两种抗体功能的稳定靶细胞株。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]3[/font][font=宋体])基因工程法:利用基因工程技术对抗体进行改造,从而形成多种形式的双特异性抗体。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州在重组抗体生产方面具有扎实的专业知识和经验,利用优化的成熟哺乳动物细胞表达平台,为您提供快速高效的双特异性抗体表达服务。从抗体序列开始,我们可以表达多种双特异性抗体形式,如[/font][font=Calibri]BiTE[/font][font=宋体]、[/font][font=Calibri]Diabody[/font][font=宋体]、[/font][font=Calibri]CrossMab[/font][font=宋体]和[/font][font=Calibri]DVD-IgG[/font][font=宋体]。义翘神州服务优势:[/font][/font][font=宋体][font=宋体]①[/font][font=Calibri]20+[/font][font=宋体]种[/font][font=Calibri]BsAb[/font][font=宋体]生产经验[/font][/font][font=宋体] [/font][font=宋体][font=宋体]②成功率[/font][font=Calibri]90%[/font][/font][font=宋体] [/font][font=宋体][font=宋体]③自主优化的[/font][font=Calibri]HEK293/CHO[/font][font=宋体]平台[/font][/font][font=宋体] [/font][font=宋体]④多种纯化技术[/font][font=宋体] [/font][font=宋体]⑤强大的质控分析能力[/font][font=宋体] [/font][font=宋体][font=宋体]⑥最高产量[/font][font=Calibri]250 mg/L[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体][url=https://cn.sinobiological.com/services/bispecific-antibody-service][b]双特异性抗体生产服务[/b][/url]内容与抗体结构可以关注:[/font][font=Calibri]https://cn.sinobiological.com/services/bispecific-antibody-service[/font][/font]
[font=宋体][font=宋体]原核表达(这里是指[/font] [font=宋体]大肠杆菌表达系统[/font] [font=宋体])是目前常用的重组蛋白表达方式之一,操作相对简便,要求较低。相对哺乳动物表达系统更加经济节约。但是也常常遇到一些问题,比如原核表达蛋白表达量低?蛋白不表达?蛋白表达不在上清易形成包涵体等情况。本文主要根据实验经验总结[/font] [font=宋体]原核蛋白表达[/font] [font=宋体]的两个问题蛋白为什么不表达和蛋白表达为什么不在上清,并提出针对性的解决方案,帮助我们提高实验的成功率。原核表达[/font][font=Calibri]FAQ[/font][font=宋体]主要内容如下:[/font][/font][font=宋体] [/font][font=宋体]一、蛋白表达为什么不在上清?[/font][font=宋体] [/font][font=宋体][font=宋体]蛋白在大肠杆菌中的表达部位:细胞质中、细胞周质中、细胞外。[/font] [/font][font=宋体]蛋白在细胞周质中表达:细胞周质是指革兰氏阴性菌中、位于内膜和外膜之间的结构部分。周质中表达的蛋白质,分离纯化简单,而且周质中的氧化环境有利于蛋白质的正确折叠,但是蛋白产量很低。[/font][font=宋体]蛋白在胞外表达:胞外分泌是使大肠杆菌中的外源蛋白分泌到培养基中。[/font][font=宋体]途径:[/font][font=宋体]①用大肠杆菌细胞固有的途径,使真正属于分泌的蛋白直接分泌到胞外培养基中。大肠杆菌在正常情况下只有极少的蛋白可以分泌到胞外,且不是特别有效。[/font][font=宋体]②诱导大肠杆菌细胞的外膜发生有限的渗漏,从而使细胞内的蛋白向胞外培养基中分泌。[/font][font=宋体] [/font][font=宋体]二、蛋白的分泌表达优点[/font][font=宋体][font=Calibri]1[/font][font=宋体]、一些可被细胞内蛋白酶所降解的蛋白质分泌到周质或培养基中可增加其稳定性;[/font][/font][font=宋体][font=Calibri]2[/font][font=宋体]、有些在细胞内表达时无活性的蛋白分泌表达时能够按适当的方式进行准确折叠,增加到蛋白的活性;[/font][/font][font=宋体][font=Calibri]3[/font][font=宋体]、 由于蛋白质信号肽和编码序列间被切割,所以分泌蛋白产物不含氨基酸起始密码子[/font][font=Calibri]ATG[/font][font=宋体]所编码的甲硫氨酸,而甲硫氨酸会影响许多蛋白的活性。[/font][/font][font=宋体] [/font][font=宋体]三、如何提高蛋白的可溶性?[/font][font=宋体]重组蛋白在大肠杆菌中大量表达时,很容易在胞内形成不可溶的包涵体,为后期的纯化、复性带来麻烦,而且复性所得到的蛋白活性很低甚至没有活性。因此,提高重组蛋白在大肠杆菌中的可溶性表达是十分必要的。[/font][font=宋体] [/font][font=宋体]四、蛋白为什么不表达?[/font][font=宋体]真核基因在原核细胞中的的特点[/font][font=宋体]①使用原核启动子[/font][font=宋体][font=宋体]原核细胞[/font][font=Calibri]RNA[/font][font=宋体]聚合酶能识别真核基因启动子。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]②真核基因要置于原核载体[/font][font=Calibri]SD[/font][font=宋体]序列后[/font][/font][font=宋体][font=宋体]从真核[/font][font=Calibri]DNA[/font][font=宋体]转录的[/font][font=Calibri]mRNA[/font][font=宋体]缺乏结合原核核糖体的[/font][font=Calibri]SD[/font][font=宋体]序列,不能启动翻译过程。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]③使用[/font][font=Calibri]cDNA[/font][/font][font=宋体][font=宋体]真核基因中含有内含子,而原核细胞缺乏转录后加工体系,[/font][font=Calibri]mRNA[/font][font=宋体]中内含子不能切除,不能形成成熟的[/font][font=Calibri]mRNA[/font][font=宋体],也就不能表达真核蛋白。[/font][/font][font=宋体] [/font][font=宋体]④表达无需糖基化等修饰的蛋白[/font][font=宋体]原核细胞缺乏真核细胞所特有的蛋白翻译后的修饰系统,不利于表达需要糖基化、磷酸化修饰才有活性的真核蛋白。[/font][font=宋体] [/font][font=宋体]⑤真核基因必须切除信号肽序列[/font][font=宋体]蛋白具有信号肽序列的真核基因在真核细胞内先表达成蛋白前体,在其穿越细胞膜向外分泌时,会被细胞膜上信号肽识别序列切除而分泌到细胞外。但是在原核细胞内表达时,不但影响蛋白的表达,同时由于大肠杆菌缺乏加工处理体系,不能正确切除信号肽,而表达的分泌蛋白的前体没有实物活性,常聚集在胞内。[/font][font=宋体] [/font][font=宋体]五、影响原核表达的因素[/font][font=宋体][font=Calibri]1[/font][font=宋体]、翻译起始位点[/font][/font][font=宋体]现在大部分的表达载体都提供起始位点,所以它已经把起始密码子与核糖体结合位点的距离进行了优化,一般情况下不需要自己再添加,不过还是要留意载体图谱上是否注明有起始密码子和终止密码子。[/font][font=宋体] [/font][font=宋体][font=Calibri]2[/font][font=宋体]、[/font][font=Calibri]GC[/font][font=宋体]含量[/font][/font][font=宋体][font=宋体]表达序列中的[/font][font=Calibri]GC[/font][font=宋体]含量超过[/font][font=Calibri]70%[/font][font=宋体]的时候可能会降低蛋白在大肠杆菌中的表达水平。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3[/font][font=宋体]、[/font][font=Calibri]mRNA[/font][font=宋体]二级结构[/font][/font][font=宋体][font=宋体]在起始密码子附近的[/font][font=Calibri]mRNA[/font][font=宋体]二级结构可能会抑制翻译的起始或者造成翻译暂停从而产生不完全的蛋白。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4[/font][font=宋体]、密码子的偏爱性[/font][/font][font=宋体]如果外源基因密码子的使用频率和宿主菌高效表达的基因密码子的使用频率差异较大,翻译时核糖体在稀有密码子处就会产生停顿,这不仅降低蛋白质的合成效率,导致新生肽链的错误折叠而影响延伸,甚至会停止翻译。[/font][font=宋体] [/font][font=宋体][font=Calibri]5[/font][font=宋体]、质粒载体的选择[/font][/font][font=宋体]构建质粒载体时,要考虑质粒上的元件包括启动子,多克隆位点,终止密码子,融合标签,复制子,筛选标记基因等因素。[/font][font=宋体] [/font][font=宋体][font=Calibri]6[/font][font=宋体]、基因或者蛋白的大小[/font][/font][font=宋体][font=宋体]一般来说小于[/font][font=Calibri]10kd[/font][font=宋体]和大于[/font][font=Calibri]100kd[/font][font=宋体]的蛋白都是难以表达的。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]7[/font][font=宋体]、外源基因对宿主有毒性[/font][/font][font=宋体]外源基因在宿主内会抑制宿主菌的生长甚至导致宿主死亡,表观的现象:宿主菌在诱导后菌体量上升缓慢或不在生长。[/font][font=宋体] [/font][font=宋体][font=Calibri]8[/font][font=宋体]、基因突变(移筐突变)[/font][/font][font=宋体]碱基的突变、插入或缺失对阅读框的影响,可能会导致表达的蛋白质结构改变,或蛋白质合成过早终止。[/font][font=宋体] [/font][font=宋体][font=Calibri]9[/font][font=宋体]、培养诱导条件[/font][/font][font=宋体][font=宋体]培养基成分([/font][font=Calibri]C/N[/font][font=宋体])及培养条件(温度、诱导时机、诱导剂,浓度、诱导时间)也是影响蛋白表达的。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多关于[url=https://cn.sinobiological.com/resource/protein-review/protein-expression][b]蛋白表达[/b][/url]详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/protein-expression[/font][/font][font=Calibri] [/font]
在原核蛋白表达体系中,如E.coli(大肠埃希菌)系统,外源基因通常需要诱导剂的诱导才能进行表达,本文详细讲述了常用诱导剂IPTG 对外源蛋白诱导表达的原理以及实验步骤。
我的蛋白为RNases,表达在包涵体中,理论上有4对二硫键,8个游离巯基。我把包涵体溶在8M脲中,然后加入5mMDTT,还原过夜。然后用 AEMTS终浓度100mM烷化1h做MALDI-TOF。结果显示烷化上了6个游离巯基。请问是烷化条件不够还是DTT没有将包涵体的二硫键全部还原?还是蛋白本身构象问题使一个二硫键埋在内部,DTT作用不到?急,求救!
[font='calibri'][size=13px]抗体fc段和Fab段什么意思?抗体的功能有哪些?[/size][/font]抗体(antibody),是一种由浆细胞(效应B细胞)分泌,被免疫系统用来鉴别与中和外来物质如细菌、病毒等的大型Y形蛋白质,仅被发现存在于脊椎动物的血液等体液中,及其B细胞的细胞膜表面。抗体能识别特定外来物的一个独特特征,该外来目标被称为抗原。Fab段:抗原结合片段(fragment of antigen binding,Fab),相当于抗体分子的两个臂,由一个完整的轻链和重链的VH和CH1结构域组成。Fc段:可结晶段(fragment crystallizable,Fc)相当于Ig的CH2和CH3结构域,是Ig与效应分子或者细胞相互作用的部位。由以上信息可以看出:Fab段包含完整的可变区,以及恒定区的CH1区域。Fc段仅指Ig恒定区CH2和CH3的区域,相当于Y字结构下面那一部分。抗体的功能有哪些?(1)特异性结合抗原:抗体本身不能直接溶解或杀伤带有特异抗原的靶细胞,通常需要补体或吞噬细胞等共同发挥效应以清除病原微生物或导致病理损伤。然而,抗体可通过与病毒或毒素的特异性结合,直接发挥中和病毒的作用。(2)激活补体:IgM、IgG1、IgG2和IgG3可通过经典途径激活补体,凝聚的IgA、IgG4和IgE可通过替代途径激活补体。(3)结合细胞:不同类别的免疫球蛋白,可结合不同种的细胞,参与免疫应答。(4)可通过胎盘及粘膜:免疫球蛋白G(IgG)能通过胎盘进入胎儿血流中,使胎儿形成自然被动免疫。免疫球蛋白A(IgA)可通过消化道及呼吸道粘膜,是粘膜局部抗感染免疫的主要因素。(5)具有抗原性:抗体分子是一种蛋白质,也具有刺激机体产生免疫应答的性能。不同的免疫球蛋白分子,各具有不同的抗原性。(6)抗体对理化因子的抵抗力与一般球蛋白相同:不耐热,60~70℃即被破坏。各种酶及能使蛋白质凝固变性的物质,均能破坏抗体的作用。抗体可被中性盐类沉淀。在生产上常可用硫酸铵或硫酸钠从免疫血清中沉淀出含有抗体的球蛋白,再经透析法将其纯化。(7)通过与细胞Fc受体结合发挥多种生物效应。①调理作用 IgG、IgM的Fc段与吞噬细胞表面的FcγR、FcμR结合,增强其吞噬能力,通常将抗体促进吞噬细胞吞噬功能的作用称为抗体的调理作用 (opsonization)。②发挥抗体依赖的细胞介导的细胞毒作用。义翘神州在重组抗体表达方面具有丰富的经验,除了表达全长抗体外,还可以表达各种形式的抗体片段,如单链抗体 (scFv)、抗原结合片段(Fab)、纳米抗体 (VHH) 和抗体融合蛋白 (antibody-fusion proteins)等。基于优化的哺乳动物蛋白平台,义翘神州可在HEK293或CHO细胞中的表达和生产Fab抗体片段。 利用此技术生产的Fab片段较酶切全长抗体获得的Fab片段具有更好的质量。scFv可以在微生物系统如E. coli中表达, 也可以通过瞬转技术在哺乳动物细胞中表达。义翘神州具备在不同系统中表达不同抗体片段的能力,您可以根据实际需求进行选择。您只需将抗体片段的基因序列发送给我们,义翘神州负责完成从基因合成到最终纯化抗体片段的整个过程。更多抗体片段生产服务可以参看:https://cn.sinobiological.com/services/fab-scfv-antibody-production-service
[font=宋体]在生物医学领域,蛋白抗体已成为研究细胞生物学、疾病机制和药物开发的重要工具。然而,在选择和使用蛋白抗体时,许多科研人员可能会遇到一些常见问题。本文将详细解析这些问题,帮助大家更好地理解和使用蛋白抗体。[/font][font=宋体] [/font][font=宋体][b][font=Calibri]WB[/font][font=宋体]、[/font][font=Calibri]IHC[/font][font=宋体]、[/font][font=Calibri]ChIP...[/font][font=宋体]你的抗体选对了吗?[/font][/b][/font][font=宋体] [/font][font=宋体][font=Calibri]Q1. [/font][font=宋体]做流式的抗体和免疫组化的抗体是一样的吗?[/font][/font][font=宋体] [/font][font=宋体][font=宋体]不一定能通用。流式是用直接标记还是间接标记?如果是直接标记的话,那这个抗体一般不是[/font][font=Calibri]FITC[/font][font=宋体]标记或者就是[/font][font=Calibri]TRITC[/font][font=宋体],[/font][font=Calibri]PE[/font][font=宋体]之类的。如果恰好你的免疫组化,也是想用荧光素标记的抗体来直接标记,那就可以通用。如果你的免疫组化要用其它的标记的话,或者是间接标记的话,就有麻烦,因为荧光素的标记很可能会影响二抗和一抗的结合。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Q2. [/font][font=宋体]为什么我的抗体做[/font][font=Calibri]WB[/font][font=宋体]非常好,而做不了[/font][font=Calibri]IF[/font][font=宋体],[/font][font=Calibri]IHC[/font][font=宋体]等其他任何实验?[/font][/font][font=宋体] [/font][font=宋体][font=宋体]首先恭喜你有一个[/font][font=Calibri]WB[/font][font=宋体]非常好的抗体,毕竟能获得做[/font][font=Calibri]WB[/font][font=宋体]非常好的抗体也不容易。其次,你这个抗体很可能是通过人工合成多肽得到的,和上面所述,你用来做抗原的多肽恰好被包埋在蛋白质的中心,因此只能识别[/font][font=Calibri]WB[/font][font=宋体]中线性的部分。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Q3. [/font][font=宋体]如何选择免疫组化抗体?[/font][/font][font=宋体] [/font][font=宋体][font=宋体]首先,一抗是选择单克隆抗体还是多克隆抗体,单克隆抗体特异性强,灵敏度低;多克隆抗体灵敏度高,特异性弱。根据你的实验结果,如果非特异多,那么选择单克隆抗体;如果阳性信号弱,不妨选择多克隆抗体试试。一般家兔来源的都是多克隆,小鼠来源的是单克隆。其次是要弄明白该一抗能够识别什么种属的抗原,抗体说明书上面一般注明有,比如小鼠[/font][font=Calibri]Mus, [/font][font=宋体]大鼠[/font][font=Calibri]Rat, [/font][font=宋体]人[/font][font=Calibri]Hum[/font][font=宋体]。再次比较重要的是要注意一抗的来源。比如我们在人的癌组织中做[/font][font=Calibri]p53[/font][font=宋体]的免疫组化,一抗我们采用的是小鼠来源的[/font][font=Calibri]p53[/font][font=宋体]抗体,那么二抗我们一定要选择抗小鼠的二抗比如(山羊抗小鼠,兔抗小鼠),这一点非常重要。最后,一般的抗体说明书都会注明能做什么实验,如果标明了不可以做免疫组化,一定不要选择;反过来说,即使标明了可以做免疫组化,也不一定能够做,商家只会夸大其效果。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Q4. WB[/font][font=宋体]和[/font][font=Calibri]IF[/font][font=宋体]的二抗是一样的吗?[/font][/font][font=宋体] [/font][font=宋体][font=宋体]很明显,不是!免疫荧光抗体是用于[/font] [font=宋体]免疫荧光试验的,是用[/font][font=Calibri]FITC[/font][font=宋体]或[/font][font=Calibri]PE[/font][font=宋体]等标记的抗体,结果需要紫外线激发并用荧光显微镜观察[/font][font=Calibri]WB[/font][font=宋体]抗体一般是[/font][font=Calibri]HRP[/font][font=宋体]或碱性磷酸酶等标记的抗体,需显色底物(如[/font][font=Calibri]OPDTMB[/font][font=宋体]等)直接显色(肉眼)或化学发光法显影(需特殊仪器)。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Q5. [/font][font=宋体]做[/font][font=Calibri]CHIP[/font][font=宋体]的抗体是否可以用来做[/font][font=Calibri]WB[/font][font=宋体]抗体?[/font][/font][font=宋体] [/font][font=宋体][font=宋体]不一定,一般来说做[/font][font=Calibri]CHIP[/font][font=宋体]级别的抗体对抗体纯度特异性方面都要求比较高,基本上能做[/font][font=Calibri]CHIP[/font][font=宋体]的抗体都可以做[/font][font=Calibri]WB[/font][font=宋体]。但是如果[/font][font=Calibri]CHIP[/font][font=宋体]的抗体识别的是构象表位(比如是由两个实际靠在一起但变为线性结构之后相隔很远的两端序列),而不是线性表位,这种[/font][font=Calibri]CHIP[/font][font=宋体]抗体做不了[/font][font=Calibri]WB[/font][font=宋体]。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Q6. [/font][font=宋体]抗体说明书上面没有写该抗体能够用于某项实验怎么办?[/font][/font][font=宋体] [/font][font=宋体][font=宋体]一般而言,抗体研发出来之后都要经过[/font][font=Calibri]WB[/font][font=宋体],[/font][font=Calibri]IP[/font][font=宋体],[/font][font=Calibri]IF[/font][font=宋体],[/font][font=Calibri]IHC[/font][font=宋体]实验。档发现浓度不够做[/font][font=Calibri]IF[/font][font=宋体],[/font][font=Calibri]IHC[/font][font=宋体]时候,国外的抗体一般都是写未检测,国内的抗体一般是不写。所以尽量不要抱着试试的心里去尝试,往往只会浪费时间。你想啊,如果抗体能够做该实验,他们肯定会写上去啊。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Q7. [/font][font=宋体]做[/font][font=Calibri]ELISA[/font][font=宋体]的抗体能否用来做[/font][font=Calibri]WB[/font][font=宋体]?[/font][/font][font=宋体] [/font][font=宋体][font=宋体]通常用[/font][font=Calibri]WB[/font][font=宋体]抗体稀释浓度为[/font][font=Calibri]1:1000[/font][font=宋体],[/font][font=Calibri]IF/IHC[/font][font=宋体]为[/font][font=Calibri]1:100[/font][font=宋体],而如果可以做[/font][font=Calibri]ELISA[/font][font=宋体]则可以稀释[/font][font=Calibri]1:10000[/font][font=宋体]。如果一个抗体用来做[/font][font=Calibri]ELISA[/font][font=宋体]的,那么言外之意就是该抗体效价不高。但不是说[/font][font=Calibri]ELISA[/font][font=宋体]的抗体不能用于做[/font][font=Calibri]WB[/font][font=宋体],抗体说明书提示做[/font][font=Calibri]ELISA[/font][font=宋体]稀释比例为[/font][font=Calibri]1:1000[/font][font=宋体],那么你可以试试[/font][font=Calibri]1:100[/font][font=宋体]做做[/font][font=Calibri]WB[/font][font=宋体]。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多详情可以关注义翘神州[url=https://cn.sinobiological.com/resource/antibody-technical/antibody-purification][b]抗体纯化[/b][/url]:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/antibody-purification[/font][/font]