(港、澳、台)化学药品医药产品注册 2006年02月20日 发布 一、项目名称:(港、澳、台)医药产品注册 二、许可内容: (港、澳、台)化学药品医药产品注册,其分类按《药品注册管理办法》附件二注册分类,即: 注册分类1、未在国内外上市销售的药品: 注册分类3、已在国外上市销售但尚未在国内上市销售的药品: 三、设定和实施许可的法律依据: 《中华人民共和国药品管理法》第三十九条、《中华人民共和国药品管理法实施条例》第二十九条、《药品注册管理办法》 四、收费: 进口药审评及审批收费45300元。 完成临床以后的注册申请,因申请进口临床试验时已收费,故不收费。 收费依据:《国家计委、财政部关于调整药品审批、检验收费标准的通知》[计价格(1995)340号]。 五、数量限制:本许可事项无数量限制 六、申请人提交材料目录: 《进口药品注册申请表》 (一)综述资料: 资料编号1、药品名称; 资料编号2、证明性文件; 资料编号3、立题目的与依据; 资料编号4、对主要研究结果的总结及评价; 资料编号5、药品说明书、起草说明及相关参考文献; 资料编号6、包装、标签设计样稿。 (二)药学研究资料: 资料编号7、药学研究资料综述; 资料编号8、原料药生产工艺的研究资料及文献资料;制剂处方及工艺的研究资料及文献资料; 资料编号9、确证化学结构或者组份的试验资料及文献资料; 资料编号10、质量研究工作的试验资料及文献资料; 资料编号11、药品标准及起草说明,并提供标准品或者对照品; 资料编号12、样品的检验报告书; 资料编号13、原料药、辅料的来源及质量标准、检验报告书; 资料编号14、药物稳定性研究的试验资料及文献资料; 资料编号15、直接接触药品的包装材料和容器的选择依据及质量标准 。 (三)药理毒理研究资料: 资料编号16、药理毒理研究资料综述; 资料编号17、主要药效学试验资料及文献资料; 资料编号18、一般药理学的试验资料及文献资料; 资料编号19、急性毒性试验资料及文献资料; 资料编号20、长期毒性试验资料及文献资料; 资料编号21、过敏性(局部、全身和光敏毒性)、溶血性和局部(血管、 皮肤、粘膜、肌肉等)刺激性等特殊安全性试验资料和文献资料; 资料编号22、复方制剂中多种成份药效、毒性、药代动力学相互影响的试验资料及文献资料; 资料编号23、致突变试验资料及文献资料; 资料编号24、生殖毒性试验资料及文献资料; 资料编号25、致癌试验资料及文献资料; 资料编号26、依赖性试验资料及文献资料; 资料编号27、非临床药代动力学试验资料及文献资料。 (四)临床试验资料: 资料编号28、国内外相关的临床试验资料综述; 资料编号29、临床试验计划及研究方案; 资料编号30、临床研究者手册; 资料编号31、知情同意书样稿、伦理委员会批准件; 资料编号32、临床试验报告。 以上申报材料具体要求详见《药品注册管理办法》附件二。 七、对申请资料的要求: (一)申报资料的一般要求: 1、申报资料首页为申报资料项目目录,目录中申请资料项目按《药品注册管理办法》(国家食品药品监督管理局令第17号)附件二的顺序排列。每项资料封面上注明:药品名称、资料项目编号、项目名称、申请机构联系人姓名、电话、地址。 2、申报资料应使用A4规格纸打印或复印,内容完整、规范、清楚,不得涂改,数据真实、可靠。 3、资料按套装入档案袋,档案袋封面注明:申请分类、注册分类、药品名称、本袋所属第X套第X袋每套共X袋、原件/复印件 联系人、联系电话、申请注册代理机构名称。 4、注册申请报送2套完整申请资料(至少1套为原件)和1套综述资料复印件,申请表4份(2份原件,2份复印件)分别装入各套资料中(全套原件资料内放入1份申请表原件,1份申请表复印件)。 5、《进口药品注册申请表》:从国家食品药品监督管理局网站(www.sfda.gov.cn)下载,按要求填写后打印并保存,要有境外申请人的盖章或签字及国内代理机构盖章签字。 6、申请人对下述药品注册申报资料应当同时提交电子文本:资料编号:1、3~7、16和28;以上项目资料中的证明性文件、图形图像或者文献资料的复印件,可暂不要求提供电子文本。 7、在邮寄或者递交申请资料前应将申请表的电子版发送到以下药品注册专用电子邮箱地址:ypzcsl@sda.gov.cn和ypzcsl@nicpbp.org.cn 和ypzcsl@vip.sina.com和ypzcsl@vip.163.com。 8、待确定我局已经收到电子资料后,向我局提交或邮寄申报资料的纸质资料。 9、电子版资料与纸质资料应相同,申请表的核对码应一致。 10、外文资料应翻译成中文。 (二)申报资料的具体要求: 1、《进口药品注册申请表》的填写应准确、规范,符合填表说明的要求。 (1)药品注册分类:参照《药品注册管理办法》(国家食品药品监督管理局令第17号)附件的相应条款填写。申请未在国内外获准上市销售的药品,按照注册分类1类的规定报送资料;其他品种按照注册分类3类的规定报送资料.属于注册分类1类的药物,应当至少是已在国外进入II期临床试验的药物. (2)附加申请事项:可同时提出非处方药等附加申请。 (3)规格:申请注册的药品有多个规格的,应当根据提交资料是否独立成套确定规格项填写一个或多个规格;各规格独立成套的,一表一规格,各自发给受理号;各规格资料共用一套,一表填入多个规格,只发给一个受理号。
进口药品注册标准号字母JX、JF有什么意义和区别吗?
药品质量标准论坛网 http://standard.joinbbs.net/附件为注射用尼麦角林进口注册标准
国家食品药品监督管理总局日前发布《关于调整药品注册受理工作的公告》(2017年第134 号)称,凡依据现行法律、法规和规章,由国家食品药品监督管理总局审评审批、备案的注 册申请均由国家食品药品监督管理总局受理,包括新药临床试验申请、新药生产(含新药证 书)申请、仿制药申请,国家食品药品监督管理总局审批的补充申请等;由省级食品药品监 督管理部门审批、备案的药品注册申请仍由省级食品药品监督管理部门受理。
国家食品药品监督管理总局日前发布《关于调整药品注册受理工作的公告》(2017年第134 号)称,凡依据现行法律、法规和规章,由国家食品药品监督管理总局审评审批、备案的注 册申请均由国家食品药品监督管理总局受理,包括新药临床试验申请、新药生产(含新药证 书)申请、仿制药申请,国家食品药品监督管理总局审批的补充申请等;由省级食品药品监 督管理部门审批、备案的药品注册申请仍由省级食品药品监督管理部门受理。
食品药品监管总局组织制定了化学药品注册分类改革工作方案(以下简称方案),已于2016年3月4日正式发布实施。现就有关问题解读如下:[b]一、方案的出台背景。[/b] 2015年8月9日,国务院发布《关于改革药品医疗器械审评审批制度的意见》,明确调整药品注册分类。2015年11月4日,第十二届全国人民代表大会常务委员会第十七次会议审议通过《关于授权国务院在部分地方开展药品上市许可持有人制度试点和有关问题的决定》,同意国务院组织开展药品注册分类改革。为落实上述政策要求,满足实际工作需要,食品药品监管总局制定发布了本方案。[b]二、方案的适用范围。[/b] 本方案仅针对化学药品注册分类进行了调整,适用于方案发布实施后新受理的化学药品注册申请(包括临床、生产、进口注册申请)。[b]三、新注册分类中,关于新药的含义是什么?[/b] 新药指中国境内外均未上市的药品,分为创新药和改良型新药。 新注册分类1为创新药,强调含有新的结构明确的、具有药理作用的化合物;新注册分类2为改良型新药,在已知活性成份基础上进行优化,强调具有明显的临床优势。[b]四、创新药具体包括什么?[/b] 创新药指含有新的结构明确、具有药理作用的化合物,且具有临床价值的药品,不包括改良型新药中2.1类的药品。[b]五、新注册分类中,关于仿制药的含义是什么?[/b] 仿制药是指仿制已上市原研药品的药品,分为两类,一是仿制境外已上市境内未上市原研药品,二是仿制境内已上市原研药品。仿制药要求与原研药品质量和疗效一致。 如果已上市药品的原研药品无法追溯或者原研药品已经撤市的,建议不再申请仿制;如坚持提出仿制药申请,原则上不能以仿制药的技术要求予以批准,应按照新药的要求开展相关研究。[b]六、新注册分类中,关于第5类药品的含义是什么?[/b] 第5类药品是指境外上市的药品申请在中国境内上市,分为原研药品和非原研药品两类。对应原化学药品注册分类中的进口药品类别。[b]七、含有未知活性成份的新复方制剂按什么申报?[/b] 含有新的结构明确的、具有药理作用的化合物的新复方制剂,应按照新注册分类1进行申报。[b]八、仿制药是否要求处方工艺、规格、用法用量等均与原研保持一致?[/b] 仿制药要求与原研药品具有相同的活性成分、剂型、规格、适应症、给药途径和用法用量,不强调处方工艺与原研药品一致,但强调仿制药品必须与原研药品质量和疗效一致。[b]九、新注册分类下的技术标准有何变化?[/b] 对按新注册分类申报的化学药品注册申请实行新的审评技术标准。其中,对于创新药,一是强调“创新性”,即应当具备“全球新”的物质结构,二是强调药物具有临床价值;对于改良型新药,强调“优效性”,即相较于被改良的药品,具备明显的临床优势;对于仿制药,强调“一致性”,被仿制药品为原研药品,且质量与疗效应当于原研药品一致。[b]十、新注册分类的监测期设置是如何考虑的?[/b] 《中华人民共和国药品管理法实施条例》第三十四条规定,国务院药品监督管理部门根据保护公众健康的要求,可以对药品生产企业生产的新药品种设立不超过5年的监测期。新注册分类中的第1类、第2类属于新药范畴,因此设置监测期。同时,参照《药品注册管理办法》中原化学药品注册分类的监测期期限设置,对于新注册分类中与原注册分类相类似或者相近的情形分别设置了相应的监测期限。[b]十一、已经受理的原注册申请在新注册分类实施后如何过渡?[/b] 方案发布实施后新申报的化学药品注册申请(包括临床、生产、进口申请),其注册分类按照新注册分类有关要求执行。 方案发布实施前已受理尚未完成审评审批的化学药品第3类及6类报生产注册申请,申请人可以选择继续按照原规定进行审评审批,符合要求的,在批准时,注册分类项注明相应的原注册分类;申请人也可以申请按照新注册分类进行后续申报、审评审批。 对于申请按照新注册分类进行审评审批的注册申请,由食品药品监管总局药审中心优先按照新注册分类的要求加快审评审批;经审查不符合要求的,不再要求补充资料,直接不予批准。[b]十二、方案中“补交相关费用”具体如何执行?[/b] 方案“二、相关注册要求”中第(四)部分提及的“补交相关费用”是指,2015年5月27日前已经受理的化学药品注册申请,申请按照新注册分类进行审评审批的,应当按照《关于发布药品、医疗器械产品注册收费标准的公告》(2015年第53号)公布的《药品、医疗器械产品注册收费标准》补交相关注册收费;2015年5月27日以后受理的、已按照上述标准交费的化学药品注册申请,申请按照新注册分类进行审评审批的,无须补交费用。[b]十三、新注册分类实施后,后续有何细化工作要求?[/b] 新注册分类实施后,食品药品监管总局将组织相关部门尽快提出《新注册分类申报资料项目及要求》、《新注册分类受理审查指南》、《新注册分类核查检查要点》、《新注册分类技术审评指导原则》等在内的一系列相关细化工作要求,以便指导申请人合理研发申报相关产品,进一步提高药品质量。
全方位解读《药品注册管理办法》发布日期:2008-05-15 一、新《药品注册管理办法》的修改重点 28号局令针对原有章节的框架作了部分调整,对临床前研究、临床试验等在其它规章中已有规定的内容,本次修订予以简化;对药品标准、新药技术转让等将制定其它具体办法进行规定的,28号局令不再重复规定。 28号局令由原来的16章211条变为现在的15章177条,重点修订的内容主要在3个方面(见后)。 二、新《药品注册管理办法》(下简称《办法》)关于部分名词术语的定义 新《办法》关于部分名词术语的定义 第三条 药品注册,是指国家食品药品监督管理局根据药品注册申请人的申请,依照法定程序,对拟上市销售药品的安全性、有效性、质量可控性等进行审查,并决定是否同意其申请的审批过程。 第十条 药品注册申请人(以下简称申请人),是指提出药品注册申请并承担相应法律责任的机构。 第十二条 新药申请,是指未曾在中国境内上市销售的药品的注册申请。 对已上市药品改变剂型、改变给药途径、增加新适应症的药品注册按照新药申请的程序申报。 仿制药申请,是指生产国家食品药品监督管理局已批准上市的已有国家标准的药品的注册申请;但是生物制品按照新药申请的程序申报。 进口药品申请,是指境外生产的药品在中国境内上市销售的注册申请。 补充申请,是指新药申请、仿制药申请或者进口药品申请经批准后,改变、增加或者取消原批准事项或者内容的注册申请。 再注册申请,是指药品批准证明文件有效期满后申请人拟继续生产或者进口该药品的注册申请。 第三十一条 申请新药注册,应当进行临床试验。仿制药申请和补充申请,根据本办法附件规定进行临床试验。 临床试验分为I、II、III、IV期。 I期临床试验:初步的临床药理学及人体安全性评价试验。观察人体对于新药的耐受程度和药代动力学,为制定给药方案提供依据。 II期临床试验:治疗作用初步评价阶段。其目的是初步评价药物对目标适应症患者的治疗作用和安全性,也包括为III期临床试验研究设计和给药剂量方案的确定提供依据。此阶段的研究设计可以根据具体的研究目的,采用多种形式,包括随机盲法对照临床试验。 III期临床试验:治疗作用确证阶段。其目的是进一步验证药物对目标适应症患者的治疗作用和安全性,评价利益与风险关系,最终为药物注册申请的审查提供充分的依据。试验一般应为具有足够样本量的随机盲法对照试验。 IV期临床试验:新药上市后应用研究阶段。其目的是考察在广泛使用条件下的药物的疗效和不良反应,评价在普通或者特殊人群中使用的利益与风险关系以及改进给药剂量等。 生物等效性试验,是指用生物利用度研究的方法,以药代动力学参数为指标,比较同一种药物的相同或者不同剂型的制剂,在相同的试验条件下,其活性成份吸收程度和速度有无统计学差异的人体试验。 三、药品注册管理办法中关于不予再注册的规定 第一百二十六条 有下列情形之一的药品不予再注册: (一)有效期届满前未提出再注册申请的; (二)未达到国家食品药品监督管理局批准上市时提出的有关要求的; (三)未按照要求完成IV期临床试验的; (四)未按照规定进行药品不良反应监测的; (五)经国家食品药品监督管理局再评价属于疗效不确、不良反应大或者其他原因危害人体健康的; (六)按照《药品管理法》的规定应当撤销药品批准证明文件的; (七)不具备《药品管理法》规定的生产条件的; (八)未按规定履行监测期责任的; (九)其他不符合有关规定的情形。 四、新《办法》中关于临床试验的规定 总则 第二条 在中华人民共和国境内申请药物临床试验、药品生产和药品进口,以及进行药品审批、注册检验和监督管理,适用本办法。 第五条 国家食品药品监督管理局主管全国药品注册工作,负责对药物临床试验、药品生产和进口进行审批 基本要求 第十六条 药品注册过程中,药品监督管理部门应当对非临床研究、临床试验进行现场核查、有因核查,以及批准上市前的生产现场检查,以确认申报资料的真实性、准确性和完整性。 第二十条 按照《药品管理法实施条例》第三十五条的规定,对获得生产或者销售含有新型化学成份药品许可的生产者或者销售者提交的自行取得且未披露的试验数据和其他数据,国家食品药品监督管理局自批准该许可之日起6年内,对未经已获得许可的申请人同意,使用其未披露数据的申请不予批准;但是申请人提交自行取得数据的除外。 第二十六条 药品注册申报资料中有境外药物研究机构提供的药物试验研究资料的,必须附有境外药物研究机构出具的其所提供资料的项目、页码的情况说明和证明该机构已在境外合法登记的经公证的证明文件。国家食品药品监督管理局根据审查需要组织进行现场核查。 第二十七条 药品监督管理部门可以要求申请人或者承担试验的药物研究机构按照其申报资料的项目、方法和数据进行重复试验,也可以委托药品检验所或者其他药物研究机构进行重复试验或方法学验证。 五、新《办法》中关于特殊审批的规定 第四条 国家鼓励研究创制新药,对创制的新药、治疗疑难危重疾病的新药实行特殊审批。 第四十五条 国家食品药品监督管理局对下列申请可以实行特殊审批: (一)未在国内上市销售的从植物、动物、矿物等物质中提取的有效成份及其制剂,新发现的药材及其制剂; (二)未在国内外获准上市的化学原料药及其制剂、生物制品; (三)治疗艾滋病、恶性肿瘤、罕见病等疾病且具有明显临床治疗优势的新药; (四)治疗尚无有效治疗手段的疾病的新药。 符合前款规定的药品,申请人在药品注册过程中可以提出特殊审批的申请,由国家食品药品监督管理局药品审评中心组织专家会议讨论确定是否实行特殊审批。 特殊审批的具体办法另行制定。 第四十九条 药品注册申报资料应当一次性提交,药品注册申请受理后不得自行补充新的技术资料;进入特殊审批程序的注册申请或者涉及药品安全性的新发现,以及按要求补充资料的除外。申请人认为必须补充新的技术资料的,应当撤回其药品注册申请。申请人重新申报的,应当符合本办法有关规定且尚无同品种进入新药监测期。 第一百三十一条 获准进入特殊审批程序的药品,药品检验所应当优先安排样品检验和药品标准复核。 六、新《药品注册管理办法》中关于药品标准和药品标准物质的规定 药品注册标准 第一百三十六条 国家药品标准,是指国家食品药品监督管理局颁布的《中华人民共和国药典》、药品注册标准和其他药品标准,其内容包括质量指标、检验方法以及生产工艺等技术要求。 药品注册标准,是指国家食品药品监督管理局批准给申请人特定药品的标准,生产该药品的药品生产企业必须执行该注册标准。 药品注册标准不得低于中国药典的规定。 第一百三十七条 药品注册标准的项目及其检验方法的设定,应当符合中国药典的基本要求、国家食品药品监督管理局发布的技术指导原则及国家药品标准编写原则。 第一百三十八条 申请人应当选取有代表性的样品进行标准的研究工作。 药品标准物质 第一百三十九条 药品标准物质,是指供药品标准中物理和化学测试及生物方法试验用,具有确定特性量值,用于校准设备、评价测量方法或者给供试药品赋值的物质,包括标准品、对照品、对照药材、参考品。 第一百四十条 中国药品生物制品检定所负责标定国家药品标准物质。 中国药品生物制品检定所可以组织有关的省、自治区、直辖市药品检验所、药品研究机构或者药品生产企业协作标定国家药品标准物质。 第一百四十一条 中国药品生物制品检定所负责对标定的标准物质从原材料选择、制备方法、标定方法、标定结果、定值准确性、量值溯源、稳定性及分装与包装条件等资料进行全面技术审核,并作出可否作为国家药品标准物质的结论。
[table=100%][tr][td][b]一、国内上市销售的制剂增加已在国外批准的新适应症按什么申报?[/b] “国内上市销售的制剂增加已在国外批准的新适应症”相关申请事项,可按照现行《药品注册管理办法》附件4中国家局审批的补充申请事项第3项进行申报。 [b]二、国内上市销售的制剂增加国内外均未批准的新适应症按什么申报?[/b] 按照新注册分类2.4进行申报。 [b]三、化学药品新注册分类2.4类中已知活性成份的含义?[/b] 已知活性成份指“已上市药品的活性成份”,包含境内境外已上市。 [b]四、新注册分类3、4类,如何提出注册申请?[/b] 按照申报生产形式提出注册申请。 [b] 五、关于进口化学药品新注册分类5类如何收费?[/b] (一)新注册分类 5类药品的注册费按照进口无需临床试验的生产/上市、进口需临床试验的生产/上市注册费标准收费。申请临床试验的注册费为36.76 万元,完成临床试验后申请生产/上市的需要补交差额13.44万元;申请无需临床试验的生产/上市注册费为36.76 万元,经技术审评需要临床试验的需要补交差额13.44万元;申请需临床试验的生产/上市注册费为50.20 万元。 (二)新注册分类5类药品的临床试验申请经批准予以减免临床试验的,申报生产/上市时需补交6.72万元。[/td][/tr][tr][td] [/td][/tr][/table]
日前,国家食品药品监督管理局正式发布[url=http://www.sda.gov.cn/09ypzcnb/09ypzcnb.rar][color=#800080]《2009年药品注册审批年度报告》。[/color][/url]报告由2009年药品注册管理工作情况、2009年批准药品生产上市情况、2009年批准药品临床研究情况、2009年重要治疗领域的药品批准情况、2009年药品注册申请受理情况和结语6部分组成。报告共7000余字,图文并茂地展示了2009年药品注册工作的进展与成效。 报告从完善药品注册法规体系、加强药品研究过程的监管、加大技术审评科学公开透明、完成应急防控药品审批四个角度,阐述了2009年药品注册工作的重要举措。 报告显示,2009年的药品注册申请受理总量为6428件,其中,境内申请5128件,包括2336件新申请和2792件补充申请;境外申请1300件,包括新申请614件和补充申请686件。药品注册申请全年受理总量已连续3年稳定在6000至7000件左右。 报告显示,2009年国家局共批准生产上市药品申请3100件(以受理号计,下同),其中含2008年集中审评后续批准的过渡期品种2308件。按照新的《药品注册管理办法》规定,审评并批准了新药、改剂型、仿制药及进口药品注册申请共计792件。其中,化药548件,中药92件,生物制品38件。 2009年化药新药占化药批准品种总数的比例为32%,中药新药占中药批准品种总数的比例为78%。2009年首次出现了批准新药比率升高、重复申请降低的现象。这表明2007年新版《药品注册管理办法》颁布以后,我国采取的一系列规范审评、鼓励创新的政策导向产生了良好效应。 通过开展药品注册现场核查、药品批准文号清查、过渡期品种集中审评、实施新修订的《药品注册管理办法》及其配套法规文件等措施,经过连续几年的努力,药品审评审批改革已经取得显著成效,药品注册管理不断规范,药品研制秩序持续好转,药品注册申请数量趋于理性,质量进一步提高,有效保障了人民群众用药安全有效。 从今年起,国家食品药品监督管理局将逐步建立和完善药品注册审批年度报告制度,积极推进药品注册审批信息公开和工作透明,为鼓励新药创制,促进医药产业结构调整和产品结构优化提供有效指导。[table=100%,#d7eaf9][tr][td]附件1:[/td][td][url=http://www.cde.org.cn/attachmentout.do?mothed=list&id=3500]2009年药品注册审批年度报告.rar[/url][/td][/tr][/table]
一、新加坡现行药品管理体制主要有如下五个法规: 药品法-Chapter 176 药品法(广告与销售)--Chapter 药品滥用误用规程(主要法规—药品滥用法) 有毒药品法—Chapter 234 药品销售法—Chapter 282 新加坡的药品注册主要是在药品法在大框架下实施,药品注册的要求为安全、有效、质量可控。注册权是由新加坡卫生科学局的药品审评中心负责药品的审评工作。 二、新加坡的药品注册分为如下四种: NDA:创新药。 GDA:普通制剂,与在新加坡已注册的药品类似。 已有药品批准件的变化申请(相当于中国的补充申请) MAV:已有药品批准件的重大改变; MIV:已有药品批准件的微小改变 三、新药申请提交文件类型 3.1 完整文档 如果要申报的药品在新加坡注册之前,没有全球任何一家药品管理机构批准,含有新药学/生物实体,或化学/生物实体的组成的新复合制剂, 或是已注册药品的的新用途。完整的化学/生物或药学/遗传研究数据,毒理学和药理学数据及临床文献也需提交(参考申请列表) 审评时间为210个工作日和60天行政决议,不包括停止时间表。 3.2 精简文档 此部分是为已通过根据世界卫生组织定义的有能力的药品管理机构的批准的进口药品。 原产国的药品管理机构颁发的药品证明书(CPP)(见Part C, Section 3, 1.8&1.9条款的解释) 药品说明书(PI)/由发布CPP的管理机构批准的药品特点总结; 药品说明书(PI)/HAS药品注册基准规则机构批准的药品特点总结; 如果药品还未被原产国批准,HAS要求提供药品状态的声明。对于想在新加坡销售的进口药品,所销售的药品的成分、生产地和用途必须与药品管理机构批准颁发的CPP上所批准的项目一样。 ,除了上述段落中所提到的文档外,要求提供的文档还包括: 完整的质量文档; 非临床研究综述; 临床综述、总结和选择性研究报告(请见申请列表)。 审评时间为210个工作日和60天行政决议,不包括停止时间表。 注:只要临床实验按照GCP的要求开展的,新加坡就可接受别国的临床实验,不需在新加坡开展临床实验。 3.3 验证文档 如果药品已被下列中至少两个以上药品管理机构批准,那么此药的申请则只需提交验证性文档。 澳大利亚TGA; 加拿大卫生局; 欧洲医药局(EMEA); 英国医药卫生制品管理局(MHRA); 美国食品药品管理局 四、 数据要求 支持申请所需的数据可分为:管理信息、质量、安全和有效性数据。HAS接受根据东盟(ASEAN)通用技术文档格式(ACTD)或ICH格式(ICH CTD)组织的文档。 建议申请者阅读相关ASEAN解释条例或ICH指导原则和本指导原则中的PART C中的列表,以便获取每种申请和文档的全部信息。 为推动审评流程,申请都应遵照指导原则的要求。如果没有不能充分做到,请为HAS考虑提供说明偏差的理由。如果需要对药品的质量、安全和有效需做进一步的评价,HAS也样要求提供额外的信息或
SFDA发布内容:一、严格准入门槛,申报走势出现拐点 自2007年10月1日新修订的《药品注册管理办法》实施以来,我们围绕法规建设、审评审批、现场核查、注册检验、风险管理等方面加强药品注册全过程的监管,经过近两年的努力,工作取得一定成效,药品注册出现了可喜变化:申报数量大幅减少,申报质量不断提高,申报机构更加趋于理性,药品研发呈现新的局面。 [color=#DC143C]从2007年10月1日至2009年6月底,国家食品药品监督管理局共受理药品注册申请4403件,年申报数量减少2/3。其中,创新药84个、仿制药1682个。[/color] [color=#00008B]此外,新《药品注册管理办法》实施至今,同品种申报的比率也从2006年的1:6下降为今年的1:3,中药已经几乎没有重复申报现象。[/color] 从批准情况看,2009年1-6月国家食品药品监督管理局批准新药临床申请173件;新药生产申请238件,其中一类新药8件;仿制药申请1074件;进口药申请388件。 综上可见,药品注册申报总量减少,重复申报减少,质量明显提高,结构发生改变,这充分说明药品注册逐渐回归正常,药品研发日益符合国情,新的《药品注册管理办法》的实施导向正确,达到了预期目标。 二、集中技术力量,清理历史遗留问题 近年来,国家食品药品监督管理局不断深化审评审批制度改革,形成了完备的法律法规及部门规章构成的制度体系,设置了合理的审评程序,建立了权威的专家技术资源,实现了依法科学审评审批,彻底扭转药品审评审批工作的被动局面,从源头上提升了药品安全的保障水平。 为解决药品注册管理工作存在的突出问题,国家食品药品监督管理局按照国务院的部署积极稳妥地开展了药品研制环节的专项整治工作。[color=#DC143C]通过对3.3万个药品开展注册现场核查撤回了7999个药品注册申请;通过开展药品批准文号清查注销了4337个批准文号;通过开展过渡期品种集中审评处理了2.5万积压品种,其中不批准1.5万个品种(大多为化学药5/6类、中药8/9类),不批准率达61%,[/color]这些卓有成效的工作,较大程度上规范了药品注册秩序,净化了药品研发环境,卸下了历史包袱,也为新《药品注册管理办法》的实施扫清了障碍,奠定了基础。 三、采取多项政策措施,鼓励药品研发创新 为规范药品技术转让注册行为,保证药品安全、有效和质量可控,根据《药品注册管理办法》的有关规定,[U]近日,国家食品药品监督管理局发布实施了《药品技术转让注册册管理规定》。它是继《中药注册管理补充规定》、《药品注册现场核查管理规定》、《新药注册特殊审批管理规定》之后发布的第四个配套文件,自此,以《药品注册管理办法》为核心的我国药品注册管理法规体系初步形成,[/U]我国药品注册进入了一个鼓励创新、引导创新的时代。 鼓励创新、引导创新,这在多个法规文件中都有体现并且相互配合形成合力,首先,新修订的《药品注册管理办法》严格了新药证书的发放范围,进一步提高了新药证书的含金量。其次,在《新药注册特殊审批管理规定》中通过采取早期介入、优先审评、多渠道交流沟通、动态补充资料等措施鼓励、支持创新药物研发。第三,《药品注册现场核查管理规定》规定了严格的注册现场核查和检查要求,保证了申报资料的真实性,维护了注册审批的公正性和严肃性,使各项鼓励创新政策能够真正落到实处。第四,在《中药注册管理补充规定》中为鼓励中药新药在新功能主治领域的研发,还对“治疗尚无有效治疗手段的疾病的新药”增加内涵,将“主治病证未在国家批准的中成药【功能主治】中收载的新药”,纳入特殊审批的范围,充分发挥中药在疑难杂症和新出现疾病方面的治疗作用。并采取具体措施拓宽中药复方制剂的组方内涵,鼓励中药创新和发展。 《药品技术转让注册管理规定》出台后,对进一步鼓励创新,促进资源合理配置发挥重要作用。 一是有效控制批准文号数量。[U]技术转让批准后,原来已经取得的批准文号同时注销,避免了一家转多家,[/U]引导药品生产企业减少简单改变剂型和仿制药品的申报数量,从根本上解决低水平重复问题。 二是促进专业化程度提高。药品技术转让新政策的确立,有利于企业间或者企业内部改变产品结构,合理分配和调整生产资源,实现优势产品重组和重点发展,减少低水平重复和同质化。随着产品生产的专业化程度的提高,围绕产品专业化生产和监管水平将会得到促进,推进以产品为核心的CGMP实施,进一步保证产品质量。 三是利用技术手段,提高技术门槛,加强风险控制。《[U]规定》对新药技术转让和生产技术转让所要求的技术资料,基本参照仿制药的要求,作了大幅度增加,并强调了转让前后的技术比较。[/U]增加了技术审评程序,参照改变产地的基本技术特点,相对于仿制药品的审评提高了技术审评的可对比性和可评价性。对经审评需要进行临床试验或者生物等效性试验的,还要完成规定的试验,[U]彻底改变了过去新药技术转让无需进行技术审评和临床试验的状况,[/U]极大提高了技术要求。《规定》还设置了“不予批准情形”:对于经国家食品药品监督管理局确认存在安全性问题的药品,其技术转让注册申请不予受理,已经受理的不予批准,从而进一步加强了风险控制。 四是品种管理由“静态”转变为“动态”。据了解,[color=#00008B]目前许多药品生产企业超过一半以上的批准文号闲置,常年生产的品种占企业总批准文号的比例不到四分之一。一方面大量批准文号闲置,另一方面仍然有大量药品生产企业申请新注册批准文号。[/color]批准文号闲置造成的生产技术闲置不仅仅是社会资源的浪费,而且对药品生产监管、上市药品的再评价和不良反应监测都非常不利。高质量的药品监管必须建立在药品正常生产和正常销售使用的基础上,也即动态基础上。药品技术转让,特别是生产技术转让,可以使本企业不使用的药品生产技术转让到其他需要该品种的企业,有利于产品资源的优化组合,有利于医药行业的健康发展。 国家食品药品监督管理局出台这个规定,就是要让技术作为一种产品,在市场上有序流通起来,鼓励一些技术有条件向外部转让。允许新药、上市多年药品、进口药品在一定条件下进行技术转让,鼓励先进科研成果和成熟生产技术的应用和推广,让国外的先进生产技术落户国内;有利于发挥市场配置资源的作用,有利于产品和资源优势重组,做大做强医药产业。
有没有新药品注册报批类的资料,急求,谢谢~
资料一:《药品管理法实施条例》第6条规定,新开办药品生产企业应当自取得药品生产证明文件或者经批准正式生产(我理解成应该是指注册批件)之日起30日内提出认证申请,省以上药品监督管理部门应当自收到申请之日6个月内组织对进行认证,认证合格的发给GMP认证证书(注:GMP即药品生产质量管理规范)。这段话很清楚,要先取得药品生产证明文件,再申请GMP认证资料二:《药品注册管理办法》中附件2: 化学药品注册分类及申报资料要求 2.资料项目2证明性文件: (1)申请人机构合法登记证明文件(营业执照等)、《药品生产许可证》及变更记录页、《药品生产质量管理规范》认证证书复印件,申请生产时应当提供样品制备车间的《药品生产质量管理规范》认证证书复印件;这个是首次申请药品注册的资料要求,为什么注册的时候就要提供GMP证书了呢?
药品注册,是国家食品药品监督管理局依照《药品管理法》的规定,根据药品注册申请人的申请,对拟上市销售药品的安全性、有效性、质量可控性等进行审查,并决定是否同意其申请的审批过程。在药品研制、生产、流通、使用的全过程监管中,药品注册管理是从源头上对药品安全性和有效性实施监管的重要手段,其根本目的是通过科学评价,保证上市药品安全有效,保障和促进公众健康。 1 2010年药品注册管理的重要举措 2010年,药品注册管理工作继续践行科学监管理念,紧紧围绕“质量和效率”这个中心,以风险效益评估和风险管理为核心,坚持“规范审批、公开透明、鼓励创新”的原则,全面推进体制机制改革和法制建设,强化学药品物研究全程监管,进一步推进审评审批公开公平,提高审评审批效率,较好地履行了《药品管理法》赋予的职责。 1.1 完善药品注册管理法规体系 一是发布了《药物临床试验伦理审查工作指导原则》,规范和指导伦理委员会的药物临床试验伦理审查工作,加强药物临床试验的质量管理和对受试者的保护,提高药物临床试验伦理审查工作质量。继续开展《药用原辅材料登记备案管理规定》、《药品标准管理办法》、《药物临床试验生物样本分析实验室管理规定》、《药物Ⅰ期临床试验管理指导原则》、《药物临床试验中严重不良事件报告与监测管理规定》及天然药物注册技术要求等法规和规范性文件的研究起草工作。
新华网北京4月20日电(记者吕诺、吴晶)国家食品药品监管局局长邵明立20日在《药品注册管理办法》征求意见座谈会上说,深化药品注册制度改革,应把握好强化药品安全、鼓励自主创新、鼓励发展中药和民族药、提高监管效能、健全责任体系等原则。 邵明立说,为确保上市药品的安全,必须强化风险意识,提高药品研制和注册申报资料的真实性、科学性和规范性。要不断完善药品技术评价体系,加大对药品研制原始数据和生产现场的检查力度,依法严厉打击药品研制和申报注册中的各种造假行为,切实解决好“研制不规范”的问题。 针对我国医药自主创新能力严重不足的现状,邵明立提出,要完善自主创新药物研制的早期介入机制,实行特殊审批程序;要科学设定自主创新药物技术转让相关要求,鼓励自主创新科技成果向生产力转化;要加大对仿制药的宏观调控,逐步提高仿制药的技术标准;要适度限制简单改剂型药品注册,坚决遏制药品研制的“低水平重复”;要统筹安排和合理分配监管资源,适当调整自主创新药和其他药品的审评审批工作时限。 邵明立说,中药和民族药是我国医药事业发展的特色和优势。我们必须探索建立符合中药和民族药特色的注册管理机制;要鼓励利用现代科学技术,提高中药和民族药的质量控制、疗效评价水平,支持利用新工艺、新技术对传统中成药和民族药进行二次开发;要理顺中药注册与中药品种保护的关系,依法完善和加强中药品种保护;要加强基础性研究,特别是对改变传统给药途径的中药注册申请强化风险评估。 药品注册涉及多个部门、多个监管环节,邵明立表示要强化地方监管部门的初步审查和现场核查职责,对有条件的地方,可以委托承担相应的审评审批等工作;要进一步明确技术监督机构在药品注册工作中的职责,有效整合监管资源;要建立科学规范的审评审批流转和协调机制,提高工作效率,减轻企业负担;要积极探索药品上市后再评价与再注册相结合的工作机制,建立健全药品退市制度。 由于药品注册过程涉及申请、受理、核查、检验、技术审评和行政审批等行为主体,邵明立指出必须明确各个行为主体的权力和责任,一方面要确立注册申请者为药品注册及上市质量保证的第一责任人,另一方面,药品监管部门必须依法履行监管职责,坚决维护“国药准字”的公信力。 “任何失职、渎职行为,都必须受到严厉的追究。”他强调。
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=45528]药品注册人员必读[/url]内容包括:注册检查注册人员必修课注册人员定级注册新手必读注册员办事流程图
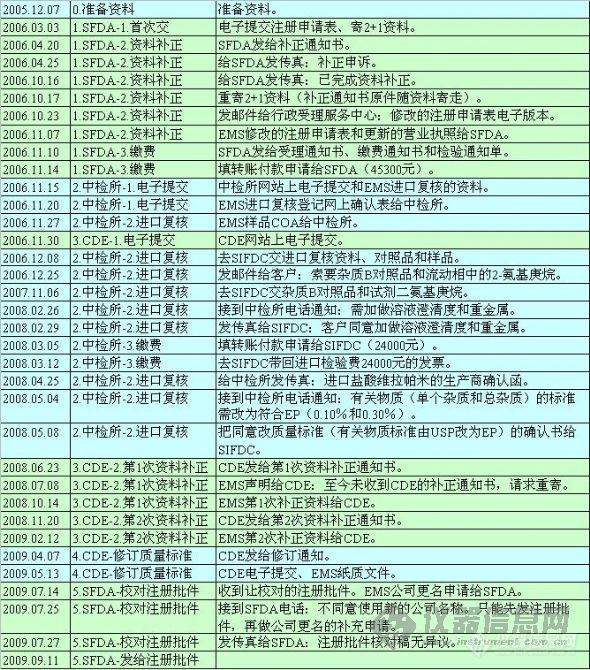
看看一个进口API注册的全部流程吧。这是我入行后全程负责并获得进口药品注册证的第二个API,历时近四年。其它半路插手的、补充申请的、地产的和出口的就不说了。[em09511][img]http://ng1.17img.cn/bbsfiles/images/2009/09/200909111626_170816_1612179_3.jpg[/img]
国内药品注册流程 以往主要是做国际注册的,接触国内的比较少,第一次做国内注册,没想到比国外注册麻烦多了,远比我想象的复杂,考虑到以后俺还会重复这些工作,而且越往后大脑将越来越不好使,本着好记性不如烂笔头的原则,现在把整个程序记录下来,不仅可以与同行分享,也可以方便以后的工作。关于国内注册的法规或攻略、介绍其实已经很多了,看得我头晕,相信刚刚接触注册的同行跟我也是一样的,所以我这里只是将整个流程梳理一遍,目的是在大脑中首先形成一种思路,知道自己需要做哪些事情,然后再具体了解如何去做这些事情。 整个程序的大致流程是这样的:法规学习(药品注册管理办法→确定药品注册的分类→确定需要准备的资料项目)→资料的准备与收集→资料的装订与提交→等待评审一、法规学习 在做这些工作之前,首先你得看《药品注册管理办法》,这是做药品注册工作必看的法规文件,当然还有其它很多的法规文件,但是那么多内容不可能全都记住,可以重点关注相关的内容(比方说你要做补充申请,那就看与补充申请有关的,要做原料药注册,那就看与原料药注册申请有关的),其它暂时只需了解。 第二,管理办法最后面的几个附件你得仔细看了,还是同样的原则,内容太多只看相关的,看多了也记不住,从这些附件中可以确定你所要注册品种的分类,根据分类就能确定需要准备哪些资料了。 相关的法规性文件可以参考学习下面的帖子:http://bbs.instrument.com.cn/shtml/20081018/1537892/二、资料的准备与收集,这是整个程序的重点和难点。 为了清晰明了化,下面就举一个例子说明一下: 比方说阿司匹林原料药的注册。1、阿司匹林为化学原料药,我们需要学习《药品注册管理办法》附件2化学药品注册分类及申报资料要求,从中可以了解到,该药为注册分类的第6类。2、申请注册分类6的药品,按照《申报资料项目表》的要求需报送资料包括:(一)综述资料(1~6)(二)药学研究资料(7~15)(三)药理毒理研究资料(16~27)(四)临床试验资料(28~32) 从申报资料项目表里可以知道,对于阿司匹林原料药,因为已有临床试验的数据,无需做临床试验,因此阿司匹林原料药需要报送的资料项目是1~16和28项。2.1 1~6是综述资料,对于原料药,阿司匹林不需要准备第5项关于药品说明书的内容。这6项资料中,3和4的准备是难点,需要对整个项目有很详细的了解,对于第4项,还需要具有一定的药学药理毒理知识,并能对这些内容进行分析总结与评价。2.2 7~15是药学研究资料,包括了药品研发、生产、过程控制与检验、稳定性考察等的整个生命周期,这部分内容目前提倡用CTD格式来准备。这9项资料是整个申报资料的核心,其中关于杂质研究以及工艺的研究是重点和难点,杂质研究不彻底也是众多申报资料被退审的主要原因。关于CTD资料的准备,可以参见下面的帖子:http://bbs.instrument.com.cn/shtml/20130331/4648949/2.3 16和28项资料,通常用文献资料代替,这就需要有一定的查询文献资料的功底了。三、资料的装订与递交。 看似简单,但是在实际装订的时候会遇到很多细节方面的问题,俺可是在咨询了很多人之后才搞定的。1、提交资料的份数: 需要提交的份数为2+1套,也就是有1套中只需要有资料项目(一)综述资料;另外2套中均包括了资料项目中(一)(二)(三)(四)的完整部分,这2套中,至少有1套里面提供的所有资料均为原件。2、资料的装订与装袋:
国家食品药品监督管理局021201药品注册申请表原始编号:XXXXXXXXX受 理 号:XXXXXXXXX申请事项1.申请分类:○ 新药申请 ○已有国家标准药品的申请2.申报阶段:○ 临床试验 ○生产3.注册分类:○中药、天然药物____类 ○化学药品____类 ○治疗用生物制品____类 ○预防用生物制品____类 ○生物制品增加新适应证 ○其他:4.附加申请事项:□非处方药 □减或者免临床研究 □国际多中心临床研究 □其他:药品情况5.药品名称: 6.英文名/拉丁名:7.汉语拼音: 8.化学名:9.其他名称:10.商品名称:○不使用 ○使用,中文: 11.药品名称来源:○国家药品标准 ○国家药典委员会 ○文献 ○自拟12.制剂类型○非制剂:○原料药 ○中药材 ○中药饮片 ○有效成份 ○制剂中间体 ○有效部位 ○其他:○制剂:剂型: 属于:○《中国药典》剂型 ○新剂型,英文:规格: 13. 包装:直接接触药品的药包材: 包装规格:14.药品有效期: 个月15.处方内药物活性成份或者中药药味(均含处方量):16.处方内辅料(含处方量):17.制剂中化学原料药来源: 序号来源原料药名称批准文号(注册号或受理号)生产企业18.制剂中的中药材标准:○全部法定 ○含非法定者,药材名称: ○无19.药品标准依据:○采用国家标准 ○自拟标准来源: ○中国药典_______________________版 ○生物制品规程_________________版○局颁/部颁___________________第______册 标准号____________________ ○注册标准或注册证号: ○国外药典及版次: ○其他20.主要适应症或者功能主治: 适应症分类:适应症:21.给药途径及特殊用法:相关情况22.是否特殊管理药品:○否 ○是: □麻醉药品 □精神药品 □放射性药品23.专利: □有中国专利:□化合物专利 □工艺专利 □处方专利 □其他专利专利名称: 专利人: 专利到期日期: 本申请是否得到专利权人的实施许可:○是 ○否□有外国专利: 专利名称:专利权人:24.同品种药品保护:□药品行政保护 保护截止日期: □中药品种保护 保护截止日期: □已知有申请者 □新药过渡期 截止日期:□原新药保护 保护截止日期: 25.同品种新药监测期:○无 ○有,起始日期: 终止日期:26.本次申请为:○首次申请 ○再次申请,其首次申请:□曾经撤回,原因:□曾被退审(或者退回),日期: 原因:27.境外是否获准上市:○否 ○不详 ○是,国家(地区): 日期:申请人28.机构1(国内药品生产企业):○无 ○有 □本机构负责缴费 名 称: 组织机构代码: 《药品生产许可证》编号:法定代表人: 职位:注册地址: 邮政编码:生产地址: 邮政编码:注册申请负责人: 职位:电话(含区号及分机号): 传真:电子信箱: 注册地址所在省份:联系人: 手机号码: 电话:是否持有相应的《药品生产质量管理规范》认证证书:○持有 未持有,原因:○新开办企业 ○新建车间 ○新增剂型 ○新原料药 ○无需提供 ○正在改造29.机构2(新药证书申请人): ○无 ○有 □本机构负责缴费名 称:组织机构代码: 法定代表人: 职位:注册地址: 邮政编码:注册申请负责人: 职位:电话(含区号及分机号): 传真:电子信箱: 联系人: 电话: 手机号码:30.机构3(新药证书申请人):○无 ○有 □本机构负责缴费名 称:组织机构代码: 法定代表人: 职位:注册地址: 邮政编码:注册申请负责人: 职位:电话(含区号及分机号): 传真:电子信箱:联系人: 电话: 手机号码:31.机构4(新药证书申请人):○无 ○有 □本机构负责缴费名 称:组织机构代码: 法定代表人: 职位:注册地址: 邮政编码:注册申请负责人: 职位:电话(含区号及分机号): 传真:电子信箱:联系人: 电话: 手机号码:32.机构5(新药证书申请人):○无 ○有 □本机构负责缴费名 称:组织机构代码: 法定代表人: 职位:注册地址: 邮政编码:注册申请负责人: 职位:电话(含区号及分机号): 传真:电子信箱:联系人: 电话: 手机号码:33.其他新药证书申请人: ○无 ○有34. 指定联系机构: 机构_____为指定联系机构 邮政编码: 通讯地址: 对本项注册申请单独以该机构名义提交的文件是否能够代表全部申请机构 ○是 ○否 ○无相关受理号35.相关申请受理号:声 明36.我们保证:①本申请遵守《中华人民共和国药品管理法》、《中华人民共和国药品管理法实施条例》和《药品注册管理办法》等法律、法规和规章的规定;②申请表内容及所提交资料、样品均真实、来源合法,未侵犯他人的权益,其中试验研究的方法和数据均为本药品所采用的方法和由本药品得到的试验数据;③一并提交的电子文件与打印文件内容完全一致。如查有不实之处,我们承担由此导致的一切法律后果。37.其他特别申明事项:38.各申请机构名称、公章、法定代表人签名、签名日期:经审查,本表填写符合形式审查要求。审查机关审查机关: 审查人签名: 日期: 年 月 日
[color=#DC143C][center]药品注册新旧办法差异分析[/center][/color] 药品注册工作是保障药品质量的源头,也是药品监管中心的环节。2005 年5月1 日,《药品注册管理办法》正式施行,在两年多的实施过程中,为药品注册做出了重要贡献,使我国成为真正意义上的仿制药大国,尽管尚没有制剂走出国门步入欧美市场。最近听说华海药业固体制剂通过FDA 认证,海南普利也正在紧锣密鼓的准备着,国产制剂进军欧美指日可待,令人为之一振。话题扯远了,历时一年多的核查,令人精疲力竭,甚至感到沮丧。算了,甭提了,新的注册管理办法业已于2007 年7 月10 日公布,并将和其他一些相关规定将于10 月1 日粉墨登场。民间出版社总编来到我公司,希望我公司能在07 办法布满月时,编写一本关于新旧注册管理办法对比分析的书。大核查刚过,百废待兴,实难抽身,然推诿不过,只好忙里偷闲对新旧办法进行了比较。由于本人水平有限,且对07 版办法稍有成见,再者时间仓促,文中难免偏颇之词,哗众取宠甚至吹毛求疵之语。唯希望读者口下留情,因为此书旨在和大家共同学习理解新的注册管理办法,进而达到真做药,做真药,做好药之目的。尽管现状不容乐观,但莫要灰心丧气;尽管不断有故人远离这领域,但更有新军涉足该行业,虽然改变现状凭 一己之力,不足挂齿,但是众人心齐,泰山可移。药界的明天仍然值得期待。 再过不到俩月,05 版注册管理办法就要结束自己的使命,让我们和旧的注册管理办法挥手告别,和新的注册管理办法来一个硕大的拥抱,在新法的指下沿着创新的轨道一路奔跑。书中后面还整理了新药仿制药注册流程,同时将附件附在本书后面,以飨读者。书中不妥不当之词,欢迎指正。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=143597]新旧办法差异分析[/url]
《药品注册现场核查要点及判定标准》课件-11-14版(幻灯片)药品注册现场核查工作方案1106 药品注册现场核查要点及判定标准发文报表7个(附表1药品注册撤回申请表,附表2药品注册申请撤回汇总报表,附表3药品注册自查报告表,附表4药品注册全面现场核查报告表,附表5药品注册全面现场核查汇总报表,附表6药品注册现场核查委托表,附表7药品注册现场核查委托报告表)[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=52224]都在这一个包里了[/url]
[b]一、化学药品新注册分类申报资料要求的《原料药药学信息汇总表》《制剂药学信息汇总表》《非临床研究信息汇总表》《临床信息汇总表》填报时格式、目录及项目编号能否进行修改?[/b] 答:2016年5月4日,《总局关于发布化学药品新注册分类申报资料要求(试行)的通告》(2016年第80号),附件《化学药品新注册分类申报资料要求(试行)》中申报资料撰写说明,信息汇总表中的信息是基于申报资料的抽提,各项内容和数据应与申报资料保持一致,并在各项下注明所对应申报资料的项目及页码。主要研究信息汇总表的格式、目录及项目编号不能改变。即使对应项目无相关信息或研究资料,项目编号和名称也应保留,可在项下注明“无相关研究内容”或“不适用”。对于以附件形式提交的资料,应在相应项下注明“参见附件(注明申报资料的页码)”。 [b]二、药品申报资料中临床试验报告的封面有哪些要求?[/b] 答:依据《总局关于发布化学药品新注册分类申报资料要求(试行)的通告》(2016年第80号),临床试验报告参照《化学药物临床试验报告的结构与内容技术指导原则》,该指导原则要求临床试验封面应包括受试药物通用名、研究类型、研究编号、研究开始日期、研究完成日期、主要研究者(签名)、研究单位(组长)(盖章)、统计学负责人签名及单位盖章、药品注册申请人(盖章)、注册申请人的联系人及联系方式、报告日期、原始资料保存地点。同时,按照《关于印发化学药药学资料CTD格式电子文档标准(试行)和药品注册申报资料的体例与整理规范的通知》(食药监办注〔2011〕98号)附件2要求,临床试验报告封面应加盖临床研究基地有效公章,印章应加盖在文字处,并符合国家有关用章规定,具有法律效力。 [b]三、如何办理化学药品新注册分类费用的补交或退还?[/b] 答:关于补交方式。申请人须按照《关于化学药品新注册分类收费标准有关事宜的通告》(2016年第124号)中,提交补交费用申请及相关材料至原受理部门,由原受理部门开具“行政许可事项缴费通知书(补交)”,申请人持缴费通知书办理缴费。 关于退还方式。申请人须按照《关于化学药品新注册分类收费标准有关事宜的通告》(2016年第124号),提交补交费用申请及相关材料至原受理部门,原受理部门按照“全款方式”即先补交全款的费用,再办理与其相对应费用的退还。 [b]四、对于BE过程中处方工艺有变动的是否可在总局药审中心网站BE试验备案平台上备案?[/b] 答:BE试验过程中,参比制剂、原料药、制剂处方、工艺等发生变更,注册申请人可通过备案平台如实备案,申报生产时,在申报资料中一并提交历次变更及备案资料。 [b]五、研发机构在新注册分类发布前已基本完成研发的原注册分类第3类产品如何注册申报?[/b] 答:《药品注册管理办法》第七十三条规定,仿制药申请人应当是药品生产企业。《关于发布化学药品注册分类改革工作方案的公告》规定,新注册分类3、4类别药品应按仿制药的程序申报。考虑到部分研发机构在新注册分类发布前已基本完成原注册分类第3类产品的研发,对于此类情形,若研发机构仍希望继续申报的,可向省局提出书面申请,经省局确认,如确属在新分类工作方案发布前完成相关研究工作,并需要开展临床试验的,可按新注册分类和仿制药的程序受理。 研发机构位于药品上市许可持有人试点行政区域内的,申请人应按照持有人试点方案要求进行申报。
药品注册管理办法[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=53471]药品注册管理办法[/url]
[B]下面这份注册申请表是翻译给国外供应商看的,放上来大家讨论。涉及到专业方面的内容很少,主要是行政方面的,大家都能看明白的。有些地方我觉得老外可能不明白,就自己加了注释。[/B]2009.02.22更新的word版本:[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=137973]进口药品注册申请表[/url][color=#DC143C][B]表头:[/B][/color]数据核对码:Bar Code[sup][1][/sup]原始编号:Original Application No. [sup][2][/sup]受理号:Accept No. [sup][3][/sup]国家食品药品监督管理局STATE FOOD AND DRUG ADMINISTRATION药品注册申请-境外申请人用表DRUG REGISTRATION APPLICATION -- FOR FOREIGN APPLICANTS[1]: The bar code is created randomly by the software. Each time the application form is amended, a new bar code will be created.[2], [3]: To be given by SFDA after the application is accepted.
[center]浅析《药品注册现场核查管理规定》[/center]时一篇论文,大家看看吧[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=160127]浅析《药品注册现场核查管理规定》[/url]
欧盟药品注册管理浅析[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=167268]欧盟药品注册管理浅析[/url]
药品注册 药品为一特殊商品,其质量的好坏将直接关系到广大人民群众的健康问题。药品的上市必须通过国家食品药品监督管理部门监管,并基于对药品的安全、有效、质量可控等特性审核、批准。 项目负责人提供资料□ 注册申请表7份 □ 注册申请资料报送一式5套 ○公司留底1套原件 ○省局注册处1套原件 ○省药检所送检用资料(5#、8#、10#、11#、 12#、14#) ○寄国家局2+1套(两套原件全部资料,一套第一部分综述资料复印件)资料封面格式 注册分类:(中药/化学药品/生物制品) 药品名称 资料项目名称----资料项目编号(*——*) 研究机构:(加盖公章) 研究机构地址: 研究机构电话: 研究机构主要研究者姓名:(签字) 试验者姓名: 试验起止日期: 原始资料的保存地点: 联系人姓名、电话 药品注册申请人名称:(加盖公章) 药品代理机构名称:(加盖公章)□资料按套装入档案袋 □档案袋正面:药品名称 本袋所属第×套第×袋每套共×袋 本袋内装入的资料项目编号 申请申请人名称 药品代理机构名称 ☆省局报送资料前应将省局发给的原始编号、申请编号写在档案袋正面和申请表右上角。 ☆国家局受理后,应将国家局的受理号标注在档案袋封面和申请表右上角。~~~~~~~~~~~~~~ [img]http://bbs.instrument.com.cn/images/affix.gif[/img][url=http://bbs.instrument.com.cn/download.asp?ID=199254]ҩ Ʒ ע %B2%E1%C9%EA%C7%EB%D7%CA%C1ϵ %C4%D0%CEʽ Ҫ %C7%F3.rar[/url]
来源:健康报 相关人士从国家食品药品监督管理局获悉,药监部门目前正在修订现行的《药品注册管理办法》。该局副局长吴浈4月20日在修订征求意见座谈会上表示,本次修订将堵塞药品审评审批中存在的漏洞,规范注册秩序,打击注册申报材料弄虚作假,遏制大量低水平重复申报,提高新药质量和安全性。 吴浈说,目前存在的问题,一是现行《药品注册管理办法》对原始材料的审查、产品质量检验要求不够。一些申报单位为了经济利益,放松自律,出现了研究材料不规范,甚至弄虚作假的严重问题。二是鼓励创新不够,没有从法规上设定必要的限制。受各种因素的影响,简单改剂型品种和仿制品种申报数量急剧增多。三是监督不到位,审评审批权力配置不合理,存在标准不够完善、程序不够严密、过程不够透明等问题。 吴浈表示,修订后的《药品注册管理办法》将解决申报资料不真实的问题。申报生产品种,在批准上市前均须进行现场生产检查,并抽样检验,不合格的不予批准。修订后的注册管理办法将不批准其他企业对监测期内药物进行改剂型的申请,已上市品种改变剂型但不改变给药途径的注册,只有原剂型批准证明文件持有者才能申请。 吴浈介绍说,修订后的《药品注册管理办法》将规定,逐步取消对新药技术转让及委托生产的限制,鼓励研究单位将精力放在研究开发上,将有限的资金使用到研究开发上,而不是一味进行仿制药的研发。
化学药品注册时产品需要做结构确证,产品中的杂质是否也需要做结构确证呢?

化学药品注册改革了,分享一下《化学药品注册分类改革工作方案》政策解读(三),供药物注册的同仁参考。[img=,690,635]http://ng1.17img.cn/bbsfiles/images/2017/10/201710181644_01_2700892_3.png!w690x635.jpg[/img][img=,690,481]http://ng1.17img.cn/bbsfiles/images/2017/10/201710181644_02_2700892_3.png!w690x481.jpg[/img]