注射用油中的麻油是什么?到底是黑芝麻油还是白芝麻油?
有关注射用水的条款讨论2007版GMP认证检查评定标准第*3402内容如下:注射用水的制备、储存和分配应能防止微生物的滋生和污染,储罐的通气口应安装不脱落纤维的疏水性除菌滤器,储存应采用80℃以上保温、65℃以上保温循环或4℃以下保温循环。生物制品生产用注射用水应在制备后6小时内使用;制备后4小时内灭菌72小时内使用。有人认为生物制品生产用注射用水只要满足:制备后6小时内使用;制备后4小时内灭菌72小时内使用。就可以了我认为生物制品生产用注射用水既要满足:储存应采用80℃以上保温、65℃以上保温循环或4℃以下保温循环;又要满足:在制备后6小时内使用;制备后4小时内灭菌72小时内使用。大家怎样理解啊?请参与!
注射用水与纯化水的水质区别 如将美国药典中纯化水与注射用水的水质标准作一比较,就可看出二者的主要区别。它们的理化指标相同,但注射用水对热原及微生物的要求高于纯化水。表1.1列出了美国药典中纯化水和注射用水热原和微生物的区别。 表1.1 美国药典中纯化水与注射用水热原和微生物的区别 种 类 项 目纯化水注射用水 微生物100CFU/mL 10CFU/100mL 热原 不指定 0.25EU/mL 生产方法 蒸馏 离子交换 反渗透 其他适当的方法蒸馏 反渗透 纯化水与注射用水二者的区别还在于制水工艺,纯化水的制备工艺可以有各种选择,但各国药典对注射用水的制备工艺均有限定条件,如美国药典明确规定注射用水的制备工艺只能是蒸馏及反渗透,中国药典则规定注射用水的生产工艺必须是蒸馏。这些是各国根据本国的实际情况用以保证注射用水质量的必要条件。
如果非正常连续生产,车间注射用水不是采取保温或者循环处理的,只是在生产前进行一次各取样口的全检,然后如果结果合格,车间认为该系统注射用水无问题,如次日无生产安排,则放掉制好的注射用水,等待次日重新制水,如此是否可行?个人认为检验合格的注射用水是针对于当时制备的,如新制水应再进行取样检验,但是,注射用水也有其检验周期,我们定的是1周,所以,似乎也说的过去,不知大家是什么情况呢?欢迎讨论,谢谢![em61]
本人急需注射用头孢他啶(Ceftazidime)和注射用头孢米诺钠(Cefminox sodium)EP6.0的标准,复印件也行,谢谢!
在我们每天的注射用水监控中,发现在注射用水罐总出水口的需氧菌总数总是会多于总回水口的需氧菌总数,不知为什么,按道理不是应该总出水口要少于总回水口吗?
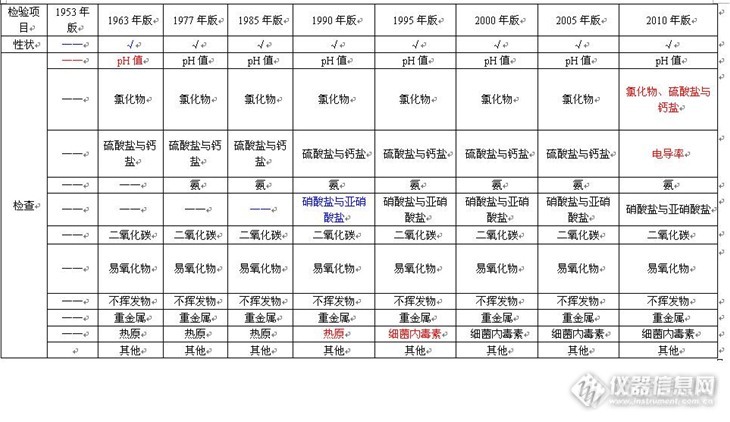
打过针的同学都知道,打点滴用的是生理盐水或者葡萄糖水。而屁股针或皮下针一般都是用的灭菌注射用水。药剂或者灭菌药粉用灭菌注射用水稀释或者溶解后,才能正常使用。不然,就有可能不治病,反致命!所谓灭菌注射用水,就是灭过菌的注射用水。因为注射用水一般是用蒸馏纯化水的方法得到的。学过物理的同学都知道,水在100℃的时候就会沸腾变成水蒸气,也就是说,这种蒸馏方式得到的注射用水,最高也就经受了100℃温度的洗礼。学过生物的同学还知道,100℃的温度,对于嗜热的细菌以及耐热的芽孢来说,完全就是泡一次澡而已。要想干掉这些致命的玩意儿,必须下狠招,也就是说,必须来上更猛烈的“暴风雨”!因此,利用高压灭菌锅,利用蒸汽的压力,可以产生115℃的温度,30分钟内杀灭其中的所有生灵(相对概念上的意义哦)!这样,才能保证我们用药的安全。中国药典中规定了灭菌注射用水的检验标准。只有检验合格的灭菌注射用水才是安全的。而灭菌注射用水的检验标准,随着时代的流逝,也经历了一些变化。具体见下表:http://ng1.17img.cn/bbsfiles/images/2013/12/201312272159_485078_1609327_3.jpg其演变的历程与注射用水的历程同步。主要为以下:1. 灭菌注射用水与注射用水相比较,检验项目的设置基本一致,但是限度更低,更为苛刻;2. 1953年版没有关于灭菌注射用水的描述,可能与当时的认识水平有关;3. 1953年的版本,对“形状”没有专门规定,而从1963年开始,有了专业而具体的规定;4. 1953年命名为为“酸碱度”的检验项目,1963年更名为pH值,使得测量更加科学与准确;5. 从1953年至2005年,一直沿用的是“氯化物、硫酸盐与钙盐”这个项目名称,2010年替换为电导率测量;6. 1953年为“铵盐”的检验项目,1963年改为“氨”的测定;7. 1985年之前,一直没有检验“硝酸盐与亚硝酸盐”,随着认识的提高,1985年版中国药典增加了该检验项目;8. 2010年版中国药典将以前的“二氧化碳”与“易氧化物”的检验项目,合并为“总有机碳”检验项目;9. 1953年至1990年,一直沿用的“热原”检验项目,在1995年更名为“细菌内毒素”;10. 从2005年版开始,增加了“微生物限度”检验项目。
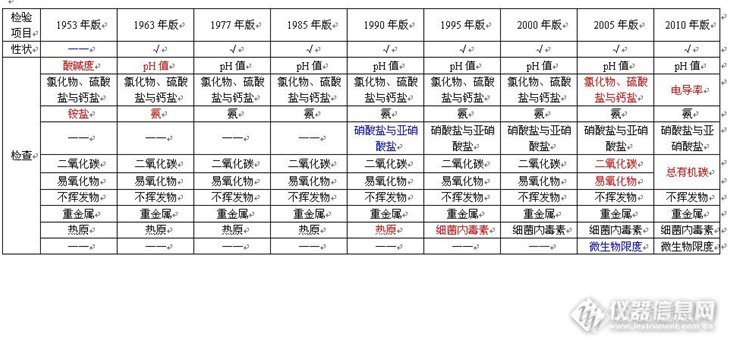
生病要打针吃药,打针需要用到灭菌药粉或注射剂。灭菌药粉就是粉末状的药物,这个且不说它。而注射剂又分为两类,一种为油性注射剂,另一种就是水针注射剂。生产水针注射剂,必须要用到注射用水。中国药典规定:注射用水必须为纯化水经蒸馏所得的水。这个注射用水,是制药企业最基础的原材料之一。不光配置药剂用的上,清洗仪器也要用。因此,我在这里说道说道和每个人都会发生联系的注射用水在中国药典中的演变历程。中国药典是制药行业的圭臬。中国药典从诞生的那一天起,就一直收录着“注射用水”这个品种,几十年走来,这个品种一直都存在,只是检验项目因为人们的认识水平的提高而发生了不少的改变。具体怎么个改变法,我想用一个表格来说明一下:http://ng1.17img.cn/bbsfiles/images/2013/12/201312262255_484901_1609327_3.jpg从表中可以看到:1. 1953年的版本,对“形状”没有专门规定,而从1963年开始,有了专业而具体的规定;2. 1953年命名为为“酸碱度”的检验项目,1963年更名为pH值,使得测狼更加科学与准确;3. 从1953年至2005年,一直沿用的是“氯化物、硫酸盐与钙盐”这个检验项目,2010年替换为电导率测量;4. 1953年为“铵盐”的检验项目,1963年改为“氨”的测定;5. 1985年之前,一直没有检验“硝酸盐与亚硝酸盐”,随着认识的提高,1985年版中国药典增加了该检验项目;6. 2010年版中国药典将以前的“二氧化碳”与“易氧化物”的检验项目,合并为“总有机碳”检验项目;7. 1953年至1990年,一直沿用的“热原”检验项目,在1995年更名为“细菌内毒素”;8. 从2005年版开始,增加了“微生物限度”检验项目。你知道检验项目进行修正的出发点和目的是什么吗?欢迎进行讨论。懒惰的人可以静等我的下回分解哦。
谁做过注射用左卡呢汀?我们做有关物质时在主峰后面约2分多的位置上经常会有一个小峰,有它在有关物质就不合格。这个小峰时而出现,时而不出现。曾经做过原料、辅料的对比。辅料没有峰,同样的检测条件,原料也有一个类似的峰,但原料检验是合格的(用原料的质量标准检验)。恳请高人帮忙指导!
注射用头孢西丁钠生产工艺验证方案[~74687~]

《中国药典》2015年版四部P491"甘油(供注射用)"有如下图片内容。我们生产的注射液使用甘油(供注射用)作为辅料,注射液为最终灭菌产品,请问作为辅料的甘油,是否还需要检验无菌?我的理解是,由于产品是最终灭菌产品,作为辅料,控制微生物限度和细菌内毒素是必要的,因此不需要无菌检验,但是,也有不同意见,说因为生产的注射液属于无菌制剂,且由于其生产过程无除菌工艺,因此,图中的“无菌(供无除菌工艺的无菌制剂用)”这一项应该进行检测。如此,我认为还是矛盾,如果无菌都检测,微生物限度还有必要测吗?另外,最终灭菌的产品,有必要对其辅料检测无菌吗?谢谢!
本人刚刚开始从事检验工作,希望得到广大网友的支持首先,请大家给我发个注射用水检验相关的资料,谢谢
请教,哪位有关于纯化水和注射用水的资料,在下想学习一下.
本文以世界卫生组织(WHO)验证的成都生物制品研究所乙脑疫苗项目为实例,分析注射用水储存与配送系统的设计、采购、安装、验证。重点分析注射用水环路以及冷环路的设计,以及项目采购材料的分析,安装时的焊接控制,试车与安装操作验证整合方法。
注射用无菌粉末需要测定渗透压吗?使用时是溶解在0.9%氯化钠或5%葡萄糖中,静脉滴注。 我是这么想的:药品溶解在0.9%氯化钠或5%葡萄糖,其渗透压应该是略微变大的吧,这样还有必要做这个实验吗? 我看了下2010药典,渗透压的标准是多少啊?注射用无菌粉末都没有表明渗透压范围啊?但是我找一些注射液的标准里面就有具体的渗透压范围。
药友制药紧急召回炎琥宁 10余名婴幼儿用后休克 中国消费者报http://i1.sinaimg.cn/cj/consume/puguangtai/20120914/1347578725_oozdma.jpg 图1为重庆药友制药有限公司生产的注射用炎琥宁。洪敬谱/摄 http://i2.sinaimg.cn/cj/consume/puguangtai/20120914/1347578725_aZmg7E.jpg 图2为幼儿正在医院抢救的情景。资料图片 本报合肥讯(记者洪敬谱)9月初,安徽省合肥市10余名婴幼儿因为感冒发烧在安徽医科大学第一附属医院(以下简称安医大第一医院)治疗后,普遍出现休克状况。经医院积极救治,这些孩子目前病情稳定。9月11日中午,合肥市药品不良反应监测中心致电本报记者称,目前正在对这些婴幼儿使用的注射用炎琥宁进行检测,会及时向本报公布检测结果。目前,重庆药友制药有限责任公司已将该省内使用的生产批号为12102863、规格为80mg的注射用炎琥宁全部召回。 9月9日晚上,合肥市民刁先生等10多位婴幼儿家长向本报记者反映称,自己的孩子在安医大第一医院看病输液,之后出现休克情况,家长们怀疑使用的药品存在安全问题。
中国药典2005年版二部附录细菌内毒素检查法中的干扰试验,说:"使用的供试品溶液应为未检查出内毒素且不超过最大有效稀释倍数(MVD)的溶液."请问如果做注射用水的细菌内毒素,那么供试品溶液是什么样的注射用水?怎样处理不含内毒素?后面的"凝胶半定量试验"A "从通过干扰试验的稀释倍数开始"这个稀释倍数是定值吗?怎样求?"系列溶液A中每一系列平行管的终点稀释倍数乘以λ,"什么是终点稀释倍数?
不知那位高手可以提供注射用水电导(USP 或Eu P)测试方法,万分感谢!![em61] [em61] [em61]
按理说,应该根据验证结果确认,请问大家现行工作中注射用水、纯化水全检周期是多长时间?谢谢参与讨论![em44] [em17]
大家一般都是用制水机,除此之外,有没有去制水室取注射用水(生产型)做为实验用水的?你们是怎么保存,拿什么保存?有效期是多久啊?
用了很久的超纯水了,换了个单位,发现在配流动性时用注射用水,电导率和cot都合格,不知是否可以,个人认为还是用超纯水好,大家说说自己的看法
大家一般都是用制水机,除此之外,有没有去制水室取注射用水(生产型)做为实验用水的?你们是怎么保存,拿什么保存?有效期是多久啊?
求注射用水系统验证方案和报告.每小时100升.
[center]FDA批准10年来首个新型静脉注射用抗高血压药[/center]The Medicines公司8月4日宣布,美国FDA已批准其静脉注射用制剂丁酸氯维地平(clevidipine butyrate,Cleviprex)注射用乳剂在不适用或不希望使用口服制剂的情况下用于高血压的治疗。本品是10年来美国FDA批准的首个新型静脉注射用抗高血压药。 本品作为1种新型静脉注射用抗高血压药,代表了当前高血压治疗中的一大进步,其可以在危重病护理中快速、精确地控制血压。来自急诊室、手术室和重症监护室的综合资料显示,本品将成为医生控制患者血压时的重要选择手段。 本品可迅速起效,可用于精确控制血压。与现有静脉注射用抗高血压药通过肾脏和(或)肝脏代谢不同,本品在血液和组织中代谢,不在体内产生蓄积。信息来源:中国医药123网
项目需要,请问一下美国药典规定的无菌注射用水的要求是什么?谢谢
超纯水和注射用水,哪个级别更高呢?更干净?
目前我单位注射用水和纯化水检验周期是按照2003版验证指南进行验证后的日常检验周期,现在因为任务量很大,考虑将检验水的周期延长,延长的根据就是基于对以往连续性测试结果的分析。如何对这些检验数据进行汇总分析呢?怎样的限度范围内是可以延长的?延长到多久?依据又是什么呢?
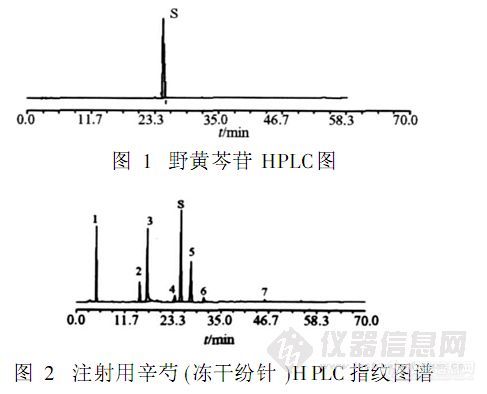
【作者中文名】苏红; 王爱民; 王永林; 兰燕宇; 何迅; 李勇军;【作者英文名】SU Hong; WANG Ai-min; WANG Yong-lin; LAN Yan-yu; HE Xun; LI Yong-jun(School of Pharmacy; Guiyang Medical College; Guiyang 550004; China);【作者单位】贵阳医学院药学院; 贵阳医学院药学院 贵州贵阳; 贵州贵阳;【摘要】目的:采用RP-HPLC建立注射用辛芍(冻干粉针)的指纹图谱测定方法。方法:采用Diamonsil C18色谱柱,80%乙腈-0.1%磷酸溶液为流动相进行梯度洗脱,流速1.0 mL.min-1,柱温40℃,检测波长为230 nm。结果:在相同色谱条件下获得药材、中间体和制剂的各色谱峰分离较好,建立了注射用辛芍的HPLC对照指纹图谱,标注了制剂中的8个共有指纹峰,制剂与药材、中间体的指纹图谱有良好的相关性,10批样品相似度大于0.97,达到指纹图谱的技术要求。结论:该方法准确、重复性好,可作为注射用辛芍(冻干粉针)质量控制的重要依据之一。http://ng1.17img.cn/bbsfiles/images/2012/08/201208131742_383598_2379123_3.jpg
请问有谁知道注射用无菌粉末怎样测定渗透压摩尔浓度?谢谢
中国药典(2000版)欧洲药典(2000增补版)USP24来源本品为纯化水经蒸馏所得的水为符合法定标准的饮用水或纯水经适当方法蒸馏而得由符合美国环境保护协会或欧共体或日本法定要求的饮用水经蒸馏或反渗透纯化而得性状无色澄明液体,无臭,无味无色澄明液体,无臭,无味/PH5.0~7.0//氨0.2μg/ml//氯化物、硫酸盐与钙盐、亚硝酸盐、二氧化碳、不挥发物符合规定//硝酸盐0.06μg/mL0.2μg/mL/重金属0.5μg/mL0.1μg/mL/铝盐/用于生产渗析液时方控制此项/易氧化物符合规定符合规定/总有机碳(TOC)/0.5μg/mL0.5μg/mL电导率/1.1μS/cm(20℃)符合规定细菌内毒素0.25E.U./ml0.25E.U./ml0.25E.U./ml微生物纠偏限度(action limit)/10个/100ml10个/100ml注:1. 美国药典中规定:企业自用的注射用水(原料)监测TOC和电导率,供商用的注射用水(不包括美国药典中规定的无菌注射用水),应符合无菌纯水的试验要求。表中所列为企业自用注射用水的监测项目。欧洲药典中TOC和易氧化物项目,可任选一项监控。