求中药颗粒的制备过程?
中药颗粒剂如何质量控制? 为了保证颗粒剂成品质量的一致性和稳定性,从休止角、堆密度、吸湿性三个方面对半成品的质量进行了控制,具体方法和结果如下: 一、 休止角的测定: 取适量半成品颗粒,用固定漏斗法测定休止角,结果见下表: https://ng1.17img.cn/bbsfiles/images/2024/09/202409182050407176_6502_2204446_3.png!w552x189.jpg 结果表明,该颗粒休止角小于40度,流动性好,易于分装。 二、堆密度的测定:称取一定量的半成品颗粒,装入10ml量筒中,以一定高度落下(尽可能控制高度一致),使松紧适宜,以重量及容积计算其堆密度,结果见下表: https://ng1.17img.cn/bbsfiles/images/2024/09/202409182052049344_2683_2204446_3.png!w533x205.jpg 实验结果表明,该颗粒剂的平均堆密度为0.50 g/ml,为成品的包装提供了依据。 三、颗粒剂吸湿性的研究: 取底部盛有NaCl过饱和溶液的玻璃干燥器,干燥器内置一称量瓶,放入25℃恒温干燥箱内恒温24小时,此时干燥器内的相对湿度为75%。取样品5g,精密称定,置称量瓶中, 将盛皿盖打开,与25℃恒温干燥箱内保存,每隔一定时间称重一次,计算各时间的吸湿百分率,结果见下表. https://ng1.17img.cn/bbsfiles/images/2024/09/202409182137529912_59_2204446_3.png!w511x182.jpg 以测定时间为横坐标,颗粒吸湿率为纵坐标绘制曲线,即得颗粒吸湿平衡曲线,结果见下图: https://ng1.17img.cn/bbsfiles/images/2024/09/202409182139027276_8927_2204446_3.png!w492x207.jpg 由颗粒吸湿平衡曲线可见,本颗粒剂在168小时内基本不在吸湿,吸湿百分率为19.21。 临界相对湿度的测定:水分对固体制剂稳定性影响很大,而环境的湿度是颗粒剂稀释的一个重要来源,为了尽量减少颗粒吸潮,本研究测定了扶正固本颗粒(无糖型)的临 界相对湿度,为控制该制剂的制备及分装车间的相对湿度提供参考依据。 测定方法:取样品颗粒14份,分为2组,每组7份,每份2g,置于敞口的称过重量并编号的称量瓶中,精密称定,打开称量瓶盖,分别放入不同湿度的玻璃干燥器中,在25℃ 烘箱放置168小时,取出称量瓶,加盖后精密称定,计算样品的水分含量,结果见下表.以水分百分含量为纵坐标,相对湿度为横坐标作曲线,结果见下图. https://ng1.17img.cn/bbsfiles/images/2024/09/202409182140178751_4701_2204446_3.png!w555x661.jpg 可见,相对湿度在[font=宋体]61%以下时,颗粒的吸水率较小,而在61%以上,颗粒吸湿性明显增加。同时,根据吸湿曲线显示,该品种的临界相对湿度为61%,故在制粒、分装的过程中,环境湿度必须控制在61%以下,以减少水分对药物性质及稳定性的影响。
[size=6][b]中药配方颗粒国际组织标准呼之欲出[/b][/size]2010-02-08 14:51作者:中国中医药报[url=http://info.pharmacy.hc360.com/list/zhongyao.shtml]中药[/url]配方颗粒以其使用方便、质量规范、安全有效、稳定可控,且保持饮片组方灵活、加减随机等传统特色与优势,在国内外都存在着巨大的市场前景。然而,由于不同企业间中药配方颗粒产品在生产、标准等方面缺乏统一的生产工艺和质量标准,严重影响了中药配方颗粒的推广和应用。因此,针对中药配方颗粒生产的各个环节,建立一套配方颗粒规范化生产和管理的技术标准体系,已成为当前一项非常紧迫的工作。 中药配方颗粒的科研情况 在中药配方颗粒的科研方面,一些企业做了大量的工作。 1.在工艺和标准的研究方面,建立了每个品种的制备工艺和质量标准。尊重中药汤剂水煎历史,最大限度地保留水煎汤剂的有效成分。确定每味药的加水量、升温煮沸时间、煎煮次数;先煎后下品种挥发油的提取方法,加入比例;选择合适除杂工艺;摸索不同性质品种的喷雾干燥工艺;研制基本不加[url=http://info.pharmacy.hc360.com/zt/yyfl/index.shtml]辅料[/url]前提下的制粒工艺等。 2.在鉴别方法的专属性研究方面,建立了200个品种的专属性鉴别方法,使其具有独特的特征。 3.在质量标准的示范性研究方面,从种子到成品,形成一套技术体系和标准平台。 制定原料标准:研究并选定产地、品种、等级;为避免硫磺熏蒸,80多个品种采用新鲜[url=http://www.pharmacy.hc360.com/]药材[/url]投料;全部测定含量及重金属,农药残留量易超标品种测定农残量、黄曲霉素。 制定[url=http://info.pharmacy.hc360.com/list/yuanliao.shtml]中间体[/url]、成品检测标准:采用高效液相色谱法(HPLC)、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法(GC)、薄层扫描法(TLCS)等方法进行鉴别和含量测定。其中建立薄层鉴别方法400多个品种,含量测定方法100多个品种。出版发行《中药配方颗粒薄层彩色图谱集》。产品从原料到成品经五道化验检测合格后才能出厂。 浸膏防湿研究:从[url=http://info.pharmacy.hc360.com/list/bzcl_zl.shtml]包装材料[/url]上选择突破口,使产品可以保持5年以上不吸潮。 制定GMP各项管理文件3000多个,严格控制每一环节的生产质量。 4.在标准提升与安全性研究方面,开展重金属、农残、黄曲霉素等安全性指标研究。 5.在生产装备与制备关键技术研究方面,应用现代[url=http://www.pharmacy.hc360.com/]制药[/url]技术,实现了数字化和在线控制自动化。 6.在疗效研究方面,开展分煎、合煎临床疗效比较研究,药效学比较研究。江阴天江药业先后开展了20个经典方的分煎和合煎临床疗效比较研究,42个药效学比较实验研究,结果显示中药配方颗粒疗效与汤剂基本一致。在安全性方面,临床使用18年10多亿人次,实践证明配方颗粒是安全的。 中药配方颗粒国际组织标准研制取得新进展 国家科技部“十一五”支撑计划中设立了“关键技术标准推进工程”重点专项,中[url=http://www.pharmacy.hc360.com/]医药[/url]作为我国最具国际相对优势的领域,被纳入标准专项予以支持。中药配方颗粒国际标准研制作为“中医药领域重要基础国际标准研制”课题的主要研究内容,由世界中联、江阴天江药业有限公司、广东一方制药有限公司、北京康仁堂药业有限公司、南宁培力药业有限公司等单位的专业人员承担。 该课题自2009年3月启动以来,研究进展顺利。 1.确定了常用中药配方颗粒的遴选原则和300味中药品种。 遴选原则是:常用品种;[url=http://info.pharmacy.hc360.com/zt/yaodian/index.shtml]药典[/url]收载品种;列为基本药物目录;炮制品如不能区别,只选生品;优先考虑试点企业统一的50个品种及国家中医药管理局100个专属性鉴别品种。 2.确定了标准条目设定。 在“术语与定义”项,对中药配方颗粒、薄层色谱法、薄层色谱法、粒度测定法、水分测定法、溶化性、微生物限度检查法、重金属及有害元素测定法、有机氯农药残留量测定法、高效液相色谱法等重要术语概念进行了界定和解释。 在每味中药配方颗粒之下,规定了品名、来源、性状、鉴别、检查、含量测定、功能与主治、用法与用量、注意、规格、贮藏、有效期等12项。其中“检查”项包括:常规检查(粒度、水分、溶化性、装量、微生物限度)、安全性检查(重金属、农药残留检查方法及指标)。 3.完成《中药配方颗粒国际组织标准(草案)》的起草工作。 目前正进入“征求意见阶段”,拟在广泛听取专家意见和建议的基础上,进一步修订。按照世界中联《标准制定和发布工作规范》要求,形成报批稿,报送世界中联理事会审议。
中新网1月20日电 据食品药品监管总局网站消息,食药监总局日前发布关于16批次药品不合格的通告,成都地奥集团天府药业股份有限公司生产的批号为151208的沉香化气丸,以及河南省百泉制药有限公司生产的批号为140201的小儿泻速停颗粒等药品上榜。通告称,经云南省食品药品检验所等7家药品检验机构检验,标示为山西康威制药有限责任公司等11家药品生产企业生产的白带丸等16批次药品不合格。现将相关情况通告如下:一、不合格产品的标示生产企业、药品品名和生产批号为:山西康威制药有限责任公司和山东孔圣堂制药有限公司生产的批号分别为4140303和15050100的白带丸,成都地奥集团天府药业股份有限公司生产的批号为151208的沉香化气丸,山东临清华威药业有限公司和华润三九(临清)药业有限公司生产的批号分别为14031902、14061702、14082301和15050101的磁朱丸,国药集团三益药业(芜湖)有限公司和上海通用药业股份有限公司委托上海世康特制药有限公司生产的批号分别为160302、160401、160501和150503、150401的醋酸氟轻松冰片乳膏,上海旭东海普药业有限公司生产的批号为140301的辅酶Q10胶囊,锦州本天药业有限公司生产的批号为150213的蒲地蓝消炎片,河南省百泉制药有限公司生产的批号为140201的小儿泻速停颗粒,四川省三星堆制药有限公司生产的批号为151211的炎可宁片。不合格项目包括性状、含量测定,以及检查项下的细菌数、装量差异、溶散时限、有关物质、重量差异等(详见附件)。二、对上述不合格药品,山西、辽宁等省(区、市)食品药品监督管理局已采取查封扣押等控制措施,要求企业暂停销售使用、召回产品。国家食品药品监督管理总局要求生产企业所在地的省(区、市)食品药品监督管理局对上述企业依据《中华人民共和国药品管理法》等规定立案调查,依法处理;并责令生产企业彻查原因,彻底整改;相关情况及时向社会公开。
[B]看到圈子里面这一个话题:[/B]引用0楼 wind_61于2010-1-10 10:15:31的回复:--------------------------------------------------------------------------------中药配方颗粒是以符合炮制规范的中药饮片为原料,经现代工业提取、浓缩、干燥、制粒而成的系列中药产品。它既保持了原中药饮片的药效、药性,可供中医临床辨证施治、随证加减,又具有不需煎煮、直接冲服、服用量少、疗效确切、卫生安全等优点。根据《药品管理法》的有关规定,为推进中药饮片实施批准文号管理,规范中药配方 颗粒的试点研究,中药配方颗粒将从2001年12月1日起纳入中药饮片管理范畴,实行批 准文号管理。在未启动实施批准文号管理前仍属科学研究阶段,该阶段采取选择试点企业 研究、生产,试点临床医院使用。试点生产企业、品种、临床医院的选择将在全国范围内进行。试点结束后,中药配方颗粒的申报及生产管理将另行规定。全国试点生产企业有一方、三九、新绿色、首创、江阴等。 --------------------------------------------------------------------------------[B][color=#00008B]你是如何看待中药配方颗粒?你看好它吗?[/color][/B]
现在在医院,出现了便捷的中药配方颗粒,但是做为制剂,大家应该都明白里面是添加了辅料的,中药配方颗粒和中药材的剂量换算,能够完全按照包装上说明的那样来换算使用吗?
水溶性颗粒剂的制备方法一、水溶性颗粒剂的制备方法提取方法因中药含有效成分的不同及对颗粒剂溶解性的要求不同,应采用不同的溶剂和方法进行提取。多数药物用煎煮法提取,也有用渗漉法、浸渍法及回流法提取。含挥发油的药材还可用“双提法”。1.煎煮法系将药材加水煎煮取汁的方法。一般操作过程如下:取药材,适当地切碎或粉碎,置适宜煎煮容器中,加适量水使浸没药材,浸泡适宜时间后,加热至沸,浸出一定时间,分离煎出液,药渣依法煎出2-3次,收集各煎出液,离心分离或沉降滤过后,低温浓缩至规定浓度.稠膏的比重一般热测(80-90℃)为1.30-1.35。为了减少颗粒剂的服用量和引湿性.常采用水煮醇沉淀法,即将水煎煮液蒸发至一定浓度(一般比重为1:1左右),冷后加入1-2倍置的乙醇,充分混匀.放置过夜,使其沉淀,次日取其上清液(必要时滤过),沉淀物用少量50%-60%乙醇洗净,洗液与滤液合并,减压回收乙醇后,待浓缩至一定浓度时移置放冷处(或加一定量水.混匀)静置一定时间,使沉淀完全,率过,滤液低温蒸发至稠膏状。煎煮法适用于有效成分能溶于水,且对湿、热均较稳定的药材。煎煮法为目前颗粒剂生产中最常用方法,除醇溶性药物外,所有颗粒剂药物的提取和制稠膏均用此法。2.浸渍法系将药材用适当的溶剂在常温或温热条件下浸泡,使有效成分浸出的一种方法。其操作方法如下:将药材粉碎成粗末或切成饮片,置于有盖容器中,加入规定量的溶剂后密封,搅拌或振荡,浸渍3-5天或规定时间,使有效成分充分浸出,倾取上清液,滤过,压榨残液渲,合并滤液和压榨液,静止24小时,滤过即得。浸渍法适宜于带粘性、无组织结构、新鲜及易于膨胀的药材的浸取,尤其适用于有效成分遇热易挥发或易破坏的药材。但是具有操作用期长,浸出溶剂用量较大,且往往浸出效率差,不易完全程出等缺点。3.渗漉法系将经过适宜加工后的药材粉末装于渗漉器内,浸出溶剂从渗漉器上部添加,溶剂渗过药材层往下流动过程中浸出的方法。其一般操作方法如下:进行渗漉前,先将药材粉末放在有盖容器内,再加入药材量60%-70%的浸出溶剂均匀润湿后,密闭,放置15分钟至数小时,使药材充分膨胀以免在渗漉筒内膨胀。取适量脱脂棉,用浸出液湿润后,轻轻垫铺在渗漉筒的底部,然后将已润湿膨胀的药粉分次装人渗漉筒中,每次投入后均匀压平。松紧程度根据药材及浸出溶剂而定。装完后.用滤纸或纱布将上面覆盖,并加一些玻璃珠或石块之类的重物,以防加溶剂时药粉浮起;操作时.先打开渗漉筒浸出液出口之活塞,从上部缓缓加入溶剂至高出药粉数厘米,加盖放置浸渍24-48小时,使溶剂充分渗透扩散。渗漉时,溶剂渗入药材的细胞中溶解大量的可溶性物质之后,浓度增高,比重增大而向下移动,上层的浸出溶剂或较稀浸出溶煤置换其位置,造成良好的细胞壁内外浓度差。渗漉法浸出效果及提取程度均优于浸渍法。渗漉法对药材粒度及工艺条件的要求较高,一般渗漉液流出速度以1kg药材计算,慢速浸出以1—3ml/min为宜;快速浸出以3—5ml/min为宜。渗漉过程中,随时补充溶剂,使药材中有效成分充分浸出。浸出溶剂的用量一般为1:4—8(药材粉末:浸出溶剂)。4.其它(1)动态温浸工艺:将原药材破碎到规定粒度.使药材与溶媒有效接触面积扩大.在适当的温度范围内保持恒温;用机械搅拌促进流动,实现药材界面内外浓度差,有利于有效成分快速浸提,而低温温浸,药液不沸腾,避免了淀粉的过分裂解糊化.既方便了固液分离和离心除杂,又避免了水蒸气共沸蒸馏成分的损失。因此,动态温浸工艺与传统的静态沸腾提取工艺相比,具有提取效率高,保存有效成分多,缩短工时,降低耗能等优点。(2)超速离心除杂与超滤除杂技术:与传统的醇醉沉除杂工艺相比,超速离心与超滤(采用微孔滤膜,经加压滤过)除杂技术,避免了具有免疫调节作用的多糖和肽类成分的损失,天然成分保留较完全,既使中药汤剂的特色得到发挥,同时又缩小了剂量,制得的颗粒质量高.稳定性好”。(二)浓缩、干燥技术药材中指标成分提提取后,制成原颗粒之前应得到流动性粉末为宜,因此提取液必须浓缩与干燥,需要一定温度除去水,伴随有效成分的损失与破坏。如长瓣金莲花的水煎液常压浓缩1小时、16小时及26小时,总黄酮含量分别降低6.25%、20%及39%,时间越长有效成分破坏越多。又如采用常压浓缩或减压浓缩制备三黄泻心汤干浸膏,结果成品中番泻苷、黄芩苷的含量降低了23%-94%,改用逆渗透液缩和喷雾干燥技术,含量仍降低1%—6%,当归芍药汤的汤液作成软膏后.其仓术醇和β-桉醇含量分别只有原药材的0.04%和0.14%。通常浓缩最简易是采用真空度1.33kPa(即10mmHg),温度约40℃即可,若采用薄膜浓缩、离心薄膜浓缩则效率可提高,且可降低对有效成分的影响。浓缩液一般浓缩到20%—50%,进行干燥,喷雾干燥操作简便、速度快,产品细度均匀,干燥过程液滴干燥的实际温度仅35-50℃,在几秒或十几秒钟完成,被干燥物料不致发生过热现象,不耐热或对热不稳定的成分不致破坏,如大黄浓缩液以进风温度20℃、出风温度105℃进行干燥,其番泻苷A几乎不分解,但高于上述温度会分解。大多数中药成分浓缩液的进风温度在110-130℃,出风温度65-80℃,都能喷出流动性好的粉末。近年来,有人认为最佳干燥条件应从控制液温和浸膏粒度大小着手。液滴大小可用激光测定,其原理是激光的折射角能定量地随粒度大小而变化.该平均粒径随着雾化器转速的增加而减小,干浸膏粉末的粒度大小由光学显微镜或库氏测定仪改为精确度高的激光测定,干浸膏粉末粒度和汤液雾滴大小是相互关联的,如庶黄附子细辛汤的干浸膏粉末的粒度比其雾滴直径要小得多。浸膏剂的浓缩与干燥方法很多,最近常用于中药浸膏的浓缩或干燥的新技术有:薄膜浓缩、反渗透法和喷雾干燥、离心喷雾干燥、微波干燥及远红外干燥技术等。现举例说明喷雾干燥与冷冻干燥技术的在中药颗粒剂制备中的应用。1.喷雾干燥与干法制粒工艺该法是将药材浸出液经喷雾干燥制成于浸膏粉,加入辅料.先预压成粗片,然后粉碎成颗粒的一种新工艺。它实现了瞬间干燥,防止了有效成分损失,同时保证了颗粒和性状的均一性,使颗粒具有较稳定的崩解性和溶散性,从而克服了湿法造粒工艺的溶媒残留、变色、储存不稳定等缺点。上海中药制药一厂利用动态水提取和干法制粒工艺,成功地研制出粒度集中、不易粘连的六昧地黄丸(颗粒型)冲剂。2.冷冻浓缩与冷冻干燥技术冷冻浓缩技术是使药液于—5~—20℃低温冷冻,通过不断搅拌使结出冰块成为微粒,然后以离心机除去冰屑而得到浓缩的浸膏。此种超低温浓缩可达到有效成分的高保留率。如桂枝芍药汤中的有效成分桂皮醛,采用冷冻浓缩法可保留该成分为一般真空加热浓缩法的50倍之多。但反潮性强,成本高,未能用于大量生产。小太郎株式会社为了保证成品质量,在生药煎液高真空浓缩后采用冷冻干燥,先降温至—50℃.在高真空下干燥。冷冻浓缩和冷冻干燥技术,可以保证中药挥发性有效成分在生产中不被破坏或损失。
能测定原药经制粒后其流动性,有依据分辨出颗粒流动性的好坏
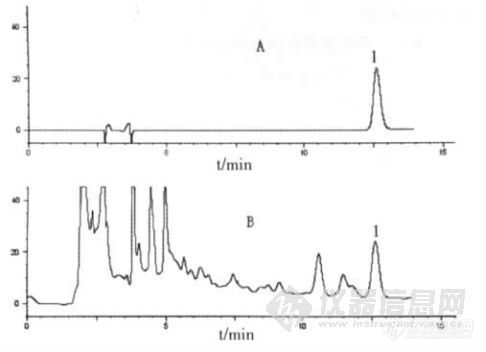
做一味中药复方颗粒制剂的指纹图谱,甲醇溶解的颗粒,A是0.1%磷酸,C是乙腈,D是纯水,用的C18-AQ柱。想问一下,出峰是不是太早了,没有保留啊,该怎么往后调啊?基线不稳是因为梯度变化吗?还有峰太密集了该怎么调啊?恳求各位大佬解答一下[img=,690,517]https://ng1.17img.cn/bbsfiles/images/2022/07/202207111932024713_9166_5606348_3.png[/img][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2022/07/202207111932032184_7030_5606348_3.png[/img][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2022/07/202207111933405270_9075_5606348_3.png[/img][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2022/07/202207111933413164_6798_5606348_3.png[/img]
【作者】 李尔伟; 张超;【机构】 广州市花城制药厂; 广东天之骄药物开发有限公司 510555; 510610;【摘要】 目的 :建立天龙熄风颗粒中天麻素的含量测定方法。方法 :样品经SepPakC18微柱处理后用高效液相色谱法测定。色谱条件 :DiamonsilC18柱 (5 μm ,4 6× 15 0mm)为分析柱 ,甲醇 磷酸盐溶液 (7∶93)为流动相 ,检测波长为 2 70nm ;流速 1ml/min ;结果 :天麻素的平均回收率为 98 2 % ,RSD =2 1(n =5 )。结论 :用SepPakC18微柱固相萃取法代替传统的回流、提取的预处理 ,用高效液相色谱法测定天麻素含量 ,可用于天龙熄风颗粒的质量控制。 更多还原【关键词】 天龙熄风颗粒; 天麻素; 高效液相色谱;
薄层色谱鉴别是中药配方颗粒的主要鉴别方法。由于中药配方颗粒的制备工艺是由药材经水提、浓缩、干燥、制粒而成,为保证对照药材与样品薄层色谱斑点的对应性,对照药材也应尽量先用水煎煮,得到的水溶液再照样品的制备方法处理。但部分品种标准中规定的对照药材前处理方法缺少水煎煮提取的步骤,如板蓝根配方颗粒,标准中规定取板蓝根对照药材直接用稀乙醇提取浓缩点样。此外,炮制品种的薄层色谱,大多使用未经炮制的原药材作为对照药材,上述情况均有可能导致样品斑点与对照药材的斑点不完全一致,给结果判定造成障碍。此外,还有部分品种的薄层方法需要优化,如蜜百部(对叶百部)配方颗粒使用的显色剂是改良碘化铋钾试液,试验中喷该显色剂后对照药材和样品均未出现斑点,改为喷碘化铋钾试液后,斑点出现;黄柏配方颗粒的薄层展开剂含水,斑点展开效果较差,且在日光下观察,斑点信息较少,建议参考《中华人民共和国药典》2020年版第一部中大补阴丸鉴别的方法对该项目进行修订。

作者:曾中强(怀化市中医院药剂科,湖南怀化,418000)摘要: 目的:建立高效液相色谱法测定益母草药材及其颗粒制剂中水苏碱含量的方法.方法:色谱柱为Diamonsil C18(4.6mm×250mm);流动相为甲醇-0.05mol/L磷酸二氢钾溶液(70:30);检测波长210 nm,柱温25℃,流速1.0mL/min.结果:益母草药材及其制剂中水苏碱的保留时间均为15.1 min,色谱峰分离良好,对照品水苏碱线性范围为1.01~30.39 ug/mL(R2=O.9997,n=5),方法回收率为100.1%,RSD为1.03%。结论:该法可用于益母草流浸膏中及其颗粒制剂中水苏碱的含量测定,可以用来对提取物及相关制剂进行质量控制。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208071358_382237_1609970_3.jpg
大家有谁知道农药颗粒剂的物理指标:分散时间测定方法?目前本人只查到分散性的测定方法有人知道的请指教!
[align=center][size=24px][b]中药颗粒剂矫味剂如何筛选 [/b][/size][/align][align=left][font=宋体][size=14px] [b]由于xx中药颗粒剂中含有黄芩等味苦药材,处方去除蔗糖后产品口感较苦,为保证口感就需重新选择矫味剂,无糖型颗粒是颗粒剂发展的大趋势,常用的无糖[/b][/size][/font][b][font=宋体]型矫味剂主要有甜蜜[/font][font=宋体][font=宋体]素、甜菊素、安赛蜜、木糖醇等,其中木糖醇由于甜度小,用量较大,会导致最终服用量增加,而甜蜜素、安赛蜜为化学合成甜味剂,存在[/font][/font][font=宋体][font=宋体]一定安全风险,故本制剂选择天然甜味剂甜菊苷作矫味剂,甜度高、用量少,尤其适用于糖尿病等限糖患者服用。[/font][/font][font=宋体][font=宋体]稀释剂的选择[/font] [font=宋体]蔗糖、糊精是传统的中药制剂稀[/font][/font][font=宋体][font=宋体]释剂,原制剂中这两种辅料均有使[/font][/font][font=宋体]用,作为无糖制剂,蔗糖糖需被其他矫味剂替代,仅保留糊精作为稀释剂,并重新调整清膏和糊精比例,确定最优配比。[/font][/b][/align] [font=宋体][font=宋体] [b] 制剂成型工艺是将药物半成品与辅料进行加工处理,制成剂型,形成最终产品的过程。在制备工艺的研究中,发现影响颗粒成型效果的主要因素有:清膏与稀[/b][/font][/font][font=宋体][font=宋体][b]释剂的比例、矫味剂的含量(甜菊素[/b][/font][font=宋体][b]/清[/b][/font][/font][font=宋体][font=宋体][b]膏),因此将这2种因素分别进行考察,每个因素选取3个水平,设计实验筛选最佳原辅料配比。[/b][/font][/font] [font=宋体][font=宋体][b] 实验结果表明,清膏与糊精的用量比例为[/b][/font][font=宋体][b]1:2,甜菊素用量为清膏的2/100,成型效果很好,甜味适当。 其因素水平表和实验结果见下表: [/b] [img=,656,535]https://ng1.17img.cn/bbsfiles/images/2024/09/202409122247184165_6276_2204446_3.png!w656x535.jpg[/img] [b] 总结[/b][/font][/font] [font=宋体][font=宋体][font=宋体] [b]因甜菊素的代谢不需要胰岛素参与,糖尿病患者及其他禁糖患者可安全服用;同时[/b][/font][font=宋体][b]原来的提取和成型工艺均未改变,对药物的吸收、利用不会产生明显影[/b][/font][/font][/font][font=宋体][font=宋体][font=宋体][b]响,也不会引起安全性、有效性的明显改变。[/b][/font][/font][/font] [font=宋体][font=宋体] [/font][/font]
目前,许多地方已根据政府工作报告中提出的“推进燃煤电厂低浓度排放改造”要求,确定了相关规定,明确颗粒物排放不得高于 10 mg/m3,某些省份规定不得高于 5 mg/m3。那么有必要要针对低浓度颗粒物测定制定一个新的测试方法标准吗?
动态颗粒图像分析仪的研制摘要:本文论证了研制动态颗粒图像分析仪的必要性与背景, 介绍了winner100实现动态颗粒测试的方法以及技术特征。评价了动态颗粒图像分析仪的实用价值与科学意义。关键词.. 动态颗粒, 图像分析, 粒度与形状,3 维一、问题的提出颗粒是组成材料的基本单元, 影响材料的性能的不仅是颗粒的化学组成, 颗粒的大小与颗粒的形态对材料的性能影响巨大, 因此颗粒粒度与形态的检测越来越受到各行业的重视。目前检测颗粒大小和颗粒形态的方法有多种,激光粒度分析仪、沉降粒度仪、电阻法粒度亦、颗粒图像分析技术是最常用的技术。激光粒度分析仪、沉降粒度仪、电阻法粒度仪, 只能检测颗粒大小, 不能检测颗粒形状;颗粒图像分析技术是一种不仅可以检测颗粒大小也可以检测颗粒形状对唯一方法, 但是由于此种技术有几个致命的缺点限制了它的进一步发展:1.样品制备困难。颗粒在载玻片上很难得到充分的分散, 由于颗粒粘连使得颗粒分析的准确性大受影响; 2.颗粒处于静态, 非球形颗粒的取向会对测试结果造成偏离;3.由于显微镜的视场有限, 被测得颗粒数目受到很大限制, 因此取样的代表性差, 重复性不好。由于以上问题, 颗粒测试中急需一种性能更加优越的测试装置, 能够获得颗粒的准确图像, 操作简便, 满足颗粒形状和颗粒粒度分析的更高要求。国际上荷兰安米德公司、德国新帕泰克公司、德国莱驰公司均推出了同时测定颗粒粒与形状的图像分析仪。国内尚无此种产品, 济南微纳公司通过3年的攻关研制的winner100 颗粒图像分析仪填补了此项空白。二、动态颗粒测试的方法与技术特征Winner100突破了传统的颗粒图像仪的工作模式, 采用超声样品分散系统分散颗粒, 高速摄像头对动态颗粒图像进行采集, 1微秒可以采集一幅颗粒图像, 用计算机对图像进行分析处理, 达到对颗粒粒度与形态进行三维同时测试的目的。其主要技术特征有:1.彻底改变了手工制样操作繁琐的局面, 样品制备操作非常简单, 分散效果好; 2.采用功能强大的动态颗粒图像分析软件, 具有高速采样、自动颗粒图像处理, 实时显示当前图像、实时分析粒度分布、连续统计分析结果, 处理策略自行编程, 多种粒径定义选择, 粒度统计、形状分析等多种功能。打印报告允许自行编辑。3.动态测试使颗粒采样数量无限增加, 统计结果真实可靠, 代表性好、重复性高;4.动态测试使颗粒不同侧面得到采样, 实现了三维测试, 彻底消除了二维测试的颗粒取向误差;粒度测试结果可以与激光粒度分析仪比美。5.winner100动态图像分析专用软件具有强大的图像处理功能;6.支持多种粒径选择和多种粒度分布, 具有多种图像处理功能及其集成处理, 支持图像采集间隔设定与实时显示颗粒形貌与当时粒度分布和累计粒度分布, 记录并显示粒度波动图, 可以输出多种分析图表, 高性能的软件使使用者的颗粒分析工作变得十分轻松方便。7.本成果不仅可用于实验室颗粒分析, 也适用于颗粒在线粒度与粒形监测。对杜会经济发展和科学进步的意义本项目突破了显微静态图像分析的局限, 在国内率先提出动态颗粒图像分析的概念;由于颗粒运动中测试, 克服了二维颗粒图像分析的弊病, 大大提高了采样代表性, 消除了颗粒取向误差, 使颗粒粘连问题彻底解决。本项成果克服了静态颗粒图像仪的缺陷, 提供了一种对运动颗粒同时进行粒度与形状分析的先进手段, 具有操作简单, 测试范围广, 代表性好, 准确可靠, 直观可视, 适用于1-6000微米的各种固体颗粒。可以广泛应用于建材、化工、石油、金属与非金属、环保、轻工、国防等众多领域的实验室和在线颗粒粒度与形状分析。无疑, 对于提高我国各行业颗粒测试水平和经济发展具有重要的实用价值。颗粒测试的基础是颗粒的表征, 本项成果提供了一种颗粒动态测试的实用手段, 因此颗粒的三维表征问题就提到了议事日程上来, 颗粒的三维表征对颗粒学的进步与发展具有重要的意义。[color=blac
中药配方颗粒试点生产企业的垄断局面正在被打破。 安徽亳州市安徽济人药业有限公司已于2011年底获得安徽省中药配方颗粒试点生产企业资质,并正在申请成为国家试点生产企业,有望于明年年初获批。吉林敖东亦透露旗下力源药业已于2011年8月获得吉林省中药配方颗粒试点生产企业资质,并将在合适时机申请国家试点生产企业资质。这些现状显示多家企业相继获得省内中药配方颗粒试点生产资质,意味着此前对于中药配方颗粒试点生产的垄断格局正在被打破。中药配方颗粒管理一直从严“我们公司早在2011年年底就获得了安徽省中药配方颗粒试点生产企业资质,目前正在申请国家试点生产企业资质。”12月11日,位于“中药之都”安徽亳州的安徽济人药业有限公司称这一申请最快将在2013年年初取得结果,并且很有希望获得批准。就在昨日,吉林敖东亦透露早在2011年8月份,吉林省药监局发布了 ,确定将旗下力源药业作为吉林省中药配方颗粒研究生产试点单位,进行中药配方颗粒的研究生产。据吉林敖东证券事务部人士称,力源药业会在合适的时候积极争取国家试点企业的资质。中国中药协会一位人士表示,2001年7月,原国家药品监督管理局颁发 ,明确将中药配方颗粒纳入中药饮片管理的范畴。此后,对中药配方颗粒试点生产企业资质的管控一直处于从严管控状况,仅有6家企业先后获得这一资质。国际标准已获得通过资料显示,实施以来,相继获得国家试点生产企业资质的6家企业分别为:上海家化子公司江阴天江药业、红日药业子公司康仁堂、华润三九、培力(南宁)药业有限公司以及四川绿色药业科技发展股份有限公司。济人药业前述负责人表示,“中药有500亿元左右的销售额。如果其中有60%的市场转化成60%的中药颗粒的份额,体量都非常大,而现在6家企业只做到了30多亿元的销售额,所以短期内一两家企业的介入不会改变当前的市场格局。”上述中国中药协会人士则表示,2011年4月,由世界中医药学会联合会牵头制定的中药配方颗粒国际标准获得通过,规定了300味中药配方颗粒的药品名称、来源、炮制、性状、重金属限度检查、农药残留限度检查、功能主治、用法用量等项目。“但目前主要起的还是指导作用,没有得到真正意义上的推行。”
颗粒状农药粉尘测定方法有哪些?有没有相应的国标?
中药配方颗粒特征/指纹图谱的分析难度相对较大。第一是超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url](Ultra Performance Liquid Chromatography,UPLC)方法的耐用性不佳,色谱柱型号和色谱仪品牌对分离效果有较大影响。如百部/蜜百部(对叶百部)配方颗粒,使用标准正文中对照特征图谱下标注的参考色谱柱,能得到色谱行为与标准图谱相似的色谱图,但此前尝试使用3种其他型号相似规格的色谱柱,均未能达到理想的分离。而山萸肉/酒萸肉配方颗粒、北柴胡配方颗粒等品种使用参考色谱柱得到的色谱图却很不理想,更换其他型号的色谱柱后才得到与对照图谱类似的色谱图。另外,由于不同品牌色谱仪的死体积与泵混合差异,在小流量梯度洗脱时色谱仪品牌对色谱行为有非常大的影响,如葛根配方颗粒、蛇床子配方颗粒和大黄配方颗粒,使用某品牌超高压[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url]的分离效果较差,更换另一品牌仪器后,试验结果较为理想。第二是部分品种对照药材的前处理方法与样品前处理方法不完全一致,不能很好地起到随行对照的作用。如苦杏仁(西伯利亚杏)配方颗粒,对照药材直接水煎煮过滤后进样,而样品采用50%甲醇提取,如此制备的对照药材溶液浑浊,且色谱峰峰形不好;防风配方颗粒对照药材直接用50%甲醇提取,缺少水煎煮过程,而样品是用甲醇提取,结果对照药材色谱图中峰5不符合标准规定,建议统一对照药材和样品的前处理方法。第三是缺少法定对照物质。少数炮制品种使用了相应的“对照饮片”为随行对照,如炒桃仁/ 桃仁配方颗粒使用炒桃仁/ 桃仁对照饮片和麸炒苍术配方颗粒使用麸炒苍术对照饮片,但目前尚无法定对照物质的发行,导致相应品种无法全检;白芍配方颗粒中使用的1,2,3,4,6-五没食子酰葡萄糖和苯甲酰芍药苷对照品,黄芪(蒙古黄芪)配方颗粒使用的黄芪皂苷Ⅰ和黄芪皂苷Ⅱ对照品也无法定对照物质,检验中使用第三方提供的标准物质,质量和可及性无法保证。
【作者】:杨立平【摘要】:目的: 建立阿归养血颗粒中芍药苷的含量测定方法。方法: 采用高效液相法测定阿归养血颗粒中芍药苷含量, 色谱柱 : Diamonsil C18( 4.6 mm×250 mm, 5 μm) ; 流动相: 乙腈- 0.05%磷酸( 16∶84) ; 检测波长: 230 nm; 流速: 1 mL/min。结果: 芍药苷在92.5- 740 ng范围内线性关系良好, 平均回收率为99.32%。结论: 该方法简便可行、重复性好, 可作为阿归养血颗粒质量评价的依据。【作者单位】:湖南省肿瘤医院【关键词】: 阿归养血颗粒; 高效液相色谱法; 芍药苷http://ng1.17img.cn/bbsfiles/images/2012/07/201207311302_380825_1838299_3.jpg
[center]嘉应制药受让金沙药业35%股权[/center]嘉应制药今天公告,12月5日,公司与陈鸿金、林少贤、颜振基、陈磊等自然人(下称“联合竞拍方”),参加由天津产权交易市场组织的关于受让湖南金沙药业股份有限公司股权的拍卖会,以5760万元竞得湖南金沙药业控股有限公司所持金沙药业73%的股权,以640万元竞得深圳市白沙物流有限公司所持8.1%金沙药业的股权。联合竞拍方以1304万元受让金沙药业高管张衡、文化、杨旭昌所持有的合计16.5%股权。 根据嘉应制药与联合竞拍方的竞拍结果和事前协议安排,嘉应制药将支付约计2800万元对价款,取得金沙药业35.52%的股权。 金沙药业主营为生产销售片剂、颗粒剂、硬胶囊剂。嘉应制药认为,金沙药业在主营业务方面存在一些优势,竞拍成功将有利于嘉应制药进一步提升综合竞争实力。信息来源:医药新闻网
2015版药典新增和修订了多种药品的HPLC检测方法。针对这些提高和修订,默克密理博应用实验室发出了一系列的应用方法,帮助客户以最快速度满足药典的技术要求。当归调经颗粒的修订涉及当归调经颗粒中的芍药苷含量测定。默克应用实验室根据2015版药典对这些检测项目的技术要求,推出了完全符合药典要求的解决方案。方案细节请见附件。
[color=#333333]环境保护部近日印发《固定污染源废气 低浓度颗粒物的测定 重量法》(HJ836-2017)国家环境保护标准,环境监测司负责人就相关问题回答了记者提问。[/color][color=#333333][/color][hr/]问:为什么要针对低浓度颗粒物测定制定一个新标准,原先的方法标准有哪些不适用的地方?[color=#333333]答:我国正在大力推进燃煤电厂低浓度排放改造,要求改造后的颗粒物排放浓度不大于5mg/m3,而现行的颗粒物监测标准方法《固定污染源排气中颗粒物测定与气态污染物采样方法》(GB/T 16157-1996),在颗粒物浓度较低、烟气湿度较大的情况下,监测结果准确度相对较差,主要原因一是沉积在采样嘴及采样管前段的颗粒物无法回收,造成监测结果偏低;二是在烟气湿度较大的情况下,长时间采样容易造成滤筒受潮破损,影响颗粒物测试的准确度。为解决上述问题,满足现行污染源排放的监测需求,特制定本标准。同时在《固定污染源排气中颗粒物测定与气态污染物采样方法》(GB/T 16157-1996)修改单中规定:当测定固定污染源排气中颗粒物浓度时,浓度小于等于20 mg/m3时,适用HJ 836(《固定污染源废气 低浓度颗粒物的测定重量法》);浓度大于20mg/m3且不超过50mg/m3时,与HJ 836同时适用。[/color][color=#333333][/color][hr/]问:低浓度颗粒物方法标准的技术路线和GB/T 16157-1996的区别是什么?[color=#333333]答:GB/T 16157-1996采用干燥皿冷却,并只称量采样滤筒。而本标准则采用恒温恒湿平衡—整体称重,恒温恒湿平衡,就是样品在采样前后要在统一的温湿度状况下平衡稳定后称量,与GB/T 16157-1996相比,恒温恒湿平衡可以有效减少称量波动,提高称量的稳定性;整体称重,就是将滤膜封装在采样头内采样,并将采样头整体进行称量,这种方式能有效避免滤膜破损,并保证沉积在采样嘴及采样管前段的样品得到回收,提高了测定的准确度。[/color][color=#333333][/color][hr/]问:如何保证低浓度测定结果的准确性?[color=#333333]答:在低浓度颗粒物监测过程中,样品污染会引起较大的监测误差,本标准引入了“全程序空白”质控要求,可判断样品在测定过程中是否受到污染。“全程序空白”指除采样过程中采样嘴背对气流不采集废气外,其他操作与实际样品操作完全相同获得的样品。标准规定,任何低于全程序空白增重的样品均无效。[/color][color=#333333]本标准对采样准备、布点、采样、运输、预处理和称量等各个环节的质量控制提出了更为严格的要求,提高了测定结果的准确性。[/color][color=#333333]以上内容来自于:中国环境报[/color]
目录 一.概述 二.验证目的 三.验证小组组成 四.清洗方法及检测方法 五.取样方法检测方法及残留量的计算 六.检测结果 七.偏差及变更的处理 八.验证结论 九.再验证 十.验证结果 一. 概述 204车间无菌精烘包内生产的是环磷酰胺,其设备均为专用设备,为了防止批与批之间的污染,特制定204车间无菌精烘包摇摆式颗粒机的清洗验证报告。 二.验证目的 1) 为摇摆式颗粒机清洗程序的建立提供依据。 2) 证明该清洗方法充分有效。 3) 摇摆式颗粒机清洗后,残留物符合生产下一批要求。 三.验证小组组成 组成 部门/姓名 工作内容 组长: 验证报告批准 组员: 验证报告审核 组员: 验证报告起草 组员: 验证实施过程中的监督,管理 四.清洗及检测方法 清洗方法:将摇摆式颗粒机的过筛部分取下,送至洗涤间,用注射用水反复冲洗,直至目视无残留。再用注射用水冲洗1分钟,倒扣在架子上晾3分钟。 检测方法:以注射用水润湿棉球擦拭摇摆式颗粒机加料斗面积25 cm2。擦拭棉球以注射用水分三次萃取,萃取液以注射用水稀至50ml。 进行外观检查和HPLC检查。
[font=宋体]中药配方颗粒是现代化的中药形式,类似于中药的速溶咖啡,方便快捷。[/font][font=宋体][/font][font=宋体] [/font][font=宋体]但是,由于一些中药配方颗粒还没有统一的标准,目前只有大约200种规定,并且还有一些地方标准。[/font][font=宋体][/font][font=宋体] [/font][font=宋体]这些规定的中药种类并不足以涵盖临床需要的400多种中药,所以医生在开处方时可能会发现缺少一些需要的中药种类,这就限制了中医药在临床上的应用。[/font][font=宋体][/font][font=宋体] [/font][font=宋体]1.[/font][b][font=宋体]认为中药饮片汤剂效果更好:[/font][font=宋体][/font][/b][font=宋体]中药饮片汤剂就是把一些中草药放在一起煎煮,这样可以让药物的功效更好。[/font][font=宋体][/font][font=宋体] [/font][font=宋体]比如,一起煎煮能够增强药物的治疗效果,让药物更容易被身体吸收,而且还可以降低药物的毒性。比方说,大黄、甘草和黄连、黄柏煎在一起,能够减轻药物的苦味。[/font][font=宋体][/font][font=宋体] [/font][font=宋体]但是,中药配方颗粒就不同了,它是把每种草药分别装在小包里,倒在一起搅拌溶解喝下去,不会有像“合煎”那样增效的作用。比如一起溶解,药物的味道也不会有太大变化。[/font][font=宋体][/font][font=宋体] [/font][font=宋体]总的来说,中药饮片通过“合煎”可以让药物一起配合起来,发挥更好的治疗效果。而中药配方颗粒则没有这个好处,不会影响药物的功效。[/font][font=宋体][/font][font=宋体] [/font][font=宋体]2.[/font][b][font=宋体]认为中药配方颗粒效果更好:[/font][font=宋体][/font][/b][font=宋体][size=12px][color=#000000]中药配方颗粒临床研究有效率和治愈率的随机对照试验Meta分析结果显示,从7个常见的比较类型来看,中药配方颗粒在纳入的研究中不论是痊愈率还是有效率要高于西医常规治疗 [/color][/size][/font][font=宋体][color=#000000][/color][/font][font=宋体][color=#000000] [/color][/font][b][font=宋体]在西医常规治疗的基础上配方颗粒的疗效更佳 与中成药比较,疗效要优于中成药 与汤药比较,疗效有微弱的优势,可能与依从性有关 与安慰剂比较,疗效约为安慰剂的1.5倍 与中医非药物疗法比较,疗效也显示出优势。综上,中药配方颗粒的临床疗效较好。[/font][/b][font=宋体]小结:[/font][font=宋体]中药配方颗粒不是对中药饮片的替代,而是在临床应用上给医生和患者多一种选择[/font][font=宋体]。[/font]

作者:陈静; 谷铁波; 陈贵平;(湘潭市第一人民医院药剂科; 福寿堂制药有限公司;)摘要:目的建立复方羊角颗粒中欧前胡素的含量测定方法。方法采用高效液相色谱法。色谱柱为Diamonsil C18柱(200 mm×4.6 mm,5μm);流动相为甲醇-水(65∶35);检测波长为248 nm;流速为1.00 mL.min-1。结果欧前胡素进样量在0.010 6~0.095 4μg与其峰面积值呈良好的线性关系(r=0.999 8),平均加样回收率为99.1%。RSD为0.8%。结论该方法操作简便,结果准确可靠,可用于复方羊角颗粒的质量控制。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208061101_381743_1606903_3.jpg
【序号】:1【作者】:宓英其【题名】:壳聚糖季铵盐基载药纳米颗粒的制备及抗肿瘤活性研究【期刊】:中国科学院大学(中国科学院烟台海岸带研究所)【年、卷、期、起止页码】:2021【全文链接】:https://kns.cnki.net/kcms2/article/abstract?v=3uoqIhG8C447WN1SO36whFuPQ0yKi4pXSQlJ_W8wBD9JRPlAs_d8B08_Rb1JUznAFb2v97acEb09IrgYlNXMTwfPMLqRO91a&uniplatform=NZKPT
2013年4月16日 ,由默克密理博主办的制药高峰论坛在上海龙之梦万丽酒店成功召开。默克集团化工董事会成员,默克化工集团首席执行官伯纳德-雷克曼(Bernd Reckmann)先生出席了论坛并致开幕辞。共有250余位来自制药行业的专家,学者和企业代表参与了此次论坛。 http://blog.merckmilliporechina.com/editor/upload/image/1B0A18F3_C6F48447.png 药品安全已经成为我国当前热议的民生和公共安全话题,在过去的一年中,毒胶囊、工业明胶等事件已经严重的影响了国民的对药品安全体系的信心。同时,药品安全也是我国“十二五规划”中重点关注的领域,“提高国家药品标准、强化药品全过程质量监管、健全药品检测检验体系、提升药品安全检测预警水平”是十二五时期药品安全工作重点。 默克密理博全球副总裁兼大中华区总裁Ray Shin先生为大会作了欢迎辞。随后,Najib Sehat博士简要介绍了美国和欧盟制药行业的监管发展和趋势以及新版《全球化学品统一分类和标签制度》。制药企业如何有效的执行质量管控以避免风险成本,默克密理博微生物监测业务全球总裁Roland Heinrich博士以多年的经验详细的阐述了他的见解。他深刻的指出,美国制药行业出现的质量管控问题有三成都是来自微生物的污染,可见微生物监测在制药行业质控的重要性。来自汤森路透集团的解决方案专家,英国皇家化学会会员李寅博士则从数据分析的角度讲解了对于国内成品制剂生产商的海外市场外贸商机。http://blog.merckmilliporechina.com/editor/upload/image/1B0AC2C6_68E7FC36.png 下午部分的环节分为4个分会场进行。分别是药物分析分论坛,制药风险管理分论坛,化学制药分论坛和生物制药分论坛。涵盖化学制药和生物制药领域,讨论如何通过产品、工艺、法规等全面提高药品安全标准。 全面提高药品安全生产标准,提升药品安全品质,促进医药行业持续健康发展,增强民众的用药信心,是默克密理博致力推动的方向。为此, “2013默克密理博制药高峰论坛”的成功举办将成为一个交流平台,与国内外专家共同探讨制药行业从研发到生产各环节的安全保障解决方案。希望通过我们的不懈努力,与业界同僚精诚合作,共同创造和实现药品的安全生产,为国民安全用药略尽绵薄之力。
写本文的目的主要是充实一下本版的内容!正在整理的还有中药注射剂、片剂、胶囊剂等一些传统的剂型!待整理完毕后会及时送上![color=#dc143c][size=4][font=黑体][center]深度剖析中药颗粒剂的制备过程目录[/center][/font][/size][/color]前言制备方法质量检查注意事项例子目前中药制剂品种参考文献
我国加入世贸组织(WTO),是机遇也是挑战。以制药行业来说产量大、价格低是优势,但出口药品除质量指标以外,还要由进口国或国际公认的机构对该药品的生产过程(包括接触药品的设备)进行检查,符合有关规定和要求方可出口。我国现行实施的规范是国家药品监督局1998年修订的《药品生产质量管理规范》及药品生产管理规范附录。上述规范及附录已由国家经贸委医药行业信息中心于1999年10月汇集于《药品GMP认证》一书中,该书同时收入了《美国现行药品生产质量管理替代规范》(CGMP)1998版和《日本药品生产质量管理规范》1990版。对于制药装备,国家经贸委中国制药装备行业协会也于2000年1月编刊了《制药装备实施GMP指南》,2000年9月上海医药设计院等还在沪召开了“制药机械GMP技术宣讲会”,探讨执行新版本《药品生产质量管理规范》以及实施制药机械GMP评审中心检测等相关事宜,会议的主要内容已经刊行。中国制药设备行业协会又于2001年8月编印了《制药装备实施GMP新技术、新产品信息文集》,文集除收入我国现行GMP文件外,还对制药装备验证、制药用水验证、若干制药及制剂设备对GMP的要求作了阐述。 用于医药生产的各种干燥装置都必须符合GMP(Good Manu facturing Practice缩写)的有关要求,其目的是要保证药品生产质量整批均一,以及不存在积料等。同时各该设备还必须达到可以原位清洗(Cleaning in Place, -CIP)、原位灭菌(Sterilizing in Place, - SIP)要求;对直接接触药品的设备材质也有要求,一般情况下用316不锈钢;进入干燥系统的热空气须经精密过滤,1 m3空气中≥0.5μm的尘埃粒子不得超过3500个,活微生物数1。 1.药品的干燥根据不同的性状和要求,大致可采用下述两类方法:一类是从水溶液直接喷雾干燥成为颗粒,如链霉素、庆大霉素等;另一类是溶液经结晶、过滤后将结晶物进行干燥,对于热敏性药物(如若干生物制剂等)可选用冷冻干燥。那些结构复杂不易清洗或灭菌的干燥形式,则不能应用于药品的干燥。