关于欧洲药典色氨酸有关物质检查的流动相问题,调节ph之前溶液总体积已达1700ml,再用2.9g/L磷酸溶液调节ph到2.3结果倒入400ml左右,才勉强能达到2.3,这是否合理?有人做过这个检查吗,有相关的色谱图可供参考吗?
作为一个新药,对其纯度的检查是保证安全有效的重要指标之一,而纯度检查的内容,根据各个药物的性质和特点有些不同,但基本上均要涉及各自的“有关物质”检查研究。关于有关物质的检查,在国际上已早为“人用药品注册技术规范协调会(ICH)”所关注,国内在新药的有关文件中也提出了供参阅的一些具体要求,并逐渐引起研制新药者的重视。 由于一个新药从合成原料药到制备有关的制剂,再经贮藏、运输、使用,要经历一段较为复杂和漫长的过程,在此期间,每一过程都有可能产生有关的物质,如生产中可能带入起始原料、试剂、中间体、副产物和异构体等;在贮藏和运输过程中,可能产生降解产物、聚合物或晶型转变等特殊杂质。为保证药物的安全有效,同时也要考虑到生产实际情况,因此,国内外对药物的研究,可允许含有一定限量的无害或低毒性的有关物质,但对毒性较大,能危害人体健康的、无效的或能影响药物稳定性的有关物质则必须严格控制。 因有关物质的量微小,故检测方法至关重要,必须选择专属性强、灵敏度高、重复性好的方法。目前,首选的是色谱法,可根据新药的具体品种及其有关物质的性质采用TLC,HPLC及GC等,有的还应采用其他有关的色谱或波谱法。对于一、二类新药更应重视,必要时可采用HPLC/UV二极管阵列、HPLC/MS或GC/MS等联机技术,对有关物质进行定性定量分析。 现将有关物质检查中常见到的一些问题讨论如下。1 未提供研究方法的专属性 申报资料中常见到有关物质检查的结论是“未检出有关物质”,甚至在稳定性各影响因素考察中,样品颜色已明显变化,但其结果仍是“未检出降解产物”,因而提供的TLC图上只有1个斑点,HPLC图上只有1个主药的峰。对于此类情况,应考虑方法的专属性,如采用的是HPLC,则在方法研究中可按中国药典附录的要求,进行系统适用性试验,考察方法的专属性,具体方法有:①如有关物质为已知的某中间体、副产物或降解产物,则可在原料药中加入该杂质适量进行试验,以证明能达到分离;②如有关物质为未知,可用含有杂质的粗品进行试验,以证明能达到分离;③将精制品经强光、高温、高湿、氧化剂或酸碱等分别处理,使样品光解、分解、氧化或水解后进行试验,以证明能分离出杂质。经上述方法试验能分离出杂质,即证明采用的方法具有一定的专属性。2 未提供研究方法的灵敏度 申报资料中,有的把试验的最低浓度作为灵敏度,甚至有的只有文字叙述而无任何数据和图谱,而未提供详细方法学研究资料和图谱来证明该最低浓度为最低检出量。因此,提供的灵敏度缺乏试验依据,不能反映所采用方法的真实检出灵敏度。对此,研究者在研究的方法具有专属性后,应考虑方法的灵敏度。如采用HPLC分析时,一般使最低检出量相当于基线噪音的3倍峰高时注入的样品量;如采用TLC分析时,应将样品配制成一系列的不同浓度,分别点样、展开、显色,以确定灵敏度和最低检出量。3 未提供定性和定量的依据 在申报资料中,除极少数用已知杂质作对照,对样品中有关物质进行定性、定量外,多数强调了制备杂质对照品的困难。因此,对有关物质的定性和定量是用主成分自身对照法或面积归一化法,但因未提供所检测的杂质在设置的检出波长处的响应因子,而不同杂质的的响应因子有可能不同,且差别较大,至使虽有定性和定量结果,但可靠性较差。因此,有关物质定性、定量的最佳方法是采用已知对照品的方法,使所提供的定性和定量有充分依据。4 未提供有关物质的来源及其性质 申报新药中的有关物质,绝大多数为未知,即使其有关物质含量大于2%或一类创新药,也常把在HPLC主峰以外的各杂质峰统归为未知的杂质,而未研究其杂质的来源、性质及其确切的含量。为保证新药应有的纯度,特别是一类新药,对有关物质检查应严格要求,对其主要杂质要确证化学结构,对主要杂质和其他杂质要分别定出限量。5 色谱图记录时间太短或进样量过小 在资料中,有不少HPLC图谱不符合要求,表现在主峰的保留时间记录刚完毕,即停止记录,致使一些比主成分峰保留时间大的有关物质不能检出或进样量过小,杂质检不出。由于有的药物与其有关物质分子结构的极性相差较大,因此,在HPLC分析中,有关物质的保留时间可能在主成分峰之后出现,故记录时间应比主成分峰的保留时间延长2~3倍,并应考虑样品配制浓度或进样量致使主成分峰为一矩形峰,以确保样品中的有关物质能全部检出。6 提供的色谱图不合要求 资料中常见提供的色谱图失真,例如TLC分析提供的是手工绘制的正圆形示意图,或虽是图谱的照片,但无样品点样点,无溶剂前沿,斑点未标示Rf值,样品无批号或文字说明等;HPLC分析中亦有用手工描绘图谱的,有的原图缩得过小以至图上数据模糊不清,或提供的图谱无样品批号,无保留时间,无文字说明,或各峰积分值与列表数据不相吻合等;在稳定性考察降解产物中,上述情况更为严重,致使无法审查。因此,研究者应认真参考新药审批的有关技术指导原则进行试验,提供符合要求的色谱图。7 资料前后缺乏相关性 在有关物质检查研究中,有的用HPLC进行了较深入的方法学研究,以已知中间体或杂质作对照,证明方法较好,专属性较强,但在制订质量标准研究中的图谱却未出现相同的杂峰,而是其他杂质峰,致使样品研究中的有关物质与制订标准中的有关物质不相关,且在资料中对此无说明。对此情况,应进一步深入研究,弄清是产品工艺不稳定带入的其他有关物质,还是产品本身不稳定的降解产物或残留有机溶剂所致,使研究的结果与制订标准的结果一致。8 未说明有关物质的个数及其总量 资料除极少数研究了有关物质的个数和总量,并放入质量标准外,大多数对有关物质的数和量未做精密研究,对有关物质只是笼统的订为不得大于百分之多少,这就难以保证产品的有关物质是否稳定在规定的限度范围内。因此,在研究并确定了有关物质数和量的基础上,应对若干批工艺稳定后的产品进行分析,积累数据,对有关物质订出个数,并对主要有关物质、未知及总的有关物质分别订出限量,以保证产品质量。
螺内酯片有关物质检查有人做过吗?发图看一下
螺内酯片有关物质检查有人做过吗?发图看一下
【摘要】本文针对审评原料药有关物质检查方法中存在的问题,介绍欧洲和英国药典关于原料药已知杂质的研究现状和有关物质方法建立及质量控制,以供申请人参考。【关键词】有关物质、方法学、分离度。 笔者审评原料药有关物质检查方法中发现,大多申请人越来越多地认识到控制原料药有关物质的重要性,自行建立方法考察原料药中存在的有关物质。但在研究中往往片面认为样品通过了破坏性试验和1%自身对照法后的系统适用性试验就符合了要求。因此,忽视对主成分中杂质产生原因的分析,忽视仪器的检测灵敏度的分析、忽略色谱柱(柱效)的选择、流动相及比例的选择、检测波长的选择。忽视主成分和可能产生的杂质分离度的问题。 1、原料药有关物质方法建立应关注的问题:原料药中的杂质来源于合成的中间体、副产物、以及降解产物,建立方法初期,仅采用破坏性试验的方法考察降解产物的做法是片面的。由于降解产物的量较小,如果选择的方法不好,比如,柱效低,波长选择不合理、流动相及流动相比例不合适,即使有降解产物,也达不到有效的灵敏度和有效的分离。因此,一个好的分析方法的建立首要问题应是围绕主成分和杂质的分离度和检测波长进行。对于生产原料药的企业来讲,由于可以通过工艺得到中间体、副产物,在方法建立初始,首先应该将可能的中间体和副产物作为杂质对待,进行柱效、流动相及流动相比例、波长和分离度等方法学的研究。方法建立成熟后,可根据中间体和副产物的安全性和工艺得到的难易程度决定是否固定为已知杂质。如果工艺中难以得到,且比较安全,可考虑采用杂质校正因子加上相对保留时间的方法。或采用杂质相对保留时间加上自身对照方法。上述三种方法均有好的分离度和响应值(灵敏度)作保证。也是研发和审评中应当提倡的。如果原料合成中确实得不到副产物,对于有紫外吸收的样品可以用二极管阵列检测器,考察未精制的粗品,并对比已精制过的样品,确定粗品中各成分的分离度和样品中可能杂质的检测波长。方法确立后,可采用自身对照方法或面积归一化法控制杂质。对于后一方法,在研发和审评中应当慎重选用。如果证明上述四个方法是比较成熟的方法后,如果再加上破坏性试验考察降解产物,其方法就更加完整和适用。 2、介绍欧洲和英国药典控制有关物质关注的问题 欧洲和英国药典的原料药标准后面,大部分都附有可能产生的中间体和副产物的结构,在有关物质质量控制中有些采用已知杂质的方法;有些采用杂质校正因子加上相对保留时间的方法;杂质相对保留时间加上自身对照方法和自身对照方法或面积归一化法。例如:核黄素磷酸钠的有关物质检查就是采用HPLC的已知杂质-核黄素、其他杂质相对保留时间加上自身对照的方法。取本品0.1g,用水50ml溶解,并用流动相稀释至100ml,取该溶液8ml,用流动相稀释至50ml,作为供试品溶液。另取核黄素对照品60mg,加盐酸试液1ml溶解,用水稀释至250ml, 取该溶液4ml,用流动相稀释至100ml,作为对照品溶液(a)。再另取核黄素磷酸钠对照品0.1g,用水50ml溶解,并用流动相稀释至100ml,取该溶液8ml,用流动相稀释至50ml,作为对照品溶液(b)。用十八烷基硅烷键合硅胶为填充剂(填充剂粒度:5μm;柱长:0.25m;内径:4.6mm);以甲醇-7.35g/L磷酸二氢钾溶液(150:850)为流动相;检测波长266nm;流速2ml/分。5-单磷酸核黄素的保留时间为20分钟;其他相对保留时间:3,4-二磷酸核黄素大约0.2;3,5-二磷酸核黄素大约0.3;4,5-二磷酸核黄素大约0.5;3-单磷酸核黄素大约0.7;4-单磷酸核黄素大约0.9;核黄素大约2。 取对照溶液(a)100μl注入液相色谱仪,调节主峰高度为满量程的50%;再注入对照溶液(b)100μl,记录色谱峰直到核黄素的峰面积能被准确计算,且4-单磷酸核黄素峰与5-单磷酸核黄素峰的分离度应不小于1.5。精密量取供试品溶液、对照溶液(a)和对照溶液(b)各100μl,分别注入液相色谱仪,供试品溶液的色谱图中,如有与核黄素峰保留时间相应的色谱峰,其峰面积不得大于对照溶液(a)主峰面积(6.0%),二磷酸核黄素面积的和不得大于对照溶液(a)主峰面积(6.0%),且均应以干燥品计。 3、结合国内研发核黄素磷酸钠的状况提几点建议在审评核黄素磷酸钠原料和注射剂有关物质的过程中发现,申请人常参照中国药典收载的核黄素磷酸钠及注射液标准项目进行。忽视了国内外标准和国内同品种质量的调研,盲目申报。一些资料中单磷酸核黄素的分离度并不好,从图谱看起来,表面上其质量比国外标准的质量好,但实际上是单磷酸核黄素等多个组分并未得到有效分离。虽然国外将各单磷酸盐均看成有效成分,而未作为杂质控制,但在方法学研究中,的确关注了各单磷酸盐的分离度,这应是方法学研究的重点。如果建立的方法不能使每一个成分分离,这个方法就不是一个好的方法。从这个例子分析,审评中不能简单认为杂质个数少了,质量就好,杂质个数多了,质量就差,一定要结合分析方法的好坏,经过综合分析判断后下结论。否则,容易犯主观主义和片面主义的错误,将由于因分析方法的分离度较差而导致的杂质个数少的药品误认为质量好。其实,药品中包含着没有分开的成分,这个成分很可能是最不安全的成分。因此,一个药品的有关物质方法的评价更应重视分离度方法的评价,在分离度合适的情况下,比较检出杂质的个数才有意义,不能简单的以检出杂质的个数多少论质量。 对核黄素磷酸钠,引起重视的应是分离度方法的问题,在有了好的分离度方法基础上,再根据每一个成分的安全性和生产工艺的成本,考虑对每一个成分的合理控制,这是有关物质研究的重点。在可能的情况下,推荐使用国外药典标准的有关物质检查方法和限度。建议在仿制原料药时,首先应查阅国外药典同品种质量标准,借鉴国外的有关物质检查方法和限度,减少建立方法学和质量研究工作的盲目性。在未有文献可借鉴时,根据我国实际的研究水平,建立有关物质的检查方法。 其二,由于国内仿制的原料药是可以豁免临床研究的,不同的合成工艺对主药的影响不同,而可能的中间体、副产物、降解产物会不同。有关物质方法的确定一定要以工艺中的理论上的各成分的分离度为依据,并与已上市药品进行质量对比,确定可能的已知杂质或杂质相对保留时间保证方法的分离度。 其三,关注工艺杂质并兼顾原料药的降解产物的安全剂量,其限度可以以已上市药品的对照数据为依据。 原料药有关物质的控制方法对质量控制来说至关重要,它是衡量质量和稳定性一致性的尺子。因此,不能忽视有关物质检查方法的验证或方法建立。 上面是以审评核黄素磷酸钠原料和注射剂有关物质方法为例,说明方法建立应关注的重点问题是分离度,没有分离度作保证,方法的根基就不牢固。希望能对申请人的研发起到帮助,并减少申报资料的发补率。
我们公司现在增加了甘露醇的有关物质检查(HPLC),用的是磺化交联的的苯乙烯二乙烯基苯共聚物为填充剂的强阳离子钙型交换柱的色谱柱,原先都没用过,有谁用过吗?用的是什么厂家的柱子,性能怎么样?如:[url=http://www.instrument.com.cn/netshow/SH101062/Q715859.htm]SUGAR SC系列强阳离子钙型交换柱[/url] 怎么样?
【摘要】本文针对审评原料药有关物质检查方法中存在的问题,介绍欧洲和英国药典关于原料药已知杂质的研究现状和有关物质方法建立及质量控制,以供申请人参考。【关键词】有关物质、方法学、分离度。笔者审评原料药有关物质检查方法中发现,大多申请人越来越多地认识到控制原料药有关物质的重要性,自行建立方法考察原料药中存在的有关物质。但在研究中往往片面认为样品通过了破坏性试验和1%自身对照法后的系统适用性试验就符合了要求。因此,忽视对主成分中杂质产生原因的分析,忽视仪器的检测灵敏度的分析、忽略色谱柱(柱效)的选择、流动相及比例的选择、检测波长的选择。忽视主成分和可能产生的杂质分离度的问题。1、原料药有关物质方法建立应关注的问题:原料药中的杂质来源于合成的中间体、副产物、以及降解产物,建立方法初期,仅采用破坏性试验的方法考察降解产物的做法是片面的。由于降解产物的量较小,如果选择的方法不好,比如,柱效低,波长选择不合理、流动相及流动相比例不合适,即使有降解产物,也达不到有效的灵敏度和有效的分离。因此,一个好的分析方法的建立首要问题应是围绕主成分和杂质的分离度和检测波长进行。对于生产原料药的企业来讲,由于可以通过工艺得到中间体、副产物,在方法建立初始,首先应该将可能的中间体和副产物作为杂质对待,进行柱效、流动相及流动相比例、波长和分离度等方法学的研究。方法建立成熟后,可根据中间体和副产物的安全性和工艺得到的难易程度决定是否固定为已知杂质。如果工艺中难以得到,且比较安全,可考虑采用杂质校正因子加上相对保留时间的方法。或采用杂质相对保留时间加上自身对照方法。上述三种方法均有好的分离度和响应值(灵敏度)作保证。也是研发和审评中应当提倡的。如果原料合成中确实得不到副产物,对于有紫外吸收的样品可以用二极管阵列检测器,考察未精制的粗品,并对比已精制过的样品,确定粗品中各成分的分离度和样品中可能杂质的检测波长。方法确立后,可采用自身对照方法或面积归一化法控制杂质。对于后一方法,在研发和审评中应当慎重选用。如果证明上述四个方法是比较成熟的方法后,如果再加上破坏性试验考察降解产物,其方法就更加完整和适用。2、介绍欧洲和英国药典控制有关物质关注的问题欧洲和英国药典的原料药标准后面,大部分都附有可能产生的中间体和副产物的结构,在有关物质质量控制中有些采用已知杂质的方法;有些采用杂质校正因子加上相对保留时间的方法;杂质相对保留时间加上自身对照方法和自身对照方法或面积归一化法。例如:核黄素磷酸钠的有关物质检查就是采用HPLC的已知杂质-核黄素、其他杂质相对保留时间加上自身对照的方法。取本品0.1g,用水50ml溶解,并用流动相稀释至100ml,取该溶液8ml,用流动相稀释至50ml,作为供试品溶液。另取核黄素对照品60mg,加盐酸试液1ml溶解,用水稀释至250ml, 取该溶液4ml,用流动相稀释至100ml,作为对照品溶液(a)。再另取核黄素磷酸钠对照品0.1g,用水50ml溶解,并用流动相稀释至100ml,取该溶液8ml,用流动相稀释至50ml,作为对照品溶液(b)。用十八烷基硅烷键合硅胶为填充剂(填充剂粒度:5μm;柱长:0.25m;内径:4.6mm);以甲醇-7.35g/L磷酸二氢钾溶液(150:850)为流动相;检测波长266nm;流速2ml/分。5-单磷酸核黄素的保留时间为20分钟;其他相对保留时间:3,4-二磷酸核黄素大约0.2;3,5-二磷酸核黄素大约0.3;4,5-二磷酸核黄素大约0.5;3-单磷酸核黄素大约0.7;4-单磷酸核黄素大约0.9;核黄素大约2。取对照溶液(a)100μl注入液相色谱仪,调节主峰高度为满量程的50%;再注入对照溶液(b)100μl,记录色谱峰直到核黄素的峰面积能被准确计算,且4-单磷酸核黄素峰与5-单磷酸核黄素峰的分离度应不小于1.5。精密量取供试品溶液、对照溶液(a)和对照溶液(b)各100μl,分别注入液相色谱仪,供试品溶液的色谱图中,如有与核黄素峰保留时间相应的色谱峰,其峰面积不得大于对照溶液(a)主峰面积(6.0%),二磷酸核黄素面积的和不得大于对照溶液(a)主峰面积(6.0%),且均应以干燥品计。
[size=3][b]请教已有药典标准的原料药的质量标准细节[/b][/size]我们现在做一个仿制药,质量标准收在美国药典。对于其中的一些细节问题向大家请教一下,先谢谢各位老师了。1、稳定性实验:加速试验、影响因素试验是不是每次取样进行含量测定、有关物质检查时都要做方法验证?2、采用药典方法还需要做详细的方法验证吗?具体哪些需要做,哪些可不必做?3、不用杂质对照品进行杂质定量时(采用主成分的对照品作为对照溶液,供试品中杂质的峰面积与对照溶液峰面积之比),方法验证需要做哪些?非常感谢!
最近在做克拉霉素有关物质检查,却发现很多奇怪的现象,让我百思不解,写出来跟大家讨论讨论。仪器:岛津2010A/C(一新一旧),25cm的C18柱两根,210nm,05版药典二部方法,流动相为缓冲盐:乙腈(6:4),缓冲盐中加0.2%三乙胺,用磷酸调pH至5.5,柱温45度,分析时间30min。奇怪现象如下:1。柱温为室温(20度)时,主峰在6min左右出峰,柱温为45度时,主峰在8-9min出峰,有点反常。2。平衡好柱子后进样,系列进样,前几个样走得比较正常,比如到第3个样,第十几分钟后基线出现个大包(疑似进气泡的现象),连续3针基线都是波浪式的,但过了这几针却又好了。大家都说是检测池进气泡了,但是我每次做这个样品的时候都出现这个情况,而且流动相我每次都要超声10min,使用新的仪器(刚买不到1个月)也这样,而这台仪器做其它样品的时候一切正常,所以,让我很头疼,不知道有没有跟我碰到一样的情况。3。样品用流动相溶解,当进空白溶剂(即流动相)时,在2.4min出现一个小峰,峰高大约在1mAU,克拉霉素原料在2.4min也出现杂质峰,峰高要大一点,而克拉霉素片用的辅料也在2.4min出峰,所以做有关物质时就犯难了,这个峰怎么处理,也不能当溶剂或辅料峰扣掉,不扣的话,这个杂质峰就已经超标了。
有关物质检查的检查在新药研发中应引起重视 对于一个新药,对其纯度的检查是保证安全有效的重要指标之一,而纯度检查的内容,根据各个药物的性质和特点有些不同,但基本上均要涉及各自的“有关物质”检查研究。关于有关物质的检查,在国际上已早为“人用药品注册技术规范协调会(ICH)”所关注,国内在新药的有关文件中也提出了供参阅的一些具体要求,并逐渐引起研制新药者的重视。 由于一个新药从合成原料药到制备有关的制剂,再经贮藏、运输、使用,要经历一段较为复杂和漫长的过程,在此期间,每一过程都有可能产生有关的物质,如生产中可能带入起始原料、试剂、中间体、副产物和异构体等;在贮藏和运输过程中,可能产生降解产物、聚合物或晶型转变等特殊杂质。为保证药物的安全有效,同时也要考虑到生产实际情况,因此,国内外对药物的研究,可允许含有一定限量的无害或低毒性的有关物质,但对毒性较大,能危害人体健康的、无效的或能影响药物稳定性的有关物质则必须严格控制。 因有关物质的量微小,故检测方法至关重要,必须选择专属性强、灵敏度高、重复性好的方法。目前,首选的是色谱法,可根据新药的具体品种及其有关物质的性质采用TLC,HPLC及GC等,有的还应采用其他有关的色谱或波谱法。对于一、二类新药更应重视,必要时可采用HPLC/UV二极管阵列、HPLC/MS或GC/MS等联机技术,对有关物质进行定性定量分析。
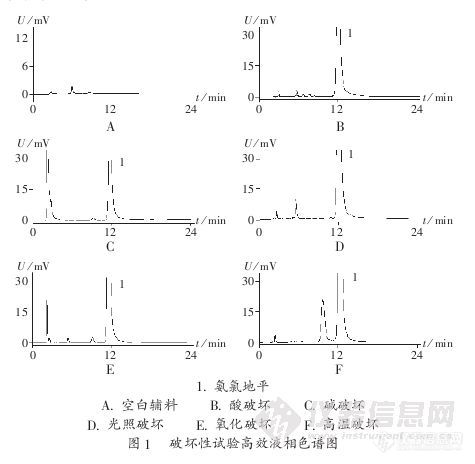
作者:秦书德 马晓伟 陈静 郭兴杰作者单位沈阳药科大学,摘 要:目的建立检查苯磺酸氨氯地平有关物质的反相高效液相色谱法。方法采用Diamonsil C18色谱柱(200 mm×4.6 mm,5μm)进行分离,流动相为甲醇-30 mmol/L磷酸二氢钾溶液(60∶40),流速1.0 mL/min,检测波长238 nm。结果所用色谱条件能很好地分离氨氯地平及其降解产物,氨氯地平质量浓度在0.71~3.57μg/mL范围内与峰面积线性关系良好。结论反相高效液相色谱法专属性强、准确、灵敏,可用于苯磺酸氨氯地平片中有关物质的检查:http://ng1.17img.cn/bbsfiles/images/2012/08/201208201631_384755_2379123_3.jpg
【讨论目的】现在的有关物质检查几乎都涉及到了特定杂质的检查,采用校正因子计算特定杂质越来越普遍,园子里面也很多战友讨论了很多。但是一定还有跟我一样对此问题存疑的战友,或许过去认为已了解的战友也存在不够准确的认识。【提出讨论】所提出讨论的问题也许你觉得很简单无聊,但非常希望你能参加讨论给出你的看法①现在问到你,校正因子计算公式,你如何回答?②为什么我们能看到的文献都是按公式(1)所得校正因子(如果是用这个公式,在计算时不能将杂质峰面积乘以校正因子,而是除以校正因子?)③我们是不是把校正因子和响应因子搞混淆了,校正因子与响应因子的倒数关系,是通过什么得到的?④中国药典中的规定和公式说明存在误导?带着这些问题,就查找到的信息汇总说明:1、公认的公式??查了很多资料,包括园里讨论的,包括药检所老师所写文章,几乎大家说到相对校正因子的计算方法都为:F=(A杂/C杂)/(A样/C样) 公式(1)这个公式在我所查到资料里可以认为是最普遍公认的公式2、中国药典的规定中国药典“加校正因子的主成分自身对照法”中规定计算方法:色谱图上各杂质的峰面积,分别乘以相应的校正因子后与对照溶液主成分的峰面积比较,计算各杂质含量。这里规定的“校正因子”计算方法是按内标法校正因子:F=(A内标/C内标)/(A对照/C对照) 公式(2)根据公式(2),我们直接把内标换成杂质,即得到与上面的公式(1)一样的公式,即认为是杂质斜率与主成分斜率的比值,得下面公式(3)F= 杂质斜率/ 供试品斜率 公式(3)药典规定用F乘以杂质峰面积,假设通过该公式计算的校正因子是1.5,则说明杂质峰的响应值要大于主成分,如果在计算时再将杂质峰面积乘以1.5,结果正确吗?那这个公式对吗?3、公式推导 假设响应因子为k,则有k=A/m(单位质量的物质相当于多少峰面积),令杂质k杂=A杂/m杂,主成分k样=A样/m样,则主成分中杂质含量w=m杂/m样*100%,即有:w=(A杂/k杂)/(A样/k样)*100%=(k样/k杂)*(A杂/A样)*100% 公式(4)根据药典,理论上,加校正因子以自身对照法计算杂质含量的公式简易表示应是:w=F * A杂/ A对 公式(5)由公式(4)(5)两式可知,计算杂质时加入的校正因子F:F=k样/k杂=(A样/C样)/(A杂/C杂) 公式(6)4、公式(6)和公式(1)的区别倒数关系,相对响应因子(RRF)与校正因子F的关系如下:F=1/RRF= Slope 主峰/ Slope imp 公式(7)其中:Slope imp是指对应杂质的斜率,Slope 主峰是指主峰的斜率。5、对中国药典的看法①药典中对有关物质计算方法中的校正因子的描述,也许是拐了一个弯,对于我这种没脑子的人来讲容易误导而绕进去出不来。药典中公式对针对内标法测含量设计,不适用于杂质计算。②药典中对“校正因子”的描述与色谱类专业书籍的不符,我所查到的是:校正因子= C/A 公式(8)响应因子= A/C 公式(9)
问题: 我想问下有关物质检查中主峰保留时间改变辅料峰保留时间是不是不会改变
关于HPLC主成分自身对照法检查有关物质时检测波长确定的讨论审评二部张玉琥有关物质检查,包括对产品中残留合成原料、中间体、副产物及可能的降解产物的检查,是控制药品质量的重要指标,目的是检查药品中所含的上述杂质是否符合安全性的要求,同时也是药品稳定性评价中需重点考察的项目。有关物质检查常用的方法之一是HPLC主成分自身对照法(紫外检测器),即将HPLC色谱图中杂质峰面积与主成分自身对照液峰面积进行比较,以确定杂质限度是否合格。采用此方法时确定的检测波长是否合理直接影响到方法的可行性,因此检测波长的选择是方法学研究的重要内容。在审评中发现一些申报单位在采用HPLC主成分自身对照法检查有关物质时直接或间接地以主成分的最大吸收波长作为检测波长,由于有关物质检查的对象是杂质,若将主药的最大吸收波长确定为检测波长,则杂质在此波长下的吸收可能偏低,某些杂质甚至无吸收,这样会造成对杂质含量的低估甚至漏检,从而不能反映产品的真实质量,影响了对品种质量可控性及稳定性的评价。在有关物质检测波长确定方面,申报资料中比较常见的做法有:1.直接将主药的最大吸收波长选作检测波长。2.简单地套用含量测定的色谱条件。在HPLC法进行含量测定时,为提高方法的灵敏度,降低干扰,往往选用主成分的最大吸收波长作为检测波长。若套用含量测定的色谱条件,实际仍是以主药的最大吸收波长作为有关物质检测波长。3.以样品进行破坏性试验(酸、碱、热、光照、氧化等)后的溶液做紫外扫描,将扫描图谱中最大吸收波长确定为有关物质的检测波长。因破坏性试验后溶液中存在尚未破坏的主药、降解产物、辅料等,此溶液的紫外吸收为各成分紫外吸收的加和,并不能反映降解产物的紫外吸收特性。由于未破坏主药所占比例较大,故破坏性试验后溶液的最大吸收波长一般仍为主药的最大吸收波长。采用HPLC主成分自身对照法检查有关物质,其前提之一是需检查的杂质与主成分在确定的检测波长下应有相近的紫外吸收(响应值接近),选择检测波长时需对产品中可能存在的杂质(合成原料、中间体、副产物以及降解产物)的紫外吸收特性进行研究。已知杂质的紫外吸收特性可采用对其流动相溶液直接进行扫描的方法考察,未知杂质(如未知降解产物等)可通过二极管阵列检测器考察其紫外吸收情况,根据各主要杂质及主成分的紫外吸收特性,选取响应值基本一致的波长作为有关物质的检测波长。若对不同杂质难于找到均适宜的检测波长,可考虑选择在不同波长下分别测定,也可考虑采用加校正因子的主成分自身对照法。只有经试验研究确认主成分的最大吸收波长符合有关物质检查对测定波长的要求时,为方便操作,可选作有关物质的检测波长,以与含量测定的色谱条件一致。另外,HPLC主成分自身对照法检查有关物质比较适用于对微量杂质总量的控制,也可用于单个杂质的限度(一般不超过0.5%)控制。对于具有明确归属的已知杂质,建议采用杂质对照品法进行检查。对于有毒有害杂质,更应采用质对照品法单独测定,并制定严格的限度。
马上准备要做稳定性试验了,有一些问题向大家请教下,烦请大家不吝赐教,先谢过了!1、做影响因素长期、加速试验时,每次取样做含量测定和有关物质检查时,是否都要重新做标曲?2、 用外标法定量时,对照品溶液可否在冰箱存放,隔月再用呢?对照品溶液最多可以用多长时间呢?3、 加速试验、长期试验做满6个月后,如何做数据的统计分析呢?有效期又该如何算呢?请做过的老师指点迷津。

放射性物质检查系统是一种专门用于放射性恐怖活动和放射性物质非法转移的新型安检系统。该系统采用非常稳定和可靠的探测材料,对放射性物质探测灵敏度高,具有结构轻巧,便于安装、携带,检测信息能经过有线或无线进行网络传输,实现远程控制与监测,是保护社会和公众免受放射性危害的理想检查系统。特点:1.系统结构简单,安装方便2.灵敏度高,对放射源方位有较好辨别能力应用范围: *机场、海关口岸*车站、码头*体育和会议场馆等用于监测和检查行人、行李等是否携带放射性物质*CIAE1108A型:与危险品检查通道相配合用于行李、手提箱的检测;*CIAE1108B型:与金属探测安检门配合用于非金属包壳的放射性物品检测。
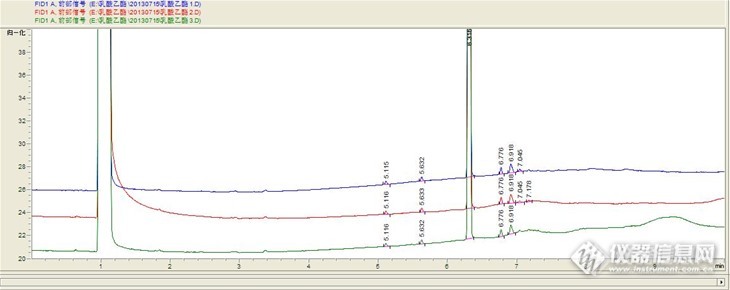
前面关于乳酸乙酯的那个帖子中以及提到,我们的一个制剂中要用到乳酸乙酯作为药用辅料。但是国家没有批准乳酸乙酯作为药用辅料的生产产家,只有食品添加剂的生产厂家。(详见http://bbs.instrument.com.cn/shtml/20130726/4872328/测定乳酸乙酯纯度的方法筛选) 东风兄说,对于国家没有批准药物辅料的品种,如果是口服制剂的话,可以用食品级的来代替。这个方案是完全可以的。我们曾经有一个品种,里面有很多原来没有药用级的辅料,因为这个事儿也头疼了很久,后来咨询国家局的专家,给的就是这样一个答复,前提是必须做好内控,切实的控制好质量。但是对于目前的这个品种来说,仅仅内控是不够的了,因为这个不是口服制剂,而是注射剂。因此,估计要在申报制剂的同时,要拖着报一个药用辅料才行。基于这样的思路,就不得不对乳酸乙酯多做一些研究。对于注射剂的药用辅料来说,除了常规的理化检验,含量测定和有关物质检查就是重点中的重点了。前面已经摸索了含量的测定方法了,这里,对有关物质也要进行一个方法摸索。乳酸乙酯,一般是乳酸和乙醇在催化剂的存在下发生的酯化反应。可能的有关物质,无怪乎就是乳酸、乙醇、甲醇、乳酸甲酯等等或者还有别的几种东西。在做含量的时候,选择正己烷做溶剂,也是包含了这方面的考虑的了。前面已经有了含量测定的色谱条件,因此,在那个条件的基础上,把升温速率稍微的温和一些,把采集时间稍微长一些,应该就可以有效的检测其有关物质。 试了几个条件,选择了效果最好的一个初步定为有关物质检查方法。其色谱条件如下:色谱柱为WEL-PEG20M,30m*0.32mm 0.25μm,(Cat NO:01918-32001;Serial NO:GC20131102);进样口温度为200℃;检测器温度为250℃;升温程序还需要暂时保密哦(不好意思,不得不如此,还望大家可以理解)。 我的色谱图为:http://ng1.17img.cn/bbsfiles/images/2013/07/201307311836_455030_1609327_3.jpg三针色谱图的重叠图:http://ng1.17img.cn/bbsfiles/images/2013/07/201307311836_455031_1609327_3.jpg从图谱上看,保留时间还是很稳定的吧?就是基线有些漂动。但是分离度还是可以的。总体上讲,作为乳酸乙酯有关物质检查的分析,还是可以满足要求的。如果需要,就是一些微调而已。还是很满意这样的效果的。
今天做维生素B6时的有关物质检查时,看到这样一句“照含量测定项下的色谱条件,取对照液10微升注入色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的10%。”请问这个要怎么调??我用的是岛津LC-10AT的机子,N2000工作站。新手,多多指教!!!!
有关物质检查,包括对产品中残留合成原料、中间体、副产物及可能的降解产物的检查,是控制药品质量的重要指标,目的是检查药品中所含的上述杂质是否符合安全性的要求,同时也是药品稳定性评价中需重点考察的项目。 有关物质检查常用的方法之一是HPLC主成分自身对照法(紫外检测器),即将HPLC色谱图中杂质峰面积与主成分自身对照液峰面积进行比较,以确定杂质限度是否合格。采用此方法时确定的检测波长是否合理直接影响到方法的可行性,因此检测波长的选择是方法学研究的重要内容。 在审评中发现一些申报单位在采用HPLC主成分自身对照法检查有关物质时直接或间接地以主成分的最大吸收波长作为检测波长,由于有关物质检查的对象是杂质,若将主药的最大吸收波长确定为检测波长,则杂质在此波长下的吸收可能偏低,某些杂质甚至无吸收,这样会造成对杂质含量的低估甚至漏检,从而不能反映产品的真实质量,影响了对品种质量可控性及稳定性的评价。1.直接将主药的最大吸收波长选作检测波长。2.简单地套用含量测定的色谱条件。在HPLC法进行含量测定时,为提高方法的灵敏度,降低干扰,往往选用主成分的最大吸收波长作为检测波长。若套用含量测定的色谱条件,实际仍是以主药的最大吸收波长作为有关物质检测波长。 3.以样品进行破坏性试验(酸、碱、热、光照、氧化等)后的溶液做紫外扫描,将扫描图谱中最大吸收波长确定为有关物质的检测波长。因破坏性试验后溶液中存在尚未破坏的主药、降解产物、辅料等,此溶液的紫外吸收为各成分紫外吸收的加和,并不能反映降解产物的紫外吸收特性。由于未破坏主药所占比例较大,故破坏性试验后溶液的最大吸收波长一般仍为主药的最大吸收波长。 采用HPLC主成分自身对照法检查有关物质,其前提之一是需检查的杂质与主成分在确定的检测波长下应有相近的紫外吸收(响应值接近),选择检测波长时需对产品中可能存在的杂质(合成原料、中间体、副产物以及降解产物)的紫外吸收特性进行研究。已知杂质的紫外吸收特性可采用对其流动相溶液直接进行扫描的方法考察,未知杂质(如未知降解产物等)可通过二极管阵列检测器考察其紫外吸收情况,根据各主要杂质及主成分的紫外吸收特性,选取响应值基本一致的波长作为有关物质的检测波长。若对不同杂质难于找到均适宜的检测波长,可考虑选择在不同波长下分别测定,也可考虑采用加校正因子的主成分自身对照法。只有经试验研究确认主成分的最大吸收波长符合有关物质检查对测定波长的要求时,为方便操作,可选作有关物质的检测波长,以与含量测定的色谱条件一致。 另外,HPLC主成分自身对照法检查有关物质比较适用于对微量杂质总量的控制,也可用于单个杂质的限度(一般不超过0.5%)控制。对于具有明确归属的已知杂质,建议采用杂质对照品法进行检查。对于有毒有害杂质,更应采用杂质对照品法单独测定,并制定严格的限度。 转自——中国植提论坛
求助下起始物料4-溴甲基喹啉酮的有关物质检查方法
【序号】: 1【作者】: 徐燕 兰婉玲 傅超美 何瑶【题名】: 甘露醇及甘露醇注射液有关物质检查的研究【期刊】: 成都医学院学报【年、卷、期、起止页码】: 2008年3期【全文链接】:帮你编辑了,下次请注意一下!
氟罗沙星有关物质检查请教.用HPLC,流动相(三乙胺-磷酸-水,乙腈),C18分离,前后杂质无法与主峰分开,曾改变乙腈比例无明显改善,把磷酸改为柠檬酸也无明显改善。请高手不吝赐教。
【作者】 江燕;【机构】 湖北省药品检验所 湖北武汉430064;【摘要】 目的 :建立了艾司唑仑和艾司唑仑片中的有关物质检查和控制方法。方法 :高效液相色谱柱Diamonsil C1 8(2 0 0mm× 4 .6mm ,5 μm) ,流动相为甲醇 水 (6 5∶35 ) ,检测波长 2 2 3nm ,流速 1 .0mL·min-1 。结果 :合成反应中 3个重要中间体能够得到有效分离 ,最低检出量为 4ng,控制总杂质量不得超过 1 .0 %。结论 :本方法准确 ,有效 ,简便。 更多还原【关键词】 艾司唑仑; 中间体; 高效液相色谱法;
有关物质检查方法的验证重点关注专属性、灵敏度和耐用性,以及杂质的相应因子。⑴ 专属性 专属性应确保杂质从主成分峰中分离出来或各杂质与主成分峰互相之间应分离,并且分离度应符合要求。 原料药可用合成反应(特别是后三步合成反应)的原料、中间体,粗品、重结晶母液等考察杂质与主成分的分离情况。仅采用破坏性试验考察,可能会漏掉合成原料、中间体、立体异构体等杂质,应当引起注意。同时配合不同柱效的色谱柱、不同波长(或用DAD全光谱检测)和不同流动相比例来考察。 破坏性试验适合于考察降解产物,更适合于制剂有关物质检查方法的验证。一般用酸、碱、光、热、氧化反应等加速破坏性来验证,应当注意破坏程度不宜太大,一般以使主成分降解5~10%为好,同时应该充分注意质量平衡原则,防止分解产物无法被检出的情况发生。用过期或变质的样品来验证,也是较好的选择。杂质峰响应值与主成分峰的不一致、杂质峰无法检出或被破坏等均能引起质量不平衡。 如果有液相色谱—串联质谱联用仪,可以对主成分峰进行质谱扫描,以验证主成分峰是否还包含杂质。DAD 的峰纯度指数一般不能作为主成分峰是否单纯的验证方法,因为杂质的量很小对峰的贡献很小,对峰纯度指数的影响也很小,即便纯度指数指示为纯峰并不能代表主成分峰不包含杂质。再则如果主成分峰与杂质峰完全重迭或杂质的光谱与主成分相似,报告的峰纯度指数仍然是很高的。⑵ 灵敏度 灵敏度是有关物质检查的重要指标。灵敏度应满足测定所关注杂质的要求,至少应达到所关注杂质限量的10%。由于不同的高效液相色谱仪的灵敏度不相同,建议在标准中设立或检验时配制灵敏度试验溶液,灵敏度试验溶液的浓度一般不大于供试品溶液的 0.05%,杂质量大的可以浓一些,杂质量小的应当稀一些。灵敏度溶液主峰的信噪比应当不小于10。⑶ 耐用性 耐用性一般可以考察三个以上品牌色谱柱、流动相比例变化±2%~5%、流动相 pH 值变化±0.2、柱温变化±5℃、检测波长变化±5nm。在上述条件下,均能较好地满足设定的系统适用性试验要求。 ⑷ 单个杂质的响应因子在具有杂质对照品时,考察杂质相对于主成分的相应因子以及色谱峰的相对保留时间,并观察其稳定性。 ⑸ 溶液稳定性试验除特殊情况外,应在室温下考察。主要应关注杂质峰个数、位置及其峰面积与杂质总峰面积是否发生变化。
对于采用杂质外标和1%自身对照结合的有关物质定量方法,做有关物质方法学验证线性试验时,是否必须将1%这个浓度也括进去?个人认为理论上来说,应该将它括进去,但貌似不少人没有这样做吧?
我最近在做一种制剂的有关物质检查。原先是在岛津的机器上UV检测器做的,主药在254nm处有最大吸收,故确定在此波长下检测。然后专家认为应该对杂质检查中杂质的检测波长进行优化,而不是依据主药的最大吸收波长来测。但是我们岛津没有配备DAD,是到Agilent1100上做的全波长扫描,但是很奇怪在Agilent的仪器上原本7分多钟的主药峰变成了20多分钟甚至更长,或者干脆就不出峰。进了好几针重现性很差,其他色谱条件都没有变动,就是换了一台仪器。而同一个样品再换到岛津上检测又是好的了。另外我的待测样品有点粘度,不知道是不是跟这个有关?真的百思不得其解这其中的问题所在,望高人帮忙想一下,非常感谢!
2010版药典中辅料丙二醇增加了有关物质的气相检查,其中有杂质一缩二丙二醇、二缩三丙二醇,但据了解,这两种东西均为异构体混合物,我们买了杂质对照品(均为色谱标准品),一缩二丙二醇、二缩三丙二醇均出好几个峰,且有的峰不能完全分离不知怎么理解标准中对其控制的要求?有做过的同仁,望不吝赐教!
浅谈对已有国家标准化学药物杂质检查方法学研究资料的审评体会审评五部 李志万 《已有国家标准化学药品研究技术指导原则》(征求意见稿)中“质量研究方法的选择及方法学验证”部分提出“对于原料药的有关物质检查,重点通过采用合成中间体、粗品等考察方法的专属性;对于制剂的有关物质检查,重点通过破坏试验等考察方法的专属性”。 已有国家标准的(注册分类6的仿制)药物注册占我国目前的药物注册绝大部分。可能因为对新制订的《化学药物杂质研究技术指导原则》的理解不同,仿制药物申报资料中杂质研究部分多数存在这样或那样的问题,需要以书面或非书面的形式进行说明或完善,严重影响了对药品评价和注册的进度。笔者拟根据自己对此问题的理解,简略谈一下自己对仿制药物杂质检查方法研究的几点认识。 本文所阐述的杂质主要为药物中的有机杂质,但不包括残留有机溶剂。 一 正确认识仿制药物杂质研究的意义 可能有部分研究人员认为鉴于仿制药物的安全性已经验证,其杂质研究可否不再进行,可否不经验证直接沿用已有标准中(有关物质检查)方法。对上述观点,笔者认为因不同研发单位所用的原辅料不同,所引入的杂质不同;不同研发单位所采用的制备路线、制备工艺不同,所产生的杂质可能会不同。因此,有必要对仿制药物中的杂质重新进行研究,已有标准中方法是否适用于自制品也需实验验证。 二、已有标准药物杂质检查方法研究的几点考虑 与其它定量检查方法相比,杂质检查更着重于方法的专属性和灵敏度;仿制药物杂质研究亦是如此,但因有同品种标准可供参考,也有其特殊性。下面拟以已有标准中有无杂质检查项,以及在相应情况下原料药和制剂的杂质如何研究分别阐述。 1 已有标准中有有关物质检查项的仿制药物杂质检查 此时的原料药杂质研究如采用已有标准中方法,方法专属性和灵敏度验证的主要对象应药物粗品中杂质和药物制备过程中的中间体,尤其是后期制备中间体,而非原料降解物。之所以不对原料降解物作更多关注,是基于药物结构一致,其降解物亦应一致的推断;而已有标准中检查方法对(相同)降解物检测的可行性是已经验证过的。以此相反,仿制的制剂杂质研究主要关注点则是已有方法对制剂中主药(在适宜条件下)降解物的检测专属性和灵敏度是否符合要求。这是因为:(1)原料药中杂质及其制备中间体已经得到检控。(2)因不同制剂的处方、制备工艺不同,导致主药存在的环境不同;在酸、碱、氧化、热、光照等条件的“催化下攠,主药产生的降解物可能会不同。(3)不同的辅料对主药降解物检测的干扰性不同。因此,验证已有方法是否仍适用于新制剂中的杂质检测很有必要。 对于已有明确认识的有毒降解物,如对乙酰氨基酚之对氨基酚、葡萄糖之5-甲基糠醛等,无论原料药还是制剂,均建议采用杂质对照品验证所用方法的可行性。 如可能因条件限制,或认识的不同,仿制药物研发单位采用有别于已有标准中的其他方法,笔者则建议进行全面的(自拟)杂质检查方法学研究为宜,具体要求见《化学药物杂质研究技术指导原则》。值得强调的是,自拟方法与已有方法对相同供试品中杂质进行对比研究,对评价自拟方法的可行性很有意义。 2 已有标准中无有关物质检查项的仿制药物杂质检查 如已有标准中未收载有关物质检查项,在无相关研究结论支持的条件下,不能简单地推断所仿制的药物稳定而不需进行有关物质研究。笔者认为无论从质量标准的提高方面,还是从自制品质量研究、稳定性的考察方面(本文前面已说明自制品杂质可能与被仿制品杂质不同,稳定性亦可能有所差异),均有必要对仿制的原料药和/或制剂进行相应的杂质研究,并根据研究结果选用可行的杂质检查方法检控自制品的质量。具体要求亦请参见《化学药物杂质研究技术指导原则》。 考虑到原料药有时不会即时制成制剂,在贮存期间可能会有一定的降解,同时便于制剂厂家检测市购原料药的质量,建议制订适宜限度将有关物质检查项列入(原料药)质量标准;制剂质量标准中是否制订有关物质检查项,可根据杂质的毒性(安全性)、制剂的稳定性综合考虑。 欢迎对上述观点进行讨论、指正。
最近早报一个药品,做杂质检查,此杂质是辅料降解产生的有害杂质.发现,杂质检查有两种方法,一个是定量试验,一个是限度试验.什么情况下按定量做,什么情况下按限度试验方法做呢.有什么具体的规定吗.我看了不少都是用的限度试验.
[size=3]以下是2010年版药典二部中关于盐酸小檗碱中有关物质检查的描述:[检查]有关物质 取本品适量,精密称定,加流动相溶解并定量稀释制成每1ml中含1mg的溶液,作为供试品溶液;另取盐酸药根碱对照品和盐酸巴马汀对照品适量,精密称定,加流动相溶解并定量稀释制成每1ml中含0.1mg的溶液,分别作为对照品溶液(1)和(2);精密量取供试品溶液2ml和对照品溶液(1)和(2)各10ml,置100ml量瓶中,用流动相稀释至刻度,摇匀,作为对照溶液;取对照品溶液(2)1ml,用供试品溶液稀释至10ml,摇匀,作为系统适用性试验溶液。照高效液相色谱法(附录V D)试验,用十八烷基硅烷键合硅烷为填充剂;以0.01mol/L磷酸二氢铵溶液(用磷酸调节pH值至2.8)-乙腈(75:25)为流动相;检测波长为345nm。取系统适用性试验溶液10ul,注入液相色谱仪,巴马汀峰与小檗碱峰间的分离度应符合要求。另取对照溶液10ul,注入液相色谱仪,调节检测灵敏度,使小檗碱色谱峰的峰高约为满量程的25%。精密量取对照溶液与供试品溶液各10ul,分别注入液相色谱仪,记录色谱图至主成分色谱峰保留时间的2倍。供试品溶液的色谱图中,如有与药根碱峰和巴马汀峰保留时间一致的色谱峰,按外标法以峰面积计算,均不得过1.0%;[color=#fe2419]其他杂质峰面积的和不得大于对照溶液中小檗碱峰的峰面积(2.0%)。[/color]我的问题是:最后一句是什么意思?为什么供试品溶液色谱图中的其他杂质峰与对照溶液色谱图中的小檗碱峰面积进行比较?而不在一张色谱图内比较?如果按上面说,我们的结果是50%以上;而最后的括号中的2.0%是什么意思?[/size]