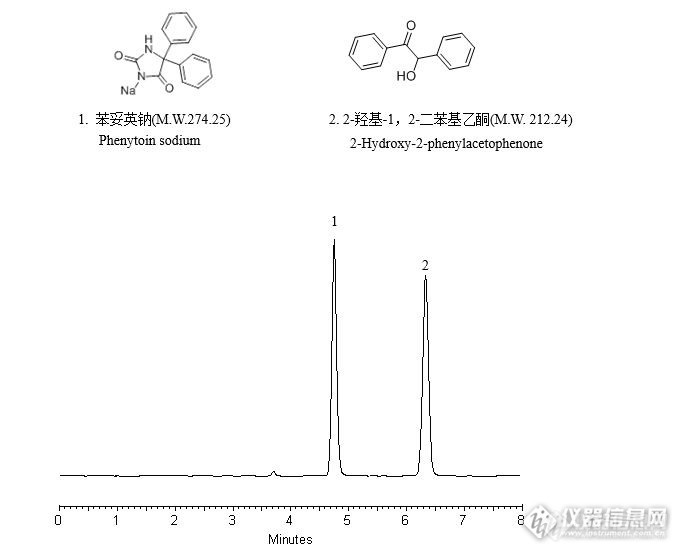
苯妥英钠是抗癫痫药、抗心律失常药。以下为使用资生堂CAPCELL PAK MG色谱柱,按照2015年版《中国药典》苯妥英钠含量测定项下方法进行分析得到的数据,请参考。http://ng1.17img.cn/bbsfiles/images/2017/01/201701031121_01_2222981_3.jpg【色谱条件】色谱柱:CAPCELL PAK C18 MG S5; 4.6 mm i.d.×250 mm流动相:0.05mol/L磷酸二氢铵(用磷酸调节pH值至2.5)/乙腈/甲醇=45/35/20流 速 : 1.5 mL/min温 度 : 35 °C检 测 : UV220nm进样量 : 20 µL
应用范围: 本方法采用滴定法测定苯妥英钠片中苯妥英钠的含量。本方法适用于苯妥英钠片。 方法原理: 供试品加水振摇溶解,加乙醚振摇,加溴酚蓝指示液,用盐酸滴定液(0.1mol/L)滴定,随滴随用强力振摇,至水层蓝灰色,分取水层,置具塞锥形瓶中,乙醚层用水5mL洗涤,洗液并入锥形瓶中,加乙醚继续用盐酸滴定液(0.1mol/L)滴定,随滴随用强力振摇,至水层淡绿色。根据滴定液使用量,计算苯妥英钠的含量。 试剂: 1. 乙醚2. 溴酚蓝指示液3. 盐酸滴定液(0.1mol/L)4. 甲基红-溴甲酚绿混合指示液5. 基准无水碳酸钠 仪器设备: 试样制备: 1. 溴酚蓝指示液 取溴酚蓝0.1g,加0.05mol/L氢氧化钠溶液3.0mL使溶解,再加水稀释至200mL,即得。2. 盐酸滴定液(0.1mol/L)配制:取盐酸9.0mL,加水适量使成1000mL,摇匀,得0.1mol/L盐酸滴定液。标定:取在270~300℃干燥至恒重的基准无水碳酸钠约0.15g,精密称定,加水50mL使溶解,、加甲基红-溴甲酚绿混合指示液10滴,用本液滴定至溶液由绿色转变为紫红色时,煮沸2分钟,冷却至室温,继续滴定至溶液由绿色变为暗紫色。每1mL盐酸滴定液(0.1mol/L)相当于5.30mg的无水碳酸钠。根据本液的消耗量与无水碳酸钠的取用量,算出本液的浓度。3. 甲基红-溴甲酚绿混合指示液 取0.1%甲基红的乙醇溶液20mL,加0.2%溴甲酚绿的乙醇溶液30mL,摇匀。 操作步骤: 取供试品10片(100mg规格)或20片(50mg规格),精密称定,研细,精密称取适量(相当于苯妥英钠0.3g),置分液漏斗中,加水25mL,振摇使苯妥英钠溶解,加乙醚50mL振摇,加溴酚蓝指示液10滴,用盐酸滴定液(0.1mol/L)滴定,随滴随用强力振摇,至水层蓝灰色,分取水层,置具塞锥形瓶中,乙醚层用水5mL洗涤,洗液并入锥形瓶中,加乙醚20mL,继续用盐酸滴定液(0.1mol/L)滴定,随滴随用强力振摇,至水层淡绿色。每1mL盐酸滴定液(0.1mol/L)相当于27.43mg的C15H11N2NaO2。注:“精密称取”系指称取重量应准确至所称取重量的千分之一。“精密量取”系指量取体积的准确度应符合国家标准中对该体积移液管的精度要求。
测定苯巴比妥、苯妥英钠和卡马西平
一直买不上苯妥英钠的标准样品,实验室用苯妥英加氢氧化钠合成了一些,做了红外图谱,始终同2002药典的标准图谱不吻合,药典上羰基峰有2个,而我们只有一个,请各位做过的大侠帮忙。

【作者中文名】程振田; 郭瑞臣; 王本杰; 魏春敏; 袁桂艳; 孔祥麟;【作者英文名】CHENG Zhen-tian1; GUO Rui-chen2; WANG Ben-jie2; WEI Chun-min2; YUAN Gui-yan2; KONG Xiang-lin2(1.Yidu Central Hospital of Weifang; Qingzhou 262500; China; 2.Institute of Clinical Pharmacology; Qilu Hospital of Shandong University; Jinan 250012; China);【作者单位】潍坊市益都中心医院; 山东大学齐鲁医院临床药理研究所; 山东大学齐鲁医院临床药理研究所 山东青州;摘要】目的建立能同时测定人血清苯巴比妥(PB)、卡马西平(CBZ)、苯妥英钠(PT)3种药物浓度的高效液相色谱(HPLC),并与常规荧光偏振免疫法(FPIA)测定结果进行相关性分析。方法以乙酸乙酯-二氯甲烷(4∶1)为提取溶剂,固定相Diamon-sil C18柱(4.6 mm×250 mm,5μm),流动相为乙腈-水(40∶60),紫外检测波长285 nm,流速1.0 mL.min-1。收集癫痫患者服药后稳态谷浓度血样,分别用HPLC和FPIA法测定,考察2种方法的相关程度。结果PB,CBZ,PT的标准曲线范围分别为1.0~45.0,0.1~15.0,1.0~25.0 mg.L-1,最低检测浓度分别为0.5,0.05,0.5 mg.L-1,提取回收率分别为80.2%,78.2%,86.2%,日内和日间RSD均小于9%。PB、PT2种方法的测定值无统计学差异(P0.05),但CBZ测定值FPIA法高于HPLC(P0.01)。结论HPLC操作简单、灵敏、准确,适用于治疗药物监测;PB和PT2种测定方法有良好的相关性,CBZ不同测定方法,结果存在差异。http://ng1.17img.cn/bbsfiles/images/2012/08/201208271738_386595_2379123_3.jpg
大洋网3月7日报道 根据卫生部通知要求,黑龙江省卫生厅3月6日晚连夜发出内部明传电报,要求全省各级各类医疗机构立即停止使用吉林一心制药股份有限公司生产的注射用泮托拉唑钠。据悉,3月6日卫生部收到国家食品药品监督管理局通报,经吉林省食品药品监食管理局抽检,吉林一心制药股份有限公司生产的注射用泮托拉唑钠(批号为0809022、0810011、0810012、0810021、0810022)可见异物,检查不合格。国家食品药品监督管理局已于 3 月 6 日下发通知要求停止销售和使用该药品。黑龙江省卫生厅接到卫生部办公厅紧急通知后,连夜发出内部明传电报,要求各级各类医疗机构立即停止使用并封存该批号的药品,并做好相关记录,保证信息完整,可追溯。一经发现与该批药品有关的不良事件,要全力做好医疗救治工作,有效保护好患者的生命安全,并按照规定立即报告同级卫生行政部门和药监部门。目前,黑龙江省医疗机构药品不良反应监测系统尚未接到该药品发生不良事件的报告。(来源:中国广播网)
1、茶水中含有鞣酸,它可与许多药物发生化学反应,生成不溶沉淀,从而影响药品疗效的发挥,受影响的药物包括各种含金属离子的药物,如硫酸亚铁、抗生素(红霉素、麦迪霉素、罗红霉素、阿奇霉素)、酶制剂(胃蛋白酶、胰酶、淀粉酶等) 2、茶水中含有咖啡因 ,它有兴奋中枢神经的作用,可与镇静催眠药(如苯巴比妥、安定等),中枢镇咳药(如可待因等)的作用相对抗,使药物疗效下降,也可使某些中枢兴奋作用的药物的兴奋作用加强,导致过量兴奋、失眠、血压升高的不良反应。高血压病一旦确诊,就应合理、安全、地服药治疗。现介绍其用药五忌: 3、茶水中含茶碱,它可影响呋喃坦啶、苯妥英钠等药物在胃肠道的吸收,影响吡哌酸、磺胺类药物在肾小管的重吸收,从而降低了这些药物的疗效。
新华社伦敦11月28日电 (记者刘石磊)英国一项最新研究发现,一些解热镇痛药、维生素补充剂等药品中钠含量较高,可能增加服用者罹患心血管疾病的风险。专家呼吁生产商应明确标注药品中的钠含量,并提示可能引发的健康风险。 英国伦敦大学学院等机构研究人员近日在《英国医学杂志》上报告说,他们对超过120万英国人的健康状况和服药情况进行了长达7年的跟踪调查。结果发现,与经常服用不含钠药物的对照组相比,常服用同类、含钠药物的人群死于心脏病、中风等心血管疾病的风险高出16%,出现高血压的风险更是比对照组高出7倍。 这项研究调查的药物包括解热镇痛药扑热息痛、阿司匹林、布洛芬,以及维生素和矿物质补充剂维C片、钙片和锌片等。据介绍,这些药物加入钠成分主要是为了帮助吸收,但往往不会明确标注这一成分。 领导这项研究的临床药理学专家雅各布·乔治说,这些药物十分普遍,甚至有的在超市都能买到,因此有必要在包装上明确标注其中的钠含量,并告知消费者可能由此引发的健康风险。医生也应注意评估这一风险,结合患者具体情况谨慎为其开药。 不过研究人员同时指出,这一研究结果并非意味着所有患者应停止服用此类药物,而是提醒他们注意相关风险,最好在医生指导下服药。
四川省食品药品监督管理局关于进一步规范药品委托检验的通知 川食药监安〔2011〕51号 2011-11-07 13:33 各市(州)食品药品监督管理局,各直属单位,各药品生产企业: 为进一步规范我省药品生产委托检验行为,保障药品生产质量安全,根据药品管理的法律法规规定和我省实际,经局办公会议研究决定,对进一步规范我省药品生产委托检验有关问题作如下通知。 一、药品生产企业进行委托检验限于以下情形: (一)动物试验(疫苗制品、血液制品的动物试验除外); (二)对进厂原辅料、直接接触药品包装材料的检验中,缺乏且使用频次较少(每年不足10批次)的检验仪器设备(核磁共振波谱仪、红外光谱仪、原子吸收光谱仪、液-质联用仪、气-质联用仪和高效液相色谱法中较少使用的蒸发光散射检测器、荧光检测器、电导检测器、示差检测器以及气相色谱仪顶空法等)而无法完成的项目; (三)中药材及中药饮片检验中,缺乏且使用频次较少(每年不足10批次)的检验仪器设备(气相色谱仪、原子吸收光谱仪等)而无法完成的项目; (四)药监部门认为可以委托检验的其他情形。 二、委托检验受托方,应是具有相应的检测能力,并通过国家(省)计量认证的食品药品检验机构,或者依法取得资质认定的其他检验机构;或者通过GMP认证的药品生产企业。 三、委托方和受托方应签订书面委托检验合同,明确委托项目、委托时限、检验执行质量标准、双方权利和义务,合同的各项内容应当符合国家药品管理的相关规定;受托方应保持相对稳定,受托方不得进行再委托。 四、委托方应按规定抽样,提供有代表性的样品,样品标签应标明样品名称、批号、规格、生产单位等基本信息;向受托方提供质量标准,并注明相应的委托检验信息;对最终的检验报告负责。 五、受托方应依照委托方的要求及提供的质量标准进行检验,并向委托方提供书面检验结果及原始记录(或复印件);受托方应接受委托方所在地食品药品监管部门的监督检查。 六、委托方和受托方双方必须互相审核资质,并保留相关证明文件,包括《药品GMP证书》、《药品生产许可证》和《营业执照》、检验机构资质证书和能力范围证书等。 七、委托方在实施委托检验前,应向省食品药品监督管理局备案,并按照《药品委托检验备案办事指南》提供包括以下资料在内的相关资料: (一)委托检验申请; (二)四川省药品生产委托检验事项备案表(见附件);[/
各省、自治区、直辖市食品药品监督管理局(药品监督管理局): 为贯彻落实2004年全国食品药品监督管理工作会议精神,做好全面监督实施药品GMP工作,进一步统一药品GMP认证标准,根据《药品管理法》、《药品管理法实施条例》及《药品生产质量管理规范认证管理办法》等有关规定,经研究,现将有关事宜通知如下: 一、凡新开办药品生产企业、药品生产企业新建药品生产车间或者新增生产剂型,须按《药品管理法实施条例》第六条规定,在取得药品生产证明文件后,方可提出GMP认证申请。对未取得药品生产证明文件的,一律不得受理并进行GMP认证。 二、除新开办企业外,不得核发1年期GMP证书。原已取得1年有效期《药品GMP证书》的企业,在证书到期时,仍未取得药品生产批准证明文件的,暂不予认证。待取得药品生产批准证明文件后,按规定申请GMP认证。 三、《药品GMP证书》有效期期满的药品生产企业,应按规定向省级食品药品监督管理局(药品监督管理局)或国家食品药品监督管理局提出药品GMP认证申请。 原《药品GMP证书》认证范围如既有注射剂、放射性药品、国家规定的生物制品,又有其它制剂的企业,可以一并按程序向国家食品药品监督管理局提出认证申请。如分别向国家食品药品监督管理局和省级食品药品监督管理局(药品监督管理局)提出申请的,须在向国家食品药品监督管理局申请药品GMP认证的申请表中注明。 四、药品生产企业对放行出厂的制剂产品必须按药品标准项下的规定完成全部检验项目。除动物试验暂可委托检验外,其余各检验项目不得委托其他单位进行。 菌、疫苗制品的动物试验不得委托检验。对于已通过GMP认证的动物试验允许委托检验的菌、疫苗制品企业(或车间),应在2004年12月31日前整改到位。 药品生产企业在对进厂原辅料、包装材料的检验中,如遇使用频次较少的大型检验仪器设备(如核磁、红外等),相应的检验项目可以向具有资质的单位进行委托检验。 上述检验项目如有委托行为,受托方应相对稳定,有关委托情况(包括变更受托方)须报省级药品监督管理部门备案。企业在申请药品GMP认证时,有关委托协议复印件须加盖本企业公章随申报资料一并上报。在生产活动中,企业应将委托行为纳入药品GMP自检重点范畴。各级药品监督管理部门须对有药品检验委托行为的企业加强药品GMP监督检查。 五、药品生产企业的环境保护、废气废水排放、安全消防等须符合国家有关法律规定,所取得的有关合格证明、证书和标志,须列入药品GMP管理文件中。企业在申请药品GMP认证时,有关证明、证书和标志复印件应随申报资料一并上报。 六、手工包装胶囊和安瓿包装粉针剂等药品生产工艺,已被国家列为淘汰工艺,对已通过GMP认证但仍使用该工艺的企业,由省、自治区、直辖市食品药品监督管理局(药品监督管理局)进行排查并责令其限期改正。 七、青霉素类药品的生产必须为独立厂房,不得与其它车间共用同一建筑物。对已取得《药品GMP证书》且有和其它药品生产共用同一建筑物的青霉素类药品生产企业,由各省、自治区、直辖市食品药品监督管理局(药品监督管理局)进行排查,责令其于2004年12月31日前改正完毕。 八、药品GMP认证现场检查观察员应是地市级以上药品监督管理部门选派的药品监督管理人员。检查疫苗车间,观察员应是省级药品监督管理部门人员。观察员代表当地药品监督管理部门,与药品GMP检查组协调和联络有关工作,现场检查中如发现企业有违背《药品管理法》及相关规定等问题,检查组应通过观察员及时移交所在地省级食品药品监督管理局(药品监督管理局)查处,并在检查报告中说明有关情况。 国家食品药品监督管理局 二○○四年四月十二日
药品研究实验记录暂行规定 第一条 为加强对药品研究的监督管理,保证药品研究实验记录真实、规范、完整,提高药品研究的质量,根据《中华人民共和国药品管理法》、《国家档案法》以及药品申报和审批中的有关要求,制定本规定。 第二条 凡在我国为申请药品临床研究或生产上市而从事药品研究的机构,均应遵循本规定。 第三条 药品研究实验记录是指在药品研究过程中,应用实验、观察、调查或资料分析等方法,根据实际情况直接记录或统计形成的各种数据、文字、图表、声像等原始资料。 第四条 实验记录的基本要求:真实、及时、准确、完整,防止漏记和随意涂改。不得伪造、编造数据。 第五条 实验记录的内容通常应包括实验名称、实验目的、实验设计或方案、实验时间、实验材料、实验方法、实验过程、观察指标、实验结果和结果分析等内容。 (一)实验名称:每项实验开始前应首先注明课题名称和实验名称,需保密的课题可用代号。 (二)实验设计或方案:实验设计或方案是实验研究的实施依据。各项实验记录的首页应有一份详细的实验设计或方案,并由设计者和(或)审批者签名。 (三)实验时间:每次实验须按年月日顺序记录实验日期和时间。 (四)实验材料:受试样品和对照品的来源、批号及效期;实验动物的种属、品系、微生物控制级别、来源及合格证编号;实验用菌种(含工程菌)、瘤株、传代细胞系及其来源;其它实验材料的来源和编号或批号;实验仪器设备名称、型号;主要试剂的名称、生产厂家、规格、批号及效期;自制试剂的配制方法、配制时间和保存条件等。实验材料如有变化,应在相应的实验记录中加以说明。 (五)实验环境:根据实验的具体要求,对环境条件敏感的实验,应记录当天的天气情况和实验的微小气候(如光照、通风、洁净度、温度及湿度等)。 (六)实验方法:常规实验方法应在首次实验记录时注明方法来源,并简述主要步骤。改进、创新的实验方法应详细记录实验步骤和操作细节。 (七)实验过程:应详细记录研究过程中的操作,观察到的现象,异常现象的处理及其产生原因,影响因素的分析等。 (八)实验结果:准确记录计量观察指标的实验数据和定性观察指标的实验变化。 (九)结果分析:每次(项)实验结果应做必要的数据处理和分析,并有明确的文字小结。 (十)实验人员:应记录所有参加实验研究的人员。 第六条 实验记录用纸 (一)实验记录必须使用本研究机构统一专用的带有页码编号的实验记录本或科技档案专用纸。记录用纸(包括临床研究用病历报告表)的幅面,由研究单位根据需要设定。 (二)计算机、自动记录仪器打印的图表和数据资料,临床研究中的检验报告书、体检表、知情同意书等应按顺序粘贴在记录本或记录纸或病历报告表的相应位置上,并在相应处注明实验日期和时间;不宜粘贴的,可另行整理装订成册并加以编号,同时在记录本相应处注明,以便查对。 (三)实验记录本或记录纸应保持完整,不得缺页或挖补;如有缺、漏页,应详细说明原因。 第七条 实验记录的书写 (一)实验记录本(纸)竖用横写,不得使用铅笔。实验记录应用字规范,字迹工整。 (二)常用的外文缩写(包括实验试剂的外文缩写)应符合规范。首次出现时必须用中文加以注释。实验记录中属译文的应注明其外文名称。 (三)实验记录应使用规范的专业术语,计量单位应采用国际标准计量单位,有效数字的取舍应符合实验要求。 第八条 实验记录不得随意删除、修改或增减数据。如必须修改,须在修改处划一斜线,不可完全涂黑,保证修改前记录能够辨认,并应由修改人签字,注明修改时间及原因。 第九条 实验图片、照片应粘贴在实验记录的相应位置上,底片装在统一制作的底片袋内,编号后另行保存。用热敏纸打印的实验记录,须保留其复印件。 第十条 实验记录应妥善保存,避免水浸、墨污、卷边,保持整洁、完好、无破损、不丢失。 第十一条 实验记录的签署、检查和存档 (一)每次实验结束后,应由实验负责人和记录人在记录后签名。 (二)课题负责人或上一级研究人员要定期检查实验记录,并签署检查意见。 (三)每项研究工作结束后,应按归档要求将药品研究实验记录整理归档。 第十二条 本规定由国家药品监督管理局负责解释。 第十三条 本规定自发布之日起实施。
[center]实验室各种化学药品的管理 [/center]一、各种化学药品的管理。化验室的化学药品及试剂溶液品种很多,化学药品大多具有一定的毒性及危险性,对其加强管理不仅是保证分析数据质量的需要,也是确保安全的需要。化验室只宜存放少量短期内需用的药品。化学药品建议按无机物、有机物、生物培养剂分类存放,无机物按酸、碱、盐分类存放,盐类中按金属活跃性顺序分类存放,生物培养剂按培养菌群不同分类存放,其中属于危险化学药品中的剧毒品应锁在专门的毒品柜中,由专人加锁保管、实行领用经申请、审批、双人登记签字的制度。(一)、哪些是属于危险品的化学药品:1、易爆和不稳定物质。如浓过氧化氢、有机过氧化物等。2、氧化性物质。如氧化性酸,过氧化氢也属此类。3、可燃性物质。除易燃的气体、液体、固体外,还包括在潮气中会产生可燃物的物质。如碱金属的氢化物、碳化钙及接触空气自燃的物质如白磷等。4、有毒物质。5、腐蚀性物质。如酸、碱等。6、放射性物质。(二)、化学试剂的使用管理制度1、要遵循既有利于使用,又要保证安全的原则,管好用好化学药品,加强安全教育。2、化学药品必须根据化学性质分类存放,易燃、易爆、剧毒、强腐蚀品不得混放。化学药品要存放在专用柜内,有存放专用柜的储藏室;有阴凉、通风、防潮、避光等条件;有防火防盗安全设施。3、所有药品必须有明显的标志。对字迹不清的标签要及时更换,对过期失效和没有标签的药品不准使用,并要进行妥善处理。4、试验药剂容器都要有标签,对分装的药品在容器标签上要注明名称、规格、浓度;无标签或标签无法辩认的试剂都要当成危险物品重新鉴别后小心处理,不可随便乱扔,以免引起严重后果。实验室中摆放的药品如长期不用,应放到药品储藏室,统一管理。5、化学药品盛装容器应封闭,防止漏气、潮解。见光容易起变化的化学药品应装在深色的玻璃容器或避光的容器里,对化学药品包装和药品质量要定期检查。6、要加强对火源的管理。化学药品储藏室周围及内部严禁火源;实验室的火源要远离易燃、易爆物品,有火源时,不能离人。7、储存的易燃易爆物品应避光、防火和防电等,实验室存放的易燃易爆物品,要确定合理的储存量,不许过量且包装容器应密封性好。易燃易爆试剂应贮于铁柜(壁厚1mm以上)中,柜子的顶部都有通风口。遇水能分解或燃烧、爆炸的药品,钾、钠、三氯化磷、五氯化磷、发烟硫酸、硫磺等不准与水接触,不准放置于潮湿的地方储存。8、危险物品的采购和提运按公安部门和交通运输部门的有关规定办理。剧毒、放射性物体及其它危险物品,要单独存放,由双人双锁专人管理。存放剧毒物品的药品柜应坚固、保险,要健全严格的领取使用登记。9、要经常检查危险物品,防止因变质、分解造成自燃、自爆事故。对剧毒物品的容器、变质料、废渣及废水等应予妥善处理。10、不外借药品,特殊需要借药品时,必须经领导批准签字。11、取用化学试剂的器皿必须分开,每种试剂用一件器皿,不得混用。12、使用有机溶剂和挥发性强的试剂的操作应在通风良好的地方或在通风橱内进行。任何情况下,都不允许用明火直接加热有机溶剂。13、凡使用强酸强碱等化学试剂时,应按规定要求操作和贮存。
用气相色谱仪测山梨酸、苯甲酸所用药品等级
一、防毒 1. 有毒气体如氯气、氟化氢、氰化氢(HCN,习惯上常称氢氰酸)、二氧化硫、硫化氢、一氧化碳、光气(COCl2)等的制取和使用要在通风橱中进行。工业上生产或较大量地使用这些气体时,有关人员必须带上防毒面具。对其中剧毒的(如HCN,CO,COCl2)即使少量使用时也应戴上防毒面具。 2. 实验室中常见的有毒液体或固体药品有液溴、苯、四氯化碳、二硫化碳以及碘、白磷、亚硝酸盐、苯酚等等,品种很多。对其中易挥发的,在制取、使用时与有毒气体采取同样措施。对皮肤有腐蚀性的(如液溴、碘、苯酚、白磷等),取用时要注意不与皮肤接触(带上乳胶手套)。一般对使用过的容器等应及时清理干净。特殊情况更为应注意,例如取用过白磷的镊子必要时应在置于通风橱内的煤气灯或酒精灯上灼烧,取用白磷时用过的纸应烧掉。 3. 使用剧毒药品如氰化钾、氰化钠、三氧化二砷、氯化汞等进行实验时应戴乳胶手套,并准备好解毒药品。 4. 磷化钙、磷化铝吸水后放出剧毒的磷化氢,氰化物(如NaCN)吸水后能产生氢氰酸,故应放在干燥器中密封保存。使用它们时不仅要戴乳胶手套,还应带防毒面具。 二、防燃 实验室中不宜大量保存易燃药品。少量易燃药品应放在阴凉、通风处、且远离电源、热源。 1. 易燃气体有氢气、一氧化碳、甲烷、乙烯、乙炔等。实验室需点燃易燃气体时要先检察其纯度,以免发生爆炸。 2. 易燃液体有醇、汽油、苯、乙醚、丙酮、乙酸乙酯等。不能直接加热易燃液体,若要加热,应在水浴或油浴中进行,易燃液体不能倒入下水道,应回收或作无害处理。 3. 易燃固体有白磷、红磷、硫、镁粉、萘、硝酸纤维、碱金属、磷化钙等。白磷在空气中易自燃,应保存在水中,切割白磷应在水中进行。金属钠、钾钙应保存在煤油中,锂包裹在石蜡中。若碱金属着火,应用砂或石棉灭火,不能用水、二氧化碳或由氯化碳作为灭火剂。 三、防挥发 易挥发的物质有挥发性酸与碱如浓盐酸、浓硝酸与氨水等,和某些有机物如醇、醛、羧酸、酯、乙醚、二硫化碳,以及汞、液溴等。这些试剂一般可通过油封、水封或蜡封的方法保存。 1. 油封:主要适用于浓盐酸、浓硝酸和氨水等无机液的保存,在液体面上加一薄层矿物油即可防止挥发。 2. 水封:如二硫化碳、汞等加水后可长期保存。 3. 蜡封:乙醚、乙醇、甲酸等比水轻易溶于的挥发液体,以及易挥发的固体如碘、萘等,应在瓶口进行蜡封。液溴在试剂瓶中用水封外,在瓶口还应蜡封,同时将蜡封后的瓶置于装有活性炭的塑料筒内,筒口再进行蜡封。 四、防变质 1. 防水:(1)三氯化磷、五氯化磷遇水强烈水解,为防止与空气中的水蒸气反应而变质,应蜡封。 (2)防结块:硝酸铵、硫酸钠等易吸水而结块,以致不能从试剂瓶中倒出,且易使玻璃试剂瓶破裂故应放在塑料瓶中,且应蜡封。 (3)漂白粉、过氧化钠、五氧化二磷、氧化钠、氧化钙、碳化钙、无水醋酸钠等易吸水变质,均应密封保存。 2. 防氧化:亚硫酸钠、硫酸亚铁、苯酚等在空气中易被氧化,应密封保存。 3. 防止与空气中的二氧化碳反应:硅酸钠、氢氧化钠、氢氧化钾、各种过氧化物等均易吸收空气中的二氧化碳而变质,应注意密封保存。 4. 为防止亚铁离子、亚锡离子的溶液水解以及被氧化,应在溶液中加几滴相应的酸并分别加入少量铁的锡,同时密封保存。 5. 防分解:浓硝酸、碳酸氢铵等受热易分解,应置于低温阴凉处。 6. 防风化:碳酸钠、硫酸铜等结晶水合物失去结晶水而风化,应密封保存。 五、防光 1. 硝酸银、卤化银、浓硝酸、氯水、过氧化氢等见光分解的试剂应保存在棕色瓶中若无棕色瓶可用黑纸包裹,且置于低温阴凉处。 2. 大部分有机试剂应避光保存在棕色瓶中。 六、防腐蚀 1. 取用强腐蚀性药品如强酸、强碱、浓氨水、三氯化磷、浓硫酸、溴水等时,一定在小心,宜戴上橡胶手套,护目眼镜。 2. 装具有强酸性如浓硫酸、浓硝酸、浓盐酸或强氧化性物质如高锰酸钾等药品的试剂瓶要用玻璃塞不能用橡皮塞或木塞,以免塞子被腐蚀并使药品变质。 3. 装苯、乙醚、四氯化碳等有机试剂的试剂瓶不能用橡皮塞,因为些试剂会溶解橡胶。 4. 装碱性强的物质如氢氧化钠、氢氧化钾、碳酸钠、氢氧化钡等试剂以及它们的水溶液的试剂瓶要用橡皮塞而不是用玻璃塞,以防瓶口与瓶塞粘结。
日前,国家药品不良反应监测中心发布了第39期《药品不良反应信息通报》并表示,近期国外药品管理部门发现苯佐卡因可能引起高铁血红蛋白血症的严重不良反应。考虑到此类风险在我国临床应用中也同样存在,且苯佐卡因产品多为非处方药,为使广大医务人员和患者及时了解该药品的使用风险,国家食品药品监督管理局提醒广大医务人员、药品生产企业和公众关注苯佐卡因引起高铁血红蛋白血症的安全性信息。 苯佐卡因是局部麻醉药,主要用于皮肤病止痒,创面、痔疮及溃疡面等止痛,在我国主要作为非处方药使用。 2011年4月,美国和加拿大药品管理当局发布警示信息,警惕苯佐卡因可能引起的严重不良反应高铁血红蛋白血症,涉及主要人群是2岁以下儿童,用药目的是使用苯佐卡因制剂缓解出牙引起的不适。 高铁血红蛋白血症虽然罕见,但为可危及生命的严重不良反应。高铁血红蛋白血症降低红细胞在全身输送氧气的能力,其体征和症状包括白色、灰色或蓝色皮肤、口唇和甲床,呼吸急促、乏力、意识错乱、头痛、头晕、恶心以及心率的变化。在罕见的情况下,高铁血红蛋白血症可以导致麻痹、昏迷甚至死亡。 FDA建议2岁以下儿童不要使用苯佐卡因产品,除非在医生的建议和监督下;成人使用苯佐卡因凝胶和溶液缓解口腔疼痛应严格按照产品说明书使用,并将本品放在儿童不能接触的地方。 虽然我国尚未收到苯佐卡因导致高铁血红蛋白血症的报告,但是国外药品不良反应监测数据表明,苯佐卡因可以引起高铁血红蛋白血症,此风险在我国临床应用中也同样存在。 国家食品药品监督管理局建议患者在使用含苯佐卡因药物时要严格按照说明书使用,如果在使用过程中出现高铁血红蛋白血症的体征和症状,如皮肤、口唇粘膜、甲床青紫,呼吸急促、心率加快、乏力、意识错乱、头痛、头晕等,请及时就医。2岁以下儿童应在医师指导下使用。 国家食品药品监督管理局建议生产企业及时完善产品说明书;增加相关安全性信息;加强合理用药的宣传,确保产品的安全性信息及时传达给患者和医生;并加强药品不良反应监测。 广大医务工作者、药品生产企业和公众如需了解详细信息,请登陆国家食品药品监督管理局网站(http://www.sfda.gov.cn)或国家药品不良反应监测中心网站(http://www.cdr.gov.cn)查询。
一、各种化学药品的管理。化验室的化学药品及试剂溶液品种很多,化学药品大多具有一定的毒性及危险性,对其加强管理不仅是保证分析数据质量的需要,也是确保安全的需要。化验室只宜存放少量短期内需用的药品。化学药品建议按无机物、有机物、生物培养剂分类存放,无机物按酸、碱、盐分类存放,盐类中按金属活跃性顺序分类存放,生物培养剂按培养菌群不同分类存放,其中属于危险化学药品中的剧毒品应锁在专门的毒品柜中,由专人加锁保管、实行领用经申请、审批、双人登记签字的制度。(一)、哪些是属于危险品的化学药品:1、易爆和不稳定物质。如浓过氧化氢、有机过氧化物等。2、氧化性物质。如氧化性酸,过氧化氢也属此类。3、可燃性物质。除易燃的气体、液体、固体外,还包括在潮气中会产生可燃物的物质。如碱金属的氢化物、碳化钙及接触空气自燃的物质如白磷等。4、有毒物质。5、腐蚀性物质。如酸、碱等。6、放射性物质。(二)、化学试剂的使用管理制度1、要遵循既有利于使用,又要保证安全的原则,管好用好化学药品,加强安全教育。2、化学药品必须根据化学性质分类存放,易燃、易爆、剧毒、强腐蚀品不得混放。化学药品要存放在专用柜内,有存放专用柜的储藏室;有阴凉、通风、防潮、避光等条件;有防火防盗安全设施。3、所有药品必须有明显的标志。对字迹不清的标签要及时更换,对过期失效和没有标签的药品不准使用,并要进行妥善处理。4、试验药剂容器都要有标签,对分装的药品在容器标签上要注明名称、规格、浓度;无标签或标签无法辩认的试剂都要当成危险物品重新鉴别后小心处理,不可随便乱扔,以免引起严重后果。实验室中摆放的药品如长期不用,应放到药品储藏室,统一管理。5、化学药品盛装容器应封闭,防止漏气、潮解。见光容易起变化的化学药品应装在深色的玻璃容器或避光的容器里,对化学药品包装和药品质量要定期检查。6、要加强对火源的管理。化学药品储藏室周围及内部严禁火源;实验室的火源要远离易燃、易爆物品,有火源时,不能离人。7、储存的易燃易爆物品应避光、防火和防电等,实验室存放的易燃易爆物品,要确定合理的储存量,不许过量且包装容器应密封性好。易燃易爆试剂应贮于铁柜(壁厚1mm以上)中,柜子的顶部都有通风口。遇水能分解或燃烧、爆炸的药品,钾、钠、三氯化磷、五氯化磷、发烟硫酸、硫磺等不准与水接触,不准放置于潮湿的地方储存。8、危险物品的采购和提运按公安部门和交通运输部门的有关规定办理。剧毒、放射性物体及其它危险物品,要单独存放,由双人双锁专人管理。存放剧毒物品的药品柜应坚固、保险,要健全严格的领取使用登记。9、要经常检查危险物品,防止因变质、分解造成自燃、自爆事故。对剧毒物品的容器、变质料、废渣及废水等应予妥善处理。10、不外借药品,特殊需要借药品时,必须经领导批准签字。11、取用化学试剂的器皿必须分开,每种试剂用一件器皿,不得混用。12、使用有机溶剂和挥发性强的试剂的操作应在通风良好的地方或在通风橱内进行。任何情况下,都不允许用明火直接加热有机溶剂。13、凡使用强酸强碱等化学试剂时,应按规定要求操作和贮存。
[center]欧盟重新修订草本药品GMP指南 提高草本药物入市门槛[/center] 中国医药保健品进出口商会消息,日前,欧盟正式公布了经过修订的欧盟人用药品与兽药GMP指南的附录7部分。此部分针对草本药品,内容涉及原则、厂房与设备、文件和质量控制等方面,尤其对于起始物料的控制、贮存和加工过程有了明确规定。修订版本将从2009年9月1日开始实施。医保商会的专家认为,此次对草本药品GMP进行的修订,意味着欧盟进一步提高了草本药品的入市门槛。 据了解,在修订版本的原则部分,此次清晰地定义了草本药品制造过程中的起始物料可以是药用植物、草本物质或草本制剂。在对厂房与设备的规定中,强调草本物质应当储存在隔离区域,以防止虫咬、发酵、霉变及交叉污染等,并对清洁度、湿度、温度、避光保护、可监控等提出了要求;在生产区域里,强调对除尘系统、专用厂房等方面的要求;用于制造过程的设备、过滤材料等,要求一定要相容于提取溶剂,以防止任何物质释放到溶剂中,或有任何物质吸附到设备或过滤材料上,从而影响产品质量。 对文件系统的规定,要求有起始物料的详细说明,包括供应商的审计记录,供应商是否符合良好种植和采集规范等;在规格标准方面,要记录各种名称、来源细节、干燥系统、辨别实验、水分规定、微生物污染、有毒金属及类似污染物、活性成分含量分析、外源物质测定等等;在工艺指令方面,要求记录所有操作过程,容器检查情况、过滤筛分方法等,制剂厂家要记录溶剂、时间、温度等详细内容以及详细的浓缩步骤和使用的方法。 对于质量控制方面的规定,主要是针对取样的要求,如人员的专业性、对照样品的有关规定等。 医保商会的专家认为,随着欧盟植物药市场需求的不断扩大,相关的市场监管也会越来越严格,中国企业要想进入该市场,就必须随时注意了解相关信息,并严格按照其要求去规范生产和管理,尤其在相关标准方面要早动手,早做准备。
实验室常见的有毒有害的化学药品和试剂一、致癌物质黄曲霉素B1、亚硝胺、3-4苯并芘等(以上为强致癌物质)、2-乙酰氨基芴、4-氨基联苯、联苯胺及其盐类、3-二氯联苯胺、4-二甲基氨基偶氮苯、1-萘胺、2-萘胺、4-硝基联苯、N-亚硝基二甲胺、β-丙内脂、4-甲叉(双)-2-氯苯胺、乙撑亚胺、氯甲甲醚、二硝基萘、羧基镍、氯乙烯、同苯二酚、二氯甲醚等。二、剧毒六氯苯、羧基铁、氰化钠、氢氟酸、氢氰酸、氯化氰、氯化汞、砷酸汞、汞蒸气、砷化氢、光气、氟光气、磷化氢、三氧化二砷、有机砷化物、有机磷化物、有机氟化物、有机硼化物、铍有其化合物、丙烯腈、乙腈等。三、高毒氟化钠、对二氯苯、甲基丙烯腈、丙酮氰醇、二氯乙烷、三氯乙烷、偶氮二异丁腈、黄磷、三氯氧磷、五氯化磷、三氯化磷、五氧化二磷、三氯甲烷、溴甲烷、二乙烯酮、氧化亚氮、铊化合物、四乙基铅、四乙基锡、三氯化锑、溴水、氯气、五氧化二钒、二氧化锰、二氯硅烷、三氯甲硅烷、苯胺、硫化氢、硼烷、氯化氢、氟乙酸、丙烯醛、乙烯酮、氟乙酰胺、碘乙酸乙酯、溴乙酸乙酯、氯乙酸乙酯、有机氰化物、芳香胺、迭氮钠、砷化钠等。看看你们的实验室里面都有那些有毒有害的药品和试剂,安全第一,防患于未然
9月12日,国家食品药品监督管理总局公布了关于公布第一批过度重复药品品种目录的公告。公告原文如下:为更好地引导药品合理申报,避免市场药品同水平重复,防止研发投入风险,促进药品产业健康发展,依据《中华人民共和国药品管理法》、《药品注册管理办法》等有关法律法规,国家食品药品监督管理总局对在国内已上市药品和正在申报注册的药品进行全面调查,选出第一批过度重复的已上市药品品种34个、过度重复申报注册的药品品种16个,现予以公布(见附件)。国家食品药品监督管理总局提醒相关单位,应充分了解市场供需状况,评估药品研发风险,慎重进行投资经营决策。各省、自治区、直辖市食品药品监督管理部门要加强对相关药品注册申请的受理审查、研制现场核查和生产现场检查,对已经公布的过度重复药品品种,做好宣传引导工作。特此公告。国家食品药品监督管理总局2014年9月12日附件一:过度重复的已上市药品品种目录序号活性成分通用名给药途径1葡萄糖注射2维生素C口服3安乃近口服4对乙酰氨基酚口服5复方磺胺甲恶唑口服6氯化钠/葡萄糖注射7土霉素口服8氯化钠注射9小檗碱注射10诺氟沙星口服11维生素B1口服12对乙酰氨基酚/咖啡因/马来酸氯苯那敏/人工牛黄口服13四环素口服14利福平口服15红霉素口服16维生素C注射17乙酰螺旋霉素口服18甲硝唑口服19头孢氨苄口服20西咪替丁口服21氨基比林/非那西丁口服22氯霉素口服23肌苷口服24异烟肼口服25阿司匹林口服26呋喃唑酮口服27布洛芬口服28萘普生口服[td=1,1,11
化学药品管理、使用制度一、要遵循既有利于使用,又要保证安全的原则,管好用好化学药品,加强安全教育。二、化学药品必须根据化学性质分类存放,易燃、易爆、剧毒、强腐蚀品不得混放。化学药品要存放在专用橱(柜)内,有存放专用橱(柜)的储藏室;有阴凉、通风、防潮、避光等条件;有防火防盗安全设施。三、存放药品要专人管理、领用,存放要建帐,所有药品必须有明显的标志。对字迹不清的标签要及时更换,对过期失效和没有标签的药品不准使用,并要进行妥善处理。四、试验药剂容器都要有标签,对分装的药品在容器标签上要注明名称、规格、浓度;无标签药品,不能擅自乱扔、乱倒,必须经化学处理后方可处置。实验室中摆放的药品如长期不用,应放到药品储藏室,统一管理。五、化学药品盛装容器应封闭,防止漏气、潮解。见光容易起变化的化学药品应装在深色的玻璃容器或避光的容器里,对化学药品包装和药品质量要定期检查。六、要加强对火源的管理。化学药品储藏室(橱)周围及内部严禁火源;实验室的火源要远离易燃、易爆物品,有火源时,不能离人。七、储存的易燃易爆物品应避光、防火和防电等,实验室存放的易燃易爆物品,要确定合理的储存量,不许过量且包装容器应密封性好。遇水能分解或燃烧、爆炸的药品,钾、钠、三氯化磷、五氯化磷、发烟硫酸、硫磺等不准与水接触,不准放置于潮湿的地方储存。八、危险物品的采购和提运按公安部门和交通运输部门的有关规定办理。剧毒、放射性物体及其它危险物品,要单独存放,由双人双锁专人管理。存放剧毒物品的药品柜应坚固、保险,要健全严格的领取使用登记。九、要经常检查危险物品,防止因变质、分解造成自燃、自爆事故。对剧毒物品的容器、变质料、废渣及废水等应予妥善处理。十、管理人员要建立化学药品(化学药品)各类帐册,药品购进后,及时验收、记帐,使用后及时消帐,掌握药品的消耗和库存数量;不外借(给)药品,特殊需要借(给)药品时,必须经领导批准签字。
实验室试剂药品的存放要求1试剂的规格和分类: 化学试剂按其纯度和杂质杂志含量的高低分为四种等级。化学试剂的级别分为:试剂级别:一等品;二等品;三等品;四等品;纯度分类:优级纯(GR);分析纯(AR);化学纯(CP);实验试剂(LR)标签颜色:绿色;红色;蓝色;黄色(1)优级纯试剂,亦称保证试剂,为一级品,纯度高,杂质极少,主要用于精密分析和科学研究,常以GR表示。(2)分析纯试剂,亦称分析试剂,为二级品,纯度略低于优级纯,杂质含量略高于优级纯,适用于重要分析和一般性研究工作,常以AR表示。(3)化学纯试剂为三级品,纯度较分析纯差,但高于实验试剂,适用于工厂、一般性的分析工作,常以CP表示。(4)实验试剂为四级品,纯度比化学纯差,但比工业品纯度高,主要用于一般化学实验,不能用于分析工作,常以 LR表示。除上述几个等级外,还有基准试剂、光谱纯试剂及超纯试剂等。基准试剂相当或高于优级纯试剂,专作滴定分析的基准物质,用以确定未知溶液的准确浓度或直接配制标准溶液,其主成分含量一般在99.95%~100.0%,杂质总量不超过0.05%。光谱纯试剂主要用于光谱分析中作标准物质,其杂质用光谱分析法测不出或杂质低于某一限度,纯度在99.99%以上。超纯试剂又称高纯试剂,是用一些特殊设备如石英、铂器皿等特殊设或工艺生产的。2试剂药品的存放要求:试剂在贮存时常因保管不当而变质。有些试剂容易吸湿而潮解或水解;有的容易跟空气里的氧气、二氧化碳或扩散在其中的其他气体发生反应,还有一些试剂受光照和环境温度的影响会变质。因此,必须根据试剂的不同性质,分别采取相应的措施妥善保存(这句话很重要!!试剂的存放不能找出一个万能的通用方法)。一般有以下几种保存方法:1.密封保存试剂取用后一般都用塞子盖紧,特别是挥发性的物质(如硝酸、盐酸、氨水)以及很多低沸点有机物(如乙醚、丙酮、甲醛、乙醛、氯仿、苯等)必须严密盖紧。有些吸湿性极强或遇水蒸气发生强烈水解的试剂,如五氧化二磷、无水AlCl3等,不仅要严密盖紧,还要蜡封。在空气里能自燃的白磷保存在水中。活泼的金属钾、钠要保存在煤油中。2.用棕色瓶盛放和安放在阴凉处避光保存光照或受热容易变质的试剂(如浓硝酸、硝酸银、氯化汞、碘化钾、过氧化氢以及溴水、氯水)要存放在棕色瓶里,并放在阴凉处,防止它分解变质。3.危险药品或者相互反应的药品分开存放具有易发生爆炸、燃烧、毒害、腐蚀和放射性等危险性的物质,以及受到外界因素影响能引起灾害性事故的化学药品,都属于化学危险品。它们存放一定要单独存放,例如高氯酸不能也有机物接触,否则易发生爆炸。强氧化性物质和有机溶剂能腐蚀橡皮,不能盛放在带橡皮塞的玻璃瓶中。容易侵蚀玻璃而影响试剂纯度的试剂,如氢氟酸、含氟盐(氟化钾、氟化钠、氟化铵)和苛性碱(氢氧化钾、氢氧化钠),应保存在聚乙烯塑料瓶或涂有石蜡的玻璃瓶中。剧毒药品必须存放在保险柜中,加锁保管。取用时要有两人以上共同操作,并记录用途和用量,随用随取,严格管理。腐蚀性强的试剂要设有专门的存放橱。3进一步说明:试剂药品的保存肯定不仅仅是上面几条就可以涵盖,需要根据使用要求,试剂本身的性质来制定保存的方案,欢迎各位同行补充
一个朋友想个人做个药品检测,但询问了几家药检所,都说不对个人?谁知道为什么食品药品检验机构不受理个人对药品的委托检测?难道个人消费者不算客户?通过认可的实验就是这样选择服务客户?
1. 对于实验室领用后暂时不用的危险化学品应存放于固定存放点;2. 保证与禁忌物分开存放并保证与“避免接触的条件”不接触;3. 并做好防挥发、防泄露、防火等安全措施;4. 有毒的化学品,要由专人负责保管,对药品的使用及领取作详细记录;5. 使用腐蚀性化学品时要注意个人的防护;6. 禁止口尝、直接鼻嗅、手直接接触的方法鉴别化学药品或危险物质。7. 用移液管、吸管吸取有毒或腐蚀性液体时,严禁用嘴直接吸。8. 药品在器皿中加热时,必须放置平稳,瓶口或管口禁止对着人;在移动沸腾的液体时,应放置在隔热石棉网上,轻拿轻放。9. 不能把浓酸、浓碱气化剂和有机物质放在一起,否则会引起爆炸和燃烧。10. 使用易燃易爆化学品时,应在通风橱内进行,远离热源、火源,在使用过程中需要加热挥发,须采用水浴加热,严禁用明火,并在通风橱内进行(电源开关、电源插头等须在通风橱外)。11. 对于无标签或掉标签的药品需要经过鉴定,贴上标签后方可使用,无法鉴定的药品和试剂按危险物处理,严禁使用不明内容物的药品。12. 使用药品时,药品瓶应轻拿轻放,避免碰撞以致打碎药瓶。
(港、澳、台)化学药品医药产品注册 2006年02月20日 发布 一、项目名称:(港、澳、台)医药产品注册 二、许可内容: (港、澳、台)化学药品医药产品注册,其分类按《药品注册管理办法》附件二注册分类,即: 注册分类1、未在国内外上市销售的药品: 注册分类3、已在国外上市销售但尚未在国内上市销售的药品: 三、设定和实施许可的法律依据: 《中华人民共和国药品管理法》第三十九条、《中华人民共和国药品管理法实施条例》第二十九条、《药品注册管理办法》 四、收费: 进口药审评及审批收费45300元。 完成临床以后的注册申请,因申请进口临床试验时已收费,故不收费。 收费依据:《国家计委、财政部关于调整药品审批、检验收费标准的通知》[计价格(1995)340号]。 五、数量限制:本许可事项无数量限制 六、申请人提交材料目录: 《进口药品注册申请表》 (一)综述资料: 资料编号1、药品名称; 资料编号2、证明性文件; 资料编号3、立题目的与依据; 资料编号4、对主要研究结果的总结及评价; 资料编号5、药品说明书、起草说明及相关参考文献; 资料编号6、包装、标签设计样稿。 (二)药学研究资料: 资料编号7、药学研究资料综述; 资料编号8、原料药生产工艺的研究资料及文献资料;制剂处方及工艺的研究资料及文献资料; 资料编号9、确证化学结构或者组份的试验资料及文献资料; 资料编号10、质量研究工作的试验资料及文献资料; 资料编号11、药品标准及起草说明,并提供标准品或者对照品; 资料编号12、样品的检验报告书; 资料编号13、原料药、辅料的来源及质量标准、检验报告书; 资料编号14、药物稳定性研究的试验资料及文献资料; 资料编号15、直接接触药品的包装材料和容器的选择依据及质量标准 。 (三)药理毒理研究资料: 资料编号16、药理毒理研究资料综述; 资料编号17、主要药效学试验资料及文献资料; 资料编号18、一般药理学的试验资料及文献资料; 资料编号19、急性毒性试验资料及文献资料; 资料编号20、长期毒性试验资料及文献资料; 资料编号21、过敏性(局部、全身和光敏毒性)、溶血性和局部(血管、 皮肤、粘膜、肌肉等)刺激性等特殊安全性试验资料和文献资料; 资料编号22、复方制剂中多种成份药效、毒性、药代动力学相互影响的试验资料及文献资料; 资料编号23、致突变试验资料及文献资料; 资料编号24、生殖毒性试验资料及文献资料; 资料编号25、致癌试验资料及文献资料; 资料编号26、依赖性试验资料及文献资料; 资料编号27、非临床药代动力学试验资料及文献资料。 (四)临床试验资料: 资料编号28、国内外相关的临床试验资料综述; 资料编号29、临床试验计划及研究方案; 资料编号30、临床研究者手册; 资料编号31、知情同意书样稿、伦理委员会批准件; 资料编号32、临床试验报告。 以上申报材料具体要求详见《药品注册管理办法》附件二。 七、对申请资料的要求: (一)申报资料的一般要求: 1、申报资料首页为申报资料项目目录,目录中申请资料项目按《药品注册管理办法》(国家食品药品监督管理局令第17号)附件二的顺序排列。每项资料封面上注明:药品名称、资料项目编号、项目名称、申请机构联系人姓名、电话、地址。 2、申报资料应使用A4规格纸打印或复印,内容完整、规范、清楚,不得涂改,数据真实、可靠。 3、资料按套装入档案袋,档案袋封面注明:申请分类、注册分类、药品名称、本袋所属第X套第X袋每套共X袋、原件/复印件 联系人、联系电话、申请注册代理机构名称。 4、注册申请报送2套完整申请资料(至少1套为原件)和1套综述资料复印件,申请表4份(2份原件,2份复印件)分别装入各套资料中(全套原件资料内放入1份申请表原件,1份申请表复印件)。 5、《进口药品注册申请表》:从国家食品药品监督管理局网站(www.sfda.gov.cn)下载,按要求填写后打印并保存,要有境外申请人的盖章或签字及国内代理机构盖章签字。 6、申请人对下述药品注册申报资料应当同时提交电子文本:资料编号:1、3~7、16和28;以上项目资料中的证明性文件、图形图像或者文献资料的复印件,可暂不要求提供电子文本。 7、在邮寄或者递交申请资料前应将申请表的电子版发送到以下药品注册专用电子邮箱地址:ypzcsl@sda.gov.cn和ypzcsl@nicpbp.org.cn 和ypzcsl@vip.sina.com和ypzcsl@vip.163.com。 8、待确定我局已经收到电子资料后,向我局提交或邮寄申报资料的纸质资料。 9、电子版资料与纸质资料应相同,申请表的核对码应一致。 10、外文资料应翻译成中文。 (二)申报资料的具体要求: 1、《进口药品注册申请表》的填写应准确、规范,符合填表说明的要求。 (1)药品注册分类:参照《药品注册管理办法》(国家食品药品监督管理局令第17号)附件的相应条款填写。申请未在国内外获准上市销售的药品,按照注册分类1类的规定报送资料;其他品种按照注册分类3类的规定报送资料.属于注册分类1类的药物,应当至少是已在国外进入II期临床试验的药物. (2)附加申请事项:可同时提出非处方药等附加申请。 (3)规格:申请注册的药品有多个规格的,应当根据提交资料是否独立成套确定规格项填写一个或多个规格;各规格独立成套的,一表一规格,各自发给受理号;各规格资料共用一套,一表填入多个规格,只发给一个受理号。
[center]药品标准与药品批准文号综述[/center]1 国家药品标准1.1 建国以来,卫生部和SDA颁布的国家药品标准《中华人民共和国药典》 (以下简称中国药典)有1953年版、1963年版、1977年版、1985年版、 1990年版、1995年版、2000年版和2005年版, 1985年版以后的各版《中国药典》都颁布有增补本。1.2 卫生部颁布的国家药品标准有1963年版抗菌素部颁标准,以后数年大多颁布的是单行本的部颁药品标准。 1.3 1989年5月31日,卫生部发布《关于颁布第一批“乙肝扶正胶囊”等一百七十种中成药“卫生部药品标准”的通知》[卫药发(89)第28号],即《部颁标准“中药成方制剂” (第一册)》,该《通知》规定:《部颁标准“中药成方制剂”(第一册)》从1991年1月1日起开始执行,升为部颁标准后的同品种原地方药品标准即停止使用。从此以后,卫生部共颁布了中成药部颁标准1~20册、化学药品部颁标准1~6册。这些药品标准目前正在使用。 1.4 1998年SDA和2003年SFDA成立后,共颁布了局颁中药标准1—14册、化学药品标准1~16册、局颁新药转正标准1~45册。这些药品标准目前正在使用。 2 地方药品标准 2.1 1978年7月30日,国务院颁布《药政管理条例》(试行)(国发[1978]154号),该《条例》第十九条规定:“药品标准是国家对药品质量规格和检验方法所作的技术规定,必须遵照执行。药品标准分为三类:第一类:国家标准,即中华人民共和国药典(简称《中国药典》);第二类:卫生部颁发的药品标准(简称部颁标准);第三类:,地方标准,即各省、市、自治区卫生局审批的药品标准”。地方药品标准的法律地位首次以法规的形式予以明确规定,与中国药典、部颁标准一样作为药品生产、经营、使用、检验和药品监督管理部门共同遵循的法定依据。 2.2 1980年9月10日,卫生部颁布《药品标准工作管理办法》,该《办法》对中国药典、部颁标准、地方药品标准各自应收载的药品范围作了具体的划分。之后,各省级卫生厅(局)相继发布地方药品标准。 2.3 1984年9月20日,全国人大常委会六届七次会议通过的1985年7月1日实施的《中华人民共和国药品管理法》(以下简称《药品管理法》)第二十三条规定:“药品必须符合国家标准和省、自治区、直辖市药品标准。”地方药品标准又由国家以法律的形式确定其法律地位。2.4 1986年,卫生部开始进行地方药品标准的再评价工作,对中西药地方药品标准分期分批地开展整顿,拟逐步形成以国家药品标准为主体的药品标准。整顿的主要原因是各省之间制定的地方药品标准的技术规定差距较大,地方药品标准过多过滥。整顿的内容主要为同方异名、同名异方、药品组方不合理、药品疗效不确切等问题。 2.5 1994年8月17日,卫生部发布《关于中成药整顿工作有关问题的通知》[卫药发(1994)第 30号],该《通知》第二条规定: “根据我部卫药字(90)第?号文件精神,全面推行中成药国家标准,加速省(区、市)标准逐步过渡到国家药品标准的进程,争取1995年上半年完成中成药整顿全部品种的医学审查工作,1996年完成药学审查和部颁标准的颁布工作”。 2.6 1995年10月6日,卫生部发布《关于中成药国家标准问题的通知》 [卫药发(1995)第69号],该《通知》第1条规定: “根据卫药发 (1994)第30号文‘1996年完成药学审查和部颁标准的颁布工作’和卫药字(90)第7号文‘对治疗性中成药在1996年以后将全部实行国家药品标准的做法’的要求,请各地和药典会加快部颁标准的起草和审核工作,以使中成药品种由地方标准过渡到国家标准顺利进行”。第3条规定:“凡国家已颁布的中药品种质量标准,任何单位和个人必须坚决执行,同时原质量标准废止。如发现不按国标生产,或在流通和使用时发现与国标不符的药品,一律按《药品管理法》有关规定以劣药论处”。2.7 2001年2月16日,SDA发布《关于强化中成药国家标准管理工作的通知》(国药监注[2001] 83号),该《通知》就解决中成药地方标准的基本原则、方法和要求作了具体规定,并规定从2003年1月1日起,地方药品标准品种不得在市场上流通。 2.8 2001年2月28日,全国人大常委会九届二十次会议通过的2001年12月1日实施的《药品管理法》(修订)第三十二条规定:“药品必须符合国家标准”。“国务院药品监督管理部门颁布的《中华人民共和国药典》和药品标准为国家药品标准”。明确地取消了地方药品标准。 2.9 2001年11月30日,SDA发布《关于有关地方药品标准执行问题的公告》 (国药管注[2001] 522号),《公告》的事项是《国务院办公厅关于施行(药品管理法有关药品标准延期执行问题的复函》(国办函[2001]68号):“从2001年12月1日起至2002年11月30日,国家药品监督管理局应当对《药品管理法》修订前各省、自治区、直辖市药品监督管理部门按照当时实行的地方药品标准批准生产的药品品种,逐个进行审查,经审查,对符合《中华人民共和国药品管理法》有关规定的,纳入国家药品标准,可以继续生产;对不符合规定的,立即停止该品种的生产并撤销其批准文号”。 2.10 按照地方标准生产药品的使用期限 2.10.1 2001年3月25日,SDA印发《关于妥善处理地方标准品种问题的通知》(国药监注(20013 96号),该《通知》规定:“(一)未纳入国家药品标准管理的地方药品标准品种应立即停止生产、销售和使用。(二)已纳入国家药品标准管理的原地方药品标准品种,有关药品生产企业应按我局颁布的国家药品标准组织生产;尚未换发批准文号的,可以使用原地方批准文号。按照国家药品标准生产的药品,可以在药品的有效期内流通和使用。(三)已纳入国家药品标准管理的原地方药晶标准品种,按照原地方药品标准生产的药品,可流通和使用至 2003年12月31日”。 2.10.2 SDA和SFDA2003年底以前共公布了三批停止使用的化学药品地标品种,规定被停止使用的化学药品标准从发文之日起,不再具有法律效力。在此之前生产并在市场上流通的品种,由生产企业在6个月内自行收回销毁。

实验室药品的摆放实验室中的药品可按单质(金属与非金属)、氧化物、酸、碱和 盐分类。根据药品性质,酸性物质和碱性物质,氧化剂和还原剂不能混在一起存放,固体试剂与配置溶液也要分开;易挥发的药品要用蜡密封保存,时间长的话可涂些石蜡;见光易变质的药品要避光保存;易燃药品要特殊保管;贵重药品、剧毒药品及强腐蚀性药品要封好瓶口放入专柜。实验室仪器的摆放化学实验室仪器大致可以分三类:精密仪器、玻璃仪器、木制和金属制器材等。它们各有各自的存贮要求,在管理中应该有所区别。玻璃仪器特点是种类多,数量大、易碰碎。应按仪器的性能(存储类:广口瓶,细口瓶,滴瓶。容器类:试管,烧杯,烧瓶,锥形瓶,量筒,漏斗等。加热类:酒精灯,酒精喷灯,燃烧匙。其他类等)、分规格分类存放;对于一些磨口器皿,如各种试剂瓶,用完洗净后要在磨口上涂一薄层凡士林或垫一层纸片,避免因长期不用而粘在一起,如果分不开,可用木棒轻轻敲击,就可分开。有些带活塞的仪器,如分液漏斗等,把活塞用橡皮筋与仪器拴在一起,既便于操作,也可防止活塞脱落或配错,能避免不必要的损失和消耗。还有一些铁制仪器:如铁架台、坩埚钳、止水夹、镊子等,用完后要保持干燥,若有必要,还可涂些油等防止锈蚀。实验完毕后应该及时清洗干净放回原处,以免损坏或丢失,从而造成损失。实验室药品试剂管理普遍存在哪些问题?1.无试剂专库。试剂储藏室与实验准备在同一房间内,致使室内空气的相对湿度过大,药品试剂易变质失效。2.保管环境不良。缺乏良好的通风设备,既影响药品试剂的质量,也影响工作人员的身体健康。3.无清库制度。某些试剂库存时间过长、库存过多,造成浪费。4.缺乏规范分类知识与措施。药品试剂分类不科学,使用不方便。5.环保意识差。过期药品试剂不经过无害处理就随意丢弃。如何进行科学管理?实验室应实施七项管理原则:Ø 专人专库专柜原则;Ø 分类保管原则;Ø 先出先用原则;Ø 定期查、报原则;Ø 出入库登记原则;Ø 危险品“五双管”原则;Ø 注意环保原则。1. 专人、专库、专柜管理原则设定具有相应专业水平、管理水平和高度责任心的专职管理人员,从事药品试剂的保管工作,管理人员必须熟悉药品试剂的性能、用途、保存期、贮存条件等。设立独立、朝北的房间作为储藏室。挂窗帘,避免阳光直射(室湿过高导致试剂分解失效)。室内安装通风换气设备,不设水池,以保证室内空气干燥。将试剂柜架制成阶梯状,并从上到下依次编序。试剂柜安装有色玻璃。特殊试剂的试剂柜,应选用耐腐蚀或具有屏蔽作用材料做成的各小柜的组合体,各小柜之间密封性要好,有利于特殊试剂的隔离存放。2. 分类保管的原则合理的系统分类,是良好的规范化管理的必要保证。将所有药品试剂分类依其名称、规格、厂家、批号、包装、储存量以及储存位置一一登记造册、编号,并建立查找方式。药品柜贴上本柜贮存的药品目录,方便取用。(1)药品试剂一般分类、存放方法,见下表:http://ng1.17img.cn/bbsfiles/images/2016/01/201601271515_583692_1321233_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/01/201601271515_583693_1321233_3.jpg3.先出先用原则根据出厂日期和保质期,先出厂的或保质期快到的药品试剂应先用,以免过期失效,造成浪费。4.定期查、报原则查看储藏室内药品试剂保存环境的条件是否合格,如有变化,立刻采取措施;查看药品试剂的瓶签,如被腐蚀,应立即重新补写,写明试剂名称、规格、分子式、分子量等,不可只写名称;查包装,如有破损,立即采取弥补措施;查试剂质量,如有失效,应立刻清理出柜;查库存量,决定采购与否。5. 出入库登记原则设立药品试剂入账本和出账本,做好领用登记。6.危险品“五双管”原则双人保管;双人收发;双人领料;双本帐;双锁。7.注意环保原则管理人员应具有强烈的环保意识以及相应的环保知识,对失效、变质的药品试剂应集中存放,小心保管,尽快由专业人员或在专业人员指导下进行无害处理,切不可将未经处理的药品试剂,随意丢入垃圾箱或冲入下水道,避免造成对环境的污染或意外事故的发生。
如题,我觉得有可能,苯甲酸含量较大,或与主药成盐不是很稳定,都应该测苯甲酸的含量以控制整个药品的质量啊。不知道大家知道这种情形不?
苯酚(酚) C6H5OH(Phenol)(一)理化性状和用途无色或粉红色晶体。易溶于乙醇和乙醚,有特臭味。密度:1.1,熔点:41℃,闪点:78℃,沸点:182℃。蒸汽密度:3.2,自燃点:710℃,易溶于水。用于生产炸药、油漆、橡胶、酚醛树脂、织物和药品。(二)毒性属高毒类,为细胞原浆毒物。对皮肤和粘摸有强烈腐蚀作用。最高容许浓度:5mg/m3。(三)短期暴露的影响吸入:如吸入高浓度酚蒸汽,可迅速发生头痛、眩晕、无力、虚脱。皮肤:酚液污染皮肤可造成皮肤化学灼伤。酚大面积(占体表面积的25%)接触皮肤,可造成皮肤吸收致死。口服:误服酚,可引起口腔和咽喉强烈的灼伤和腹痛,吐血性液体,全身冷汗,休克。还可能引起胃肠穿孔。口服致死量2~15g。(四)长期暴露的影响长期吸入低浓度的酚,可有呕吐、吞咽困难、腹泻于食欲减退、头痛、眩晕等症状。长期接触酚,可引起褐黄病。表现胃眼孔膜褐耳壳上色素沉着,色素为棕褐色或黑色。(五)火灾和爆炸本品可燃,应禁明火及吸烟。于78℃以上时其蒸汽与空气混合物(3~10%)具爆炸性,此时必须密封操作并加强通风。着火时,用大量喷水、二氧化碳、干粉等办法灭火。(六)化学反应性本品能腐蚀铅、锌和铝。(七)人身防护吸入:如蒸汽浓度超过暴露限值时应佩戴防毒口罩。眼睛:戴化学防溅眼镜。皮肤:使用手套、工作服、工作鞋。工作场所应备有可用的安全淋浴和眼睛冲洗器具。(八)、急救吸入:将患者移离现场至新鲜空气处。眼睛:酚液溅入眼内,应立即张开眼睑,用清水冲至少20分钟。皮肤:酚液污染皮肤后,应立即脱去衣服,长时间用大量水冲洗皮肤后,再用聚乙烯乙二醇和酒精混合液擦洗。口服:应分秒必争地抢救。如患者意识清楚,立即口服植物油15-30毫升,随即使之吐出并急送医院救治。注:所有患者都应请医生或送至最近医疗机构救治。(九)、储藏与运输防火、干燥。包装号为:2、5、6、8。(十)、安全与处理凡加热酚的操作,应采取密闭,辅以吸风装置以及防皮肤接触。在冲洗酚的容器时,应加强个人防护。
化学试剂和药品是实验室必备的物品,如果保存管理不当就会对人类健康造成威胁,本文就如何妥善管理这些物品提出几点建议,来规范实验室化学品的管理。 (一)化学试剂、药品的贮存 1.化学药品贮存室应符合有关安全规定,有防火、防爆等安全措施,室内应干燥、通风良好,温度一般不超过28℃,照明应是防爆型。 2.化学药品贮存室应由专人保管,并有严格的账目和管理制度。 3.室内应备有消防器材。 4.化学药品应按类存放,特别是化学危险品按其特性单独存放。
化 学 药 品 的 管 理 2.1 药品的贮存 (1) 药品贮存不当,就会发生事故。 例如在实验室桌上放一个玻璃瓶,瓶后放了一瓶乙醚,阳光射在玻璃瓶上,如果正好聚焦於乙醚瓶,乙醚温度会骤升,瓶内产生高压,将塞子冲开,或瓶子炸裂,瓶中的乙醚蒸气被聚光点着,可能发生爆炸。 又如将活性碳放在硝酸旁边,不慎二个瓶子都破了,二者互相反应着火,引着其他药品,后果亦不堪设想。 贮存药物的原则 ①所有药品都有明显标签,标明药品名称、质量规格及来货日期;最好还有危险性质的明显标志。 标签日久会受腐蚀气体损坏,甚至全部剥落,如果不及时换新标签,就会变成无名物,有误用的危险。 注上来货日期,或制造日期,对於易变质物可以正确判定应否销毁。 ②分类存放,互相作用药品不能混放,必须隔离存放。易燃物、易爆物及强氧化剂只能少量存放。 ③贮存室或药柜必须保持整齐清洁。 ④经常检查药品瓶子或其他包装完整情况,标签是否完整,有无其他危险潜伏。 ⑤无名物、变质物要及时清理销毁。 (2)危险药物分类存放的原则及存放要求 ①易挥发药品:远离热源火源,于避光阴凉处保存,通风良好,不能装满。 这类药品多属一级易燃物、有毒液体。对这类药品贮存要加以特别注意,最好保存在防爆冰箱内,家庭冰箱指示灯、恒温控制开关、马达起动都可能打火,因此使用家庭冰箱时,不要联接内指示灯,并将冰箱放在宽阔通风良好处,这样冷冻机排出的热气便易於散开。 大量易燃物存放室应隔离建造,或在一楼,符合易燃物建筑标准。 存放易燃物的地方应挂有易燃物标志和不准吸烟的牌子。 存放易燃物室内应通风良好,但是室内不应有排风扇。 存放附近应有灭口器材及处理洒出药物的器材。 ②腐蚀性液体:放於底下,以免不慎跌下,洒出发生烫伤事故。 ③发生有毒气体或烟雾的药品:存於通风橱中。 ④剧毒药品:锁上。 ⑤致癌药品:有致癌药品的明显标志,锁上。 ⑥互相作用的药品:隔离存放。 ⑦特别保存的物品: 金属钠、钾等碱金属,贮於煤油中。黄磷,贮於水中。上述两种药物,很易混淆,要隔离贮存。苦味酸,湿保存,要时常检查是否放干了。镁、铝(粉末或条片),避潮保存,以免积聚易燃易炸氢气。吸潮物、易水解物,贮於干燥处,封口应严密。易氧化易分解物,存於阴凉暗处,用棕色瓶或瓶外包黑纸盛装。但双氧水不要用棕色瓶(有铁质促使分解)装,最好用塑胶瓶装外包黑纸。 ⑧放射性物品未经幅射物质管理部门批准,不得存放使用! 见表3-1 危险药品贮存要求一览表 (3) 不能混放的药品 凡能互相起化学作用的药品都要隔离,对那些互相反应产生危险物、有害气体、火焰或爆炸等危险的药品,尤其要特别注意。 下述几类是必须隔离的药品: ①氧化剂与还原剂及有机物等不能混放。 ②强酸尤其是硫酸忌与强氧化剂的盐类(如高猛酸钾、氯酸钾……等)混放;与酸类反应发生有害气体的盐类(如氰化钾、硫化钠、亚硝酸钠、氯化钠、亚硫酸钠等等),不能与酸混放。 ③易水解的药品(如醋酸酐、乙酰氯、二氯亚砜等等)忌水、酸及碱。 引发剂忌单体混放。潮湿保存。 ④卤素(氟、氯、溴、碘)忌氨、酸及有机物。 ⑤氨忌与卤素、汞,次氯酸、酸类及汞等接触。 ⑥许多有机物忌氧化剂、硫酸、硝酸及卤素。 ⑦两种药品互相反应,放出有害或剧毒气体。 见表3-2 不能混合的常用药品一览表 (4) 贮存药品辅助材料 下面介绍一些材料,有助於保护和隔离各类药品。 ①聚乙烯塑胶袋:封住瓶口,或装着整个药品,可以隔绝潮气,防止液体挥发,防溅出药品。例如在五氯化磷、三氯化铅,低温溶剂瓶的瓶口加聚乙烯袋封口。 ②蜡封:防潮、防氧化。例如用於金属氢化物瓶口加封。 ③塑胶盘:将药品放在塑胶盘上,即使瓶子漏了,也便於和其他药物隔离,亦便於清理。因此盛放强氧化剂及其他剧毒品比较好。例如水银,一旦瓶子破了,水银只溅於盘上,能立即处理。 ④有沙子的塑料盘:上放金属钾、钠等危险药物,强氧化剂、强腐蚀性液体和封管药品。 ⑤综色瓶盛放光敏性药品,或曝光下产生危险反应之药物。亦可用黑漆或黑纸封住。 ⑥聚乙烯塑胶瓶盛氢氧化钠溶液、强酸、双氧水等。 ⑦一些特别危险的药品,如雷酸等,按原包装保存。 2.2 化学危险品废物的处理 凡是具有毒性、腐蚀性、强氧化性、强还原性、自燃性、恶臭的物质及其溶液,以及易爆、易燃物质均为化学危险品。如在实验中经常接触和使用的碱金属、金属氢化物、有机金属化合物、毒性气体、氰化物、酰卤、重氮化合物、硝基化合物、N-亚硝胺、过氧化物、毒性有机膦化物、氯磺酸、发烟硫酸、汞、重金属盐皆属危险品之列。这些危险品一旦成为实验后的废物,必须及时妥善处理或销毁,以免造成意外事故。 实验室中常见危险品废物的销毁方法列于表3-3中。 2.3 实验废弃物的处理 废气处理 实验中经常会产生某些有毒的气体、液体和固体,需要及时排弃。如不经处理直接排出可能污染周围空气和水源,使环境污染,损害人体健康。因此对废液、废气和废渣要经过一定的处理后,才能排弃。 对产生少量有毒气体的实验应在通风橱内进行。通过排风设备将少量毒气排到室外(使排出气在外面大量空气中稀释),以免污染室内空气。产生毒气量大的实验必须备有吸收或处理装置。如NO2,SO2,Cl2,H2S,HF等可用导管通入碱液中使其大部分吸收后排出,CO可点燃转成CO2。 在反应、加热、蒸馏中,不能冷凝的气体,排入通风橱之前,要进行吸收或其他处理,以免污染空气。常用的吸收剂及处理方法如下: ①氢氧化钠稀溶液:处理卤素、酸气(如HCl,SO2,H2S,HCN等等)、甲醛、酰氯等等。 ②稀酸(H2SO4或HCl):处理氨气、胺类……等等。 ③浓硫酸:吸收有机物。 ④活性碳、分子筛等吸附剂:吸收气体、有机物气体。 ⑤水:吸收水溶性气体,如氯化氢、氨气等。为避免回吸,处理时用防止回吸的仪器。 ⑥氢气、一氧化碳、甲烷气:如果排出量大,应装上单向阀门,点火燃烧。但要注意,反应体系空气排净以后,再点火。最好,事先用氮气将空气赶走再反应。 ⑦较重的不溶於水挥发物:导入水底,使下沉。吸收瓶吸入后再处理。 ⑧汞蒸气及其它废气 长期吸入汞蒸气会造成慢性中毒,为了减少汞液面的蒸发,可在汞液面上覆盖化学液体;甘油效果最好,5%Na2S.9H2O溶液次之,水效果最差。 对于溅落的汞,应尽量拣拾起来,颗粒直径大于的汞可以用吸气球或真空泵抽吸的拣汞器拣起来。拣过汞的地点可以洒上多硫化钙、硫黄或漂白粉,或喷洒药品使汞生成不挥发的难溶盐,干后扫除。药品为: (a)20%三氯化铁溶液;(b)1%碘-1.5%碘化钾溶液,每平方米使用300-500ml。 对吸附在墙壁、地板及设备表面上的汞可以用加热薰碘法除去,按每平方米0.5g碘,加热薰蒸,或按每10m2,用0.02m2蒸发面积的碘片,下班前关闭门窗,任其自然升华,次日移去。 以上除汞方法中,三氯化铁及碘蒸气对金属有腐蚀作用,采用这两种方法时要注意对室内精密仪器的保护。 另外,也可用紫外灯除汞,紫外辐射激发产生的臭氧可使分散在物体表面和缝隙中的汞氧化为不溶性的氧化汞。紫外灯(市售品常为30W,220V的安装方法与一般荧光灯相同。高度2.5-3.0m每1m30.5-0.8W。可以利用无人的非工作时间辐照。 化验室的少量废气一般可由通风装置直接排至室外,排气管必须高于附近屋顶3m,毒性大的气体可参考工业废气处理办法用吸附、吸收、氧化、分解等方法处理后排放。