最近要做血液样品了,以前从未做过。听说血液样品比较简单,可以加点什么试剂然后直接上机测定,该如何做呢? 如果必须要消解,那么取1ml样品加7ml硝酸1ml双氧水上微波消解就可以了吧?或者有更好的方法?
[color=#444444]用高效液相色谱检测血液样品中的一些物质,看到文献中有很多前处理的方法,请问血液的前处理有什么依据和需要注意的方面?还有,看到文献上都有加入一些内标物,请问内标物是否一定要加?谢谢[/color]
求助,请问血液样品消解,用微波消解好,还是电热板消解好呢?两者有哪些区别呢?多谢
小弟想向各位打下请教,国内做血液处理时,都是使用SPE座预处理做,还是可以实现血样再现预处理分析?
使用葡萄糖氧化酶GOD来探索酶传感器实现方法的研究做的是最多的了。大家有没有进一步做血液或血清样品中葡萄糖浓度的检测?有几个问题请教。如下:1. 样品前处理一般如何操作?2. 具体采取哪种电化学方法更为合适?循环伏安法,时间-电流法,计时电流法?还是其它?不同的方法获得的传感器参数(检测极限,线性范围,灵敏度等)不一样,操作起来的方便程度也不一样。3. 如何让修饰的电极真正成为传感器,即具有可知的且较稳定性能指标的检测装置?有哪些方面需要考虑?欢迎讨论。
谁能告诉我血液样品(抗凝全血)做微量元素(如铜、锌、钙、镁、铁)的样品处理方法和方式?有几种处理方法吗?
请教各位兄弟采取的血液如何处理,才可以破坏里面的大分子物质。
利用ICP-MS测定血液中的铅含量,ICP-MS现在是出了点问题,工程师在修呢,估计要两天以后才能用。但是血液样品已经前处理好了,已经经过了赶酸操作,要怎么保存,才能不让最后的检测结果受影响啊?
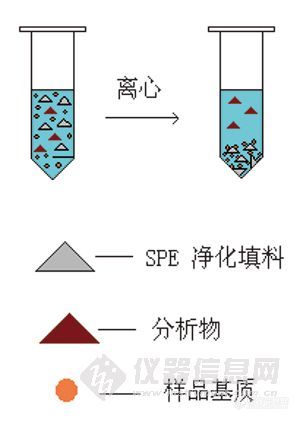
【百家争鸣第六期】您如何去除血液样品中脂肪和蛋白? 相信不少版友从事过血液中化学物的检测工作,和其他样品分析一样,即使有高灵敏度的液质、气质,但样品前处理仍然是不可缺少的,以此得到富集、降低基质效应。 那么,除了脂肪和蛋白,血浆/血清中有哪些物质需要被去除掉?相信不少版友会被这样的问题所困扰。您是采用的哪些方法去处血液样品中的这些杂质的?欢迎版友们分享。http://ng1.17img.cn/bbsfiles/images/2011/11/201111032211_328402_1644952_3.jpg链接:【百家争鸣第一期】样品分析中如何做标准曲线?http://bbs.instrument.com.cn/shtml/20110416/3253183/【百家争鸣第二期】基质效应可以忽略吗?http://bbs.instrument.com.cn/shtml/20110426/3272262/【百家争鸣第三期】如何进行样品分析中的质量控制?http://bbs.instrument.com.cn/shtml/20110511/3300126/【百家争鸣第四期】内标法是万能的吗?http://bbs.instrument.com.cn/shtml/20110602/3344063/【百家争鸣第五期】如何计算检出限?http://bbs.instrument.com.cn/shtml/20110623/3378013/【百家争鸣第七期】如何合理使用质谱定性http://bbs.instrument.com.cn/shtml/20120401/3957279/
血液样品预处理的标准操作 一、目的规范高效液相色谱分析中血液样品预处理的操作。二、职责1. 实验室分析测试人员对本规程的实施负责。2. 对于每一项具体的研究课题,具体的操作步骤应由实验室负责人负责制定,并由实验室分析测试人员严格实施。3. 实验室负责人负责对本规程的修订。三、血液样品预处理的标准操作1. 实验仪器与设备的准备1.1 试管 一般采用有盖子和刻度的尖底试管,要求密封性好,编号清楚准确,并摆放整齐。1.2 EP管 一般采用的规格有1ml、1.5ml、2 ml。要求密封性好,编号清楚准确,并摆放整齐。1.3 [url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液器[/color][/url][/color][/url] 要求定量准确,重复性好。1.4 其它 涡流混合器、离心机、真空泵、烧杯、量筒、记号笔、试管架、标签纸等。 2. 样品的均匀化 2.1 将装有血浆(血清)样品的EP管放置在冰箱冷藏室内,缓慢解冻为血浆(血清)溶液。2.2 然后取出放置至室温,置涡流混合器上混匀或往复振摇亦可到达均匀的目的。3. 液-液提取 3.1 提取溶剂的准备 3.1.1 常用的溶剂有氯仿,二氯甲烷,乙酸乙酯,乙醚等。3.1.2 提取溶剂可以是一种也可以是几种溶剂的混合溶液,目的是调整提取溶液的剂性,既保证待测样品被充分萃取进入提取溶剂,同时又有很好的选择性。3.2 根据待测样品的需要用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液器[/color][/url][/color][/url]定量吸取血浆(血清)至试管中,盖好试管塞。3.3 必要时调整血浆(血清)溶液的pH值,根据待测样品的性质加入酸、碱或缓冲溶液。3.4 用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液器[/color][/url][/color][/url]定量吸取提取溶液至装有血浆(血清)的试管中,盖好试管塞。3.5 溶液的混匀 3.5.1涡流混匀 将试管置于涡流混合器上进行旋涡,并保证样品溶液旋涡充分混匀,旋涡时间一般为2-3分钟。3.5.2 摇床混匀 将试管置于摇床上往复振摇,振摇时间一般为5-10分钟。3.6 样品的离心 将试管置于离心机中,分离过程中一般采用3000-4000r/min。离心之前注意要平衡,加速时应注意缓慢逐步加速,以防加速过快试管炸裂,离心时间一般为15-20分钟。3.7 离心分离后试管中样品分为上下两层,用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液器[/color][/url][/color][/url]吸取上层有机相,转移至另一试管中。3.8 溶剂的挥发 经过以上处理后得到的样品溶液,如果待测物的浓度在定量限以上,而且溶剂对HPLC系统没有干扰,就可以直接进样分析。但是在很多情况下需要除去溶剂,即浓缩甚至干燥样品。除溶剂时最重要的是不丢失或破坏待分析物质,同时还要考虑安全性和经济等。3.8.1 自然挥发 将样品溶液放置在室温下挥发,有时还可适当加热,加速溶液挥发。3.8.2 氮气吹干 氮气流能防止发生氧化,为了加快挥散速度,将样品溶液置于氮气流下吹干。3.8.3 减压蒸发 在密闭容器内,通过抽真空以降低液体表面的压力,使其沸点降低,样品溶液很快挥发,减少了蒸发过程中样品与空气的接触,避免由此引起的分解等副反应,适于热不稳定的样品。3.9 样品的复溶 用于样品溶液残渣复溶的溶液通常采用流动相或其它有机溶剂。用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液器[/color][/url][/color][/url]准确定量吸取,并且复溶样品应充分混合均匀。3.10 预处理样品的储存 预处理后的样品应保存在冰箱冷藏室,样品应竖直放置、排列整齐、编号准确清楚。待样品进样分析以前取出,以保证样品的稳定。3.11 乳化现象3.11.1防止乳化 可增加有机溶剂的体积,避免猛烈振摇或加入适当的试剂改变其表面张力等方法防止乳化。3.11.2 破乳 若已发生严重的乳化现象,应采取适当的方法消除乳化。3.11.2.1 离心 可将试管置于离心机中离心消除乳化。3.11.2.2 冷冻 可将试管置于冰箱中冷冻消除乳化。3.11.2.3 加入电解质。3.11.2.4 加入适当的稀释液稀释。4. 去蛋白处理 4.1 有机溶剂的准备 甲醇与乙腈是反相液相色谱法中常用的蛋白沉淀剂,因为它们与流动相的组成相同。甲醇沉淀蛋白的优点是上清液清澈,沉淀为絮状易于分离;乙腈与之相反,产生细的蛋白沉淀,但沉淀效率较甲醇高。4.2 根据待测样品的需要用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液器[/color][/url][/color][/url]定量吸取血浆(血清)至试管中,盖好试管塞。4.3 必要时调整血浆(血清)溶液的pH值,根据待测样品的性质加入酸、碱或缓冲溶液。4.4 用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液器[/color][/url][/color][/url]定量吸取有机溶液至装有血浆(血清)的试管中,盖好试管塞。4.5 溶液的混匀 有机溶剂使蛋白质变性而析出沉淀,从而把与蛋白质结合的药物解离出来。与此同时待测样品大部分被萃取进入有机溶剂。4.5.1涡流混匀 将试管置于涡流混合器上进行旋涡,并保证样品溶液旋涡充分混匀,旋涡时间一般为2-3分钟。4.5.2 摇床混匀 将试管置于摇床上往复振摇,振摇时间一般为5-10分钟。4.6 离心去除蛋白 将试管置于离心机中,分离过程中一般采用3000-4000r/min。离心之前注意要平衡,加速时应注意缓慢逐步加速,以防加速过快试管炸裂,离心时间一般为15-20分钟。4.7 离心分离后变性蛋白质沉淀于试管底部,用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液器[/color][/url][/color][/url]吸取上层有机溶液,转移至另一试管中。4.8 过滤 经过去蛋白处理后的样品溶液用0.45μm的滤膜过滤。4.9 高速离心 将过滤后的样品溶液转移至EP管中,采用25000-30000 r/min。离心之前注意要平衡,加速时应注意缓慢逐步加速,以防加速过快试管炸裂,离心时间一般为5-10分钟。4.10经过以上处理后得到的样品溶液,如果待测物的浓度在定量限以上,而且溶剂对HPLC系统没有干扰,就可以直接进样分析。如果需要除去溶剂,即浓缩甚至干燥样品,方法同3.8-3.9。4.11 预处理样品的储存 预处理后的样品应保存在冰箱冷藏室,样品应竖直放置、排列整齐、编号准确清楚。待样品进样分析以前取出,以保证样品的稳定。5. 固相萃取5.1 固相萃取柱的准备5.1.1 柱管 由血清级的聚丙烯制成(也有由玻璃制成的),一般为注射器性状。柱管下断有一突出的头,尺寸已标准化。5.1.2 烧结垫 聚乙烯是常见的烧结垫材料,对于特殊要求也可采用特氟隆或不锈钢片。5.1.3 SPE固定相 根据样品溶液的性质和组成选择不同类型和重量的固定相。SPE固定相最常见的是键合的硅胶材料,一般采用孔径60A不规则形状的40μ硅胶微粒作为原材料,然后将各种官能团键合上去。5.1.3.1 正相 CN、DIOL、Si、NH2等可作为正相固定相,用来保留极性物质。5.1.3.2 反相 C18、C8、C2、CH、PH等可作为反相固定相,用来保留非极性物质。5.1.3.3 离子交换 5.2 固定相活化 5.2.1 净化固定相 将第一溶液加入到固定相,真空抽滤,倒掉洗脱液。用量约为1-2ml/100mg固定相。5.2.2 将终溶剂加入固定相,真空抽滤,倒掉洗脱液。用量约为1-2ml/100mg固定相,终溶剂应该与样品溶剂性质相似。5.2.3 在活化的过程中和结束时,固定相都不能抽干,因为这将导致填料床出现干裂,如果在活化步骤中出现干裂,所有活化步骤都要重做。5.3 根据待测样品的性质将酸、碱或缓冲溶液加入到血浆(血清)溶液中,溶解稀释血浆(血清)溶液并且调整pH值。5.4 上样 将样品溶液加入到固相萃取柱,然后真空抽滤,使样品进入固定相,倒掉洗脱液。5.5 淋洗 样品中分析物得到保留后,将淋洗液加入到固相萃取柱进行淋洗,真空抽滤,倒掉淋洗液,以洗掉干扰组分。溶液体积可为0.5-0.8ml/100mg固定相。5.6 洗脱 将洗脱液加入到固相萃取柱进行洗脱,真空抽滤,并收集洗脱液。洗脱液一般为0.5-0.8ml/100mg固定相。5.7 经过以上处理后得到的洗脱液可以直接进样分析。如果需要除去溶剂,即浓缩甚至干燥样品,方法同3.8-3.9。5.8 预处理样品的储存 预处理后的样品应保存在冰箱冷藏室,样品应竖直放置、排列整齐、编号准确清楚。待样品进样分析以前取出,以保证样品的稳定。5.9 注意事项 5.9.1 在上样、淋洗、洗脱时注意溶剂极性的选择。可以是一种也可以是几种溶剂的混合溶液。5.9.2 溶剂的互溶性 后一种流过柱床的溶剂必须与前一溶剂互溶。如果使用互溶的溶剂有困难,就必须干燥柱床。干燥的方法是让氮气或空气通过柱床10-15min;或把SPE在1000-1500r/min离心5min。
我的朋友用BUCK的210做儿童血液的金属含量测定。测量的元素有钙、铁、锌、铅。其中钙、铁、锌采用火焰法,铅采用石墨炉法。钙的样品浓度为3ppm左右,但是测量的结果均偏低;铁和锌样品含量为100ppb左右,误差非常大,而且标准曲线也不好做;铅样品浓度为100ppb左右,误差更大,而且背景吸收很高。 我建议她提高样品的浓度,但是他告诉我,因为是儿童的血液,样品量不可能很多,现在的样品量,病人就有意见了。 不知道同行中有没有进行儿童血液分析的,请问是怎么处理的?
上次问如何从生物样品(尿液、血液)分离有机汞、无机汞、有机铅、无机铅;用什么柱子、具体方法。专家建议如下:1用固相萃取前处理方法只能分析生物样品中的有机化合物。生物样品中的无机成分前处理方法多用高温炉灰化、微波消解等方法。但请问,,分离有机汞、有机砷是否可以用固相萃取的方法进行分离?如果可以,具体用什么柱子、具体方法?
[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]测血液、粪便等铁含量,血铁含量可以用全血吗?应该用什么样品处理方法
摘要传统ICP-OES仪器的气动雾化器相对效率差,雾化室体积大。也就是说该技术一般需要3-5ml的最小进样量,从而限制在某些方面的应用如临床或法医检定。本文探讨了仅使用1.5ml的进样量,对主量和微量元素进行准确测定所需的仪器条件和分析方法。虽然原实验是用血液进行的临床分析,但该方法同样适合于任何小体积样品的分析应用。仪器条件分析使用美国热电公司的IRIS Intrepid II垂直炬ICP-OES。Intrepid II是IRIS家族第四代使用电荷注入式(CID)检测器的高分辨率中阶梯光谱仪。CID技术的发展使该检测器较以前版本具有更高的灵敏度和更低的噪音,改进了仪器的检出极限。选择垂直观测等离子体减少基体干扰。由于IRIS垂直设计中有一个后反射镜光路系统以改进灵敏度接近于水平炬设计,同时没有基体干扰效应。使用改进的进样系统处理小样品量,包括高盐微量雾化器、20ml玻璃Cinnabar旋流雾化室和小孔管。
初次接触肉制品和血液制品的检测,都是食品的。这个样品的前处理应该怎么做?都会用到什么设备?还请不吝赐教!
目前[font=宋体]GA/T 842-2019《血液酒精含量的检验方法》和[font=宋体]GA/T 1073—2013《生物样品血液、尿液中乙醇、甲醛、正丙醇、乙醛、丙酮、异丙醇和正丁醇的顶空-[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]检验方法》都是可以使用的,那么在公检法单位委托相关鉴定机构对血样进行乙醇定性定量鉴定的情况,是否有标准或条款规定要求优先使用19年最新的标准?[/font][/font][font=Times New Roman][color=#000000][/color][/font]
血液中的还原性物质有哪些 他们在血液中的含量范围大致是什么 血液中水杨酸和氨基乙酸的含量是什么范围 谢谢、、、
血液中乙醇分析检验记录表案件名称及编号: XXX案[font=times new roman] [/font][font=times new roman][color=fuchsia]XXX[/color][/font]检材接收时间:[color=fuchsia]2022.9.8[/color] 检材开始时间:[color=fuchsia]2022.9.13[/color]提取净化操作过程一、试剂1.1乙醇对照品标准溶液:分别精密称取对照品乙醇适量, 用水配成10.0mg/mL乙醇对照品标准储备溶液, 置冰箱中冷藏保存, 保存时间为6个月。(试验中所用其他浓度的对照品标准溶液均从上述储备液用水稀释而得)。1.2内标物叔丁醇对照品标准溶液:精密称取叔丁醇适量, 用水配制成5.0mg/mL叔丁醇对照品标准储备溶液, 置冰箱中冷藏保存, 保存时间为6个月。将储备液用水稀释得40ug/mL叔丁醇内标工作液, 置冰箱中冷藏保存, 保存时间为3个月。1.3[font=宋体]乙醇标准溶液配制:[/font]精密仪器取适量乙醇分别配制系列浓度0.1[font=times new roman]mg/mL[/font]、0.2[font=times new roman]mg/mL[/font]、0.5[font=times new roman]mg/mL[/font]、0.8[font=times new roman]mg/mL[/font]、1.0[font=times new roman]mg/mL[/font]、2.0[font=times new roman]mg/mL[/font]乙醇溶液。1.4标准曲线制作:分别取[font=宋体]0.1[/font]mg/mL[font=宋体]、0.2[/font]mg/mL[font=宋体]、0.5[/font]mg/mL[font=宋体]、0.8[/font]mg/mL[font=宋体]、1.0[/font]mg/mL[font=宋体]、2.0[/font]mg/mL乙醇标准溶液各0.1mL,分别加入0.5mL叔丁醇内标液。按照顶空[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法标准条件分别测定。二、仪器及器材2.1[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]: Agilent 8890 (G3540A)2.2顶空自动进样器2.3 10ul微量注射器2.4 1/10000电子天平2.5 100~1000uL、10~500uL、10~50uL[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url]各一支2.6 实验室常用器材三、检验方法及仪器参考条件说明3.1[font=times new roman]参照SF/Z JD0107001-2016血液中乙醇的测定-顶空[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法[/font]。将检材及叔丁醇内标工作液置于顶空小瓶内, 盖上硅橡胶垫。用密封钳加封锅帽, 混匀, 待测。3.2[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]参考条件Agilent 8890 (G3540A)色谱柱(1): DB - ALC1(30m×0.32mm×1.8μm) 柱;色谱柱(2): DB - ALC2(30m×0.32mm×1.2μm) 柱;色谱柱温程: 恒温40℃;色谱柱: 初始温度70℃, 以50℃/m n程序升温至170℃, 保持5min;进样口温度: 150℃;检测器温度: 300℃;载气: 高纯氮气, 纯度大于等于99.999%;柱流量: 4mL/min-8mL/min。3.3顶空自动进样器进样将样品置于顶空自动进样器样品架上, 顶空自动进样器自动加热、进样。顶空自动进样器参考条件:加热箱温度: 60℃;定量环温度: 100℃;传输线温度: 110℃;[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相[/color][/url]循环时间: 5.5min( 色谱柱1、 色谱柱2);样品瓶加热平衡时间: 10.0min;样品瓶加压时间: 0.10min;定量环充满时间: 0.10min;定量环平衡时间: 0.05min;进样时间: 1.00min。四、检材及质控样品制备血液约10mL(分装在2管中),具塞塑料管包装,检材编号为[color=fuchsia]XXX[/color]。4.1案件样品制备取待测血液100μL及叔丁醇内标工作液500μL置于顶空小瓶内, 盖上硅橡胶垫。用密封钳加封锅帽, 混匀, 待测。4.2添加样品及空白样品取0.01[font=times new roman] [/font]mg/mL乙醇标准溶液100μL及叔丁醇内标工作液500μL作为检测限添加样品, 另取空白血液100μL及叔丁醇内标工作液500μL作为空白样品。按上述操作与案件样品平行提取和分析。4.3内标-标准曲线配制系列浓度0.1mg/mL、0.2mg/mL、0.5mg/mL、0.8mg/mL、1.0mg/mL、2.0mg/mL的乙醇的对照品标准溶液, 取以上标准溶液100μL各两份,样品制备同4.1。案件样品中乙醇的浓度应在校准曲线的线性范围内。4.4定性检出限取0.01mg/mL、0.03mg/mL、0.05mg/mL、0.08mg/mL的乙醇的对照品标准溶液, 取以上标准溶液100μL,样品制备同4.1测定定性检出限。4.4定量检出限将一定量乙醇加入空白血中配制系列0.01mg/mL、0.03mg/mL、0.05mg/mL、0.08mg/mL的溶液, 取以上溶液100μL,样品制备同4.1测定定量检出限。4.4质量控制将0.198(±0.129)mg/mL浓度的乙醇质控样品进样后,经4.3标准曲线测定后其乙醇浓度为0.202mg/mL,在质控范围内。4.5进样将样品置于顶空自动进样器样品架上,顶空自动进样器自动加热、进样。五.结果评价分别取空白溶剂、空白对照、案件样品、系列浓度的标准溶液样品、定性检出限样品、定量检出限样品、质量控制样品依次进样分析。(每次进样前均进空白溶剂呈阴性)(附:检测原始谱图)附图谱目录:表一:血液中乙醇含量检测原始记录(样品1)表二:血液中乙醇含量检测原始记录(样品2)图1:空白对照图2-13:0.1mg/mL、0.2mg/mL、0.5mg/mL、0.8mg/mL、1.0mg/mL、2.0mg/mL的乙醇的对照品标准溶液两次进样色谱图图14-16:标准曲线图图17:0.198(±0.129)mg/mL乙醇质量控制图18:样品1平行1色谱图图19:样品1平行2色谱图图20:样品2平行1色谱图图21:样品2平行2色谱图图22:定性检出限图23:定量检出限5.1定性结果评价添加样品中出现乙醇的色谱峰(图2-13), 空白对照样品中未出现相应的色谱峰(图1), 而案件样品1、2中均出现相应的乙醇色谱峰(图18-21), 且保留时间为1.345min、1.346min(表一、二)与添加样品中乙醇的色谱峰保留时间比较, 相对误差在±2%内。 经选择不同的色谱条件,结果一致,可以认定案件样品中含有乙醇成分。经测定乙醇定性检出限为0.01mg/mL。阳性结果可靠。对照品和内标的保留时间参见[font=times new roman]表一、二[/font]。乙醇校准曲线参见[font=times new roman]图14-16[/font]。5.2定量结果评价样品1中[font=times new roman]乙醇[/font]含量为[font=times new roman]1.12mg/mL[/font],相对相差为[font=times new roman]0.98%[/font],小于5%,结果可靠。样品2中[font=times new roman]乙醇[/font]含量为[font=times new roman]0.68 mg/mL[/font],相对相差为[font=times new roman]0.59[/font]%,小于5%,结果可靠。经测定乙醇定量检出限为0.05mg/mL。图谱见18-23,详细数据见表一、二。[color=black]5.2质量控制[/color]5.2.1标准曲线:配制乙醇质量浓度为0.1mg/mL、0.2mg/mL、0.5mg/mL、0.8mg/mL、1.0mg/mL、2.0mg/mL的对照品标准溶液, 按4.1步骤进样分析, 以乙醇与内标叔丁醇的峰面积比(Y) 为纵坐标、乙醇浓度(X)为横坐标进行线性回归。得线性回归方程Y=0.0452X-0.01399 R=0.99987 R[sup]2[/sup]=0.999745.2.2检出限:经测定乙醇的定性检出限均为0.01mg/mL。(图22)经测定乙醇定量检出限为0.05mg/mL。(图23)5.2.3质控样品:将0.198(±0.129)mg/mL浓度的乙醇质控样品进样后,经4.3标准曲线测定后其乙醇浓度为0.202mg/mL,在质控浓度范围内,实验结果可靠。六.检材使用记录检材保存: [color=fuchsia]2022年9月13日[/color],取所送检材4mL用于检验。剩余检材置于-4℃冰箱中保存两个月备查。检材保存负责人:操作者:检验完成时间:[align=center]表一:血液中乙醇含量检测原始记录[/align][table][tr][td][align=center]检案号[/align][/td][td][align=center][color=fuchsia]XXX[/color][/align][/td][td][align=center]样品名称[/align][/td][td][align=center]血液[/align][/td][/tr][tr][td][align=center]样品编号[/align][/td][td][align=center]样品1[/align][/td][td][align=center]检测项目[/align][/td][td][align=center]血液中乙醇的定性定量检测[/align][/td][/tr][tr][td][align=center]检测方法[/align][/td][td][align=center]SF/Z JD0107001-2016[/align][/td][td][align=center]对照物[/align][/td][td][align=center]40ug/mL叔丁醇[/align][/td][/tr][tr][td][align=center]环境温度[/align][/td][td][align=center]22℃[/align][/td][td][align=center]环境湿度[/align][/td][td][align=center]40%[/align][/td][/tr][tr][td=4,1]样品处理:[size=13px]1.外观(1)凝血 有( )无(√); (2)密封 无渗漏(√)有渗漏( )无密封( )[/size]2.取0.1ml待测血液2份,置于两个样品瓶内,分别加0.5ml内标液,橡胶垫、铝盖密封,进样分析。[/td][/tr][tr][td=4,1]仪器操作条件:[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]型号:[font=times new roman]Agilent 8890 (G3540A)[/font]色谱柱(1): DB - ALC1(30m×0.32mm×1.8μm) 柱;色谱柱(2): DB - ALC2(30m×0.32mm×1.2μm) 柱;柱温:恒温40℃ 载气:高纯度氮气 进样口温度:150℃ 检测器温度:300℃传输线温度:110℃ 加热箱温度:60℃ 样品瓶加热平衡时间:10.0min 进样时间:1.0min[/td][/tr][tr][td=4,1]测定结果: [table][tr][td][align=center]待测样品1[/align][/td][td][align=center]乙醇峰面积[/align][/td][td][align=center]叔丁醇峰面积[/align][/td][td][align=center]乙醇保留时间[/align][/td][td][align=center]叔丁醇保留时间[/align][/td][td][align=center]结果[font=times new roman]mg/100mL[/font][/align][/td][td][align=center]结果mg/mL[/align][/td][/tr][tr][td][align=center]平行1[/align][/td][td][align=center]84.564[/align][/td][td][align=center]67.833[/align][/td][td][align=center]1.345min[/align][/td][td][align=center]1.994min[/align][/td][td][align=center]111.80[/align][/td][td][align=center]1.118[/align][/td][/tr][tr][td][align=center]平行2[/align][/td][td][align=center]79.998[/align][/td][td][align=center]64.817[/align][/td][td][align=center]1.345min[/align][/td][td][align=center]1.994min[/align][/td][td][align=center]110.70[/align][/td][td][align=center]1.107[/align][/td][/tr][tr][td][/td][td][/td][td][/td][td][/td][td][align=center]结果平均值:[/align][/td][td][align=center]111.25[/align][/td][td][align=center]1.12[/align][/td][/tr][tr][td][/td][td][/td][td][/td][td][/td][td][align=center]相对偏差:[/align][/td][td][align=center]0.98%[/align][/td][td][/td][/tr][/table]备注:测试人:XX 日期:2022.9.16复核人:XX 日期:2022.9.16[/td][/tr][/table][align=center]表二:血液中乙醇含量检测原始记录[/align][table][tr][td]检案号[/td][td][align=center][color=fuchsia]XXX[/color][/align][/td][td][align=center]样品名称[/align][/td][td][align=center]血液[/align][/td][/tr][tr][td]样品编号[/td][td][align=center]样品2[/align][/td][td][align=center]检测项目[/align][/td][td][align=center]血液中乙醇的定性定量检测[/align][/td][/tr][tr][td]检测方法[/td][td][align=center]SF/Z JD0107001-2016[/align][/td][td][align=center]对照物[/align][/td][td][align=center]40ug/mL叔丁醇[/align][/td][/tr][tr][td]环境温度[/td][td][align=center]22℃[/align][/td][td][align=center]环境湿度[/align][/td][td][align=center]40%[/align][/td][/tr][tr][td=4,1]样品处理:[size=13px]1.外观(1)凝血 有( )无(√); (2)密封 无渗漏(√)有渗漏( )无密封( )[/size]2.取0.1ml待测血液2份,置于两个样品瓶内,分别加0.5ml内标液,橡胶垫、铝盖密封,进样分析。[/td][/tr][tr][td=4,1]仪器操作条件:[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]型号:[font=times new roman]Agilent 8890 (G3540A)[/font]色谱柱(1): DB - ALC1(30m×0.32mm×1.8μm) 柱;色谱柱(2): DB - ALC2(30m×0.32mm×1.2μm) 柱;柱温:恒温40℃ 载气:高纯度氮气 进样口温度:150℃ 检测器温度:300℃传输线温度:110℃ 加热箱温度:60℃ 样品瓶加热平衡时间:10.0min 进样时间:1.0min[/td][/tr][tr][td=4,1]测定结果: [table][tr][td][align=center]待测样品2[/align][/td][td][align=center]乙醇峰面积[/align][/td][td][align=center]叔丁醇峰面积[/align][/td][td][align=center]乙醇保留时间[/align][/td][td][align=center]叔丁醇保留时间[/align][/td][td][align=center]结果[font=times new roman]mg/100mL[/font][/align][/td][td][align=center]结果mg/mL[/align][/td][/tr][tr][td][align=center]平行1[/align][/td][td][align=center]47.634[/align][/td][td][align=center]63.844[/align][/td][td][align=center]1.346min[/align][/td][td][align=center]1.994min[/align][/td][td][align=center]67.60[/align][/td][td][align=center]0.676[/align][/td][/tr][tr][td][align=center]平行2[/align][/td][td][align=center]45.481[/align][/td][td][align=center]60.565[/align][/td][td][align=center]1.347min[/align][/td][td][align=center]1.995min[/align][/td][td][align=center]68.00[/align][/td][td][align=center]0.680[/align][/td][/tr][tr][td][/td][td][/td][td][/td][td][/td][td][align=center]结果平均值:[/align][/td][td][align=center]67.80[/align][/td][td][align=center]0.68[/align][/td][/tr][tr][td][/td][td][/td][td][/td][td][/td][td][align=center]相对偏差:[/align][/td][td][align=center]0.59%[/align][/td][td][/td][/tr][/table]备注:测试人:XX 日期:2022.9.16复核人:XX 日期:2022.9.16[/td][/tr][/table]
请问大家怎么用原子荧光光谱法测定鼠血液和尿液用的有机汞,无机汞及总汞含量,样品的前处理怎么处理?及测定步骤
请问大家怎么用原子荧光光谱法测定鼠血液和尿液用的有机汞,无机汞及总汞含量,样品的前处理怎么处理?及测定步骤
你们好,请教一下用液相色谱仪怎么来检测血液中氯霉素等抗生素的含量,包括样品的前处理过程!谢谢各位,拜托拉!
血液中常见毒物的定性定量分析能力验证计划[align=center]结果反馈表[/align]参加编号:样品收到日期: 2022.9.8 样品测定日期: 2022.9.12样品外观描述: 血液约10ml(分装在2管中),具塞塑料管包装,检材编号为2022采用的检测方法:[font=黑体] [/font] 1.参照《SF/Z JD0107014-2015 血液和尿液中108中毒(药)物的[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]-质谱检测方法》。2.参照《GA_T 1322-2016法庭科学血液中地西泮等十种苯骈二氮杂类药物[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]-质谱检验方法》。3.将检材分别在酸性、碱性条件下用氯仿:甲醇=3:2的混合萃取剂提取、离心后分离提取液,直接进样供8890-5977B GC/MS分析。最低检出限:[table][tr][td][align=center][color=black]样品[/color][/align][/td][td][align=center][color=black]保留时间[/color][/align][align=center][color=black](min)[/color][/align][/td][td][align=center][color=black]检出限[/color][/align][align=center][color=black]([/color][size=16px][color=black]u[/color][/size][color=black]g/m[/color][size=16px][color=black]L[/color][/size][color=black])[/color][/align][/td][td][align=center][color=black]样品[/color][/align][/td][td][align=center][color=black]保留时间[/color][/align][align=center][color=black](min)[/color][/align][/td][td][align=center][color=black]检出限[/color][/align][align=center][color=black](ug/m[/color][size=16px][color=black]L[/color][/size][color=black])[/color][/align][/td][/tr][tr][td][align=center][color=black]甲基苯丙胺[/color][/align][/td][td][align=center][color=black]3.841[/color][/align][/td][td][align=center][color=black]0.10[/color][/align][/td][td][align=center][color=black]氯胺酮[/color][/align][/td][td][align=center][color=black]7.715[/color][/align][/td][td][align=center][color=black]0.10[/color][/align][/td][/tr][tr][td][align=center][color=black]苯巴比妥[/color][/align][/td][td][align=center][color=black]8.343[/color][/align][/td][td][align=center][color=black]1.00[/color][/align][/td][td][align=center][color=black]美沙酮[/color][/align][/td][td][align=center][color=black]8.860[/color][/align][/td][td][align=center][color=black]0.10[/color][/align][/td][/tr][tr][td][align=center][color=black]卡马西平[/color][/align][/td][td][align=center][color=black]9.651[/color][/align][/td][td][align=center][color=black]0.20[/color][/align][/td][td][align=center][color=black]奥沙西泮[/color][/align][/td][td][align=center][color=black]9.730[/color][/align][/td][td][align=center][color=black]0.50[/color][/align][/td][/tr][tr][td][align=center][color=black]地西泮[/color][/align][/td][td][align=center][color=black]10.284[/color][/align][/td][td][align=center][color=black]0.05[/color][/align][/td][td][align=center][color=black]咪达唑仑[/color][/align][/td][td][align=center][color=black]11.225[/color][/align][/td][td][align=center][color=black]0.10[/color][/align][/td][/tr][tr][td][align=center][color=black]唑吡坦[/color][/align][/td][td][align=center][color=black]13.082[/color][/align][/td][td][align=center][color=black]0.10[/color][/align][/td][td][align=center][color=black]氯氮平[/color][/align][/td][td][align=center][color=black]13.836[/color][/align][/td][td][align=center][color=black]0.10[/color][/align][/td][/tr][tr][td][align=center][color=black]艾司唑仑[/color][/align][/td][td][align=center][color=black]14.423[/color][/align][/td][td][align=center][color=black]0.50[/color][/align][/td][td][align=center][color=black]阿普唑仑[/color][/align][/td][td][align=center][color=black]14.963[/color][/align][/td][td][align=center][color=black]0.50[/color][/align][/td][/tr][/table]定量方法采用: 内标法 √外标法[table][tr][td]样品测定结果:[/td][/tr][tr][td]定性定量结果:检出的成分请在相应方框内打钩“√”,并将定量结果填写在相应位置。(数值保留小数点后两位)□甲基苯丙胺 [size=13px]μg/mL(微克每毫升)[/size] [/td][/tr][tr][td] □ 氯 胺 酮 [size=13px]μg/mL(微克每毫升)[/size][/td][/tr][tr][td] 地 西 泮 [size=13px]μg/mL(微克每毫升)[/size][/td][/tr][tr][td] 艾司唑仑 [size=13px]μg/mL(微克每毫升)[/size][/td][/tr][tr][td]□ 咪达唑仑 [size=13px]μg/mL(微克每毫升)[/size][/td][/tr][tr][td]√ 阿普唑仑 0.89 [size=13px]μg/mL(微克每毫升)[/size][/td][/tr][tr][td]□ 奥沙西泮 [size=13px]μg/mL(微克每毫升)[/size][/td][/tr][tr][td]□ 卡马西平 [size=13px]μg/mL(微克每毫升)[/size][/td][/tr][tr][td]□ 苯巴比妥 [size=13px]μg/mL(微克每毫升)[/size][/td][/tr][tr][td]□ 氯 氮 平 [size=13px]μg/mL(微克每毫升)[/size][/td][/tr][tr][td]□ 唑 吡 坦 [size=13px]μg/mL(微克每毫升)[/size][/td][/tr][tr][td]□ 美 沙 酮 [size=13px]μg/mL(微克每毫升)[/size][/td][/tr][/table]对整个检测过程的描述: 1.样品测定方法:2022.09.08日收到血液约10ml(分装在2管中),具塞塑料管包装,检材编号为2022。[font=times new roman]2022.09.12日开始进行样品测定,[/font]参照《SF/Z JD0107014-2015 血液和尿液中108中毒(药)物的[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]-质谱检测方法》。参照《GA_T 1322-2016法庭科学血液中地西泮等十种苯骈二氮杂类药物[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]-质谱检验方法》。将检材分别在酸性、碱性条件下用氯仿:甲醇=3:2的混合萃取剂提取、离心后分离提取液,直接进样供8890-5977B GC/MS分析。 [font=宋体]2.进样分析:分别取空白溶剂、12种混合标准品、空白血液、空白对照(加标)、检材样品、系列浓度的混合标准溶液(检出限)、阿普唑仑系列浓度标准溶液、检材样品、质量控制样品依次进行分析。 [/font] [font=宋体]3.定性分析:通过GC/MS分析认为: [/font](1)检材血样中阿普唑仑色谱峰的GC平均保留时间15.02min;与混合标准溶液中的阿普唑仑平均保留时间一致。空白血液、空白对照(加标)对定性分析无干扰。(2)利用质谱库检索功能,在NIST库中对检材血液中总离子流图逐峰检索,确认检材血液中检出阿普唑仑,其质谱离子碎片特征和丰度与混合标准品中阿普唑仑的质谱离子碎片特征及丰度一致; 空白血样、空白对照(加标)对定性分析无干扰。(3)定性检验结果:空白对照、混合标准品对照检验、与标准品的保留时间各特征离子及其丰度对比,结果检出阿普唑仑。未检出甲基苯丙胺、氯胺酮、地西泮、咪达唑仑、阿普唑仑、苯巴比妥、氯氮平、奥沙西泮、唑吡坦、卡马西平、美沙酮成分 。 4.定量分析:配制阿普唑仑质量浓度为0.5ug/mL、1.0ug/mL、2.0ug/mL、4.0ug/mL、8.0ug/mL的对照品标准溶液,进样分析,以阿普唑仑的峰面积(Y)为纵坐标、阿普唑仑质量浓度(X)为横坐标进行线性回归。得线性回归方程: Y=376.119863*X-187.274050 R[sup]2[/sup]=0.99256704 血液中阿普唑仑含量为[font=宋体]0.89[/font]ug/mL,[font=宋体]相对相差为[/font]2.7%[font=宋体],小于5%,定量数据可靠。[/font] 5.质量控制 (1)检出限测定:20ng/mL、50ng/mL、100ng/mL、200ng/mL、500ng/mL、1ug/mL、2ug/mL的添加混合标准品依次进样后,得到含12种目标物的方法检出限,其中阿普唑仑的方法检出限为0.5ug/mL。 (2)质控样品测定:将4.5ug/mL质量浓度的阿普唑仑质控样品进样后,经4.2.2曲线测定后其阿普唑仑质量浓度为4.587ug/mL,与质控已知质量浓度一致,实验结果可靠。 6.综合上述分析:检材血液中检出阿普唑仑成分。阿普唑仑含量为0.89ug/mL,相对相差为[font=times new roman]2.7%[/font],小于5%,定量数据可靠。阿普唑仑方法检出限为0.5[font=times new roman]ug/mL,可以确认从检材血液中检出阿普唑仑,阳性结果可靠。 [/font] 7. 2022年9月12日,取所送血液检材约4mL用于检验,剩余检材放置于-4℃冰箱中保存2个月备查。 检验完成时间:2022年9月22号
各位版友,我现在有一个问题,如果采用双柱双FID来检测血液中酒精的含量,但样品就一个,是顶空的时候重复进样还是怎么弄?如果是重复进样的话,第二次进样是否就不准确了,只能辅助定性,而只能采用第一次进样来做定量分析。另外还有一种方式就是一个进样口采用三通分流道两根色谱柱上面,但准确性怎么样?谢谢!

刚上手,很多不明白[img=,690,327]https://ng1.17img.cn/bbsfiles/images/2021/08/202108201556550979_1806_5332243_3.png!w690x327.jpg[/img]1、因为血液的颜色是红色的,调节ph不怎么看得出,调节的不准确影响药物的提取吗?有没有什么好的对策2、关于检出限ug/ml的疑问。国标参考数据如巴比妥血液检出限5ug/ml,在做添加样品的时候是加入5ug/ml的浓度10ul;还是加入15ug/ml的浓度10ul,最后复溶至30ul使得其浓度变为5ug/ml?我觉得应该是后者吧。[img=,505,123]https://ng1.17img.cn/bbsfiles/images/2021/08/202108201604496697_4085_5332243_3.png!w505x123.jpg[/img]3、这个定性条件我的理解是否准确:首先看添加样品和待测样品的保留时间在2%内;再看添加样品的“实际%”与待测样品的“实际%”比较。比如说添加样品实际50%,待测样品40%,这样误差在20%,如果标准上最大误差15%就不可以定,标准最大误差25%就可以定。标准中的特征碎片离子是指目标离子和参考离子吗,有时候低浓度扫描发现没有个别参考离子,但是相似度检索还是出的来,在缺少个别参考离子的时候,能定性吗?[img=,395,77]https://ng1.17img.cn/bbsfiles/images/2021/08/202108201607143387_1807_5332243_3.png!w395x77.jpg[/img]4、scan、sim方法。两种方法都做了,待测样品来的时候一般是采取哪种方法?5、标准曲线。按照说明书做了三个点的标曲,后面QC/SN的时候,检出限按照浓度按照1和5ppm的数据做出来结果是不一样的,没搞明白这个检出限是啥[img=,690,203]https://ng1.17img.cn/bbsfiles/images/2021/08/202108201618423527_3202_5332243_3.png!w690x203.jpg[/img]
问问各位大神,有没有能在血液样品(血清,血浆)中做皮克级pg/mL蛋白的定量经验?特别想听的是利用AB的QTRAP4500(其他QQQ类也行)定量血浆低丰度蛋白的经验。我主要对低丰度的各种细胞因子和免疫因子感兴趣。各位推荐什么高丰度蛋白去除方法?试剂盒好还是柱子好?希望激起各位大神的围观和讨论。谢谢!http://simg.instrument.com.cn/bbs/images/brow/em01.gif
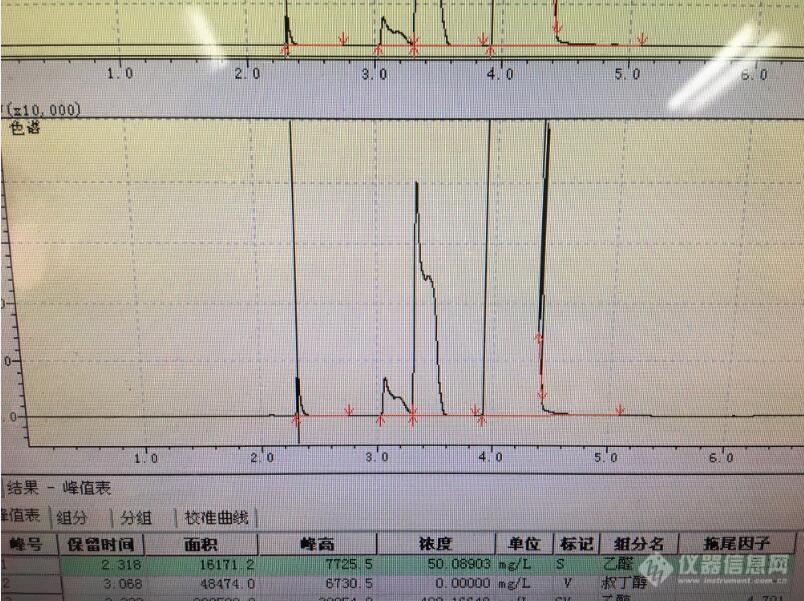
岛津[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url][url=https://insevent.instrument.com.cn/t/Mp]gc[/url] 2014C,色谱柱wondacap wax 30*0.25*0.25,进样口温度250℃,检测器温度250℃,程序升温:初始温度48℃,以30℃/min升温至55℃,再以30℃/min升温至200℃,保留2min。柱流量1.5mL/min,分流进样,分流比10,进样量1uL。用以上方法分析血液样品中乙醛和乙醇含量,叔丁醇作为内标,样品处理用乙腈沉淀蛋白,离心后过膜,自动进样器进样。最近分时时乙醛峰拖尾严重,拖尾因子达到2.0以上,叔丁醇和乙醇峰下降过程疑似出现分裂。但不加血样直接进样分析乙醛和乙醇溶液时,所有峰型只是拖尾,不出现峰分裂现象,当分析血液样品时,就会出现下面图中的异常峰型。希望得到您的指导,解决这个问题,谢谢![img=,690,515]https://ng1.17img.cn/bbsfiles/images/2019/07/201907101146426113_3121_1750127_3.jpg!w690x515.jpg[/img]
谁有用近红外检测血液的谱图呢?有文章更好。
血液透析水中的硫酸盐和氟化物一般是多少?
请问有人采用过非顶空进样的方式检测血液中的乙醛和乙醇吗?样品前处理是怎么操作的呢?
原子吸收测血液\尿液的国标是什么啊请问下大家原子吸收:测血液和尿液中的Pb As Hg的国标是那个啊?