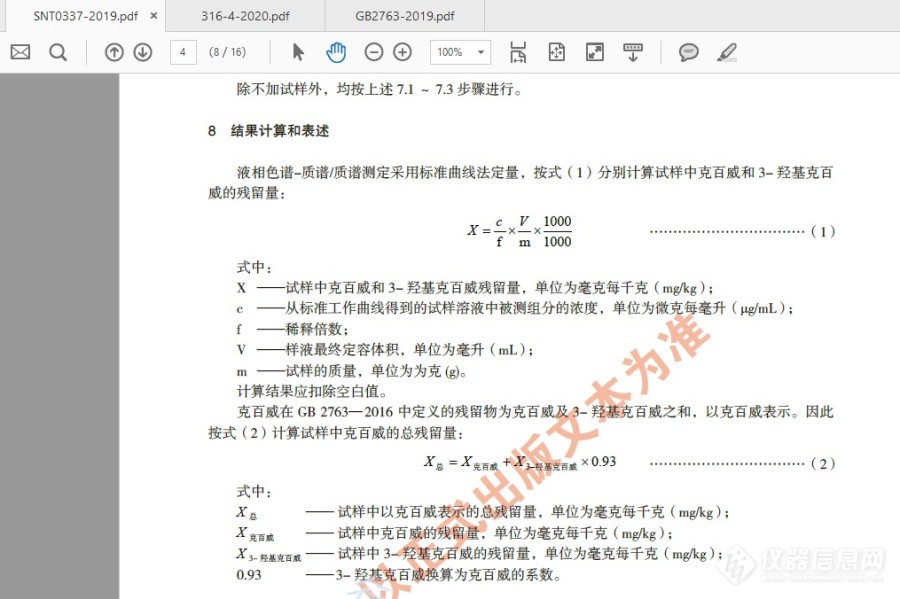
关于克百威(以克百威和3-羟基克百威之和计)结果计算问题的请教。想请教一下:当样品中克百威,3羟基克百威都有检出的情况下,按照GB 2763-2019的要求,克百威是“以克百威和3-羟基克百威之和计”,请问是直接将两者进行求和,还是进行换算后再求和。例如:某蔬菜样品中克百威检出值为 A mg/Kg,3-羟基克百威检出值为 B mg/Kg,现在要填报“克百威(以克百威和3-羟基克百威之和计)”的结果,应该怎样计算才正确。计算方式一:样品中 克百威(以克百威和3-羟基克百威之和计)含量=(A+B)mg/Kg,计算方式一:参照 SN/T 0337-2019标准中的计算方式,样品中 克百威(以克百威和3-羟基克百威之和计)含量=(A+B*0.93)mg/Kg。请各位老师指教。附:SN/T 0337-2019 部分截图:[img=,690,459]https://ng1.17img.cn/bbsfiles/images/2021/04/202104301427586649_3321_3463672_3.jpg!w690x459.jpg[/img][img=,690,459]https://ng1.17img.cn/bbsfiles/images/2021/04/202104301427586649_3321_3463672_3.jpg!w690x459.jpg[/img]
2763 中克百威和3羟基克百威都用克百威表示!这样还有必要在资质认定的时候把3羟基克百威当参数来认证吗?
各位老师,克百威(克百威和三羟基克百威)检出限怎么写,两者之和么么
今年我单位做丁硫克百威残留登记试验,不知道有没有试验单位有3-羟基克百威和3-乙基克百威,如能提供少许(几十毫克就行),真的不胜感激,联系人:万宇 0551-5854938 /0551-5851928 /13866151614
购买克百威的标液,除了买克百威,还要买三羟基克百威,那么丁硫克百威和他们之间的关系是什么呢?
用761方法液相柱后衍生法做涕灭为亚砜、涕灭威砜和三羟基克百威都没有出峰,不知道在前处理的过程中应该注意什么才能出峰?求高手赐教!我们要计量认证考核,急!
你们进液质的涕灭威亚砜,涕灭威砜3-羟基克百威标样从哪里买?什么规格型号,我们买的国标液是钠盐形式。好友回复:你到国家标准物质网查询, GSB和SB是农业部环境保护科研监测所制的,BW是国家计量院的,CDCT是德国Dr的,一般是固体的
克百威和丙硫克百威是同一种物质吗?有的资料上是测克百威的。而日本有限制的是丙硫克百威。
第一次做农残中丁硫克百威的检测。质谱优化的离子对的质量数跟标准上的一致,质谱段进丁硫克百威的标准品可以正常出峰。再用液相进样的时候丁硫克百威的两个离子对都不出峰,反而出的是克百威的离子对。我又用克百威单标、丁硫克百威单标和两者的混标进样,出的峰都是克百威。各位老师帮忙看一下是哪里除了问题?流动相: 乙腈 0.2%乙酸水 梯度洗脱 采集时间20min质谱是 AB 5500
对天敌和有益生物毒性较低,即克百威农药低毒化衍生物,属高效安全、使用方便的杀虫杀螨剂,是剧毒农药克百威较理想的替代品种之一。其杀伤力强,见效快,具有胃毒及触杀作用。特点是脂溶性、内吸性好、渗透力强、作用迅速、残留低、有较长的残效、使用安全等,对成虫及幼虫均有效,对作物无害。可防治柑橘等水果及蔬菜、玉米、棉花、水稻、甘蔗等多种经济作物害虫,对蚜虫的防治效果尤为优异。如:柑桔锈壁虱、蚜虫、潜叶娥、介壳虫,棉花蚜虫、棉铃虫、棉叶蝉,果树蚜虫,蔬菜蚜虫、蓟马,甘蔗蔗螟、玉米蚜虫、蝽蟓、茶树蚜虫、小绿叶蝉,水稻蓟马、螟虫、叶蝉、飞虱,麦类蚜虫等。 问题是:丁硫克百威是由二丁胺与二氯化硫反应制得二丁氨基氯化硫,再与克百威反应而得。能保证丁硫克百威是纯品?
下周实验室要做克百威的残留啦,好像是水稻和土壤中的,求大家给个可行的方法呀~谢谢啦~[em0808]
哪位帮忙发一下克百威和涕灭威的质谱棒图或各3-5个定性离子
5009.218水果蔬菜中的克百威,氧乐果,甲拌磷国标上说的是让用-5ms柱子了,请问可以用1701ms柱吗?
最近实验室在用[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]做克百威,但标准出峰出两个峰,并且两个峰初逢时间间隔比较大,谱库检索分子式都是克百威,想问问大家也是这样吗
克百威的检测,你们是用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]法来检测,还是用[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url](GCMS)法来检测,或者是按照NY/T761-2008中的第三法液相色谱配荧光检测器来检测?
在气相中农残克百威标准品是怎样配制的?
我刚刚做色谱,遇到了一些问题特向各位高手请教!!我使用的是美国热电的GC2000,大口径色谱柱.在做克百威是开始出峰时间为37min左右,但一段时间后出峰时间变为15min左右,这是为何?另外,其灵敏度刚开始就不高,10ug/ml其峰高才一点,而现在100ug/ml才出峰,我如何才能提高其灵敏度呢?色谱条件是50℃保持5min,15℃/min至180℃保持1min,4℃/min至270℃保持60min
克百威用液相来做,需要衍生吗?如何衍生?
克百威的线性不好,如何解决?只有一个9,是离子对与电压值不对吗?用的是[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]AB4500,配的曲线是0.005 0.01 0.05 0.1 0.2ug/mL。大家提供一下它的离子对与电压值。
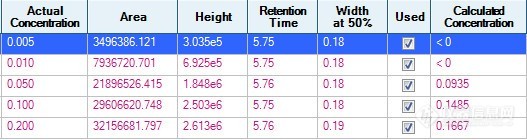
仪器为AB 4500 克百威的离子对是222 165/123 DP:70 CE:17/291. 克百威标液浓度为0.005ug/mL、0.01ug/mL、0.05ug/mL、0.1ug/mL、0.2ug/mL。直线r=0.98 混标24种标液,其它直线可以达到0.995以上2. 流动相为纯水+0.005%甲酸+1mM甲酸铵,有机相为纯甲醇。3. 用纯甲醇配制直线,用样品基质配制直线,直线都很差。4. 同时做不直的还有速灭威、辛硫磷,负离子模式下有氟甲腈、氟虫腈硫醚、氟虫腈砜等。5. 不用怀疑配直线的手法,因为其它农药直线很好,做的是24种混标。6. 进样量为5uL。进样量为1uL时也试过,也是这个样子。[img=,527,140]https://ng1.17img.cn/bbsfiles/images/2022/04/202204071148489957_5150_1645480_3.jpg!w527x140.jpg[/img][img=,690,246]https://ng1.17img.cn/bbsfiles/images/2022/04/202204071148496446_2797_1645480_3.jpg!w690x246.jpg[/img]
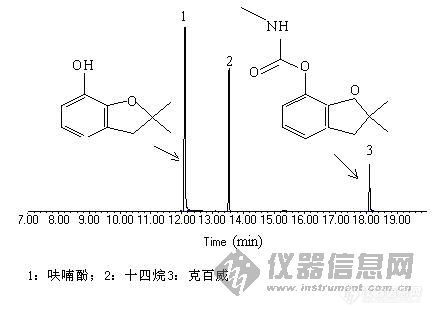
哪位高手帮我做个克百威分解总离子流图(Agilent5973),小弟想比较以下,不甚感激!克百威标液加内标(正十四烷,没有也可以,主要是想看看分解情况)我做的色谱图在附件中色谱分析条件:色谱柱:DB-5MS石英毛细管柱,30m×0.25mm×0.25µ m;氦气作载气,恒流1.0mL/min,采用常规进样口,进样量1µ L,不分流。柱温程序升温条件:起始温度45℃,以5℃/min升至80℃,再以20℃/min升至180℃,保持12 min;离子源为EI源,能量70 eV。离子源温度230oC。传输线温度280oC,四极杆温度150oC。Scan全扫描模式。溶剂延迟4 min。联系方式:QQ:3733818E-mail:yardin@126.com[img]http://ng1.17img.cn/bbsfiles/images/2008/01/200801072111_75839_1640263_3.jpg[/img]
各位老师,农药中克百威用什么方法做?网上查了,方法都作废了
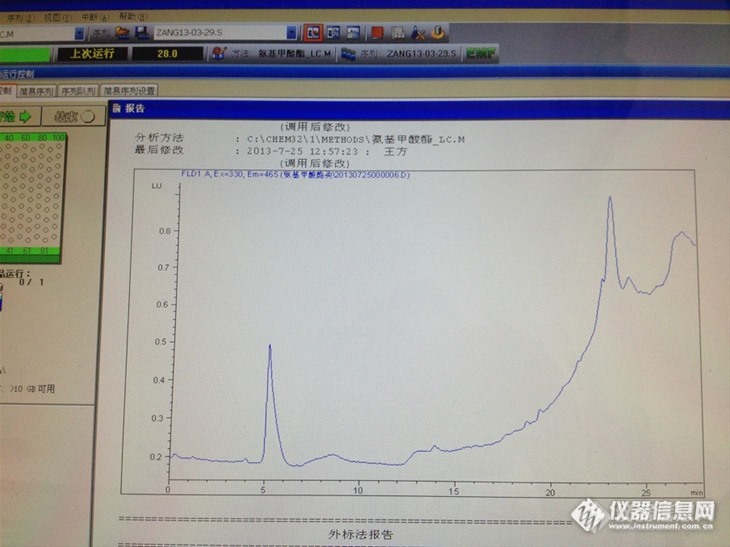
http://ng1.17img.cn/bbsfiles/images/2013/07/201307261126_453820_2691896_3.jpghttp://ng1.17img.cn/bbsfiles/images/2013/07/201307261127_453821_2691896_3.jpg我是新手,第一次根据NY/T761-2008标准检测克百威,安捷伦液相1200检测克百威,感觉峰比较怪,求大家帮忙,我的问题出在哪里,应该怎么改?
哪家单位能做地下水涕灭威 克百威,我这有样分包,能做的单位联系我邮箱31097719@qq.com
我单位新买了一台VARIAN Saturn 2200 [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/MS/MS,我用VF-5ms柱做克百威,条件为:进样口270度、氦气流量1ml/min、柱箱80度1分钟-20度/分钟-230度3分钟、把溶剂延迟设为6min、传输线280度、阱150度,总离子流图在8.42min出现164的离子流峰,当我把溶剂延迟改为4.5min时,在5.65min又发现一个一样的164的离子流峰,请问各位,在5.65min出现的是否也是克百威?
克百威测定采用761液相方法,荧光检测器,用OPA衍生试剂柱后衍生,峰行不稳定、异常
用NY/T761-2008的方法进了丁硫克百威标样,居然不出峰,其他几个氨基甲酸酯类农药都出峰了,是不是丁硫克百威不能用荧光检测器检测啊?
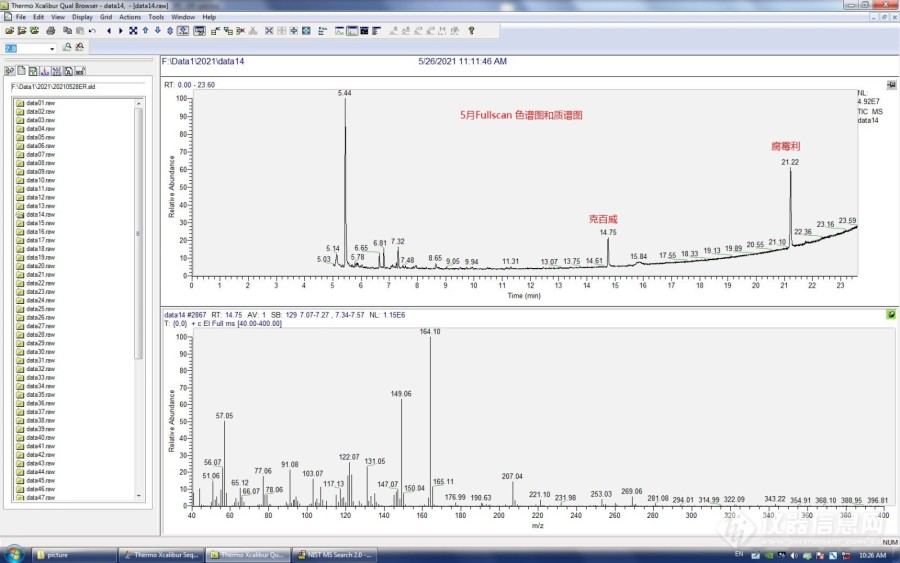
[align=left][b][font=宋体][/font][/b][/align][align=center][b][font=宋体] [size=16px]“探秘”消失的农残克百威组分到哪里去了?[/size][/font][/b][/align][size=16px]一、摘要:[font=宋体]采用[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url][/font][font='Times New Roman','serif']-[/font][font=宋体]质谱分析农药残留组分时,一般做法,先配制好各组分标液,按照规范方法进行测定,得到图谱后先进行定性分析,谱库检索,再可以提取各组分特征离子,以其保留时间定性。以此确定各组分的出峰时间,确定好各组分峰后再进行定量分析,拟合曲线,达标后就可以开始进行样品测试了。小编在一次克百威(呋喃丹)农残检测时,根据年度监测方案要求,上下半年各进行一次采样检测,其中上半年克百威标准组分做得很正常,但到下半年再次做时,却发现克百威组分在原来出峰的位置上消失不见了!所有实验条件都是一样的,而且同时测定其他农残组分都正常,就偏偏克百威组分峰不见了!百思不得其解!下面就跟随小编一起“探秘”解析消失的克百威到哪里去了呢?看看我们能不能成功把它找回来![/font][b][font=宋体]二、实验过程[/font][/b][/size][align=left][size=16px][b][font='Times New Roman','serif']1[/font][font=宋体]、[/font][/b][font=宋体]监测方案:小编的实验室负责食品安全风险检测任务,每年都会进行一些蔬菜水果类型样品的农药残留检测,分批按上下半年进行两次检测,今年监测任务如下表。三月份收到监测任务后,制定试剂耗材采购计划,申报,四月底左右实验物资采购到位,五月开始按方案实施检测工作。其中[/font][font=宋体]采购的克百威(呋喃丹)标物如下图,因为要分上下半年监测,所以同一个批号购买了两支,有效期限为[/font][font='Times New Roman','serif']2[/font][font=宋体]年。[img=,690,361]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021656347539_2906_2694188_3.png!w690x361.jpg[/img][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021700398354_673_2694188_3.png!w690x517.jpg[/img][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021701121334_6415_2694188_3.png!w690x517.jpg[/img][/font][/size][/align][align=left][size=16px][b][font='Times New Roman','serif']2[/font][font=宋体]、[/font][/b][font=宋体]实验操作:[/font][font=宋体]按照监测手册方法要求进行操作,使用设备、仪器条件、标准物质如下表。仪器操作软件为[/font][font='Times New Roman','serif'] Xcalibur [/font][font=宋体]谱库检索库为[/font][font='Times New Roman','serif'] NIST MS search2.0[img=,690,545]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021702088719_7524_2694188_3.png!w690x545.jpg[/img][b][font=宋体]三、五月份的实验结果[/font][/b][/font][/size][/align][align=left][size=16px][b][font='Times New Roman','serif']1[/font][font=宋体]、[/font][/b][font=宋体]五月中旬上半年采样一半量送检,具体实验结果分析如下:[/font][font=宋体]([/font][font=&]1[/font][font=宋体])稀释配制好标准系列溶液,按方法进行仪器设置,调谐,达到最佳状态后开始实验。进样测定,先进中间[/font][font=&]0.5ug/ml[/font][font=宋体]标液,进行[/font][font=&]Fullscan[/font][font=宋体]([/font][font=&]40-400[/font][font=宋体])检测,得到如下色谱图和质谱图。克百威组分在[/font][font=&]14.75min[/font][font=宋体]处出峰,[/font][font=&]21.22min[/font][font=宋体]为腐霉利。[img=,690,431]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021703586897_8935_2694188_3.jpg!w690x431.jpg[/img][/font][/size][/align][align=left][size=16px][font=宋体]([/font][font='Times New Roman','serif']2[/font][font=宋体])对[/font][font='Times New Roman','serif']14.75min[/font][font=宋体]峰进行定性谱库检索,结果如下图。右上框为实测标液的质谱图,右下框为谱库匹配度最高物质的谱图。[img=,690,431]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021705163915_213_2694188_3.jpg!w690x431.jpg[/img][/font][font=宋体]([/font][font='Times New Roman','serif']3[/font][font=宋体])提取克百威三个特征离子[/font][font='Times New Roman','serif']164[/font][font=宋体],[/font][font='Times New Roman','serif']149[/font][font=宋体],[/font][font='Times New Roman','serif']221[/font][font=宋体],得到色谱图如下。可以明显看到三个特征离子的保留时间均一致。综合这些信息判断[/font][font='Times New Roman','serif']14.75min[/font][font=宋体]峰为克百威组分峰。同法得出[/font][font='Times New Roman','serif']21.22min[/font][font=宋体]为腐霉利组分峰。[img=,690,431]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021706572612_3011_2694188_3.jpg!w690x431.jpg[/img][/font][font=宋体]([/font][font='Times New Roman','serif']4[/font][font=宋体])再进行[/font][font='Times New Roman','serif']SIM[/font][font=宋体]([/font][font='Times New Roman','serif']164[/font][font=宋体],[/font][font='Times New Roman','serif']149[/font][font=宋体],[/font][font='Times New Roman','serif']221[/font][font=宋体])检测,得到色谱图和质谱图如下。出峰时间与全扫描完全一致。[img=,690,431]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021707598290_6320_2694188_3.jpg!w690x431.jpg[/img][/font][font=宋体]([/font][font='Times New Roman','serif']5[/font][font=宋体])最后对标准系列图谱进行数据处理,拟合标准曲线,结果如下图。[img=,690,431]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021709171133_6340_2694188_3.jpg!w690x431.jpg[/img][/font][/size][/align][align=left][size=16px][b][font='Times New Roman','serif']2[/font][font=宋体]、[/font][/b][font=宋体]综合分析,五月份做的农残组分分析过程都比较顺利,按照方法进行各个组分识别,图谱解析,都符合预期。让我们觉得挺有成就感的,然而到了下半年再次进行测定时,却出现了一些意想不到的情况,几番波折。[b][font=宋体]四、九月份的实验结果[/font][/b][/font][font='Times New Roman','serif']1[/font][font=宋体]、[/font][font=宋体]九月中旬下半年采样另一半量送检,具体实验结果分析如下:[/font][font=宋体]([/font][font='Times New Roman','serif']1[/font][font=宋体])九月再测,按照完全相同的方法,仪器设置状态也是完全一样,实验结果,标准溶液图谱如下。同一批的另一支克百威标液配制标准系列,相同的浓度,相同的仪器方法。最后做出来的结果却不一样了!出现异常情况!在全扫描中克百威组分在[/font][font='Times New Roman','serif']14.75min[/font][font=宋体]处消失不见了!其他组分如腐霉利却正常还是[/font][font='Times New Roman','serif']21.22min[/font][font=宋体]!真是太奇怪了![img=,690,431]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021712282188_7927_2694188_3.jpg!w690x431.jpg[/img][/font][/size][/align][align=left][size=16px][font=宋体]([/font][font='Times New Roman','serif']2[/font][font=宋体])再进行[/font][font='Times New Roman','serif']SIM[/font][font=宋体]([/font][font='Times New Roman','serif']164[/font][font=宋体],[/font][font='Times New Roman','serif']149[/font][font=宋体],[/font][font='Times New Roman','serif']221[/font][font=宋体])检测,也没有在[/font][font='Times New Roman','serif']14.75min[/font][font=宋体]处找到克百威组分!图谱如下。真是大惑不解啊!克百威怎么就不翼而飞了?到底怎么回事?反思实验过程都和五月做的完全一样啊?为什么得到不同的结果?挠头![img=,690,431]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021713243112_5137_2694188_3.jpg!w690x431.jpg[/img][font=宋体]([/font][font='Times New Roman','serif']3[/font][font=宋体])对无端消失的克百威组分进行查因,先是检查仪器状态都是正常;再是检查标液都是在有效期限内使用,配制过程也没发现异常;最后又更换寸管、隔垫,再次测定,结果还是异常!就是找不到克百威组分!虐心啦[/font][font='Times New Roman','serif']……[/font][font=宋体]改进一个大浓度的标液,结果稍微好一点,[/font][font='Times New Roman','serif']14.75[/font][font=宋体]处有一个很小的峰![/font][font='Times New Roman','serif']……[/font][font=宋体]这似乎看到了一些希望?![/font][font='Times New Roman','serif']……[/font][font=宋体]再次对图谱进行分析,发现端倪了!!结果在[/font][font='Times New Roman','serif']7.32min[/font][font=宋体]处发现有一个比较大的异常的未知峰,对其进行谱库检索,结果如下图。[/font][img=,690,431]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021714351977_5610_2694188_3.jpg!w690x431.jpg[/img][/font][font=宋体]([/font][font='Times New Roman','serif']4[/font][font=宋体])检索结果显示[/font][font='Times New Roman','serif']7.32min[/font][font=宋体]匹配度最高的化合物是呋喃酚![/font][font='Times New Roman','serif']……[/font][font=宋体]呋喃酚([/font][font='Times New Roman','serif']CAS[/font][font=宋体]号[/font][font='Times New Roman','serif']1563-38-8[/font][font=宋体])?呋喃丹([/font][font='Times New Roman','serif']CAS[/font][font=宋体]号[/font][font='Times New Roman','serif']1563-66-2[/font][font=宋体])?两者看着很相似!到底怎么关系?通过[/font][font='Times New Roman','serif']CAS[/font][font=宋体]化合物号码查询,两者谱库里的标准质谱图如下。查资料结果如下:[img=,690,431]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021715584878_1169_2694188_3.jpg!w690x431.jpg[/img][img=,690,431]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021716053486_9007_2694188_3.jpg!w690x431.jpg[/img][/font][font=宋体]([/font][font='Times New Roman','serif']5[/font][font=宋体])网上查询资料,显示呋喃酚是合成呋喃丹的中间体!!一定条件下,呋喃丹的首步降解途径为氨基甲酸酯键发生水解断裂生成呋喃酚!!!综合上述实验资料,至此,终于恍然大悟,原来是标准溶液克百威发生了降解,变成新的组分呋喃酚!新的化合物!分子结构不一样了,所以在相同的色谱质谱条件下,当然不会在原来位置上出峰了!!所以标准峰“漂移”到[/font][font='Times New Roman','serif']7.32min[/font][font=宋体]处出现!!原本应该出峰的位置[/font][font='Times New Roman','serif']14.75min[/font][font=宋体]处就没有了!!至于后面高浓度标液该处又有峰,说明呋喃丹大部分降解变成呋喃酚!但扔有少许未降解,浓度较低[/font][font='Times New Roman','serif'],[/font][font=宋体]所以加大浓度测定后才在[/font][font='Times New Roman','serif']14.75min[/font][font=宋体]处出现小峰!标液此时是大部分呋喃酚和少许呋喃丹的混合状态!——如此理解,之前的所有异常现象就都可以解释得通了!!!为印证此想法,我们又对五月份做的全扫描质谱图进行解析,发现五月做的图谱,虽然克百威在[/font][font='Times New Roman','serif']14.75min[/font][font=宋体]处正常出峰,但在[/font][font='Times New Roman','serif']7.32min[/font][font=宋体]处也存在呋喃酚组分峰出现!只是峰很小!当时做完没注意到而已!!提取特征离子图,如下图(呋喃丹[/font][font='Times New Roman','serif']164[/font][font=宋体]、[/font][font='Times New Roman','serif']149[/font][font=宋体]、[/font][font='Times New Roman','serif']221[/font][font=宋体]保留时间均一致,而呋喃酚[/font][font='Times New Roman','serif']164[/font][font=宋体]、[/font][font='Times New Roman','serif']149[/font][font=宋体]时间一致,[/font][font='Times New Roman','serif']221[/font][font=宋体]不一致时间有偏差,因为呋喃酚没有该特征离子)。说明克百威标液从四月购买到五月第一次测定,再到九月第二次测定,一直有在降解,只是五月降解少,没有出现异常,一直到九月降解很多了,再做就出现这种异常情况!!如此解释,感觉所有的实验异常情况都豁然而通了!所有的疑惑都解除了![img=,690,431]https://ng1.17img.cn/bbsfiles/images/2022/11/202211021717345001_3752_2694188_3.jpg!w690x431.jpg[/img][/font][font=宋体][b][font=宋体]五、追根究底[/font][/b][font=宋体] 最后总结分析,五月九月前后两次做的克百威(呋喃丹)组分实验出现反差的原因,最大可能就是标液保存不当造成的待测组分降解导致结果异常!经查克百威(呋喃丹)标液一直保存在冰箱冷藏柜[/font][font='Times New Roman','serif']4[/font][font=宋体]度左右!查看标液证书说明,建议保存条件为[/font][font='Times New Roman','serif']-18[/font][font=宋体]度!如此才最低减少呋喃丹的降解!最后我们还就此问题咨询了上级监测部门,说起此“灵异”事件,不巧他们以前也曾经发生过类似问题![/font][font='Times New Roman','serif']……[/font][font=宋体]一语言之,要多交流学习,才能少走弯路啊![/font][b][font=宋体]六、[/font][font=宋体]后记[/font][/b][font='Times New Roman','serif'] [/font][font=宋体]话说,既然克百威(呋喃丹)较易降解,那我们日常监测的水果蔬菜样品中的农残呋喃丹组分,会不会也降解了?那我们只检测呋喃丹组分会不会造成偏差导致结果误判呢?或者还是需要增加做一下降解物呋喃酚?[/font][/font][font=宋体][/font][/size][/align][size=16px][font=宋体][/font][font=宋体][b][font=宋体][/font][/b][/font][/size][font=宋体][/font]
请问谁有用安捷伦GC7890A做过蔬菜中的克百威和多菌灵啊?我用FPD检测器,HP 5柱只能做出一般的有机磷,但是克百威和多菌灵测不出来,用DB 17就都测不出来了。谁有相关的实验条件吗?请告知啊,急用,谢谢啦!
克百威衍生一定要柱后衍生吗?能不能自己手动衍生再上机?有没有做过呢?