背照式CMOS图像传感器工艺中_硅晶圆背面抛光的新技术!
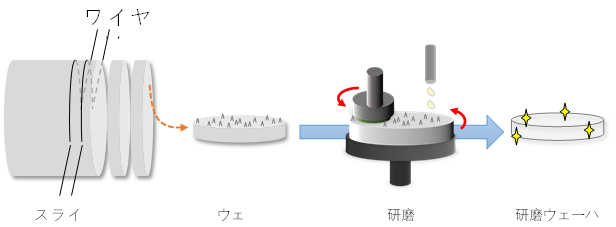
新加坡科技研究局微电子研究所Institute of Microelectronics Agency for Science的Venkataraman等人与奥地利Nexgen Wafer Systems公司以及新加坡格罗方德公司GlobalFoundries的工程师组成研究团队,共同开发出一种新的晶圆背面抛光技术。在光检测与测距(LiDAR)等各种应用中,背照式三维堆叠CMOS图像传感器备受该领域专家们关注。这种三维集成器件的重要挑战之一,是对单光子雪崩二极管(SPAD)晶圆的精确背面抛光,该晶圆与CMOS晶圆堆叠,晶圆背面抛光通常通过背面研磨和掺杂敏感湿法化学蚀刻硅的组合来实现。研究团队开发了一种湿法蚀刻工艺,基于HF:HNO3:CH3COOH定制化学试剂,能够在p+/ p硅过渡层实现蚀刻停止,掺杂剂选择性高达90:1。他们证明了全晶圆300mm内厚度变化仅约300nm的可行性。此外,也对HNA蚀刻硅表面的着色和表面粗糙度进行了表征,最后,提出一种湿法锥蚀方法来降低表面粗糙度。该研究成果发表于2023年5月30日至6月2日在美国佛罗里达州奥兰多召开的第73届电子组件与技术会议(ECTC)上。论文录用日期为2023年8月3日,并被IEEE Xplore 收录。这项突破将有可能推动背照式CMOS图像传感器在汽车智能驱动等领域的应用。