黄芪饮片按照中国药典2015年版方法测定黄芪甲苷液相图谱为2个峰,用含黄芪的超微粉制成的颗粒,测定其黄芪甲苷,液相图谱为1个峰,为什么?颗粒不只含有黄芪,含有其他成分,求解答,谢谢
黄芪静脉输液中黄芪甲苷和黄芪多糖的含量测定摘要:建立黄芪静脉输液中黄芪甲苷和黄芪多糖的含量测定方法。方法:用高效液相色谱法测定黄芪甲苷的含量,用碘量法测定黄芪多糖的含量。结果:黄芪甲苷和黄芪多糖的平均回收率分别为9751%、9918%,相对标准差分别为248%、191%。结论:本文建立的方法准确可靠、灵敏度高、重现性好,可作为黄芪静脉输[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]量控制的有效方法。关键词:黄芪甲苷;黄芪多糖;高效液相色谱法;碘量法; 英文摘要:ToestablishthemethodfordeterminationofastragalosideIVandastragaluspolysaccharidesinRadixAstragaliinjectionMETHODS:AstragalosidewasdeterminedbyHPLCandastragaluspolysaccharidesbyiodometryRESULTS:Therecoveriesofastragalosideandastragaluspolysaccharideswere9751%RSD=248%and9918%(RSD=191%)respectivelyCONCLUSION:Thismethodisaccurate,sensitiveandrepeatable,andcanbeusedforqualitycontrolofthepreparation英文关键词:astragaloside;astragaluspolysaccharide;HPLC;iodometry;contentdetermination黄芪为补气药,性甘温,归肺、脾经,具有补气固表、利尿托毒、排脓、敛疮生肌之功效。医疗实践证明,黄芪注射液对心气虚损、血脉瘀阻、病毒性心肌炎、心功能不全、脾虚困湿之肝炎有较好的疗效,也是肿瘤、免疫功能低下等较理想的辅助治疗药物。目前临床所使用的黄芪注射液为小容量针剂,需稀释后滴注,且不含黄芪多糖,所以疗效不够理想。为此,武警四川总队乐山医院和四川省乐山市三民药物研究所共同研制了含黄芪多糖、黄酮、苷类等有效成分的黄芪静脉输液。黄芪注射液的含量检测尽管WS3-β-3335-98执行标准仅要求采用薄层色谱法,但因高效液相色谱法操作更简便,精密度更高,故笔者参照文献以蒸发光散色高效液相色谱法[1]测定黄芪静脉输液中的黄芪甲苷含量;至于黄芪多糖含量的检测则选择采用碘量法。1仪器与试药11仪器美国奥泰公司高效液相色谱仪,包括蒸发光散射(ELSD)500检测器、Alltech426主机泵;电动离心机(江苏金坛公司);TP-150超声波清洗机(北京天鹏公司)。12试药黄芪甲苷对照品(中国药品生物制品检定所,批号:0781-9908);甲醇、乙醇、正丁醇、氢氧化钠、硫酸、葡萄糖均为分析纯;乙腈为色谱纯;水为重蒸馏水。2方法和结果21黄芪甲苷含量的测定211色谱条件:色谱柱为ODS柱(250mm×40mm),柱温为40℃,流动相为乙腈-水(36∶64),流速为06ml/min,进样量为20μl。212漂移管温度选择:根据ELDS检测使用手册推荐,设置气体流速为300slpm,漂移管温度为75℃,观察流动相(不进样)进入检测器的基线噪音,不断改变漂移管温度(步长为5℃),根据基线随温度的变化情况,选择95℃为试验最优温度。213载气流速选择:设定漂移管温度为95℃,取黄芪甲苷对照液恒量,得相应峰面积,不断改变气体流速(步长为025slpm)观察峰面积和基线的变化情况,最终选择270slpm为试验最优载气流速。214最低检测限试验:精密称取黄芪甲苷对照品适量,加甲醇溶解并稀释成浓度为1mg/ml的溶液作为贮备液,精密量取适量,逐步稀释测定,直到黄芪甲苷主峰信号为检测器噪声水平的3倍为止。得黄芪甲苷最低检测限为153ng。215线性试验:取“214”项黄芪甲苷对照品贮备液适量,精密量取10、20、30、40、50、60分别置于10ml容量瓶中,加甲醇稀释至刻度(约相当于黄芪甲苷01、02、03、04、05、06mg)。以对照品峰面积的常用对数值为横坐标(X),以进样量的常用对数值(Y)为纵坐标进行线性回归,得回归方程为Y=06001X—34896(r=09991),黄芪甲苷进样量在20μg~120μg范围内线性关系良好。216精密度试验:精密称取黄芪甲苷对照品适量,加甲醇溶解并稀释至浓度为025mg/ml的溶液作为对照溶液,注入液相色谱仪,连续重复进样6次,测得黄芪甲苷的相对标准差为179%,精密度符合规定。217重现性试验:精密量取黄芪注射液适量(相当于黄芪甲苷约20mg)5份,按“2110”项下方法制备,测定黄芪甲苷含量。结果黄芪注射液中黄芪甲苷为2390mg,RSD=201%,表明方法重现性良好。218稳定性试验:取“217”项下样品溶液,分别于0、1、2、3、5、8h取样测定峰面积,结果RSD=107%,表明黄芪甲苷溶液在8h内基本稳定。219回收率试验:分别精密量取黄芪注射液适量(约相当于黄芪甲苷10、12、14mg)共3份,每份各精密加入对照溶液(0404mg/ml)25、30、35ml,按“2110”项下方法制备,测定黄芪甲苷含量,结果详见表1。由表1可见,平均回收率为9751%,RSD=248%,符合规定,说明方法具有可行性。2110样品中黄芪甲苷的含量测定:精密量取黄芪注射液100ml,置于烧杯中浓缩至10ml,加无水乙醇40ml沉淀,放置20min,离心,沉淀用80%的乙醇溶液洗涤2次,每次10ml,合并离心液与洗涤液,置水浴上蒸干。残渣加1%NaOH溶液10ml溶解,用饱和的正丁醇水溶液提取3次,每次20ml,合并正丁醇的水溶液,蒸干,残渣再加1%NaOH溶液5ml溶解,通过已处理的D101大孔吸附树脂柱(Φ15×20cm,内装树脂高约10cm)吸附,以1%NaOH溶液50ml洗脱,弃去,用蒸馏水洗至中性,再用30%乙醇溶液50ml洗脱,弃去洗脱液,继续用70%乙醇液50ml洗脱,收集洗脱液并蒸干,残渣加甲醇溶解并定容至10ml,得供试品溶液。精密称取黄芪甲苷对照品适量,加甲醇溶解并稀释成浓度为01、03mg/ml的溶液作为对照溶液。分别精密量取上述溶液各20μl注入液相色谱仪,记录色谱图,并以峰面积和进样量的对数值按二点法计算,详见图1;3批样品按上述方法制备测定,结果详见表2。22黄芪多糖含量的测定[2,3]221线性试验:精密称取105℃干燥至恒重的葡萄糖适量,加水溶解并稀释成浓度为10mg/ml的标准溶液,分别精密量取此标准溶液100、90、80、70、60ml,置于250ml碘量瓶中,分别加水0、10、20、30、40ml,然后精密加入01mol/L碘滴定液25ml,在不断振摇的情况下缓缓滴加01mol/LNaOH40ml,密塞,在暗处放置10min,然后加入05mol/LH2SO4液6ml,摇匀,立即用01mol/LNa2S2O3滴定液滴定,近终点时,加淀粉指示液2ml,继续滴定至蓝色消失,并同时作空白试验校正。以取样量(X)与Na2S2O3的消耗量(Y)进行线性回归,得回归方程为Y=009766X—000244,(r=09999),表明葡萄糖在60mg~100mg的范围内线性关系良好。222重现性试验:精密量取黄芪注射液100ml,按“224”项下方法制备5份,测定黄芪多糖含量,结果为10423mg,RSD=099%,表明方法重现性良好。223回收率试验:分别精密量取黄芪注射液(多糖含量为10423mg/100ml)120、150、180ml,每份各加入葡萄糖标准液(25002mg/ml)50、60、70ml制成80%、100%、120%浓度的溶液。分别浓缩至10ml,加无水乙醇40ml,放置20min,离心。沉淀用80%乙醇洗涤2次,每次10ml,弃去离心液与洗涤液,沉淀加热蒸馏水10ml溶解,并转移至25ml容量瓶中,定容,摇匀。分别精密量取3种不同浓度的溶液80、70、60ml置于250ml碘量瓶中,分别精密加水2、3、4ml,按“224”项方法测定,每个浓度测定3次,共9次,计算得到回收率为9918%,RSD=191%,详见表3。224样品中黄芪多糖的含量测定:精密量取黄芪注射液100ml,浓缩至10ml,加无水乙醇40ml,放置20min,离心。沉淀用80%乙醇洗涤2次,每次10ml,加热蒸馏水3ml使沉淀溶解并定容至10ml,摇匀。移置于250ml碘量瓶中,加入1mol/LH2SO420ml,置于水浴中水解2h,取出,放冷,加入2mol/LNaOH溶液调节pH值=7,冷却至室温。精密加入碘滴定液(01mol/L)25ml,在不断振摇的情况下缓缓滴加01mol/LNaOH40ml,密塞,置暗处放置10min。然后加入05mol/LH2SO46ml,摇匀,立即用Na2S2O3滴定液(01mol/L)滴定,至近终点时,加淀粉指示液2ml,继续滴定至蓝色消失,并同时作空白试验校正,计算即得(每1ml上述碘滴定液相当于9008mg的C6H12O6)。3批黄芪注射液样品,按上述方法测定多糖含量均符合规定,结果详见表4。3讨论测定黄芪甲苷含量时,如将精密量取的黄芪注射液浓缩后仅采用正丁醇的水饱合液提取制得供试品溶液,则所得的样品杂质峰多,基线略有漂移,因此不宜采用。黄芪多糖主要为葡萄糖,因此,可采用以葡萄糖或葡聚糖作对照品的苯酚-浓硫酸法[4]、蒽酮-浓硫酸法[5]或水解后用碘量法等测定其含量,但一般多采用后两种方法。采用蒽酮-浓硫酸法时,由于其线性试验回归方程为C=98481A+08314(r=09663),浓度线性范围为35~165μg/ml,线性关系不好,故不宜采用。
食疗方--【黄芪补气茶】【食材】黄芪10克、西洋参10克、枸杞子10克。【做法】煎水服用。【效果】益气滋阴、清热降火、消除疲劳、增强大脑记忆力。
黄芪有促雌激素样作用,可使小鼠动情期(通常为一日)延续达10日之久。黄芪对小鼠的发育亦有良好影响。另有报告谓黄芪浸膏、黄芪内酯和黄芪固醇对大鼠和小鼠体重、提肛肌或肾脏等重量均无明显影响,表明无同化激素或雄激素样作用。红芪(多序岩黄芪)为黄芪的同科不同属植物,其多糖可明显升高老年大鼠血清睾酮含量。注:摘自《医学中央杂志》、《新医药学杂志》、《北京生理科学会1964年学术年会论文摘要》、《甘肃中医学院学报》
想问问各位你们都是用什么测黄芪甲苷的,用什么牌子的仪器,感觉怎么样?国家对测黄芪甲苷的仪器有什么灵敏度或者是其他方面的规定吗?我们公司想买蒸发光散射检测器来测黄芪甲苷,大家觉得哪个好些?老板的心理价位就8-10万吧,谢谢各位[em58]
检测黄芪药材中的黄芪甲苷,用elsd检测器,c18柱,雾化管30 漂移管70 药典方法乙腈比水32比68 对照品塔板数11000,但是样品塔板数才2800,含量合格,要求塔板数是4000这是怎么回事,重做了好多次塔板数就是上不去
[align=center][color=#333333]黄芪含量测定[/color][/align]1 材料与试剂 乙腈(色谱级)、正丁醇、氨水、甲醇(分析纯)、黄芪甲苷(购自中检院)、血竭样品(送检样品)。2 色谱条件 LC-20AT液相色谱仪(日本岛津),色谱柱:Zorbax SB C18(250mm*4.6μm*5μm)(安捷伦),流动相:以乙腈-水(30:70);蒸发光检测器(奥泰);柱温35℃。3 样品制备(参照2015年版药典) 3.1 标准品溶液的制备 取黄芪甲苷对照品适量,精密称定,加甲醇溶解,即得。[align=center][img=,555,177]https://ng1.17img.cn/bbsfiles/images/2019/09/201909121553061421_926_1858223_3.jpg!w555x177.jpg[/img][/align]3.2 样品溶液的制备 取本品中粉约4g,精密称定,置索氏提取器中,加甲醇40ml,冷浸过夜,再加甲醇适量,加热回流4小时,提取液回收溶剂并浓缩至干,残渣加水10ml,微热使溶解,用水饱和的正丁醇振摇提取4次,每次40ml,合并正丁醇液,用氨试液充分洗涤2次,每次40ml,弃去氨液,正丁醇液蒸干,残渣加水5ml使溶解,放冷,通过D101型大孔吸附树脂柱(内径为1.5cm,柱高为12cm),以水50ml洗脱,弃去水液,再用40%乙醇30ml洗脱,弃去洗脱液,继用70%乙醇80ml洗脱,收集洗脱液,蒸干,残渣加甲醇溶解,转移至5ml量瓶中,加甲醇至刻度,摇匀,即得。[align=center][img=,583,180]https://ng1.17img.cn/bbsfiles/images/2019/09/201909121553295651_9515_1858223_3.jpg!w583x180.jpg[/img][/align]3.3 计算方法 分别精密吸取对照品溶液10μl、20μl,供试品溶液20μl,注入液相色谱仪,测定,用外标两点法对数方程计算,即得。小结:每次接到黄芪样品大家都会来一句怎么又有黄芪,大概黄芪是比较受嫌弃的中药材之一了,药典上的方法过程比较繁琐,一般需要2-3天才能把前处理处理完。检测简述流程:浸泡过夜——索氏提取4h——旋干——萃取 (4次+2次)——蒸干(这个正丁醇不太好旋干比较耗时)——过大孔树脂柱(上样之前要洗至无醇味,然后上样后用3种溶剂洗脱)——旋干——定容待测。为了减少误差及节省时间,我们考察了正丁醇的萃取次数对含量的影响,我们用2次80ml和4次40ml进行对比发现结果相当,实验操作过程中萃取次数越多反而容易引起操作误差,值得大家注意的是大孔树脂上样前要洗至无醇味,这个对结果影响还是有的,保证数据的平行性,用同体积的水进行洗至无醇味。
黄芪多糖提取用水提,还是醇提出膏率跟纯度哪个好一点
建立高效液相色谱-蒸发光散射检测器测定黄芪甲苷含量的方法。方法:采用一种新的检测器-蒸发光散射检测器(ELSD)以黄芪甲苷为对照品对黄芪中的黄芪甲苷进行HPLC分析,色谱柱:Phenomenex-ODS;流动相:乙腈-水(37∶63);流速:0.85mL/min;ELSD参数;漂移管温度:100℃;载气流速:2.7L/min。结果:黄芪甲苷在0.396~3.564μg范围内呈线性,回收率为97~94%(RSD=0.68%)。结论:本法具有良好的精密度和重现性,结果准确可靠,可作为原料的质量控制方法。
咳嗽喝黄芪陈皮饮。取黄芪15克、陈皮5克、红枣(去核)2—4枚,将所有原料放入锅中,加适量清水煎煮30分钟即可。该茶饮有助补肺、固表、健脾,适用于疲倦乏力、咳嗽不止者。??皮饮。取黄芪15克、陈皮5克、红枣(去核)2—4枚,将所有原料放入锅中,加适量清水煎煮30分钟即可。该茶饮有助补肺、固表、健脾,适用于疲倦乏力、咳嗽不止者。??
高效液相色谱法测定黄芪中黄芪甲苷含量的计算方法
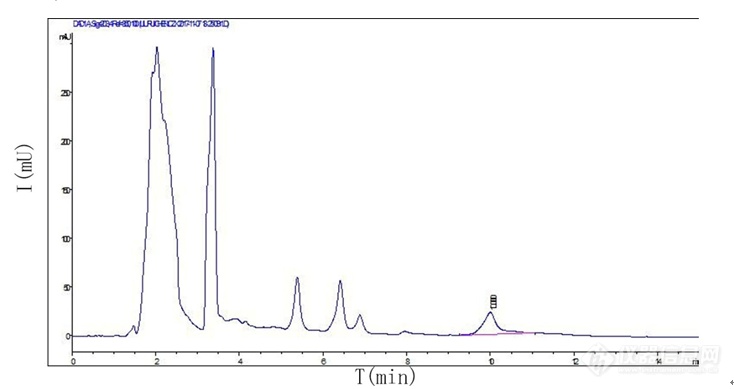
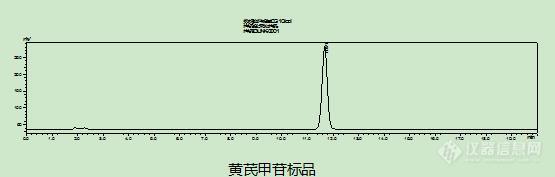
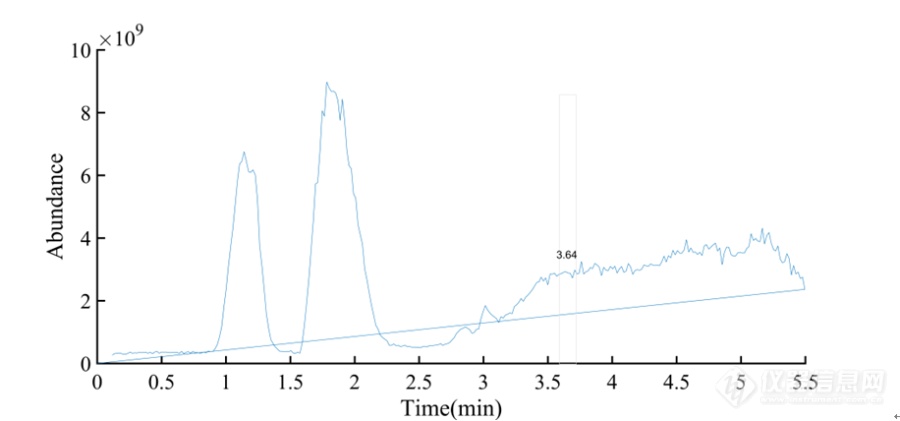
[align=center][b]HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS法测定黄芪醇提物中的黄芪甲苷的含量[/b][/align][b]黄芪甲苷是黄芪皂苷提取物中的特征性成分,也是具有代表性的主要成分,黄芪甲苷可以促进患者心肌细胞的供氧能力,使冠状动脉供血区供血充足,避免因缺血导致的大范围心肌坏死,继而缓解患者心绞痛症状,平稳心跳速率[sup][/sup]。药典中有关于黄芪药材中黄芪甲苷含量的测定方法,但此方法并不完全适用于黄芪醇提物中的黄芪甲苷的含量测定,而且黄芪水提物与黄芪醇提物中化学成分有差异,预实验中发现测定黄芪水提物中黄芪甲苷含量建立的方法也不适应于黄芪醇提物中中黄芪甲苷含量的测定。本章实验利用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用仪[/color][/url]建立黄芪醇提物中黄芪甲苷含量测定方法,并利用该方法测定其含量,计算出黄芪甲苷的转移率,用于黄芪醇提最佳提取工艺的优选。同时,本章实验系统地验证所建立的方法的可行性,为选择黄芪甲苷的含量测定方法提供参考。[b]1 材料和仪器1.1 样品 [/b] 收集9组黄芪醇提物样品,所有黄芪药材均由济宁华能制药厂提供。[b]1.2 试剂 [/b]黄芪甲苷对照品(成都瑞芬思生物科技有限公司批号H-013-170117);乙腈为色谱纯(赛默飞世尔科技有限公司);D101大孔吸附树脂(廊坊淼阳化工有限公司生产20160310);盐酸溶液(国药集团化学试剂有限公司生产);氢氧化钠溶液(国药集团化学试剂有限公司生产20160824);超纯水。[b]1.3 仪器 [/b]液相色谱仪系统(美国Agligent Technology 公司1260型液相色谱仪,包括G1312B二元泵,G1322A在线脱气机,G1316A柱温箱);NASCA F5100型自动进样器(日本SHISEIDO公司);资生堂CAPCELL PAC CN 色谱柱(2.0*150 mm,5 mm,日本SHISEIDO公司);API 4000型三重四级杆串联离子肼质谱仪(美国Applicated Biosystem Scuex公司)。[b]2 方法学考察2.1 色谱条件[/b]色谱柱为 Synergi C18 80A(250 mm×4.6 mm,4 μm),以十八烷基硅烷键合硅胶为填充剂,以乙腈-水(35 : 65)进行等度洗脱;进样量10 μL;检测波长为203 nm;柱温30 ℃,流速为1 mL/min。黄芪甲苷保留时间约为10 min。黄芪醇提物和黄芪甲苷标准品HPLC色谱图见表5-1,表5-2。[/b][align=center][img=,690,365]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131711071808_2711_3237657_3.png!w690x365.jpg[/img][/align][align=center]图5-1 黄芪醇提物HPLC色谱图[/align][align=center][img=,690,373]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131711240945_4181_3237657_3.png!w690x373.jpg[/img][/align][align=center]图5-2 黄芪甲苷标准品HPLC色谱图[/align][b]2.2 质谱条件 [/b]电喷雾电离,正离子模式(喷雾电压:4.5 kV);鞘气压力:30 arb;辅助气压力:10 arb;离子传输管温度:550 ℃;扫描模式:全扫描;扫描范围:m/z 100-1000。按“2.1.3”项下色谱条件进样,进样量10 μL。为进一步验证10 min出峰的物质是黄芪甲苷,利用LC/MS技术对黄芪皂苷提取物的化学成分进行研究,采用正离子源ESI检测。黄芪甲苷分子量784.97 Da,由于仪器差异,黄芪甲苷出峰时间后移至12.5 min,此峰的鉴定结果质谱图显示含大量黄芪甲苷。图5-3为黄芪皂苷提取物的正离子模式HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]总离子流图、分离子流图和质谱图。[align=center][img=,690,426]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131711415732_2681_3237657_3.png!w690x426.jpg[/img][/align][align=center]图5-3 黄芪甲苷正离子模式HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url] 总离子流图、分离子流图和质谱图[/align][b]2.3 供试品溶液的制备[/b]对D101大孔吸附树脂预处理:第一步用乙醇或甲醇清洗吸附柱内壁,向柱内加入称量好的树脂体积0.4-0.5倍的乙醇或甲醇,然后将新的D101大孔吸附树脂投入吸附柱中,使乙醇液面高于D101大孔吸附树脂层0.5 m,浸泡过夜。用2 个柱体积的乙醇或甲醇通过D101大孔吸附树脂层,用乙醇缓慢浸泡D101大孔吸附4-5 h,观察洗脱液加水后不呈白色浑浊为止。再用蒸馏水以2 BV洗柱,洗至洗脱液呈中性。用2 BV的5 %盐酸溶液以4-6 BV/h过柱,浸泡2-4 h。用蒸馏水以2 BV/h洗至洗脱液呈中性。用2 BV的2 %氢氧化钠溶液以4-6 BV/h过柱,浸泡2-4 h。最后用蒸馏水洗D101大孔吸附树脂,洗至洗脱液显中性即可。上样:取黄芪醇提物加水溶解至15 mL得黄芪提取液,以1 mL/min过树脂,先以4 BV蒸馏水洗脱,弃去水液,再用4 BV的70 %乙醇溶液洗脱,用烧杯收集吸附柱内的洗脱液,转入蒸发皿,水浴蒸干后,用甲醇溶解并转移至10 mL容量瓶定容。[b]2.4 对照品溶液的制备[/b]用万分之一天平精密称取10.1 mg黄芪甲苷对照品至10 mL容量瓶,加甲醇定容,得1.01mg/mL的对照品溶液,用0.22μm的微孔滤膜过滤,备用。[b]3 结果3.1 线性关系考察[/b]精密量取黄芪甲苷标准品10.1 mg黄芪甲苷,用甲醇10 mL制备成1.01 mg/mL黄芪甲苷储备液,然后吸取相应体积稀释成浓度梯度为150 μg/mL、250 μg/mL、300 μg/mL、400 μg/mL 、500 μg/mL的对照品溶液,上述对照品溶液按“2.3”项下色谱条件分别进样10 μL,利用自动积分功能测定峰面积积分值,以黄芪皂苷提取物中黄芪甲苷的峰面积积分值对标准品浓度进行线性回归,所得回归方程为y = 2821.6x + 12.438(回归系数[i]R[sup]2[/sup][/i]= 0.9989),证明蒙古黄芪中黄芪甲苷在150~500 μg/mL范围内线性关系良好,黄芪甲苷对照品标准曲线如图5-4所示。[align=center][img=,542,346]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131711574358_4557_3237657_3.png!w542x346.jpg[/img][/align][align=center]图5-4 黄芪甲苷标准曲线[/align][b]3.2 精密度试验[/b]在拟定分析条件下,精密吸取供试品溶液10 μL,连续进样 6 次,记录提取离子流图峰面积,测定黄芪甲苷量,计算得相对标准偏差RSD为1.9% ,提示该方法具有较好的精密度。[b]3.3 重复性实验[/b]取同一黄芪样品 6份,按2. 2 项下方法制备供试品溶液,在拟定分析条件下,准确吸取10 μl 进样分析,测定黄芪甲苷量,计算得 RSD为2.0%,提示该方法重复性良好。[b]3.4 稳定性试验[/b]取黄芪药材供试品溶液,分别在0 h、3 h、6 h、9 h、24 h、48 h后,在拟定分析条件下,准确吸取10 μl 进样分析,测定黄芪甲苷量,计算得RSD为 4.4% ,提示黄芪供试品溶液稳定性较差。[b]3.5 加样回收率试验[/b]精密称取 6 份黄芪甲苷量已知的黄芪水提物样品,每份折合黄芪药材 0. 5 g,分别准确加入浓度为 0. 0 342 mg /ml 黄芪甲苷溶液1 ml,1 ml,2ml,2ml,3ml,3ml,按 2. 2 项下方法制备供试品溶液,准确吸取 1. 0 μl 进样分析,测定黄芪甲苷量,计算回收率,结果见表3-1。由表3-1可见,方法平均回收率为 97.92%,表明该方法具有较好的回收率。[align=center]表5-1 黄芪甲苷加样回收率测定结果[/align] [table][tr][td] [align=center]样号[/align] [/td][td] [align=center]样品中的量/mg[/align] [/td][td] [align=center]加入量/mg[/align] [/td][td] [align=center]测得量/mg[/align] [/td][td] [align=center]回收率/%[/align] [/td][td] [align=center]平均值/%[/align] [/td][td] [align=center]RSD/%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]0.96 [/align] [/td][td] [align=center]2.88 [/align] [/td][td] [align=center]97.92 [/align] [/td][td=1,6] [align=center]97.92 [/align] [/td][td=1,6] [align=center]0.7 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]0.96 [/align] [/td][td] [align=center]2.89 [/align] [/td][td] [align=center]98.96 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]1.92 [/align] [/td][td] [align=center]3.83 [/align] [/td][td] [align=center]98.44 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]1.92 [/align] [/td][td] [align=center]3.81 [/align] [/td][td] [align=center]97.40 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]2.88 [/align] [/td][td] [align=center]4.76 [/align] [/td][td] [align=center]97.92 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]2.88 [/align] [/td][td] [align=center]4.73 [/align] [/td][td] [align=center]96.88 [/align] [/td][/tr][/table][b]3.6 黄芪甲苷的含量测定结果[/b]取9组黄芪水提物按照“2.3”项下操作,制备供试品溶液,准确吸取 1 0 μL 进样分析,在拟定的分析条件下,测定黄芪甲苷峰面积积分值,计算相应的黄芪甲苷含量。9组蒙古黄芪中黄芪甲苷含量测定结果如表5-2所示。[align=center]表5-2 9组蒙古黄芪中黄芪甲苷含量测定结果[/align] [table][tr][td] [align=center]试验号[/align] [/td][td] [align=center]峰面积[/align] [/td][td] [align=center]含量(mg/g)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]560.07 [/align] [/td][td] [align=center]0.13 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]501.70 [/align] [/td][td] [align=center]0.12 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]564.61 [/align] [/td][td] [align=center]0.13 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]507.19 [/align] [/td][td] [align=center]0.12 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]524.05 [/align] [/td][td] [align=center]0.12 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]477.02 [/align] [/td][td] [align=center]0.11 [/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]921.07 [/align] [/td][td] [align=center]0.21 [/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]783.88 [/align] [/td][td] [align=center]0.18 [/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]924.71 [/align] [/td][td] [align=center]0.22 [/align] [/td][/tr][/table][b]3.7 黄芪甲苷转移率正交试验设计及结果[/b]醇提的黄芪甲苷转移率考察正交试验与醇提的出膏率考察正交试验设计相同,首先以乙醇作为提取溶剂,把影响药材提取效果的提取溶剂乙醇用量(A)、提取次数(B)、提取时间(C)确定为考察因素,以上三个考查因素各分3个水平考察,见表5-3。[align=center]表5-3 实验因素水平表[/align] [table][tr][td=1,2] [align=center]水平[/align] [/td][td=3,1] [align=center]因素[/align] [/td][/tr][tr][td] [align=center]A(乙醇用量/倍)[/align] [/td][td] [align=center]B(提取次数/次)[/align] [/td][td] [align=center]C(提取时间/h)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]4[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]8[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]10[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][/tr][/table]黄芪甲苷转移率=各实验组黄芪提取物中黄芪甲苷含量/原黄芪药材中黄芪甲苷含量×100%。原药材中毛蕊异黄酮苷的含量按照药典的方法测得的结果为0.4042mg/g。跟据实验数据,得到水提实验中设定的不同工艺条件下的毛蕊异黄酮苷的转移率,其中因素D为误差项,作直观分析表和方差分析表,见表5-4,5-5。[align=center]表5-4 黄芪甲苷转移率考察 L[sub]9[/sub](3[sup]4[/sup])正交试验表[/align] [table][tr][td] [align=center]试验号[/align] [/td][td] [align=center]A[/align] [/td][td] [align=center]B[/align] [/td][td] [align=center]C[/align] [/td][td] [align=center]D[/align] [/td][td] [align=center]黄芪甲苷 转移率/%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]32.01 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]28.60 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]32.28 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]28.92 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]29.91 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]27.16 [/align] [/td][/tr][tr][td] [align=center]试验号[/align] [/td][td] [align=center]A[/align] [/td][td] [align=center]B[/align] [/td][td] [align=center]C[/align] [/td][td] [align=center]D[/align] [/td][td] [align=center]黄芪甲苷 转移率/%[/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]53.11 [/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]45.09 [/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]53.33 [/align] [/td][/tr][tr][td] [align=center]K1[/align] [/td][td] [align=center]92.89[/align] [/td][td] [align=center]114.04[/align] [/td][td] [align=center]104.26[/align] [/td][td] [align=center]115.25[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]K2[/align] [/td][td] [align=center]85.99[/align] [/td][td] [align=center]103.60[/align] [/td][td] [align=center]110.85[/align] [/td][td] [align=center]108.87[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]K3[/align] [/td][td] [align=center]151.53[/align] [/td][td] [align=center]112.77[/align] [/td][td] [align=center]115.30[/align] [/td][td] [align=center]106.29[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]优水平[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]R[/align] [/td][td] [align=center]65.54[/align] [/td][td] [align=center]9.17[/align] [/td][td] [align=center]11.04[/align] [/td][td] [align=center]8.96[/align] [/td][td] [align=center] [/align] [/td][/tr][/table][align=center]表5-5 黄芪甲苷转移率考察方差分析结果[/align] [table][tr][td] [align=center]方差来源[/align] [/td][td] [align=center]离差平方和[/align] [/td][td] [align=center]自由度[/align] [/td][td] [align=center]F[/align] [/td][td] [align=center]显著性[/align] [/td][/tr][tr][td] [align=center]A[/align] [/td][td] [align=center]864.64[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]46.01[/align] [/td][td] [align=center]*[/align] [/td][/tr][tr][td] [align=center]B[/align] [/td][td] [align=center]21.63[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]0.07[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]C[/align] [/td][td] [align=center]20.57[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]0.07[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]D [/align] [/td][td] [align=center]14.18[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]-[/align] [/td][/tr][/table]注:F[sub]0.1[/sub](2,2)=9,F[sub]0.05[/sub](2,2)=19,*为有显著性,-为无显著性。从正交试验结果可知:醇提实验中,各因素对黄芪甲苷转移率的影响大小顺序为:A(乙醇用量)B(提取次数)C(提取时间);每个因素3水平之间的趋势为A[sub]3[/sub]A[sub]1[/sub]A[sub]2[/sub],B[sub]1[/sub]B[sub]3[/sub]B[sub]2[/sub],C[sub]3[/sub]C[sub]2[/sub]C[sub]1[/sub],直观分析得最佳提取工艺为A[sub]3[/sub]B[sub]1[/sub]C[sub]3[/sub],即加醇10倍量,提取1次,每次3h。表5-5的方差分析结果表明: A因素的影响具有统计学差异(PB(提取次数)C(提取时间);每个因素3水平之间的趋势为A[sub]3[/sub]A[sub]1[/sub]A[sub]2[/sub],B[sub]1[/sub]B[sub]3[/sub]B[sub]2[/sub],C[sub]3[/sub]C[sub]2[/sub]C[sub]1[/sub],直观分析得最佳提取工艺为A[sub]3[/sub]B[sub]1[/sub]C[sub]3[/sub],即加醇10倍量,提取1次,每次3h。表5-7的方差分析结果表明: A因素的影响具有统计学差异(P0.05),即乙醇用量对黄芪甲苷转移率具有显著影响。[b]4 讨论[/b]本章实验利用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]技术,测定了黄芪醇提物中黄芪甲苷的含量,并系统地验证所建立的方法的可行性,经过试验条件的摸索,黄芪甲苷的色谱条件为35 %乙腈洗脱,所建立的方法能够较好的将黄芪甲苷与其他成分分开,可用于黄芪皂苷中黄芪甲苷含量测定,黄芪甲苷稳定性试验结果RSD值高于2 %,可能是由于黄芪皂苷Ⅰ或黄芪皂苷Ⅱ在酸性水解的条件下易转化成黄芪皂苷Ⅳ,即黄芪甲苷,使黄芪水提物中黄芪甲苷在48h内的稳定性不好。根据三个因素水平趋势可知,随着乙醇的用量增加,黄芪甲苷的提取效率越来越高,实验设置中每次10倍量是最大乙醇用量,这是从大工业生产和节能降耗等方面考虑的结果。根据煎煮次数水平趋势,提取1次的黄芪甲苷转移率最大,这有可能是因为黄芪皂苷Ⅰ或黄芪皂苷Ⅱ在酸性水解的条件下易转化成黄芪皂苷Ⅳ,即黄芪甲苷,而黄芪皂苷Ⅰ或黄芪皂苷Ⅱ在第一次就较完全的被提取出来,随着时间增加,转换成黄芪皂苷Ⅳ,即黄芪甲苷,第二次时黄芪皂苷Ⅰ或黄芪皂苷Ⅱ的结构可能被破坏,影响其转化成黄芪甲苷。第三次时可能黄芪甲苷被提取的更彻底,转移率又开始小幅增大。在3h内,当提取时间增加,黄芪甲苷会逐渐增大,原因可能是黄芪甲苷的提取更加彻底,黄芪皂苷Ⅰ或黄芪皂苷Ⅱ转化成黄芪甲苷最多。实验设置中每次3h是最大提取时间,这也是从综合成本与效率的角度考虑的结果。因此,综合考虑,将加醇10倍量,提取1次,共3h作为最佳醇提实验工艺。由黄芪甲苷转移率结合出膏率的到的综合评分的结果可以看出,不同提取工艺对黄芪醇提物中黄芪甲苷的含量和出膏率的影响不同,其中7、8、9组评分较高,三个组的黄芪甲苷转移率相较于其他组也是最高,但第8组出膏率却相对较低,另外出膏率高低的顺序也不与黄芪醇提物中黄芪甲苷的转移率高低的顺序项一致,这说明出膏率与黄芪醇提物中黄芪甲苷的转移率并无明显的对应关系。[align=center]参考文献[/align] 朱燕辉, 严奉祥. 黄芪甲苷及其生物学活性.现代生物医学进展,2008, 8 ( 4 ) : 781-783.
使用蒸发光检测器做黄芪甲苷含量不出峰怎么办?使用的液相是伍丰手动的
[color=#06948c][size=18px][b]伏天为何易气血不足[/b][/size][/color][b]1.高温消耗:[/b]高温环境下,人体为了散热会大量出汗,汗液排出过多不仅带走了水分,也带走了体内的电解质和一部分营养物质,从而加剧了气血的消耗。[b]2.饮食不节:[/b]夏季人们往往偏好冷饮、生冷食物,这些食物容易损伤脾胃,影响消化吸收功能,进而导致营养吸收不足,气血生成减少。[b]3.作息不规律[/b]:伏天炎热,人们容易晚睡早起,睡眠质量下降,作息不规律进一步影响了气血的恢复和生成。[b]4.过度劳累:[/b]夏季人体代谢加快,加上工作或生活压力大,容易导致身体过度劳累,进一步消耗气血。[b]当归黄芪蛋有什么功效?[/b]当归黄芪蛋,作为中医里一道著名的滋补药膳,融合了药与食的精髓,既具有药物的治疗作用,又保留了食物的温和与营养。[back=url(&]这道药膳的配方简单却精妙,主要包括[/back][b][back=url(&]当归、黄芪、红枣、红糖和鸡蛋[/back][/b][back=url(&]。[/back]当归,被誉为“血中圣药”,具有补血活血、调经止痛、润肠通便等多种功效,对于血虚萎黄、月经不调等症状有显著疗效。黄芪,则被誉为“补气之长”,擅长补气升阳、固表止汗、利水消肿,是治疗气虚乏力的良药。两者结合,既能补血又能补气,相得益彰,共同作用于人体,达到气血双补的效果。[b]1.补气养血:[/b]当归和黄芪的组合,既能补血又能补气,对于气血不足的人群尤为适宜。当归补血活血,黄芪补气升阳,两者协同作用,能够显著改善[color=var(--weui-LINK)]气血两虚的症状[i][/i][/color]。[b]2.活血调经:[/b]当归具有活血调经的功效,对于月经不调、经闭痛经的女性尤为有益。在月经前两天食用当归黄芪蛋,有助于缓解经期不适症状,促进月经恢复正常。[b]3.健脾益胃:[/b]红枣和红糖的加入,不仅增加了药膳的口感,还起到了健脾益胃的作用。红枣能益气补血,入脾胃经,有助于提升脾胃的运化功能;红糖则能温中散寒,暖胃止痛。[b]4.增强免疫力:[/b]长期食用当归黄芪蛋,还能增强人体的免疫力,提高身体抵抗疾病的能力。当归中的多糖成分和黄芪中的皂苷成分都具有增强免疫功能的作用。[color=#06948c][size=18px][b]当归黄芪蛋怎么做?[/b][/size][/color][b]原料:[/b]当归6克,黄芪6克(传统比例为5:1,但药膳中可适当调整),红枣5颗,红糖适量,鸡蛋1个。[b]做法:[/b]鸡蛋清水煮5~10分钟,捞出过凉水,剥去蛋壳,用竹签在蛋壳上戳几个小孔,以便药性渗透。红枣切片备用。将处理好的鸡蛋、红枣、当归、黄芪一同放入砂锅中,加水适量,大火煮开后转小火慢炖。炖煮约15分钟后,加入红糖调味,继续煮至红糖完全融化即可。食用建议:每日食用1~2个当归黄芪蛋,连续食用一个月。可根据个人体质和需求适当调整食用量。[size=18px][b][color=#06948c][/color][/b][/size][color=#06948c][size=18px][b]食用当归黄芪蛋时需注意以下3点[/b][/size][/color][b]1.适量食用:[/b]药膳虽好,但也不宜过量食用。应根据个人体质和需求适量调整食用量,避免补益过度。[b]2.避免与药物同服:[/b]当归、黄芪等中药材不宜与降血压、降血脂、扩张血管类药物同服,以免发生[color=var(--weui-LINK)]药物相互作用[i][/i][/color]。在食用前最好咨询医生或药师的[back=url(&]建议[/back]。[b]3.禁忌人群:[/b]实证及阴虚阳盛者、大便泄泻湿盛中满者忌服当归黄芪蛋。此外,孕妇在食用前也应咨询医生意见。
黄芪中重金属的来源有内源和外源两个方面。内源如黄芪的生长环境条件(大气、土壤、水、化肥和农药的施用等)和黄芪对重金属的吸收富集能力;外源如黄芪后期仓储污染和加工污染。内源中药材黄芪在种植期间会富集土壤、环境中的重金属。重金属作为地壳的构成物质,在不同地域土壤中有不同种类和含量。研究表明,不同地域的黄芪中重金属的含量存在较大差异,并且黄芪中的重金属含量与其在土壤中含量呈现较强的正相关。因此,种植土壤中的重金属类别和含量对黄芪中重金属有直接的关系。随着工业的发展,工业“三废”(废水、废气、废渣)对中药材有着直接和间接的污染。含有重金属元素的工业废水、废渣通过灌溉农田,使重金属元素沉积和富集在土壤中,间接地加重了药材的污染。工业的废气中含有多种有害物质,如钢铁厂的烟尘中含有铅、镉、汞、砷等重金属,废气排放后沉降到植物叶面,被植物茎叶吸收从而造成污染。为防治药材病虫害喷晒的农药中含有砷、汞、铜、铅等重金属元素,这些重金属通过农药喷洒到药材植物叶面,经过药物代谢运转到植物内部,导致药材污染。药用植物栽培过程中往往需要施用化肥,但是化肥生产过程中可能混入重金属元素。施肥后重金属在土壤中积累,通过黄芪根茎吸收从而造成重金属污染。此外,与黄芪的本身对重金属的吸收和富集能力有关,影响因素包括黄芪的种类、栽培方式、生长周期、重金属的种类和重金属的作用部位等。外源中药材仓储过程中,为防治霉变、虫害和鼠害,通常使用硫磺熏蒸黄芪,也会引入As、Pb等有毒重金属。在黄芪加工炮制过程(清洗、打粉或切片、加工、包装等工序生产环节)中由于器具含有重金属元素可能会造成重金属二次污染。
[align=center][b]UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS法测定黄芪水提物中的黄芪甲苷含量[/b][/align][b] 传统中药的煎煮,大多是用水作为溶剂,因此研究药材的水提物中有效成分的含量对药材的工业生产和实际应用具有不可忽视的指导意义。据文献报道[sup][/sup],黄芪水提物中主要为糖类和皂苷类成分,而水提物药渣中则是提取后剩余的淀粉、纤维素、木质素等原药材的基体成分和一些不易溶于水的酯类、酮类和芳香类成分。黄芪甲苷作为黄芪皂苷中一类重要的物质,已被药典收录为黄芪含量测定的指标成分。为了保证临床应用制剂的质量和进一步开发利用中药黄芪,研究黄芪水提物中黄芪甲苷的含量显得格外重要。在预实验中,笔者发现药典中测定黄芪中黄芪甲苷含量的方法并不完全适用于黄芪水提物中黄芪甲苷含量的测定,预处理时出现乳化现象导致萃取不完全,另外利用药典中规定的蒸发光检测器液相色谱仪测定无法得到理想的线性方程。因此,笔者结合黄芪水提物的性质和仪器灵敏性等特点,利用UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS法考察黄芪水提物中的黄芪甲苷含量测定的方法学和并利用该方法测定黄芪水提物中黄芪甲苷的含量。[b]1 材料和仪器1.1 样品 [/b] 收集9组黄芪水提取物样品,黄芪饮片为济南济成堂中药饮片有限公司提供(批号18033101)。[b]1.2 试剂 [/b]黄芪甲苷对照品(成都瑞芬思生物科技有限公司批号H-013-170117),乙腈为色谱纯(天津市科密欧化学试剂有限公司);超纯水。[b]1.3 仪器 [/b]Waters XevoTQ-S三重四级杆质谱仪(美国Waters公司)。ACQUITY UPLC H-CLass超高效液相色谱仪(美国Waters公司);超声波清洗机KS-300E(宁波科生仪器厂);电子天平MS205DU(梅特勒/瑞士)。[b]2 方法学考察2.1 色谱与质谱条件[/b]色谱条件:色谱柱为ACQUITY UPLC BEH C18柱(2.1*50 mm,1.7 mm)。流动相为乙腈-水(A∶B)系统。梯度洗脱,A相:0→1 min A保持30%;1→2 min A为30→60%;2→3 min A为60→70%;3→4 min A保持70%;4→4.5 min A为70→30%;A相:4.5→5.5 min A保持30%。流速 0. 2 mL/min,柱温为40 ℃,进样体积 1. 0 μL。质谱条件:电喷雾正离子检测模式,毛细管电压;3.0 kV;脱溶剂气流:N2,流速800 L h[sup]-1[/sup],脱溶剂温度400 ℃;锥孔电压:40 V,锥孔气流:N2,流速150 Lh[sup]-1[/sup];离子源温度: 400 ℃;雾化气压力为7.0 bar碰撞气体: 氩气。采用MRM 定量模式,质量扫描范围为100~1 000 amu。该条件下,获得黄芪甲苷的分子离子峰 m /z 785. 42,子离子峰m /z 143.08。黄芪甲苷提取总离子流图和一级质谱图分别见图3-1和图3-2。[/b][align=center][img=,690,322]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131701299261_9069_3237657_3.png!w690x322.jpg[/img][/align][align=center]图3-1 黄芪甲苷的总离子流图[/align][align=center][img=,690,331]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131701493040_8991_3237657_3.png!w690x331.jpg[/img][/align][align=center]图3-2 黄芪甲苷的一级质谱图[/align][b]2.2 供试品溶液的制备[/b]精密称定1/200重量的黄芪水提物样品(折合黄芪药材0.5g)置于锥形瓶中,精密加入4%氨水溶液100 mL,称定重量,超声30 min,取出放至室温,用4%氨水溶液补足减失的重量,摇匀,过滤,精密吸取续滤液10 mL过Dikma ProElut C18-U-SPE柱(先以甲醇20 mL活化,再以水20 mL平衡),上样后用10 mL水淋洗,弃去,再用适量甲醇洗脱,收集洗脱液,定容至10 mL容量瓶中,摇匀,用0.22 μm的微孔滤膜过滤,即得。[b]2.3 对照品储备溶液的制备[/b]精密称取黄芪甲苷标品1.01mg至10 mL容量瓶中,用甲醇溶解后定容,吸取1 mL至100 mL容量瓶中,用甲醇定容,制成浓度为1.01 μg/mL的对照品储备溶液。[b]3 结果3.1 线性关系考察[/b]精密吸取 2. 3 项下对照品储备溶液 1,3,5 mL,用甲醇稀释并定容到 10mL 容量瓶中,制备0.1,0.3,0.5 mgmL[sup]-1[/sup]质量浓度对照品溶液。另吸取0.1,0.3 mg/mL质量浓度对照品溶液5 mL至10 mL容量瓶,用甲醇定容,得到0.05,0.15 mg/mL质量浓度对照品溶液。在拟定分析条件下,准确吸取 10. 0 μL 进样分析。黄芪甲苷离子选择 m/z 785. 42 为母离子,143.08 为子离子,准确吸取1 0 μL 进样分析。以质量浓度为横坐标,以提取离子流图峰面积为纵坐标进行线性回归,如图3,得回归方程为:Y=46.135X + 1938.8(r[sup]2[/sup]= 0. 9984),提示黄芪甲苷在0. 05~0.5 mg/m L 范围内线性关系良好。黄芪甲苷对照品标准曲线如图3-3所示。[align=center][img=,690,423]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131702057366_9110_3237657_3.png!w690x423.jpg[/img][/align][align=center]图3-3 黄芪甲苷标准曲线[/align][b]3.2 精密度实验[/b]在拟定分析条件下,精密吸取供试品溶液1.0 μL,连续进样 6 次,记录提取离子流图峰面积,测定黄芪甲苷量,计算得相对标准偏差RSD为1.1% ,提示该方法具有较好的精密度。[b]3.3 重复性实验[/b]取同一黄芪样品 6份,按2. 2 项下方法制备供试品溶液,在拟定分析条件下,准确吸取 1. 0 μL 进样分析,测定黄芪甲苷量,计算得 RSD为2.0%,提示该方法重复性良好。[b]3.4 稳定性实验[/b]取黄芪药材供试品溶液,分别在0 h、3 h、6 h、9 h、24 h、48 h后,在拟定分析条件下,准确吸取 1. 0 μL 进样分析,测定黄芪甲苷量,计算得 RSD 为 4.7% ,提示黄芪供试品溶液稳定性较差。[b]3.5 加样回收率实验[/b]精密称取 6 份黄芪甲苷量已知的黄芪水提物样品,每份折合黄芪药材 0. 5 g,分别准确加入浓度为 0. 0 342 mg /mL 黄芪甲苷溶液1 ml,1 ml,2 ml,2 ml,3 ml,3 ml,按 “2. 2 ”项下方法制备供试品溶液,准确吸取 1. 0 μL 进样分析,测定黄芪甲苷量,计算回收率,结果见表3-1。由表3-1可见,方法平均回收率为 102.35% ,表明该方法具有较好的回收率。[align=center] [/align][align=center]表3-1 黄芪甲苷加样回收率测定结果[/align] [table][tr][td] [align=center]样号[/align] [/td][td] [align=center]样品中的量/mg[/align] [/td][td] [align=center]加入量/mg[/align] [/td][td] [align=center]测得量/mg[/align] [/td][td] [align=center]回收率/%[/align] [/td][td] [align=center]平均值/%[/align] [/td][td] [align=center]RSD/%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]0.069[/align] [/td][td] [align=center]0.034[/align] [/td][td] [align=center]0.1[/align] [/td][td] [align=center]101.68[/align] [/td][td=1,6] [align=center]102.35[/align] [/td][td=1,6] [align=center]2.8[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]0.069[/align] [/td][td] [align=center]0.034[/align] [/td][td] [align=center]0.11[/align] [/td][td] [align=center]104.44[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]0.069[/align] [/td][td] [align=center]0.068[/align] [/td][td] [align=center]0.14[/align] [/td][td] [align=center]104.17[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]0.069[/align] [/td][td] [align=center]0.068[/align] [/td][td] [align=center]0.13[/align] [/td][td] [align=center]96.42[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]0.069[/align] [/td][td] [align=center]0.10 [/align] [/td][td] [align=center]0.17[/align] [/td][td] [align=center]102.78[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]0.069[/align] [/td][td] [align=center]0.10 [/align] [/td][td] [align=center]0.18[/align] [/td][td] [align=center]104.63[/align] [/td][/tr][/table][align=center] [/align][b]3.6 黄芪甲苷的含量测定结果[/b]取9组黄芪水提物按照“2.2”项下操作,制备供试品溶液,准确吸取 1. 0 μL 进样分析,测定黄芪甲苷的含量。黄芪甲苷对照品和黄芪水提物样品的MRM 离子流图见图3-4、图3-5。供试品黄芪甲苷含量测定结果见表3-2。[align=center][img=,690,348]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131702286759_7988_3237657_3.png!w690x348.jpg[/img][/align][align=center]图3-4 黄芪甲苷对照品的 MRM 离子流图[/align][align=center][img=,690,344]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131702391650_7279_3237657_3.png!w690x344.jpg[/img][/align][align=center]图3-5 黄芪水提物样品的 MRM 离子流图[/align][align=center] [/align][align=center]表3-2 9组黄芪水提物中黄芪甲苷含量测定结果[/align] [table][tr][td] [align=center]试验号[/align] [/td][td] [align=center]峰面积[/align] [/td][td] [align=center]含量(mg/g)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]5120.00 [/align] [/td][td] [align=center]0.14 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]6744.00 [/align] [/td][td] [align=center]0.21 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]10275.67 [/align] [/td][td] [align=center]0.36 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]26955.00 [/align] [/td][td] [align=center]1.08 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]10599.00 [/align] [/td][td] [align=center]0.38 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]7212.33 [/align] [/td][td] [align=center]0.23 [/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]11247.33 [/align] [/td][td] [align=center]0.40 [/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]8008.33 [/align] [/td][td] [align=center]0.26 [/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]9171.00 [/align] [/td][td] [align=center]0.31 [/align] [/td][/tr][/table][align=center] [/align][b]3.7 正交试验设计及结果[/b]水提的黄芪甲苷转移率考察正交试验与水提的出膏率考察正交试验设计相同,即以水作为提取溶剂,把影响药材提取效果的用水量(A)、提取时间(B)、提取次数(C)确定为考察因素,以上三个考查因素各分3个水平考察,见表3-3。[align=center]表3-3水提实验因素水平表[/align] [table][tr][td=1,2] [align=center]水平[/align] [/td][td=3,1] [align=center]因素[/align] [/td][/tr][tr][td] [align=center]A(用水量/倍)[/align] [/td][td] [align=center]B(提取时间/h)[/align] [/td][td] [align=center]C(提取次数/次)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]4[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]8[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]10[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][/tr][/table][b] [/b]黄芪甲苷转移率=各实验组黄芪提取物中黄芪甲苷含量/原黄芪药材中黄芪甲苷含量×100%。原药材中毛蕊异黄酮苷的含量按照药典的方法测得的结果为0.4042mg/g。跟据实验数据,得到水提实验中设定的不同工艺条件下的毛蕊异黄酮苷的转移率,其中因素D为误差项,作直观分析表和方差分析表,见表3-4,表3-5。[align=center]表3-4 黄芪甲苷转移率考察L[sub]9[/sub](3[sup]4[/sup])正交试验表[/align] [table][tr][td] [align=center]试验号[/align] [/td][td] [align=center]A[/align] [/td][td] [align=center]B[/align] [/td][td] [align=center]C[/align] [/td][td] [align=center]D[/align] [/td][td] [align=center]黄芪甲苷 转移率/%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]34.12 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]51.54 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]89.41 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]268.30 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]92.88 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]56.56 [/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]99.83 [/align] [/td][/tr][tr][td] [align=center]试验号[/align] [/td][td] [align=center]A[/align] [/td][td] [align=center]B[/align] [/td][td] [align=center]C[/align] [/td][td] [align=center]D[/align] [/td][td] [align=center]黄芪甲苷 转移率/%[/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]65.10 [/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]77.56 [/align] [/td][/tr][tr][td] [align=center]K1[/align] [/td][td] [align=center]175.07 [/align] [/td][td] [align=center]402.25 [/align] [/td][td] [align=center]155.78 [/align] [/td][td] [align=center]204.56 [/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]K2[/align] [/td][td] [align=center]417.74 [/align] [/td][td] [align=center]144.42 [/align] [/td][td] [align=center]397.40 [/align] [/td][td] [align=center]207.93 [/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]K3[/align] [/td][td] [align=center]242.49 [/align] [/td][td] [align=center]223.53 [/align] [/td][td] [align=center]282.12 [/align] [/td][td] [align=center]422.81 [/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]优水平[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]R[/align] [/td][td] [align=center]242.67 [/align] [/td][td] [align=center]257.83 [/align] [/td][td] [align=center]241.62 [/align] [/td][td] [align=center]218.25 [/align] [/td][td] [align=center] [/align] [/td][/tr][/table][align=center] [/align][align=center]表3-5 黄芪甲苷转移率考察方差分析结果[/align] [table][tr][td] [align=center]方差来源[/align] [/td][td] [align=center]离差平方和[/align] [/td][td] [align=center]自由度[/align] [/td][td] [align=center]F[/align] [/td][td] [align=center]显著性[/align] [/td][/tr][tr][td] [align=center]A[/align] [/td][td] [align=center]10460.75[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1.13[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]B[/align] [/td][td] [align=center]7698.00[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]0.75[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]C[/align] [/td][td] [align=center]9736.83[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1.02[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]D[/align] [/td][td] [align=center]10424.20[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]-[/align] [/td][/tr][/table]注:F[sub]0.1[/sub](2,2)=9,F[sub]0.05[/sub](2,2)=19,*为有显著性,-为无显著性。从正交试验结果可知,水提实验中,各因素对黄芪甲苷转移率的影响大小顺序为:A(用水量)C(提取次数)B(提取时间);每个因素3水平之间的趋势为A[sub]2[/sub]A[sub]3[/sub]A[sub]1[/sub],B[sub]1[/sub]B[sub]3[/sub]B[sub]2[/sub],C[sub]2[/sub]C[sub]3[/sub]C[sub]1[/sub],直观分析得最佳提取工艺为A[sub]2[/sub]B[sub]1[/sub]C[sub]2[/sub],即加水8倍量,提取2次,每次1h。表3-5的方差分析结果表明: A、B、C三因素对黄芪甲苷转移率的影响都无统计学差异(P0.05)。[b]4 讨论[/b]本章实验利用超高效液相串联三重四级杆质谱仪测定黄芪水提物中黄芪甲苷的含量,相比药典中测定黄芪药材中黄芪甲苷的方法,此方法预处理步骤更少,用时更短,目标峰与其他相邻峰的分离度也更大,适合于黄芪水提物中黄芪甲苷含量的测定。但美中不足的是,供试品的预处理需要过SPE柱,仪器的使用和维护费用更高,实验者在测定样品的含量前需要综合考虑。从测定结果来看,设置的三个因素中,用水量对黄芪甲苷的转移率影响最大,但仍无统计学差异(P0.05),说明用水量、提取次数、提取时间三种工艺的改变对黄芪水提物中黄芪甲苷的含量无显著性影响。第4、5、7组的黄芪甲苷转移率相比其他组的更高,尤其是第4组测得的黄芪甲苷的含量远高于用药典方法测得的药材中黄芪甲苷的含量,正交实验分析结果也说明加水8倍量,提取2次,每次1h是最佳提取工艺。这一结果与水提实验中第3、4、7组测得的出膏率较高有些差异,第4组实验的出膏率也不算低,但不是最高,而出膏率最高的第3组黄芪甲苷的转移率却不高,这说明出膏率与黄芪水提物中黄芪甲苷的转移率并无明显的对应关系。合乎标准要求的有效成分含量是保证药物疗效稳定可靠的硬性指标,实现有效成分提取的最大化是优化工艺条件的重要目标。本章关于不同提取工艺条件下黄芪甲苷转移率的考察研究,对芪龙胶囊和黄芪配方颗粒工艺的优化具有指导性意义。[align=center]参考文献[/align] 黄冬兰,徐永群,陈小康. 黄芪药材及其水提物的红外光谱分析. 光谱实验室,2012,29(5):2823-2826.

【作者】 刘近荣;【机构】 山西泰盛制药有限公司;【摘要】 目的建立以高效液相色谱法测定黄芪总皂苷氯化钠注射液中黄芪甲苷含量的方法。方法色谱柱为DiamonsilC18(5μm,4.6×250mm),流动相为乙腈-水(36:64),流速为0.8ml/min,柱温为室温。结果黄芪甲苷进样量在5μg~40μg范围内与峰面积积分值线性关系良好(r=0.9993,n=5),平均加样回收率为99.75%(RSD=0.57%)。结论本方法测定结果准确、操作简便、灵敏度高、重复性好,可用于本品的质量控制。 更多还原http://ng1.17img.cn/bbsfiles/images/2012/08/201208131255_383443_2379123_3.jpg
大茴香酸-硫酸荧光体系测定黄芪甲苷刘养清 杜鸣 徐秉玖关键词: 黄芪甲苷; 大茴香酸; 黄芪; 中药复方补阳还五汤; 荧光分光光度法中图分类号: R927.2 R284.1 文献标识码: A 文章编号: 0513-4870(2000)07-0544-03黄芪甲苷(astragaloside)是中药膜荚黄芪Astragalus membranaceus (Fisch.) Bge.和蒙古黄芪Astragalus membranaceus (Fisch.) Bge. var. mongholicus (Bge.) Hsiao的主要活性成分,有抗炎、降压、镇痛、镇静、升高血浆中cAMP水平、促进小鼠再生肝DNA的含量[1,2]以及促进免疫功能等生理活性。黄芪甲苷的测定方法主要有:紫外分光光度法[3,4]、薄层扫描法[5,6]和HPLC法[7,8]。光度法常用香草醛在浓硫酸作用下与甲苷显色反应,空白值较高,干扰严重;薄层扫描法操作繁琐,准确度相对较差。黄芪甲苷仅在200 nm处有末端吸收,对HPLC法不利。黄芪甲苷的荧光分析尚未见报道。本文首次根据在浓硫酸条件下黄芪甲苷与大茴香酸反应产物具有荧光的特性建立了荧光分光光度法测定黄芪甲苷,方法灵敏度高、选择性好、线性范围宽、检出限低、操作简便。可直接用于黄芪生药、中药复方、黄芪制剂以及含药血清等多种样品的测定,无干扰。材料与方法 仪器 日本岛津RF-540型荧光分光光度计。 试剂 黄芪甲苷对照品(中国药品生物制品检定所提供)配成1.0 mg.mL-1的甲醇溶液。2%大茴香酸的无水乙醇溶液,72%硫酸溶液,85%磷酸溶液。所用试剂均为分析纯。 样品及处理 黄芪口服液(上海福达制药有限公司生产,批号980502)。取口服液1.00 mL,加入无水乙醇2.00 mL,离心分离沉淀,上清液蒸干,用甲醇1 mL溶解,备用。补阳还五汤复方汤剂煎煮3次,合并水煎液,分别用石油醚、氯仿、正丁醇萃取4次,每次萃取剂用量为水煎液体积的一半。合并正丁醇相,总体积为800 mL。取正丁醇萃取液2 mL,蒸干,用甲醇2 mL溶解,备用。含药猪血清样品(北京医科大学药学院生药研究室提供):用补阳还五汤复方浸膏连续3 d喂猪,3 d后取血,分离猪血清,取猪血清50 mL,用正丁醇萃取4次,每次萃取剂用量为原血清体积的一半。得含药血清样品100 mL,取正丁醇萃取液4 mL,蒸干,用甲醇2 mL溶解,备用。黄芪生药样品:按文献[3]方法提取分离,甲醇溶样,备用。结果与讨论1 黄芪甲苷反应产物的激发光谱和发射光谱 取1.0 mg.mL-1黄芪甲苷对照品0.1 mL,于5 mL量瓶中,加入2%大茴香酸溶液0.6 mL、72% H2SO4溶液0.8 mL,于60℃水浴中反应20 min,迅速冷却后,用无水乙醇定容至刻度,摇匀,在荧光分光光度计测荧光光谱黄芪甲苷反应产物最大激发波长Ex=320 nm,最大发射波长Em=387 nm。2 大茴香酸用量的影响 取大茴香酸0.1,0.3,0.5,0.6,0.7,0.9 mL按照分析方法操作,选择大茴香酸最佳用量。结果表明大茴香酸用量0.6 mL较合适(图1)。3 稀释液的选择 准确移取1.0 mg.mL-1黄芪甲苷0.1 mL,按照分析方法操作,体积定容时选无水乙醇、甲醇、冰醋酸和水作稀释液,测得其荧光强度(If)分别为77.6,48.4,35.0,1.3。可见无水乙醇对荧光强度影响最小。本文采用无水乙醇作为稀释液。 Fig 1 Effect of amount of anisic acid4 酸的种类和用量的影响 选72% H2SO4, 85% H3PO4及浓HClO4进行实验,结果发现选用72% H2SO4时反应产物的荧光强度最大。对72%硫酸的用量进行选择,结果表明72% H2SO4取0.8 mL为最佳(图2)。 Fig 2 Effect of amount of sulphuric acid5 反应温度的影响 准确移取1.0 mg.mL-1黄芪甲苷对照品0.1 mL,按分析方法内容操作,分别在40,50,60,70,80,90℃和沸水浴中反应20 min,同时做空白。考察荧光强度随温度的变化,结果表明:60℃时反应空白小,荧光强度较高。故实验选择60℃为反应温度较适宜。6 加热时间的影响 将温度控制在60℃,改变加热时间,考察加热时间对反应的影响。结果表明加热时间选20 min为宜。7 反应产物的稳定性 准确移取1.0 mg.mL-1黄芪甲苷对照品0.1 mL,按照分析方法操作,测定荧光强度值,每间隔5 min测定1次,对产物稳定性进行考察。结果表明反应产物在90 min内均稳定。8 工作曲线及检出限 分别准确移取1.0 mg.mL-1黄芪甲苷对照品0.010,0.025,0.050,0.100,0.150和0.200 mL,在最佳实验条件下,测定工作曲线,得回归方程为:Y=-0.4201+1.575X,γ=0.9993。黄芪甲苷浓度在2.0~40 μg.mL-1与荧光强度呈良好的线性关系。检出限为0.02 μg.mL-1。9 干扰考察 为解决基体太浓或基体不一致所造成的影响,在适当稀释溶液后,采用标准加入法测定样品。为考察此反应选择性,利用薄层分离黄芪甲苷[6]后测定样品中其他物质的荧光强度,证明杂质荧光强度与样品总荧光强度的比1.2%。10 样品的测定与回收率实验 取被测样品6份各0.1 mL,依次加入1.0 mg.mL-1黄芪甲苷对照品0.0,0.01,0.02,0.03,0.04和0.05 mL,按照分析方法操作,分别测定了黄芪、复方补阳还五汤、黄芪口服液及猪血清样品中黄芪甲苷的含量,测定结果及回收率实验见表1。SampleContent/%Recovery/%RSD/%HQOL0.210±0.00298.5~101.91.8BYHWT0.280±0.02098.8~102.12.1AMB0.420±0.00498.6~102.02.0PS0.063±0.00198.8~102.41.9黄芪是补阳还五汤的君药,黄芪甲苷定量分析是黄芪中药制剂质量控制的重要指标,本方法灵敏度高,选择性好,操作简便且无干扰,可作为黄芪甲苷的质控方法。基金项目: 九五攀登计划项目杜鸣(北京医科大学药学院分析化学与药物分析研究室,北京 100083 )徐秉玖(北京医科大学药学院分析化学与药物分析研究室,北京 100083 )刘养清(山西师范大学化学系,山西 临汾 041004)收稿日期: 1999-08-03
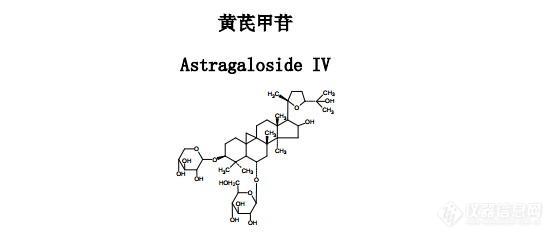
液相质谱方法优化了很长时间,样品处理办法由开始的沉淀蛋白换成了液液萃取,还是在血浆中没有检测到。该化合物分子量为785.6,我的MRM是+,即807.6-627.5我看到文献有做成功的,可含量也很低Cmax=16ng,请问是黄芪甲苷在大鼠胃内被酸化了吗?还是有别的原因?灌胃液中含黄芪甲苷大于1mg/mL。[img=,555,239]https://ng1.17img.cn/bbsfiles/images/2019/03/201903211951256531_6859_3255306_3.jpg!w555x239.jpg[/img]
今天同时做的甘草和黄芪有机氯前处理,按照药典一部来的,加了盐之后,黄芪中丙酮析出,且有机相都位于下层。可是甘草丙酮析出不好,明显上层溶液多于下层溶液,并且用无水硫酸钠做了检查,发现上层的才是有机相。现在黄芪和甘草有机相的位置是相反的,一个在上,一个在下,不明白为何会出现这种情况,希望哪位大虾能帮忙解决下,谢谢了。
现在黄芪农残做9种的还是22种?有版友知道的吗?
活血通络颗粒是由黄芪、丹参、当归、赤芍、地龙、川芎等多味中药组成的复方制剂,具有益气活血、抗凝、降脂等功效。主要用于中风后遗症、脑血栓、脑动脉硬化及高血压、高血脂、心绞痛等心脑血管疾病。黄芪为方中君药,黄芪甲苷为其指标成分,中药复方中黄芪甲苷含量测定已有文献报道。本研究参考文献方法,建立测定活血通络颗粒中黄芪甲苷含量的方法,为控制本品质量打下基础。 1 仪器与试药 薄层扫描仪(日本岛津CS一9000),硅胶G薄层板(青岛海洋化工厂,10cm×10cm),定样毛细管(美国Drumond公司),电子分析天平(梅特勒一托利多仪器上海有限公司),黄芪、丹参、当归等原料药(医药公司),黄芪甲苷对照品(中国药品生物制品检定所),活血通络颗粒剂(本院自制,批号20020326,20020410,20020419)。所用试剂均为分析纯。
[center]研究发现中药黄芪对艾滋病病毒有抑制作用[/center]美国科学家通过长期研究发现,中药黄芪中含有一种可有效抑制艾滋病病毒细胞分裂的化学物质——TAT2,对治疗艾滋病有非凡的功效。 美国加利福尼亚大学洛杉矶分校艾滋病研究协会近日公布的最新研究成果显示,中药黄芪中包含一种特殊的化学物质——TAT2,研究人员发现TAT2是对付艾滋病主要元凶——“淋巴细胞杀手”的有效手段。黄芪有望取代传统的艾滋病治疗方式——抗逆转录病毒疗法,成为治疗艾滋病的主要方式。 抗逆转录病毒药物可以阻止艾滋病病毒与宿主细胞结合。最近,德国一名医生在南非和其他一些国家报纸上发表文章,提出抗逆转录治疗具有毒副作用。 此外美国研究人员还指出,黄芪还可以治疗其他免疫系统疾病,尤其对病毒性感染和慢性病有奇效。
各位高手,请闾问除了药典05年版一部中的黄芪药材的含量测定方法外,用高效液相色谱法还有什么方法测黄芪药材中的黄芪甲苷含量?[em09]
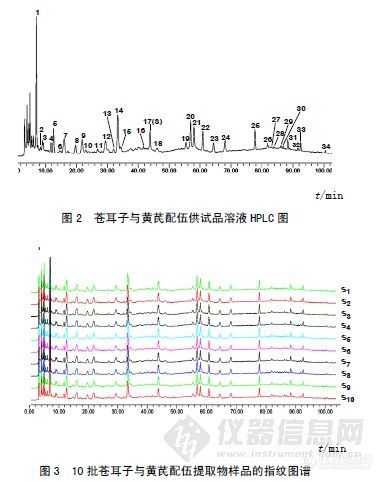
作者:曹敏; 武斌; 刘树民;(黑龙江中医药大学中医药研究院;)摘要:目的建立苍耳子配伍黄芪的高效液相色谱(HPLC)指纹图谱分析方法,研究配伍对各单味药主要特征峰的影响。方法采用HPLC分析苍耳子、黄芪单煎及苍耳子配伍黄芪合煎样品,选用Diamonsil C18色谱柱(5μm,250 mm×4.6 mm),以甲醇-0.2%甲酸水为流动相进行线性梯度洗脱,流量为0.8 mL/min,检测波长为260 nm。结果建立了苍耳子配伍黄芪的HPLC指纹图谱,基本为两单味药特征峰的加和,无明显新特征峰的增加,但配伍合煎对某些成分的溶出有明显的相互抑制作用。结论本方法简便、快捷,为临床类方的配伍应用以及制定复方质量标准提供了参考。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208061420_381877_1606903_3.jpg

10,抽取5个版友);中奖名单:莫名其妙(注册ID:moyueqiu)捌道巴拉巴巴巴(注册ID:v3082413)夏天的雪(注册ID:bingwang228)http://ng1.17img.cn/bbsfiles/images/2017/02/201702171503_01_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2017/02/201702171503_02_1610895_3.jpg【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================HPLC-ELSD法测定祝艾康胶囊中黄芪甲苷的含量方法:HPLC基质:动物提取物应用编号:102891化合物:黄芪甲苷固定相:Diamonsil C18(2)色谱柱/前处理小柱:Diamonsil 5μm C18(2), 250 x 4.6mm色谱条件:色谱柱:Diamonsil C18 250 mm× 4.6 mm, 5μm(Cat#:99603) 流动相: 乙腈-水(33∶67) 流速: 1.0 mL/min 柱温: 35℃ 进样量: 20 μL 检测器: ELSDS文章出处:中国实验方剂学杂志 2010, 16(4):60-62关键字:祝艾康胶囊; 黄芪甲苷; 高效液相-蒸发光散射检测法, Diamonsil C18, 钻石二代,含量测定谱图:摘要:目的:建立中药复方祝艾康胶囊中黄芪甲苷的含量测定方法。方法:采用Diamonsil C18色谱柱(4.6 mm×250mm,5μm),乙腈-水(33∶67)为流动相,流速1.0 mL.min-1,柱温35℃,漂移管温度105℃,空气流速2.7 L.min-1。结果:黄芪甲苷在1.515~7.575μg具良好的线性关系(r=0.999 96),平均回收率98.83,RSD 1.8%。结论:该法准确、可靠、重复性好,可用于控制祝艾康胶囊的质量。http://www.dikma.com.cn/Public/Uploads/images/106-7.JPG
有没有哪位大神用紫外或者示差测过黄芪甲苷啊,我们这边没有蒸发光散射,只能用紫外和示差,但是跟着文献上搜出来的资料完全没有走出来的迹象啊。仪器条件如下:1:紫外:流动相30%乙腈水,色谱柱150mm的C18柱子走,检测波长203。2:示差 流动相:67%甲醇水,色谱柱:150mm C18。以上,标都是用甲醇配的,最大浓度是500ppm。
[align=center][font=宋体][color=black]黄芪配方颗粒的研究现状[/color][/font][/align][align=left][font=宋体][color=black]传统中药饮片在煎煮时大多以水为溶剂,在应用上存在一定的缺陷,例如用量不好掌控、携带不便、煎煮也略显繁琐等,这些都与现代生活的快节奏难以相适应。中药配方颗粒剂又名中药颗粒饮片,它还有免煎饮片、单味中药浓缩颗粒等美称。中药配方颗粒剂是依据传统中医药理论和现代临床应用的需要,利用现代先进的生产工艺设备和技术,对中药材饮片进行单味药材的批量生产而成的一种新的颗粒剂型。中药配方颗粒剂作为替代传统中药饮片的一种新剂型,它具有服用方便、携带快捷、食用安全、质量卫生、方法科学等特点[/color][/font][sup][color=black][13][/color][/sup][font=宋体][color=black]。中药配方颗粒剂为中药国际化发展提供了机会,对中药配方颗粒进行相关研究也日益广泛和深入,必将推动中药事业的良好发展[/color][/font][sup][color=black][1][/color][/sup][font=宋体][color=black]。[/color][/font][/align][font=宋体][color=black]传统中药汤剂在煎煮时存在耗费时间、煎煮后汤剂口感苦、携带困难等问题,这些问题使中药传统剂型在现代社会的传播中受到限制。而中药配方颗粒剂却获得越来越多人的认可。将中药配方颗粒以调查问卷的形式发放到社会中,结果表明大多数调查对象赞同研究中药配方颗粒[/color][/font][sup][color=black][2][/color][/sup][font=宋体][color=black]。[/color][/font][font=宋体][color=black]中药配方颗粒剂在我国中药的发展中仍存在的弊端:药物的基原不同,一味中药由多种产地混合组成,如中药黄连就有三种来源,分别为为毛食黄连、三角叶黄连或云连,其有效成分及含量不同,应当在颗粒剂说明书中备注多基原的中药并标明药材的基原。药材的炮制品种多样,中药有多种炮制方法,包括蜜炙、酒炙等,不同的炮制方法造成药材的有效成分及含量不同。应当在颗粒剂说明书中备注药材炮制方法。颗粒剂的说明书至关重要,若未能详细的列出各药材的基原和炮制方法,将不利于中药配方颗粒在市场上的应用和推广[/color][/font][sup][color=black][3][/color][/sup][font=宋体][color=black]。当前中药配方颗粒已有大量科研成果,为保证其向市场稳定转化,应制定法律法规提高其质量标准[/color][/font][sup][color=black][4][/color][/sup][font=宋体][color=black]。[/color][/font][font=宋体][color=black]配方颗粒是将中药提取物作为一种新型的饮片进行配伍组合后制备而成的中药制剂。黄芪在配方颗粒中的工艺多为醇提后回收药渣再进行水提,将水提液醇沉得到多糖类化合物后,澄清溶液于醇提液混合,分别得到皂苷类部分和多糖类部分。中药中[/color][/font][color=black]“[/color][font=宋体][color=black]辨证论治[/color][/font][color=black]”[/color][font=宋体][color=black]是根据机体在病变时表现的性质、部位,以及邪正之间的关系,概括病症的[/color][/font][color=black]“[/color][font=宋体][color=black]证[/color][/font][color=black]”[/color][font=宋体][color=black]。根据辩证的结果,对不同情况决定治疗的手段、方法。中医中药讲究辨证施治,对于不同体质的患者,如阴阳不同、体质不同等,药物服用量都有严格的控制。对药材进行不同的炮制方法,其相同的药材可表现出不同的药理作用,炮制方法主要包括蒸制、熬制、醋炒制、盐水制、蜜水制、黄连制、红花制等,不同的炮制方法,功效与临床应用都有所区别。如现代配方颗粒对药材的炮制方法做了研究,对不同症状的患者选用不同炮制方法得到的药材进行治疗,例如生地黄具有清热凉血,养阴,生津等功效,而熟地黄具有滋阴补血,益精填髓的功效,生地炭则以凉血止血为主。而现代配方颗粒尚不能达到中医辨证论治的思维,无法按照中医阴阳学说辩证施治,区别对待阴虚、阳盛的体质,从而配伍同种药材不同处理方法得到的配方颗粒。因此配方颗粒具有一定的局限性,同时也表明其仍有较大的发展空间。黄芪配方颗粒作为常用药,其有效成分含量没有研究证明与其他药方中黄芪皂苷含量进行对比,应借鉴其他药方的提取工艺进一步优化黄芪皂苷的提取工艺,传统提取方法应结合现代生产工艺技术,摸索最佳方法,因此找到最有效的提取工艺亟待解决。[/color][/font][font=宋体]参考文献[/font][color=black][1] [/color][font=宋体][color=black]李建会[/color][/font][color=black],[/color][font=宋体][color=black]张霄潇[/color][/font][color=black], [/color][font=宋体][color=black]荆志伟[/color][/font][color=black]. [/color][font=宋体][color=black]中药配方颗粒合理放开竞争发展的思考[/color][/font][color=black][J]. [/color][font=宋体][color=black]中医药管理杂志[/color][/font][color=black], 2016, 24 ( 13):7-10.[/color][color=black][2] [/color][font=宋体][color=black]汪杰[/color][/font][color=black]. [/color][font=宋体][color=black]黄芪配方颗粒提取与纯化工艺研究[/color][/font][color=black][D]. [/color][font=宋体][color=black]广州中医药大学[/color][/font][color=black], 2009.[/color][color=black][3] [/color][font=宋体][color=black]孙源源[/color][/font][color=black],[/color][font=宋体][color=black]施萍[/color][/font][color=black]. [/color][font=宋体][color=black]借助中药配方颗粒推进中药国际化的对策研究[/color][/font][color=black][J]. [/color][font=宋体][color=black]中草药[/color][/font][color=black], 2013, 44 ( 08 ):929-934.[/color][color=black][4] [/color][font=宋体][color=black]张红梅[/color][/font][color=black],[/color][font=宋体][color=black]宋景政[/color][/font][color=black], [/color][font=宋体][color=black]谭红胜[/color][/font][color=black], [/color][font=宋体][color=black]等[/color][/font][color=black]. [/color][font=宋体][color=black]从汤剂到颗粒剂[/color][/font][color=black]:[/color][font=宋体][color=black]中药配方颗粒[/color][/font][color=black]20[/color][font=宋体][color=black]年回顾与展望[/color][/font][color=black][J]. [/color][font=宋体][color=black]世界科学技术[/color][/font][color=black] ( [/color][font=宋体][color=black]中医药现代化[/color][/font][color=black]) , 2012, 14 ( 04 ):1740-1753.[/color]
用奥泰的ELSD2000做黄芪甲苷一直没有峰,流动相乙腈-水32:68(药典),标准品一直没峰?加大有机相到40:60还没有,用乙腈冲出来的峰不知道是不是黄芪甲苷请各位高人指点!!!不胜感谢!!!
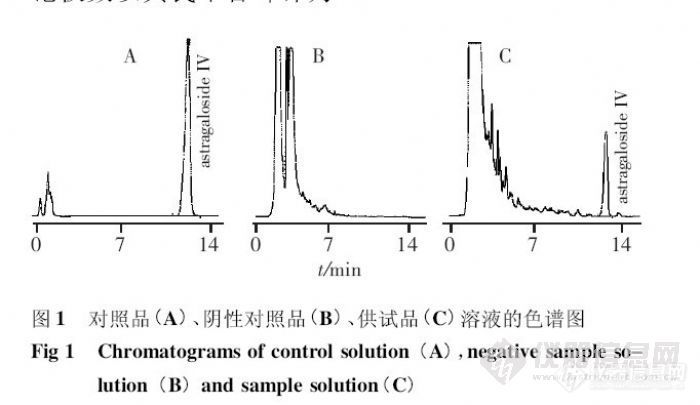
HPLC-ELSD测定芪桂消癓颗粒中的黄芪甲苷 张梦云,冯俭* ,张煜华,李煌,朱晗 (成都中医药大学附属医院,四川成都610072)摘要: 目的建立测定芪桂消癥颗粒中黄芪甲苷含量的方法。方法采用HPLC - ELSD 法,色谱柱为Diamonsil C18柱(150mm × 4. 6 mm,5. 0 μm),流动相为乙腈- 水(32∶68),流速为1. 0 mL·min - 1 ,柱温为35℃;检测器漂移管温度为80℃,氮气压力为45 psi。结果黄芪甲苷7. 72 ~ 23. 16 μg 与峰面积的线性关系良好( r = 0. 9993),平均回收率为97. 49%,RSD = 2. 08%(n = 6)。结论所建方法简便、准确、重复性好,可有效地控制芪桂消癥颗粒的质量。关键词: 高效液相色谱- 蒸发光散射检测器法;芪桂消癥颗粒;黄芪甲苷http://ng1.17img.cn/bbsfiles/images/2012/07/201207242113_379515_2432394_3.jpg