
药物名称:黄岑。货号:99603.今日抽奖结果:[align=center][img=,690,289]https://ng1.17img.cn/bbsfiles/images/2019/09/201909271612560756_6797_708_3.png!w690x289.jpg[/img][/align][align=center][img=,690,318]https://ng1.17img.cn/bbsfiles/images/2019/09/201909271613052211_8085_708_3.png!w690x318.jpg[/img][/align][align=center][img=,690,322]https://ng1.17img.cn/bbsfiles/images/2019/09/201909271613118046_1603_708_3.png!w690x322.jpg[/img][/align][align=center]=================================[color=#ff0000]活动规格[/color]====================================[/align][align=left][color=#ff0000]【活动时间】:每个工作日10:00-15:00【活动内容】:根据迪马产品资料:《药物检测应用文集》,每日会出一个化药或中药名称标题,版友根据标题找出相应迪马产品,将从回答正确者中利用抽奖软件抽取以下奖项。[/color][/align][align=left][color=#ff0000]【活动奖励】:一等奖:3个钻石(2人),二等奖:2个钻石币(3人),三等奖:1个钻石币(5个人)。[/color][/align][align=left][color=#ff0000]【注意事项】:一定要在迪马产品资料《药物检测应用文集》中找出相应迪马产品。[/color][/align]
不知道有没有老师做过GB/T 5009.149-2003 食品中栀子黄的测定,试剂部分提到需要栀子甙做标样,但是在结果计算里面写的是栀子黄色素的含量,这样的话感觉栀子甙=栀子黄,但是在帮客户查询标准品的过程中发现:A.栀子甙(Geniposide,CAS.NO 24512-63-8,phytolab);B.栀子苷Geniposide,CAS.NO有的写着24512-63-8,有的写着27745-20-6,国内的标准品品牌;同时,我在phytolab这个品牌下面查的时候,除了Geniposide又看到另外一个物质:C.Gardenoside,CAS.NO 24512-62-7,有的地方也翻译成栀子苷;看到上面这些已经很疑惑了,接下来看栀子黄。发现名称叫栀子黄也蛮多的,例如:1.栀子黄色素GARDENIA YELLOW CAS.NO 94238-00-3,WAKO,现在可能停产了;2.藏花橙G,栀子黄色素,Acid Orange 12,CAS.NO 1934-20-9,TCI;在万分的疑惑中,参考了http://bbs.instrument.com.cn/shtml/20110507/3291390/这个帖子上面的说法,看了GB 7912-2010这个标准,又查到了这个:3.栀子色素 藏红花素,Crocin,Crocetin digentiobiose ester,CAS.NO 42553-65-1,FLUKA;查到这里彻底糊涂,食品中的栀子黄检测到底是哪个呢?不知道哪位老师对这方面比较了解,希望能够我们一些意见,解开这个长久以来的疑惑。
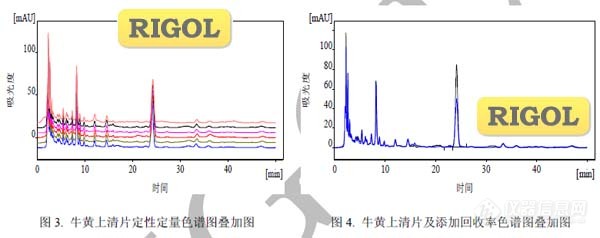
文章来源于RIGOL(北京普源精电科技有限公司)应用中心 :http://www.instrument.com.cn/netshow/SH101945/#【摘要】 本文根据中华人民共和国药典(2010版)新增品种—牛黄上清片中栀子苷的含量测定方法,对某厂家生产的牛黄上清片进行含量测定及方法学验证。实验结果为:以栀子苷峰计理论塔板数为11614(药典要求理论塔板数按栀子苷峰计算应不低于7000),牛黄上清片产品中栀子苷含量为0.62mg/片(药典要求栀子苷含量以每片计,不得少于0.40mg)。栀子苷的线性范围为1.1μg/mL~106.0μg/mL (r=0.9999),平均回收率为105.3%。实验结果表明:采用RIGOL L-3000高效液相系统进行牛黄上清片中栀子苷含量测定,能完全满足中华人民共和国药典要求,方法准确、灵敏。
铂金干锅和铂黄干锅一样嘛?不一样的话,那么他们清洗要注意那些

作者:李润文((沈阳市第六人民医院,辽宁沈阳110006)摘要:目的:建立解毒退黄合剂中栀子苷的含量测定方法。方法:采用HPLC法,色谱柱为Diamonsil C18柱(4.6mmn×250mm,5μm),流动相为乙腈一水(12:88),流速为1.0 ml/min,检测波长为238 nm。结果:栀子苷在0.142-1.424 0μg范围内线性关系良好(r=0.9998),平均回收率为100.6%,RSD为0.91%。结论:本方法灵敏、准确、重复性好,为解毒退黄合剂的质量控制提供了依据。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208211629_385067_1609970_3.jpg
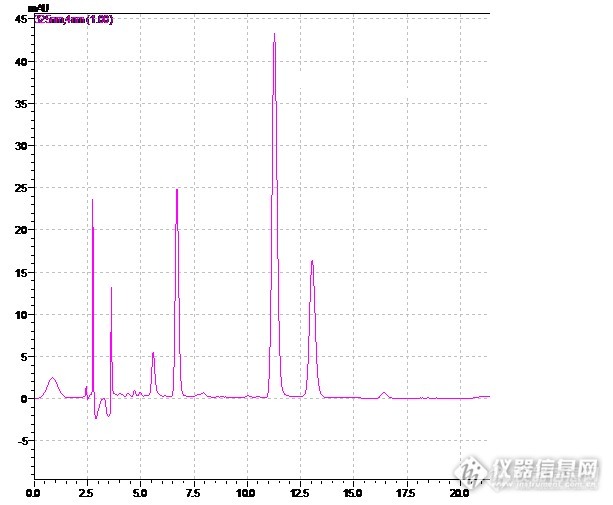
作者:黄妙婵(东莞市人民医院 药剂科, 广东 东莞 523018)摘要: 目的建立柴黄颗粒中黄芩苷的含量测定方法。方法采用迪马钻石C18(4.6mm×250mm,5μm)为色谱柱,以甲醇-0.4%磷酸(55∶45)为流动相,检测波长为280nm。结果黄芩苷在0.131μg~1.309μg范围内呈良好的线性关系,r=1.000,平均加样回收率为100.95%,相对标准偏差值(RSD)=1.38%。结论本法操作简便,结果准确、可靠、重现性好,可用于柴黄颗粒的质量控制。谱图:http://ng1.17img.cn/bbsfiles/images/2012/07/201207161426_377871_1606903_3.jpg
微波消解的植物样品,样品取0.3g,硝酸5ml盐酸2ml,反应10ml后进行消解,消解后溶液澄清。赶酸用的电热板和坩埚,160℃。经过两次加水,赶至溶液近干且无色。然后问题来了。第一次,用1+1盐酸和1%氯化铵各5ml溶解,然后定容。在坩埚中,加盐酸后变的超级黄,定容后有悬浮物和沉淀。第二次用的1%硝酸,加完还透明,转移到比色管中瞬间变黄,和用盐酸的颜色一样,而且有悬浮物,定容后依然有这些问题。此外,第二天发现第一次的溶液中 悬浮物大量减少且沉淀消失;未进行赶酸的消解后溶液在放置一天后变黄了,而且顺带消解的两个泥样格外黄。以上所说的黄色,与赶酸时出现的黄色相同。想问一下各位老师:这个黄色究竟是什么引起的?? 为什么在赶酸,两次复溶,久放的情况下出现了相同的的颜色?? 如果说是氯离子的原因的话,为什么第二次在转移的时候才瞬间变黄(比色管用蒸馏水洗过了)?? 还有那个悬浮物和沉淀是啥??[img]http://ng1.17img.cn/bbsfiles/images/2017/11/201711051739_01_3326813_3.jpeg[/img][img]http://ng1.17img.cn/bbsfiles/images/2017/11/201711051739_01_3326813_3.jpeg[/img][img]http://ng1.17img.cn/bbsfiles/images/2017/11/201711051739_01_3326813_3.jpeg[/img][img]http://ng1.17img.cn/bbsfiles/images/2017/11/201711051739_01_3326813_3.jpeg[/img]

各位大神好,本人最近在用电热板消解人发,来测量人发中的重金属。样品量头发0.5g,每个样品加了2ml硝酸+1ml双氧水。先加的硝酸后加的双氧水,加的时候液体无法完全没过头发。然后放在电热板上进行加热。温度设置200度。但是我们用温度计测量了一下,无论电热板开到多高的温度,坩埚的底部温度最高也就是120度。加热30分钟。然后打开盖子。是下图这样。先冒白烟,再冒黄烟。然后电热板温度调到了120度。开始赶酸。但是赶了大概15分钟,我又把盖子盖上,然后等了5分钟一打开又是先冒黄烟,再冒白烟,请问这算赶干净了吗?视频如下图所示。不知道传上去了没有。另外在赶酸的时候可以加一点超纯水吗?我看网上说赶酸要剩下1ml的液体再拿出来。。是我到1ml的时候拿出来,坩埚还有余热,后面坩埚的余热就把剩下的液体烤成黏的了,倒不出来了。是等剩下的液体多一点2ml再拿出来,还是剩下1ml的时候加点超纯水或者3%的稀硝酸呢?[img=图1 刚打开盖子冒黄烟,690,1495]https://ng1.17img.cn/bbsfiles/images/2019/10/201910151048585673_4450_3950572_3.jpg!w690x1495.jpg[/img][img=图2,690,1495]https://ng1.17img.cn/bbsfiles/images/2019/10/201910151050598443_5631_3950572_3.jpg!w690x1495.jpg[/img]

作者:谭志艺; 刘永路;(广东省云浮市药品检验所;)摘要:目的建立测定牛黄上清片中连翘苷含量的高效液相色谱(HPLC)法。方法色谱柱为Diamonsil(钻石)C18柱(250 mm×4.6 mm,5μm),流动相为乙腈-水(25∶75),检测波长为230 nm,流速为1.0 mL/min,柱温为30℃。结果连翘苷进样量在0.08~1.00μg范围内与峰面积线性关系良好(r=0.999 9),平均加样回收率为99.66%,RSD=0.78%(n=6)。结论 HPLC法简便、灵敏、准确、重复性好,可用于牛黄上清片的质量控制。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208271012_386283_1606903_3.jpg
广州最近发现有人用硫磺蒸菜干,不知有什么危害?如何分辨菜干是否用硫磺蒸过?
新进的批号是201004的吡啶已经是淡黄色的了,配制溶液过夜后,苯酐溶液颜色更深了,请问,吡啶变色原理是什么?对多元醇测定影响是如何产生的,请高人指点。我用的电位滴定。吡啶变黄不能用是针对使用指示剂干扰终点判断还是其他的原因呢?
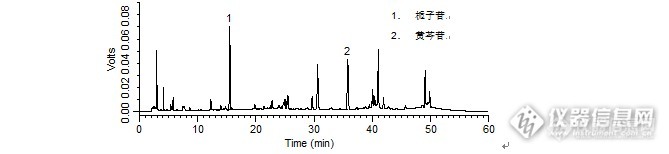
摘要: 目的 建立茵栀黄颗粒中栀子苷和绿原酸的含量测定方法。方法 采用高效液相色谱法。色谱柱:Kromasil C18柱(4.6mm×250mm,5μm);流动相:乙腈-0.1%甲酸(10:90);流速1.0ml/min;柱温:35℃;检测波长:238nm、325nm。结果:对茵栀黄颗粒中栀子苷和绿原酸进行含量测定。 栀子苷在10.43~52.15μg范围内呈线性关系(r=0.9999 ,n=6),线性方程为y=123721821.7x-6951.8(r=0.9999)。平均加样回收率为97.21% RSD为1.62% (n=6) 绿原酸在10.74~53.70μg范围内呈线性关系(r=0.9999 ,n=6),线性方程为y=29447356x-25436(r=0.9999)。平均加样回收率为96.61% RSD为1.35% (n=6)结论 该方法操作简便,结果可靠,可用于茵栀黄颗粒中栀子苷和绿原酸的含量测定。 清茵栀黄颗粒,清热解毒,利湿退黄。有退黄疸和降低谷丙转氨酶的作用。用于湿热毒邪内蕴所致急性、慢性肝炎和重症肝炎(I型)。也可用于其他型重症肝炎的综合治疗。由陈提取物、栀子提取物、黄芩苷、金银花提取物组成。为了进一步控制药品质量,我们对其中的进行了栀子苷和绿原酸含量测定,以期为后续进一步研究奠定基础!关键词:HPLC;DAD;茵栀黄颗粒;栀子苷 ;绿原酸1 仪器与试药1.1 仪器 岛津LC-20AT高效液相色谱仪,SPD-M20A检测器, LCsolution色谱工作站, Metteler AB265S(0.01mg);Sartorius BS124S(0.1mg)),必能信超声波清洗器(必能信超声有限公司)1.2 试药 绿原酸对照品(批号110753-201314)、栀子苷对照品(批号:110749-201115),均购自中国食品药品检定研究院;乙腈(色谱纯);其它试剂均为国产分析纯,蒸馏水自制。2 实验方法与结果2.1 色谱条件与图谱 色谱柱: Kromasil C18柱(4.6mmx250mm,5um); 检测波长:238nm;325nm 流速:1.0ml.min-1; 流动相:乙腈-0.1%甲酸(10:90); 柱温:35℃。2.2 溶液制备2.2.1对照品溶液 取栀子苷和绿原酸对照品适量,精密称定,加甲醇制成每1ml 分别含0.1043mg和0.1074mg 的混合溶液,即得。2.2.2供试品溶液 取本品,研细,取约0.5g,精密称定置50ml量瓶中,精密加入甲醇40ml,称定重量,超声处理30min ,再称定重量,用甲醇补足减失的重量,定容至50ml,摇匀,滤过,即得。2.3 线性关系考察 精密量取各对照品溶液,制得5个系列不同浓度的对照品溶液,各取10微升依次进样,按上述色谱条件测定峰面积,以对照品峰面积Y为纵坐标,浓度X(mg·mL )为横坐标,绘制标准曲线,结果栀子苷在10.43~52.15μg范围内呈线性关系(r=0.9999 ,n=6),线性方程为y=123721821.7x-6951.8(r=0.9999)。绿原酸在10.74~53.70μg范围内呈线性关系(r=0.9999 ,n=6),线性方程为y=58134683.4x-7988.3(r=0.9999) http://ng1.17img.cn/bbsfiles/images/2015/10/201510020006_569010_1839779_3.pnghttp://ng1.17img.cn/bbsfiles/images/2017/10/2015100200003568_01_1839779_3.png2.4精密度试验 精密吸取同一供试品溶液,重复进样6次,计算栀子苷和绿原酸对照品 峰面积的RSD分别为0.4% 和1.4% 。2.5 稳定性试验 精密吸取同一供试品溶液,分别于0,2,4,8,16,24 h测定,结果表明:栀子苷和绿原酸对照品在24 h内稳定,RSD分别为1.1% 和1.5% 。2.6 重复性实验 取同一批次的茵栀黄颗粒平行6份,制成供试品溶液,在上述色谱条件下分别进行HPLC分析,计算栀子苷和绿原酸对照品峰面积的RSD分别为1.2%和1.4% 。2.7 回收试验 取同一批茵栀黄颗粒,约取0.25g,共计6份,精密称定,按上述色谱条件进样测定,用回归方程计算回收率。2.8 样品含量测定 取3个批号的茵栀黄颗粒,配制成供试品溶液,在上述色谱条件下进行测定,栀子苷和绿原酸对照品的含量,结果见表。样品编号栀子苷(mg/g)20150729 2.54201410032.61201502162.65样品编号绿原酸(mg/g)20150729 1.04201410031.16201502161.12http://ng1.17img.cn/bbsfiles/images/2017/10/2015100111035245_01_1839779_3.bmp 图1 茵栀黄颗粒的HPLC图谱(238nm)http://ng1.17img.cn/bbsfiles/images/2017/10/2015100111125995_01_1839779_3.bmp 图2 栀子苷的HPLC图谱(238nm)http://ng1.17img.cn/bbsfiles/images/2017/10/2015100111105517_01_1839779_3.png 图3 茵栀黄颗粒的HPLC图谱(325nm)http://ng1.17img.cn/bbsfiles/images/2017/10/2015100111150072_01_1839779_3.bmp 图4 绿原酸的HPLC图谱(325
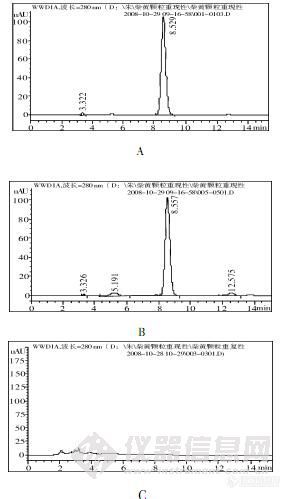
【文章来源】北京普源精电科技有限公司(RIGOL) http://www.instrument.com.cn/netshow/SH101945/index.asp【摘要】 本文根据中华人民共和国药典(2010 版)第一部中牛黄上清片中黄芩苷的含量测定方法,对某厂家生产的牛黄上清片进行含量测定及方法学验证。实验结果为:以黄芩苷峰计理论塔板数为12050(药典要求理论塔板数按黄芩苷峰计算应不低于4000),牛黄上清片产品中黄芩苷含量为1.7mg/片(药典要求黄芩苷含量以每片计,不得少于1.0mg/片)。黄芩苷的线性范围为4μ g/mL~200μ g/mL (r=0.9991),平均回收率为98.8%。实验结果表明:采用RIGOL L-3000高效液相系统进行牛黄上清片中黄芩苷含量测定,能完全满足中华人民共和国药典要求,方法准确、灵敏。完整应用文档,请点击如下链接下载 ======================= 点击打开链接 ==========================针对大家所关心的问题,RIGOL应用中心会持续为大家开展分析http://simg.instrument.com.cn/bbs/images/brow/em09511.gif部分谱图:对照品标准工作溶液及样品溶液http://ng1.17img.cn/bbsfiles/images/2011/03/201103111726_282164_2248886_3.jpg定性及定量重复性 http://ng1.17img.cn/bbsfiles/images/2011/03/201103111726_282165_2248886_3.jpg欢迎大家积极讨论哈~~http://simg.instrument.com.cn/bbs/images/brow/em09510.gif
问题:牛黄上清片中黄芩苷、栀子苷的检测:用到了迪马哪几款色谱柱?答案:Platisil ODS ,Diamonsil C18(2)、Diamonsil C18获奖名单:m3071659(ID:m3071659)梧桐(ID:mengzhou)莫名其妙(ID:moyueqiu)http://ng1.17img.cn/bbsfiles/images/2016/02/201602221622_584839_708_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/02/201602221622_584840_708_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/02/201602221622_584841_708_3.jpg【活动奖励】幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。牛黄上清片中黄芩苷、栀子苷的检测样品制备 制备方法1. 对照品:取黄芩苷对照品和栀子苷对照品适量,精密称定,加甲醇制成每1 mL含黄芩苷40 μg、栀子苷20 μg的混合溶液。2. 供试品:取本品10片(糖衣片除去包衣),精密称定,研细,取约0.5 g,精密称定置具塞锥形瓶中加入,精密称定,置具塞锥形瓶中,精密加入70%甲醇50 mL,称定重量,超声处理(功率500 W,频率40 kHz)30分钟,放冷,再称定重量,用70%甲醇补足减失的重量,摇匀,滤过,取续虑液,即得。分析条件 色谱柱Platisil ODS 250 x 4.6 mm,5 μm (Cat #:99503)流动相A:乙腈 B: 0.05% 磷酸 梯度流速1.0 mL/min柱温30 ℃检测器UV 240 nm 进样量10 μL色谱图 对照品http://ng1.17img.cn/bbsfiles/images/2016/02/201602221019_584795_708_3.png 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 15.411 469421 54969 68777.750 1.066 -- 2 35.690 398602 29220 151298.496 1.025 67.364 *药典要求理论板数按黄芩苷峰计算应不低于3000供试品http://ng1.17img.cn/bbsfiles/images/2016/02/201602221020_584796_708_3.png 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 15.485 585904 68473 69461.797 1.035 -- 2 35.751 556697 41418 154814.011 1.023 67.727 *药典要求理论板数按黄芩苷峰计算应不低于3000本品种同时使用了Diamonsil C18(2)、Diamonsil C18两款色谱柱,在药典规定条件下进行栀子苷、黄芩苷的检测,均满足药典要求。

问题:牛黄上清胶囊中黄芩苷、栀子苷的检测药典要求理论板数按黄芩苷峰计算应?答案:不低于3000【活动奖励】幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币sixingxing(注册ID:v2889187)莫名其妙(注册ID:moyueqiu)dyd3183621(注册ID:dyd3183621)http://ng1.17img.cn/bbsfiles/images/2016/02/201602171526_584548_1610895_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/02/201602171526_584549_1610895_3.png积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================牛黄上清胶囊中黄芩苷、栀子苷的检测样品制备制备方法1. 对照品:取黄芩苷对照品和栀子苷对照品适量,精密称定,加甲醇制成每1 mL含黄芩苷40 μg、栀子苷20 μg的混合溶液。2. 供试品:取装量差异项下的内容物,混匀,取约0.5 g,精密称定置具塞锥形瓶中加入,精密称定置具塞锥形瓶中加入70%甲醇50 mL,称定重量,超声处理(功率500 W,频率40 kHz)30分钟,再称定重量,用70%甲醇补足,过滤,取虑液。分析条件色谱柱Platisil ODS 250 x 4.6 mm,5 μm (Cat #:99503)流动相A:乙腈 B: 0.05% 磷酸 梯度流速1.0 mL/min柱温30 ℃检测器UV 240 nm 进样量10 μL色谱图对照品 http://ng1.17img.cn/bbsfiles/images/2016/02/201602170955_584522_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 15.411 469421 54969 68777.750 1.066 -- 2 35.690 398602 29220 151298.496 1.025 67.364 *药典要求理论板数按黄芩苷峰计算应不低于3000供试品http://ng1.17img.cn/bbsfiles/images/2016/02/201602170955_584523_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 15.491 471187 56225 71097.596 1.007 -- 2 35.749 510106 37988 154696.206 1.023 67.986 *药典要求理论板数按黄芩苷峰计算应不低于3000[align=lef
1、0.5g不透明胶囊2、加8ml硝酸,1ml氢氟酸静置3、微波消解仪程序升温,最高1.6mpa,共计55分钟,然后冷却,这时会发现,消解罐的内壁上都是黄色的4、用电热板赶酸,4小时后,剩余1ml左右,这时消解罐的内壁上都黄色的,溶液稍微显黄5、用稀硝酸定容后发现好黄啊,虽然是澄清的溶液,可是挺黄的。我担心是消解的不够完全,今天又加了1ml的双氧水,来促进硝酸的氧化还原,可是最终定容后发现比原来更黄了。而同样的胶囊,药检所做出来是很澄清无色的液体。求解
[center]秋间银杏黄文/闻禾[/center] 车行天坛东门,绕天坛墙外右行。卧床三天病初愈的我,要去上班。蓝天不动,蓝天下的白云静止。静止的蓝天白云下,各样形状、各种颜色的风筝,在不见身形的风的扶持和梳理下,自由舒展,或上下起伏、或斜线攀援,恬静安闲......坐在车窗边。望窗外,人流车流,熟视无睹。[center][img]http://it.news.tom.com/uimg/2007/11/12/songyuzhen/1194834669529_543315.JPG[/img][/center]我被环绕天坛公园围墙的银杏树深深吸住,默叹着银杏的神奇魅力。一下子就想起几天前看到的一位中学生赞美银杏树的文章。几乎用尽了华丽美妙词句,刻意赞美的那些银杏树,还是没眼前的这般景色令心垂涎,令人神往啊。百闻难抵一见。今年仲秋,见到了以为这辈子都见不到的银杏果。圆圆的,宛若桂圆。初次与其相见,是在一位同事的办公室里,那些大小比较均匀的小圆球,满满地拥挤在白色塑料袋子里。未曾剥皮见肉,据说果肉很臭。今年银杏盛产,那日去台基厂换新电表卡,崇文门大街路南有很多老牌银杏树,果实累累强压枝,几乎每棵树上,各个枝杈,都满满堆砌了圆圆的小球,疙疙瘩瘩,风吹叶落,果实欲重......多,太多了。崇文大街上的银杏果,压过了叶子的风光。我觉得结了果子的银杏树,失去了原有的美丽。这种被称之为白果、银杏果、爷孙果的果实,应该是岁月的扎染,风霜的积淀。银杏又称爷孙树,意思是爷辈栽树,孙辈方能结果。不到一定年龄,银杏树是不结果子的。化学馆前几棵硕大的颇有特色银杏树又出现在眼前。那时我刚刚认识银杏树,经常将绿色的、黄色的、形状规整的、奇异的银杏叶夹在本间书内,爱不释手。那是特别期盼能有机会与银杏果见上一见,可我守望了整整四年,最后还是一无所获。不知是性别原因(有人说,化学馆前的银杏树都是雄性的),年龄问题,还是化学反应的缘故,学校的银杏树就是不见结果实。所以在我的印象中,见到银杏果结在树上,就跟不可能实现的梦幻一样。今秋崇文门大街观银杏,一扫我一直以来天真幼稚略加疯狂的想法。不但见到了结在树上的银杏果,而且一见就是那么多!树上结的,地上落的。“要绿都绿,要黄都黄。竟然不见一叶杂色。”车子向前滑动,银杏树环围天坛墙悠悠移动,心在赞叹眼睛的发现——想起一直喜欢的梧桐树。形色俊美的大叶子,应季变换色形的梧桐球,如同涂鸦墙般的、敦实憨厚不高的树干,总是心甘情愿、欢快自豪地举着硕大唯美、挂了滴溜溜小球的树枝树叶,充分展示着幸福的骄傲。在梧桐树上,我从来读不到文人的那份过于细腻的心情感受——凄凄惨惨戚戚!感情若遭霜打一般。暮秋的梧桐,树干已斑驳,叶子多层色——干焦褐色、将干棕色、染秋黄色、犹存绿色,但它们依然在渐凉渐冷的秋风里,步岁月韵律蹈舞,唱有缘相聚幸福歌,虽有稀稀落落,依然潇潇洒洒......与梧桐树树色的杂不同,银杏颜色的变化竟如此步调一致,整齐划一。纯纯春绿,渐渐绿黄,直至满树纯黄——立正!稍息!起步走!银杏犹如自然界的仪仗队,跟随季节的口令,甩臂抬腿,齐唱“三大纪律、八项注意”,步调一致,出神入化。哦,银杏树!不知该怎么赞美你!突然想起一句毛主席语录:军民团结如一人,试看天下谁能敌!天坛公园上空,不动的蓝天,休闲的白云,隐形的微风,揉合在飘逸潇洒错落安然的风筝中,翱翔轻飞,竟放胸怀,驰骋呼吸......古香古韵的青砖墙外,一道纯天然的、齐色优雅的银杏黄......溶解在这静动行色如此动人的景色里放飞思绪的人啊,不该有不快乐、不幸福的理由?!

问题:2015药典银黄口服液中的黄芩苷的检测要求理论塔板数是?答案:【活动奖励】幸运奖(2钻石币):吕梁山(ID:shih20j07)langyabeilei(注册ID:langyabeilei)999youran(ID:999youran)http://ng1.17img.cn/bbsfiles/images/2015/12/201512031626_576208_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/12/201512031626_576209_1610895_3.jpg积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================银黄口服液中的黄芩苷的检测样品制备 制备方法1. 对照品:取黄芩苷对照品适量,精密称定,加50%甲醇制成每1 mL含50 μg的溶液,即得。2. 供试品:精密量取本品1 mL,置50 mL量瓶中,加水稀释至刻度,摇匀,精密量取3 mL,置25 mL量瓶中,加50%甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。分析条件色谱柱Platisil ODS 250 x 4.6 mm,5 μm (Cat#:99503)流动相甲醇:水:磷酸=50:50:0.2 流速1 mL/min柱温30 ℃检测器UV 274 nm 进样量10 μL 色谱图对照品 http://ng1.17img.cn/bbsfiles/images/2015/12/201512031003_576131_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 14.437 1794249 90729 12097.640 0.970 -- *药典要求理论板数按黄芩苷峰计算应不低于2500供试品http://ng1.17img.cn/bbsfiles/images/2015/12/201512031003_576132_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 14.373 1886953 90922 11499.957 0.944 -- *药典要求理论板数按黄芩苷峰计算应不低于2500本品种同时使用了Diamonsil C18、Leapsil C18两款色谱柱,在药典规定条件下进行黄芩苷的检测,均满足药典要求。
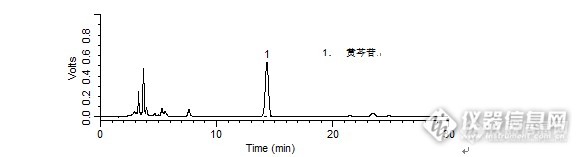
问题:银黄颗粒中的黄芩苷的检测:用到了迪马哪几款色谱柱?答案:Platisil ODS,Diamonsil C18、Leapsil C18获奖名单:zengzhengce163(ID:zengzhengce163)翠湖园(ID:hhx050)梧桐(ID:mengzhou)http://ng1.17img.cn/bbsfiles/images/2016/03/201603251742_588287_708_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/03/201603251741_588286_708_3.jpg【活动奖励】幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。银黄颗粒中的黄芩苷的检测样品制备 制备方法1. 对照品:取黄芩苷对照品适量,精密称定,加50%甲醇制成每1 mL含50 μg的溶液,即得。2. 供试品:取装量差异项下的本品,研细,取适量(相当于金银花提取物33.3 mg),精密称定,置50 mL棕色量瓶中,加50%甲醇40 mL,超声处理(功率500 W,频率40 kHz)30分钟,放冷,加50%甲醇至刻度,摇匀,滤过,取续滤液3 mL,置10 mL量瓶中,加50%甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。分析条件 色谱柱Platisil ODS 250 x 4.6 mm,5 μm (Cat#:99503)流动相甲醇:水:磷酸=50:50:0.2 流速1 mL/min柱温30 ℃检测器UV 274 nm 进样量10 μL 色谱图对照品http://ng1.17img.cn/bbsfiles/images/2016/03/201603251028_588172_708_3.png 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 14.437 1794249 90729 12097.640 0.970 -- *药典要求理论板数按黄芩苷峰计算应不低于2500供试品 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 14.437 1794249 90729 12097.640 0.970 -- *药典要求理论板数按黄芩苷峰计算应不低于2500供试品http://ng1.17img.cn/bbsfiles/images/2016/03/201603251029_588174_708_3.png 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 14.330 10524368 535290 12024.531 0.970 -- *药典要求理论数按黄芩苷峰计算应不低于2500本品种同时使用了Diamonsil C18、Leapsil C18两款色谱柱,在药典规定条件下进行黄芩苷的检测,均满足药典要求。
[size=5][b]如何识别硫磺熏制过的干枣?[/b][/size][align=left][font=宋体 ][size=3]看外表:硫磺熏制的红枣表皮,可以看到一层光泽,如同上了蜡一样。硫磺熏制的红枣“红”且“鲜”,颜色较一致。没有熏制的红枣呈暗红色,颜色有深有浅。[/size][/font][/align][align=left][font=宋体 ][size=3]看里层:购买时可先咬开几粒尝一尝或闻一闻,硫磺熏制的红枣肉体偏白,味道有点发酸且有刺鼻的气味。买红枣等干货时不能太注重外表的颜色。[/size][/font][/align]
急,本人想做甘油+黄原胶高分子溶液的拉伸流动特性,但是不知道哪里可以测?用什么测?
本人最近刚好在做色素分析,就申请了本次实验室比对,感谢仪器信息网组织本次实验室比对活动,同时也感谢北京曼哈格生物科技有限公司和北京振翔科技有限公司为本次活动提供样品和聚酰胺固相萃取柱(7月4号收到样品和固相萃取柱)。因为我的图片上传不了,我就不上传图片了。本次实验参照《GB 5009.35-2016 食品安全国家标准食品中合成着色剂的测定》来进行。样品前处理方法完全按照GB 5009.35-2016前处理方法,分析仪器为安捷伦1290 Infinity LC,色谱柱为迪马Spursil C18-EP柱(4.6mm×250mm,5μm),柱温35℃,流速0.8mL/mL,进样量10μL,DAD检测器波长254nm。梯度洗脱条件如下: [table=64%][tr][td] [align=center]时间[/align] [align=center]min[/align] [/td][td] [align=center]流速[/align] [align=center]mL/min[/align] [/td][td] [align=center]0.02mol/L乙酸铵[/align] [align=center]%[/align] [/td][td] [align=center]甲醇[/align] [align=center]%[/align] [/td][/tr][tr][td] [align=center]0[/align] [/td][td] [align=center]0.8[/align] [/td][td] [align=center]95[/align] [/td][td] [align=center]5[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]0.8[/align] [/td][td] [align=center]95[/align] [/td][td] [align=center]5[/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]0.8[/align] [/td][td] [align=center]65[/align] [/td][td] [align=center]35[/align] [/td][/tr][tr][td] [align=center]13[/align] [/td][td] [align=center]0.8[/align] [/td][td] [align=center]5[/align] [/td][td] [align=center]95[/align] [/td][/tr][tr][td] [align=center]16[/align] [/td][td] [align=center]0.8[/align] [/td][td] [align=center]5[/align] [/td][td] [align=center]95[/align] [/td][/tr][tr][td] [align=center]16.10[/align] [/td][td] [align=center]0.8[/align] [/td][td] [align=center]95[/align] [/td][td] [align=center]5[/align] [/td][/tr][tr][td] [align=center]21[/align] [/td][td] [align=center]0.8[/align] [/td][td] [align=center]95[/align] [/td][td] [align=center]5[/align] [/td][/tr][/table]通过上述条件得到的标准曲线如下表所示。 [table][tr][td] [align=center]组分[/align] [/td][td] [align=center]校正曲线[/align] [/td][td] [align=center]浓度范围(μg/mL)[/align] [/td][td] [align=center]相关系数R[sup]2[/sup][/align] [/td][/tr][tr][td] [align=center]柠檬黄[/align] [/td][td] [align=center]Y=19.927X+2.229[/align] [/td][td] [align=center]1.96~19.56[/align] [/td][td] [align=center]0.9999[/align] [/td][/tr][tr][td] [align=center]日落黄[/align] [/td][td] [align=center]Y=15.048X+0.913[/align] [/td][td] [align=center]1.46~14.58[/align] [/td][td] [align=center]1.0000[/align] [/td][/tr][/table]通过样品和标准品色谱图比较可以发现,苹果汁样品经过前处理后杂质峰已经很少,说明此前处理手段对色素测定有很好的效果。同时,我也利用寄送过来的聚酰胺固相萃取柱来进行同样过程的样品前处理,利用相同测定方法进行分析,得出结果与聚酰胺粉前处理的结果相吻合。本次草根能力对比给我印象最深的就是利用聚酰胺固相萃取柱来进行样品前处理相比于聚酰胺粉来做前处理要简单方便很多,不需要再进行减压过滤等操作,大大提高工作效率,并且对测定结果无影响。以后做色素分析的话可以考虑利用聚酰胺固相色谱柱来进行样品前处理。以上就是我做此次草根比对的过程和一点点小的体会,有什么不对的地方望广大坛友批评指正!谢谢大家!
国标5009.149-2003栀子黄检测采用了栀子苷作为标准品,对栀子黄定量。但在GB7912-2010食品安全国家标准食品添加剂栀子黄中栀子黄的主要成分是藏花素和藏花酸,栀子苷只是含量应该在1%一下的杂质。国标5009.149-2003是不是搞错了啊,这个标准有更新版吗?见过有错误的国标,但这么离谱的还是第一次见,有点不敢相信自己了。但实验室有做过栀子苷,查了下紫外谱图,发现栀子苷在可见光区确实没有吸收,因此不可能是色素添加剂吧?对栀子黄熟悉的或做过这个标准的请指教一下这个问题,谢谢!!!!!!
中文学名:人工牛黄拉丁学名:Bovis Calculus Artifactus别 称:无产 区:无属性分类:无药 性:甘,凉。归心、肝经。
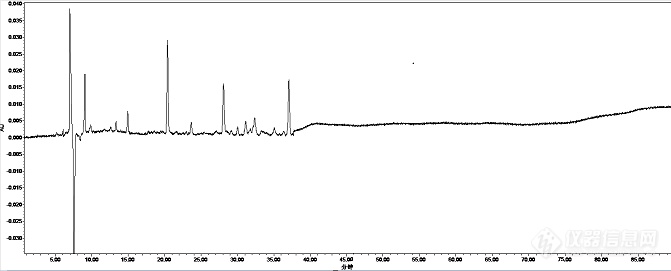
[align=center][b]一种银黄颗粒HPLC指纹图谱的检测方法及其应用[/b][/align]摘要目的:本研究介绍了银黄颗粒及其原料药黄芩和金银花的指纹图谱的建立方法,包括供试品溶液的制备、高效液相色谱仪测定及对数据和图谱的处理,以及由该方法制备得到的相应指纹图谱。方法:使用Venusil MP C18(4.6 mm × 250 mm,5 μm)+ Venusil MP C18(4.6 mm × 250 mm,3 μm)色谱柱在紫外235 nm吸收波长,选用流动相:乙腈(A)-0.3%磷酸(B)梯度洗脱,0~103 min,17%ACN 103~142 min,17%→27%ACN;142~156 min,27%→29%ACN;156~179 min,29%→41%ACN;179~219min,41%→80%CAN。结果:在测定的不同厂家 10 批次样品的色谱图中,选择90%以上批次样品均有的色谱峰为共有峰,银黄颗粒。黄芩药材、金银花药材分别确定了22,22,21 个共有峰。结论:为银黄颗粒定性鉴别提供借鉴。关键词:银黄颗粒;黄芩;金银花;指纹图谱[align=center][b]A Method for Detecting Fingerprint of Yinhuang Granules by HPLC and ItsApplication[/b][/align]Abstract Objective: To introduce the method ofestablishing fingerprint of Yinhuang granules and its raw materials,Scutellaria baicalensis and Lonicera japonica, including the preparation ofsample solution, determination by high performance liquid chromatography andthe treatment of data and chromatogram, as well as the correspondingfingerprint obtained by this method. METHODS: Venusil MP C18 (4.6 mm×250 mm, 5 mm) + Venusil MP C18 (4.6 mm×250mm, 3 mm) column was used at 235 nmultraviolet absorption wavelength. The mobile phase was selected: acetonitrile(A) - 0.3% phosphoric acid (B) gradient elution, 0-103 min, 17% ACN, 103-142min, 17% to 27% ACN, 142-156 min, 27% to 29% ACN, 156-179 min, 29% to 4% ACN.1% ACN 179 ~ 219 min, 41%80% CAN. RESULTS: In the chromatograms of 10 batchesof samples from different manufacturers, more than 90% of the samples hadcommon peaks, Yinhuang granules. Scutellaria baicalensis and Lonicera japonicahave 22, 22 and 21 peaks respectively. CONCLUSION: It can provide reference forthe qualitative identification of Yinhuang Granules.Key words: Yinhuang granules Scutellaria baicalensis Honeysuckle Fingerprint[b] 一、前言[/b]银黄颗粒组方由金银花和黄芩构成,具有清热疏风、利咽解毒的功效,用于外感风热、肺胃热盛所致的咽干、咽痛、喉核肿大、口渴、发热急慢性扁桃体炎、急慢性咽炎、上呼吸道感染等症。该复方原料金银花为忍冬科植物忍冬的干燥花蕾或带初开的花,主产于山东、河南和河北等地。该复方原料黄芩为唇形科[url=https://baike.baidu.com/item/%E9%BB%84%E8%8A%A9%E5%B1%9E][color=windowtext]黄芩属[/color][/url]多年生草本植物,产于河北,河南,陕西,山西,山东等地。黄芩提取物的主要活性成分为黄芩苷、汉黄芩苷、黄芩素及汉黄芩素,金银花提取物是从金银花中提取的有机酸类活性成分。该制剂及其原料药成分复杂,生产厂家及产地众多,样品存在差异。中药 HPLC 指纹图谱技术被认为是当前能较全面反映中药材及复方整体化学成分信息的方法,能更有效地评价中药的质量信息。本研究在分析上述研究背景的基础上,收集来源于不同产地的各50批金银花和黄芩药材,并制成银黄颗粒成品,再采用HPLC法同时建立金银花药材,黄芩药材和相应批次银黄颗粒的指纹图谱,选出各自的共有峰,从而确定不同产地,不同厂家的的药材共有物质及其数量。[b]二、材料与方法1仪器与试剂、试药1.1仪器[/b]Waters e2695高效液相色谱仪(美国Waters公司),Waters 2998紫外检测器(美国Waters公司),Waters Empower色谱工作站(美国Waters公司);AGBP210S电子天平(Sartorius公司);MILLIPORE纯水机(MILLIPORE公司);高速万能粉碎机(北京市永光明医疗仪器有限公司,FW-80型);SB4200DTS超声波双频清洗机(宁波新芝生物科技股份有限公司);KDM-A控温电热套(金坛市医疗仪器厂);Venusil MP C[sub]18[/sub](4.6 mm × 250 mm,5 μm)和Venusil MP C[sub]18[/sub](4.6 mm × 250 mm,3 μm)。[b]1.2 试剂与试药[/b]乙腈(上海星可高纯溶剂有限公司,色谱纯);甲醇(天津市科密欧化学试剂有限公司,色谱纯);其余试剂均为分析纯,水为超纯水。对照品来源:葛根素(批号:110752-200912)购自中国食品药品检定研究院。[b]2方法2.1 HPLC色谱条件的考察2.1.1不同流动相的考察[/b]比较了乙腈--0.05%甲酸、乙腈-0.4%甲酸、乙腈-0.3%甲酸的流动相系统进行洗脱。见图1。 [align=center][img=,671,271]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091124382201_5843_3255306_3.png!w671x271.jpg[/img][/align][align=center]乙腈--0.05%甲酸[/align][align=center][img=,610,288]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091124499241_4585_3255306_3.png!w610x288.jpg[/img][/align][align=center]乙腈-0.4%甲酸[/align][align=center][img=,690,286]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091124589941_1562_3255306_3.png!w690x286.jpg[/img][/align][align=center]乙腈-0.3%甲酸[/align][align=center][img=,610,286]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091125102591_3301_3255306_3.png!w610x286.jpg[/img][/align][align=center]图1 不同流动相系统下银黄颗粒指纹图谱[/align]结果表明,前二者分离度均相对较差,且乙腈-0.05%甲酸均基线噪音大。最终选用乙腈-0.3%磷酸作为流动相系统,所得色谱峰型较好,基线平稳,分离效果最佳。[b]2.1.2 梯度洗脱条件的选择[/b]本实验考察了不同比例的乙腈-磷酸的洗脱条件,尽可能多且全面展现银黄颗粒样品的峰信息,考察了以下4个洗脱程序。梯度条件一:流动相:乙腈(A)-0.1%磷酸(B)梯度洗脱,0~70 min,17%ACN;70~100 min,17%→20% ACN;100~110 min,20%→25% ACN;110~140 min,25%→55% ACN;140~150 min,55%→70%ACN。梯度条件二:流动相:乙腈(A)-0.1%磷酸(B)梯度洗脱,0~80min,17%ACN;80~139min,17% →34% ACN;139~159 min,34% →64% ACN;159~170min,64% →80% ACN。梯度条件三:流动相:乙腈(A)-0.1%磷酸(B)梯度洗脱,0~103min,17%ACN;103~142min,17%→24%ACN;142~165min,24%→33%ACN;165~195 min,33%ACN;195~280min,33%→70%ACN。梯度条件四:流动相:乙腈(A)-0.3%磷酸(B)梯度洗脱,0~103 min,17%ACN 103~142min,17%→27%ACN;142~156 min,27%→29%ACN;156~179 min,29%→41%ACN;179~219min,41%→80%CAN。结果梯度条件四下的指纹图谱,色谱图中采集的色谱峰形好,峰数多且分离度良好,基线较平稳,能展现最多的谱图信息,故确定为最终梯度条件,见图2。[align=center][img=,607,284]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091125509322_7749_3255306_3.png!w607x284.jpg[/img][/align][align=center]梯度条件一[/align][align=center][img=,607,287]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091126035685_7140_3255306_3.png!w607x287.jpg[/img][/align][align=center]梯度条件二[/align][align=center][img=,608,287]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091126106612_24_3255306_3.png!w608x287.jpg[/img][/align][align=center]梯度条件三[/align][align=center][img=,690,282]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091126155801_3154_3255306_3.png!w690x282.jpg[/img][/align][align=center]梯度条件四[/align][align=center]图2 不同洗脱条件下银黄颗粒指纹图谱[/align][b]2.1.3 不同流速的选择 [/b]分别考察同一样品供试液,以梯度条件四下的方法,测定其流速在0.9 mLmin[sup]-1[/sup]、 0.8 mLmin[sup]-1[/sup]、 0.7mLmin[sup]-1[/sup]时的分离效果。结果表明,流速在0.9 mLmin[sup]-1[/sup]和0.8mLmin[sup]-1[/sup]时,130min附近两峰分离效果不理想,而0.7 mLmin[sup]-1[/sup]时峰形及分离情况均比较理想。综合考虑,选择0.7 mLmin[sup]-1[/sup]流速。见图3。[align=center][img=,690,283]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091126346021_2490_3255306_3.png!w690x283.jpg[/img][/align][align=center]流速:0.9 mLmin[sup]-1[/sup][/align][align=center][sup][img=,690,264]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091126456661_6012_3255306_3.png!w690x264.jpg[/img][/sup][/align][align=center]流速:0.8 mLmin[sup]-1[/sup][/align][align=center][sup][img=,690,286]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091127029111_5432_3255306_3.png!w690x286.jpg[/img][/sup][/align][align=center]流速:0.7 mLmin[sup]-1[/sup][/align][align=center]图3 不同流速下银黄颗粒指纹图谱[/align][b]2.1.4 测定波长的选择 [/b]对同一银黄颗粒样品供试液在235~295 nm波长范围内,每隔20 nm测定一次,选择最佳吸收波长。其色谱图结果见图4。[align=center][img=,690,285]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091127570951_5526_3255306_3.png!w690x285.jpg[/img][/align][align=center]235 nm[/align][align=center][img=,690,283]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091128103641_8767_3255306_3.png!w690x283.jpg[/img][/align][align=center]255 nm [/align][align=center][img=,690,284]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091128182679_3036_3255306_3.png!w690x284.jpg[/img][/align][align=center]275 nm[/align][align=center][img=,690,236]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091128256647_2872_3255306_3.png!w690x236.jpg[/img][/align][align=center]295 nm[/align][align=center] 图4 不同波长下银黄颗粒指纹图谱[/align]由图4结果可知,在235 nm时,色谱图中峰形佳,各峰间比例协调,基线较平稳,且呈现的峰信息量大。因此,选用235 nm作为测定波长。[b]2.2 不同色谱柱的考察[/b]考虑到银黄颗粒中主要是黄酮类成分,故选用C[sub]18[/sub]柱,对色谱柱进行考察,分别使用VenusilMP C[sub]18[/sub](4.6 mm × 250 mm,5 μm),Venusil MP C[sub]18[/sub](4.6 mm × 250 mm,3 μm),Agela MP S/N.三根色谱柱及其不同组合,在同一梯度条件下分别对同一银黄颗粒供试液进行指纹图谱峰的采集,结果前四根色谱柱分离度相对较差,Venusil MP C[sub]18[/sub](4.6 mm × 250 mm,5 μm)+ Venusil MP C[sub]18[/sub](4.6 mm × 250 mm,3 μm)组合柱分离出的色谱峰较多,峰型较好,对流动相条件进行微调后,进行色谱图的采集。见图5。[align=center][img=,690,236]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091131336001_8004_3255306_3.png!w690x236.jpg[/img][/align][align=center]Agela MP S/N(4.6 mm × 250 mm,3 μm)[/align][align=center][img=,690,236]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091131265708_7298_3255306_3.png!w690x236.jpg[/img][/align][align=center]Agela MP S/N(4.6 mm × 250 mm,3 μm) [/align][align=center][img=,690,233]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091131195130_7680_3255306_3.png!w690x233.jpg[/img][/align][align=center]Venusil MP C[sub]18[/sub](4.6 mm× 250 mm,3 μm) [/align][align=center][img=,690,233]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091131092861_3850_3255306_3.png!w690x233.jpg[/img][/align][align=center]Agela MP S/N(4.6 mm × 250 mm,3 μm)+Venusil MP C[sub]18[/sub](4.6 mm× 250 mm,5 μm) [/align][align=center] [img=,690,285]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091130395070_4225_3255306_3.png!w690x285.jpg[/img][/align][align=center]Venusil MP C[sub]18[/sub](4.6 mm × 250 mm,5 μm)+ Venusil MP C[sub]18[/sub](4.6 mm × 250 mm,3 μm)[/align]图5 不同色谱柱银黄颗粒指纹图谱[b]2.3 方法学考察2.3.1 仪器精密度考察 [/b]取银黄颗粒同一样品供试液,10 μL进样,连续进样 5次,按“4.1”项下的色谱条件进样测定,以葛根素为参照峰,计算共有峰的峰面积和相对保留时间比值。结果显示各共有峰的相对峰面积RSD<3 %,相对保留时间RSD<3%,表明仪器精密度良好。见表1、2。[align=center]表1 银黄颗粒指纹图谱精密度(相对峰面积)[/align][align=center][img=,348,494]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091132223573_3518_3255306_3.png!w348x494.jpg[/img] [/align][align=center]表2 银黄颗粒指纹图谱精密度(相对保留时间)[/align][align=center][img=,352,511]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091132363167_2471_3255306_3.png!w352x511.jpg[/img] [/align][b]2.3.2 重复性试验 2.3.2.1银黄颗粒重复性实验考察[/b]银黄颗粒研细后精密称取细粉1.0 g,称取五份分别置于100 ml 的圆底烧瓶中,精密加入煮沸的蒸馏水100 ml于圆底烧瓶中,称重,加热回流30 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算相对峰面积值和相对保留时间值,结果见表3、4的25个峰的RSD值都接近3%,由此可以得出结论,银黄颗粒的重复性良好。[align=center]表3 银黄颗粒指纹图谱重复性(相对峰面积)[/align][align=center][img=,294,424]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091133158091_6693_3255306_3.png!w294x424.jpg[/img][/align][align=center] 表4 银黄颗粒指纹图谱重复性(相对保留时间)[/align][align=center][img=,301,407]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091133264387_6060_3255306_3.png!w301x407.jpg[/img][/align][b]2.3.2.2黄芩药材重复性实验考察[/b]黄芩药材研细后精密称取细粉0.57 g,称取五份分别置于100 ml 的圆底烧瓶中,精密加入煮沸的蒸馏水50 ml于圆底烧瓶中,称重,加热回流40 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算相对峰面积值和相对保留时间值,结果见表5、6的15个峰的RSD值都接近3 %,由此可以得出结论,黄芩药材的重复性良好。[align=center][b] [/b]表5黄芩药材指纹图谱重复性(相对峰面积)[/align][align=center][img=,521,450]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091134133924_7231_3255306_3.png!w521x450.jpg[/img][/align][align=center]表6 黄芩药材指纹图谱重复性(相对保留时间)[/align][align=center][img=,526,450]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091134223683_8185_3255306_3.png!w526x450.jpg[/img][/align][b]2.3.2.3金银花药材重复性实验考察[/b]金银花药材研细后精密称取细粉0.5 g,称取五份分别置于100 ml 的圆底烧瓶中,精密加入煮沸的蒸馏水100 ml于圆底烧瓶中,称重,加热回流30 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算相对峰面积值和相对保留时间值,结果见表7、8的15个峰的RSD值都接近3%,由此可以得出结论,金银花药材的重复性良好。[align=center] 表7 金银花药材指纹图谱重复性(相对峰面积)[/align][align=center][img=,521,453]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091135202061_4447_3255306_3.png!w521x453.jpg[/img][/align][align=center]表8 金银花药材指纹图谱重复性(相对保留时间)[/align][align=center][img=,520,450]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091135276281_796_3255306_3.png!w520x450.jpg[/img][/align][b]2.4.3 稳定性试验 2.4.3.1银黄颗粒稳定性实验考察[/b]银黄颗粒研细后精密称取细粉1.0 g置于100 ml 的圆底烧瓶中,精密加入煮沸的蒸馏水100 ml于圆底烧瓶中,称重,加热回流30 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算相对峰面积值和相对保留时间值,结果见表9、10的25个峰的RSD值都接近3 %,由此可以得出结论,银黄颗粒的稳定性良好。[align=center]表9 银黄颗粒指纹图谱稳定性(相对峰面积)[/align][align=center][img=,284,411]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091135513432_6898_3255306_3.png!w284x411.jpg[/img] [/align][align=center]表10 银黄颗粒指纹图谱稳定性(相对保留时间)[/align][align=center][img=,285,423]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091135598981_6279_3255306_3.png!w285x423.jpg[/img][/align] [b]2.4.3.2黄芩药材稳定性实验考察[/b]黄芩药材研细后精密称取细粉0.57 g置于50 ml 的圆底烧瓶中,精密加入煮沸的蒸馏水100 ml于圆底烧瓶中,称重,加热回流40 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算相对峰面积值和相对保留时间值,结果见表11、12的25个峰的RSD值都接近3 %,由此可以得出结论,黄芩药材的稳定性良好。[align=center] 表11 黄芩药材指纹图谱稳定性(相对峰面积)[/align][align=center][img=,534,451]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091136295090_8710_3255306_3.png!w534x451.jpg[/img][/align][align=center] 表12 黄芩药材指纹图谱稳定性(相对保留时间)[/align][align=center][img=,468,403]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091136437515_7524_3255306_3.png!w468x403.jpg[/img][/align][b]2.4.3.3金银花药材稳定性实验考察[/b]金银花药材研细后精密称取细粉1.0 g置于100 ml 的圆底烧瓶中,精密加入煮沸的蒸馏水100 ml于圆底烧瓶中,称重,加热回流30 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算相对峰面积值和相对保留时间值,结果见表13、表14,25个峰的RSD值都接近3 %,由此可以得出结论,金银花药材的稳定性良好。[align=center]表13 金银花药材指纹图谱稳定性(相对峰面积)[/align][align=center][img=,452,406]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091137142831_7122_3255306_3.png!w452x406.jpg[/img][/align][align=center]表14 金银花药材指纹图谱稳定性(相对保留时间)[/align][align=center][img=,441,402]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091137227371_5231_3255306_3.png!w441x402.jpg[/img][/align][b]2.5 样品共有峰的确定[/b]对10 批不同厂家的银黄颗粒及黄芩和金银花药材供试液进行分析,采集指纹图谱,并以葛根素作为参考峰,银黄颗粒选取标定了22个共有峰,见图6。黄芩药材选取标定了22个共有峰,见图7。金银花药材选取标定了21个共有峰,见图8。[align=center][img=,690,265]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091137498881_3854_3255306_3.png!w690x265.jpg[/img][/align][align=center]图6 10 批次的银黄颗粒共有特征峰[/align][align=center][img=,690,259]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091138017531_1112_3255306_3.png!w690x259.jpg[/img][/align][align=center]图7 10 批次的黄芩共有特征峰[/align][align=center][img=,690,247]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091138139735_5366_3255306_3.png!w690x247.jpg[/img][/align][align=center]图8 10 批次金银花药材的共有特征峰[/align][b]三、结果与分析[/b]本研究介绍了银黄颗粒及其原料药黄芩和金银花的指纹图谱的建立方法,包括供试品溶液的制备、高效液相色谱仪测定及对数据和图谱的处理,以及由该方法制备得到的相应指纹图谱。在测定的不同厂家 10 批次样品的色谱图中,选择90 %以上批次样品均有的色谱峰为共有峰,银黄颗粒。黄芩药材、金银花药材分别确定了22,22,21 个共有峰。[b]四、讨论与结论[/b]本研究的指纹图谱构建方法操作简单,稳定可靠,精密度高,分离度好,指纹图谱的稳定性和重现性较好,且信息量大,采用指纹图谱找出不同产地,不同厂家的同一药材的共有峰为质量控制手段,既避免了因只测定一、两个化学成分而判定制剂整体质量的片面性,又减少了为质量达标而人为处理的可能性,通过对多个批次的样品进行系统分析,能更加全面、科学评价银黄颗粒的质量,从而使产品的质量和疗效得到保证。参考文献王亚丹,杨建波,戴忠,等.中药金银花的研究进展.药物分析杂志,2014,34( 11):1928-1935 中国药典.一部.2015:1498 王彩芳,张楠,黄龙,等. HPLC法测定不同厂家银黄颗粒中黄芩苷的含量.医药论坛杂志,2006,27 (24):27-28 王彩芳,黄龙,程茜,等.高效液相色谱法测定不同厂家银黄颗粒中绿原酸的含量.时珍国医国药,2007,18(5):1143-1144黄雄,黄嬛,王峻,等.银黄颗粒的HPLC特征图谱分析.药物分析杂志,2009,29(8):1320-1323 肖小河,王永炎.从热力学角度审视和研究中医药.国际生物信息与中医药论丛.新加坡:新加坡医药卫生出版社,2004:74 贺福元,罗杰英,刘文龙,等.中药谱效学研究方向方法初探.世界科学技术-中医药现代化,2004,6(6):44-50 赵渤年,于宗渊,丁晓彦,等.黄芩质量评价谱-效相关模式的研究.中草药,2011.42(2):380-383 高燕,赵渤年,于宗渊等.金银花抗流感病毒毒谱-效相关质量评价模式的研究.中华中医药杂志,2013.28(12):3508-3511 Ke Li, Wei Cheng, Xiao-Jian Liu,hu-Bin Li, En-Guang Hou, Yan Gao, Liang Wang, Qing Liu, Bo-Nian Zhao, Zong-Yuan Yu, Mathematical Modelling for the Quality Evaluation of Baikal Skullcap Root, Applied Mechanics and Materials, 2011 王荣梅,徐丽华,林永强.HPLC法同时测定银黄含片中6个咖啡酰奎宁酸类成分的含量.药物分析杂志,2012,32(1):57-60 高苏亚,范涛,王黎等.红外光谱技术结合化学计量学方法在中药研究中的应用.应用化工,2012,41(2):324-328 王鹏,王振国,薛付忠等.基于支持向量机法的中药性状与药性相关性研究. 江西中医药,2012,43(355):65-68 Cifford MN, Johnston KL, Knight S et al. Hierarchical scheme for [url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url] identification of chlorogenic acids.J Agric Food Chem,2003 51(10):2900-2910张倩,张加余,隋丞琳,等. HPLC-DAD-ESI-MS/MS研究金银花水提工艺中绿原酸类成分的变化规律.中国中药杂志,2012 37(23):3564-3567 沈红,段金廒,钱大玮,等.黄芩及复方野马追胶囊中黄酮类成分的[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS分析.药物分析杂志,2009 29(9):1425-1429 赵胜男,李守拙.黄芩药材中黄酮类成分的HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]研究.承德医学院学报2012 29(4):345-347 Chkoshi E, Nagashima T, Sato H, et al. Simple preparation of baicalin from Scutellariae Rdixi. J Chromatogr A,2009 1216(11): 2192 -2194高燕,吕凌,王亮,等.银黄颗粒HPLC指纹图谱与模式识别分析.中华中医药杂志,2017,32(09):4238-4242 丁晓彦,刘青,李岩,等.丹参脂溶性成分的HPLC指纹图谱及模式识别研究.中华中医药杂志,2016,3(6):2254-2256
次黄嘌呤苷有腺嘌呤的结构,有共轭,为何在紫外下不显色啊?它有多个醇,如果紫外不显色,那么用何方法使其显色啊?
藤黄【英文名】Gamboge【别名】玉黄、月黄。【来源】药材基源:为藤黄科植物藤黄的树脂。拉丁植物动物矿物名:Garcinia hanburyi Hook.f.采收和储藏:在开花之前,在离地3m处将茎干的皮部作螺旋状的割伤,伤口内插一竹简,盛受流出的树脂,加热蒸干,用刀刮下,即可。【原形态】藤黄 常绿乔木,高约15-18m。小枝四棱形。单叶对生,几无柄;叶片薄革质,阔披针形,长9-13cm,先端尖,基部楔形,全缘或微波状。花单生或为聚啊伞花序;两性与单性花黄存;花绿白色,无梗;萼片5,花瓣5;雄花通常2-3朵簇生,雄蕊多数,花丝短,花药1室,横裂;雌花具退化雄蕊12枚,其基部合生而环绕子房周围,子房上位,平滑无毛,柱头盾形,为不整齐之裂片或瘤块,4室。浆果,径约2cm。种子4颗。花期11月,果熟期次年2-3月。【生境分布】生态环境:原产柬埔寨及马来西亚,印度、泰国、越南亦产。资源分布:现我国广东、广西有引种栽培。【栽培】野生【性状】性状鉴别 树脂为不规则的圆柱形或块状,棕红色或橙色,外被黄绿色粉霜,可见纵条纹。质硬脆,较易击碎,破面有空隙,具蓝褐色略带蜡样光泽。味辛,有毒。以半透明、色红黄者为佳。【化学成份】藤黄树含藤黄酸(gambogic acid),别藤黄酸(allogambogic acid),新藤黄酸(neogambogic acid)。【药理作用】1.抗菌作用:其种子衣中的色素--藤黄宁对金黄色葡萄球菌有抑制作用,体外的有效浓度为1∶10000;对若干真菌、草分支杆菌、人型结核杆菌效力很豹,对大肠杆菌亦无效闭。新藤黄宁也有抗金黄色葡韵球菌的作用。异构体(异藤黄宁及异新藤黄宁)的抗原虫作用较其母体有效(藤黄宁或新藤黄宁通过肠管时可异构化)。藤黄索在体外对非致病性原虫有抑制作用,特别是β-及γ-藤黄素效力较强。抗原虫与抗菌作用,并不平行。α1-及γ-藤黄素在各方面(如抑制革兰氏阳性细菌之能力、对小鼠人工感染葡萄球菌的保护作用、在血清或金属离干存在时的反应、对热及酸碱度的稳定性等)皆与α2-及β-藤黄素相似。2.其他作用与毒性:β-及α1-藤黄索在超过治疗量时可引起小鼠腹泻(β-藤黄索致泻力更强)。对小鼠的急性毒性(半数致死量,mg/kg)为:α1-及γ-藤黄素皮下注射均为277;腹腔注射分别为87.1及77.18;静脉注射分别为108.4及108,这些数值与α2-及β-藤黄素的毒性栖差甚微。【炮制】制藤黄:1.先用豆腐一大块,平铺于盘内,中间挖一不透底的槽,将藤黄放人,再用豆腐盖严,置于笼屉内,放入锅中,将此锅再坐于大锅内,隔水加热,蒸至藤黄溶化,取出,冷却凝固,去豆腐晒干。2.先将藤黄放入磁罐内,加入比藤黄多10倍量的鲜荷叶煎汁,将罐放入锅中,隔水加热40-60分钟,至罐内溶液呈紫红色时,倒入铜锅内再煎,浓缩成糊状,晒干。(每藤黄斤约用荷 叶半斤煎法,去渣)3.将藤黄加入鲜山羊血中,置铜锅内,加水同煮5-6小时,去山羊血晾干。(每藤黄1斤,用鲜山羊血半斤)【性味】酸;涩;凉;有毒【功能主治】消肿;攻毒;止血;杀虫;祛腐剑疮。主痈疽肿毒;溃疡;湿疮;肿癣;顽癣;跌打肿痛;创伤出血及烫伤【用法用量】外用:适量,研末调敷、磨汁涂或熬督涂。内服:0.03-0.06g,入丸剂
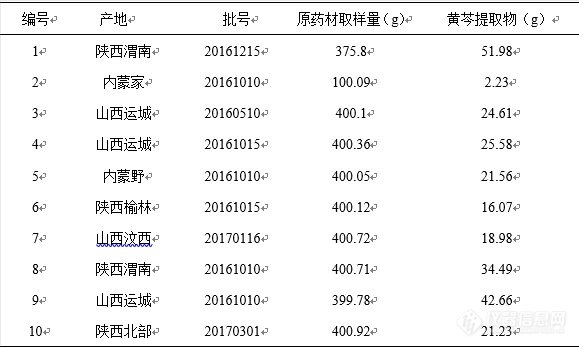
[b][/b][align=center][b]银黄颗粒质量标志物评价研究[/b][/align][b] 摘要[/b]目的:以黄芩药材、金银花药材、黄芩提取物、金银花提取物、银黄制剂为研究对象,考察并优化了样本在前处理环节的回流提取溶剂的体积、回流提取时间和提取溶剂的温度等。方法:采用高效液相色谱法,色谱柱为Venusil MP C[sub]18[/sub](4.6mm × 250 mm,5μm), Venusil MP C[sub]18[/sub](4.6mm × 250 mm,3μm)和 Agela MP S/N。以乙腈一0.3% 磷酸溶液为流动相进行梯度洗脱,流速为0.7 mLmin[sup]-1[/sup],检测波长为235 nm。结果和结论:通过各方面的考察,确定了银黄颗粒、黄芩药材和金银花药材在样品前处理环节的工艺优化参数,为银黄颗粒质量标志物研究提供借鉴指导。结论: 建立的提取方法稳定、可靠,有效成分达到最大提取效率,可用于银黄颗粒溯源检测的质量控制和综合评价。[b] 关键词:[/b]银黄颗粒;质量标志物;高效液相;黄芩;金银花[b] [/b][align=center][b][color=#333333]Evaluation of Quality Markers of Yinhuang Granules[/color][/b][/align]Objective: To investigate and optimize the volume ofreflux solvent, reflux extraction time and temperature of extraction solvent inthe pretreatment of samples, taking Scutellaria baicalensis, honeysuckle,Scutellaria baicalensis extract, honeysuckle extract and Yinhuang preparationas research objects. METHODS: High performance liquid chromatography was usedwith Venusil MP C18 (4.6 mm *250 mm, 5 micron), Venusil MP C18 (4.6 mm *250 mm,3 micron) and Agela MP S/N as chromatographic columns. The gradient elution was carried out with acetonitrile-0.3% phosphoric acid solution as mobile phase.The flow rate was 0.7 mL/min and the detection wavelength was 235nm. RESULTS AND CONCLUSION: The process optimization parameters of Yinhuanggranules, Radix Scutellariae baicalensis and Flos Lonicerae in samplepretreatment were determined through various aspects of investigation, whichcould provide reference and guidance for the study of quality markers ofYinhuang granules. CONCLUSION: The established extraction method is stable andreliable, and the effective ingredients can reach the maximum extractionefficiency. It can be used for quality control and comprehensive evaluation oftraceability detection of Yinhuang granules.Keywords: Yinhuang granules quality markers high performance liquidchromatography Scutellaria baicalensis honeysuckle[b]一、前言[/b] 银黄颗粒组方由金银花和黄芩构成,具有清热疏风、利咽解毒的功效,用于外感风热、肺胃热盛所致的咽干、咽痛、喉核肿大、口渴、发热急慢性扁桃体炎、急慢性咽炎、上呼吸道感染等症。该复方原料金银花为忍冬科植物忍冬的干燥花蕾或带初开的花,主产于山东、河南和河北等地。该复方原料黄芩为唇形科[url=https://baike.baidu.com/item/%E9%BB%84%E8%8A%A9%E5%B1%9E][color=windowtext]黄芩属[/color][/url]多年生草本植物,产于河北,河南,陕西,山西,山东等地。黄芩提取物的主要活性成分为黄芩苷、汉黄芩苷、黄芩素及汉黄芩素,金银花提取物是从金银花中提取的有机酸类活性成分。该制剂及其原料药成分复杂,生产厂家及产地众多,样品存在差异。中药质量标志物(Q-marker)已广泛应用于中成药的质量评价与控制。近年来越来越多的研究使用不同种类的分析仪器,密切联系中药有效性-物质基础- Q-marker研究,建立了丰富的中成药系统质量控制方法,为探讨建立中药全过程质量控制及质量溯源体系奠定了基础。[b]二、材料与方法1仪器与试剂、试药1.1仪器[/b] Waters e2695高效液相色谱仪(美国Waters公司),Waters 2998紫外检测器(美国Waters公司),Waters Empower色谱工作站(美国Waters公司);AGBP210S电子天平(Sartorius公司);MILLIPORE纯水机(MILLIPORE公司);高速万能粉碎机(北京市永光明医疗仪器有限公司,FW-80型);SB4200DTS超声波双频清洗机(宁波新芝生物科技股份有限公司);KDM-A控温电热套(金坛市医疗仪器厂);Venusil MP C[sub]18[/sub](4.6 mm × 250 mm,5 μm)和Venusil MP C[sub]18[/sub](4.6 mm × 250 mm,3 μm)。[b]1.2 试剂与试药[/b] 乙腈(上海星可高纯溶剂有限公司,色谱纯);甲醇(天津市科密欧化学试剂有限公司,色谱纯);其余试剂均为分析纯,水为超纯水。对照品来源:葛根素(批号:110752-200912)购自中国食品药品检定研究院。2样品的收集与前处理[b]2.1样品的收集[/b] 本研究从全国范围内收集黄芩、金银花药材各50批,分别制备相应的黄芩提取物和金银花提取物各50批,并制备银黄颗粒样品至少50批。(共计不少于250批样品)。[b]2.2黄芩、金银花药材的处理[/b] 对收集到的各批样品,均按照《中国药典》2015年版(第四部)药材取样法,四分法取样,1/4留样,剩余药材粉碎,使粉末分别过60目和20目筛,并按比例称重。所有黄芩、金银花药材样品均装袋密封,保存于冰柜(-20℃)中,备用。[b]2.3黄芩提取物的制备[/b] 取黄芩约100 g,置于1000 ml容量瓶中,加热回流两次,每次2 h,将滤液置于烧杯中浓缩至200 ml,用2 mol/L的盐酸调PH至1.0-2.0,80 ℃保温1 h,静置24 h.减压抽滤,沉淀加一倍量水混匀,用40 %氢氧化钠调节PH至7.0,加等量乙醇,搅拌溶解,滤过,滤液用2 mol/L的盐酸调PH 1.0-2.0, 60 ℃保温1 h,静置24 h,滤过,沉淀物加水洗至PH 5.0,95%乙醇洗至中性,挥尽乙醇,干燥,即得。[align=center]表1 黄芩提取物的提取[/align][align=center][img=,579,348]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091021374879_6392_3255306_3.png!w579x348.jpg[/img][/align][b]2.4金银花提取物的制备[/b] 称取金银花50.05 g置于圆底烧瓶中,加纯水回流提取三次,第一次8倍量水400 ml回流提取1 h,滤过,残渣加8 倍量水400 ml二次回流提取1 h,滤过,合并煎液,残渣加6倍量水300 ml,合并煎液,浓缩成浸膏,加浸膏量50%的淀粉混匀,置于烘箱中,60 ℃干燥,粉碎成粉,即得。[align=center]表2 金银花提取物的提取[/align][align=center] [img=,552,347]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091021550706_5584_3255306_3.png!w552x347.jpg[/img][/align][b]3供试品溶液方法考察的制备3.1供试品溶液制备方法考察3.1.1提取溶剂的选择[/b] 根据银黄颗粒的服用说明,该样品采用水为溶媒制备供试品溶液,由于临床应用中黄芩,金银花多采用水煎内服的用法,因此研究中以水作为提取溶媒,制备样品溶液。[b]3.1.2内标物溶液的制备[/b] 经查阅大量文献,本实验适用的内标物为葛根素。取葛根素对照品适量精密称定,以水超声溶解并定容制成浓度为30 μg*mL[sup]-1[/sup]的内标溶液[b]3.2银黄颗粒供试液制备方法考察3.2.1银黄颗粒不同料液比的考察[/b] 银黄颗粒研细后精密称取细粉1.0 g,称四份,置于100 ml或250 ml的圆底烧瓶中,分别精密加入煮沸的蒸馏水25 ml、50 ml、100 ml、150 ml于圆底烧瓶中,称重,加热回流30 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后0.5 ml等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表3、图1。[align=center]表3 银黄颗粒不同料液比单位质量色谱峰面积比较[/align][align=center] [img=,289,425]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091023281381_1955_3255306_3.png!w289x425.jpg[/img][/align][align=center]图1 银黄颗粒不同料液比单位质量色谱峰面积比较[/align][align=center][img=,289,123]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091023402582_6283_3255306_3.png!w289x123.jpg[/img][/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取体积为100 ml时值最大,最终选择回流提取体积为100 ml。[b]3.2.2银黄颗粒不同提取时间的考察[/b] 银黄颗粒研细后精密称取细粉1.0 g,称四份分别置于100 ml 的圆底烧瓶中,精密加入煮沸的蒸馏水25 ml于圆底烧瓶中,称重,分别加热回流20 min、30 min、40 min、60 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后0.5 ml等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表4、图2。[align=center]表4 银黄颗粒不同提取时间单位质量色谱峰面积比较[/align][align=center] [img=,292,421]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091024007921_8570_3255306_3.png!w292x421.jpg[/img][/align][align=center][img=,577,251]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091024513811_6890_3255306_3.png!w577x251.jpg[/img][/align][align=center]图2 银黄颗粒不同提取时间单位质量色谱峰面积比较[/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取时间为30 min时值最大,最终选择回流提取时间为30 min。[b]3.2.3银黄颗粒冷热水的考察[/b] 银黄颗粒研细后精密称取细粉1.0 g,称两份分别置于250 ml的圆底烧瓶中,第一份精密加入煮沸的蒸馏水100 ml于圆底烧瓶中,第二份精密加入100 ml常温蒸馏水,称重,加热回流30 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表5、图3。[align=center]表5 银黄颗粒冷热水单位质量色谱峰面积比较[/align][align=center][img=,287,427]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091025490101_4911_3255306_3.png!w287x427.jpg[/img][/align][align=center][img=,574,270]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091026003331_9248_3255306_3.png!w574x270.jpg[/img][/align][align=center]图3 银黄颗粒冷热水单位质量色谱峰面积比较[/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取溶剂为热水时值最大,最终选择提取溶剂为热水。[b]3.3黄芩药材供试液制备方法考察 3.3.1黄芩药材不同料液比的考察[/b] 按比例称取2 0~60目和过60目筛的黄芩药材粉末,共0.57 g,称取三份,置于100 ml或250 ml的圆底烧瓶中,分别精密加入煮沸的蒸馏水25 ml、50 ml、100 ml于圆底烧瓶中,称重,加热回流30 min ,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表6、图4。[align=center]表6 黄芩药材不同料液比单位质量色谱峰面积比较[/align][align=center][img=,291,425]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091026251557_1424_3255306_3.png!w291x425.jpg[/img][/align][align=center][img=,567,260]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091026352391_8450_3255306_3.png!w567x260.jpg[/img][/align][align=center]图4 黄芩药材不同料液比单位质量色谱峰面积比较[/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取体积为50ml时值最大,最终选择50ml为最佳提取容积。[b]3.3.2黄芩药材不同提取时间的考察[/b] 按比例称取2 0~60目和过60目筛的黄芩药材粉末,共0.57 g,称取四份,分别置于100 ml 的圆底烧瓶中,精密加入煮沸的蒸馏水25 ml于圆底烧瓶中,称重,分别加热回流20 min、30 min、40 min、60 min ,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表7、图5。[align=center]表7 黄芩药材不同提取时间单位质量色谱峰面积比较[/align][align=center][img=,289,424]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091027053867_9448_3255306_3.png!w289x424.jpg[/img][/align][align=center][img=,605,240]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091027125561_9333_3255306_3.png!w605x240.jpg[/img][/align][align=center]图5 黄芩药材不同提取时间单位质量色谱峰面积比较[/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取时间为40 min时值最大,最终选择40 min为最佳提取时间。[b]3.3.3黄芩药材冷热水提取的考察[/b] 按比例称取2 0~60目和过60目筛的黄芩药材粉末,共0.57 g,称取二份,置于100 ml的圆底烧瓶中,第一份精密加入煮沸的蒸馏水50 ml于圆底烧瓶中,第二份精密加入50 ml常温蒸馏水,分别称重,加热回流40 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表8、图6.[align=center]表8 黄芩药材冷热水单位质量色谱峰面积比较[/align][align=center][img=,287,424]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091027401011_8981_3255306_3.png!w287x424.jpg[/img][/align][align=center][img=,619,293]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091027478961_1794_3255306_3.png!w619x293.jpg[/img][/align][align=center][/align][align=center]图6 黄芩药材冷热水单位质量色谱峰面积比较[/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取溶剂为热水时值最大,最终选择热水提取是最佳的。[b]3.4金银花药材供试液制备方法考察3.4.1金银花药材不同料液比的考察[/b] 按比例称取2 0~60目和过60目筛的金银花药材粉末,共0.5 g,称取三份,置于100 ml或250 ml的圆底烧瓶中,分别精密加入煮沸的蒸馏水50 ml、100 ml、200 ml于圆底烧瓶中,称重,加热回流30 min,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表9、图7。[align=center]表9 金银花药材不同料液比单位质量色谱峰面积比较[/align][align=center][img=,358,511]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091031346401_7706_3255306_3.png!w358x511.jpg[/img][/align][align=center][img=,636,256]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091031349941_1562_3255306_3.png!w636x256.jpg[/img][/align][align=center]图7 金银花药材不同料液比单位质量色谱峰面积比较[/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取容积为100 ml,200 ml时值较大,100 ml与200 ml比较,两者的成分含量差别不大,所以选择100 ml提取较好。[b]3.4.2金银花药材不同提取时间的考察[/b] 按比例称取2 0~60目和过60目筛的黄芩药材粉末,共0.5 g,称取四份,分别置于250 ml 的圆底烧瓶中,精密加入煮沸的蒸馏水100 ml于圆底烧瓶中,称重,分别加热回流20 min、30 min、40 min、60 min ,回流后放冷,补重,过滤,取续滤液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液,注入高效液相色谱仪,按照既定方法采集色谱指纹图谱,计算各共有峰的单位质量的峰面积值,比较其差异,结果见表10、图8。[align=center]表10 金银花药材不同提取时间单位质量色谱峰面积比较[/align][align=center][img=,290,424]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091030005792_6136_3255306_3.png!w290x424.jpg[/img][/align][align=center][img=,555,215]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091030053727_8053_3255306_3.png!w555x215.jpg[/img][/align][align=center][/align][align=center]图 9 金银花药材冷热水提取单位质量色谱峰面积比较[/align] 由上述表图分析:各主要共有峰的单位质量峰面积在提取溶剂为热水时值最大,最终选择热水提取最佳。[b]3.5 黄芩提取物,金银花提取物供试液制备方法考察[/b] 通过实验得知黄芩提取物,金银花提取物供试液制备方法考察同银黄颗粒供试液制备方法考察一致。[b]3.6 含葛根素内标的银黄颗粒、黄芩药材、金银花药材、黄芩提取物、金银花提取物供试液配制方法的确定3.6.1含葛根素内标银黄颗粒供试品溶液的配制[/b] 银黄颗粒研细后精密称取细粉1.0 g,置于250 ml圆底烧瓶内,精密加入煮沸的蒸馏水100 ml,称重,加热回流30 min(提前打开电热套预热),放冷,补重,过滤,取续滤液。另取葛根素对照品适量精密称定,以水超声溶解并定容制成浓度为30μg• mL-1的内标溶液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液。[b]3.6.2含葛根素内标黄芩药材供试品溶液的配制[/b] 从冰柜中取出黄芩药材粉末,放置室温。采用四分法取样,按比例称取2 0~60目和过60目筛的黄芩药材粉末,共0.57 g,置于100 ml圆底烧瓶中,精密加入煮沸的蒸馏水50 ml,称重,加热回流40 min(提前打开电热套预热),放冷,补重,过滤,取续滤液。另取葛根素对照品适量精密称定,以水超声溶解并定容制成浓度为30 μg• mL-1的内标溶液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液。[b]3.6.3含葛根素内标金银花药材供试品溶液的配制[/b] 从冰柜中取出金银花药材粉末,放置室温。采用四分法取样,按比例称取2 0~60目和过60目筛的黄芩药材粉末,共0.25 g,置于100 ml圆底烧瓶中,精密加入煮沸的蒸馏水50 ml,称重,加热回流30 min(提前打开电热套预热),放冷,补重,过滤,取续滤液。另取葛根素对照品适量精密称定,以水超声溶解并定容制成浓度为30 μg• mL-1的内标溶液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液。[b]3.6.4含葛根素内标金银花提取物供试品溶液的配制[/b] 从冰柜中取出金银花提取物粉末,按比例精密称取0.2 g,置于250 ml圆底烧瓶中,精密加入煮沸的蒸馏水100 ml,称重,加热回流30min(提前打开电热套预热),放冷,补重,过滤,取续滤液。另取葛根素对照品适量精密称定,以水超声溶解并定容制成浓度为30 μg• mL-1的内标溶液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液。[b]3.6.5含葛根素内标黄芩提取物供试品溶液的配制[/b] 从冰柜中取出黄芩提取物粉末,按精密称取0.04 g,置于250 ml圆底烧瓶中,精密加入煮沸的蒸馏水100 ml,称重,加热回流30 min(提前打开电热套预热),放冷,补重,过滤,取续滤液。另取葛根素对照品适量精密称定,以水超声溶解并定容制成浓度为30 μg• mL-1的内标溶液。将样品溶液与内标溶液经0.45 μm微孔滤膜滤过后等体积混匀,作为供试品溶液。[b]三、结论[/b] 实验考察了银黄颗粒在样本处理环节的回流提取溶剂的体积、回流提取时间和提取溶剂的温度等。最终选择回流提取体积为100 ml,选择回流提取时间为30 min,选择提取溶剂为热水。考察了黄芩药材在样本处理环节的回流提取溶剂的体积、回流提取时间和提取溶剂的温度等。最终选择50ml为最佳提取容积,选择40 min为最佳提取时间,选择热水提取是最佳的。考察了金银花药材在样本处理环节的回流提取溶剂的体积、回流提取时间和提取溶剂的温度等。最终选择100 ml体积提取溶剂,选择30 min提取是最佳的,选择热水提取最佳。本实验还确定了含葛根素内标的银黄颗粒、黄芩药材、金银花药材、黄芩提取物、金银花提取物供试液配制方法。[align=left][b]参考文献[/b][/align] 王亚丹,杨建波,戴忠,等.中药金银花的研究进展.药物分析杂志,2014,34(11):1928-1935 中国药典.一部.2015:1498 王彩芳,张楠,黄龙,等. HPLC法测定不同厂家银黄颗粒中黄芩苷的含量.医药论坛杂志,2006,27(24):27-28 王彩芳,黄龙,程茜,等.高效液相色谱法测定不同厂家银黄颗粒中绿原酸的含量.时珍国医国药,2007,18(5):1143-1144黄雄,黄嬛,王峻,等.银黄颗粒的HPLC特征图谱分析.药物分析杂志,2009,29(8):1320-1323 肖小河,王永炎.从热力学角度审视和研究中医药.国际生物信息与中医药论丛.新加坡:新加坡医药卫生出版社,2004:74 贺福元,罗杰英,刘文龙,等.中药谱效学研究方向方法初探.世界科学技术-中医药现代化,2004,6(6):44-50 赵渤年,于宗渊,丁晓彦,等.黄芩质量评价谱-效相关模式的研究.中草药,2011.42(2):380-383 高燕,赵渤年,于宗渊等.金银花抗流感病毒毒谱-效相关质量评价模式的研究.中华中医药杂志,2013.28(12):3508-3511 Ke Li, Wei Cheng, Xiao-Jian Liu, hu-Bin Li, En-Guang Hou, Yan Gao, Liang Wang, Qing Liu, Bo-Nian Zhao, Zong-Yuan Yu, Mathematical Modelling for the Quality Evaluation of BaikalSkullcap Root, Applied Mechanics and Materials, 2011 王荣梅,徐丽华,林永强.HPLC法同时测定银黄含片中6个咖啡酰奎宁酸类成分的含量.药物分析杂志,2012,32(1):57-60 高苏亚,范涛,王黎等.红外光谱技术结合化学计量学方法在中药研究中的应用.应用化工,2012,41(2):324-328 王鹏,王振国,薛付忠等.基于支持向量机法的中药性状与药性相关性研究. 江西中医药,2012,43(355):65-68 Cifford MN, Johnston KL, Knight S et al. Hierarchical scheme for [url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url] identification ofchlorogenic acids.J Agric Food Chem,2003 51(10):2900-2910张倩,张加余,隋丞琳,等. HPLC-DAD-ESI-MS/MS研究金银花水提工艺中绿原酸类成分的变化规律.中国中药杂志,2012 37(23):3564-3567 沈红,段金廒,钱大玮,等.黄芩及复方野马追胶囊中黄酮类成分的[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS分析.药物分析杂志,2009 29(9):1425-1429 赵胜男,李守拙.黄芩药材中黄酮类成分的HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]研究.承德医学院学报2012 29(4):345-347 Chkoshi E, Nagashima T, Sato H, et al. Simple preparation ofbaicalin from Scutellariae Rdixi. JChromatogr A,2009 1216(11): 2192 -2194高燕,吕凌,王亮,等.银黄颗粒HPLC指纹图谱与模式识别分析.中华中医药杂志,2017,32(09):4238-4242 丁晓彦,刘青,李岩,等.丹参脂溶性成分的HPLC指纹图谱及模式识别研究.中华中医药杂志,2016,3(6):2254-2256
黄原胶又称黄胶、汉生胶,由糖类经黄单胞杆菌发酵,产生的胞外微生物多塘。黄原胶性能优越,是目前世界上生产规模大且用途极为广泛的食用胶/食品胶/亲水胶体,特别是饮料等液状食品中应用极其广泛。但黄原胶也有缺点,比如一般的黄原胶产品在氯化钾中具有较高的粘度,却在淡水中的粘度较低,这样就造成在淡水体系中,要想达到预期的增稠效果就需要添加较多的黄原胶,导致使用黄原胶的厂家生产成本增加,最终影响黄原胶的巿场销售。为了解决黄原胶在淡水中粘度较低的问题,一种提高黄原胶在淡水中粘度的技术应运而生。这种技术能使黄原胶在淡水中的粘度提高了200cp以上,且不影响其悬浮稳定能力,是一种比较理想的淡水体系增稠稳定剂。具体操作步骤如下1、在黄原胶溶液中加入乙醇,要求溶液中乙醇的浓度体积比在60%,搅拌30-60分钟 2、将步骤1所得溶液搅拌后进行固液分离,提取黄原胶 3、将固液分离得到的黄原胶固体加入到乙醇中,控制溶液中乙醇浓度的体积比在75%,混合搅拌30-60分钟 4、再将步骤3的溶液进行固液分离,再次提取黄原胶 5、将步骤4所得黄原胶固体进行干燥,干燥温度保持在70℃6、将干燥后的固体黄原胶进行粉碎,按黄原胶重量的1-3%添加丙酮酸钙混合均匀,包装,即得在淡水中粘度高的黄原胶。
在超市买的干黄花菜,昨天用水泡了一天,水变黄了,碗底居然还有黄色沉淀,难道是硫磺漂白过的吗,泡出的是硫磺?那哪敢再吃这个菜了呀!还请各位多多指教!