看到过有人用NMR跟踪一个比较慢的反应的动力学,但如果反应速率很快,如加入催化剂后即发生反应,还可以用这样的方法跟踪反应么?谢谢!
紫外/可见光度分析用于反应动力学研究,是[url=http://www.mai17.com/class/guangduji.htm][color=#839432]光度计[/color][/url]的另一大类重要用途,它可以得到反应过程的一些重要信息,一般常用的动力学分析方法有以下两类: (1)一定波长下的吸光度对时间的动力学测定,可以从仪器自动画出的曲线上看到反应快慢,如果将曲线变换成导数动力学曲线,可以推测反应进程中的反应速率变化规律,如果吸光度为几种物质的A加和,可以通过数学解析得到单一物质的速率变化规律,恒定波长的动力学测定可以同时测定若干个波长的动力学曲线; (2)按一定时间间隔进行光谱扫描,可得到一组光谱曲线,根据不同时间的光谱曲线变化,不但能发现一定波长下的吸光度变化规律,还能发现最大吸收波长的移动(如果有的话),能发现新的吸光物质的生成及生成速率,从光谱扫描-时间曲线组里可以得到任何指定波长下的吸光度-时间的动力学曲线。 因此,紫外/[url=http://www.mai17.com/class/guangduji.htm][color=#839432]可见光度分析[/color][/url]用于反应动力学研究,这是色谱分析所不能代替的。并且,紫外/可见光度分析中的光谱信息与物质内部结构的关系(包括根据有机组成推算摩尔吸光系数的经验公式)远比色谱分析有用得多,就结构分析而言,只用色谱峰的保留时间来判断物质种类和结构是比较“粗糙”的,理论研究意义相对较小。色谱分析不可能代替紫外/可见光度分析。

请教下各位高手,我要做一种未知高聚物的反应动力学分析,DSC程序升温速率和升至什么温度该怎么设定啊,或者是可以参考什么标准来确定吗?
生化反应动力学与反应器 一本很不错的书 理论与实际接合
在变换升温速率测反应动力学时,是否要求每次放入的试样量是一样的啊?先谢谢了!
动力学分光光度法是利用反应速率与反应物、反应产物或催化剂的浓度之间的定量关系,通过测量与反应速率成比率关系的吸光度,来定量样品溶液中待测组分浓度. 出差前给大家先提供几个话题,先讨论着,哈哈,俺两星期后回来.
动力学分光光度法(kinetic spectrophotometry)是利用反应速率与反应物,反应产物或催化剂的浓度之间的定量关系,通过测量与反应速率成比率关系的吸光度,来定量样品溶液中待测组分的浓度。 这种方法要选择一个反应速率与待测组分浓度相关的指示反应,且要求这个指标反应的反应物与产物的吸收光谱不同,反应速率适中,测量吸光度的瞬间待测组分浓度不变等。1 动力学分光光度法定量基础令某以基本反应如下:K为催化剂M+N P+Q在其他条件固定时,则反应速率方程为:=k (1)反应初期,如控制M和N浓度较大,则基本反应速率主要决定微量催化剂k的浓度。=k1 (2)积分得 = k1 t (3)根据朗伯-比尔定律=A/εL,则(3)式变为A= k1εLt= k2t (4)其中 k2= k1εL按(4)式,便可通过测得产物P或Q的吸光度A,对催化剂k浓度定量。2 测量方法2.1在t时刻,终止基本反应,然后测定反应产物吸光度A,则A= k2t= k3 (5)绘制A-标准曲线,通过测量样品溶液A后,在标准曲线上求浓度。2.2测定样品溶液的吸光度A达到某以预定值所需时间,则= = k4 [/su
1 米氏方程(Michaelis-Menten方程)米氏方程是酶促反应动力学最重要的一个数学表达式,它定量的描述了酶促反应的速率与底物浓度之间的关系。典型的酶促反应如下式所示:E+S=E-S=P+E其中k1, k2, k3分别代表相关反应的速率常数。酶促反应的速率与酶-底物结合物(E-S)的形成和分解速率直接相关。
多相催化反应动力学基础[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=14957]多相催化反应动力学基础[/url]
[size=4][font=宋体]动力学分光光度法[/font][/size][size=4][/size][size=4][font=宋体]动力学:测定吸光度随时间的变化,由变化率求出酶的活性值。[/font][/size][size=4][/size][size=4][font=宋体]可选择:一波长,二波长测定,比率测定,多样品池测定。[/font][/size][size=4][/size][size=4][font=Times New Roman]1 [/font][/size][size=4][font=宋体]米[/font][/size][size=4][font=宋体]氏方程([/font][/size][size=4][font=Times New Roman]Michaelis-Menten[/font][/size][size=4][font=宋体]方程)[/font][/size][size=4][/size][size=4][font=宋体]米氏方程是酶促反应动力学最重要的一个数学表达式,它定量的描述了酶促反应的速率与底物浓度之间的关系。[/font][/size][size=4][/size][size=4][font=Times New Roman][/font][/size][size=4][font=宋体]典型的酶促反应如下式所示:[/font][/size][size=4][/size][size=4][font=Times New Roman]E+S=E-S=P+E[/font][/size][size=4][font=宋体]其中[/font][/size][size=4][font=Times New Roman]k1[/font][/size][size=4][font=宋体],[/font][/size][size=4][font=Times New Roman] k2[/font][/size][size=4][font=宋体],[/font][/size][size=4][font=Times New Roman] k3[/font][/size][size=4][font=宋体]分别代表相关反应的速率常数。[/font][/size][size=4][/size][size=4][font=宋体]酶促反应的速率与酶[/font][/size][size=4][font=Times New Roman]-[/font][/size][size=4][font=宋体]底物结合物([/font][/size][size=4][font=Times New Roman]E-S[/font][/size][size=4][font=宋体])的形成和分解速率直接相关。[/font][/size][size=4][/size]
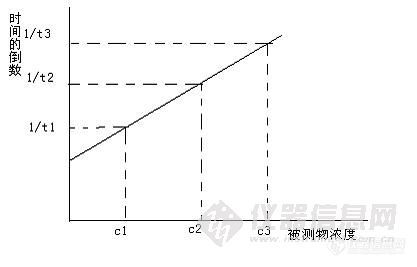
动力学:浓度与反应速率的关系:化学动力学的基本定律是质量作用定律,它表明当温度一定时,化学反应的速率与作用物的浓度成正比,且每种作用物浓度具有一定的指数,最简单的情况下等于计量方程中该物质的计量系数。固定时间法和固定浓度法的选择主要根据反应时间,预测组份的性质和所用的检测技术而定。当分析信号与浓度成直线关系时,固定时间法较为优越,如酶反应中底物的测定当分析信号随着浓度呈非线性关系改变时,固定浓度法则比较合适,两种方法是相互补充的。1 起始斜率法(正切法) 根据线性曲线斜率来测定未知物浓度的方法。所利用的基本动力学方程是x=kcxt。在该法中至少配制3个标准系列,每隔一定时间分别测定反应产物x的浓度并作图,得到一组直线,见图1http://ng1.17img.cn/bbsfiles/images/2011/02/201102192037_278489_1644065_3.jpg再用外推法将时间外推到零而求出各直线的起始斜率,将其tga值与对应的浓度做图,见图2 ,即为校正曲线,未知物的浓度cx可由所得的tga值从图2得到。在该法中,每一个c0A值应至少选取三个时间间隔,即对反应产物进行三次测量。http://ng1.17img.cn/bbsfiles/images/2011/02/201102192037_278490_1644065_3.jpg图2特点:准确度高,但费时2 固定时间法当反应进行到预定的时间t0后,测定反应物或反应产物的浓度,分两种情况:2.1如经t0时间后反应进行的程度不大,则可利用以下动力学方程式:x=kckt来计算。C0k=(1/kt)x。此时C0k -x应为直线关系,见图3。http://ng1.17img.cn/bbsfiles/images/2011/02/201102192039_278491_1644065_3.jpg图3 Ck量不同时的x-t图http://ng1.17img.cn/bbsfiles/images/2011/02/201102192039_278492_1644065_3.jpg图4 被测物浓度校正曲线2.2如经过t0时间后反应物浓度有较大改变,则动力学方程应为log 在分光光度法中,用吸光度代替浓度log 式中A0是反应物A的起始吸光度,At是t时刻的瞬间吸光度。固定时间法比斜率法简便,但其准确度要差一些,对有明显诱导期的指示反应难于得到可靠的结果。2.3固定浓度法测定指示反应中某反应物或反应产物的浓度达到一定值所需要的时间,可根据动力学方程进行计算。http://ng1.17img.cn/bbsfiles/images/2011/02/201102192040_278493_1644065_3.jpg图5 Ck量不同时x-t图http://ng1.17img.cn/bbsfiles/images/2011/02/201102192040_278494_1644065_3.jpg[
农药在农作物、环境中的残留量随时间变化负指数函数递减的规律变化一级反应动力学方程公式计算,CT = Co e-KT 请问各位怎么来理解这句话?谢谢
请问一下Flynn-wall-Ozawa是不是只能用于多重扫描速率法计算动力学参数呢?非常感谢
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=155132]无机化学反应动力学实验的改进[/url]
好书推荐 《电化学动力学》 pdf格式书 名 电化学动力学 作 者 吴浩青 李永舫 出 版 社 高等教育出版社 出版时间 1998年6月第1版 内容提要 本书主要介绍电化学动力学的基本知识、研究方法及其最新进展。全书内容分为三部分:前三章介绍电极/溶液界面双电层的结构以及电化学反应动力学和扩散过程的理论;第四至七章介绍几种重要电化学研究方法(电位阶跃、电位扫描、控制电流、交流阻抗)中的电化学动力学 最后两章介绍电化学动力学在半导体光电化学和电化学嵌入反应中的应用和发展。 本书可供物理化学(电化学)专业研究生作教材,也可作为化学系高年级学生、从事电化学和物理化学的研究和教学人员以及从事电化学实际工作的工程技术人员的参考书。目录: 第一章电极-电解质溶液界面上的双电层第二章电化学反应动力学第三章扩散第四章电位阶跃下的电化学反应第五章电位扫描下的电化学反应第六章控制电流下的电化学反应第七章电极交流阻抗第八章半导体光电化学基础第九章电化学嵌入反应 [img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=14587]《电化学动力学》 [/url][em17]
单位想购买一台紫外可见分光光度计,领导让我查查紫外仪器资料,说是要能测反应动力学的,我查下紫外仪器分单光束、双光束和双波长的,这些哪个能测反应动力学还是都能测啊,还有谁能给我推荐几款型号啊,由于之前没接触过,不懂,还请高手指点!
请教:催化动力学荧光中的反应有:一级反应、假一级反应、假零级反应,是怎么区分的?ΔF与t的关系?还有表观活化能怎么算?什么书上有?
新药研发是一个快速发展的领域,随着组合化学等高技术和天然药物分离制备技术的发展,加快了候选药物的出现。在这些候选药物中,不仅需要对其药效学进行评价,药物代谢和动力学性质也是非常重要的新药筛选指标。理想的药物需要具有持久的药物作用时间和良好的生物利用度。每年都会有大量的候选药物因为其药代动力学参数和代谢特征不佳而被淘汰。因此,在新药的设计、筛选过程中应该考虑候选药物可能出现的代谢特征以及药代参数特点,以获得更为有效的药物。体内药物动力学和代谢研究在新药的研发过程中是相当重要的,需要申报临床研究的药物都需要进行临床前药代动力学研究。除了传统的动物试验以外,目前一些体外实验技术也在新药研发筛选过程中应用,包括组合给药技术,代谢预测模型以及体外肝代谢研究等,这些技术的应用将使对于药物代谢及动力学的筛选变得简便,几种技术的互补将大大加快新药研发的进程。全国科学技术名词审定委员会1999年公布的药学名词“pharmacokinetics”定名为“药动学”,而 “药物代谢动力学”与“药代动力学”为不推荐用名。本文综述的是药物动力学及代谢的应用,故采用 “药代动力学”(pharmacokinetics and metabolism)表达以上意思。1 药代动力学研究的内容药代动力学是应用动力学原理与数学处理方法,定量描述药物在体内的动态变化规律,研究通过各种途径进入人体的药物,其吸收(absorption)、分布(distribution)、代谢(metabolism)和排泄(excre- tion),即ADME过程,并且探讨药物在体内发生的代谢或者生物转化途径,进一步确证代谢产物的结构,研究代谢产物的药效或者毒性,使其结果为新药的定向合成、结构改造和筛选服务。描述药物体内过程的药动学参数主要有以下几个,速率常数(rate constant),包括吸收速率常数(ka)、总消除速率常数(k)以及尿药排泄速率常数(ke)等:生物半衰期(biological half life,t1/2),表征药物在体内的量或者血药浓度消除一半所需的时间,是衡量一种药物从体内消除快慢的指标;表观分布容积(apparent volume of distribution,AUC),是体内药量与血药浓度间相互关系的一个比例常数,是药物的特征参数,对于一个具体的药物来说,其值大小能够表示出该药的分布特性;清除率(clearance),指单位时间从体内消除的含药血浆体积或单位时间从体内消除的药物表观分布容积,常用Cl,又称体内总清除率表示。
大家好!这是我一直很疑惑的问题,怎么用热重确定动力学参数?请大家不要见笑。 因为最近在做轮胎热解,想用热重做热解动力学,我之前的理解是在不同的升温速率下做几组数据,然后数学处理,就可以了。但后来又看到有人说动力学数据需要大量的统计数据,因此很疑惑。我找了些相关的书看,但总是不得要领。 希望大家不吝赐教,不用说具体的算法,只用解答我上面的疑惑即可。多谢了。:)
[size=4][font=宋体]动力学分光光度法[/font][/size][size=4][/size][size=4][font=宋体]动力学分光光度法([/font][/size][size=4][font=Times New Roman]kinetic spectrophotometry[/font][/size][size=4][font=宋体])是利用反应速率与反应物,反应产物或催化剂的浓度之间的定量关系,通过测量与反应速率成比率关系的吸光度,来定量样品溶液中待测组分的浓度。[/font][/size][size=4][/size][size=4][font=Times New Roman] [/font][/size][size=4][font=宋体]这种方法要选择一个反应速率与待测组分浓度相关的指示反应,且要求这个指标反应的反应物与产物的吸收光谱不同,反应速率适中,测量吸光度的瞬间待测组分浓度不变等。[/font][/size][size=4][/size][size=4][font=Times New Roman]1 [/font][/size][size=4][font=宋体]动力学分光光度法定量基础[/font][/size][size=4][/size][size=4][font=宋体]令某以基本反应如下:[/font][/size][size=4][font=Times New Roman]K[/font][/size][size=4][font=宋体]为催化剂[/font][/size][size=4][/size][size=4][font=Times New Roman]M+N[/font][font=Times New Roman] [/font][font=Times New Roman]P+Q[/font][/size][size=4][font=宋体]在其他条件固定时,则反应速率方程为:[/font][/size][size=4][/size][size=4][font=Times New Roman]=k[M][N][k] (1)[/font][/size][size=4][font=宋体]反应初期,如控制[/font][/size][size=4][font=Times New Roman]M[/font][/size][size=4][font=宋体]和[/font][/size][size=4][font=Times New Roman]N[/font][/size][size=4][font=宋体]浓度较大,则基本反应速率主要决定微量催化剂[/font][/size][size=4][font=Times New Roman]k[/font][/size][size=4][font=宋体]的浓度。[/font][/size][size=4][/size][size=4][font=Times New Roman]=k[sub]1[/sub][k] (2)[/font][/size][size=4][font=宋体]积分得[/font][/size][size=4][font=Times New Roman] [N]= k[sub]1[/sub] [k]t (3)[/font][/size][size=4][font=宋体]根据朗伯[/font][/size][size=4][font=Times New Roman]-[/font][/size][size=4][font=宋体]比尔定律[/font][/size][size=4][font=Times New Roman][N]=A/[/font][/size][size=4][font=宋体]ε[/font][/size][size=4][font=Times New Roman]L,[/font][/size][size=4][font=宋体]则([/font][/size][size=4][font=Times New Roman]3[/font][/size][size=4][font=宋体])式变为[/font][/size][size=4][/size][size=4][font=Times New Roman]A= k[sub]1[/sub][/font][/size][size=4][font=宋体]ε[/font][/size][size=4][font=Times New Roman]L[k]t= k[sub]2[/sub][k]t [/font][/size][size=4][font=宋体]([/font][/size][size=4][font=Times New Roman]4[/font][/size][size=4][font=宋体])[/font][/size][size=4][/size][size=4][font=宋体]其中[/font][/size][size=4][font=Times New Roman] k[sub]2[/sub]= k[sub]1[/sub][/font][/size][size=4][font=宋体]ε[/font][/size][size=4][font=Times New Roman]L[/font][/size][size=4][font=宋体]按([/font][/size][size=4][font=Times New Roman]4[/font][/size][size=4][font=宋体])式,便可通过测得产物[/font][/size][size=4][font=Times New Roman]P[/font][/size][size=4][font=宋体]或[/font][/size][size=4][font=Times New Roman]Q[/font][/size][size=4][font=宋体]的吸光度[/font][/size][size=4][font=Times New Roman]A[/font][/size][size=4][font=宋体],对催化剂[/font][/size][size=4][font=Times New Roman]k[/font][/size][size=4][font=宋体]浓度定量。[/font][/size][size=4][/size]
希望高人帮我解答下面问题:本人不胜感激,当然能给小女子更详细的解答方式更是求之不得,qq:56143110(请注明“动力学分析”字样,以方便我接受您)1. 几条热分析曲线上(升温速率10、20、30C/min)同一转化率a 处的da/dt怎么求得?转化率a是根据TG曲线得到的吗?是针对整个反应过程来说的,还是自己选定的主反应过程而言的?2.da/dt指的是DTG曲线上T时刻的反应速率吗?3.不同升温速率下的da/dt与1/T的关系图,通过origin可以做出来吗?
本人求解动力学三因子一头雾水 求高人指点啊 帮忙求解啊 能列出步骤最好了 附件已经上传 2组实验都是先恒温3600s左右 再升温速率1摄氏度每分钟升温到278℃ 最后以1.5℃/MIN 降温 .............. 升温过程的活化能怎么才能准确求出呢 求啊.......
呵呵,本人是做催化剂还原的动力学分析的一小菜研究生。关于热动力学分析方法的问题,想和做者方面工作交流一下经验。我先把我做的有关工作表述一下。如有不对的地方还请指点。我做的反应体系是: A-------》B + C (g)可能每个人不同的体系用的方法不一样。我用的是比较法. 第一步是利用ozawa法和kissinger法求出反应的活化能.(利用TG数据,计算出da/dT。) 第二步 利用Achar method and Coats method 代入所选取的n种机理函数(一般是18种 31种,41种)。计算出不同机理函数的Ea和A。 和第一步计算出的活能值进行比较。选取出和ozawa法计算出的活化能值 相接近且线性系数较好的机理函数。即为反应的机理函数。 这是我所用的动力学方法,其中有什么不足之处请之处。不知道各位用的动力学方法是什么,说一下大家可以相互交流一下。
比如反应动力学或者平衡的问题
问题1: 在求反应所包含的热量的时候,是不是连接两个外推温度(开始和结束),求得他们与dsc曲线上的交点,那么反应所包含的热量是两个交点温度所包含的DSC曲线所包含的面积呢?能不能用示意图表示一下?问题2: 我在用动力学计算反应激活能的时候,遇到一个问题。 根据ln[(dy/dt)*f(y)] 与 1/t之间的斜率求激活能。 dy/dt是这个反应的产物转变量与温度之间的导数,那么反应的开始温度,是以哪个温度为准呢?以外推温度?还是以两个外推温度连线与dsc曲线的交点温度?还是dsc曲线上的开始温度?谢谢!
我做的是吸附实验,用液相色谱测试一系列物质吸附前后的浓度,计算动力学,准二级方程中的k2有的为负数,从而导致初始吸附速率计算结果为负数,这个属于正常吗,我分析的时候是看负数还是他的绝对值呢?谢谢大家
请教大家,用DSC求动力学参数的时候,如果有两个明显的放热峰,是不是要分别求两个放热阶段的动力学参数值啊?
【篇名】 催化动力学光度法测定痕量铁的综述【作者】 黄晓东. 叶桂英. 吴冷贞. 颜鹭红. 【刊名】 福州师专学报 1998年02期【机构】 福州师专!350011. 【关键词】 催化. 动力学. 光度法. 铁. 分析应用. 灵敏度. 【摘要】 本文综述我国催化动力学光度法测定痕量铁的近展状况,提出了一些尚待开发的新指示反应的设想。
DSC法研究聚异氰酸酯环氧树脂胶粘剂的固化反应动力学及固化工艺DSC处理
量子电动力学(Quantum Electrodynamics,简写为QED),是量子场论中最成熟的一个分支,它研究的对象是电磁相互作用的量子性质(即光子的发射和吸收)、带电粒子的产生和湮没、带电粒子间的散射、带电粒子与光子间的散射等等。它概括了原子物理、分子物理、固体物理、核物理和粒子物理各个领域中的电磁相互作用的基本原理。 量子电动力学是从量子力学发展而来。量子力学可以用微扰方法来处理光的吸收和受激发射,但却不能处理光的自发射。电磁场的量子化会遇到所谓的真空涨落问题。在用微扰方法计算高一级近似时,往往会出现发散困难,即计算结果变成无穷大,因而失去了确定意义。后来,人们利用电荷守恒消去了无穷大,并证明光子的静止质量为零。量子电动力学得以确立。量子电动力学克服了无穷大困难,理论结果可以计算到任意精度,并与实验符合得很好,量子电动力学的理论预言也被实验所证实。到20世纪40年代末50年代初,完备的量子电动力学理论被确立,并大获全胜。 量子电动力学认为,两个带电粒子(比如两个电子)是通过互相交换光子而相互作用的。这种交换可以有很多种不同的方式。最简单的,是其中一个电子发射出一个光子,另一个电子吸收这个光子。稍微复杂一点,一个电子发射出一个光子后,那光子又可以变成一对电子和正电子,这个正负电子对可以随后一起湮灭为光子,也可以由其中的那个正电子与原先的一个电子一起湮灭,使得结果看起来像是原先的电子运动到了新产生的那个电子的位置。更复杂的,产生出来的正负电子对还可以进一步发射光子,光子可以在变成正负电子对……而所有这些复杂的过程,最终表现为两个电子之间的相互作用。量子电动力学的计算表明,不同复杂程度的交换方式,对最终作用的贡献是不一样的。它们的贡献随着过程中光子的吸收或发射次数呈指数式下降,而这个指数的底,正好就是精细结构常数。或者说,在量子电动力学中,任何电磁现象都可以用精细结构常数的幂级数来表达。这样一来,精细结构常数就具有了全新的含义:它是电磁相互作用中电荷之间耦合强度的一种度量,或者说,它就是电磁相互作用的强度。