多糖和淀粉的粒度是多大?是10纳米还是1纳米左右?
多糖在重水中溶解度是多少?
我想买根糖柱,要有一下几点要求:1.测定多糖分子量为12000左右的果实多糖;2.最好还能够将多糖衍生化后测单糖构成和摩尔比。3.价钱不是问题请问我要买为什么规格的柱子,什么牌子的?[em0716]
高手请指教!色谱柱被多糖堵了,水反冲柱不起作用,用乙腈冲压力又升高了,咋办呀?
我也不知道要在哪个论坛发布这个求助帖,就在这发个先!急!跪求香菇多糖的毒性报告?谢谢了!
黄芪多糖提取用水提,还是醇提出膏率跟纯度哪个好一点
本人最近测定枸杞多糖含量时,所用测定方法均为2005年版药典枸杞项下,结果出现如下问题:测定枸杞提取物(注:厂家未提供提取方法)枸杞多糖含量时,直接称样水溶解然后测定,结果所测提取物含量高达95%;按药典方法进行前处理,测出值也高达70%;而厂家提供的是50%。另外,我们公司有一种产品,45度白酒,其中添加了葛根黄酮提取物和这种枸杞提取物,结果所测枸杞多糖含量也与理论添加量有很大差别。请问:像我这种情况,在测定枸杞多糖时,需要像药典中那样前处理吗?有哪些更好的方法?多糖测定时葛根黄酮会不会影响?测定提取物和测定白酒中多糖含量时方法是否可以一致?不行的话又分别该怎样测定? 恳请问各位专家朋友指点迷津!谢谢![/color][/color][/color]
多糖的分析是一个大问题啊!和大家讨论一下吧,经综合各种文献我认为多糖结构分析内容:要搞清1. 多糖的单糖组成(种类、比例)2. 每个单糖残基的D-、L-构型,吡喃环式或呋喃环式3. 羟基被取代情况(糖苷键的位置)4. 糖苷键及构型(α、β异头异构体)5. 重复单元方法:1、单糖组成:(对照品:葡萄糖、岩藻糖、半乳糖、甘露糖、木糖、阿拉伯糖、鼠李糖)a:水解: 纸层析薄层层析气相色谱(糖氰乙酸酯衍生物、糖醇乙酸酯)液相色谱(ZORBAX-NH2、HRC-NH2、RID)首选气相,灵敏度高,液相RSD、ELSD灵敏度低b:TFA酸解:气相色谱(乙酰化物)c:甲醇解:气相色谱(三甲基硅醚)2:高碘酸钠氧化和Smith降解a:每摩尔己糖基的高碘酸消耗量、甲酸释放量。(目的:判断可氧化糖基与不可氧化糖基之比例)b:Smith降解完全水解,气相分析,如有葡萄糖(表示有1-3键糖基)、甘油(有1-6或1-2糖基)、甲酸(有1-6糖基)Smith降解部分水解,说明主干糖苷键类型。3:甲基化分析(Hakrmor法)-支链分布多糖—甲基化—水解—还原得甲基化单糖醇—乙酰化得糖醇衍生物—GC-MS检测。 对照品 2,3,4,6-四甲基葡萄糖 糖苷键类型 1—2,4,6- 三甲基葡萄糖 1—32,3,4-三甲基葡萄糖 1—62,4-二甲基葡萄糖 1—3,6 4:IR图谱解析a:吡喃环式或呋喃环式α、β异头异构体5:1HNMR及13CNMR解析(构型)6:纯度检查:a: 紫外吸收光谱(280、260)b:电泳(琼脂糖电泳、聚丙烯酰胺凝胶、醋酸纤维素薄膜)c:薄层色谱(多糖不水解)7:X射线衍射,立体构型。好多啊!想和大家讨论讨论多糖的HPLC分析,我们试验室用的液相是C18柱,紫外检测器,做多糖含量及纯度检测,这样的装备够不够用呀?是不是做前必须衍生化或有其它方法,如用示差折射仪作检测器,是不是不需衍生化?多糖的HPLC分析,用得较多用HPGPC测分子量及分子量分布。一般纯多糖紫外吸收较弱,多用RID或ELSD。至于含量测定多用硫酸蒽酮比色或苯酚硫酸法。http://img.dxycdn.com/images_new/smiles/smile_angry.gif
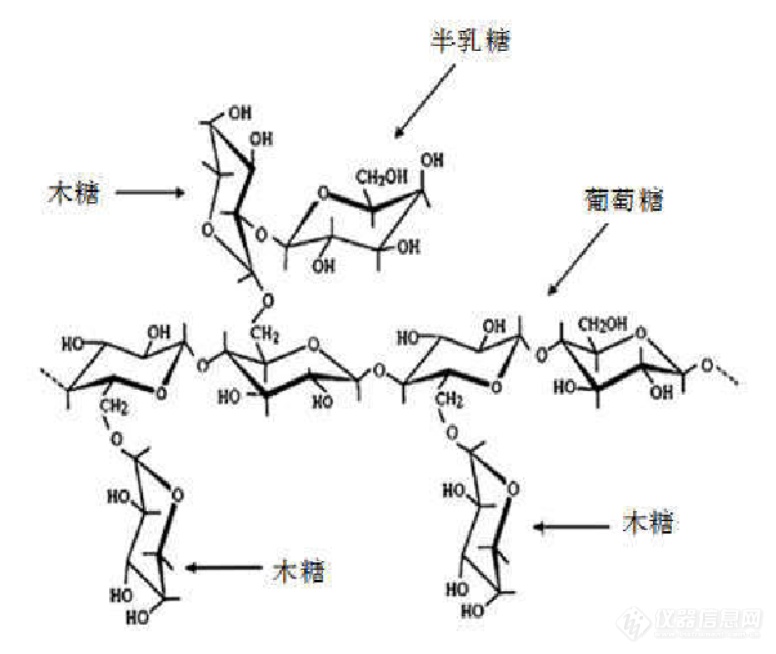
罗望子多糖胶的理化性质,应用和标准陈炳坤[align=center][/align][align=center][font='黑体'][size=20px]罗望子多糖胶的理化性质,应用和标准[/size][/font][/align][align=left][font='times new roman'][size=18px]一、引言[/size][/font][/align][align=left][font='times new roman']罗望子(Tamarindus indica L.)又称酸角、酸豆、罗晃子、酸梅(海南)、“木罕”(傣语),为苏木科(Caesalpiniaceae)酸角属(Tamarindus)的一种高大的常绿乔木植物。罗望子原产于热带非洲,经苏丹引入印度后开始繁衍种植,现广泛分布于除南、北极洲外的其他各大洲。主要分布在我国广西、广东、福建、四川等省区的南部以及海南、台湾等海拔低于 1400m 旱坡、荒地和干热河谷地区,而我国罗望子资源最丰富的地区是云南省的南部、西南部和西部地区。此外在老挝、印度、孟加拉、缅甸、斯里兰卡、马来西亚、泰国等国也有分布。[/font][/align][align=left][font='times new roman']罗望子胶又称为罗望子多糖(Tamarind[/font][font='times new roman'] [/font][font='times new roman']Seed[/font][font='times new roman'] [/font][font='times new roman']Polysaccharide,简称TSP)。它是从豆科罗望子属植物罗望子(又称酸角)的种子胚乳中提取分离出来的一种中性多糖,易分散于冷水中,加热则形成粘稠状液体。罗望子胶有良好的耐热、耐盐、耐酸、耐冷冻和解冻性,具有稳定、乳化、增稠、凝结、保水、成膜的作用,其水溶液的粘稠性较强,黏度不受酸类和盐类等的影响,是一种用途广泛的食用胶。[/font][/align][align=left][font='times new roman'][size=18px]二、[/size][/font][font='times new roman'][size=18px]罗望子多糖胶的理化性质[/size][/font][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107161936326977_6875_1608728_3.png[/img][font='calibri']罗望子胶的分子主要由[/font][font='calibri']D-[/font][font='calibri']半乳糖、[/font][font='calibri']D-[/font][font='calibri']木糖、[/font][font='calibri']D-[/font][font='calibri']葡萄糖三种单糖构成,三种单糖以[/font][font='calibri']1:2:3[/font][font='calibri']的比例组成了罗望子胶的中性聚多糖。也有研究结果表示,他们三种单糖的比例是[/font][font='calibri']1:2.25:2.8[/font][font='calibri'],其分子结构图如图[/font][font='calibri']1[/font][font='calibri']所示。除中性聚多糖存在外,也有少量的[/font][font='calibri']L-[/font][font='calibri']阿拉伯糖是以游离的形式存在于罗望子胶分子内。据报道,用不同的方法测定罗望子胶的分子量,其结果差异也有所不同。据报道,用黏度法、渗透法、铜值法和3,5-二硝基水杨酸还原法测定的结果分别是523500、546000、556000和115000。[/font][/align][align=center][font='times new roman'][color=#000000]图1[/color][/font][font='times new roman'][color=#000000].[/color][/font][font='times new roman'][color=#000000]罗望子多糖胶的分子结构[/color][/font][/align][align=left][font='calibri']罗望子胶为自由流动、无臭无味、乳白色或淡米黄色的粉末,随着胶的纯度降低,制品的颜色逐渐加深,有油脂气味和手感,易结块,不溶于冷水,但是能在冷水中分散,能在热水中溶解,不溶于大多数有机溶剂和硫酸铵、硫酸钠等盐溶液。它本身不带电荷,属于中性植物性胶。但是当罗望子胶用金属氢氧化物或碱式盐溶液处理后,得到相应的金属络合物,能变成阴离子或阳离子衍生物。[/font][/align][align=left][font='calibri']望子胶是一种亲水性较强的植物胶。当罗望子胶在冷水中分散后被加热到85°C以上就会溶解,形成均匀的胶体溶液。胶液的黏度与质量浓度有关,当罗望子胶溶液的质量浓度小于158g/L左右时,溶液表现出牛顿流体性质 但当质量浓度大于158g/L左右时,罗望子胶溶液显示出非牛顿型流体的流变特性,即溶液具有剪切变稀的触变性或假塑性。加热煮沸对罗望子胶溶液的黏度影响相当大,罗望子胶溶液在煮沸20~30min时黏度首先达到最大值,然后下降,但热稳定性较高,在煮沸约5h以后其黏度只下降至最大值的一半。在97°C加热1h后的黏度残存率是瓜尔豆胶的2.5倍。而在-20°C下冷冻1h后测试,它的黏度影响很小。因此罗望子胶具有冷冻融化稳定性。罗望子胶在pH7.0~7.5时比较稳定,超过这个范围其黏度则会降低,在无机酸介质中黏度降低得特别显著,但在使用有机酸时,在pH2.0~7.0范围内溶液黏度受pH值的影响很小,黏度下降的原因是由于其高聚物的解聚引起的 而pH在7.0~7.5时黏度达到最高是由于其分子伸展的缘故。罗望子胶浆料的黏度随温度的降低而增加,但罗望子胶浆料遇冷不胶凝或变稠,且容易进行再分散,甚至贮藏几天之后也是如此。提纯的罗望子胶其溶液的黏度更高,以致很难制备质量浓度大于20g/L的流动性溶胶,其黏度也不受pH及钠盐、钙盐或铁盐的影响,反而随着盐溶液浓度的增高,其黏度有所增加。如添加蔗糖、D-葡萄糖、淀粉糖浆和其他低聚糖都可使其黏度增加,而添加过氧化氢会使其黏度大大降低。罗望子胶水溶液的稠性强,一般不溶于醇、醛、酸等有机溶剂,能与甘油、蔗糖、山梨醇及其他亲水性胶互溶,但遇乙醇会产生凝胶,与四硼酸钠溶液混合则形成半固态,而加热会变成稀凝胶。[/font][/align][align=left][font='calibri']凝胶是由微量的多糖类等物质与水作用并使之变硬的状态,也称果冻,从分子水平看,由于多糖类高分子链间的相互作用,形成立体的网状结构,他们之间的微小空间中的水处于被包围状态,在水溶液中,当高分子之间的相互作用力与高分子、水分子之间的相互作用力达到平衡时,就形成凝胶。多糖类的这种性质称为胶凝性[7]。罗望子胶溶液干燥后能形成有较高强度、较好透明度及弹性的凝胶。罗望子胶凝胶与果胶凝胶形成的模式相同,属于必须有糖存在下才能形成凝胶的氢键结合法,不同的是相同浓度的罗望子胶与果胶相比,凝胶强度要高得多。罗望子胶凝胶形成时,凝胶强度随煮沸时间的延长而极大地提高,当煮沸时间分别为5、7、10min时,凝胶强度分别为420、540、650N/cm[/font][font='calibri'][size=13px]2[/size][/font][font='calibri']。此外,罗望子胶能在很宽的pH范围内与糖形成凝胶,在中性溶液中煮沸长达2h而凝胶强度几乎不受影响,而在热的酸或碱性介质中,罗望子胶也会像果胶一样迅速降解,碱的降解作用与酸相比不太明显。[/font][/align][align=left][font='times new roman'][size=18px]二、[/size][/font][font='times new roman'][size=18px]罗望子多糖胶在食品工业中的应用[/size][/font][/align][align=left][font='calibri']罗望子多糖胶是一种多功能的食品添加剂,与其他动植物胶相比,罗望子多糖胶具有优良的化学性质和热稳定性。[/font][/align][align=left][font='times new roman'][size=18px]1. 在冰淇淋中的应用[/size][/font][/align][align=left][font='calibri']罗望子多糖胶作为稳定剂,分散于冰淇淋料液中,逐渐与水结合,使大量水分子与氢键相连,在结构上形成三维网状结构,控制了残余水相的流动性,使料液具有一定的粘稠度,这种性能有利于冰淇淋在凝冻时有效充入的空气,并且其无韧性的粘性使冰淇淋入口后融化性好,从而使冰淇淋组织细腻、致密、柔软,并使之有良好的保形性、抗融性和抗热震荡能力。此外,还能使冰淇淋形成纹理细小的冰晶。[/font][/align][align=left][font='calibri']罗望子多糖胶与其它稳定剂的兼容性好,表现在与卡拉胶、黄原胶、魔芋胶、刺槐豆胶、CMC 等胶体复配使用具有较好的效果,可弥补其它胶体冰晶粗大的缺陷。不会掩盖或吸附冰淇淋中的风味物质,有利于香味的充分释放,风味释放性明显优于其他胶体。一般情况下,罗望子多糖胶与其它胶体并用的协同增效作用不明显,但是每一种胶各自的优点不会互相抵消。[/font][/align][align=left][font='times new roman'][size=18px]2. 罗望子多糖胶在水冰中的应用[/size][/font][/align][align=left][font='calibri']在水冰类产品中,添加罗望子多糖胶对改善产品的组织结构非常明显,能够有效抑制冰晶的增长,得到组织非常细腻、表面光滑的产品。在此类产品中,罗望子多糖胶的粘结力强但不粘口,成型性好,耐酸、耐盐、抗融性好,既爽口又能增加产品的实物感。罗望子多糖胶的存在还可以使切片产品切面光滑,口感细腻润滑。[/font][/align][align=left][font='times new roman'][size=18px]3. 罗望子多糖胶在饮料中的应用[/size][/font][/align][align=left][font='calibri']罗望子多糖胶能在低浓度(0.05%~1.5%)下形成溶胶,粘度受酸度影响不大,在 pH 值3.2~10.5 的范围内,其粘度和色泽基本上没有变化。用作果汁饮料的增稠剂,可以增加饮用时爽滑、厚实、细腻的口感。同时,罗望子多糖胶的悬浮性还可防止果汁因长期放置而导致的小颗粒沉淀,使细小的果肉颗粒均匀地悬浮于果汁中,大大降低下沉速度。[/font][/align][align=left][font='times new roman'][size=18px]4[/size][/font][font='times new roman'][size=18px]. 用作果冻和糕点的胶凝剂[/size][/font][/align][align=left][font='calibri']罗望子多糖胶具有强保水作用,可有效地阻止温度降低时果冻和弹性糕点中的水分冷凝析出,从而形成细腻的冰晶。与其它种子胶相比,罗望子多糖胶具有优良的化学和热稳定性,使其在制作过程中加热、冷却时保持较稳定的性质。有关人员经过实验表明,制作马蹄糕时,分层现象是由于调粉浆时,有部分马蹄淀粉颗粒和其他淀粉颗粒没有充分溶胀。蒸煮过程中,未充分溶胀的淀粉颗粒因密度差而沉降使蒸出的糕体分层。当加人罗望子多糖胶后,因其对马蹄粉的增粘作用使得粉浆混合体系的粘度大大提高。因此,那些未充分溶胀的淀粉颗粒不发生沉降,形成很好的悬浮液体系,使得蒸出的糕体均匀无分层现象。制出不起丝,无黏性,耐酸性好,保形性优良,有咬劲、有弹性、润滑爽口的马蹄糕。[/font][/align][align=left][font='times new roman'][size=18px]5[/size][/font][font='times new roman'][size=18px]. 用作淀粉品质改良剂[/size][/font][/align][align=left][font='calibri']淀粉是广泛用于加工食品方面的材料,具有粘性,还可以形成食品的骨架,但是淀粉在加工各种食品的过程中,存在着许多缺点,最主要的就是已经糊化(α化)的淀粉在放置的过程中会老化(β化),致使粘度上升,甚至形成凝胶,透明的食品变成半透明或不透明,析水并生成不溶化的淀粉粒甚至沉淀等,所有这些现象都将导致食品的口感和风味受损、稳定性下降、品质变差,而加入罗望子多糖胶作为淀粉的品质改良剂能抑制淀粉老化。[/font][/align][align=left][font='calibri']罗望子多糖胶是相对分子质量 50 万以上、侧链极多的高分子多糖,添加到淀粉中时,侧链上的-OH 通过氢键与淀粉相互作用,形成一种更巨大的高分子体,这种高分子体很难定向,能够稳定地存在。另一方面,在加工过程中淀粉粒容易破裂受损,罗望子多糖胶与淀粉并用,就可以将淀粉包裹起来,防止破裂,起到保护淀粉的作用,使加工的产品在放置过程中不会出现淀粉粒的聚集和老化。此外,罗望子多糖胶还有优良的保水性,可防止析水。[/font][/align][align=left][font='calibri']罗望子多糖胶与乳化剂同时存在,抑制淀粉老化的效果比单独使用罗望子多糖胶或乳化剂大大提高。因此,罗望子多糖胶用作淀粉的品质改良剂,能稳定食品品质,改善质地和结构,提高口感和风味。[/font][/align][align=left][font='times new roman'][size=18px]6[/size][/font][font='times new roman'][size=18px]. 用于牛奶中[/size][/font][/align][align=left][font='calibri']在牛奶中添加 0.5%左右的罗望子多糖胶可增强制品的稠厚感和甜味,同时不会有黏口的感觉,用于低脂牛奶或脱脂牛奶,口感就像全脂牛奶一样;用于咖啡牛奶或果汁牛奶,可以同时增强浓厚感和甜味。[/font][/align][align=left][font='times new roman'][size=18px]7[/size][/font][font='times new roman'][size=18px]. 用于调味汁中 [/size][/font][/align][align=left][font='calibri']一些西餐用调味汁因为加入食醋使 pH 降低,这些调味汁要求有较高的粘度,若添加少量的罗望子多糖胶,由于其耐酸并有一定的增稠作用,所以可以改善调味汁的口感和稳定性。同时,罗望子多糖胶的黏附性能良好,对于烧肉、烧鸡以及蔬菜等的调味汁要求黏附在制品表面不脱落,单独使用罗望子多糖胶或将罗望子多糖胶与其它胶体并用,都能取得显著的效果。[/font][/align][align=left][font='times new roman'][size=18px]8[/size][/font][font='times new roman'][size=18px]. 用于保健食品[/size][/font][/align][align=left][font='calibri']罗望子多糖胶中的多糖是葡聚木糖,它是一种理想的膳食纤维来源。可起到防治高血症的作用,另外尚可增加小肠非扰动层的厚度,减弱糖类物质的吸收,防治糖尿病的发生发展。[/font][/align][align=left][font='calibri']总之,罗望子多糖胶在食品中的作用可以归结为以下几个方面:冰晶稳定作用,增稠稳定作用,保水作用,乳化稳定作用,悬浮稳定作用,品质改良作用,胶凝作用,保健作用。[/font][/align][align=left][font='times new roman'][size=18px]三[/size][/font][font='times new roman'][size=18px]、[/size][/font][font='times new roman'][size=18px]罗望子多糖胶在其他领域的应用[/size][/font][/align][align=left][font='times new roman'][size=18px]1.[/size][/font][font='times new roman'][size=18px] [/size][/font][font='times new roman'][size=18px]罗望子多糖胶在牙膏中的应用[/size][/font][/align][align=left][font='calibri']罗望子多糖胶可以作为牙膏中的粘结剂和增稠剂,其用量为0.5%~1.2%。使用罗望子多糖胶的牙膏具有较好的稳定性,牙膏在﹣2℃的低温和55℃的高温下贮存24,其膏体的硬度和挤出性均无明显改变。特别是在加酶牙膏中,其稳定性更为突出。当采用羧甲基纤维素钠(CMC)时,牙膏膏体硬度在贮存2个月后即会降低到原值的1/6,而采用罗望子多糖胶贮存4个月后,膏体的硬度基本不变。[/font][/align][align=left][font='times new roman'][size=18px]2. 罗望子多糖胶在洗涤剂中的应用[/size][/font][/align][align=left][font='calibri']罗望子多糖胶在液体洗涤剂中作为增稠剂和稳定剂使用时,能够确保液体洗涤剂在贮存期内粘度基本不变。从而保证液体洗涤剂在垂直的硬表面上有较好的滞留性,能够充分发挥洗涤剂的清洗效果。同时,罗望子多糖胶还有一定的乳化能力和抗再沉积能力,因为罗望子多糖胶具有耐盐、耐热、耐酸性的增稠稳定作用,其粘度不受酸类和盐类等的影响。因此,它是液体洗涤剂中良好的增稠稳定剂.[/font][/align][align=left][font='times new roman'][size=18px]3. 罗望子多糖胶在烟草工业中的应用[/size][/font][/align][align=left][font='calibri']罗望子多糖胶是良好的天然粘合剂。在烟草工业中,查正根等研究发现罗望子多糖胶是生产再生烟丝(重组烟丝、膨胀烟丝)良好的粘合剂;在医药工业中,罗望子多糖胶既是药片良好的粘合剂,又是膏霜类药物的增稠剂和稳定剂。[/font][/align][align=left][font='times new roman'][size=18px]4. 罗望子多糖胶在医药行业的应用[/size][/font][/align][align=left][font='calibri']罗望子多糖胶应用于医药行业它可控制药物的释放、并具有高药物容量和高的热稳定性。例如高义霞等以罗望子多糖制备的纳米硒,可能具有硒和罗望子多糖的双重生物学功效,将在癌症的化学预防和治疗方面有光明的前景,同时可能在动物生产中将有广阔的应用前景。[/font][/align][align=left][font='times new roman'][size=18px]四[/size][/font][font='times new roman'][size=18px]、[/size][/font][font='times new roman'][size=18px]罗望子多糖胶的国家标准[/size][/font][/align][align=left][font='calibri']根据国家标准G[/font][font='calibri']B [/font][font='calibri']2760-2014的规定,罗望子多糖胶的使用标准如表1所示[/font][/align][align=center][font='times new roman'][color=#000000]表1[/color][/font][font='times new roman'][color=#000000].[/color][/font][font='times new roman'][color=#000000]罗望子多糖胶的使用标准[/color][/font][/align][table][tr][td][align=center][font='times new roman'][color=#000000]食品名称[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]最大使用量([/color][/font][font='times new roman'][color=#000000]g/kg)[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]备注[/color][/font][/align][/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]冷冻饮品(食用冰除外)[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]2[/color][/font][font='times new roman'][color=#000000].0[/color][/font][/align][/td][td] [/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]可可制品、巧克力和巧克力制品(包括代可可脂巧克力及制品)以及糖果[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]2[/color][/font][font='times new roman'][color=#000000].0[/color][/font][/align][/td][td] [/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]果冻[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]2[/color][/font][font='times new roman'][color=#000000].0[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]如用于果冻粉,按冲调倍数增加使用量[/color][/font][/align][/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]半固体复合调味料[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]7[/color][/font][font='times new roman'][color=#000000].0[/color][/font][/align][/td][td] [/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]液体复合调味料[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]3[/color][/font][font='times new roman'][color=#000000].0[/color][/font][/align][/td][td] [/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]果酱[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]5[/color][/font][font='times new roman'][color=#000000].0[/color][/font][/align][/td][td] [/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]果糕类[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]2[/color][/font][font='times new roman'][color=#000000]0.0[/color][/font][/align][/td][td] [/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]果蔬汁(浆)类饮料[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]3[/color][/font][font='times new roman'][color=#000000].0[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]以即饮状态计,相应的固体饮料按照稀释倍数增加使用量[/color][/font][/align][/td][/tr][/table][align=left][/align][align=left][font='times new roman'][color=#000000]罗望子多糖胶没有国家检测标准,这是因为罗望子多糖胶是一种中性多糖,在检测时无法分辨罗望子多糖胶与其他多糖,因此没有专门的国家检测标准。[/color][/font][/align][align=left][font='times new roman'][size=16px][color=#000000]参考文献:[/color][/size][/font][/align]
做了个多糖,可是没有凝胶柱,也没示差,也没标准物,请问哪里可以测呢?谢谢
有关多糖换算因素的计算问题,求助高手,如下面的换算因素怎么计算:其中W是用哪个数据,还有稀释因素是多少?至于具体的换算因素结果,不需要 精密称取干燥的多糖约25.00mg,置100ml容量瓶中,用蒸馏水稀释至刻度,摇匀,作为贮备液。精密吸取贮备液 5.0ml,稀释至 50ml,取其中的2.0ml置试管中,照标准曲线的制备项下的方法测定吸收度,从回归方程中求出多糖液中的果糖含量,按下式计算,换算因素f=W/(C×D),其W 为多糖的重;C为多糖液中果糖浓度;D为多糖稀释因数. 计算 f值。结果,测得A=0.360,算出f=。
亚甲基蓝比色法测定海参不同组织酸性黏多糖含量http://www.cnki.com.cn/Article/CJFDTotal-HYKX201103014.htm不知道有没有版友做过海参中的多糖呀?看到这样一篇文章不知道有没有版友手里有呀?是否能分享一下如果有做过的版友也可以分享一下你的经验,谢谢!!
大家好!我想做多糖的圆二色谱,不知道哪里可以做?我是在广州的,没找到广州有这仪器的信息.谢谢!
苯酚-硫酸法是一种常用的检测粗多糖含量的方法,其原理是苯酚-硫酸试剂可与游离的寡糖、多糖中的己糖、糖醛酸起显色反应,在480-490 nm处有最大吸收值,吸收值与糖含量呈线性关系。此法是先用标准品多糖制作标准曲线后,再通过多糖的显色反应测定吸光度,然后根据其在曲线上的位置推算出多糖的浓度从而推算其含量。此法操作简单、快速、灵敏、重复性好,对每种多糖仅需制作一条标准曲线[1]。目前大家研究较多的、生物活性较高的一些真菌多糖,如香菇多糖、灵芝多糖、姬松茸多糖、猴头菇多糖、灰树花多糖等[2],在结构上大多是以β-(1→3)、β-(1→4)或β-(1→6)糖苷键连接的葡聚糖,另外,分子量也一般分布在十几万到几十万之间。因此,由北京卫生防疫站建立,经中国预防科学院营养与食品卫生研究所验证的《粗多糖含量的测定方法》中建议使用50万分子量的葡聚糖作为标准品[3]。为行业内粗多糖含量的测定统一了标准,使各企业之间多糖类产品更具有可比性。燕麦β-葡聚糖是一种β-(1→3)-(1→4)键接的线性葡聚糖,在结构、粘度等其他物理性质上与常见的植物和真菌多糖很相似,适合作为植物、真菌来源多糖含量测定的标准品。但由于多糖纯化困难,市面上不少葡聚糖纯度较低,不适合作为标准品。下面,我们来比较两种不同纯度的燕麦β-葡聚糖产品作为多糖标准品的区别。1 材料与方法1.1 实验材料高纯度燕麦β-葡聚糖PS-Con-Ⅰ由武汉百特纯大分子科技有限公司提供,纯度大于97%(其中,另外3%主要是结合水),低纯度燕麦β-葡聚糖由某食品研究所提供,纯度约50%,苯酚、浓硫酸均为化学纯。1.2 实验方法样品溶解:高纯度燕麦β-葡聚糖经70℃水浴,15min后完全溶解。低纯度燕麦β-葡聚糖70℃水浴,30min后仍有不溶物,升高溶解温度至90℃后继续溶解30min,仍有少量不溶物,过滤。溶液配制:配制0.1mg/ml葡聚糖标准溶液,50mg/ml苯酚溶液备用。标准曲线的制作:精密吸取葡聚糖标准液0.10,0.40, 0.80,1.20,1.60,2.00ml(分别相当于葡聚糖0.01,0.04,0.08,0.12,0.16,0.20mg),补充水至2.0mL,加入苯酚溶液1.0ml,混匀,再加入浓硫酸5ml,混匀,沸水浴2分钟,混匀,冷却后用分光光度计在485nm波长处以试剂空白溶液为参比,测定吸光度值(A),以A为横坐标,葡聚糖含量C为纵坐标绘制标准曲线。2 结果与分析2.1 样品溶解高纯度燕麦β-葡聚糖溶解速度较快,溶液澄清透明,说明此产品溶解性良好。低纯度燕麦β-葡聚糖难以溶解,且溶解1h后仍有不溶物存在,说明此产品溶解性差,杂质较多。 2.2 标准曲线下表为两种标准品分别配制不同葡聚糖浓度(含量)反应后得到的吸光值:葡聚糖含量(mg)0.010.040.080.120.162.00高纯度标样吸光值0.0530.0800.2000.2620.3530.450低纯度标样吸光值0.0010.0550.1130.1730.2400.320通过数据处理,得到标准曲线如下:高纯度燕麦β-葡聚糖 C=0.4657A-0.0068 (R=0.9955)低纯度燕麦β-葡聚糖 C=0.609A+0.0101(R=0.9985)比较这两个标准曲线发现,当待测样品吸光值一定,使用低纯度葡聚糖作为标准品得到的标准曲线计算葡聚糖含量值时,明显高于高纯度标准品。究其原因,低纯度葡聚糖所含杂质较多,在作为标准品时,部分杂质不能溶解,却计入了标准品葡聚糖总量,因此,使得结果偏高。另外,即使溶解的物质中,也有可能存在部分不能参加反应的蛋白等杂质,同样会造成结果偏高。由以上数据和分析可以得出,测定粗多糖含量不能使用低纯度葡聚糖作为标准品,应尽量选用高纯度葡聚糖标准品,按照国家建议方法和行业标准进行检测,这样才能保证各企业多糖系列产品在含量和纯度上的可比性,有利于规范企业行为和保健品市场。参考文献[1] 胡居吾,范青生,肖小年. 粗多糖测定方法的研究. 江西食品工业. 2005, 1[2] 李明元. 真菌粗多糖测定方法的研究. 食品研究与开发. 2007, 5[3] 粗多糖的测定方法. 北京卫生防疫站建立,经中国预防科学院营养与食品卫生研究所验证. 食品伙伴网[em0805]

[b]摘要:目的:[/b][color=#000000]探索提取温度、液固比和提取时间对泽泻多糖产率的影响,得到提取泽泻[/color][color=#000000]多糖最优工艺条件。[/color][b]方法:[/b][color=#000000]用均匀设计实验优化泽泻[/color][color=#000000]多糖的提取工艺,用苯酚硫酸法测出每次实验所得多糖的纯度,再求得每次实验纯多糖的得率,然后应用回归分析的方法分析实验得出的数据,以纯多糖的得率为指标,对提取温度、液固比、提取次数和提取时间3个因素进行分析,得出最佳工艺条件,并进行验证。[/color][b]结果:[/b][color=#000000]实验得出茵陈多糖的最佳提取条件是:提取温度100℃、提取时间135 min、提取液固比40:1。[/color][b]结论:[/b][color=#000000]验证实[/color][color=#000000]验平均得率为8.83%,预测值是8.28%,二者很接近,说明我们得到的最佳工艺条件是可靠的。[/color]1前言[color=#000000]泽泻为泽泻科植物泽泻[i]Alsima orientalis(sam.)Juzep.[/i]的干燥块茎,分布在中国、韩国和日本等国。性味甘、淡、寒,归肾、膀胱经[sup][/sup]。作为常用中药,是六味地黄丸、龙胆泻肝丸、五苓散等临床常用重要方剂的主要组成[sup][/sup]。具有利水渗湿,泄热,化浊降脂等功效,用于治疗小便不利,水肿胀满,泄泻尿少,痰饮眩晕,热淋涩痛,高脂血症等症[sup][/sup]。1.1泽泻的化学成分泽泻中的三萜类化合物主要有:泽泻醇A、泽泻醇A-24-乙酸酯、泽泻醇B-23-乙酸酯、表泽泻醇A、11-去氧泽泻醇A、泽泻醇C、泽泻醇C-23-乙酸酯、16,23-氧化泽泻醇E、泽泻醇F、阿里泽泻醇A和阿里泽泻醇B等原萜烷型四环三萜[sup][/sup]。从生物途径归纳,三萜类都是由 23- 泽泻醇 B 衍生而来[sup][/sup]。中药泽泻中获得的倍半萜类化合物多数为愈创木烷型。现分离到的倍半萜化合物主要有:泽泻醇,环氧泽泻烯,Orientalol A,B,C,Sulfooriental A,B,C,D[sup][/sup]。Yamaguchi等首次从泽泻鲜品中分离出一个贝壳杉烷型四环二萜类化合物,并最终确定了绝对构型为(-)-16R-ent-kauranre-2,12-doine[sup][/sup]。彭国平等从泽泻中分离出两个新的贝壳杉烷型四环二萜类化合物:泽泻二萜醇(Oriediterpenol)及泽泻二萜醇苷 (Oriediter-penoside)[sup] [/sup]。泽泻除了萜类成分外,此外,泽泻还含挥发油、多糖、蒽醌、磷脂、蛋白质及淀粉等成分[sup][/sup]。如胡萝卜素-6-硬酸脂、β-谷甾醇、三十烷、正二十烷、卫矛醇、挥发油(内含糖醛)、少量生物碱、天门冬素、脂肪酸、树脂、植物凝集素、大黄素、酸性多糖,胆碱,以及大量淀粉、蛋白质、氨基酸和钾、钙、镁等金属元素[sup][/sup]。1.2 泽泻的药理作用现代研究表明,泽泻有明显的利尿,抑制肾结石形成,降血压,降血脂及抗动脉粥样硬化,抗脂肪肝,抗肾炎活性和调节免疫等作用[sup][/sup]。1.3立题依据多糖具有多种生物活性, 具有提高免疫, 降血糖,抗肿瘤, 抗病毒等功能, 被认为是构成生命的四大基本物质之一。由于其独特功能和较低的毒性, 多糖类化合物在抗衰老、 抗病毒和肿瘤治疗、 糖尿病治疗等方面有良好的应用前景。另外,多糖可以改善食品的食用品质、加工特性和外观特性, 可用于抑制脂质氧化, 稳定酸性饮料, 也可作为乳化剂等, 在食品中的用途十分广泛[sup][/sup]。目前已发现的天然多糖有几百种,其中植物多糖对肿瘤治疗及调节机体免疫力效果显著,同时还有治疗肝炎、抗衰老等药理作用,且毒副作用很小[sup][/sup]。由于泽泻的药理作用显著,而关于泽泻多糖研究的文献很少,因此对于泽泻多糖的研究也具有很大的意义。开发泽泻多糖产品,首先需要把多糖从泽泻中提取出来。笔者决定对泽泻多糖的提取工艺进行研究,对其提取条件进行优化,从而为泽泻多糖的深入开发利用提供实验依据。本课题我们就重点探讨泽泻多糖的最佳提取条件,通过对泽泻多糖提取过程中影响泽泻多糖产率、纯度的因素进行单因素实验,然后进行均匀设计实验,用线性回归的分析方法分析实验得出的数据,寻找泽泻多糖的最优化工艺条件。1.4提取方法的确定提取植物多糖的方法有多种,一般是采用水提醇沉法,采用水提醇沉法提取,可防止引起糖苷键的断裂[sup][/sup]。李小凤等[sup][/sup]通过单纯的水提醇沉法对泽泻多糖进行了提取和含量测定。此外,很多研究对多糖的水提醇沉工艺做了优化,如朱秀灵等[sup][/sup]采用超声波辅助提取银杏叶多糖;缪建等[sup][/sup]采用酶法结合水提醇沉法提取银杏叶多糖;金汝城等[sup][/sup]采用均匀设计优化超声波法提取黄芪多糖。由于实验设备有限,本实验采用水提醇沉法对泽泻多糖进行提取。[/color][color=#000000]2 实验材料2.1实验仪器FA2104N型电子分析天平(上海民桥精密科学仪器有限公司)HH-1数显恒温水浴锅(金坛市晶玻实验仪器厂)80-2离心机(上海荣泰生化工程有限公司)RE-52A旋转蒸发仪(上海亚荣生化仪器厂)GZX-9070电热恒温鼓风干燥箱(上海博讯实业有限公司医疗设备厂)DZF-6050真空干燥箱(巩义市予华仪器责任有限责任公司)SHD-Ⅲ型循环水式多用真空泵(保定市新区阳光科教仪器厂)BCD-223MT冰箱(河南新飞电器有限公司)722可见分光光度计(上海菁华科技仪器有限公司)24目,100目标准筛(浙江上虞市华丰五金仪器有限公司)2.2实验材料和试剂泽泻(河北省安国药材市场)无水乙醇(分析纯,天津市美琳工贸有限公司)蒸馏水(实验室自制)葡萄糖(分析纯,天津市科密欧化学试剂有限公司)苯酚(分析纯,天津市福晨化学试剂厂)浓硫酸(分析纯,北京化工厂)[/color][color=#000000]3实验方法3.1泽泻粗多糖的提取流程将预备好的泽泻放入70℃真空烘箱中干燥2h,粉碎取过24目筛,不可过100目筛的粉末,装在密封袋中置于干燥器中备用。泽泻多糖提取的实验流程如下:精密称定已制备的泽泻粉末5.000g于500mL圆底烧瓶中,加入规定液固比的蒸馏水,用恒温水浴锅T℃水浴加热不同时间,先用脱脂棉过滤得粗滤液,然后用布氏漏斗抽滤粗滤液,通过旋蒸仪旋转蒸发将所得滤液浓缩至约10mL,加95%乙醇30mL,置具塞锥形瓶中,冰箱4℃放置约18h,然后用10mL试管离心(3000rpm,10min),弃去上清液,得沉淀,于50℃、0.099MPa真空干燥箱中放置3.5h后,关闭电源,真空放置过夜。然后,将所得沉淀与离心管一起称重,通过差量法计算多糖产率。其中,液固比、水浴温度T、提取时间t及提取次数根据实验过程中考察因素的改变,作相应更改。粗多糖产率=粗多糖质量/泽泻样品质量×100%3.2 泽泻纯多糖含量的测定本课题中,泽泻提取工艺最佳条件分析中所用的是纯多糖含量,粗多糖的数值只是作为参考数值。本实验中是通过苯酚-浓硫酸反应使多糖显色,在紫外可见分光光度计490nm处测得吸光度,然后通过将数据代入当天测得的标准曲线中,计算出相应多糖浓度,从而计算出不同提取条件下泽泻中纯多糖的含量。3.2.1 标准曲线的绘制标准液的配制:称取葡萄糖0.1259g于100mL容量瓶中,加蒸馏水至刻度,摇匀得1.259g/L的储备液,分别精密量取储备液1.0mL、0.8mL、0.6mL、0.4mL、0.2mL,置于25mL的容量瓶中,加水至刻度,摇匀。则得五个不同浓度的标准液。配制5%苯酚溶液:称取苯酚1.2508g于烧杯中,用加热至约50℃的蒸馏水溶解,转移至25mL的容量瓶中,加水至刻度,摇匀,避光保存以备用。标准曲线的绘制:取2mL移液管,分别取2mL蒸馏水和五个标准溶液于六根具塞试管中,再用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]移取1mL5%的苯酚溶液,快速加入上述具塞试管中,充分混匀,用5mL移液管取5mL浓硫酸快速加入上述试管中,盖好试管塞,充分摇匀。从放入沸水浴中计时,沸水浴15min,冷水浴10min,室温放置5min(六个溶液之间间隔3min加硫酸)。将上述反应30min后的溶液分别在490nm处测定吸光度,以吸光度A为纵坐标,以葡萄糖标准溶液C(Co=50.36)为横坐标,绘制标准曲线。(见图1-1)标准曲线的线性范围为:0.10072×10[sup]-4[/sup]g/mL ~0.50360×10[sup]-4[/sup]g/mL曲线方程:A=0.0165C-0.0216,相关系数:r=0.9998[/color][align=center][img=,619,343]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261725042952_9256_3237657_3.png!w619x343.jpg[/img][/align][align=center]图1-1 标准曲线[/align][align=center] [/align]3.2.2 苯酚-浓硫酸法测多糖含量分别取不同提取条件下所得粗多糖0.040g于小烧杯中,加少量温水搅拌使其溶解,转移至250mL容量瓶中,加蒸馏水至刻度,摇匀。使用前用布氏漏斗抽滤,滤去不溶物,得澄清滤液。然后用2mL移液管分别移取2mL上述滤液于具塞试管中,再用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]移取1mL 5%的苯酚溶液,快速加入上述具塞试管中,充分混匀,用5mL移液管取5mL浓硫酸快速加入上述试管中,充分摇匀,盖好试管塞。沸水浴15min,冷水浴10min,室温放置5min,反应完全后在490nm处测定其吸光度,每次需配制空白对照用来校正可见分光光度计。将测得的吸光度带入标准曲线方程中计算出所配溶液的多糖浓度,进而可计算出纯多糖的产率。3.2.3 纯多糖产率的计算纯多糖产率=(纯多糖浓度×体积×粗多糖质量)/(粗多糖测样量×泽泻质量)×100%3.3 单因素实验3.3.1 液固比对泽泻多糖提取率的影响考察液固比,是为了能够在使用较少溶剂的情况下提取出最多的多糖,这不光能够减少工业生产中单位产量水的使用量,同样也为多糖提取液后期处理减少了时间和成本,具有重要的经济和生态效益。在结合前人相关中药材多糖提取实验的基础上,确定考察液固比为10:1、20:1、30:1、40:1、50:1。纯多糖产率见表3-1。[align=center] 表3-1 液固比对多糖提取率的影响 [/align] [table=582][tr][td]提取温度[/td][td] [align=center]80℃[/align] [/td][td=2,1] 提取时间[/td][td] [align=center]2.5h[/align] [/td][td=2,1] [align=center]提取次数[/align] [/td][td]1[/td][/tr][tr][td] [align=center]液固比(mL/g)[/align] [/td][td=2,1] 10:1[/td][td=2,1] 20:1[/td][td]30:1[/td][td]40:1[/td][td] [align=center]50:1[/align] [/td][/tr][tr][td]多糖产率(%)[/td][td=2,1] 3.38[/td][td=2,1] 3.46[/td][td]5.43[/td][td]7.87[/td][td]6.81[/td][/tr][/table]3.3.2 提取温度对泽泻多糖提取率的影响中药材提取过程中,温度是极其重要的条件。通过查阅文献及综合各方面考虑,确定提取温度为60℃、70℃、80℃、90℃、100℃。多糖产率见表3-2。[align=center]表3-2 提取温度对多糖提取率影响[/align] [table=640][tr][td]液固比[/td][td] [align=center]20:1[/align] [/td][td=2,1] [align=center]提取时间[/align] [/td][td] [align=center]2.5h[/align] [/td][td=2,1] [align=center]提取次数[/align] [/td][td=2,1] [align=center]1次[/align] [/td][/tr][tr][td]提取温度[/td][td=2,1] [align=center]60℃[/align] [/td][td=2,1] [align=center]70℃[/align] [/td][td] [align=center]80℃[/align] [/td][td=2,1] [align=center]90℃[/align] [/td][td] [align=center]100℃[/align] [/td][/tr][tr][td]多糖产率(%)[/td][td=2,1] [align=center]1.81[/align] [/td][td=2,1] [align=center]2.87[/align] [/td][td] [align=center]4.55[/align] [/td][td=2,1] [align=center]5.75[/align] [/td][td] [align=center]9.57[/align] [/td][/tr][/table][color=fuchsia] [/color]3.3.3 提取时间对泽泻多糖提取率的影响通过查阅文献,本实验确定考察时间为0.5h、1h、1.5h、2h、2.5h、3h、3.5h。多糖产率见表3-3。[align=center]表3-3 提取时间对多糖提取率的影响[/align] [table=653][tr][td]液固比[/td][td] [align=center]20:1[/align] [/td][td=2,1] [align=center]提取温度[/align] [/td][td] [align=center]80℃[/align] [/td][td=3,1] [align=center]提取次数[/align] [/td][td=2,1] [align=center]1次[/align] [/td][/tr][tr][td] [align=center]提取时间(h)[/align] [/td][td=2,1] 0.5[/td][td=2,1] 1[/td][td] [align=center]1.5[/align] [/td][td]2[/td][td] [align=center]2.5[/align] [/td][td]3[/td][td] [align=center]3.5[/align] [/td][/tr][tr][td] [align=center]多糖产率(%)[/align] [/td][td=2,1] [align=center]3.57[/align] [/td][td=2,1] 3.38[/td][td] [align=center]4.75[/align] [/td][td] [align=center]5.04[/align] [/td][td] [align=center]5.00[/align] [/td][td] [align=center]4.55[/align] [/td][td] [align=center]5.15[/align] [/td][/tr][/table]3.3.4 提取次数对泽泻多糖提取率的影响众所周知,在最合适的料液比、提取温度、提取时间条件下,提取次数越多,药物的有效成分在中药材中溶出的就会越多,提取率相应就会越高,但提取次数决定操作成本,提取次数越多,成本越高,且工艺用水量大。所以根据前人提取数据,将提取次数定为1次、2次、3次。多糖产率见表3-4。[align=center]表3-4 提取次数对多糖提取率的影响[/align] [table=582][tr][td]提取温度[/td][td] [align=center]80℃[/align] [/td][td=2,1] [align=center]提取时间[/align] [/td][td] [align=center]2.5h[/align] [/td][td] [align=center]液固比[/align] [/td][td] [align=center]20:1[/align] [/td][/tr][tr][td]提取次数[/td][td=2,1] [align=center]1[/align] [/td][td=2,1] [align=center]2[/align] [/td][td=2,1] [align=center]3[/align] [/td][/tr][tr][td]多糖产率(%)[/td][td=2,1] [align=center]3.46[/align] [/td][td=2,1] [align=center]5.71[/align] [/td][td=2,1] [align=center]8.68[/align] [/td][/tr][/table]3.4 均匀设计实验3.4.1 均匀设计实验方案在泽泻(均为5g干粉)多糖提取工艺中,我们要考察的主要因素有:提取温度、料液比及提取时间三个因素。根据单因素实验结果确定各因素的取值范围:提取温度X[sub]1[/sub] :55℃~100℃;料液比X[sub]2[/sub]:1:15~1:60:提取时间X[sub]3[/sub]:1.5h~3.75h。再根据各种因素的取值范围、试验精度要求,按提取温度间隔5℃,液料比间隔5,提取时间间隔0.25h,设计出一个3因素10水平的均匀设计表。根据均匀设计表中所列的提取条件,按照泽泻粗多糖的提取流程,对泽泻粗多糖进行提取,并计算其产率。(见表4-1)提取得到粗多糖并测定多糖纯度,进而求得纯多糖产率。[align=center]表4-1 均匀设计实验数据[/align] [table=638][tr][td] [table][tr][td] [table=100%][tr][td] 条件 编号[/td][/tr][/table] [/td][/tr][/table][img=,98,65]https://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img][img=,84,52]https://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img][/td][td] [align=center]温度(℃)[/align] [/td][td] [align=center]料液比[/align] [align=center](g/mL)[/align] [/td][td] [align=center]时间(min)[/align] [/td][td] [align=center]粗多糖产率(%)[/align] [/td][td] [align=center]纯多糖产率(%)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]55[/align] [/td][td] [align=center]1:35[/align] [/td][td] [align=center]180[/align] [/td][td] [align=center]14.24[/align] [/td][td] [align=center]1.22[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]60[/align] [/td][td] [align=center]1:60[/align] [/td][td] [align=center]120[/align] [/td][td] [align=center]15.44[/align] [/td][td] [align=center]1.67[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]65[/align] [/td][td] [align=center]1:30[/align] [/td][td] [align=center]225[/align] [/td][td] [align=center]12.72[/align] [/td][td] [align=center]1.27[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]70[/align] [/td][td] [align=center]1:55[/align] [/td][td] [align=center]165[/align] [/td][td] [align=center]14.94[/align] [/td][td] [align=center]2.50[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]75[/align] [/td][td] [align=center]1:25[/align] [/td][td] [align=center]105[/align] [/td][td] [align=center]13.62[/align] [/td][td] [align=center]3.74[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]80[/align] [/td][td] [align=center]1:50[/align] [/td][td] [align=center]210[/align] [/td][td] [align=center]23.82[/align] [/td][td] [align=center]6.55[/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]85[/align] [/td][td] [align=center]1:20[/align] [/td][td] [align=center]150[/align] [/td][td] [align=center]23.19[/align] [/td][td] [align=center]5.98[/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]90[/align] [/td][td] [align=center]1:45[/align] [/td][td] [align=center]90[/align] [/td][td] [align=center]23.05[/align] [/td][td] [align=center]5.71[/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]95[/align] [/td][td] [align=center]1:15[/align] [/td][td] [align=center]195[/align] [/td][td] [align=center]16.52[/align] [/td][td] [align=center]4.92[/align] [/td][/tr][tr][td] [align=center]10[/align] [/td][td] [align=center]100[/align] [/td][td] [align=center]1:40[/align] [/td][td] [align=center]135[/align] [/td][td] [align=center]39.93[/align] [/td][td] [align=center]8.74[/align] [/td][/tr][/table]3.4.2 最优提取条件的选择用SPSS 19.0统计软件,以纯多糖得率为评价指标对各因素进行线性回归分析,模型的优度通过复相关系数和方差分析来判定。结果如表4-2。[align=center]表4-2 回归方程[/align] [table=638][tr][td] [align=center] [/align] [/td][td] [align=center]回归方程式[/align] [/td][td] [align=center]R[/align] [/td][td] [align=center]P[/align] [/td][/tr][tr][td] [align=center]回归方程1[/align] [align=center]回归方程2[/align] [align=center]回归方程3[/align] [/td][td] [align=center]Y=-9.850+0.164X[sub]1[/sub]+0.033X[sub]2[/sub]+0.001X[sub]3[/sub][/align] [align=center]Y=-7.595+0.153X[sub]1[/sub][/align] [align=center]Y=3.780-0.002X[sub]2[/sub] X[sub]3[/sub]+3.004E-5 X[sub]1[/sub]X[sub]2[/sub] X[sub]3[/sub] [/align] [/td][td] [align=center]0.919[/align] [align=center]0.902[/align] [align=center]0.960[/align] [/td][td] [align=center]0.008[/align] [align=center]0.000[/align] [align=center]0.000[/align] [/td][/tr][/table]表4-2中,Y为纯多糖得率,X1为提取温度,X2为液固比,X3为提取时间。方程1,R[sup]2[/sup]= 0.844,P值为0.008,回归非常显著,常数项和X1项P值分别0.041和0.002小于0.05 ,回归显著,有统计意义,而X2,X3均回归不显著,方程1多糖产率预测值为7.98%;方程2为将各项及其交叉乘积项全部纳入进行逐步回归的结果,我们发现,最后的方程中只保留了X1项,方程2的 R[sup]2[/sup]= 0.813,常数项和X1项P值分别为0.006和0.000,均小于0.01,回归亦非常显著有效,其预测值为7.66%。方程3为全体向后回归分析结果,R[sup]2[/sup]= 0.922,P值为0.000,常数项乘积项P值分别为0.001,0.000和0.000,均小于0.01 。故回归非常显著,其预测值为8.28%。3.4.3 最优提取条件的验证综合上述三方程的回归结果,及均匀设计和单项实验的结果,我们采取提取温度100℃、提取时间为135 min、提取料液比为40,即第10组的条件为最佳条件,并重复3次进行实验验证。结果见表4-3。[align=center]表4-3 最优提取条件测得的多糖含量[/align] [table][tr][td] [align=center]实验编号[/align] [/td][td] [align=center]提取条件[/align] [/td][td] [align=center]粗多糖得率(%)[/align] [/td][td] [align=center]纯多糖得率(%)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td=1,4] [align=center]提取温度:100℃[/align] [align=center]料液比:1:40[/align] [align=center]提取时间:135 min[/align] [/td][td] [align=center]32.24[/align] [/td][td] [align=center]8.57[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]28.64[/align] [/td][td] [align=center]8.99[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]28.99[/align] [/td][td] [align=center]8.92[/align] [/td][/tr][tr][td] [align=center]平均值[/align] [/td][td] [align=center]29.96[/align] [/td][td] [align=center]8.83[/align] [/td][/tr][/table]4 实验结果4.1 单因素实验结果4.1.1 液固比采用提取温度80 ℃,加热2.5h,提取1次,考察了液固比对提取收率的影响。图4-1表明,固液比从10:1增到20:1多糖产率并无太大变化,液固比从20:1增到30:1纯多糖产率提高了56.94 %,同样,从30:1到40:1纯多糖产率又提高了44.94%。而在40:1到50:1之间,反而下降。主要是由于开始增加提取液体积有利于细胞内容物的溶出,而液固比到达40:1之后,多糖成分已基本溶出,故多糖产率并没有提高,反倒降低。考虑到工业生产中水的用量和多糖产率的综合因素,可以得出40:1应为最佳提取液固比。[align=center][img=,542,271]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261726359481_8405_3237657_3.png!w542x271.jpg[/img][/align][align=center]图4-1 液固比对泽泻粗多糖得率的影响[/align][align=center] [/align]4.1.2 提取温度采用液固比为20:1,提取时间2.5h,提取1次,考察了提取温度对多糖产率的影响,结果见图4-2。由图中可以看出,当温度从60 ℃上升到70 ℃时,粗多糖得率共提高了58.56%,从70℃到80℃,提高了58.54%,80℃到90℃,提高了26.37%,从90℃到100℃,提高了66.43%。随着温度的上升,多糖产率一直在增加,说明温度的提高对多糖的溶出有显著影响。显然,从60℃到90℃,多糖产率几乎呈线性上升,从90℃到100℃,较60℃到90℃上升更快,且产率最高。过低的温度会造成提取物溶出少甚至不溶出,而较高温度会显著提高多糖产率。所以,即使较高的温度会略微增加能源上的成本,但是却使多糖产率增加数倍,提高药材利用率,大大降低总生产成本。综合以上各方面因素考虑,得出多糖的最佳提取温度为100 ℃。[align=center][img=,556,281]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261727189034_3165_3237657_3.png!w556x281.jpg[/img][/align][align=center]图4-2 提取温度对泽泻多糖得率的影响[/align][align=center] [/align]4.1.3 提取时间中药材有效药物成分溶出需要一定的时间,较短会造成药物有效成分无法最大限度地溶出,过长的提取时间则会导致有效成分分解。采用提取温度80 ℃,液固比20:1,提取1次,考察了提取时间对多糖得率的影响,结果见图4-3。可以看出,提取时间超过2h后多糖得率并未继续增加,反而下降;而2h之前,多糖得率增加显著,从1h到2h增加了49.11%。虽然在3.5h处总产率较2h增加了0.11%,但是提取时间却较2h多出将近一倍,大大增加了生产成本,故2h为最佳提取时间。[align=center][img=,560,260]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261727397775_5830_3237657_3.png!w560x260.jpg[/img][/align][align=center]图4-3 提取时间对泽泻多糖得率的影响[/align]4.1.4 提取次数采用提取温度80 ℃,提取时间2.5h,液固比20:1,考察了提取次数对多糖得率的影响,结果见图4-4。结果发现:提取3次时多糖得率最高,比1次提取提高了1.5倍,差别显著。而提取两次较提取一次,也提高了65.03%,提高显著。提取三次的多糖产率是提取一次的2.5倍。因此,从约成本,提高药材利用率的角度考虑,确定最佳提取次数为3次。[align=center][img=,548,269]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261727581933_5743_3237657_3.png!w548x269.jpg[/img][/align][align=center]图4-4 提取次数对泽泻多糖得率的影响[/align][align=center] [/align]4 . 2 均匀设计实验结果本实验采用水提醇沉法提取泽泻多糖,通过对料液比、提取时间、提取温度等三个可控条件进行均匀设计实验,结合实验及生产实际,确定了泽泻多糖提取的最优条件,并利用该最优条件测定了泽泻多糖的含量,计算出了纯多糖的得率。结果见表4-4。[align=center]表4-4 泽泻多糖提取最优条件及多糖含量[/align] [table][tr][td=4,1] [align=center]最优提取条件[/align] [/td][td=1,2] [align=center]粗多糖得率[/align] [align=center](%)[/align] [/td][td=1,2] [align=center]纯多糖得率[/align] [align=center](%)[/align] [/td][/tr][tr][td] [align=center]提取温度[/align] [/td][td] [align=center]提取料液比[/align] [/td][td] [align=center]提取时间[/align] [/td][td] [align=center]提取次数[/align] [/td][/tr][tr][td] [align=center]100℃[/align] [/td][td] [align=center]1:40[/align] [/td][td] [align=center]135 min[/align] [/td][td] [align=center]1次[/align] [/td][td] [align=center]29.96[/align] [/td][td] [align=center]8.83[/align] [/td][/tr][/table]所得纯多糖实际产率8.83%与理论得率8.28%十分接近。[color=#000000]5 讨论5 . 1多糖提取与含量测定过程(1)在多糖提取过程中,除待测因素温度、料液比、提取时间按要求改变外,其他条件均应保持一致,以减少系统误差,增加数据的准确性。(2)在转移多糖溶液的过程中要尽可能的减少损失及其操作的一致,如粗过滤完抽滤时滤渣滤棉中残余多糖成分的转移,旋蒸浓缩提取液后的转移和离心过程中多糖的转移应最大程度减少多糖损失量,并保持操作的一致性。(3)在绘制标准曲线及用苯酚-硫酸法测多糖含量时,加入苯酚后一定要混匀,以防止硫酸直接氧化苯酚,导致糖类反应不完全。此外,苯酚须现用现配,避光保存。(4)在硫酸与糖反应时,一般方法是加入苯酚和硫酸后摇匀,直接室温放置30min后测其吸光度,为了保证反应完全,本实验在加入硫酸并摇匀后,先沸水浴15min,再冷水浴10min,再室温放置5min后测量吸光度。并在测量时保证每组的反应时间一致。(5)纯多糖含量的测定过程,为了保证数据的准确性,单因素实验中同一组的最好同时测,均匀设计实验的十组最好同一天测完。(6)由于实验时间有限,对于泽泻多糖测定时,采用的是以往经验的可见光范围490nm进行测定,这是实验中不完善的地方,准确的操作应通过实验找到多糖吸光度最大的波长进行测定。5 . 2 单因素实验由于单因素只是考虑单个提取条件对产率的影响,不能考虑到多种因素共同的影响,所以只是作为参考结果,对于单因素对多糖提取的影响具有参考价值,但是从总的生产上来说,均匀设计具有更加实用的价值。本实验中,单因素最优条件为:液固比40:1,提取温度100℃,提取时间2h,提取次数3次。单因素中提取次数的结果中提取两次较提取一次产率的增长值,还没有提取三次较提取两次的增长值大。可能是因为提取温度不够高,多糖溶出较慢所致。单从单因素的角度来看提取三次为最佳条件。但是从生产过程考虑,提取次数的增加会增加很大工作量,一般会选择一次就能提取完全的条件。而均匀设计实验中也证明,在100℃,40:1,135min条件下多糖的产率就可以达到8.74%,比单因素实验中提取三次的量还要高,故选择一次为最佳提取次数。5 . 3 均匀设计实验均匀设计实验结果8.83%同实验分析的理论结果8.28%较为接近,这也证明了实验数据的准确性,并通过回归分析确定了实验的最佳提取条件。均匀设计是在单因素的基础上进行的,综合两个实验的数据结果,不难发现提取的最佳条件为:提取温度100℃、提取时间为135 min、提取料液比为40、提取一次。5 . 4 整体结果讨论单因素实验中,我们可以得到以下关于单因素对多糖提取率的影响。提取次数与多糖产率呈正相关,提取时间也是呈正相关。提取时间与多糖产率的关系是到一定时间就达到稳定,即超过这个时间显著性不过。液固比与多糖产率的关系是存在一个峰值,低于此值,产率随液固比增加而增加,超过此值则随液固比增加而产率降低。这也给我们一些启发,对于这些植物药中似多糖类水溶性物质的提取条件也应存在此种规律,可作为以后研究的参考。均匀设计实验是在单因素的基础上,综合考虑了提取时间、温度和液固比对多糖产率的影响,是较符合实际生产条件的一项实验,具有较高的应用参考价值。当然,除了本课题中考虑到的因素,可能还有其他未被考虑到的一些因素。均匀设计只是以线性回归的方式对实验数据进行分析,而现在有更为先进的如响应面分析法等。这都说明多糖的提取工艺有很大的提升空间。参考文献 中药大辞典.上海:上海科学技术出版社,2006:2067Xie Min.Phmaracology of traditional Chinese medical formulas.Beijing:The People’s Public Health Publish House,2007 国家药典委员会编.中国药典(一部).中国医药出版社,2010:213 黄珍,刘咏松.泽泻降血脂药理作用及物质基础研究进展.山西中医学院学报,2008,9(5):55~56 陈曦.泽泻的研究现状与进展.中国民族民间医药,2011,20(9):50~51,53 臧萍.泽泻的研究现状及展望.中国中医药现代远程教育,2009,07(6):180~182Yamaguchi K.Akauurane derivative isolated from Alisma orientale Acta Crystallogr SectC Cryst. Struct .医药导报,2003,22(5):295Peng GP,LouFC.Isolation and indentification of diterpenoids fromAlisma orientalis .Actapharmaceutica sinica,2002,37:950~954 丁霞,吴水生.泽泻的研究进展.中医药信息,2008,25(5):19~21 王建平,傅旭春,泽泻的药理作用和临床研究进展.2011年浙江省医学会临床药学分会学术年会论文汇编,2011 冯欣煜,姚志凌.泽泻药理研究与临床新用.中国医药指南,2007,S1:37~38 尹艳,高文宏,于淑娟,等.多糖提取技术的研究进展.食品工业科技,2007,28(2):248~250 吴华振.植物多糖的药理作用及应用进展.实用医技杂志,2005,12(7):1803~1804 杨艳,徐应淑.川、黔地区金钗石斛多糖的含量测定.中国药房,2010,21(27):2552~2554 李小凤,韦庆宁,史柳芝,等.泽泻多糖的提取及含量测定.山东化工,2012,41(7):26~28 朱秀灵,戴清源,冯宏波.超声波辅助提取银杏叶多糖工艺研究. 安徽工程科技学院学报,2010,25(3):6~8 缪建,杨文革,周彬.银杏叶多糖提取工艺的优化. 中国食品添加剂,2007,12(2):153~156 金汝城,周术涛,张东博,等.均匀设计优化超声波法提取黄芪多糖的研究. 安徽农业科学,2009,37(12):5498~5499[/color][align=center] [/align]
苯酚-硫酸法是一种常用的检测粗多糖含量的方法,其原理是苯酚-硫酸试剂可与游离的寡糖、多糖中的己糖、糖醛酸起显色反应,在480-490 nm处有最大吸收值,吸收值与糖含量呈线性关系。此法是先用标准品多糖制作标准曲线后,再通过多糖的显色反应测定吸光度,然后根据其在曲线上的位置推算出多糖的浓度从而推算其含量。此法操作简单、快速、灵敏、重复性好,对每种多糖仅需制作一条标准曲线[1]。目前大家研究较多的、生物活性较高的一些真菌多糖,如香菇多糖、灵芝多糖、姬松茸多糖、猴头菇多糖、灰树花多糖等[2],在结构上大多是以β-(1→3)、β-(1→4)或β-(1→6)糖苷键连接的葡聚糖,另外,分子量也一般分布在十几万到几十万之间。因此,由北京卫生防疫站建立,经中国预防科学院营养与食品卫生研究所验证的《粗多糖含量的测定方法》中建议使用50万分子量的葡聚糖作为标准品[3]。为行业内粗多糖含量的测定统一了标准,使各企业之间多糖类产品更具有可比性。燕麦β-葡聚糖是一种β-(1→3)-(1→4)键接的线性葡聚糖,在结构、粘度等其他物理性质上与常见的植物和真菌多糖很相似,适合作为植物、真菌来源多糖含量测定的标准品。但由于多糖纯化困难,市面上不少葡聚糖纯度较低,不适合作为标准品。下面,我们来比较两种不同纯度的燕麦β-葡聚糖产品作为多糖标准品的区别。1 材料与方法1.1 实验材料高纯度燕麦β-葡聚糖PS-Con-Ⅰ由武汉百特纯大分子科技有限公司提供,纯度大于97%(其中,另外3%主要是结合水),低纯度燕麦β-葡聚糖由某食品研究所提供,纯度约50%,苯酚、浓硫酸均为化学纯。1.2 实验方法样品溶解:高纯度燕麦β-葡聚糖经70℃水浴,15min后完全溶解。低纯度燕麦β-葡聚糖70℃水浴,30min后仍有不溶物,升高溶解温度至90℃后继续溶解30min,仍有少量不溶物,过滤。溶液配制:配制0.1mg/ml葡聚糖标准溶液,50mg/ml苯酚溶液备用。标准曲线的制作:精密吸取葡聚糖标准液0.10,0.40, 0.80,1.20,1.60,2.00ml(分别相当于葡聚糖0.01,0.04,0.08,0.12,0.16,0.20mg),补充水至2.0mL,加入苯酚溶液1.0ml,混匀,再加入浓硫酸5ml,混匀,沸水浴2分钟,混匀,冷却后用分光光度计在485nm波长处以试剂空白溶液为参比,测定吸光度值(A),以A为横坐标,葡聚糖含量C为纵坐标绘制标准曲线。2 结果与分析2.1 样品溶解高纯度燕麦β-葡聚糖溶解速度较快,溶液澄清透明,说明此产品溶解性良好。低纯度燕麦β-葡聚糖难以溶解,且溶解1h后仍有不溶物存在,说明此产品溶解性差,杂质较多。 2.2 标准曲线下表为两种标准品分别配制不同葡聚糖浓度(含量)反应后得到的吸光值:葡聚糖含量(mg)0.010.040.080.120.162.00高纯度标样吸光值0.0530.0800.2000.2620.3530.450低纯度标样吸光值0.0010.0550.1130.1730.2400.320通过数据处理,得到标准曲线如下:高纯度燕麦β-葡聚糖 C=0.4657A-0.0068 (R=0.9955)低纯度燕麦β-葡聚糖 C=0.609A+0.0101(R=0.9985)比较这两个标准曲线发现,当待测样品吸光值一定,使用低纯度葡聚糖作为标准品得到的标准曲线计算葡聚糖含量值时,明显高于高纯度标准品。究其原因,低纯度葡聚糖所含杂质较多,在作为标准品时,部分杂质不能溶解,却计入了标准品葡聚糖总量,因此,使得结果偏高。另外,即使溶解的物质中,也有可能存在部分不能参加反应的蛋白等杂质,同样会造成结果偏高。由以上数据和分析可以得出,测定粗多糖含量不能使用低纯度葡聚糖作为标准品,应尽量选用高纯度葡聚糖标准品,按照国家建议方法和行业标准进行检测,这样才能保证各企业多糖系列产品在含量和纯度上的可比性,有利于规范企业行为和保健品市场。参考文献[1] 胡居吾,范青生,肖小年. 粗多糖测定方法的研究. 江西食品工业. 2005, 1[2] 李明元. 真菌粗多糖测定方法的研究. 食品研究与开发. 2007, 5[3] 粗多糖的测定方法. 北京卫生防疫站建立,经中国预防科学院营养与食品卫生研究所验证. 食品伙伴网
我的多糖在做单糖组成时测到有葡萄糖、果糖、甘露糖、木糖,而做的核磁解析出了果糖、葡萄糖,另外解出一个鼠李糖,但是单糖组成并未测到鼠李糖,想问一下这种情况正常吗,会不会被审稿人所质疑
本人最近测定枸杞多糖含量时,所用测定方法均为2005年版药典枸杞项下,结果出现如下问题:测定枸杞提取物(注:厂家未提供提取方法)枸杞多糖含量时,直接称样水溶解然后测定,结果所测提取物含量高达95%;按药典方法进行前处理,测出值也高达70%;而厂家提供的是50%。另外,我们公司有一种产品,45度白酒,其中添加了葛根黄酮提取物和这种枸杞提取物,结果所测枸杞多糖含量也与理论添加量有很大差别。请问:像我这种情况,在测定枸杞多糖时,需要像药典中那样前处理吗?有哪些更好的方法?多糖测定时葛根黄酮会不会影响?测定提取物和测定白酒中多糖含量时方法是否可以一致?不行的话又分别该怎样测定? 恳请问各位专家朋友指点迷津!谢谢!
公司新生产的药中含有一种叫云芝多糖的原料,在检验过程中遇到了一些问题,想请教一下论坛里的老师。云芝多糖是多孔菌科植物云芝的干燥子实体提取的多糖。其中一项理化检验标准:取本品(云脂多糖原料)适量,置锥形瓶中,加斐林试液甲、乙各10ml,煮沸3-4分钟,冷却,滤过,取滤液适量,用12%的盐酸调至酸性,取5ml加热10分钟,冷却中和,再加斐林试液甲乙各10ml,煮沸2分钟,溶液中应析出红色氧化亚铜沉淀。但是我在做的过程中发现:加斐林试液甲乙各10ml煮沸后冷却,就有红色沉淀物析出,过滤后照标准做下去,得不到最后的结论??不知道是什么原因?想请教一下论坛里的老师帮忙给解答一下。谢谢!
[align=center][/align][font=宋体]一、原理[/font][font=宋体]1.[/font][font=宋体]多糖的分级与纯化[/font][font=宋体]多糖纯化的实质是将粗多糖中的杂质(包括蛋白质、色素、低聚糖、无机盐等非糖物质)除去而获得分子量和极性均一的多糖组分。比较常用的方法有:醇沉法、超滤法和柱层析法等。其中柱层析法应用比较普遍,多用于样品的精细分级,具有操作简单,重现性好的优点,但样品上样量小。用于多糖分离的柱层析主要有两类:一类是通过分子量大小进行分级的凝胶柱层析,如Sephadex G-100(200、50、25、10)、SepharoseCL-6B等系列;另一类是离子交换层析,是根据多糖所带电荷的性质不同选择相应的离子交换柱对多糖进行分级。如待分离的多糖带有负电荷,可选择阴离子型的DEAE-纤维素柱或DEAE-Sepharose柱进行分级,以获得均一的多糖组分。[/font][font=宋体]通过热水煮提方法提取的多糖,通常是混合物,且分子量不均一,其单糖组成、分子结构和聚合度往往不同,可通过柱层析的方法,对其进行分级以达纯化的目的。本实验中,采用[/font]DEAE-[font=宋体]纤维素柱层析的方法对中草药中水溶性粗多糖进行分级纯化,分离纯化出各级分多糖,[/font][font=宋体]为后续研究多糖的结构特征和生物活性奠定基础。[/font][font=宋体]2.[/font][font=宋体]苯酚—硫酸法[/font][font=宋体]游离的寡糖、多糖中的己糖或糖醛酸在浓硫酸的作用下,脱水生成糠醛,再与苯酚作用起显色反应,在一定范围内其颜色深浅与糖的含量成正比,吸收值与糖含量呈线性关系。且己糖在[/font]490 nm[font=宋体]处(戊糖及糖醛酸在[/font]480 nm[font=宋体])有最大吸收,故用比色法测定多糖含量。该法简单,快速,灵敏,且颜色持久,同一台设备同一光源仅需制作一条标准曲线。[/font][font=宋体] [/font][font=宋体]二、步骤[/font]1.[font=宋体]中草药水溶粗多糖的提取流程[/font][font=宋体]中草药粉末[/font][font=Symbol][/font][font=宋体]蒸馏水浸泡过夜[/font][font=Symbol][/font][font=宋体]超声[/font]/[font=宋体]微波[/font][font=Symbol][/font][font=宋体]水浴浸提[/font][font=Symbol][/font][font=宋体]过滤去除药渣[/font][font=Symbol][/font][font=宋体]定容[/font][font=Symbol][/font][font=宋体]多糖含量测定[/font][font=宋体]加等体积[/font]95%[font=宋体]乙醇[/font][font=Symbol][/font]4[font=宋体]℃冰箱过夜,醇沉多糖[/font][font=Symbol][/font]5000r/min[font=宋体]离心去上清液[/font][font=Symbol][/font][font=宋体]粗多糖[/font][font=Symbol][/font][font=宋体]脱蛋白[/font][font=Symbol][/font][font=宋体]脱色素[/font][font=Symbol][/font][font=宋体]透析[/font][font=Symbol][/font][font=宋体]浓缩[/font][font=Symbol][/font][font=宋体]冷冻干燥得水溶多糖[/font][font=Symbol][/font]DEAE-[font=宋体]纤维素色谱柱[/font][font=Symbol][/font][font=宋体]收集多糖组分[/font][font=Symbol][/font][font=宋体]测定每[/font]50s[font=宋体]洗脱液的[/font]OD[font=宋体]值[/font][font=Symbol][/font][font=宋体]绘制横坐标为管数与纵坐标为[/font]OD[font=宋体]值的洗脱曲线[/font][font=宋体]根据洗脱曲线收集多糖溶液[/font][font=Symbol][/font]4[font=宋体]℃无水乙醇醇沉过夜[/font][font=Symbol][/font][font=宋体]离心[/font][font=Symbol][/font][font=宋体]多糖沉淀[/font][font=Symbol][/font][font=宋体]常规干燥[/font][font=Symbol][/font][font=宋体]纯度鉴定[/font][font=Symbol][/font][font=宋体]纯多糖[/font]2.[font=宋体]脱蛋白[/font][font=宋体]由于粗多糖中含有一定量游离的和结合的蛋白,为保证多糖的纯度,必须将蛋白质脱去。常用的脱蛋白方法有[/font]Sevag[font=宋体]法、三氯乙酸法和蛋白酶法(如链蛋白酶、胰蛋白酶、木瓜蛋白酶)等。[/font][font=宋体]([/font]1[font=宋体])[/font]Sevag[font=宋体]法[/font][font=宋体]根据蛋白质在有机溶剂(如氯仿)中易发生变性析出的特点[/font][font=宋体],把多糖配制成[/font]5%[font=宋体]的糖液,然后按照[/font]1:3[font=宋体]的体积比加入[/font]Sevag[font=宋体]试剂(氯仿∶正丁醇[/font]=4[font=宋体]∶[/font]1[font=宋体]),混匀后剧烈振荡,静置分层后吸去水层与溶剂层交界处的变性蛋白质,重复操作多次,直到除尽蛋白质为止。[/font][font=宋体]([/font]2[font=宋体])三氯乙酸法[/font][font=宋体]将粗多糖配成[/font]5%[font=宋体]的糖液,加入[/font]30%[font=宋体]三氯乙酸溶液,使三氯乙酸终浓度为[/font]15%[font=宋体],在[/font]4℃[font=宋体]冰箱中放置过夜,离心弃去沉淀,得无蛋白的多糖溶液,再用[/font]1 mol/L NaOH[font=宋体]溶液中和至[/font]PH[font=宋体]为[/font]7[font=宋体]。[/font][font=宋体]([/font]3[font=宋体])蛋白酶法[/font][font=宋体]将粗多糖配成[/font]5%[font=宋体]的糖液,用酸碱调[/font]pH[font=宋体]至中性,加链蛋白酶[/font]0.5 L[font=宋体],放恒温箱中[/font]37℃[font=宋体]保温[/font]24 h[font=宋体]后,加热升温至[/font]80℃[font=宋体]使酶失活,离心,得无蛋白的多糖溶液。[/font]3.[font=宋体]脱色[/font][font=宋体]([/font]1[font=宋体])[/font] [font=宋体]活性炭法[/font][font=宋体]将脱蛋白后的多糖配成[/font]5%[font=宋体]的糖液,用[/font]NaOH[font=宋体]溶液调[/font]pH[font=宋体]为[/font]4.5[font=宋体],加入活性炭粉末,于[/font]80℃[font=宋体]保温[/font]2 h[font=宋体]后过滤。反复进行[/font]3[font=宋体]次,直到溶液颜色不再降低为止。[/font][font=宋体]([/font]2[font=宋体])过氧化氢法[/font][font=宋体]将脱蛋白后的多糖溶液,用浓氨水调至[/font]pH[font=宋体]为[/font]8.0[font=宋体],逐滴滴加[/font]20%H[sub]2[/sub]O[sub]2[/sub][font=宋体]至溶液为浅黄色,[/font]50℃[font=宋体]水浴,保温[/font]2 h[font=宋体]后过滤。[/font]4.[font=宋体]透析脱盐[/font][font=宋体]将脱蛋白、脱色后多糖配成[/font]5%[font=宋体]溶液,置于透析袋中,先用自来水逆向流水透析[/font]72 h[font=宋体]后,再用蒸馏水透析[/font]24 h[font=宋体],每[/font]4 h[font=宋体]换水一次。[/font]5.[font=宋体]干燥[/font][font=宋体]将脱蛋白、脱色、脱盐后的中草药多糖溶液,水浴[/font]80℃[font=宋体]浓缩至[/font]10 mL[font=宋体],加三倍体积的无水乙醇过夜,离心取沉淀,经无水乙醇、乙醚洗涤后,常规干燥得中草药去蛋白去色素的多糖。[/font]6.[font=宋体]多糖含量测定[/font][font=宋体]采用苯酚[/font]-[font=宋体]硫酸法测定样品中的多糖含量。绘制标准曲线,根据葡萄糖标准曲线和样品吸光值计算其糖含量。[/font][font=宋体]标准曲线的制作:准确称取[/font]105℃[font=宋体]干燥恒重的标准葡萄糖[/font]50 mg[font=宋体]定容于[/font]500 mL[font=宋体]容量瓶中,加水至刻度,用移液管分别吸取[/font]0[font=宋体]、[/font]0.1[font=宋体]、[/font]0.2[font=宋体]、[/font]0.3[font=宋体]、[/font]0.4[font=宋体]、[/font]0.5[font=宋体]、[/font]0.6[font=宋体]、[/font]0.7[font=宋体]、[/font]0.8[font=宋体]、[/font]0.9[font=宋体]、[/font]1.0 mL[font=宋体]转入试管中,各以蒸馏水补至[/font]1.0 mL[font=宋体],每个浓度重复四个平行。然后分别向每支试管中加入[/font]4%[font=宋体]苯酚试剂[/font]1mL[font=宋体]及浓硫酸[/font]2 mL[font=宋体],摇匀,沸水浴中煮沸[/font]10 min[font=宋体],冷却至室温,放置[/font]10 min[font=宋体]后在[/font]λ= 480 nm[font=宋体]处测定吸光值[/font]A[font=宋体]。以吸光值[/font]A[font=宋体]为纵坐标,糖含量[/font]C[font=宋体]为横坐标,得糖的标准曲线。[/font][font=宋体]样品溶液制备:精密称取水溶性粗多糖[/font]5 mg[font=宋体],先加[/font]10 mL[font=宋体]蒸馏水溶解,然后定容至[/font]50 mL[font=宋体]。[/font][font=宋体]样品含量测定:用移液管吸取样品液[/font]1.0 mL[font=宋体],加入[/font]4%[font=宋体]苯酚溶液[/font]1 mL[font=宋体]及浓硫酸[/font]2 mL[font=宋体],按上述方法进行操作,测其吸光值,以标准曲线计算样品糖含量[/font][font=宋体]按下式计算中草药多糖的质量浓度与得率。[/font] [img=,300,41]https://ng1.17img.cn/bbsfiles/images/2021/11/202111021041176368_5305_3528941_3.gif!w300x41.jpg[/img]7.[font=宋体]分级[/font][font=宋体]([/font]1[font=宋体])[/font] DEAE-[font=宋体]纤维素的预处理和装柱[/font][font=宋体]将[/font]DEAE-[font=宋体]纤维素用蒸馏水充分浸泡溶胀后,倾倒除去水分,再用[/font]0.5 M NaOH[font=宋体]溶液浸泡[/font]1 h[font=宋体],用蒸馏水反复洗涤至[/font]PH[font=宋体]等于[/font]7[font=宋体]。再用[/font]0.5 M[font=宋体]的[/font]HCl[font=宋体]溶液浸泡[/font]1 h[font=宋体],用蒸馏水洗至中性,真空清除气泡,备用。[/font][font=宋体]装柱时,先将[/font]DEAE-[font=宋体]纤维素沿着玻璃棒缓慢倒入,以防产生气泡。柱子装好后,依次用[/font]5[font=宋体]倍柱体积的蒸馏水、[/font]3[font=宋体]倍柱体积的[/font]1.0 M NaCl[font=宋体]和[/font]5[font=宋体]倍柱体积的蒸馏水进行平衡,流速设定为[/font]20 cm/ h[font=宋体]。[/font][font=宋体]([/font]2[font=宋体])水溶性粗多糖的离子交换柱层析的线性梯度洗脱[/font][font=宋体]称取[/font]50 mg[font=宋体]水溶性粗多糖,溶于[/font]5 mL[font=宋体]蒸馏水中,在已平衡好的[/font]DEAE-[font=宋体]纤维素离子交换柱([/font]1.5 × 14 cm[font=宋体],[/font]Cl[sup]-[/sup][font=宋体]型)上进行上样,先用[/font]100 mL[font=宋体]蒸馏水做流动相进行洗脱,再用[/font]0~1.0 M NaCl[font=宋体]溶液[/font]300 mL[font=宋体]进行线形梯度洗脱,流速[/font]1.0 mL/min[font=宋体],每个试管收集[/font]3 mL[font=宋体]洗脱液,苯酚—硫酸法测定洗脱液中相对的糖含量分布。[/font]8.[font=宋体]纯度鉴定[/font][font=宋体]([/font]1[font=宋体])高效液相色谱法[/font][font=宋体]采用高效液相色谱仪系统,[/font] 10A[font=宋体]检测器,[/font]CLASS-Vp[font=宋体]工作站,[/font]TSK-gel G-3000PWXL[font=宋体]不锈钢色谱柱([/font]7.8 × 300 mm)[font=宋体],柱温为[/font]40℃[font=宋体]。[/font][font=宋体]取各级多糖样品溶于[/font]0.7 M Na2SO4[font=宋体]溶液中,其多糖终浓度为[/font]2 mg/mL[font=宋体],上样[/font]20 μL[font=宋体],流动相为[/font]0.7 M Na2SO4[font=宋体]溶液,流速为[/font]0.5 mL/min[font=宋体]。[/font][font=宋体]([/font]2[font=宋体])紫外光谱分析[/font][font=宋体]将水溶性粗多糖各级分多糖样品配成[/font]0.1 mg/mL[font=宋体]的溶液,用[/font]752PC[font=宋体]型紫外可见分光光度计于[/font]200-400 nm[font=宋体]处扫描检测。[/font][font=宋体]([/font]3[font=宋体])旋光仪分析[/font][font=宋体]不同的多糖具有不同的比旋度,它们在不同浓度的乙醇中具有不同溶解度,所以,如同一多糖水溶液经不同浓度的乙醇沉淀所得的沉淀物,具有相同比旋度,则证明该多糖为均一组分。[/font][font=宋体]将评估多糖样品溶于水,成为近似半饱和溶液,置于磁力搅拌器上,在搅拌下加乙醇,使溶液中乙醇浓度达到[/font]20%[font=宋体],搅拌片刻,使沉淀完全,离心得沉淀。上清液中再继续滴加乙醇,使溶液中乙醇浓度达[/font]40%[font=宋体],所产生的沉淀再经离心。前后两次沉淀,分别干燥后在相同条件下测定其水溶液的比旋度。[/font][font=宋体]将[/font]10 mL5%[font=宋体]饱和糖液用国产[/font]WXG[font=Symbol]-[/font]6[font=宋体]型自动旋光仪,钠灯光源,以蒸馏水调零点,[/font]1dm[font=宋体]管室温下测定。[/font]
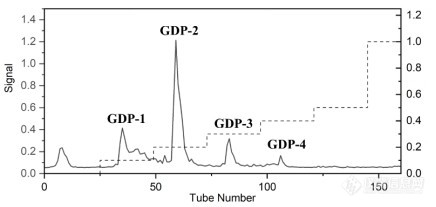
[align=center][b][font=Arial][font=宋体]天然多糖研究体积排阻色谱柱选择初探[/font][/font][/b][/align][font=Arial][font=宋体]多糖是最丰富的生物聚合物,已被发现参与许多生物过程,例如细胞间通讯、胚胎发育、细菌和[/font]/[font=宋体]或病毒感染以及体液和细胞免疫。因此,多糖与核苷酸、蛋白质、脂质一起构成了生命科学中最重要的四大生物大分子。[/font][/font][font=Arial][font=宋体]尽管多糖已在各种工业应用中使用了几十年,例如[/font] [font=宋体]药物、生物材料、食品和营养以及生物燃料,对多糖在生命科学中的重要性的日益了解和深入研究正在推动多糖用于新型(生物分子)应用的开发。不断有来自植物(膳食纤维、草药和木本植物)、藻类和地衣的生物活性多糖,以及来自动物的其他生物活性多糖(例如肝素、硫酸软骨素和透明质酸)被报道。[/font][/font][font=Arial][font=宋体]天然多糖发现的主要方法为提取纯化得到相对较纯的多糖组分,从而进行结构表征和活性评价。具体而言,通过水提醇沉得到粗多糖,再通过弱阴离子交换色谱法([/font]DEAE[font=宋体])进行纯化,得到不同盐梯度洗脱的组分。对于这些组分,需要通过体积排阻色谱法([/font][font=Arial]SEC[/font][font=宋体])分析判定,是否需要进一步纯化;得到纯品之后,需要测定多糖组分的分子量;研究多糖在体内的降解规律,也需要[/font][font=Arial]SEC[/font][font=宋体]判定多糖分子量的变化。因此,多糖研究实验室往往需要多支[/font][font=Arial]SEC[/font][font=宋体]色谱柱,以适应不同的用途。研究人员热切期望有一只首选[/font][font=Arial]SEC[/font][font=宋体]色谱柱,可以快速开展研究。本文以小秦艽多糖的研究为例,说明[/font][font=Arial]BioCore SEC-1000[/font][font=宋体]作为多糖研究的首选色谱柱,在多个用途中的效果。[/font][/font][font=Arial][font=宋体]小秦艽,学名为达乌里秦艽[/font]([/font][i][font=Arial]Gentiana dahurica Fisch[/font][/i][font=Arial])[font=宋体],为龙胆科植物龙胆属多年生草本植物,始载于《神农本草经》,列为中品,具有祛风湿、清湿热、止痹痛、退虚热的功效。小秦艽多糖经过提取和除杂后,通过中压制备[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]([/font][font=Arial]DEAE[/font][font=宋体]填料)填料纯化,得到四个组份。在后续多糖组份纯度判定和降解规律研究中,使用了[/font][font=Arial]BioCore SEC-1000[/font][font=宋体]色谱柱。[/font][/font][b][font=Arial][font=宋体]一、实验条件与方法[/font][/font][font=Arial]1.1. [font=宋体]仪器及色谱条件[/font][/font][/b][font=Arial][font=宋体]高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url]:安捷伦[/font] 1260 infinity II[font=宋体],配有[/font][font=Arial]Wyatt[/font][font=宋体],[/font][font=Arial]Optilab T-REX[/font][font=宋体]示差折光检测器([/font][font=Arial]RI[/font][font=宋体])[/font][font=Arial] [/font][font=宋体]岛津[/font][font=Arial]LC-2030C[/font][font=宋体],配有岛津[/font][font=Arial]RID-20A1.2[/font][font=宋体]示差折光检测器([/font][font=Arial]RI[/font][font=宋体]);大连依利特有限公司 [/font][font=Arial]Elite 1100 [/font][font=宋体][url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url],配有岛津[/font][font=Arial]RF-20AXS[/font][font=宋体]荧光检测器([/font][font=Arial]FLD[/font][font=宋体])。[/font][/font][font=Arial][font=宋体]色谱柱:[/font]T (13μm[font=宋体],[/font][font=Arial]7.8×300mm)[/font][font=宋体]或[/font][font=Arial]Biocore SEC-1000[/font][font=宋体]([/font][font=Arial]5μm, 7.8×300mm[/font][font=宋体]);[/font][/font][font=Arial][font=宋体]流动相:[/font]50 mM NH[/font][sub][font=Arial]4[/font][/sub][font=Arial]OAc (80%)+Methanol (20%)[font=宋体];[/font][/font][font=Arial][font=宋体]流速:[/font]0.5 mL/min[font=宋体];[/font][/font][font=Arial][font=宋体]柱温:[/font]25[/font][font=宋体]℃[/font][font=Arial][font=宋体];[/font][/font][font=Arial][font=宋体]进样量:[/font]20 μL[font=宋体];[/font][/font][font=Arial][font=宋体]采集时间:[/font]30 min[font=宋体]。[/font][/font][b][font=Arial]1.2 [font=宋体]样品处理[/font][/font][/b][font=Arial]1[font=宋体])秦艽多糖组份纯度分析:称取秦艽多糖[/font][font=Arial]GDP-3[/font][font=宋体](即样品[/font][font=Arial]0.3 M[/font][font=宋体])约[/font][font=Arial]5 mg[/font][font=宋体],溶于流动相,配制成[/font][font=Arial]10 mg/mL[/font][font=宋体]溶液。上样前用[/font][font=Arial]0.22 μm[/font][font=宋体]滤膜过滤。[/font][/font][font=Arial]2[font=宋体])多糖[/font][font=Arial]GDP-2[/font][font=宋体]体外稳定性的考察: [/font][font=Arial]GDP-2[/font][font=宋体]的经 [/font][font=Arial]FITC[/font][font=宋体]荧光标记(产物为[/font][font=Arial]FGDP-2[/font][font=宋体]),进行体外模拟消化。模拟胃液由胃蛋白酶[/font][font=Arial](10 g/L)[/font][font=宋体]和稀[/font][font=Arial]HCl (16.4 mL/L)[/font][font=宋体]组成,调节[/font][font=Arial]pH[/font][font=宋体]至[/font][font=Arial]1.3[/font][font=宋体]。将[/font][font=Arial]FGDP-2 (25 mg/mL)[/font][font=宋体]与各人工胃液和人工肠液[/font][font=Arial]10 mL[/font][font=宋体]混合,[/font][font=Arial]37[/font][/font][font=宋体]℃[/font][font=Arial][font=宋体]孵育。分别于[/font]0 h[font=宋体]、[/font][font=Arial]4 h[/font][font=宋体]、[/font][font=Arial]6 h[/font][font=宋体]、[/font][font=Arial]12 h[/font][font=宋体]取孵育液各[/font][font=Arial]500 μL[/font][font=宋体]作为[/font][font=Arial]HPLC-FLD[/font][font=宋体]测定样品。用[/font][font=Arial]0.2 M NaOH[/font][font=宋体]和[/font][font=Arial]TCA (20 % , w/w)[/font][font=宋体]终止反应。[/font][/font][b][font=Arial][font=宋体]二、结果与讨论[/font][/font][/b][font=Arial][font=宋体]多糖纯度及分子量的测定是多糖结构解析及构效关系研究的关键步骤。小秦艽多糖的纯化色谱洗脱曲线如图[/font]1[font=宋体]所示,一共得到四个组份。[/font][/font][align=center][img=,348,]https://ng1.17img.cn/bbsfiles/images/2023/02/202302081451227890_6619_3237657_3.jpg!w436x207.jpg[/img][/align][align=center][font=Arial][font=宋体]图[/font]1 [font=宋体]小秦艽多糖的[/font][font=Arial]DEAE[/font][font=宋体]纯化色谱图(硫酸苯酚法重构)[/font][/font][/align][font=Arial][font=宋体]组份经透析、冻干后,首先需要确定它的纯度。如果组份不纯,则后续的核磁分析将是徒劳无功的。我们实验室前期配备了三支不同孔径的[/font]SEC[font=宋体]色谱柱,经分析组份[/font][font=Arial]1[/font][font=宋体]和[/font][font=Arial]2[/font][font=宋体]较纯,而[/font][font=Arial]3[/font][font=宋体]和[/font][font=Arial]4[/font][font=宋体]不纯。如果不纯,则需要通过凝剂渗透色谱([/font][font=Arial]GPC[/font][font=宋体])进一步纯化。[/font][font=Arial]SEC[/font][font=宋体]分析可以确定组份的数目,以在[/font][font=Arial]GPC[/font][font=宋体]纯化时收集馏分。[/font][/font][font=Arial][font=宋体]在用实验室已有[/font]SEC[font=宋体]色谱柱分析时(图[/font][font=Arial]2[/font][font=宋体]上),色谱峰数目不明确。该色谱柱孔径为[/font][font=Arial]450?[/font][font=宋体],粒径为[/font][font=Arial]13 μm[/font][font=宋体],分离度不理想,可能分子量超出其适用范围。于是改用孔径更大且粒径为[/font][font=Arial]5 μm[/font][font=宋体]的[/font][font=Arial]Biocore SEC-1000[/font][font=宋体]柱进行试验(图[/font][font=Arial]2[/font][font=宋体]下),结果表明分离效果好,明显识别为三个色谱峰。为该组份的后续纯化以及多糖稳定性的考察提供基础。[/font][/font][align=center][img=,264,]https://ng1.17img.cn/bbsfiles/images/2023/02/202302081451353696_6101_3237657_3.jpg!w331x346.jpg[/img][/align][align=center][font=Arial][font=宋体]图[/font]2 [font=宋体]秦艽多糖分子量的分析色谱图[/font][/font][/align][align=center][font=Arial][font=宋体](上图,实验室已有色谱柱[/font]T[font=宋体];下图,纳谱[/font][font=Arial]Biocore SEC-1000[/font][font=宋体])[/font][/font][/align][font=Arial][font=宋体]此外,该色谱柱,分离中等分子量多糖标准品([/font]36 kDa ~ 131 kDa[font=宋体])时,也呈现了较好的线性关系。因此,我们认为该色谱柱具有分子量适用范围宽的优点,可以作为多糖分析中的通用[/font][font=Arial]SEC[/font][font=宋体]色谱柱。[/font][/font][font=Arial][font=宋体]为了确定秦艽多糖的体外消化模式,选取了经测量相对较纯的秦艽多糖[/font]GDP-2[font=宋体]组分进行荧光标记,建立了[/font][font=Arial]HPLC - FLD[/font][font=宋体]分析方法,进行体外稳定性考察。通过上述实验对[/font][font=Arial]SEC[/font][font=宋体]柱的比较分析,选取了分离效果较好的[/font][font=Arial]Biocore SEC-1000[/font][font=宋体]进行该实验。[/font][font=Arial]FGDP-2[/font][font=宋体]在模拟胃液中的分子量随时间变化色谱图如图[/font][font=Arial]3[/font][font=宋体]所示,发现色谱峰的相对峰高向小分子偏移,说明[/font][font=Arial]FGDP-2[/font][font=宋体]在消化[/font][font=Arial]4 h[/font][font=宋体]后发生部分降解。可能是由于多糖对酶和强酸敏感,导致多糖的糖苷键断裂。然而,观察到整个消化系统中没有单糖出现,胃和肠道不会造成多糖结构的过度损失。[/font][/font][align=center][img=,288,]https://ng1.17img.cn/bbsfiles/images/2023/02/202302081451479308_4610_3237657_3.jpg!w361x212.jpg[/img][/align][align=center][font=Arial][font=宋体]图[/font]3[font=宋体]模拟胃液消化过程中[/font][font=Arial]FGDP-2[/font][font=宋体]的[/font][font=Arial]HPLC - FLD[/font][font=宋体]表征[/font][/font][/align][font=Arial][font=宋体]三、小结[/font][/font][font=Arial][font=宋体]多糖研究人员往往面对不同来源的多糖分子,分子量差异较大,从几万到上百万的多糖分子量。在多糖的研究过程中,需要一支通用的[/font]SEC[font=宋体]色谱柱,进行快速分子量判断,以确定后续研究操作。[/font][font=Arial]BioCore SEC-1000[/font][font=宋体]在我们对小秦艽多糖的分子量纯度分析、分子量测定和体外消化稳定性等研究中,均获得了良好的效果。我们认为,[/font][font=Arial]BioCore SEC-1000[/font][font=宋体]可以作为多糖研究实验室的首选[/font][font=Arial]SEC[/font][font=宋体]色谱柱。[/font][/font][font=Arial] [/font][font=Arial][font=等线]公司:[/font][/font][font=等线][font=等线]苏州大学药学院[/font][/font][font=等线][font=等线]色谱柱信息:[/font][/font][font=Arial]BioCore SEC-1000 5μm, 7.8×300mm[/font][font=宋体] [/font]
请问用原子力显微镜观察多糖的分子形貌,制样时需要注意那几个方面,在用轻敲模式时有没有相关经验可以分享,每次做出来的图都是圆形的,粒径都很大,不知道怎么解释
大家好 我现在用药典方法 提取多糖 测黄精中多糖含量 即取60度干燥恒重的生黄精粉末0.25g,精密称定,置圆底烧瓶中,加80%乙醇150ml回流提取1h,趁热滤过,残渣用80%乙醇洗涤3次,每次10ml,将残渣及滤纸置烧瓶中,加水150ml,加热回流1h,趁热滤过,残渣及烧瓶用水洗涤4次,每次10ml,合并滤液与洗液,放冷,转移至250ml容量瓶中,加水至刻度,摇匀 精密吸取1ml至10ml具塞干燥试管中,加水至2ml,摇匀,在冰水浴中缓慢滴加0.2%蒽酮-硫酸溶液,至刻度,混匀,放冷后至水浴用保温10min,取出,立即置冰水浴中冷却10min,取出,以相应试剂为空白,照紫外可见分光光度计在582nm波长处测定吸光度。 我分别按上述方法提了6次样品,测得多糖含量 68% 左右。 实在搞不懂到底哪里出了问题,使测出的多糖含量这么高。。。 在做含量测定时,分别吸取1ml多糖液、1ml水和8ml0.2%蒽酮硫酸溶液时 都是用吸量管吸取的 这样重复性比较好 但是就是含量出奇的高 求高人指点 是我哪个地方需要注意下么?

[align=center]保健品中粗多糖含量的测定[/align]本文研究了苯酚-硫酸法检测不同基质的保健品中粗多糖的含量,论述了不同基质的前处理方法和经验。1 前言市场上常见的保健品多种多样,胶囊、口服液、药片等等。多糖含量作为保健品中的有效成分之一,越来越引起人们的关注。从药理学上讲,多糖具有抗肿瘤、抗病毒、增强免疫力、抗氧化、抗心血管疾病等。因为具有诸多功效,许多保健品生产公司也开发越来越多的含多糖保健品,通过在保健品中添加含有多糖的中药材或者海洋生物,从而使该保健品具有较高的多糖含量,增强其功效。不仅在胶囊、口服液等常规的保健品中添加含有多糖的成分,甚至在一些咖啡、饮料、食品中也添加含有多糖的组分,使其成为功能性的产品。多糖的含量对其功效的发挥至关重要,那么怎么准确、有效地检测出保健品中多糖的含量是一个重要的环节。保健品由于种类繁多,基质复杂,找到一种简单、有效的检测方法,能够检测出各种基质的保健品中多糖的含量具有重要的意义。本实验中采用了常见的苯酚-硫酸法检测保健品中粗多糖含量,选用乙醇提取以除去单糖、低聚糖、甙类及生物碱等干扰成分,然后用去离子水提取其中所含的多糖类成分。多糖在硫酸作用下,水解成单糖,并迅速生成糖醛衍生物与苯酚综合成有色化合物,用分光光度法测定其多糖含量。2 实验部分2.1 试剂95%乙醇 葡萄糖:优级纯;葡萄糖标准液:精确称取105℃干燥恒重的葡萄糖100 mg,置100 ml容量瓶中,加蒸馏水溶液解并稀释至刻度(可加几滴甲苯或几粒苯甲酸防腐)。此标准溶液1.00 ml含葡萄糖1.00 mg,储存于冰箱冷藏;苯酚;苯酚液:称取优级纯苯酚10.0 g,加水150 g ,置棕色瓶中备用,储存于冰箱;浓硫酸。2.2 仪器分光光度计。2.3 分析步骤2.3.1 样品预处理(1) 口服液等液体样品准确移取2.00~10.00 mL液体口服液试样,置于250 mL圆底烧瓶中,加入9倍体积的95%乙醇,混匀,静置1 h,回流提取1 h,趁热过滤,残渣用95%乙醇5 ml洗涤三次。将残渣连同滤纸置于烧瓶中,加蒸馏水50 mL,在60℃水浴中加热提取30 min,趁热过滤,残渣用5 mL热水洗涤三次,洗液并入滤液,放冷后移至100 mL容量瓶中,稀释至刻度,备用。(2)内容物为膏状的胶囊样品或者膏状类样品准确称取0.50~1.00 g膏状内容物或膏状样品,倘若其中含有油脂类辅料,加入乙醚或者石油醚脱脂,离心,弃去乙醚或者石油醚层。再用一定体积的水溶解,转移至250 mL圆底烧瓶中,加入9倍体积的95%乙醇,混匀,静置1 h,回流提取1 h,趁热过滤,残渣用95%乙醇5 ml洗涤三次。将残渣连同滤纸置于烧瓶中,加蒸馏水50 mL,在60℃水浴中加热提取30 min,趁热过滤,残渣用5 mL热水洗涤三次,洗液并入滤液,放冷后移至100 mL容量瓶中,稀释至刻度,备用。(3)内容物为粉状的胶囊样品或者粉状片剂、咖啡等准确称取0.10~0.50 g均质后的粉状样品,倘若其中含有脂肪类辅料,先加入一定体积的水,溶解粉状样品,再加入乙醚或者石油醚脱脂,离心,弃去乙醚或者石油醚层。将水层转移至250 mL圆底烧瓶中,加入9倍体积的95%乙醇,混匀,静置1 h,回流提取1 h,趁热过滤,残渣用95%乙醇5 ml洗涤三次。将残渣连同滤纸置于烧瓶中,加蒸馏水50 mL,在60℃水浴中加热提取30 min,趁热过滤,残渣用5 mL热水洗涤三次,洗液并入滤液,放冷后移至100 mL容量瓶中,稀释至刻度,备用。2.3.2 标准曲线的制备吸取葡萄糖标准液0.25 mL、0.50 mL、1.00 mL、1.50 mL、2.00 mL、2.50 mL,分别置于50 mL容量瓶中,加水定容。吸取上述溶液各2.00 mL,再加苯酚液1.00 mL,涡旋混合均匀,迅速沿管壁加入浓硫酸5.00 mL,摇晃后涡旋混合,放置5 min,置沸水浴中加热15 min,取出后冷却至室温,于490 nm处以水代替样品作参比测吸光度,绘制标准曲线。2.3.3 样品中多糖含量测定吸取2.00 mL样品液,置于10 ml容量瓶中,加水定容。吸取2.00 mL上述溶液,按标准曲线制备项下方法测定吸光度。另以2.00 mL水,同上操作做空白。查标准曲线得样品液中葡萄糖含量。2.3.4 液体样品分析结果的计算计算液体样品中酸性多糖的含量按式(1)或者(2)计算,分别以mg/mL或者mg/g表示。[img=,503,114]https://ng1.17img.cn/bbsfiles/images/2024/03/202403181709449978_4859_3246897_3.png[/img][sub] [/sub] 式中: X—保健品中酸性多糖含量(以葡萄糖计), mg/g或者mg/mL表示;A—从浓度-吸光度曲线上查得样品溶液的葡萄糖浓度,μg;B—从浓度-吸光度曲线上查得空白溶液的葡萄糖浓度,μg;V[sub]1[/sub]—多糖溶液总体积,mL,如按本方法为100 mL;V[sub]2[/sub]—移取多糖溶液的初始体积,mL,如按本方法为2 mL V[sub]3[/sub]—待测多糖浓度溶液的总体积,mL,如按本方法为10 mL;V[sub]4[/sub]—待测多糖溶液的移取体积,mL,如按本方法为2 mL m—保健品的称取质量,g;V[sub]0[/sub]—保健品的测试体积,mL;如两次测定符合允许差时,取两次测定结果的算术平均值作为结果,报告结果取三位有效数字。2.3.5 允许差同一样品的两次测定值之差不得超过两次测定平均值的10%。2.3.6 结果与分析(1)含油脂类样品脱脂与否的影响含有油脂类的保健品,脱脂前后采用上述方法进行酸性多糖含量测定时,多糖含量有一定的差别,未脱脂的样品进行多糖含量测定时,过滤过程十分缓慢,耗时长,多糖含量数据经常不平行,而且数值偏高。[align=center][img=,300,307]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230846_01_3246897_3.jpg[/img][/align][align=center]图1 乙醚脱脂[/align]样品经过乙醚脱脂后有明显的油脂层。[align=center][img=,300,296]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230846_02_3246897_3.jpg[/img][/align][align=center]图2 回流后的未脱脂样品[/align][align=center][img=,300,302]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230847_01_3246897_3.jpg[/img][/align][align=center]图3 回流后的脱脂样品[/align]通过比较图2和图3,脱脂后的样品溶液更加澄清,无论是过滤还是洗涤,反应更快速,洗涤效果也更好。相反,未脱脂的样品,整个容器壁上都黏附着脂肪、油脂层,即使离心后过滤,过滤速率也很差,滤液也很浑浊,如下图4所示。[align=center][img=,300,268]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230847_02_3246897_3.jpg[/img][/align][align=center]图4 脱脂前后滤液的比较[/align][align=left]没有脱脂的样品,油脂层包裹着含有单糖或者寡糖的乙醇溶液,不容易被乙醇洗涤干净,这部分残留的单糖或者寡糖导致结果偏高。因此,对相应的含油脂保健品提前进行脱脂后再检测多糖,不仅能减少操作的时间,还能获得更为准确的结果。 [/align][align=left](2)醇沉时间的影响[/align][align=left]对以含有大豆油辅料的胶囊内容物进行脱脂后沉淀粗多糖,对比了加入9倍95%乙醇后立即回流提取多糖和加入9倍95%乙醇后室温下静置1 h再回流提取多糖,结果显示,加入乙醇后立即回流提取多糖与静置1h后再回流检测出的多糖含量分别为41.69 mg/g、48.08mg/g。可以看出,室温下醇沉时间的增加可以使更多的粗多糖醇沉完全,检测含量增高。[/align][align=left](3) 苯酚硫酸法操作方法的影响[/align][align=left]苯酚硫酸法检测粗多糖含量最为常见,操作简单,适用于常规检测。在实验过程中发现,无论苯酚和浓硫酸的加入比例是1:5还是1:10,苯酚的体积分数是5%还是6%,在进行加入时最好是一个样品加完苯酚,混匀后,立即沿管壁加入浓硫酸,混匀后,再加另一个样品的苯酚和浓硫酸,这样显色更稳定。实验中发现,倘若对所有样品全加完苯酚混匀后,再统一加浓硫酸,显色及不稳定,标准曲线甚至不成线性。苯酚易挥发,长时间与空气接触也容易被氧化,造成结果不稳定。[/align][align=center][img=,300,287]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230848_01_3246897_3.jpg[/img][/align][align=center]图 5 苯酚-硫酸法检测多糖含量[/align][align=left]图5为苯酚硫酸法侧多糖含量的标准曲线和样品,采用了单个样品加完苯酚和浓硫酸后再加另一个样品的苯酚好浓硫酸,显色稳定有规律,经过分光光度计检测,线性良好,样品数据平行,能够有效避免苯酚-硫酸法重现性差这一缺点。[/align]3. 结论采用苯酚-硫酸法检测保健品中粗多糖含量时,针对各种基质进行相应的脱脂操作、增加回流前的醇沉时间、进行显色反应时加入苯酚后混匀立即加入浓硫酸,能够使检测的数据更可靠、稳定。

[align=center]均匀设计实验优化茵陈多糖的提取工艺[/align][align=center]摘 要[/align][align=center] [/align][b]目的:[/b]探索提取温度、液固比和提取时间对茵陈多糖产率的影响,得到提取茵陈多糖最优工艺条件。[b]方法:[/b]用均匀设计实验优化茵陈多糖的提取工艺,用苯酚硫酸法测出每次实验所得多糖的纯度,再求得每次实验纯多糖的得率,然后应用回归分析的方法分析实验得出的数据,以纯多糖的得率为指标,对提取温度、液固比和提取时间3个因素进行分析,得出最佳工艺条件,并进行验证。[b]结果:[/b]实验得出茵陈多糖的最佳提取条件是:提取温度100℃、提取时间80 min、提取液固比55:1。[b]结论:[/b]验证实验平均得率为1.96%,预测值是2.00%,二者很接近,说明我们得到的最佳工艺条件是可靠的。关键词:茵陈多糖;提取工艺;均匀设计Optimize the ExtractionProcess of Herba artemisiae polysaccharide by Uniform Design ExperimentsABSTRACT[b]Objective: [/b]Study the effect of extraction temperature, liquid-solidratio and extraction time on the yield of Herba artemisiae polysaccharide, andthen get the optimal process conditions of extraction. [b]Methods:[/b] optimize the extraction process of Herba artemisiae polysaccharideby uniform design experiments, measure the purity of polysaccharide obtained ineach experiment by the phenol-sulfuric acid method, and calculate the yield of purepolysaccharide in each experiment, then use the regression analysis to analyzethe experimental data, the yield of pure polysaccharides as the indicators, getthe conclusion and verify it.[b] Result: [/b]thebest extraction condition of Herba artemisiae polysaccharide is: 100℃ as the extraction temperature, 80 min asthe extraction time and 55:1 as the extraction liquid-solid ratio.[b]Conclusion: [/b]the result of verification test is 1.96%, and the predictedvalues is 2.00%.They are very close. So the technological conditions isreliable.[b]Key words:[/b]Herba artemisiae polysaccharide Extraction process Uniform design[color=windowtext][/color][align=center]1 前言[/align]多糖,又称为多聚糖,是由十个以上的单糖通过苷键连接而成的聚合物[sup][/sup]。多项研究表明,多糖具有增强免疫功能、抗肿瘤、降血糖、抗衰老、抗病毒等功能[sup][/sup]。具有生物学功能的多糖被称为“生物应答效应物”或活性多糖[sup][/sup],事实上大多数多糖为活性多糖,主要存在于菌类、藻类、根茎类药材中[sup][/sup],本实验所探究的多糖为茵陈多糖,茵陈属于全草类药材。茵陈为菊科植物滨蒿[i]Artemisia scoparia Waldst.et Kit.[/i]或茵陈蒿[i]Artemisia capillariesThumb.[/i]的干燥地上部分[sup][/sup]。应在春季幼苗高6-10cm时采收或秋季花蕾长成花初开采割,除去杂质和老茎,晒干[sup][/sup],采摘的季节不同,茵陈可分为绵茵陈和花茵陈两种,春季采摘的名为绵茵陈,秋季采摘的名为花茵陈[sup] [/sup]。茵陈生产地在我国分布广泛,不同生产地生产的茵陈质量不同,优良的茵陈性状应为多卷曲成松散的团状,灰白色或灰绿色,全体密被白色茸毛,绵软如绒,气清香,味微苦[sup][/sup]。味苦、辛、微寒、无毒,归脾、胃、肝、胆经[sup][/sup]。结合古时和现代医学研究,茵陈多糖具有利胆、护肝、调脂降压、抗菌、抗肿瘤、抗动脉粥样硬化、抗氧化、清热解毒等功效[sup][/sup]。多糖的提取方法很多,大体上包括溶剂浸提法、酶法、超声波辅助提取法、微波辅助提取法和超临界流体萃取法[sup][/sup]。本实验采用水提醇沉法对茵陈多糖进行提取,虽然该方法提取工艺中要求要控制温度、时间、加水量等,但该方法工艺简单,适合在实验室操作。本实验采用的方法为均匀设计法,在条件范围变化大而需要进行多水平实验的情况下,它能够极大的减少实验的次数,只需要与因素水平数相等次数的q,本实验即可获得正交设计的至少做q[sup]2[/sup]组实验所能获得的实验结果。[align=center]2 实验部分[/align]2.1 实验仪器和试剂752型紫外可见分光光度计(上海恒平科学仪器公司)CPJ1003型电子天平(上海奥豪斯仪器有限公司)HH-1型恒温水浴锅(金坛市晶玻实验仪器厂)80-2离心机(上海荣泰生化工程有限公司)RE-52A旋转蒸发仪(上海亚荣生化仪器厂)GZX-9070数显鼓风干燥箱(上海博讯实业有限公司医疗设备厂)ZKXF-1型真空干燥箱(郑州南北仪器设备有限公司)SHD-Ⅲ型循环水式多用真空泵(保定市新区阳光科教仪器厂)20目,100目标准筛(浙江上虞市华丰五金仪器有限公司)[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url](上海佳安分析仪器厂)茵陈(河北省安国药材市场,经本考研室徐红欣老师鉴定)无水乙醇(分析纯,天津市富宇精细化工有限公司)蒸馏水(实验室自制)葡萄糖(分析纯,天津市科密欧化学试剂有限公司)苯酚(分析纯,天津市福晨化学试剂厂)浓硫酸(分析纯,北京化工厂)2.2 茵陈粗多糖提取1、将茵陈在70℃真空干燥3h,然后用粉碎机粉碎,取20目~100目的粉末,置于干燥器中,备用。[img=,72,4]https://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img]2、精密称取2.5g的茵陈,加入规定液固比的蒸馏水,在设定温度下水浴加热回流t小时。3、先用脱脂棉过滤,再用布氏漏斗抽滤,滤液旋转蒸发直至滤液浓缩至约10mL。4、将浓缩的滤液置具塞锥形瓶中,再加30mL的无水乙醇,放入冰箱中,4℃放置24小时。5、将溶液转移至离心管内,并在3000rpm下离心10min,弃去上清液,取沉淀。6、50℃真空干燥3.5h后,过夜,取出,放凉,称重,计算产率。其中,液固比、提取时间t根据实验过程中考察因素的改变,作相应的更改,其他条件保持一致。2.3 均匀设计实验 本实验依据之前单因素实验结果,确定了温度、液固比和提取时间这三个因素的取值范围,在这个基础上,用茵陈的粗多糖的提取率作为指标,初步确定茵陈多糖的提取条件,再以纯糖的最终收率确定茵陈多糖最优提取条件。首先在茵陈质量一定的前提下,分别设定不同的提取温度、提取时间及料液比,探索它们对茵陈粗多糖提取率的影响。提取完粗多糖,得到茵陈多糖的提取条件,进而再以苯酚-硫酸法测定每组实验的纯糖含量,计算纯糖的收率,并以其作为标准得到茵陈多糖提取的最优条件,最后对最优条件进行验证。2.3.1 设计实验方案依据之前单因素实验结果,我们确定了温度、液固比和提取时间这3个因素的取值范围:提取温度X[sub]1[/sub] :55℃~100℃;液固比X[sub]2[/sub]:30:1~75:1提取时间X[sub]3[/sub]:50min~140min。设计实验方案。每小组均先称量2.5克茵陈,按照设计好的条件对茵陈进行粗多糖的提取,并测定多糖纯度,求得纯多糖产率,方案及结果见表1。[color=red] [/color][align=center]表1 均匀设计实验方案及结果[/align] [table][tr][td] [table][tr][td] [table=100%][tr][td] 条件 编号[/td][/tr][/table] [/td][/tr][/table][img=,98,65]https://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img][img=,84,52]https://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img][/td][td] [align=center]温度(℃)[/align] [/td][td] [align=center]液固比[/align] [align=center](g/mL)[/align] [/td][td] [align=center]时间(min)[/align] [/td][td] [align=center]粗多糖产率(%)[/align] [/td][td] [align=center]纯多糖产率(%)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]55[/align] [/td][td] [align=center]50:1[/align] [/td][td] [align=center]110[/align] [/td][td] [align=center]12.12[/align] [/td][td] [align=center]1.13[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]60[/align] [/td][td] [align=center]75:1[/align] [/td][td] [align=center]70[/align] [/td][td] [align=center]11.72[/align] [/td][td] [align=center]1.03[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]65[/align] [/td][td] [align=center]45:1[/align] [/td][td] [align=center]140[/align] [/td][td] [align=center]13.57[/align] [/td][td] [align=center]1.14[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]70[/align] [/td][td] [align=center]70:1[/align] [/td][td] [align=center]100[/align] [/td][td] [align=center]14.93[/align] [/td][td] [align=center]1.35[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]75[/align] [/td][td] [align=center]40:1[/align] [/td][td] [align=center]60[/align] [/td][td] [align=center]14.39[/align] [/td][td] [align=center]1.29[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]80[/align] [/td][td] [align=center]65:1[/align] [/td][td] [align=center]130[/align] [/td][td] [align=center]13.22[/align] [/td][td] [align=center]1.54[/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]85[/align] [/td][td] [align=center]35:1[/align] [/td][td] [align=center]90[/align] [/td][td] [align=center]13.64[/align] [/td][td] [align=center]1.74[/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]90[/align] [/td][td] [align=center]60:1[/align] [/td][td] [align=center]50[/align] [/td][td] [align=center]13.24[/align] [/td][td] [align=center]1.28[/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]95[/align] [/td][td] [align=center]30:1[/align] [/td][td] [align=center]120[/align] [/td][td] [align=center]16.32[/align] [/td][td] [align=center]2.36[/align] [/td][/tr][tr][td] [align=center]10[/align] [/td][td] [align=center]100[/align] [/td][td] [align=center]55:1[/align] [/td][td] [align=center]80[/align] [/td][td] [align=center]21.59[/align] [/td][td] [align=center]2.42[/align] [/td][/tr][/table]2.3.2 标准曲线的绘制储备液的制备:精密称取葡萄糖0.1246g,加蒸馏水溶解,转移于100mL容量瓶中,再加蒸馏水至刻度,最后摇匀得124.6mg/L的储备液,备用。标准液的制备:准备5个25mL容量瓶,分别标注1.0mL、0.8mL、0.6mL、0.4 mL、0.2 mL,再分别精密量取储备液1.0 mL、0.8 mL、0.6 mL、0.4 mL、0.2 mL,相应置于25 mL的容量瓶中,加水至刻度,摇匀,则得5个不同浓度的标准液,备用。5%苯酚溶液的制备:称取苯酚1.2512g于烧杯中,用约50℃的蒸馏水溶解,转移至25mL的容量瓶中,加水至刻度,摇匀,备用。标准曲线的绘制:准备6个具塞试管,分别标注1、2、3、4、5、6,先用蒸馏水润洗过的2mL移液管移取2mL蒸馏水于1号具塞试管,然后用相对应的标准溶液润洗过的2 mL移液管分别取2 mL标准溶液于具塞试管中(0.2 mL的标准液对应2号管,0.4 mL的标准液对应3号管,以此类推)。接着用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]移取1 mL 5%的苯酚溶液,快速加入上述具塞试管中,充分混匀,再用5 mL移液管移取5 mL浓硫酸快速加入上述试管中,充分摇匀,盖好试管塞(6个试管之间加硫酸间隔5min)。沸水浴15min,冷水浴10min,室温放置5min,最后分别在490nm处测定吸光度,以吸光度A为纵坐标,以葡萄糖标准溶液C为横坐标,绘制标准曲线。(见图1)标准曲线的线性范围为:0.10072×10[sup]-4[/sup]mg/mL ~ 0.50360×10[sup]-4[/sup]mg/mL曲线方程:A=0.0146C+0.074,相关系数:r[sup]2[/sup]=0.9992[align=center][img=,475,288]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261745237707_581_3237657_3.png!w475x288.jpg[/img][/align]图1 标准曲线[align=center] [/align]2.3.3 苯酚-硫酸法测多糖含量1、分别取上述实验所得粗多糖约0.0600g于小烧杯中,加少量60℃蒸馏水搅拌使其溶解,转移至250mL容量瓶中,加蒸馏水至刻度,摇匀。2、分别用布氏漏斗抽滤,取部分滤液,然后用该滤液润洗2mL移液管,移取2mL上述溶液于具塞试管中。3、再分别用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]移取1mL 5%的苯酚溶液,快速加入上述具塞试管中,充分混匀。4、接着用5mL移液管取5mL浓硫酸快速加入上述试管中,充分摇匀,盖好试管塞(两管加入浓硫酸时间间隔为5min)。紧接着放入沸水浴15min,冷水浴10min,室温放置5min。5、在490nm处测定其吸光度。(备注:每次测多糖的吸光度需配制空白对照用来校正可见分光光度计。)将测得的吸光度带入标准曲线方程中计算出所配溶液的多糖浓度,进而得到纯多糖的质量,再除以所称茵陈样品的质量,即为纯多糖得率,结果见表1。2.4 最优提取条件的确定用SPSS 19.0统计软件,以纯多糖得率为评价指标对各因素进行线性回归分析,模型的优度通过复相关系数和方差分析来判定。结果如表2。表2 回归方程 [table=638][tr][td] [align=center] [/align] [/td][td] [align=center]回归方程式[/align] [/td][td] [align=center]R[/align] [/td][td] [align=center]P[/align] [/td][/tr][tr][td] [align=center]回归方程1[/align] [/td][td] [align=center]Y=0.023X[sub]1[/sub]-0.008X[sub]2[/sub]+0.002X[sub]3[/sub][/align] [/td][td] [align=center]0.990[/align] [/td][td] [align=center]0.000[/align] [/td][/tr][tr][td] [align=center]回归方程2[/align] [/td][td] [align=center]Y=0.020X[sub]1[/sub][/align] [/td][td] [align=center]0.985[/align] [/td][td] [align=center]0.000[/align] [/td][/tr][/table]表2中,Y为纯多糖得率,X1为提取温度,X2为液固比,X3为提取时间。方程1,R[sup]2[/sup]= 0.971,P值为0.000,回归非常显著, X1项P值为0.000小于0.01,回归非常显著,有统计意义,而X2,X3均回归不显著,方程1多糖产率预测值为2.17%;方程2为将各项及其交叉乘积项全部纳入进行逐步回归的结果,我们发现,最后的方程中只保留了X1项,方程2的 R[sup]2[/sup]= 0.976,X1项P值为0.000,小于0.01,回归亦非常显著有效,其预测值为2.00%。 综合上述两方程的回归结果,及均匀设计和单项实验的结果,我们采取提取温度100℃、提取时间为80 min、提取液固比为55:1,即第10组的条件为最佳条件。2.5 最优提取条件的验证均匀设计实验优选出了茵陈多糖提取的最佳条件,即提取温度为100℃、提取时间为80 min、提取液固比为55:1。按照上述茵陈多糖的提取及苯酚-硫酸法测多糖含量测定的实验流程,对最优条件进行3次重复实验,粗多糖及纯多糖的产率均列于表3中。[align=center]表3 最优提取条件测得的多糖含量[/align] [table][tr][td] [align=center]实验编号[/align] [/td][td] [align=center]粗多糖得率(%)[/align] [/td][td] [align=center]纯多糖得率(%)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]22.61[/align] [/td][td] [align=center]1.95[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]21.24[/align] [/td][td] [align=center]2.04[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]18.55[/align] [/td][td] [align=center]1.88[/align] [/td][/tr][tr][td] [align=center]平均值[/align] [/td][td] [align=center]20.80[/align] [/td][td] [align=center]1.96[/align] [/td][/tr][/table][align=center]3 结果与讨论[/align]3.1 实验结果本实验采用水提醇沉法对茵陈多糖进行提取,在单因素实验结果基础上,通过对液固比、提取时间、提取温度等3个可控条件进行均匀设计实验,结合实验结果得出来的数据,确定了茵陈多糖提取的最优条件,并利用该最优条件测定了茵陈多糖的含量,计算出了纯多糖的得率。结果如下:[align=center]表4 茵陈多糖提取最优条件及多糖含量[/align] [table][tr][td=4,1] [align=center]最优提取条件[/align] [/td][td=1,2] [align=center]粗多糖得率[/align] [align=center](%)[/align] [/td][td=1,2] [align=center]纯多糖得率[/align] [align=center](%)[/align] [/td][/tr][tr][td] [align=center]提取温度[/align] [/td][td] [align=center]提取液固比[/align] [/td][td] [align=center]提取时间[/align] [/td][td] [align=center]提取次数[/align] [/td][/tr][tr][td] [align=center]100℃[/align] [/td][td] [align=center]55:1[/align] [/td][td] [align=center]80 min[/align] [/td][td] [align=center]1次[/align] [/td][td] [align=center]20.80[/align] [/td][td] [align=center]1.96[/align] [/td][/tr][/table]3.2 讨论(1)本实验采取的是水提醇沉法,所以在提取粗多糖时,除被考察因素温度、液固比、提取时间按要求改变外,其他条件均应保持一致,如旋蒸时的温度、水浴水位高度、干燥时的真空度,离心时的转速和时间等。若条件不一致,可能造成实验结果的误差。(2)粗多糖在真空干燥时,温度不宜过高,应在50~60℃之间,过低的温度不能将粗多糖干燥彻底,过高的温度则容易使粗多糖碳化,造成误差。(3)在旋转蒸发时,除要保证水位大致一样时,旋转时还要注意避免溶液爆沸,导致溶液进入,造成实验误差。(4)在绘制标准曲线时需注意以下几点:1、配制溶液过程中,需要将溶液转移至容量瓶时,一定得精确至刻度,并且摇匀。2、在移液时要准确迅速,用同一移液管,并且在转移之前要用相对应的溶液润洗。3、再加苯酚和浓硫酸后,要迅速充分摇匀,加浓硫酸的间隔时间个人建议为5分钟,因为间隔时间过短容易手忙脚乱导致误差。参考文献 娜日苏.天然植物多糖及复合多糖的研究进展.赤峰学院学报,2009,25(1):68~68 王超,康立源.中药多糖的药理研究进展.世界科学技术—中医药现代化,2008,10(3):82~82 刘占峰,孙汉文.多糖的化学修饰研究进展 .河北大学学报,2005,25(1):104~104 韩伟,黄兮,张玲玲,等.中药多糖的提取、分离纯化及分析方法的研究进展.工程工艺与设备,2012,332(14):19 王茜.茵陈的药理作用及其主要化学成分药物代谢动力学研究进展 .安徽中医学院学报,2012,31(4):88~88 孙涛,陈炜.茵陈药理作用研究进展.中药与临床,2010,1(3):59~59 姜波,焦文霞.茵陈的古今临床应用.中国名族民间医药,2011,21(3):36~36 温俊达,张水寒,凌翔,等.道地药材绵茵陈的生药学鉴别.时针国医国药,2007,18(3):555~556 温建炫,沈歆,孙晓泽,等.应用“动-定序贯八法”理论对茵陈药性再认识.时珍国医国药,2013,23(1):224~224 孙涛,陈炜.茵陈药理作用研究进展.中药与临床,2010,1(3):59~59 尹艳,高文宏,于淑娟.多糖提取技术的研究进展.食品工业科技,2007,28(2):248~250
请问植物多糖~就是纤维素多糖是酸性还是碱性?
最新发现与创新 科技日报上海6月29日电(记者左朝胜)今天,在上海浦东召开的化学糖生物学国际研讨会上,中科院上海药物研究所无限极多糖联合实验室公布了他们的最新研究成果:肠道为香菇多糖(Lentinan)等中草药多糖预留的秘密通道被发现。这些中草药多糖可以经由该通道被人体完整吸收,进而随血液达到全身各处,发挥其各种生物生理功效。 多糖是自然界中含量最丰富的物质之一,广泛存在于动物细胞膜、植物和微生物细胞壁中,对维持生命活动起着至关重要的作用。大量药理和临床研究发现,多糖、特别是中草药多糖,具有调节免疫、抗辐射、抗肿瘤、抗病毒、抗衰老、调节血糖、保护胃肠系统等作用。自1986年日本批准香菇多糖应用于临床以来,目前在中国、美国、韩国、日本及一些欧洲国家,已有几十种多糖被批准应用于疾病的治疗或辅助治疗。同时,多糖还被广泛应用于保健食品。 但由于多糖的分子量一般都很大,如果一个水分子相当面包屑那么大的话,一个高活性多糖分子起码会像一个汉堡包。水分子可以自由进出肠道壁细胞,多糖也可以吗?这个问题一直困惑着中外科学家。 2009年,中科院上海药物研究所丁侃研究员与无限极(中国)有限公司联合开展多糖吸收机制研究,经过几年努力,利用Caco-2细胞、多糖荧光标记等手段,终于找到了肠道给多糖预留的秘密通道——clathrin蛋白。 多糖可借助clathrin蛋白进入肠道细胞内,然后再进入毛细血管,随血液到达全身各处,与其受体结合发挥各种生物活性。该研究成果得到了美国功能性糖组学协会、国际糖复合物组织的赞赏和肯定,并得到世界各国多糖研究领域专家的关注。这项成果为多糖各种生理功效的活性机制研究奠定了坚实的基础,不但为口服吸收与口服有效提供了新依据,而且为多糖靶向治疗提供了可能性。 《科技日报》(2013-6-30 一版)

[b]摘要:目的:[/b]探索提取温度、液固比和提取时间对拳参多糖产率的影响,得到提取[color=#000000]拳参[/color]多糖最优工艺条件。[b]方法:[/b]用均匀设计实验优化[color=#000000]拳参[/color]多糖的提取工艺,用苯酚硫酸法测出每次实验所得多糖的纯度,再求得每次实验纯多糖的得率,然后应用回归分析的方法分析实验得出的数据,以纯多糖的得率为指标,对提取温度、液固比、提取次数和提取时间3个因素进行分析,得出最佳工艺条件,并进行验证。[b]结果:[/b]实验得出茵陈多糖的最佳提取条件是:提取温度100℃、提取时间135 min、提取液固比55:1。[b]结论:[/b]验证实验平均得率纯多糖实际产率5.95%与理论得率5.79%十分接近,说明我们得到的最佳工艺条件是可靠的。[align=center]1 前言[/align]拳参又名紫参,草河车,为蓼科蓼属多年生草本植物拳参[i]Polygonum bistirta[/i] L.的干燥根茎。拳参一名最早出现在《本草图经》中,其性状呈扁圆形而弯曲,两端钝圆或稍尖,质硬脆,易折断,断面棕红或赤褐色,无嗅,其性苦、涩、微寒,具有清热解毒,凉肝熄风,消肿止血的功效。临床上用于赤痢,热泻,肺热,咳嗽,痈肿,瘰疬,口舌生疮,吐血,痔疮出血,毒蛇咬伤的治疗[sup][/sup]。近十几年来研究表明,拳参的化学成分多样,主要有绿原酸、丁二酸、没食子酸、儿茶素及鞣质等。刘晓秋等[sup][/sup]从拳参的乙醇提取物中得到9个化合物,经理化常数和光谱分析,确定为没食子酸、丁二酸、槲皮素、槲皮素-5-O-β-D-吡喃葡萄糖苷、原儿茶酸[sup][/sup]、丁香苷、(+)-儿茶素、芦丁及mururin A。孙晓白[sup][/sup]对拳参根茎的化学成分进行了系统的研究,干燥根茎粉碎后用95%甲醇浸泡提取3次,减压浓缩后,依次用石油醚,乙酸乙酯,正丁醇萃取,再通过硅胶柱层析,葡聚糖柱层析,制备薄层层析和重结晶等手段,得到了20个化合物,并确定了其中的3β-acetoxy-dammara-20、24-diene、Ferenemone等17个化合物结构。肖凯等[sup][/sup]用60%的丙酮对拳参根茎进行提取,并用反向层析的方法进行分离纯化,得到10个化合物,最终确定为没食子酸、色氨酸、2,6-二羟基苯甲酸等。现代药理研究表明拳参有抗菌作用、镇痛作用、中枢抑制作用、心肌保护作用等,临床用于治疗菌痢、肠炎、肺结核、婴幼儿秋冬腹泻、湿热型痢疾等[sup][/sup]。曾靖等[sup][/sup]通过实验表明拳参的镇痛作用与氨基比林相当。刘晓秋等[sup][/sup]通过采用斜面法测定拳参各提取物和单体化合物的最低抑菌浓度,研究了拳参根茎中得到的5种不同溶剂提取物及4种单体化合物的体外抑菌活性。刘春棋等[sup][/sup]过滤纸片对拳参提取物进行了抑菌试验,结果发现不同浓度的拳参提取物对金黄色葡萄球菌和大肠杆菌有一定的抑菌效果。eepak Mittal[sup][/sup] 研究了拳参提取了拳参及其活性成分对四氯化碳和扑热息痛所造成的肝损伤的保护作用。李洪亮在首届全国方剂组成原理高峰论坛上发表的论文[sup][/sup]研究发现拳参-413本身对正常血管无明显作用,在NA致血管收缩的前提下,拳参-413对大鼠离体胸动脉环具有显著的剂量依赖性舒张作用。曾纪荣、曾庆磊等[sup][/sup]研究了拳参提取物在大鼠视网膜缺血再灌注损伤时抗氧化作用的影响。曾昭毅、王敏等[sup][/sup]用昆明小鼠证明拳参水提物有与氨基比林、吗啡相当的镇痛作用,并认为其镇痛作用并非通过阿片受体而发挥。李珂珂、栾希英等[sup][/sup]探讨了拳参水提物对正常小鼠免疫功能的影响。李珂珂、栾希英[sup][/sup]研究了拳参乙醇提取物(BRE)的免疫调节作用。近年来国内外对拳参的研究日趋深入,有关其化学成分和药理活性方面的研究已进行了一定量的工作,但通过查阅资料,关于拳参多糖的文献较少,说明目前对于拳参多糖的研究鲜有报道。因此,本课题拟对拳参多糖的提取工艺进行研究,对拳参多糖的提取条件进行优化,从而为拳参多糖的深入开发利用提供实验依据。本课题我们就重点探讨拳参多糖的最佳提取条件,通过对拳参多糖提取过程中影响拳参多糖产率、纯度的因素进行单因素实验,单因素实验包括提取时间、提取温度、液固比及提取次数,最终确定最优提取时间为2.5h,提取温度为100℃,液固比为20:1。然后根据单因素最优条件进行均匀设计实验,用线性回归的分析方法分析实验得出的数据,找出拳参多糖的最佳提取条件。[align=center]2 实验材料与方法[/align]2.1 实验仪器CPJ1003型电子天平(上海奥豪斯仪器有限公司)HH-1数显恒温水浴锅(金坛市晶玻实验仪器厂)80-2离心机(上海荣泰生化工程有限公司)RE-52A旋转蒸发仪(上海亚荣生化仪器厂)GZX-9070电热恒温鼓风干燥箱(上海博讯实业有限公司医疗设备厂)ZKXF-1型真空干燥箱(河北荣昌试验仪器厂)SHD-Ⅲ型循环水式多用真空泵(保定市新区阳光科教仪器厂)BCD-223MT冰箱(河南新飞电器有限公司)752型紫外可见分光光度计(上海恒平科学仪器公司)24目,100目标准筛(浙江上虞市华丰五金仪器有限公司)2.2 实验材料和试剂拳参(河北省安国药材市场)无水乙醇(分析纯,天津市富宇精细化工有限公司)蒸馏水(实验室自制)葡萄糖(分析纯,天津市科密欧化学试剂有限公司)苯酚(分析纯,天津市福晨化学试剂厂)浓硫酸(分析纯,北京化工厂)2.3 实验方法步骤2.3.1拳参的前处理拳参粉碎,放入真空烘箱中,70℃干燥2h,过24目筛得到拳参粉,备用。2.3.2粗多糖的提取流程拳参粗多糖提取的实验流程如下:精确称取拳参粉约5.0g于500mL圆底烧瓶中,加入规定液固比的蒸馏水,用恒温水浴锅T℃加热不同时间,先用脱脂棉过滤,然后用布氏漏斗抽滤,将滤液浓缩(旋转蒸发)至约10mL,加95%乙醇30mL,置具塞锥形瓶中,冰箱4℃放置24mL,然后用10mL试管离心(4000rpm,20min),弃去上清液,取沉淀,于50℃真空干燥箱干燥过夜,然后将所得沉淀称重,并计算粗多糖产率。其中,液固比、提取温度T、提取时间t及提取次数根据实验过程中考察因素的改变,作相应更改。2.3.3粗多糖产率的计算实验提取出的拳参粗多糖,经过烘干后,置于电子分析天平称重,得出的数据除以样品重量,即可得出拳参粗多糖的产率。2.3.4单因素实验2.3.4.1 液固比对拳参粗多糖提取率的影响采用提取温度80 ℃,加热2.5h,提取1次,考察了液固比对提取收率的影响。在结合前人相关中药材实验的基础上,确定考察液固比为10:1、20:1、30:1、40:1。粗多糖产率见表2-1。 表2-1 液固比对粗多糖提取率的影响 [table][tr][td] [align=center] 液固比(mL/g)[/align] [/td][td] [align=center]10:1[/align] [/td][td] [align=center]20:1[/align] [/td][td] [align=center]30:1[/align] [/td][td] [align=center]40:1[/align] [/td][/tr][tr][td] 粗多糖产率(%)[/td][td] [align=center]7.61[/align] [/td][td] [align=center]10.86[/align] [/td][td] [align=center]10.14[/align] [/td][td] [align=center]9.18[/align] [/td][/tr][/table]2.3.4.2 提取温度对拳参粗多糖提取率的影响采用液固比为20:1,提取时间2.5h,提取1次,考察了提取温度对粗多糖得率的影响。本实验确定考察温度为60℃、70℃、80℃、90℃、100℃。粗多糖产率见表2-2。[align=center]表2-2 提取温度对粗多糖提取率影响[/align] [table][tr][td] [align=center]提取温度[/align] [/td][td] [align=center]60℃[/align] [/td][td] [align=center]70℃[/align] [/td][td] [align=center]80℃[/align] [/td][td] [align=center]90℃[/align] [/td][td] [align=center]100℃[/align] [/td][/tr][tr][td]粗多糖产率(%)[/td][td] [align=center]6.42[/align] [/td][td] [align=center]9.24[/align] [/td][td] [align=center]10.67[/align] [/td][td] [align=center]12.11[/align] [/td][td] [align=center]17.83[/align] [/td][/tr][/table]2.3.4.3 提取时间对拳参粗多糖提取率的影响采用提取温度80 ℃,液固比20:1,提取1次,考察了提取时间对粗多糖得率的影响。通过查阅文献,本实验确定考察时间为1.5h、2h、2.5h、3h、3.5h。粗多糖产率见表2-3。[align=center]表2-3 提取时间对粗多糖提取率的影响[/align] [table][tr][td] [align=center]提取时间(h)[/align] [/td][td] [align=center]1.5[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2.5[/align] [/td][td] [align=center]3[/align] [/td][td]3.5[/td][/tr][tr][td]粗多糖产率(%)[/td][td] [align=center]8.25[/align] [/td][td] [align=center]8.85[/align] [/td][td] [align=center]11.14[/align] [/td][td] [align=center]9.90[/align] [/td][td]8.92[/td][/tr][/table]2.3.4.4 提取次数对拳参粗多糖提取率的影响采用提取温度80 ℃,提取时间2.5h,液固比20:1,考察了提取次数对粗多糖得率的影响。根据前人提取数据,将提取次数定为1次、2次、3次、4次。粗多糖产率见表2-4。[align=center]表2-4 提取次数对粗多糖提取率的影响[/align] [table][tr][td] [align=center]提取次数[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]4[/align] [/td][/tr][tr][td]粗多糖产率(%)[/td][td] [align=center]11.27[/align] [/td][td] [align=center]13.08[/align] [/td][td] [align=center]16.49[/align] [/td][td] [align=center]16.83[/align] [/td][/tr][/table]2.3.5均匀设计实验2.3.5.1 均匀设计实验方案根据单因素实验结果确定各因素的取值范围:提取温度X[sub]1[/sub] :55℃~100℃;料液比X[sub]2[/sub]:1:10~1:37:提取时间X[sub]3[/sub]:1.5h~3.75h,设计出一个3因素10水平的均匀设计表。根据均匀设计表中所列的提取条件,按照拳参粗多糖的提取流程,提取拳参粗多糖,用苯酚硫酸法测定各次实验所得粗多糖含量,计算纯多糖产率,结果见表2-5。[align=center] [/align][align=center]表2-5 均匀设计实验表及结果[/align] [table=519][tr][td] [table][tr][td] [table=100%][tr][td] 条件 编号[/td][/tr][/table] [/td][/tr][/table][img=,98,65]https://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img][img=,84,52]https://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img][/td][td] [align=center]提取温度(℃)[/align] [/td][td] [align=center]液固比[/align] [align=center](mL/g)[/align] [/td][td] [align=center]提取时间(min)[/align] [/td][td] [align=center]纯多糖产率[/align] [align=center](%)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]55[/align] [/td][td] [align=center]22[/align] [/td][td] [align=center]180[/align] [/td][td] [align=center]1.819[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]60[/align] [/td][td] [align=center]37[/align] [/td][td] [align=center]120[/align] [/td][td] [align=center]2.209[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]65[/align] [/td][td] [align=center]19[/align] [/td][td] [align=center]225[/align] [/td][td] [align=center]1.610[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]70[/align] [/td][td] [align=center]34[/align] [/td][td] [align=center]165[/align] [/td][td] [align=center]1.947[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]75[/align] [/td][td] [align=center]16[/align] [/td][td] [align=center]105[/align] [/td][td] [align=center]2.007[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]80[/align] [/td][td] [align=center]31[/align] [/td][td] [align=center]210[/align] [/td][td] [align=center]3.647[/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]85[/align] [/td][td] [align=center]13[/align] [/td][td] [align=center]150[/align] [/td][td] [align=center]3.616[/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]90[/align] [/td][td] [align=center]28[/align] [/td][td] [align=center]90[/align] [/td][td] [align=center]4.717[/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]95[/align] [/td][td] [align=center]10[/align] [/td][td] [align=center]195[/align] [/td][td] [align=center]4.852[/align] [/td][/tr][tr][td] [align=center]10[/align] [/td][td] [align=center]100[/align] [/td][td] [align=center]25[/align] [/td][td] [align=center]135[/align] [/td][td] [align=center]6.595[/align] [/td][/tr][/table]2.3.5.2 标准曲线的绘制标准液的配制:称取葡萄糖0.1246g于100mL容量瓶中,加蒸馏水至刻度,摇匀得124.6mg/L的储备液,分别精密量取储备液1.0mL、0.8mL、0.6mL、0.4mL、0.2mL,置于25mL的容量瓶中,加水至刻度,摇匀。则得5个不同浓度的标准液。配制5%苯酚溶液:称取苯酚1.2512g于烧杯中,用加热至约50℃的蒸馏水溶解,转移至25mL的容量瓶中,加水至刻度,摇匀。标准曲线的绘制:用干燥的2mL移液管取2mL标准溶液于具塞试管中,再用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]移取1mL5%的苯酚溶液,快速加入上述具塞试管中,充分混匀,用5mL移液管取5mL浓硫酸快速加入上述试管中,充分摇匀,盖好试管塞。沸水浴15min,冷水浴10min,室温放置5min(5个储备液之间间隔5min加硫酸)。再将标准液换成蒸馏水,其他操作不变配成空白待测溶液。将上述反应30min后的溶液分别在490nm处测定吸光度,以吸光度A为纵坐标,以葡萄糖标准溶液C为横坐标,绘制标准曲线。(见图2-6)标准曲线的线性范围为:0.10072×10[sup]-1[/sup] mg/mL ~0.50360×10[sup]-1[/sup]mg/mL。曲线方程:A=0.015C+0.0502,相关系数:R[sup]2[/sup]= 0.9997 [align=center] [img=,654,351]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261738563747_2538_3237657_3.png!w654x351.jpg[/img][/align][align=center]图2-6 标准曲线[/align][align=center] [/align]2.3.5.3 苯酚-硫酸法测纯多糖含量分别取均匀设计实验所得粗多糖0.0201g于小烧杯中,加少量水搅拌使其溶解,转移至500mL容量瓶中,加蒸馏水至刻度,摇匀。用2mL移液管移取2mL上述溶液于具塞试管中,再用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]移取1mL5%的苯酚溶液,快速加入上述具塞试管中,充分混匀,用5mL移液管取5mL浓硫酸快速加入上述试管中,充分摇匀,盖好试管塞。沸水浴15min,冷水浴10min,室温放置5min,反应完全后在490nm处测定其吸光度,每次需配制空白对照用来校正可见分光光度计。将测得的吸光度带入标准曲线方程中计算出所配溶液的多糖浓度,进而得到纯多糖的质量,再除以所称拳参样品的质量,即为纯多糖得率,结果见表2-5。 [table][tr][td=1,2][img=,232,45]https://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img][/td][/tr][tr][td=1,2] [table=100%][tr][td][b]×[/b]100%[/td][/tr][/table] [/td][/tr][/table][align=center]3 实验结果[/align]3.1 单因素实验结果3.1.1液固比图3-1表明,液固比在10:1和20:1之间粗多糖得率共提高42.76 %,在20:1到30:1之间以及30:1到40:1之间,反而下降。主要是由于开始增加提取液体积有利于细胞内容物的溶出,而液固比到达20:1之后,多糖成分已基本溶出,故粗多糖得率没有太大增加,并且考虑到工业生产中水的用量,所以液固比20:1最为合适。[align=center][img=,679,328]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261739157427_7789_3237657_3.png!w679x328.jpg[/img][/align][align=center]图3-1 液固比对拳参粗多糖得率的影响[/align]3.1.2提取温度结果见图3-2。由图中可以看出,当温度从60 ℃上升到70 ℃时,粗多糖得率共提高了64.59%,从70℃到80℃,提高了21.40%,80℃到90℃,提高了8.55%,从90℃到100℃,提高了54.77%。随着温度的上升,粗多糖产率一直在增加,说明温度的提高对粗多糖的溶出有帮助。显然,从60℃到70℃时,粗多糖产率上升得最快,从70℃到100℃,产率仍然在上升, 100℃时粗多糖产率达到最高得出粗多糖的最佳提取温度为100 ℃。[align=center][img=,690,332]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261739334261_7804_3237657_3.png!w690x332.jpg[/img][/align][align=center]图3-2 提取温度对拳参粗多糖得率的影响[/align][align=center] [/align]3.1.3提取时间中药材有效药物成分溶出需要一定的时间,较短会造成药物有效成分无法最大限度地溶出,过长的提取时间则会导致有效成分分解。结果见图3-3。可以看出,提取时间超过2.5h后粗多糖得率并未继续增加,反而下降;而2.5h之前,粗多糖得率增加显著,从1.5h到2.5h增加了 35.03%,故2.5h为最佳提取时间。[align=center][img=,690,354]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261739498948_3879_3237657_3.png!w690x354.jpg[/img][/align][align=center]图3-3 提取时间对拳参粗多糖得率的影响[/align]3.1.4提取次数结果见图3-4。结果发现:提取4次时粗多糖得率最高,比1次提取提高了49.33%,差别显著,提取三次较之提取一次,提高了46.32%,而提取两次较提取一次,仅提高了16.06%,提高有限,确定最佳提取次数为3次。[align=center][img=,684,350]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261740048693_1694_3237657_3.png!w684x350.jpg[/img][/align][align=center]图3-4 提取次数对拳参粗多糖得率的影响[/align][align=center] [/align]3.2 均匀设计实验结果最优提取条件的选择:用SPSS 19.0统计软件,以纯多糖得率为评价指标对各因素进行线性回归分析,模型的优度通过复相关系数和方差分析来判定。结果如表3-5。表3-5 回归方程 [table=638][tr][td] [align=center] [/align] [/td][td] [align=center]回归方程式[/align] [/td][td] [align=center]R[/align] [/td][td] [align=center]P[/align] [/td][/tr][tr][td] [align=center]回归方程1[/align] [/td][td] [align=center]Y=-6.090+0.109X[sub]1[/sub]+0.035X[sub]2[/sub]+0.001X[sub]3[/sub][/align] [/td][td] [align=center]0.933[/align] [/td][td] [align=center]0.005[/align] [/td][/tr][tr][td] [align=center]回归方程2[/align] [/td][td] [align=center]Y=-4.559+0.101X[sub]1[/sub][/align] [/td][td] [align=center]0.917[/align] [/td][td] [align=center]0.000[/align] [/td][/tr][/table]表3-5中,Y为纯多糖得率,X[sub]1[/sub]为提取温度,X[sub]2[/sub]为液固比,X[sub]3[/sub]为提取时间。方程1,R[sup]2[/sup]= 0.870,P值为0.005,回归非常显著,常数项与X[sub]1[/sub]项P值分别0.037和0.001,均小于0.05 ,回归显著,有统计意义,而X[sub]2[/sub],X[sub]3[/sub]均回归不显著,方程1多糖产率预测值为5.59%;方程2为将各项及其交叉乘积项全部纳入进行逐步回归的结果,我们发现,最后的方程中只保留了X[sub]1[/sub]项,方程2的 R[sup]2[/sup]= 0.841,常数项与X[sub]1[/sub]项P值分别为0.037和0.001,均小于0.05,回归亦显著有效,其预测值为5.79%,因第二个方程更为有效,故我们采用预测值5.79%。 综合上述两方程的回归结果,及均匀设计和单因素实验结果,我们采取提取温度100℃、提取时间为135 min、提取液固比为25:1,即第10组的条件为最佳条件,并重复3次进行实验验证。结果如下:[align=center]表3-6 均匀设计最优条件验证[/align] [table][tr][td]实验编号[/td][td]1[/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][/tr][tr][td]纯多糖产率(%)[/td][td] [align=center]6.07[/align] [/td][td] [align=center]5.80[/align] [/td][td] [align=center]5.97[/align] [/td][/tr][tr][td]平均(%)[/td][td=3,1] [align=center]5.95[/align] [/td][/tr][/table]所得纯多糖实际产率5.95%与理论得率5.79%十分接近。[align=center]4 讨论[/align](1)在研究粗多糖提取过程中单因素变量时,要保证单一变量,其他操作平行一致,若无法保证单一变量,则可能造成实验结果的误差。(2)在绘制标准曲线及用苯酚-硫酸法测多糖含量时,加硫酸时应均匀快速加入,并用力摇匀,若震摇过慢,硫酸会直接氧化苯酚,导致硫酸不能与糖类反应完全,造成误差。并在测量时保证每组的反应时间一致。(3)用苯酚-硫酸法测多糖含量时,为使测得的吸光度在标准曲线的吸光度范围之内,使其能用该标准曲线进行计算。(4)拳参多糖提取次数虽然提取3次比提取1次粗多糖产率高,但所用提取溶剂较多,且粗多糖提取量较所用时间及用料性价比不高,故采用提取1次。均匀设计法通过提高实验点均匀分散程度,使实验点具有更好的代表性,可通过较少的实验获得较多的信息,使实验结果更准确。实验得到的数据对于今后的实验研究、生产活动具有很强的指导意义。参考文献 国家药典委员会.中华人民共和国药典(一部). 北京: 化学工业出版社, 2000:239 刘晓秋, 陈发奎, 吴立军, 等.拳参的化学成分.沈阳药科大学学报, 2004, 21(5): 187~189 刘晓秋, 李维维, 生可心, 等.拳参正丁醇提取物的化学成分.沈阳药科大学学报, 2006, 1(23): 15~17 孙晓白.拳参和黄帚橐吾化学成分研究.兰州大学研究生学位论文, 2007, 5 肖凯, 宣立江, 徐亚明, 等.拳参的DNA裂解活性成分研究.中草药 2003, 34(3): 203~206 李兴玉, 李兴奎.中药拳参的研究进展.国际中医中药杂志, 2008, 30(6): 471~473 曾靖, 单热爱, 钟声, 等.拳参水提取物镇痛作用的实验观察.中国临床康复, 2005, 9(6): 80~81 刘晓秋, 李维维, 李晓丹, 等.拳参提取物及单体化合物的体外抑菌活性初步研究.中药材,2006, 9(1): 51~53 刘春棋, 王小丽, 曾靖.拳参提取物抑茵活性的初步研究.赣南医学院学报, 2006, 26(4): 489~450 Mittal Deepak Kumar*, Joshi Deepmala,Shukla Sangeeta. Hepatoprotective effects of Polygonum bistorta and activeprinciples on albino rats intoxicated with carbon tetrachloride and paracetamol. Toxicology Letters 2009, 189(1): 226~233 李洪亮, 贺方兴, 孙立波, 等.拳参-413对大鼠离体胸主动脉环的舒张作用机制研究.安徽农业科学, 2012, 40(24):12005~12006 曾纪荣, 曾庆磊, 谢明红, 等.视网膜缺血再灌注损伤后拳参提取物对大鼠抗氧化作用的影响.2011, 31(3): 332~333 曾昭毅, 王敏, 叶和扬, 等.拳参水提物的镇痛作用.中国临床康复, 2006, 10(47): 199~201 李珂珂, 栾希英, 刘现兵, 等.拳参水提物对小鼠免疫功能的影响.中药材, 2010, 33(8):1302~1306 李珂珂, 栾希英.拳参乙醇提取物的免疫调节作用.中国现代应用药学, 2011, 28(1): 21~25
[b][font=宋体]藤三七[/font][font=宋体]总[/font][font=宋体]多糖的制备、鉴别与纯度检查[/font][font=宋体]及提取[/font][font=宋体]条件优化[/font][/b][font=宋体]1.[/font][font=宋体]样品预处理[/font][font=宋体]干燥样品经粉碎机粉碎,过[/font]40[font=宋体]目筛,置密封袋中,干燥、避光条件下密封保存[/font][b][font=宋体]2.[/font][font=宋体]可见分光光度法测定条件[/font][/b][font=宋体]精密吸取葡萄糖对照品溶液和供试品溶液适量,置[/font][font=宋体]10 mL[/font][font=宋体]具塞磨口试管中,[/font][font=宋体]加入[/font]5[font=宋体] [/font]%[font=宋体]苯酚溶液[/font]1 mL[font=宋体],充分混匀后,加入浓硫酸[/font]6 mL[font=宋体],[/font]40[font=宋体] [/font][font=宋体]℃反应[/font]20 min[font=宋体],放置室温,在[/font]490 nm[font=宋体]处测得吸光度。[/font][b][font=宋体]藤三七[/font][font=宋体]总[/font][font=宋体]多糖的制备、鉴别与纯度检查[/font][font=宋体]与提取[/font][font=宋体]3.[/font][font=宋体]藤三七[/font][font=宋体]纯化[/font][font=宋体]多糖的制备[/font][/b][font=宋体]取藤三七药材干粉约[/font]10 g[font=宋体],精密称定,[/font][font=宋体]加入石油醚[/font](60[font=宋体]~[/font]90 [font=宋体]℃[/font])100 mL[font=宋体]回流提取两次,每次[/font]2 h[font=宋体],弃去[/font][font=宋体]提取液[/font][font=宋体]([/font][font=宋体]除去[/font][font=宋体]脂溶性成分[/font][font=宋体])[/font][font=宋体],药渣烘干,用[/font]80[font=宋体] [/font]%[font=宋体]乙醇[/font]100 mL[font=宋体]浸泡过夜,回流提取[/font]2[font=宋体]次,每次[/font]2 h[font=宋体]。弃去提取液[/font]([font=宋体]除去单糖、低聚糖[/font][font=宋体]和苷类等小分子物质[/font])[font=宋体],药渣烘干,[/font][font=宋体]加蒸馏水[/font]100 mL[font=宋体]回流,提取三次,每次[/font]2 h[font=宋体]。合并提取液,减压浓缩至[/font]40 mL[font=宋体],[/font][font=宋体]即得粗多糖的水溶液。[/font][font=宋体]在粗多糖水溶液中加入[/font]Sevage[font=宋体]试剂[/font][font=宋体]([/font][font=宋体]氯仿:正丁醇[/font][font=宋体]=[/font]4[font=宋体]:[/font]l[font=宋体])[/font]10 mL[font=宋体],剧烈震荡[/font]20 min[font=宋体],使其充分混合,在[/font]4000 rmin[sup] -1[/sup][font=宋体]转速下离心[/font]5 min[font=宋体],弃去中间变性蛋白层和下层有机层,水相继续重复上述操作[/font]8[font=宋体]次,直至水相与有机相中间无变性蛋白出现为止,[/font][font=宋体]即得脱蛋白多糖水溶液。[/font][font=宋体]向脱蛋白多糖水溶液中加入[/font][font=宋体]无水乙醇[/font]80 mL[font=宋体],使溶液含醇量达[/font]80[font=宋体] [/font]%[font=宋体]以上,充分[/font][font=宋体]搅拌,[/font][font=宋体]静置过夜。在[/font]4000 r min[sup] -1[/sup][font=宋体]转速下离心[/font]5 min[font=宋体],弃去上清液,所得沉淀依次用无水乙醇、丙酮、无水乙醚各洗涤[/font]3[font=宋体]次,弃去有机溶剂[/font][sup][2[/sup][sup][font=宋体]2[/font][/sup][sup]-2[/sup][sup][font=宋体]5[/font][/sup][sup]][/sup][font=宋体]后挥干沉淀,并用真空干燥机抽真空,[/font]60[font=宋体] [/font][font=宋体]℃干燥[/font]30 min[font=宋体],得到灰白色颗粒状多糖样品。[/font][b][font=宋体]4.[/font][font=宋体]藤三七[/font][font=宋体]总[/font][font=宋体]多糖的鉴别与纯度检查[/font][font=宋体]([/font]1[font=宋体])[/font]Molish[font=宋体]试验[/font][/b](1)[font=宋体]供试品溶液:取藤三七多糖[/font]10 mg[font=宋体],加[/font]10 mL[font=宋体]蒸馏水,加热溶解,[/font][font=宋体]量取[/font]1 mL[font=宋体]至试管中,[/font][font=宋体]再加入[/font]α-[font=宋体]萘酚[/font][font=宋体]乙醇溶液[/font][font=宋体];[/font](2)[font=宋体]阳性对照品溶液:取淀粉[/font]10 mg[font=宋体],加[/font]10 mL[font=宋体]蒸馏水,加热溶解,[/font][font=宋体]量取[/font]1 mL[font=宋体]至试管中,[/font][font=宋体]再加入[/font]α-[font=宋体]萘酚[/font][font=宋体]乙醇溶液[/font][font=宋体];[/font](3)[font=宋体]阴性对照品溶液:[/font][font=宋体]量取[/font]1 mL[font=宋体]蒸馏水于试管中[/font][font=宋体],加入[/font]α-[font=宋体]萘酚[/font][font=宋体]乙醇溶液[/font][font=宋体]。[/font][font=宋体]分别摇匀上述溶液,将试管倾斜,沿试管壁慢慢加入浓硫酸,竖直试管观察。结果,供试品溶液与阳性对照品溶液试管中界面呈[/font][font=宋体]紫堇[/font][font=宋体]色环,阴性对照品溶液试管界面无变化,表明供试品为糖类。[/font][b][font=宋体]([/font]2[font=宋体])[/font]Feling[font=宋体]试验[/font][/b]Feling[font=宋体]试剂的配[/font][font=宋体]制[/font][font=宋体]:[/font][font=宋体]甲液[/font][font=宋体]:[/font][font=宋体]取[/font]34.6 g[font=宋体]酒石酸钾钠[/font]KNaC[sub]4[/sub]H[sub]4[/sub]O[sub]6[/sub]4H[sub]2[/sub]O[font=宋体],[/font]14.2 g NaOH[font=宋体]固体溶于[/font]80 mL[font=宋体]水中,加水稀释到[/font]100[font=宋体] [/font]mL[font=宋体];[/font][font=宋体]乙液[/font][font=宋体]:称取[/font]7.28 g CuSO[sub]4[/sub]5H[sub]2[/sub]O[font=宋体]溶于[/font]40 mL[font=宋体]水中,加水稀释到[/font]100 mL[font=宋体]待用。使用时取等体积两溶液混合即可。[/font](1)[font=宋体]供试品溶液:[/font] [font=宋体]取上述[/font][font=宋体]多糖溶液[/font]1 mL[font=宋体]于试管中;[/font](2)[font=宋体]阳性对照品溶液:取葡萄糖[/font]10 mg[font=宋体],加[/font]10 mL[font=宋体]蒸馏水,溶解,摇匀,[/font][font=宋体]量取[/font]1 mL[font=宋体]于试管中;[/font](3)[font=宋体]阴性对照品溶液:[/font] [font=宋体]量取蒸馏水[/font]1 mL[font=宋体]于试管中。[/font][font=宋体]分别加入[/font]Feling[font=宋体]试剂[/font]2 mL[font=宋体],在沸水中加热[/font]10 min[font=宋体]。结果,供试品溶液与阴性对照品溶液为蓝色,阳性对照品溶液变为砖红色。单糖多为还原性糖,可与[/font]Feling [font=宋体]试剂反应产生砖红色,而多糖为非还原性糖,不与[/font]Feling[font=宋体]试剂反应,结果表明供试品中不含有单糖。[/font][b][font=宋体]([/font]3[font=宋体])[/font][font=宋体]紫外可见光谱分析[/font] [/b][font=宋体]将上述供试品溶液在[/font]190 ~ 500 nm[font=宋体]区间进行光谱扫描,结果在[/font]260 ~ 280 nm[font=宋体]处无明显吸收峰,而未经脱蛋白处理的藤三七粗多糖水溶液,在[/font]260 ~ 280 nm[font=宋体]处有明显吸收峰,表明多糖样品中不含有蛋白质、多肽和核酸类物质。[/font][font=宋体]通过以上三种试验证明所制藤三七多糖为不含单糖、蛋白质、多[/font][font=宋体]肽[/font][font=宋体]、核酸等物质的纯化多糖。[/font][b][font=宋体]5.[/font] [font=宋体]苯酚[/font][font=宋体]-[/font][font=宋体]硫酸法测定总[/font][font=宋体]多[/font][font=宋体]糖含量的条件优化[/font][font=宋体]检测波长的选择[/font][/b][font=宋体]吸取一定浓度的葡萄糖对照品溶液[/font] 0. 2 mL[font=宋体],用蒸馏水补充至[/font]1 mL[font=宋体],加入[/font]5[font=宋体] [/font]%[font=宋体]苯酚溶液[/font]1 mL[font=宋体],充分混匀后,加入浓硫酸[/font]6 mL[font=宋体],振摇[/font]5 min[font=宋体],至[/font]40[font=宋体] [/font][font=宋体]℃水中反应[/font] 20 min[font=宋体],放置室温,同法制得空白溶液,紫外可见分光光度计在[/font]200~800 nm[font=宋体]范围内扫描,结果表明最大吸收波长为[/font]490 nm[font=宋体]。[/font][b][font=宋体]提取方法的优化[/font][/b][font=宋体]采用正交设计,选用提取溶剂用量[/font](A)[font=宋体]、提取时间[/font](B)[font=宋体]及提取温度[/font](C)3[font=宋体]个因素,每个因素选[/font]3[font=宋体]个水平,用[/font]L[sub]9[/sub](3[sup]4[/sup])[font=宋体]正交表进行实验设计的优选,见表[/font]1[font=宋体]。[/font][font=宋体]以藤三七总多糖的含量为检测指标,[/font] [font=宋体]处理组合见表[/font]2[font=宋体] ~[/font]3[font=宋体]。[/font][align=center][font=宋体]表[/font].1 The factor-level table[/align][table][tr][td]levels[/td][td][align=center]A[/align][align=center]Quant. of solvent [/align][align=center](mL)[/align][/td][td][align=center]B[/align][align=center]Time[/align][align=center](h)[/align][/td][td][align=center]C[/align][align=center]Temp[/align][align=center]([font=宋体]℃[/font])[/align][/td][/tr][tr][td]1[/td][td][align=center]10[/align][/td][td]2[/td][td]70[/td][/tr][tr][td]2[/td][td][align=center]20[/align][/td][td]3[/td][td]80[/td][/tr][tr][td]3[/td][td][align=center]30[/align][/td][td]4[/td][td]90[/td][/tr][/table][font=宋体] [/font][font=宋体]取烘干并粉碎的藤三七药材[/font]9[font=宋体]份,每份[/font]1 g[font=宋体],精密称定,用[/font]80[font=宋体] [/font]%[font=宋体]乙醇浸泡过夜,再用[/font]80[font=宋体] [/font]%[font=宋体]乙醇回流[/font]2 h[font=宋体],残渣挥去溶剂,根据正交实验设计,分别加入不同体积水、按不同提取时间、不同提取温度提取。提取液过滤,待冷却后转移于[/font]250 m[font=宋体]L[/font][font=宋体]容量瓶,用蒸馏水稀释至刻度。精密吸取[/font]l mL[font=宋体]于试管中,再分别加入[/font]5[font=宋体] [/font]%[font=宋体]苯酚溶液[/font]1 mL[font=宋体],充分混匀后,加入浓硫酸[/font] 6 mL[font=宋体],[/font]40[font=宋体] [/font][font=宋体]℃[/font][font=宋体]反应[/font]20 min[font=宋体],放至室温,[/font]490 nm[font=宋体]处测得吸光度。[/font][align=center][font=宋体]表[/font]2 Results of L[sub]9[/sub](3[sup]4[/sup]) orthogonal design[/align][table][tr][td][align=center] [/align][align=center]Test NO.[/align][/td][td][align=center]A[/align][align=center]Volume[/align][/td][td][align=center]B[/align][align=center]Time[/align][/td][td][align=center]C[/align][align=center]Temp[/align][/td][td][align=center] [/align][align=center]Content (%)[/align][/td][/tr][tr][td][align=center]1[/align][/td][td]10[/td][td][align=center]2[/align][/td][td][align=center]70[/align][/td][td][align=center]1.66[font=宋体]2[/font][/align][/td][/tr][tr][td]2[/td][td][align=center]10[/align][/td][td][align=center]3[/align][/td][td][align=center]80[/align][/td][td][align=center]2.53[font=宋体]1[/font][/align][/td][/tr][tr][td]3[/td][td][align=center]10[/align][/td][td][align=center]4[/align][/td][td][align=center]90[/align][/td][td][align=center]3.4[font=宋体]18[/font][/align][/td][/tr][tr][td]4[/td][td][align=center]20[/align][/td][td][align=center]2[/align][/td][td][align=center][font=宋体]8[/font]0[/align][/td][td][align=center]2.31[font=宋体]4[/font][/align][/td][/tr][tr][td]5[/td][td][align=center]20[/align][/td][td][align=center]3[/align][/td][td][align=center][font=宋体]9[/font]0[/align][/td][td][align=center]3.19[font=宋体]4[/font][/align][/td][/tr][tr][td]6[/td][td][align=center]20[/align][/td][td][align=center]4[/align][/td][td][align=center][font=宋体]7[/font]0[/align][/td][td][align=center]1.80[font=宋体]3[/font][/align][/td][/tr][tr][td]7[/td][td][align=center]30[/align][/td][td][align=center]2[/align][/td][td][align=center][font=宋体]9[/font]0[/align][/td][td][align=center]4.02[font=宋体]2[/font][/align][/td][/tr][tr][td]8[/td][td][align=center]30[/align][/td][td][align=center]3[/align][/td][td][align=center][font=宋体]7[/font]0[/align][/td][td][align=center]1.90[font=宋体]4[/font][/align][/td][/tr][tr][td]9[/td][td][align=center]30[/align][/td][td][align=center]4[/align][/td][td][align=center][font=宋体]8[/font]0[/align][/td][td][align=center]2.76[font=宋体]0[/font][/align][/td][/tr][tr][td]K[sub]1[/sub][/td][td][align=center]2.537[/align][/td][td][align=center]2.663[/align][/td][td][align=center]1.787[/align][/td][td][/td][/tr][tr][td]K[sub]2[/sub][/td][td][align=center]2.433[/align][/td][td][align=center]2.54[/align][/td][td][align=center]2.533[/align][/td][td][/td][/tr][tr][td]K[sub]3[/sub][/td][td][align=center]2.893[/align][/td][td][align=center]2.66[/align][/td][td][align=center]3.543[/align][/td][td][/td][/tr][tr][td][align=center] R[/align][/td][td][align=center]0.64[/align][/td][td][align=center]0.123[/align][/td][td][align=center]1.756[/align][/td][td][/td][/tr][/table][font=宋体]表[/font]3 Results of analysis of varianee[table][tr][td][align=center]Source of[/align][align=center]variation[/align][/td][td][align=center]Sum of[/align][align=center]squares[/align][/td][td]Degrees of freedom[/td][td][align=center]F[/align][/td][td][align=center]P[/align][/td][/tr][tr][td][align=center]A[/align][/td][td][align=center]0.379[/align][/td][td][align=center]2[/align][/td][td][align=center]2.958[/align][/td][td][align=center] [/align][/td][/tr][tr][td][align=center]B[/align][/td][td][align=center]0.03[/align][/td][td][align=center]2[/align][/td][td][align=center]0.254[/align][/td][td][align=center] [/align][/td][/tr][tr][td][align=center]C[/align][/td][td][align=center]4.663[/align][/td][td][align=center]2[/align][/td][td][align=center]39.517[/align][/td][td][align=center]AB[font=宋体],最佳水平组合为[/font]A[sub]3[/sub]B[sub]1[/sub] C[sub]3[/sub][font=宋体],即加入[/font]30[font=宋体]倍体积水于[/font]90[font=宋体] [/font][font=宋体]℃水浴中提取[/font]2 h[font=宋体]。[/font][font=宋体]方差分析[/font] [font=宋体]由表[/font]2-3[font=宋体]方差分析结果可见:水浴温度对测定结果有显著性影响。[/font][font=宋体]综合分析[/font] [font=宋体]综合考虑各因素对[/font]3[font=宋体]个考察指标的影响,确定藤三七总多糖的最佳提取工艺条件为[/font]A[sub]3[/sub]B[sub]1[/sub]C[sub]3[/sub][font=宋体],即加入[/font]30[font=宋体]倍量体积水于[/font]90[font=宋体] [/font][font=宋体]℃水浴中提取[/font]2 h[font=宋体]。[/font][font=宋体]多糖提取次数的考察[/font] [font=宋体]称取藤三七药材粉末约[/font]1 g[font=宋体],精密称定,按正交试验优选的最佳工艺条件分别提取[/font]3[font=宋体]次,实验结果见表[/font]4[font=宋体]。[/font][align=center][font=宋体]表[/font]-4 Results with the different times[/align][table][tr][td][align=center]time[/align][/td][td][align=center][font=宋体]extraction rate [/font](%)[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center][font=宋体]77.63[/font][/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center][font=宋体]22.37[/font][/align][/td][/tr][tr][td][align=center]3[/align][/td][td][align=center][font=宋体]1.225[/font][/align][/td][/tr][/table][font=宋体]由表可以看出,第[/font]1[font=宋体]次和第[/font]2[font=宋体]次[/font][font=宋体]的[/font][font=宋体]多糖[/font][font=宋体]提取[/font][font=宋体]率较多,而第[/font]3[font=宋体]次多糖[/font][font=宋体]的提取[/font][font=宋体]率较少,多糖[/font][font=宋体]提取率[/font][font=宋体]不足[/font][font=宋体]1.3 [/font]%[font=宋体],所以提取次数可选为[/font]2[font=宋体]次。[/font][font=宋体]综上所述,本实验得到藤三七多糖最佳提取工艺条件为[/font]30[font=宋体]倍量体积的水,于[/font]90[font=宋体] [/font][font=宋体]℃水浴中提取[/font]2[font=宋体]次,每次[/font]2 h[font=宋体]。[/font]

灵芝子实体粗多糖提取及分析灵芝多糖具提高免疫力、抗氧化、抗肿瘤、安神、降血糖、消除放化疗副反应、除胃热、保肝解毒等功效。灵芝多糖是灵芝中最有效的成分之一,因此,也特别受到医药科技工作者的重视,研究报道也最多。现知灵芝多糖有广泛的药理活性,能提高机体免疫力,提高机体耐缺氧能力,消除自由基,抑制肿瘤、抗辐射,提高肝脏、骨髓、血液合成DNA、RNA、蛋白质能力,延长寿命,灵芝多糖还具有刺激宿主非特异性抗性、免疫特异反应以及抑制移植肿瘤生理活性的特性。材料实验所用材料购于市场,经鉴定为灵芝。前处理取灵芝子实体500g剪碎,用75%的乙醇回流脱酯2小时,反复三次,离心,上清液用旋转蒸发仪蒸除乙醇,得灵芝浸膏。提取灵芝残渣分别用pH=2的盐酸溶液、6%的尿素溶液、3%的三氯醋酸溶液室温提取24小时,透析,离心,上清液加入4倍85%乙醇醇析,得粗多糖FS。分级灵芝子实体经脱脂,分别用上述三种方法提取得粗多糖FS,对其中的FS水溶粗多糖进行乙醇分级。FS配成5%多糖溶液,搅拌滴加乙醇,使乙醇的浓度依次达到30%、50%、70%离心所得沉淀依次为FS-A、FS-B、FS-C。脱蛋白5%糖溶液,用链蛋白酶,按酶:蛋白=l:50取蛋白酶,加入糖溶液中,加少量二甲苯防腐,1%NaCI作激活剂,37度,保温24小时,按多糖液总体积1/4加入Sevgae试剂(氯仿:正丁醇=4[/size