随着现代化市场经济的迅猛发展,人们的生活条件得到了改善,对动物源性食品的需求也越来越多,其安全问题也随之越来越重要,其中,氯霉素残留是较为突出的因素之一。那么,氯霉素是什么?其在动物源性食品中的现状又是怎样的呢?动物源性食品 动物源性食品是指来源于动物,可供人类食用的动物产品,包括肉、脂肪、脏器、血液、蛋、奶等。随着国民经济的发展,我国城乡居民的生活水平和健康消费观念的提高,动物源性食品在我国居民食品结构中占有比例越来越大,需求量不断增大,拉动了畜牧业的快速发展。然而,近几年发生的“瘦肉精”“掺假羊肉”“病死猪肉”“三鹿婴幼儿奶粉”等事件使消费者谈“肉”色变,动物源性食品的安全状况已成为当今广受关注的社会话题。氯霉素http://ng1.17img.cn/bbsfiles/images/2015/08/201508251507_562769_2984502_3.jpg 氯霉素为白色针状或微带黄绿色的针状、长片状结晶或结晶性粉末,味苦,易溶于甲醇、乙醇、丙酮,微溶于水,干燥时稳定。氯霉素的化学结构含有对硝基苯基、丙二醇与二氯乙酰胺三个部分, 因其分子中含有一个不游离的氯,故命名氯霉素,其抗菌活性主要与丙二醇有关。 氯霉素是由委内瑞拉链丝菌产生的一种抑菌性广谱抗生素,它通过与核糖体的50s亚单位结合而抑制细菌蛋白质的合成。对革兰氏阳性菌和革兰氏阴性菌均有较好的抑制作用,对立克次体、衣原体也有抑制作用。因其高效廉价,曾在畜牧业中广为应用。然而由于其对造血系统有严重的不良反应,且细菌对氯霉素有发展缓慢的耐药性,所以对其临床应用已经做出严格控制。动物源性食品中氯霉素的现状 国际上对动物源性农产品的兽药残留问题亦广泛关注,世界上许多国家禁止氯霉素使用于生产食品动物,并规定了其在畜产品中的最高残留限量。欧盟、美国等均在其相关法规中规定氯霉素的残留为“零容许量” ,即不得检出。 我国农业部已将氯霉素从2000年版的《中国兽药典》中删除,作为禁用药品。在2002年底的农业部第235号公告《动物源性食品中兽药最高残留限量》中也明确规定氯霉素禁止使用,在动物性食品中不得检出。现在,氯霉素是动物性农产品的必检指标。动物源性食品中氯霉素的检测 关于动物源性食品中氯霉素的检测,主要使用的标准方法有:GB/T22338-2008《动物源性食品中氯霉素类药物残留量测定》、GB/T20756-2006《可食动物肌肉、肝脏和水产品中氯霉素、甲砜霉素和氟苯尼考残留量的测定 液相色谱-串联质谱法》、GB29688-2013《食品安全国家标准 牛奶中氯霉素残留量的测定 液相色谱-串联质谱法》、GB/T18932.19-2003《蜂蜜中氯霉素残留量的测定方法 液相色谱-串联质谱法》等。食品生产企业和销售单位应把动物源性食品中氯霉素的检测作为原料质控和进货采购验证的一项重要指标进行管理,要求供应商出具相关检测报告,必要时可委托有资质的第三方检测机构进行检测。
【关键词】 动物源食品 磺胺类药物残留 GPC法测定磺胺类药物是一类广泛使用的预防性和刺激动物生长(常作饲料添加剂)的抗生素,其在动物源性食品中的残留对人类健康的潜在危害日趋严重,被受到广泛关注。进行动物源性食品磺胺类残留分析具有重要意义〔1〕。由于动物源食品基质复杂,在进行残留分析时通常需要对样品提取液进行净化,目前报道的净化技术主要有液液萃取、固相萃取、基质分散固相萃取〔2-5〕等方法。凝胶渗透色谱(GPC)方法作为一种通用的样品净化技术已经成功应用于农药的多残留分析〔6〕,但应用于药物的多残留分析报道很少〔7〕。为了探讨GPC净化技术应用于动物源食品中药物残留分析的效果,本研究应用GPC净化技术结合高效液相色谱法(HPLC)检测了动物源食品中9种磺胺类药物残留量,取得较为满意的结果。现报告如下。
PCR技术在食品动物源性检测中的应用注:全文见资料中心。
动物源性食品中链霉素检测,使用国标GB/T 21323-2007,检测回收率不是很高,有没有其他改进的建议,谢谢
日前,欧盟食品安全局(EFSA)就其转基因动物源性食品和饲料的风险评估(包括动物健康和福利方面)指南草案,展开公众评议;评议截止日期为2011年9月30日。在该指南草案中,EFSA就申请转基因动物源性食品和饲料欧盟上市许可所须风险评估的具体数据要求和研究方法做出了规定。该风险评估方法是将转基因动物源性食品和饲料与常规动物源性产品进行比对;评估包括食品/饲料安全和动物健康及福利等方面内容。当前的指南草案规定的风险评估方法假定传统饲养动物源性食品和饲料具有长期使用安全史,从而将其作为转基因动物源性食品和饲料的风险评估基准。指南规定了开展风险评估对比分析所需的具体数据要求。风险评估的重要内容包括分子特征,成分分析和毒性、营养及潜在过敏性评估。草案还列明了转基因动物健康和福利对比评估的方法。该评估主要用于两个方面:一是对转基因动物自身,评估重点应放在动物身体系统的正常功能(比如抗病能力);二是对食品和饲料风险评估,因为动物的健康和福利状况被视为动物源性产品安全性的一个重要指标。草案强调了广泛开展转基因动物与传统动物特征和特性(包括生理参数)对比分析的必要性。草案还建议应在转基因动物生长的所有阶段进行动物健康和福利评估,直至其要获得授权的时点。草案建议的三阶段评估策略包括转基因动物最初生长的实验室环境,实验室外大量动物的实地试验以及在商业环境下的大量动物试验(授权前)。草案的最后还针对转基因动物和转基因动物源性食品和饲料的上市后监督(PMM)提出了建议,以便在相关产品获准上市后,发现其可能出现的与转基因相关的潜在不良影响。针对食品和饲料的安全问题,PMM是对全面上市前毒性测试计划的有力补充。针对一些特定情况,如营养成分改变的转基因食品和饲料,以及/或改变基因以实现特定健康效果的食品和饲料,均应实施PMM。针对动物健康和福利,PMM则旨在发现可能存在的发生率较低的长期不良性影响。
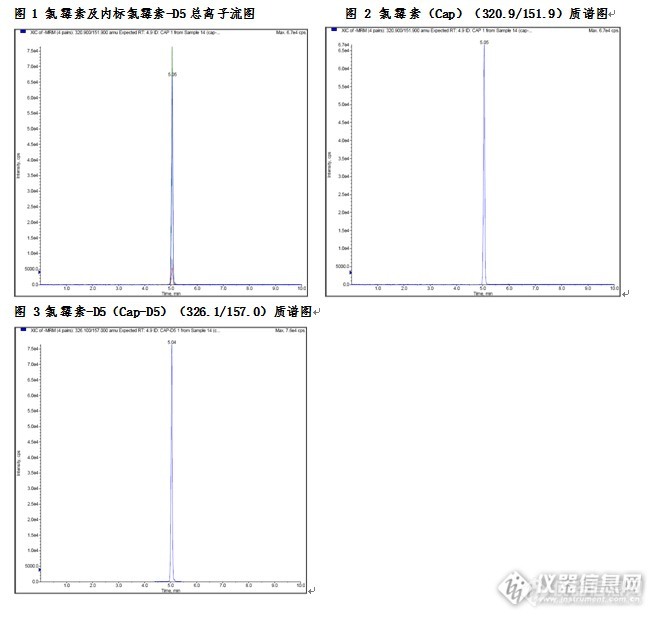
动物源性食品中氯霉素检测的固相萃取方法一、实验目的本研究利用固相萃取法作为样品的前处理方法,LC-MS法作为检测手段。该方法可简化样品的前处理过程,节省有机溶剂的使用,操作简便。 二、实验目标物氯霉素(CAS:56-75-7) 三、应用范围本方法适用于动物源性食品中氯霉素的LC-MS/MS检测及确证。 四、参考标准推荐性国家标准《GB/T 22338-2008动物源性食品中氯霉素类药物残留量测定》 五、实验材料 Biocomma®Silibase™ C18固相萃取柱6mL/1000mg。六、实验方法 1、样品提取 将称取5g试样,精确到0.01g。置于50ml于涡旋具盖离心管中,加入5ml水,于涡旋混合器上快速混合1min,使试样完全溶解。准确加入15ml乙酸乙酯,在振荡器上振荡10min,以3000r/min离心10min,准确吸取上层乙酸乙酯12ml转入15ml的离心管中,置于浓缩吹氮仪在45℃吹扫蒸干,加入5ml水溶解,待净化。 2、SPE柱净化(1)活化:依次采用5mL甲醇、5mL水活化C18固相萃取小柱。(2)净化:将提取液过C18固相萃取柱,待溶液完全流出后,用2×3ml水过柱,然后再用5ml乙腈+水淋洗柱,弃去全部淋出液。用真空泵减压抽干10min。 3、洗脱 用6ml乙酸乙酯洗脱,收集洗脱液于10ml离心管中,于45℃用氮气吹干液吹干,用乙腈+水(2:8,体积比)定容至1ml,供LC-MS/MS上机测定。 4、LC-MS条件色谱柱:Venusil ASBC18(2.1×150mm,5µm,100Å);质谱仪:API 4000流动相:A:0.1mM乙酸铵溶液(0.1%甲酸) B:甲醇溶液;流速:0.2mL/min柱温:40℃进样体积:5ul离子源:电喷雾(ESI),负离子模式检测方式:多反应监测(MRM)。 表1 质谱仪离子源参数 Source/Gas Collision Gas(CAD) 6 Curtain Gas(CUR) 30 Ion Source Gas 1(GS 1) 50 Ion Source Gas 2(GS 2) 50 Ion Spray Voltage(IS) -4500 Temperature(TEM) 550 Interface Heater(ihe) On 表2 氯霉素及内标的母离子和子离子参数表 物质名称 保留时间(min) 监测离子对 DP EP CE CXP 氯霉素 4.90 320.9/151.9 -60 -10 -25 -12 320.9/256.9 -60 -10 -25 -12 氯霉素-D5 4.90 326.1/157.0 -60 -10 -25 -12 七、实验结果1、10ppb猪肉基质氯霉素添加回收结果平均加标回收率在90%以上,RSD值小于5符合标准要求。 表3 猪肉基质氯霉素添加回收结果 名称 1(%) 2(%) 3(%) 平均回收率(%) RSD(%) 氯霉素 98.31 96.28 90.61 95.07 4.20 2、 空白样品添加氯霉素残留物色谱图http://ng1.17img.cn/bbsfiles/images/2015/08/201508141639_560777_3310_3.jpg
定动物源性食品中11种_2_受体激动剂的研究[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=122366]定动物源性食品中11种_2_受体激动剂的研究[/url]
[color=black] 如果测试样品为药品等非正常基质及可食性动物源食品的干品时[/color][color=black],[/color][color=black]由于测试受基质干扰大[/color][color=black],[/color][color=black]方法检测限[/color][color=black],[/color][color=black]样品加标回收率会有所调整[/color][color=black],[/color][color=black]根据不同情况[/color][color=black],[/color][color=black]可能会用[/color][color=black]GPC[/color][color=black]法来净化样品。此外,在处理样品时候,要防止交叉污染,样品上机前用[/color][color=black]PVD[/color][color=black]黄色滤膜过滤(若用绿色尼龙滤膜会有污染)。[/color]
动物源性食品中兽药残留的检测兽药残留检测项目针对性比较强,往往只会检测某一种或某一类药物,这比较适合采用“保留目标化合物模式”进行净化,具有净化效果好、回收率高的特点。下表是选择SPE柱的指导办法:目标化合物类型推荐中性、弱酸和弱碱性药物比如氯霉素、磺胺、呋喃类代谢物等ProElut PLS亲水亲脂平衡柱酸性药物(含有羧基或酚羟基)比如沙星类药物ProElut PXA混合型阴离子交换反相柱碱性药物(含有氨基)比如磺胺ProElut PXC混合型阳离子交换反相柱强阴离子药物(含有磺酸基、磷酸基)ProElut PWA混合型弱阴离子交换反相柱强阳离子药物(含有季铵基)ProElut PWC混合型弱阳离子交换反相柱
动物源性食品中四环素类兽药残留量检测方法,供各位版友参考!!!
CAC/GL 68-2008 Guideline for the Conduct of Food Safety Assessment of Foods Derived from Recombinant-DNA Animals中文名称:动物源性DNA重组食品安全评估指导方针[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=166131]CAC/GL 68-2008 动物源性DNA重组食品安全评估指导方针(英文)[/url]
本方法适用于动物源性食品中14种喹诺酮药物残留的检测,供大家参考!!!
[color=#333333]请问为什么要对动物源性食品中氟喹诺酮类药物残留进行检测[/color][color=#333333] [/color]
请教安捷伦[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url] 6470检测动物源性食品中氯霉素质谱条件的设置

如题:迪马科技QuEChERS方法用于动物源性食品中喹诺酮类兽药残留量测定的方法优势是?答案:方法优势1. 前处理过程简单、方便,并能同时检测马波沙星、恩诺沙星、沙拉沙星、洛美沙星、双氟沙星、萘啶酸、氟甲喹;2. 节省时间,降低基质效应;3. 回收率达85%以上,保证实验结果的准确性、重现性;4. 方法检出限均为1.0 μg/kg,优于国标方法《GB/T 21312-2007 动物源性食品中14种喹诺酮药物残留检测方法 液相色谱-质谱 质谱法》,可供广大分析工作者使用。PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。【奖励】一等奖(3钻石币):999youran(注册ID:999youran)--1楼二等奖(2钻石币):sixingxing(注册ID:v2889187)--2楼三等奖(1钻石币):莫名其妙(注册ID:moyueqiu)--3楼幸运奖(2钻石币):暗夜精灵(注册ID:jbcng)http://ng1.17img.cn/bbsfiles/images/2015/08/201508111503_559944_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/08/201508111503_559945_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/08/201508111503_559946_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/08/201508111503_559947_1610895_3.jpg
各位大神: 刚开始接触动物源性食品中硝基呋喃类代谢物检测工作,求优化好的前处理步骤[img]https://simg.instrument.com.cn/bbs/images/brow/em61.gif[/img]
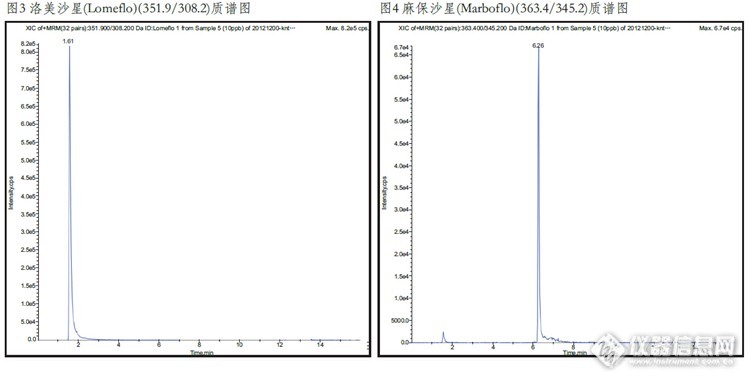
动物源性食品中喹诺酮类物质检测的固相萃取方法 一、实验目的本研究利用固相萃取法作为猪肉样品的前处理方法,LC-MS/MS法作为检测手段。该方法可简化猪肉样品的前处 理过程,节省有机溶剂的使用,操作简便。二、实验目标物三种喹诺酮类药物:依诺沙星(CAS:74011-58-8;84294-96-2),洛美沙星(CAS:98079-51-7),麻保沙星(CAS:115550-35-1)。三、应用范围本方法适用于动物源食品中喹诺酮类药物LC-MS/MS检测及确证。四、参考标准进出口行业标准《SN/T1751.2-2007动物源性食品中喹诺酮类药物残留检测方法;第2部分:液相色谱-质谱/质 谱法》。五、实验材料Biocomma® PolybaseTM HLB固相萃取柱3mL/60mg。六、实验方法1、样品提取称取均质试样5.0g试样(精确至0.01g)于50mL离心管中,加入20mL乙腈,涡旋混合1min,超声提取10min,10000r/min离心,提取三次,合并上清液。2、SPE柱净化(1)活化:加入6mL甲醇,6mL水活化。(2)上样和洗脱:当溶剂液面到达柱吸附层表面时,立即倒入上述待净化溶液,以2mL/min-3mL/min的速度过 柱,弃去滤液,用2mL5%甲醇水溶液淋洗,弃去淋洗液,将小柱抽干,在用6mL甲醇洗脱并收集洗脱液。(3)浓缩定容:50℃缓慢氮气流条件下吹至近干,用1mL0.2%甲酸水溶液溶解,1000r/min旋涡混合1min[color
[font=仿宋_GB2312]根据《中华人民共和国食品安全法》及其实施条例有关规定,市场监管总局批准发布《动物源性食品中瓜尔胶的测定》等[/font]10[font=仿宋_GB2312]项食品补充检验方法和《动物源性食品中甲氧苄啶的快速检测 胶体金免疫层析法》等[/font]9[font=仿宋_GB2312]项食品快速检测方法。名称和编号如下:[/font][font=仿宋_GB2312]动物源性食品中瓜尔胶的测定([/font]BJS 202301[font=仿宋_GB2312])[/font][font=仿宋_GB2312]冰乙酸假冒食醋的鉴别方法[/font] [font=仿宋_GB2312][url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url][/font]-[font=仿宋_GB2312]稳定同位素比值质谱法([/font]BJS 202302[font=仿宋_GB2312])[/font][font=仿宋_GB2312]食品中淫羊藿苷、金丝桃苷和补骨脂素的测定([/font]BJS 202303[font=仿宋_GB2312])[/font][font=仿宋_GB2312]果汁中植物源性成分的测定([/font]BJS 202304[font=仿宋_GB2312])[/font][font=仿宋_GB2312]麦卢卡蜂蜜中[/font]2-[font=仿宋_GB2312]甲氧基苯甲酸、[/font]2'-[font=仿宋_GB2312]甲氧基苯乙酮、[/font]4-[font=仿宋_GB2312]羟基苯基乳酸和[/font]3-[font=仿宋_GB2312]苯基乳酸的测定([/font]BJS 202305[font=仿宋_GB2312])[/font][font=仿宋_GB2312]粮食加工品中噻二唑、苯并噻二唑、噻菌灵及福美双的测定([/font]BJS 202306[font=仿宋_GB2312])[/font][font=仿宋_GB2312]蜂蜜中二羟基丙酮、甘露糖和蜜二糖的测定([/font]BJS 202307[font=仿宋_GB2312])[/font][font=仿宋_GB2312]食品中溴酸盐的测定([/font]BJS 202308[font=仿宋_GB2312])[/font][font=仿宋_GB2312]鸭血中鸭鸡鹅源性成分的测定([/font]BJS 202309[font=仿宋_GB2312])[/font][font=仿宋_GB2312]豆芽、豆制品、火锅及麻辣烫底料中喹诺酮类、磺胺类、硝基咪唑类、四环素类化合物的测定([/font]BJS 202310[font=仿宋_GB2312])[/font][font=仿宋_GB2312]动物源性食品中甲氧苄啶的快速检测[/font] [font=仿宋_GB2312]胶体金免疫层析法[/font][font=仿宋_GB2312]([/font]KJ 202301[font=仿宋_GB2312])[/font][font=仿宋_GB2312]动物肌肉组织中链霉素和庆大霉素的快速检测[/font] [font=仿宋_GB2312]胶体金免疫层析法([/font]KJ 202302[font=仿宋_GB2312])[/font][font=仿宋_GB2312]动物源性食品中四环素类药物的快速检测[/font] [font=仿宋_GB2312]胶体金免疫层析法[/font][font=仿宋_GB2312]([/font]KJ 202303[font=仿宋_GB2312])[/font][font=仿宋_GB2312]动物源性食品中红霉素、螺旋霉素、泰乐菌素、替米考星的快速检测[/font] [font=仿宋_GB2312]胶体金免疫层析法[/font][font=仿宋_GB2312]([/font]KJ 202304[font=仿宋_GB2312])[/font][font=仿宋_GB2312]豆芽中喹诺酮类药物的快速检测[/font] [font=仿宋_GB2312]胶体金免疫层析法[/font][font=仿宋_GB2312]([/font]KJ 202305[font=仿宋_GB2312])[/font][font=仿宋_GB2312]生鲜乳和畜肉中氨基糖苷类药物的快速检测[/font] [font=仿宋_GB2312]胶体金免疫层析法[/font][font=仿宋_GB2312]([/font]KJ 202306[font=仿宋_GB2312])[/font][font=仿宋_GB2312]蔬菜水果中丙环唑的快速检测[/font] [font=仿宋_GB2312]胶体金免疫层析法([/font]KJ 202307[font=仿宋_GB2312])[/font][font=仿宋_GB2312]乳及乳制品中玉米赤霉醇类物质的快速检测[/font] [font=仿宋_GB2312]胶体金免疫层析法[/font][font=仿宋_GB2312]([/font]KJ 202308[font=仿宋_GB2312])[/font][font=仿宋_GB2312]蔬菜水果中甲基异柳磷的快速检测[/font] [font=仿宋_GB2312]胶体金免疫层析法[/font][font=仿宋_GB2312]([/font]KJ 202309[font=仿宋_GB2312])[/font][font=仿宋_GB2312]以上[/font][font=仿宋_GB2312]方法文本可在市场监管总局[/font][font=仿宋_GB2312]食品补充检验方法数据库([/font]https://www.samr.gov.cn/spcjs/bcjyff/[font=仿宋_GB2312])和[/font][font=仿宋_GB2312]食品[/font][font=仿宋_GB2312]快速检测[/font][font=仿宋_GB2312]方法数据库([/font]http://www.samr.gov.cn/spcjs/ksjcff/[font=仿宋_GB2312])中查询[/font][font=仿宋_GB2312]和[/font][font=仿宋_GB2312]下载。[/font][font=仿宋_GB2312]特此公告。[/font][font=仿宋_GB2312] 市场监管总局[/font][font=仿宋_GB2312] [/font]2023[font=仿宋_GB2312]年[/font]6[font=仿宋_GB2312]月[/font]13[font=仿宋_GB2312]日[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312][/font]
附件:中华人民共和国2006年度进出口动物及动物源性食品残留物质监控抽样及检测计划(2006. 1-2006.12)中华人民共和国国家质量监督检验检疫总局 目 录●起草说明●附录1 2006年对出口动物源性食品监控的残留物质与动物种类表●附录2 2006出口动物及动物源性食品残留物质监控抽样计划表●附录3 2006年对进口动物源性食品监控的残留物质与动物种类表●附录4 2006进口动物及动物源性食品残留物质监控抽样计划表●附录5-1 2006年出口残留监控计划各局抽样与检测样品数目统计表●附录5-2 2006年进口残留监控计划各局抽样与检测样品数目统计表●附录5-3 2006年进出口残留监控计划各局抽样与检测样品数目统计表●附录6 残留监控的取样流程图和有关单证●附录7 基准实验室及其分工●附录8 残留监控样品接受人通讯录●附录9 残留监控标准物质供应中心通讯录2006年度进出口动物及动物源性食品残留监控抽样及检测计划起草说明为提高我国动物源性食品的安全卫生质量,保护人民的身体健康,增强我国动物源食品在国际市场上的竞争力,结合检验检疫的出口业务需要和实际检测能力,在总结过去5年半残留监控工作经验的基础上,重点考虑2005年监控检出和阳性情况以及出口国对我国产品的预警通报情况,同时兼顾其他国家对动物及动物源性食品的安全卫生要求,提出了《中华人民共和国2006年度出口动物及动物源性食品残留物质监控抽样及检测计划》、《中华人民共和国2006年度进口动物及动物源性食品残留物质监控抽样及检测计划》。现对有关修订情况说明如下:一、 实施时间2006年度残留监控计划的实施时间为2006年1月至12月。二、残留监控计划修订的依据和原则(一)针对我国在2005年残留监控计划实施过程中的情况和问题,如产品的调整或进出口数量的变化,适当调整各地区的取样数。(二)根据上年度残留监控结果反馈情况,特别是阳性结果的检出情况,同时根据各国预警通报的情况,适当增加对应动物和检测项目的取样数量;对于历年监测均为阴性的项目, 适当减少对应动物的取样数量。总体取样量比去年略有上升。(三) 在对过去2年进口产品监控结果数据分析的基础上,在2006年对各个项目的抽样量进行调整。针对出口情况的变化,取消了个别动物品种的监控。同时也对检测的药物种类进行了调整,取消了个别项目。(四)根据日本肯定列表的情况和我国实际检测能力,适当增加监测项目。三、主要修订之处(一)在《中华人民共和国2006年度出口动物及动物源食品残留物质监控抽样及检测计划》中:1.监控的物种、样品基质及残留标识物。(1)鉴于2005年马产品无出口,无法取样,故取消对马组织的残留监控。(2)对于牛的监控,左旋咪唑、阿维菌素、伊维菌素的监测样品基质由牛肾调整为牛肝(参照欧盟标准)。(3)对于鸡的监控,左旋咪唑、阿维菌素的监测样品基质由鸡肾调整为鸡肝(参照欧盟和日本标准)。(4)对于氯霉素残留的监控,检测样品基质由肝组织调整为肌肉组织。(5)对于硝基咪唑类残留的监控,检测样品基质由肝组织调整为肾组织,并明确需要同时检测其代谢产物2-羟甲基-1-甲基-5-硝基咪唑。(6)对于链霉素的监控,明确需同时检测其代谢产物双氢链霉素。(7)对于多氯联苯的监控,检测样品基质调整为脂肪组织。(8)对于苯并咪唑的监控,明确需同时检测其代谢产物。2.增加的检测项目。(1)牛:增加甲基氢化泼尼松、氟苯尼考、麻保沙星、萘夫西林、磺胺氯哒嗪、磺胺胍、磺胺甲氧哒嗪、氧化丙硫咪唑、氟苯哒唑、甲苯咪唑的监控。(2)羊:增加萘夫西林、磺胺氯哒嗪、磺胺胍、磺胺甲氧哒嗪、氧化丙硫咪唑、氟苯哒唑、甲苯咪唑的监控。(3)猪:增加莱克多巴胺、萘夫西林、甲砜霉素、磺胺氯哒嗪、磺胺胍、磺胺甲氧哒嗪、丙硫哒唑、氧化丙硫咪唑、氟苯哒唑、甲苯咪唑的监控。(4)禽:增加甲基氢化泼尼松、氟苯尼考、马杜霉素、萘夫西林、磺胺氯哒嗪、磺胺胍、磺胺甲氧哒嗪、丙硫哒唑、氧化丙硫咪唑、氟苯哒唑、甲苯咪唑的监控。(5)兔:增加甲基氢化泼尼松、氟苯尼考的监控。(6)水产品:增加磺胺氯哒嗪、磺胺胍、磺胺甲氧哒嗪、结晶紫的监控。(7)蛋:增加氟苯尼考的监控。3.调整的检测限和最高残留限量。(1)牛肝:磺胺喹恶啉检测限由20μg/kg调整50μg/kg,最高残留限量由20μg/kg调整为100μg/kg(参照日本标准)。(2)猪肝:强力霉素最高残留限量由300μg/kg 调整为50μg/kg(参照日本标准);伊维菌素最高残留限量由15μg/kg调整为100μg/kg (参照欧盟标准);磺胺喹恶啉检测限由20μg/kg调整为50μg/kg,最高残留限量由20μg/kg调整为100μg/kg(参照日本标准)。(3)鸡肝:强力霉素最高残留限量由300μg/kg 调整为50μg/kg(参照日本标准);链霉素的检测限100μg/kg 调整为10μg/kg,最高残留限量由500μg/kg 调整为 10μg/kg(参照日本标准);磺胺二甲嘧啶检测限由20μg/kg调整为50μg/kg,最高残留限量由20μg/kg调整为100μg/kg(参照日本标准);盐霉素最高残留限量由1800μg/kg调整为500μg/kg(参照日本标准);莫能菌素最高残留限量由50μg/kg调整为500μg/kg (参照日本标准);恩诺沙星、环丙沙星最高残留限量由200μg/kg调整为10μg/kg ,两者之和小于200μg/kg调整为小于10μg/kg(参照日本标准);沙拉沙星最高残留限量由100μg/kg调整为80μg/kg(参照日本标准); 左旋咪唑最高残留限量由10μg/kg调整为100μg/kg(参照日本标准);鸡肾的尼卡巴嗪检测限由10μg/kg调整为50μg/kg(参照日本标准);氯氰菊酯最高残留限量由200μg/kg调整为50μg/kg(参照日本标准)。(4)兔肝:甲砜霉素最高残留限量由50μg/kg调整为未制定。(5)鳗鱼:恩诺沙星、环丙沙星、诺氟沙星、氧氟沙星检测限由20μg/kg调整为10μg/kg,最高残留限量由ND调整为100μg/kg、100μg/kg、10μg/kg、100μg/kg,恩诺沙星与环丙沙星残留之和不得超过100μg/kg(参照欧盟和日本标准);磺胺类检测限由20μg/kg调整为10μg/kg(磺胺二甲嘧啶未改变),最高残留限量由ND调整为10μg/kg(磺胺二甲氧嘧啶调整为100μg/kg)(参照日本标准);(6)养殖虾:磺胺二甲嘧啶检测限由10μg/kg调整为20μg/kg;恶喹酸最高残留限量由50μg/kg调整为100μg/kg(参照日本标准)。(7)蜂王浆:链霉素最高残留限量由20μg/kg调整为未制定。(8)蜂蜜:链霉素最高残留限量由20μg/kg调整为未制定。(二)在《中华人民共和国2005年度进口动物及动物源食品残留物质监控抽样及检测计划》中:1.增加的检测项目及其检测限与最高残留限量。(1)禽类:增加甲砜霉素、磺胺氯哒嗪、磺胺胍、磺胺甲氧哒嗪、克球酚的监控。(2)水产品:增加氟苯尼考、甲砜霉素的监控。(3)奶制品:增加甲砜霉素、苄青霉素、邻氯青霉素、双氯青霉素、亚硝酸盐的监控。(4)牛组织:增加氟苯尼考、甲砜霉素的监控。(5)猪组织:增加甲砜霉素、莱克多巴胺、二恶英的监控。各监控产品增加的监控项目的检测限和最高残留限量详见附录。2.物种和抽样地区变化情况。(1)对水产品的监控:增加对云南、广西、宁波局辖区的监控,减少福建局抽样量。(2)对牛的监控:去掉深圳、山东局的抽样,减少天津局抽样量。(3)对甲壳类的监控:去掉深圳局,新增宁波局,增加上海局抽样量,减少辽宁局抽样量。(4)奶粉的监控:新增湖南局辖区的监控,减少上海、辽宁局抽样量,增加深圳局抽样量。(5)对猪组织的监控:减少山东局抽样量。(6)对禽类的监控:减少天津局抽样量。(7)对肠衣的监控:减少江苏、天津局的抽样数。四、计划外残留监控对鹅、野禽等禽类产品,牛娃,贝类、蟹、海蛰、鱿鱼等水产品的残留监控,2006年仍不列入统一的残留监控计划。请各有关直属局根据出口业务的需要并结合本局的检测能力,分别参照鸡或鱼的残留监控项目开展残留监控工作;监控结果按照有关《残留监控结果统计报表》的规定上报国家质检总局。
根据国家农药残留标准审评委员会分析方法组“关于检测方法验证工作会议纪要”的规定:植物源食品农残检测方法验证时只需验证11种代表性基质,包括:花生、玉米、芹菜、茄子、韭菜、葡萄、柑橘、香菇、大豆油、绿茶和花椒。
鄙人最近接到一个比较棘手的检测项目,做动物源性食品中的粘杆菌素,但相关的标准或是文献很是少,我是用了博纳艾杰尔的固相萃取柱处理,然后LC/MS进行检测,结果回收率还可以接受,但谱图不是很好。浓度低时谱图容易出现分叉或是肩峰,而且做一些样品后,峰形变的更不好。所以恳请哪位高手可以赐教,如何解决此类问题,是前处理的问题还是色谱柱的原因?不胜感激!
[font=&][size=14px][color=#333333]ISO于2021年3月新发布的标准ISO 23662《适用于素食主义者或严格素食主义者的食品和食品配料以及标识和声明的定义和技术标准》规定了适用于素食主义者(包括乳蛋素食者、蛋类素食者和乳类素食者)或者严格[/color][/size][/font][font=&][size=14px][color=#333333]素食主义者的食品和食品配料的技术要求,以及食品标识和声明的技术要求。[/color][/size][/font][color=#262626]LGC 深耕国际能力验证领域多年。其中运营的[/color][b][size=17px][color=#e39341][size=14px]食品化学质量能力验证计划[/size][size=14px] QFCS[/size][/color][/size][/b][color=#262626]专为提高食品中一系列分析物检测的质量和可比性,获UKAS认可(CNAS互认),提供多个食品基[/color][color=#333333]质。[/color][font=&][size=14px][color=#333333]不管出于何种动机选择了素食,人们在购买时都是希望自己所得皆所愿。LGC QFCS 目前提供多个食品掺假加鉴定能力验证样品,其中包括[/color][/size][/font][size=14px][b][color=#e39341]PT-FC-848 素食食品中动物源性DNA的鉴定。[img=,690,226]https://ng1.17img.cn/bbsfiles/images/2023/04/202304061217395680_1020_3205582_3.png!w690x226.jpg[/img][img=,690,168]https://ng1.17img.cn/bbsfiles/images/2023/04/202304061218115864_2282_3205582_3.png!w690x168.jpg[/img][/color][/b][/size]
建立测定动物源性食品中金刚烷胺的固相萃取/液相色谱-电喷雾串联质谱分析方法。以甲醇-1%三氯乙酸(50+50,v/v)作提取溶剂,采用超声波辅助溶剂萃取法萃取动物源性食品,萃取液用Waters Oasis MCX 固相萃取柱进行净化浓缩。以Thermo Hypersil Gold C18色谱柱为分离柱,在正离子模式下以电喷雾电离串联质谱仪进行测定。对流动相组分和流动相添加剂对质谱的离子化效率进行考察,在1.0~50.0?ng/mL范围内线性关系良好(r?≥?0.99)。样品在5.0μg/k,10.0μg/k和20.0μg/kg添加水平的回收率为75.9%~108.5%,相对标准偏差小于8.0%;方法的检出限为5.0μg/kg。本方法具有很高的灵敏度和准确度,能够满足动物源性食品中的金刚烷胺残留量的快速、高灵敏检测分析。
动物源性食品己烯雌酚检验方法—高效液相色谱法1 范围本方法规定了动物源性食品中己烯雌酚残留量的快速测定方法。原理试样中的残留的己烯雌酚经快速检测前处理试剂盒提供的试剂提取、浓缩、净化后用液相色谱进行检测,外标法定量。3 试剂和材料除另有规定外,所有试剂均为分析纯,水为重蒸馏水。3.1乙腈:色谱纯。3.2冰乙酸:色谱纯。3.3甲醇:色谱纯。3.4无水乙酸钠。3.5对-甲苯磺酸。3.6乙酸盐缓冲液:称取4.950g无水乙酸钠及0.950g对-甲苯磺酸,溶解于950mL水中,用冰乙酸调节溶液pH到4.5,最后用水定溶到1000mL。3.7标准品: 己烯雌酚3.8标准贮备溶液:分别称取标准品各10.0mg,用甲醇溶解后转移至10mL棕色容量瓶中,用甲醇定容,于—20℃条件下保存。使用时,用甲醇稀释上述标准储备溶液,配制成不同浓度的标准工作液。3.9己烯雌酚快速检测前处理试剂盒*。4 仪器和设备4.1高效液相色谱仪:配紫外-可见检测器。4.2匀浆机。4.3旋转蒸发仪。4.4离心机:4 000 r/min4.5聚四氟乙烯离心管:100 mL,具塞。4.6微孔滤膜:0.45 µ m。5测定步骤5.1提取、浓缩、净化准确称取已捣碎的样品10.00 g于50 mL离心管中,先加己烯雌酚快速检测前处理试剂盒中的提取剂(液体20.0 mL)、8000r/min均质1min,于4000 r/min离心5 min,取出上清液10mL用水稀释至30mL。残留物用2.0 mL蒸馏水溶解。取稀释液于层析柱中(使用前依次用5mL甲醇、5mL蒸馏水激活)挤干,加5mL洗涤剂洗涤挤干,加5mL洗脱剂洗脱,接收洗脱液,50℃水浴旋转蒸干,用1mL甲醇溶解残渣于0.45 µ m微孔滤膜过滤,供仪器测定。5.2绘制标准工作曲线移取己烯雌酚混和标准溶液, 50µ g/kg、100µ g/kg、200µ g/kg、500µ g/kg、1000µ g/kg标准工作溶液,样液用高效液相色谱仪测定,得出标准工作曲线。5.3测定5.3.1液相色谱条件a) 色谱柱: C18柱,150 mm×4.6 mm(i.d.),粒度5m b) 流动相:乙腈+乙酸盐缓冲液 (70+20,体积分数) c) 流速:1.0 mL/min d) 柱温:室温 e) 检测波长:250nmf) 进样量:20 L。5.3.2色谱测定根据样液中己烯雌酚的含量情况,选定峰面积相近的标准工作溶液。标准工作溶液和样液中的己烯雌酚响应值均应在仪器的检测线性范围内。5.3.3空白实验除不加试样外,按上述测定步骤进行。5.3.4结果计算用色谱数据处理机或按式(1)分别计算供试样品中的己烯雌酚残留量。 2 ci×Vω= …… (1)mω-样品中己烯雌酚残留量,μg/kg;ci -标准曲线上查出试样溶液中己烯雌酚标准工作溶液的浓度,μg/L;2-换算常数;V-最终定容体积数,mL;m-供试试料样品重量,g。6测定低限、回收率6.1检测限本方法的检测限己烯雌酚为10μg/kg。6.2回收率本方法回收率己烯雌酚为:85%~105%。
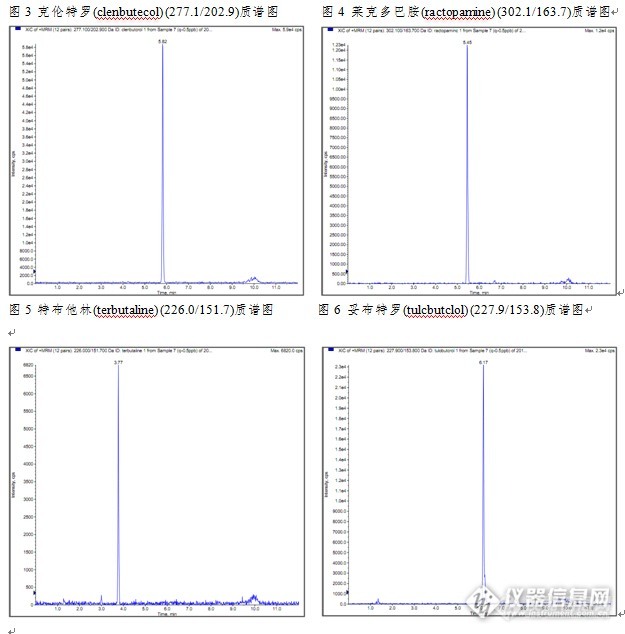
动物源性食品中β-受体激动剂检测的固相萃取方法一、实验目的本研究利用固相萃取法作为猪肉样品的前处理方法,LC-MS/MS法作为检测手段。该方法可简化猪肉样品的前处理过程,节省有机溶剂的使用,操作简便。 二、实验目标物五种β-受体激动剂物质:克仑特罗(CAS:37148-27-9),沙丁胺醇(CAS:18559-94-9),莱克多巴胺(CAS:97825-25-7),特布他林(CAS:23031-25-6),妥布特罗(CAS:41570-61-0)。 三、应用范围本方法适用于动物源性食品中β-受体激动剂LC-MS/MS检测及确证。 四、参考标准推荐性国家标准《GB/T 21313-2007 动物源性食品中β-受体激动剂残留检测方法液相色谱-质谱/质谱法》五、实验材料MCX固相萃取柱6mL/200mg。六、实验方法 1、样品提取 称取均质试样10.0g试样(精确至0.01g),加入15mLpH 5.2的乙酸-乙酸铵缓冲溶液,1000 r/min 匀浆1 min,再加入β-噗糖醛酸苷肽酶/芳香磺酸酯酶溶液100 μL,于37℃±1℃振荡酶解过夜。取出冷却后,10℃9500 r/min离心10 min。取全部上清液,待净化。 2、SPE柱净化(1)活化:加入6mL5%甲醇氨、6mL甲醇、6mL水、6mL 0.1mmol/L高氯酸(pH 4.0)溶液活化。(2)上样和洗脱:当溶剂液面到达柱吸附层表面时,立即倒入上述待净化溶液,过柱,弃去滤液,用2mL甲醇、2mL 2%甲醇水溶液淋洗,最后用7mL5%甲醇氨洗脱。(3)重新溶解:洗脱液缓慢氮气流条件下吹至近干,用甲醇-0.1%甲酸水溶液溶解定容至1.0mL,涡旋混匀1min,用于LC-MS/MS测定。 4、LC-MS条件色谱柱:Venusil ASB C18(2.1×150mm,5µm,100Å);质谱仪:API 4000流动相:A:10mM乙酸铵(0.1%甲酸)溶液 B:甲醇溶液;表1梯度洗脱条件 时间/min B/% A/% 0.00 5 95 4.00 50 50 6.00 10 90 8.00 95 5 8.01 5 95 12.00 Stop 流速:0.2mL/min 柱温:40℃ 进样体积:2μL 离子源:电喷雾(ESI),正离子模式 检测方式:多反应监测(MRM)表2质谱仪离子源参数 Source/Gas Collision Gas(CAD) 10 Curtain Gas(CUR) 30 Ion Source Gas 1(GS 1) 50 Ion Source Gas 2(GS 2) 50 Ion Spray Voltage(IS) 5500 Temperature(TEM) 550 Interface Heater(ihe) On 表3β-受体激动剂的母离子和子离子参数表 物质名称 保留时间(min) 监测离子对 DP EP CE [align

10,抽取5个版友);中奖名单:玲儿响叮当(注册ID:jshbhh)sixingxing(注册ID:v2889187)大川之子,纵横四海(注册ID:chuangu120)捌道巴拉巴巴巴(注册ID:v3082413)馨语(注册ID:huangdm)http://ng1.17img.cn/bbsfiles/images/2016/12/201612151507_01_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/12/201612151507_02_1610895_3.jpg【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================动物源食品中五氯酚残留量的测定方法:SPE/HPLC基质:动物源性食品应用编号:101822化合物:五氯酚固定相:ProElut PXA色谱柱/前处理小柱:ProElut PXA 150mg / 6ml 30/pkg样品前处理:1 样品准备 1.1肉制品 (1) 将1 g样品与10 mL提取液 *加入塑料离心管; (2) 均质提取2 min,8000 rpm下离心5 min,收集上清液; (3) 残留物用10 mL提取液重复提取一次,合并两次提取液,作为上样液,待净化。 1.2 牛奶 (1) 将1 g样品与10 mL提取液 *加入塑料离心管; (2) 涡旋2 min,超声5 min,8000 rpm下离心5 min,收集上清液,待净化。 *提取液:5%三乙胺的乙腈水溶液(乙腈:水=7:3) 2 SPE柱净化——ProElut PXA 150 mg/6 mL(Cat.#68304) (1)活 化:依次加入10 mL甲醇,10 mL水,流出液弃去; (2)上 样:将待净化液加入小柱,流出液弃去; (3)淋 洗:依次加入5 mL 5%氨水、5 mL 甲醇,流出液弃去; (4)洗 脱:10 mL 4%甲酸甲醇溶液洗脱,收集洗脱液; (5)重新溶解:将洗脱液在40 ℃下氮气准确吹至1 mL,用水定容至2 mL,上机分析。色谱条件:色谱柱:Platisil ODS,250 x 4.6 mm,5μm(Cat.# 99503) 流 速:1.0mL/min 检测器:UV 215 nm 柱 温:30℃ 进样量:20 μL 流动相: A:甲醇,B:1%乙酸水溶液,A:B=9:1文章出处:天津迪马实验室关键字:五氯酚,动物源食品,Platisil ODS,99503,ProElut PXA,68304摘要:适用于动物源食品中五氯酚残留量的测定。谱图:http://www.dikma.com.cn/Public/Uploads/images/wulvfen1(2).PNGhttp://www.dikma.com.cn/Public/Uploads/images/wulvfen2(2).PNG图例:五氯酚
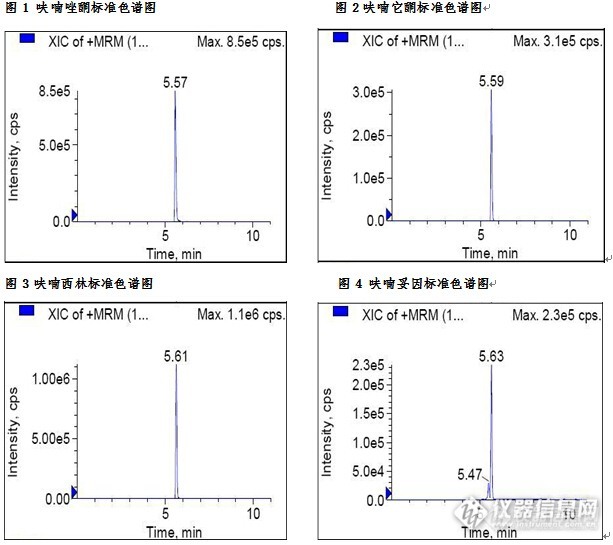
动物源性食品中硝基呋喃类药物检测的固相萃取方法一、实验目的本实验利用固相萃取法作为样品的前处理方法,LC-MS/MS法作为检测手段。该方法可简化样品的前处理过程,节省有机溶剂用量。二、实验目标物呋喃唑酮(CAS:67-45-8),呋喃它酮(CAS:139-91-3),呋喃西林(CAS:59-87-0),呋喃妥因(CAS:67-20-9)。三、应用范围本方法适用于动物源性食品中硝基呋喃类药物的LC-MS/MS检测及确证。四、参考文献 推荐性国家标准《GB/T 21311-2007 动物源性食品中硝基呋喃类药物代谢物残留量检测方法 高效液相色谱-串联质谱法》。五、实验材料 C8/SAX固相萃取柱200mg/6mL。六、实验方法1、样品前处理 将样品组织搅碎、均质。精确称取约1g(精确到0.01g)样品于15mL带螺盖的离心管中,加入1mL水和8mL甲醇,涡旋混合均匀,2000r/min离心3min(15℃),弃去上清液;加入8mL乙醇,涡旋混合均匀,2000r/min离心3min(15℃),弃去上清液;加入8mL乙酸乙酯,涡旋混合均匀,2000r/min离心3min(15℃),弃去上清液。2、水解和衍生化向质控和样品同待测样品中加入5mL 0.2mol/L的盐酸水溶液、100μL衍生化试剂、以及100μL内标工作溶液(20μg/L)和的混合标准溶液(10μg/L)。盖好盖子,充分振荡混匀,然后放入空气浴摇床,在37℃,200r/min条件下衍生化16h(过夜)。3、样品提取 加入0.3M的磷酸钠水溶液500μL。用试管滴加10mol/L的氢氧化钠溶液,涡旋混合均匀,用精密pH试纸调节pH值至7.0—7.2。9500r/min 离心10min,取上清液。4、SPE柱净化(1)活化:依次以5mL甲醇和5mL纯水预处理。(2)洗脱:上清液全部过柱,流速控制在约每秒1滴。依次以5mL水和5mL 50%甲醇/水溶液淋洗柱子。淋洗液完全通过小柱后,至少抽真空5min。以4mL 4%的甲醇氨洗脱,洗脱液用15mL试管收集。(3)浓缩定容:40℃氮气吹干。残渣以0.05%甲酸/甲醇溶液(9:1,v/v)溶解。溶解液以0.22μm的水相滤膜过滤,滤液可直接用于LC-MS/MS分析。5、LC-MS/MS条件 液相色谱-质谱/质谱仪 色谱柱:C18柱:150mm×2.1mm,2.0μm,或相当者 流动相:甲醇-5mM乙酸铵七、实验结果1、添加回收结果 向样品中加入不同水平的四环素类药物,回收率结果如下:(见表1)表1 动物组织中四环素类药物添加回收结果 样品名称 化合物名称 添加水平(ng/mL) 回收率(%) 猪肉 呋喃唑酮 50 80.75 100 82.58 呋喃它酮 50 89.74 100 90.88 呋喃西林 50 92.74 100 91.28 呋喃妥因 50 95.63 100 96.94 2、 空白样品添加农药残留物色谱图 http://ng1.17img.cn/bbsfiles/images/2015/08/201508141653_560805_3310_3.jpg
随着生活水平的不断提高,人们对动物性食品的需求量不断加大,同时对其食用安全性的要求也在进一步提高,兽药在动物源性食品中的残留问题也越来越受到关注。 在畜牧业生产过程中,兽药在预防、治疗、诊断动物疫病、促进动物生长、提高生产效率上,发挥着非常重要的作用,是发展现代养殖业的保障。在实际生产中,长期或超过用量标准使用兽药;使用违禁药物及其它有毒有害的化合物;不合理地使用和滥用兽药及饲料药物添加剂;生产环境的污染都是造成兽药残留的原因 。兽药残留的危害主要表现在:1.长期食用兽药残留的动物产品,蓄积下来可造成慢性中毒。一次性摄入量过大使人体急性中毒。2008年11月10日,浙江省嘉兴市中茂公司70名职工食用了含有盐酸克伦特罗(瘦肉精)的红烧肉发生食物中毒。今年2月,在广州发生的46人因食用猪内脏中毒,中毒原因也是市民所吃猪内脏中含有盐酸克伦特罗。2.细菌耐药性增强。由于抗菌药物长期不合理的滥用、乱用,促使很多细菌耐药性不断增强,耐药菌不断增多,人们通过食用残留有抗菌药物的动物,自身体内的耐药菌也不断增多,对人类细菌性疾病的治疗产生严重的威胁。3.产生过敏反应。一些抗生素的残留可使敏感人群发生过敏反应,引发皮炎、皮疹、瘙痒、急性血管性水肿和休克等过敏症状,如青霉素引起过敏性休克,磺胺类氨基糖药物引起皮肤和粘膜过敏性损伤,四环素引起过敏性皮炎等。4.发生激素反应,在畜牧业生产中,使用激素,如已烯雌酚(DES)、有机砷制剂等,可增加畜产品产量,调节繁殖机能,促进动物生长,但是,这些激素的残留如果残留在动物体内,被人体食用吸收,直接影响人体的机能和代谢。近几年来,屡见不鲜的小孩早熟,激素残留是一个重要原因。5.产生三致(致畸、致癌、致突变)作用。研究表明,一些药物及某些化学物质如苯丙咪唑呋喃唑酮,喹乙醇,苏丹红Ⅳ,均对人类有潜在危害,可引起基因突变或染色体畸变。(资料来源:云南省农业厅)
动物源食品中兽药残留检测方法目录 1、动物源食品中呋喃唑酮残留检测方法—————高效液相色谱法2、动物源食品中磺胺对甲氧嘧啶残留检测方法——高效液相色谱法3、动物源食品中磺胺二甲嘧啶残留检测方法———高效液相色谱法4、动物源食品中磺胺喹噁啉残留检测方法————高效液相色谱法5、动物源食品中磺胺类药物残留的检测方法———高效液相色谱法6、动物源食品中氯羟吡啶残留检测方法—————高效液相色谱法7、动物源食品中莫能菌素和盐霉素残留检测方法—高效液相色谱法8、动物源食品中乙氧酰胺苯甲酯残留检测方法——高效液相色谱法9、动物源食品中新霉素残留检测方法——————微生物学检测法10、猪尿中克伦特罗检测方法—————————酶联免疫吸附测定法
SNT 2327-2009 进出口动物源性食品中角黄素、虾青素的检测方法