请教各位大神,请问区带电泳迁移时间为何会延后。使用相同的buffer,柱子,前一天是延后,今天什么都没更换,迁移时间又恢复正常了。是仪器系统问题吗?
Q:SDS-PAGE电泳的基本原理?A:SDS-聚丙烯酰胺凝胶电泳,是在聚丙烯酰胺凝胶系统中引进SDS(十二烷基硫酸钠),SDS会与变性的多肽,并使蛋白带负电荷,由于多肽结合SDS的量几乎总是与多肽的分子量成正比而与其序列无关,因此SDS多肽复合物在丙稀酰胺凝胶电泳中的迁移率只与多肽的大小有关,在达到饱和的状态下,每克多肽可与1.4g去污剂结合。当分子量在15KD到200KD之间时,蛋白质的迁移率和分子量的对数呈线性关系,符合下式:logMW=K-bX,式中:MW为分子量,X为迁移率,k、b均为常数,若将已知分子量的标准蛋白质的迁移率对分子量对数作图,可获得一条标准曲线,未知蛋白质在相同条件下进行电泳,根据它的电泳迁移率即可在标准曲线上求得分子量。
SDS-PAGE电泳小问答 Q:SDS-PAGE电泳的基本原理? A:SDS-聚丙烯酰胺凝胶电泳,是在聚丙烯酰胺凝胶系统中引进SDS(十二烷基硫酸钠),SDS能断裂分子内和分子间氢键,破坏蛋白质的二级和三级结构,强还原剂能使半胱氨酸之间的二硫键断裂,蛋白质在一定浓度的含有强还原剂的SDS溶液中,与SDS分子按比例结合,形成带负电荷的SDS-蛋白质复合物,这种复合物由于结合大量的 SDS,使蛋白质丧失了原有的电荷状态形成仅保持原有分子大小为特征的负离子团块,从而降低或消除了各种蛋白质分子之间天然的电荷差异,由于SDS与蛋白质的结合是按重量成比例的,因此在进行电泳时,蛋白质分子的迁移速度取决于分子大小。当分子量在15KD到200KD之间时,蛋白质的迁移率和分子量的对数呈线性关系,符合下式:logMW=K-bX,式中:MW为分子量,X为迁移率,k、b均为常数,若将已知分子量的标准蛋白质的迁移率对分子量对数作图,可获得一条标准曲线,未知蛋白质在相同条件下进行电泳,根据它的电泳迁移率即可在标准曲线上求得分子量。Q:配胶缓冲液系统对电泳的影响?A:在SDS-PAGE不连续电泳中,制胶缓冲液使用的是Tris-HCL缓冲系统,浓缩胶是pH6.7,分离胶pH8.9;而电泳缓冲液使用的Tris-甘氨酸缓冲系统。在浓缩胶中,其pH环境呈弱酸性,因此甘氨酸解离很少,其在电场的作用下,泳动效率低;而CL离子却很高,两者之间形成导电性较低的区带,蛋白分子就介于二者之间泳动。由于导电性与电场强度成反比,这一区带便形成了较高的电压剃度,压着蛋白质分子聚集到一起,浓缩为一狭窄的区带。当样品进入分离胶后,由于胶中pH的增加,呈碱所以,pH对整个反应体系的影响是至关重要的,实验中在排除其他因素之后仍不能很好解决问题的情况,应首要考虑该因素。
对流免疫电泳是在琼脂扩散基础上结合电泳技术而建立的一种简便而快速的方法。此方法能在短时间内出现结果,故可用于快速诊断,敏感性比双向扩散技术高10-15倍。血清蛋白在pH8.6条件下带负电荷,所以在电场作用下都向E极移动。但由于抗体分子在这样的PH条件下只带微弱的负电荷,而且它的分子量又较大(为r球蛋白)。所以游动慢。更重要的是抗体分子受电渗作用影响较大,也就是说点渗作用大于它本身的迁移率。所谓电渗作用是指在电场中溶液对于一个固定固体的相对移动。琼脂是一种酸性物质,在碱性缓冲液中进行电泳,它带有负电荷,而与琼脂相接触的水溶液就带正电荷,这样的液体便向负极移动。抗体分子就是随着带正电荷的液体向负极移动的。而一般的蛋白质(如血清抗原)也受电渗作用的影响,使泳动速度减慢,但它的电泳迁移率远远大于电渗作用。这样抗原体就达到了定向对流,在两者相遇且比例合适时便形成肉眼可见的沉淀线。一、材料1. 诊断血清:免抗人免疫血清2. 待检血清:人血清3. 阴性对照血清4. pH8.6、离子强度0.05 M 巴比妥缓冲液配方:巴比妥1.84 g,巴比妥钠10.3 g,加蒸馏水1000 ml,调pH至8.6。5. 缓冲琼脂板:将纯化的琼脂用pH8.6离子强度0.025的巴比妥缓冲液(用0.05 M 的巴比妥缓冲液稀释一倍即可)配成1.5%的琼脂,加入0.01~0.02%流柳汞防腐,保存冰箱内备用。6. 电泳仪7. 其他:生理盐水、打孔器、微量进样器二、方法1. 琼脂板的制备根据需要可选用大玻板(6 cm×9 cm)和(小玻片)两种。大玻板约需琼脂10 ml,小玻片约需3.5 ml,凝固后按图打孔,方法同琼脂扩散实验。2. 加样:左侧孔内加患者血清(原血清及10倍稀释血清各占一孔),右侧内加抗血清,每片应有阳性对照。http://img.dxycdn.com/trademd/upload/userfiles/image/2013/02/B1361084632_small.jpg3. 电泳用国产普通电泳仪。其内加0.05 m pH8.6的巴比妥缓冲液,加至电泳槽高度的三分之二处,注意两槽内液面尽量水平。将加好样品的玻板置于电泳槽上,抗原端接负极,抗体端接正极,用2~4层滤纸浸湿作盐桥,滤纸与琼脂板联接处为0.5 cm。以板宽度计算电流,以板的长度计算电压。要求电流量为2~3 mA/cm,即大板为20 mA,小板为10 mA。电压为4~6 V/cm。通电45分钟—2小时后观察结果。4. 结果观察在黑色背景上方,用散射光多个角度观察,在对孔之间有白色沉淀线即为阳性对照应出现明显的白色沉淀线。如果抗原,两极微沉淀条纹不清晰,于37℃保温数小时可增强沉淀条纹的清晰度。5. 影响结果的因素(1)抗原抗体的比例:抗原抗体比例适应时容易出现沉淀带,反之不易发生。当抗体浓度恒定时,被检血清含甲胎蛋白浓度高时,作10倍、20倍或更高倍数稀释可以提高阳性率。随稀释度的增加,抗原抗体的比例发生变化,沉淀线由靠近抗血清孔向逐步移向两孔中间,并可出现不典型的沉淀线如弧形、八字须形、斜线形,这些也是阳性,应予注意。(2)组电泳缓冲液其电泳结果以巴比妥钠—盐酸缓冲液灵敏度最高。巴比妥—巴比妥钠次之,Tris缓冲液更差。(3)电压与电流时电泳时间需要长些:电压电流增大时,电泳时间可更短。但电压过高则孔径变形,电流过大抗原抗体蛋白易变性,干扰实验结果。一般选择5 ml/cm,电泳时间改为1.5小时。
电泳基本原理 迁移率(或泳动度)是指带电颗粒在单位电场强度下泳动的速度,可用下列公式计算: U =υ/E =(d/t)/(V/l) =dl/Vt U为迁移率(cm2•V-1•min-1);υ为颗粒泳动速度(cm•s-1);E 为电场强度( V•cm-1);d为颗粒泳动的距离(cm);l为滤纸有效长度(cm);V为实际电压(V);t为通电时间(s或min)。通过测量d, l, V, t, 即可计算出被分离物质的迁移率。 1迁移率单位= 10-5 cm2•V-1•min-1在确定的条件下,某物质的迁移率为常数,是该物质的化学特征常数。 颗粒带净电荷多,直径小而接近于球形,则在电场中泳动速度快,反之则泳动速度慢。 迁移率还与分子的形状,介质粘度,颗粒所带电荷有关,迁移率与颗表面电荷成正比,与介质粘度及颗粒半径成反比。 影响琼脂糖电泳迁移的主要因素 电场强度 溶液的pH值 溶液的离子强度 电渗现象 温度的影响 支持物的影响 按分离原理分类: 1.区带电泳 2.移界电泳 3.等速电泳 4.聚焦电泳 按有无固体支持物分类 1. 纸上电泳 2. 醋酸纤维素膜电泳 3. 薄层电泳 4. 非凝胶性支持物区带电泳(支持物有:淀粉、纤维素粉、玻璃粉、硅胶) 5. 凝胶支持区带电泳(淀粉凝胶、聚丙稀酰胺凝胶、琼脂糖凝胶) 影响琼脂糖电泳迁移的主要因素 DNA的大小 DNA的构象 琼脂糖浓度 缓冲液 不同构像质粒 缓冲液 TAE:乙酸盐缓冲液 TBE:硼酸盐缓冲液 TPE:磷酸盐缓冲液 实验操作 1. 用胶带将洗净、干燥的水平板的边缘封住,形成一个胶模并水平放置。 2. 按水平板的长×宽×0.5cm胶厚,量取0.5×TBE,并按0.7%的浓度称取agarose琼脂糖,在微波炉或电炉上加热至全熔(清澈透明)。 3. 等凝胶温度降至大约50-60以下时,加入1 mg/L溴化乙锭(EB)至终浓度为0.5ug/mL ;摇匀并轻快地倒入水平板中,除掉气泡,插入梳子。 4. 凝固后,将梳子轻轻拔出。 5.去掉胶带,将水平板放入加有0.5×TBE电泳缓冲液的电泳槽中,并且使电泳缓冲液高出凝胶约1mm。 6.在parafilm膜上依次加: ddH2O 6ul,上样Buffer 2ul ,DNA 4ul 分别混匀后点样,记录点样次序。 7. 在水平板两边的点样孔中分别加入6 μ l的λΔΝΑ/EcoRI+HindIII marker。 8. 盖好电泳槽盖子,选择适当的电泳电压(≤5V/cm)及电泳方向(DNA阴极阳极),开始电泳。 9. 当色素接近胶的先端,停止电泳,样品在紫外灯下观察、成像℃
对流免疫电泳是在琼脂扩散基础上结合电泳技术而建立的一种简便而快速的方法。此方法能在短时间内出现结果,故可用于快速诊断,敏感性比双向扩散技术高10-15倍。血清蛋白在pH8.6条件下带负电荷,所以在电场作用下都向E极移动。但由于抗体分子在这样的PH条件下只带微弱的负电荷,而且它的分子量又较大(为r球蛋白)。所以游动慢。更重要的是抗体分子受电渗作用影响较大,也就是说点渗作用大于它本身的迁移率。所谓电渗作用是指在电场中溶液对于一个固定固体的相对移动。琼脂是一种酸性物质,在碱性缓冲液中进行电泳,它带有负电荷,而与琼脂相接触的水溶液就带正电荷,这样的液体便向负极移动。抗体分子就是随着带正电荷的液体向负极移动的。而一般的蛋白质(如血清抗原)也受电渗作用的影响,使泳动速度减慢,但它的电泳迁移率远远大于电渗作用。这样抗原体就达到了定向对流,在两者相遇且比例合适时便形成肉眼可见的沉淀线。一、材料1. 诊断血清:免抗人免疫血清2. 待检血清:人血清3. 阴性对照血清4. pH8.6、离子强度0.05 M 巴比妥缓冲液配方:巴比妥1.84 g,巴比妥钠10.3 g,加蒸馏水1000 ml,调pH至8.6。5. 缓冲琼脂板:将纯化的琼脂用pH8.6离子强度0.025的巴比妥缓冲液(用0.05 M 的巴比妥缓冲液稀释一倍即可)配成1.5%的琼脂,加入0.01~0.02%流柳汞防腐,保存冰箱内备用。6. 电泳仪7. 其他:生理盐水、打孔器、微量进样器二、方法1. 琼脂板的制备根据需要可选用大玻板(6 cm×9 cm)和(小玻片)两种。大玻板约需琼脂10 ml,小玻片约需3.5 ml,凝固后按图打孔,方法同琼脂扩散实验。2. 加样:左侧孔内加患者血清(原血清及10倍稀释血清各占一孔),右侧内加抗血清,每片应有阳性对照。http://img.dxycdn.com/trademd/upload/userfiles/image/2013/02/B1361084632_small.jpg3. 电泳用国产普通电泳仪。其内加0.05 m pH8.6的巴比妥缓冲液,加至电泳槽高度的三分之二处,注意两槽内液面尽量水平。将加好样品的玻板置于电泳槽上,抗原端接负极,抗体端接正极,用2~4层滤纸浸湿作盐桥,滤纸与琼脂板联接处为0.5 cm。以板宽度计算电流,以板的长度计算电压。要求电流量为2~3 mA/cm,即大板为20 mA,小板为10 mA。电压为4~6 V/cm。通电45分钟—2小时后观察结果。4. 结果观察在黑色背景上方,用散射光多个角度观察,在对孔之间有白色沉淀线即为阳性对照应出现明显的白色沉淀线。如果抗原,两极微沉淀条纹不清晰,于37℃保温数小时可增强沉淀条纹的清晰度。5. 影响结果的因素(1)抗原抗体的比例:抗原抗体比例适应时容易出现沉淀带,反之不易发生。当抗体浓度恒定时,被检血清含甲胎蛋白浓度高时,作10倍、20倍或更高倍数稀释可以提高阳性率。随稀释度的增加,抗原抗体的比例发生变化,沉淀线由靠近抗血清孔向逐步移向两孔中间,并可出现不典型的沉淀线如弧形、八字须形、斜线形,这些也是阳性,应予注意。(2)组电泳缓冲液其电泳结果以巴比妥钠—盐酸缓冲液灵敏度最高。巴比妥—巴比妥钠次之,Tris缓冲液更差。(3)电压与电流时电泳时间需要长些:电压电流增大时,电泳时间可更短。但电压过高则孔径变形,电流过大抗原抗体蛋白易变性,干扰实验结果。一般选择5 ml/cm,电泳时间改为1.5小时。
用PH解释westernblot 原理由于SDS是一种阴离子去污剂,能与蛋白质分子的疏水部分结合,断裂分子内和分子间氢键,破坏蛋白质的二级和三级结构。由于此作用蛋白质被解聚为亚单位-多肽链,形成带负电荷的蛋白质---SDS胶束,降低及消除了蛋白质分子间的天然电荷差异,因此他的电泳迁移率只与分子量有关,而不再受电荷及形态的影响。在浓缩胶中PH为6.8,而电流缓冲液PH为8.3,可将浓缩胶看为整体,那我们说以电泳液为标准的话,浓缩胶带正电,因而带负电的SDS---蛋白质胶束就易向浓缩胶迁移,又由于分离胶的PH为8.8相对于电泳液带负电,这样就形成了我们在电泳过程中看到的样在浓缩胶和分离胶交界处形成一条线的奇观!同时也解释了换电压的问题!!!!!!!同理,转印的原理也就不攻自破了。希望我的解释能解除心中的疑惑!!!!
凝胶电泳(英语:Gel electrophoresis)或称胶体电泳 是一大类技术,被科学工作者用于分离不同物理性质(如大小、形状、等电点等)的分子。凝胶电泳通常用于分析用途,但也可以作为制备技术,在采用某些方法(如质谱(MS)、聚合酶链式反应(PCR)、克隆技术、DNA测序或者免疫印迹)检测之前部分提纯分子。凝胶电泳仪 - 使用方法凝胶电泳被广泛用于分子生物学、遗传学和生物化学:1.大的DNA或者RNA分子通常利用琼脂糖凝胶电泳(agarose gel electrophoresis)分离,也可以使用聚丙烯酰胺凝胶电泳(PAGE)。2.蛋白质的凝胶电泳通常在加入十二烷基硫酸钠的聚丙烯酰胺凝胶中进行(SDS-PAGE),或者非变性凝胶电泳,或二维电泳。 SDS-PAGE 蛋白质凝胶电泳图。 3.毛细管电泳 4.酶谱法(zymography) 5.变性梯度胶凝电泳(Denaturing Gradient Gel Electrophoresis,DGGE) 琼脂糖和聚丙烯酰胺可以制成各种形状、大小和孔隙度。琼脂糖凝胶分离DNA片度大小范围较广,不同浓度琼脂糖凝胶可分离长度从200bp至近50kb的DNA片段。琼脂糖通常用水平装置在强度和方向恒定的电场下电泳。聚丙烯酰胺分离小片段DNA(5-500bp)效果较好,其分辩力极高,甚至相差1bp的DNA片段就能分开。聚丙烯酰胺凝胶电泳很快,可容纳相对大量的DNA,但制备和操作比琼脂糖凝胶困难。聚丙烯酰胺凝胶采用垂直装置进行电泳。目前,一般实验室多用琼脂糖水平平板凝胶电泳装置进行DNA电泳。 琼脂糖主要在DNA制备电泳中作为一种固体支持基质,其密度取决于琼脂糖的浓度。在电场中,在中性pH值下带负电荷的DNA向阳极迁移,其迁移速率由下列多种因素决定:1、 DNA的分子大小。度琼脂糖凝胶中的迁移速率与DNA分子量对数成反比,分子越大则所受阻力越大,也越难于在凝胶孔隙中蠕行,因而迁移得越慢。 2、 琼脂糖浓度 一个给定大小的线状DNA分子,其迁移速度在不同浓度的琼脂糖凝胶中各不相同。DNA电泳迁移率的对数与凝胶浓度成线性关系。凝胶浓度的选择取决于DNA分子的大小。分离小于0.5kb的DNA片段所需胶浓度是1.2-1.5%,分离大于10kb的DNA分子所需胶浓度为0.3-0.7%, DNA片段大小间于两者之间则所需胶浓度为0.8-1.0%。 3、 DNA分子的构象DNA分子处于不同构象时,它在电场中移动距离不仅和分子量有关,还和它本身构象有关。相同分子量的线状、开环和超螺旋DNA在琼脂糖凝胶中移动速度是不一样的,超螺旋DNA移动最快,而开环双链DNA移动最慢。如在电泳鉴定质粒纯度时发现凝胶上有数条DNA带难以确定是质粒DNA不同构象引起还是因为含有其他DNA引起时,可从琼脂糖凝胶上将DNA带逐个回收,用同一种限制性内切酶分别水解,然后电泳,如在凝胶上出现相同的DNA图谱,则为同一种DNA。
大气压下(最好)的各种材料离子的迁移率,主要是小分子的,如氧气,臭氧,tnt等谢谢了
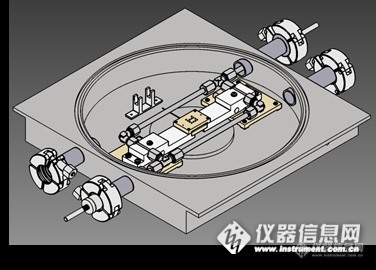
薄膜综合物性分析仪(导热系数,电导率,电阻率,赛贝克系数,霍尔系数,迁移率 载流子浓度 发射率)同步测量苏需要的热物性参数,消除样品的几何尺寸,样品物质组分和热分布不均的影响,结果非常具有可靠性。可测量30nm-30μm的涂层与薄膜样品,样品面积约25mm²采用芯片式设计,样品于传感器紧密接触,构成一个缩小的热带发导热测量模型,可配置锁相放大器,以适应3ω法对样品的in-plance和cross-plance导热进行测量。可以适应不同材质样品。无论是金属,陶瓷,半导体等无机薄膜还是有机薄膜,都可以用TFA测量模块化设计, 根据需求,添加测量模块。1:瞬态导热测量磨坏:锁相放大器 配置3ω测量单元,可测平面,交叉面导热系数,比热等2: 霍尔效应测量模块: 配置磁场单元,可测霍尔电压,迁移率,载流子浓度。3 低温附件模块:-150°-400°C 样品两侧均安装LN2管道, 有利于样品两侧温度控制。导热系数:稳态热带法,3ω法。电阻于霍尔系数:范德堡法赛贝克:静态直流法http://ng1.17img.cn/bbsfiles/images/2016/01/201601151255_581948_3060548_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/01/201601151255_581949_3060548_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/01/201601151255_581950_3060548_3.png
凝胶电泳 以淀粉胶、琼脂或琼脂糖凝胶、聚丙烯酰胺凝胶等作为支持介质的区带电泳法称为凝胶电泳。其中聚丙烯酰胺凝胶电泳(polyacrylamide gel electrophoresis,PAGE)普遍用于分离蛋白质及较小分子的核酸。琼脂糖凝胶孔径较大,对一般蛋白质不起分子筛作用,但适用于分离同工酶及其亚型,大分子核酸等应用较广: ⒈琼脂糖凝胶电泳的原理概述琼脂糖是由琼脂分离制备的链状多糖。其结构单元是D-半乳糖和3.6-脱水-L-半乳糖。许多琼脂糖链依氢键及其它力的作用使其互相盘绕形成绳状琼脂糖束,构成大网孔型凝胶。因此该凝胶适合于免疫复合物、核酸与核蛋白的分离、鉴定及纯化。在临床生化检验中常用于LDH、CK等同工酶的检测。 ⒉琼脂糖凝胶电泳分离核酸的基本技术在一定浓度的琼脂糖凝胶介质中,DNA分子的电泳迁移率与其分子量的常用对数成反比;分子构型也对迁移率有影响,如共价闭环DNA>直线DNA>开环双链DNA。当凝胶浓度太高时,凝胶孔径变小,环状DNA(球形)不能进入胶中,相对迁移率为0,而同等大小的直线DNA(刚性棒状)可以按长轴方向前移,相对迁移率大于0。 ⑴设备与试剂:琼脂糖凝胶电泳分为垂直及水平型两种。其中水平型可制备低浓度琼脂糖凝胶,而且制胶与加样都比较方便,故应用比较广泛。核酸分离一般用连续缓冲体系,常用的有TBE(0.08mol/l TrisHCl,pH8.5,0.08mol/L硼酸,0.0024mol/l EDTA)和THE(0.04mol/l TrisHCl。pH7.8,0.2mol/L醋酸钠,0.0018mol/l EDTA)。 ⑵凝胶制备:用上述缓冲液配制0.5%-0.8%琼脂糖凝胶溶液,沸水浴或微波炉加热使之融化,冷至55℃时加入溴化乙锭(EB)至终浓度为0.5μg/ml,然后将其注入玻璃板或有机玻璃板组装好的模子中,厚度依样品浓度而定。注胶时,梳齿下端距玻璃板0.5-1.0mm,待脱凝固后,取出梳子,加入适量电极缓冲液使板胶浸没在缓冲液下1mm处。 ⑶样品制备与加样:溶解于TBE或THE内的样品应含指示染料(0.025%溴酚蓝或桔黄橙)、蔗糖(10%-15%)或甘油(5%-10%),也可使用2.5%Fico Ⅱ增加比重,使样品集中,每齿孔可加样5-10μg。 ⑷电泳:一般电压为5-15V/cm。对大分子的分离可用电压5V/cm。电泳过程最好在低温条件下进行。 ⑸样品回收:电泳结束后在紫外灯下观察样品的分离情况,对需要的DNA分子或特殊片段可从电泳后的凝胶中以不同的方法进行回收,如电泳洗脱法:在紫外灯下切取含核酸区带的凝胶,将其装入透析袋(内含适量新鲜电泳缓冲液),扎紧透析袋后,平放在水平型电泳槽两电极之间的浅层缓冲液中,100V电泳2-3小时,然后正负电极交换,反向电泳2分钟,使透析袋上的DNA释放出来。吸出含DNA的溶液,进行酚抽提、乙醇沉淀等步骤即可完成样品的回收。 其它还有低融点琼脂糖法、醋酸铵溶液浸出法、冷冻挤压法等,但各种方法都仅仅有利于小分子量DNA片段(<1kb)的回收,随着DNA分子量的增大,回收量显著下降。
如题做LFGB,塑料食品接触材料中邻苯9P的迁移率怎么做,要求是每个都有限值。
第一节 概 述一. DNA的限制性内切酶酶切分析限制性内切酶能特异地结合于一段被称为限制性酶识别序列的DNA序列之内或其附近的特异位点上,并切割双链DNA。它可分为三类:Ⅰ类和Ⅲ类酶在同一蛋白质分子中兼有切割和修饰(甲基化)作用且依赖于ATP的存在。Ⅰ类酶结合于识别位点并随机的切割识别位点不远处的DNA,而Ⅲ类酶在识别位点上切割DNA分子,然后从底物上解离。Ⅱ类由两种酶组成: 一种为限制性内切核酸酶(限制酶),它切割某一特异的核苷酸序列; 另一种为独立的甲基化酶,它修饰同一识别序列。Ⅱ类中的限制性内切酶在分子克隆中得到了广泛应用,它们是重组DNA的基础。绝大多数Ⅱ类限制酶识别长度为4至6个核苷酸的回文对称特异核苷酸序列(如EcoRⅠ识别六个核苷酸序列:5'- G↓AATTC-3'),有少数酶识别更长的序列或简并序列。Ⅱ类酶切割位点在识别序列中,有的在对称轴处切割,产生平末端的DNA片段(如SmaⅠ:5'-CCC↓GGG-3');有的切割位点在对称轴一侧,产生带有单链突出末端的DNA片段称粘性未端, 如EcoRⅠ切割识别序列后产生两个互补的粘性末端。5'…G↓AATTC…3' →5'… G AATTC…3'3'…CTTAA↑G …5' →3'… CTTAA G…5'DNA纯度、缓冲液、温度条件及限制性内切酶本身都会影响限制性内切酶的活性。大部分限制性内切酶不受RNA或单链DNA的影响。当微量的污染物进入限制性内切酶贮存液中时,会影响其进一步使用,因此在吸取限制性内切酶时,每次都要用新的吸管头。如果采用两种限制性内切酶,必须要注意分别提供各自的最适盐浓度。若两者可用同一缓冲液,则可同时水解。若需要不同的盐浓度,则低盐浓度的限制性内切酶必须首先使用,随后调节盐浓度,再用高盐浓度的限制性内切酶水解。也可在第一个酶切反应完成后,用等体积酚/氯仿抽提,加0.1倍体积3mol/L NaAc和2倍体积无水乙醇,混匀后置-70℃低温冰箱30分钟,离心、干燥并重新溶于缓冲液后进行第二个酶切反应。DNA限制性内切酶酶切图谱又称DNA的物理图谱,它由一系列位置确定的多种限制性内切酶酶切位点组成,以直线或环状图式表示。在DNA序列分析、基因组的功能图谱绘制、DNA的无性繁殖、基因文库的构建等工作中,建立限制性内切酶图谱都是不可缺少的环节,近年来发展起来的RFLP(限制性片段长度多态性)技术更是建立在它的基础上。构建DNA限制性内切酶图谱有许多方法。通常结合使用多种限制性内切酶,通过综合分析多种酶单切及不同组合的多种酶同时切所得到的限制性片段大小来确定各种酶的酶切位点及其相对位置。酶切图谱的使用价值依赖于它的准确性和精确程度。在酶切图谱制作过程中,为了获得条带清晰的电泳图谱,一般DNA用量约为0.5-1μg。限制性内切酶的酶解反应最适条件各不相同,各种酶有其相应的酶切缓冲液和最适反应温度(大多数为37℃)。对质粒DNA酶切反应而言, 限制性内切酶用量可按标准体系1μg DNA加1单位酶,消化1-2小时。但要完全酶解则必须增加酶的用量,一般增加2-3倍,甚至更多,反应时间也要适当延长。二. 凝胶电泳琼脂糖或聚丙烯酰胺凝胶电泳是分离鉴定和纯化DNA片段的标准方法。该技术操作简便快速,可以分辨用其它方法(如密度梯度离心法)所无法分离的DNA片段。当用低浓度的荧光嵌入染料溴化乙啶(Ethidium bromide, EB)染色,在紫外光下至少可以检出1-10ng的DNA条带,从而可以确定DNA片段在凝胶中的位置。此外,还可以从电泳后的凝胶中回收特定的DNA条带,用于以后的克隆操作。琼脂糖和聚丙烯酰胺可以制成各种形状、大小和孔隙度。琼脂糖凝胶分离DNA片度大小范围较广,不同浓度琼脂糖凝胶可分离长度从200bp至近50kb的DNA片段。琼脂糖通常用水平装置在强度和方向恒定的电场下电泳。聚丙烯酰胺分离小片段DNA(5-500bp)效果较好,其分辩力极高,甚至相差1bp的DNA片段就能分开。聚丙烯酰胺凝胶电泳很快,可容纳相对大量的DNA,但制备和操作比琼脂糖凝胶困难。聚丙烯酰胺凝胶采用垂直装置进行电泳。目前,一般实验室多用琼脂糖水平平板凝胶电泳装置进行DNA电泳。琼脂糖主要在DNA制备电泳中作为一种固体支持基质,其密度取决于琼脂糖的浓度。在电场中,在中性pH值下带负电荷的DNA向阳极迁移,其迁移速率由下列多种因素决定:1、DNA的分子大小:线状双链DNA分子在一定浓度琼脂糖凝胶中的迁移速率与DNA分子量对数成反比,分子越大则所受阻力越大,也越难于在凝胶孔隙中蠕行,因而迁移得越慢。2、琼脂糖浓度一个给定大小的线状DNA分子,其迁移速度在不同浓度的琼脂糖凝胶中各不相同。DNA电泳迁移率的对数与凝胶浓度成线性关系。凝胶浓度的选择取决于DNA分子的大小。分离小于0.5kb的DNA片段所需胶浓度是1.2-1.5%,分离大于10kb的DNA分子所需胶浓度为0.3-0.7%, DNA片段大小间于两者之间则所需胶浓度为0.8-1.0%。
大家好,我们用的仪器是P/ACE™ MDQ的,我想问一下路过的各位仪器上通过设置自动出现的物质的Migration time问题。 用的毛细管柱是普通的石英的,样品为中性分子(标记物)和带负电荷的大分子混合而成。最终出现了对应的两个迁移时间,相对迁移时间指什么,怎样算?是不是最后只是带负电荷的大分子的电泳迁移时间?先谢大家了。
高效毛细管电泳的基本原理 高效毛细管电泳(high performance capillary electrophoresis,HPCE)是近年来发展起来的分离、分析技术,它是凝胶电泳技术的发展,是高效液相色谱分析的补充。该技术可分析的成分小至有机离子、大至生物大分子如蛋白质、核酸等。可用于分析多种体液样本如血清或血浆、尿、脑脊液及唾液等,HPLC分析高效、快速、微量。 电泳迁移不同分子所带电荷性质、多少不同,形状、大小各异。一定电解质及PH的缓冲液或其它溶液内,受电场作用,样本中各组分按一定速度迁移,从而形成电泳。电泳迁移速度(v)可用下式表示: 其中E为电场强度(E=V/L,V为电压,L为毛细管总长度)。u为电泳淌度。 电渗迁移电渗迁移指在电场作用下溶液相对于带电管壁移动的现象。特殊结构的熔合硅毛细管管壁通常在水溶液中带负电荷,在电压作用下溶液整体向负极移动,形成电渗流。带电微粒在毛细管内实际移动的速度为电泳流和电渗流的矢量和。分析化学博客-jl2~d d&6}8eE4B3q5T I5U0 分离分析类型B[D hv,m cF2Z0 根据其分离样本的原理设计不同主要分为以下几种类型:b[ _0]&uL+\$C0①毛细管区带电泳(capillaryzoneelectrophoresis,CZE);②毛细管等速电泳(capillary chromatography,CITP);③毛细管胶速电动色谱(miceller electrokinetic capillary chromatography,MECC);④毛细管凝胶电泳(capillary gelelectrophoresis,CGE);⑤毛细管等电聚焦(capillary isoelectric focusing ,CIEF)。毛细管区带电泳(CZE)为HPCE的基本操作模式,一般采用磷酸盐或硼酸盐缓冲液,实验条件包括缓冲液浓度、pH值、电压、温度、改性剂(乙腈、甲醇等),用于对带电物质(药物、蛋白质、肽类等)分离分析,对于中性物质无法实现分离。毛细管胶束电动色谱(MECC)为一种基于胶束增溶和电动迁移的新型液体色谱,在缓冲液中加入离子型表面活性剂作为胶束剂,利用溶质分子在水相和胶束相分配的差异进行分离,拓宽了CZE的应用范围,适合于中性物质的分离,亦可区别手性化合物,可用于氨基酸、肽类、小分子物质、手性物质、药物样品及体液样品的分析。毛细管等速电泳(CITP)采用先导电解质和后继电解质,构成不连续缓冲体系,基于溶质的电泳淌度差异进行分离,常用于离子型物质(如有机酸),并因适用较大内径的毛细管而可用于微制备,但本法空间分辨率较差。毛细管等电聚焦电泳(CIEF)用于具兼性离子的样品(蛋白质、肽类),等电点仅差0.001可分离的物质。毛细管凝胶电泳(CGE)依据大分子物质的分子量大小进行分离,主要用于蛋白质、核苷酸片段的分离。此外,还有毛细管电色谱(CEC)及非水毛细管电泳(CNACE),用于水溶性差的物质和水中难进行反应的分析研究。CZE和MECC用得较多,本文以两种方法为例来说明HPLC的原理。
免疫电泳实验是先将抗原物质在琼脂凝胶中做电泳分离,然后于凝胶槽中加入抗体血清。使抗原抗体进行双向扩散,在比例适宜部位形成特异的抗原抗体沉淀弧线。每条沉淀弧线代表一组抗原抗体复合物,故可用抗原成分分析;且可以根据其迁移率与抗体所出现的特异反应进行鉴定。一、材料1. 待检标本(抗原):正常人血清。2. 抗体:正常人血清的家兔免疫血清。3. 1.5%离子琼脂(系用巴比妥缓冲液配制的)。4. 电泳仪。5. pH8.6、离子强度0.05 M 巴比妥缓冲液配方:巴比妥1.84 g,巴比妥钠10.3 g,加蒸馏水1000 ml,调pH至8.6。6. 其它:载物玻片,直径3毫米打孔器,20 mm×2 mm 玻璃铸型,微量进样器。二、方法1. 取载物玻片(7.5×2.5 cm)加上3.5 ml 1.5%琼脂凝胶,制成2毫米厚的琼脂板。2. 按图位置,在琼脂板未凝固时,放入抗血清槽铸型,注意勿使铸型全部浸入琼脂中,待凝固时再打孔。http://img.dxycdn.com/trademd/upload/userfiles/image/2013/02/A1361084544_small.jpg3. 加待检标本:用微量进样器往孔中加1~5 μl。4. 电泳:电压9~7 V/cm,泳动15~20小时。5. 电泳后取出抗血清槽铸型,加入抗血清,进行双扩散,一般在24小时内沉淀弧出全。6. 观察结果:或描绘、拍照或进行染色,染色后的标本便于结果分析及保存。
在利用激光诱导荧光检测时,如果迁移时间可重复但峰面积不可重复,可能是什么原因呢
生化实验讲义(理论部分)--电泳技术 4.1 电泳技术发展简史1809年俄国物理学家Рейсе首次发现电泳现象。他在湿粘土中插上带玻璃管的正负两个电极,加电压后发现正极玻璃管中原有的水层变混浊,即带负电荷的粘土颗粒向正极移动,这就是电泳现象。1909年Michaelis首次将胶体离子在电场中的移动称为电泳。他用不同pH的溶液在U形管中测定了转化酶和过氧化氢酶的电泳移动和等电点。1937年瑞典Uppsala大学的Tiselius对电泳仪器作了改进,创造了Tiselius电泳仪,建立了研究蛋白质的移动界面电泳方法,并首次证明了血清是由白蛋白及α、β、γ球蛋白组成的,由于Tiselius在电泳技术方面作出的开拓性贡献而获得了1948年的诺贝尔化学奖。1948年Wieland和Fischer重新发展了以滤纸作为支持介质的电泳方法,对氨基酸的分离进行过研究。从本世纪50年代起,特别是1950年Durrum用纸电泳进行了各种蛋白质的分离以后,开创了利用各种固体物质(如各种滤纸、醋酸纤维素薄膜、琼脂凝胶、淀粉凝胶等)作为支持介质的区带电泳方法。1959年Raymond和Weintraub利用人工合成的凝胶作为支持介质,创建了聚丙烯酰胺凝胶电泳,极大地提高了电泳技术的分辨率,开创了近代电泳的新时代。30多年来,聚丙烯酰胺凝胶电泳仍是生物化学和分子生物学中对蛋白质、多肽、核酸等生物大分子使用最普遍,分辨率最高的分析鉴定技术,是检验生化物质的最高纯度:即“电泳纯”(一维电泳一条带或二维电泳一个点)的标准分析鉴定方法,至今仍被人们称为是对生物大分子进行分析鉴定的最后、最准确的手段,即“Last Check”。由80年代发展起来的新的毛细管电泳技术,是化学和生化分析鉴定技术的重要新发展,己受到人们的充分重视。4.2 电泳的基本原理电泳是指带电颗粒在电场的作用下发生迁移的过程。许多重要的生物分子,如氨基酸、多肽、蛋白质、核苷酸、核酸等都具有可电离基团,它们在某个特定的pH值下可以带正电或负电,在电场的作用下,这些带电分子会向着与其所带电荷极性相反的电极方向移动。电泳技术就是利用在电场的作用下,由于待分离样品中各种分子带电性质以及分子本身大小、形状等性质的差异,使带电分子产生不同的迁移速度,从而对样品进行分离、鉴定或提纯的技术。电泳过程必须在一种支持介质中进行。Tiselius等在1937年进行的自由界面电泳没有固定支持介质,所以扩散和对流都比较强,影响分离效果。于是出现了固定支持介质的电泳,样品在固定的介质中进行电泳过程,减少了扩散和对流等干扰作用。最初的支持介质是滤纸和醋酸纤维素膜,目前这些介质在实验室已经应用得较少。在很长一段时间里,小分子物质如氨基酸、多肽、糖等通常用滤纸或纤维素、硅胶薄层平板为介质的电泳进行分离、分析,但目前则一般使用更灵敏的技术如HPLC等来进行分析。这些介质适合于分离小分子物质,操作简单、方便。但对于复杂的生物大分子则分离效果较差。凝胶作为支持介质的引入大大促进了电泳技术的发展,使电泳技术成为分析蛋白质、核酸等生物大分子的重要手段之一。最初使用的凝胶是淀粉凝胶,但目前使用得最多的是琼脂糖凝胶和聚丙烯酰胺凝胶。蛋白质电泳主要使用聚丙烯酰胺凝胶。电泳装置主要包括两个部分:电源和电泳槽。电源提供直流电,在电泳槽中产生电场,驱动带电分子的迁移。电泳槽可以分为水平式和垂直式两类。垂直板式电泳是较为常见的一种,常用于聚丙烯酰胺凝胶电泳中蛋白质的分离。电泳槽中间是夹在一起的两块玻璃板,玻璃板两边由塑料条隔开,在玻璃平板中间制备电泳凝胶,凝胶的大小通常是12cm 14 cm,厚度为1mm~2 mm,近年来新研制的电泳槽,胶面更小、更薄,以节省试剂和缩短电泳时间。制胶时在凝胶溶液中放一个塑料梳子,在胶聚合后移去,形成上样品的凹槽。水平式电泳,凝胶铺在水平的玻璃或塑料板上,用一薄层湿滤纸连接凝胶和电泳缓冲液,或将凝胶直接浸入缓冲液中。由于pH值的改变会引起带电分子电荷的改变,进而影响其电泳迁移的速度,所以电泳过程应在适当的缓冲液中进行的,缓冲液可以保持待分离物的带电性质的稳定。为了更好的了解带电分子在电泳过程中是如何被分离的,下面简单介绍一下电泳的基本原理。在两个平行电极上加一定的电压(V),就会在电极中间产生电场强度(E),L是电极间距离。在稀溶液中,电场对带电分子的作用力(F),等于所带净电荷与电场强度的乘积。这个作用力使得带电分子向其电荷相反的电极方向移动。在移动过程中,分子会受到介质粘滞力的阻碍。粘滞力(F’)的大小与分子大小、形状、电泳介质孔径大小以及缓冲液粘度等有关,并与带电分子的移动速度成正比,对于球状分子,F’的大小服从Stokes定律,即:
电泳现象 电泳是指带电粒子在电场作用下向电性相反的方向迁移的现象。利用这种现象对某些化学或生物化学物质进行分离分析的技术称为电泳技术,可完成电泳分离的仪器称为电泳仪。 不同的物质粒子在同一电场中,由于它们之间有效电荷、形状、大小的差别,它们的电泳迁移就会不同,所以有可能得到分离。也就是说,物质粒子在电场中迁移速度的不同是电泳分离的基础。 毛细管电泳是将电泳的场所置于毛细管中的一种电泳分离方法,它的装置结构非常简单,通常由高压电源、铂电极、缓冲液池、样品池、毛细管、检测器和分析记录仪构成。 利用上述的仪器,我们就可以进行毛细管电泳分离。它的基本流程有进样、分离和检测三步骤。 总的来说,毛细管电泳非常广泛地应用于生命科学中生物样品的分离分析,特别是蛋白质分离、糖分析、DNA测序、手性分离、单细胞分析等。
电泳现象 电泳是指带电粒子在电场作用下向电性相反的方向迁移的现象。利用这种现象对某些化学或生物化学物质进行分离分析的技术称为电泳技术,可完成电泳分离的仪器称为电泳仪。 不同的物质粒子在同一电场中,由于它们之间有效电荷、形状、大小的差别,它们的电泳迁移就会不同,所以有可能得到分离。也就是说,物质粒子在电场中迁移速度的不同是电泳分离的基础。 毛细管电泳是将电泳的场所置于毛细管中的一种电泳分离方法,它的装置结构非常简单,通常由高压电源、铂电极、缓冲液池、样品池、毛细管、检测器和分析记录仪构成。 利用上述的仪器,我们就可以进行毛细管电泳分离。它的基本流程有进样、分离和检测三步骤。 总的来说,毛细管电泳非常广泛地应用于生命科学中生物样品的分离分析,特别是蛋白质分离、糖分析、DNA测序、手性分离、单细胞分析等。
分离的原因:电泳迁移,电渗迁移电泳迁移:在高压电场下,带电离子向相反的方向移动。电渗迁移:当毛细管内充满缓冲溶液时,毛细管壁上的硅羟基发生解离,生成氢离子溶解在溶液中,这样就使毛细管壁带上负电荷与溶液形成双电层,在毛细管的两端加上直流电场后,带正电的溶液就会整体的向负极端移动,这就形成了电渗流。在操作缓冲溶液中,带电粒子的运动速度等于电泳速度和电渗速度的矢量和,电渗速度一般大于电泳速度,因此即使是阴离子也会从阳极端流向阴极端。加大缓冲溶液的酸度、在缓冲溶液中加入有机试剂都会减少硅羟基的解离,减小电渗流。分离模式 毛细管电泳的分离模式有以下几种。 (1)毛细管区带电泳(CZE) 将待分析溶液引入毛细管进样一端,施加直流电压后,各组分按各自的电泳流和电渗流的矢量和流向毛细管出口端,按阳离子、中性粒子和阴离子及其电荷大小的顺 序通过检测器。中性组分彼此不能分离。出峰时间称为迁移时间(tm),相当于高效液相色谱和[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]中的保留时间。 (2)毛细管凝胶电泳(CGE) 在毛细管中装入单体和引发剂引发聚合反应生成凝胶,这种方法主要用于分析蛋白质、DNA等生物大分子。另外还可以利用聚合物溶液,如葡聚糖等的筛分作用进 行分析,称为毛细管无胶筛分。有时将它们统称为毛细管筛分电泳,下分为凝胶电泳和无胶筛分两类。 (3)毛细管等速电泳(CITP) 采用前导电解质和尾随电解质,在毛细管中充入前导电解质后,进样,电极槽中换用尾随电解质进行电泳分析,带不同电荷的组分迁移至各个狭窄的区带,然后依次通过检测器。 (4)毛细管等电聚焦电泳(CIEF) 将毛细管内壁涂覆聚合物减小电渗流,再将样品和两性电解质混合进样,两个电极槽中分别加入酸液和碱液,施加电压后毛细管中的操作电解质溶液逐渐形成pH梯 度,各溶质在毛细管中迁移至各自等电点(pI)时变为中性形成聚焦的区带,而后用压力或改变检测器末端电极槽储液的pH值的办法使溶质通过检测器。 (5)胶束电动毛细管色谱(MEKC或MECC) 当操作缓冲液中加入大于其临界胶束浓度的离子型表面活性剂时表面活性剂就聚集形成胶束,其亲水端朝外憎水非极性核朝内,溶质则在水和胶束两相间分配,各溶 质因分配系数存在差别而被分离。对于常用的阴离子表面活性剂十二烷基硫酸钠,进样后极强亲水性组分不能进入胶束,随操作缓冲液流过检测器(容量因子k′= 0);极强憎水性组分则进入胶束的核中不再回到水相,最后到达检测器(k′=∞)。其他常用的胶束试剂还有阳离子表面活性剂十六烷基三甲基溴化铵,胆酸 等。 (6)毛细管电色谱(CEC) 将细粒径固定相填充到毛细管中或在毛细管内壁涂覆固定相以电渗流驱动操作缓冲液(有时再加辅助压力)进行分离。
电泳技术发展简史 1809年俄国物理学家Рейсе首次发现电泳现象。他在湿粘土中插上带玻璃管的正负两个电极,加电压后发现正极玻璃管中原有的水层变混浊,即带负电荷的粘土颗粒向正极移动,这就是电泳现象。 1909年Michaelis首次将胶体离子在电场中的移动称为电泳。他用不同pH的溶液在U形管中测定了转化酶和过氧化氢酶的电泳移动和等电点。 1937年瑞典Uppsala大学的Tiselius对电泳仪器作了改进,创造了Tiselius电泳仪,建立了研究蛋白质的移动界面电泳方法,并首次证明了血清是由白蛋白及α、β、γ球蛋白组成的,由于Tiselius在电泳技术方面作出的开拓性贡献而获得了1948年的诺贝尔化学奖。 1948年Wieland和Fischer重新发展了以滤纸作为支持介质的电泳方法,对氨基酸的分离进行过研究。 从本世纪50年代起,特别是1950年Durrum用纸电泳进行了各种蛋白质的分离以后,开创了利用各种固体物质(如各种滤纸、醋酸纤维素薄膜、琼脂凝胶、淀粉凝胶等)作为支持介质的区带电泳方法。 1959年Raymond和Weintraub利用人工合成的凝胶作为支持介质,创建了聚丙烯酰胺凝胶电泳,极大地提高了电泳技术的分辨率,开创了近代电泳的新时代。30多年来,聚丙烯酰胺凝胶电泳仍是生物化学和分子生物学中对蛋白质、多肽、核酸等生物大分子使用最普遍,分辨率最高的分析鉴定技术,是检验生化物质的最高纯度:即“电泳纯”(一维电泳一条带或二维电泳一个点)的标准分析鉴定方法,至今仍被人们称为是对生物大分子进行分析鉴定的最后、最准确的手段,即“Last Check”。 由80年代发展起来的新的毛细管电泳技术,是化学和生化分析鉴定技术的重要新发展,己受到人们的充分重视。4.2 电泳的基本原理 电泳是指带电颗粒在电场的作用下发生迁移的过程。许多重要的生物分子,如氨基酸、多肽、蛋白质、核苷酸、核酸等都具有可电离基团,它们在某个特定的pH值下可以带正电或负电,在电场的作用下,这些带电分子会向着与其所带电荷极性相反的电极方向移动。电泳技术就是利用在电场的作用下,由于待分离样品中各种分子带电性质以及分子本身大小、形状等性质的差异,使带电分子产生不同的迁移速度,从而对样品进行分离、鉴定或提纯的技术。 电泳过程必须在一种支持介质中进行。Tiselius等在1937年进行的自由界面电泳没有固定支持介质,所以扩散和对流都比较强,影响分离效果。于是出现了固定支持介质的电泳,样品在固定的介质中进行电泳过程,减少了扩散和对流等干扰作用。最初的支持介质是滤纸和醋酸纤维素膜,目前这些介质在实验室已经应用得较少。在很长一段时间里,小分子物质如氨基酸、多肽、糖等通常用滤纸或纤维素、硅胶薄层平板为介质的电泳进行分离、分析,但目前则一般使用更灵敏的技术如HPLC等来进行分析。这些介质适合于分离小分子物质,操作简单、方便。但对于复杂的生物大分子则分离效果较差。凝胶作为支持介质的引入大大促进了电泳技术的发展,使电泳技术成为分析蛋白质、核酸等生物大分子的重要手段之一。最初使用的凝胶是淀粉凝胶,但目前使用得最多的是琼脂糖凝胶和聚丙烯酰胺凝胶。蛋白质电泳主要使用聚丙烯酰胺凝胶。 电泳装置主要包括两个部分:电源和电泳槽。电源提供直流电,在电泳槽中产生电场,驱动带电分子的迁移。电泳槽可以分为水平式和垂直式两类。垂直板式电泳是较为常见的一种,常用于聚丙烯酰胺凝胶电泳中蛋白质的分离。电泳槽中间是夹在一起的两块玻璃板,玻璃板两边由塑料条隔开,在玻璃平板中间制备电泳凝胶,凝胶的大小通常是12cm ? 14 cm,厚度为1mm~2 mm,近年来新研制的电泳槽,胶面更小、更薄,以节省试剂和缩短电泳时间。制胶时在凝胶溶液中放一个塑料梳子,在胶聚合后移去,形成上样品的凹槽。水平式电泳,凝胶铺在水平的玻璃或塑料板上,用一薄层湿滤纸连接凝胶和电泳缓冲液,或将凝胶直接浸入缓冲液中。由于pH值的改变会引起带电分子电荷的改变,进而影响其电泳迁移的速度,所以电泳过程应在适当的缓冲液中进行的,缓冲液可以保持待分离物的带电性质的稳定。
早期的电泳技术是由瑞典Uppsala大学物理化学系Svedberg教授提出了荷电的胶体颗粒在电场中移动的现象称其为电泳。于1937年,收ArneTiselius教授——诺贝尔奖金获得者,利用些电泳现象,发明了最早期的界面电泳,用于蛋白质分离的研究,开创了电沪泳技术的新纪元。此后,各种电泳技术及仪器相继问世,先进的电泳仪和电泳技术的不断发展,使它在生物化学实验技术中占重要地位,按电泳的原理有三种形式的电泳分离系统:原则上按电泳的原理来分,即移动界面电泳、区带电泳和稳态电泳或称置换(排代)电泳。在自由移动界面电泳,是带电分子的移动速率通过观察界面的移动来测定,该方法已成为历史。代之以采用支持介质的区带电泳。 区带电泳因所用支持体的种类、粒度大小和电泳方式等不同,其临床应用的价值也各有差异。固体支持介质可分为两类:一类是滤纸、醋酸纤维素薄膜、硅胶、矾土、纤维素等;另一类是淀粉、琼脂糖和聚丙烯酰胺凝胶。由于它们具微细的多孔网状结构,故除能产生电泳作用外,还有分子筛效应,小分子会比大分子跑得快而使分辨率提高。它的最大优点是几乎不吸附蛋白质,因此电泳无拖尾的现象。低浓度的琼脂糖电泳相当于自由界面电泳,蛋白质在电场中可自由穿透,阴力小,分离清晰,透明度高,能透过200~7000nm波长的着色区带的检测敏感性,为此第一类支持介质现已被第二类支持介质所替代。 稳太电泳或称置换电泳的特点是分子颗粒的电泳迁移在一定时间后达到稳态,如等电聚焦和等速电泳。 区带电泳是临床检验领域中应用最广泛的技术,有重要临床意义,尤其是其他新技术,更扩大了其应用范围,提高了检测技术,现对该技术的现状与发展作一评述。

检测水样中的无机阴离子(代发)介绍:该方法可以检测在天然水、饮用水和废水样品中的无机阴离子有:氯化物、亚硝酸盐、硫酸盐、硝酸盐、氟化物和磷酸盐离子。测量方法:毛细管电泳法测定无机阴离子浓度是基于阴离子在电场中因不同的电泳迁移率而产生的微分迁移的分离。分析阴离子的定性和定量检测是通过间接检测紫外吸收。[img=,690,562]http://ng1.17img.cn/bbsfiles/images/2017/09/201709032036_01_2166779_3.png[/img]时,不影响其他被分析的阴离子检测。一元酸和中性有机化合物不影响被测阴离子的检测。在场的二元酸(最多10 mg/L)及高氯酸盐和甲酸阴离子(最多3 mg/L)是可以接受的。设备和试剂以下的设备和试剂在测量中被应用: CAPEL毛细管电泳设备需要高压负电极; 标准溶液的阴离子参考浓度:Cl—(1 mg/ml)、NO2—(1 mg/ml)、SO42—(1 mg/ml)、NO3—(1 mg/ml)、F—(1 mg/ml)、HPO42—(0.5mg/ml) ; 蒸馏水; 氧化铬(VI)、分析纯; 三甲基色氨酸溴化物,试剂纯; 二乙醇胺,试剂纯; 氢氧化钠,超高级纯; 盐酸,超高级纯; 乙酸,超高级纯; 氨水溶液,超高级纯; EDTA钠盐(Trilon B)分析纯。在WINDOWS 98/ME/NT/2000/XP系统下安装采集和处理色谱数据的Chrom&Spec软件包可实现对数据的采集、收集、处理和输出。前处理步骤前处理的步骤包括:取样、样品制备,毛细管的调节、辅助和校准溶液的制备和CAPEL毛细管电泳设备的校准。天然水、饮用水和废水样品的收集应遵循ISO 5667标准。样品体积不少于100 ml。样品应通过 “蓝丝带”干燥过滤器(瓦特曼NO 44或者S&S NO 589“蓝丝带”)加以筛选。滤液的第一部分必须丢弃。样品分析必需在24小时内。采用测量校准溶液的信号对样品进行校准。通过记录校准混合物之一的电泳值测量样品,从而直接核对的校准特征的稳定性。测量步骤预测试的执行应在主测量之前:可能需要调整样品pH值,并消除干扰的阳离子和阴离子。在每一样品列中,不得少于2个抽样。如果测量的氯化物、亚硝酸盐、硫酸盐、硝酸盐和磷酸盐的浓度超过50 mg/L,或氟的含量超过25 mg/L的话,则应先用蒸馏水对样品进行稀释。数据处理Chrom&Spec软件输出一份在溶液中阴离子的浓度(mg/L)分析作为分析材料。实例分析样品: 净化污水(稀释比1:9)缓冲区:5 mmol铬酸盐 20 mmol EDA 1.65 mmol CTAB毛细管:LEFF/LTOTAL 50/60 cm ID 75 μm注射量:300 mbar*S电压: -17kV检测: 254 nm,间接[img=,517,225]http://ng1.17img.cn/bbsfiles/images/2017/09/201709032037_01_2166779_3.png[/img]测量结果1—氯化物(2.7 mg/L)2—硫酸盐(4.2 mg/L)3—氟化物(1.2 mg/L)4—磷酸盐(3.3 mg/L)5—碳酸氢盐
指示剂 核酸电泳常用的指示剂有溴酚兰和二甲苯青及银染色.溴酚兰在碱性液体中 呈紫兰色,在0.6%、1%、1.4%和2%琼脂糖凝胶电泳中,溴酚兰的迁移率分别与1Kb、 0.6Kb、0.2Kb和0.15Kb的双链线性DNA片段大致相同.二甲苯青的水溶液呈兰色,它在 1%和1.4%琼脂糖中电泳时,其迁移速率分别与2Kb和1.6Kb的双链线性DNA大致相似. 指示剂一般与蔗糖、甘油或聚蔗糖400组成载样缓冲液.载样缓冲液的作用有①增加样 品密度,使其比重增加,以确保DNA均匀沉入加样孔内.②在电泳中形成肉眼可见的指 示带,可预测核酸电泳的速度和位置.③使样品呈色,使加样操作更方便.染色剂 核酸电泳后,需经染色后才能显现出带型,最常用的是溴化乙锭染色法,其 次是银染色. 溴化乙锭(ethidium bromide,EB)是一种荧光染料,EB分子可嵌入核酸双链的碱基对 之间,在紫外线激发下,发出红色荧光.根据情况可在凝胶电泳液中加入终浓度为 0.5ug/ml的EB,有时亦可在电泳后,将凝胶浸入该浓度的溶液中染色10~15min.琼脂 糖凝胶EB染色,肉眼可见核酸电泳带,其DNA量一般5ng,当溴化乙锭太多,凝胶染 色过深,核酸电泳带看不清时,可将凝胶放入蒸馏水浸泡30min后再观察. 银染色液中的银离子(Ag+)可与核酸形成稳定的复合物,然后用还原剂如甲醛 使Ag+还原成银颗粒,可把核酸电泳带染色黑褐色.主要用于聚丙烯酰胺凝胶电泳染色. 也用于琼脂糖凝胶染色.其灵敏度比EB高200倍.但银染色后,DNA不宜回收.来源:生命经纬
单链开环。当条件变化时,情况会相反,还与琼脂糖的浓度、电流强度、离子强度及EB含量有关。(4)所加电压:低电压时,线状DNA片段的迁移速率与所加电压成正比。使分辨效果好,凝胶上所加电压不应超过5 V/cm(5)碱基组成与温度:一般影响不大4 -30 ℃(6)嵌入染料的存在:降低线性DNA迁移率,(不提倡加在电泳液中)(7)电泳缓冲液 (0.5×TBE)的组成及其离子强度影响DNA的迁移率,无离子存在时,核酸基本不泳动,离子强度过大产热厉害,熔化凝胶并导致DNA变性,一般采用1×TAE,1×TBE,1×TPE(均含EDTA pH8.0)。2. 溴化乙锭(EB)为致癌剂,操作时应戴手套,尽量减少台面污染。3. 电泳指示剂:核酸电泳常用的指示剂有两种,溴酚蓝(bromophenol blue, Bb)呈蓝紫色;二甲苯晴(xylene cyanol, Xc)呈蓝色,它携带的电荷量比溴酚蓝少,在凝胶中的的迁移率比溴酚蓝慢。
离子迁移谱和飞行时间质谱 都是依靠时间来确定物质,前者依靠迁移率来分辨,后者依靠质荷比判定。哪位分析下二者的区别,是不是飞行时间质谱在常压下,原理就与离子迁移谱一样了。
离子迁移谱技术是20 世纪 60 年代发展起来的一种痕量探测技术,国外 20 世纪 80 年代将 IMS 技术应用于现场分析检测。 IMS 技术的原理是通过气态离子的迁移率来表征各种不同的化学物质,达到对各种物质分析检测的目的,具有极高的探测灵敏度。 离子迁移率谱仪方法(IMS)是一种高效的毒品、爆炸品、生化武器等的检测方法,可以在秒级别时间内对邮件、包裹等物品内是否有爆炸物品、毒品等做出判别,同时能对人体是否隐匿爆炸物品直接进行检测,有效提高打击恐怖活动力度,确保人民生命和财产安全。因此IMS技术为各级安全机构的检测,提供了很好的检测手段。可广泛应用于机场、海关、边防、车站、码头及体育场馆等反恐缉私场所本公司对离子迁移谱仪在国内的使用情况非常感兴趣,希望使用离子迁移谱仪的用户或有兴趣的朋友共同探讨,email:[email]xiaoyixiao0@163.com[/email],QQ:543694183欢迎大家的参与和讨论。
http://img03.taobaocdn.com/bao/uploaded/i3/T1b7qIXllbXXXGluZW_023314.jpg_310x310.jpgEB溴化乙锭(Ethidium bromide)、是一种高度灵敏的荧光染色剂,用于观察琼脂糖(agarose)和聚丙烯酰胺凝胶中的DNA。溴化乙锭用标准302nm 紫外光透射仪激发并放射出橙红色信号,可用Polaroid 底片或带CCD成像头的凝胶成像处理系统拍摄。 观察琼脂糖凝胶中DNA最常用的方法是利用荧光染料溴化乙锭进行染色,溴化乙锭含有一个可以嵌入DNA堆积碱基之间的一个三环平面基团。它与DNA的结合几乎没有碱基序列特异性。在高离子强度的饱和溶液中,大约每2.5个碱基插入一个溴化乙锭分子。当染料分子插入后,其平面基团与螺旋的轴线垂直并通过范德华力与上下碱基相互作用。这个基团的固定位置及其与碱基的密切接近,导致与DNA结合的染料呈现荧光,其荧光产率比游离溶液中染料有所增加。DNA吸收254nm处的紫外辐射并传递给染料,而被结合的染料本身吸收302nm和366nm的光辐射。这两种情况下,被吸收的能量在可见光谱红橙区的590nm处重新发射出来。由于溴化乙锭-DNA复合物的荧光产率比没有结合DNA的染料高出20-30倍,所以当凝胶中含有游离的溴化乙锭(0.5ug/ml)时,可以检测到少至10ng的DNA条带。 溴化乙锭可以用来检测单链或双链核酸(DNA或RNA)。但是染料对单链核酸的亲和力相对较小,所以其荧光产率也相对较低。事实上,大多数对单链DNA或RNA染色的荧光时通过染料结合到分子内形成较短的链内螺旋产生的。 尽管在该染料存在的情况下,线状DNA的电泳迁移率约降低15%,因此,当需要知道DNA片段的准确大小(如DNA限制酶酶切图谱的鉴定),凝胶应该在无EB情况下电泳,电泳结束后用EB染色。染色完毕后,通常不需要脱色。但是在检测小量DNA(小于10ng)片段时,通常要将染色后的凝胶进行脱色。 损害 溴化乙锭可以嵌入碱基分子中,导致错配。溴化乙锭是强诱变剂,具有高致癌性! SYBR Green I和溴化乙啶(EB)Ames 测试结果显示[font=T
离子迁移谱技术是20 世纪 60 年代发展起来的一种痕量探测技术,国外 20 世纪 80 年代将 IMS 技术应用于现场分析检测。 IMS 技术的原理是通过气态离子的迁移率来表征各种不同的化学物质,达到对各种物质分析检测的目的,具有极高的探测灵敏度。 离子迁移率谱仪方法(IMS)是一种高效的毒品、爆炸品、生化武器等的检测方法,可以在秒级别时间内对邮件、包裹等物品内是否有爆炸物品、毒品等做出判别,同时能对人体是否隐匿爆炸物品直接进行检测,有效提高打击恐怖活动力度,确保人民生命和财产安全。因此IMS技术为各级安全机构的检测,提供了很好的检测手段。可广泛应用于机场、海关、边防、车站、码头及体育场馆等反恐缉私场所 本人对离子迁移谱仪在国内的使用情况非常感兴趣,希望使用离子迁移谱仪的坛友能支持我的问卷调研,并将填好后的问卷反馈给我,email:luomeina2003@163.com,欢迎大家的参与和讨论。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=61734]离子迁移谱仪用户调查[/url]